|
| Temas de FC |
P. Rodríguez Molino![]() , C. Calvo Rey
, C. Calvo Rey
Servicio de Pediatría. Enfermedades Infecciosas y Tropicales. Hospital Infantil La Paz. Madrid. Centro de Investigación Biomédica en Red en Enfermedades Infecciosas (CIBERINFEC)
| Resumen
La tuberculosis (TB) es la principal causa de muerte por un solo agente infeccioso en el mundo y contribuye de forma notable a la mortalidad infantil. Sin embargo, la TB pediátrica ha sido una epidemia oculta por su escasa capacidad infectiva y menor incidencia comparada con adultos. Actualmente, las mayores limitaciones son las dificultades en el diagnóstico y la ausencia de formulaciones pediátricas óptimas. A pesar de que en nuestro medio la mortalidad por TB pediátrica es excepcional, existe una importante morbilidad ocasionada especialmente por las formas extrapulmonares. Además, aunque España es considerada un país de baja incidencia, es el país de Europa occidental con el mayor número de casos. El papel del pediatra de Atención Primaria es fundamental en el abordaje inicial de estos pacientes y de las familias, así como en el seguimiento y acompañamiento de la enfermedad. |
| Abstract
Tuberculosis disease (TB) is the leading cause of death by a single infectious agent in the world and contributes significantly to infant mortality. Pediatric TB has been a hidden epidemic due to its low infective capacity and lower incidence compared to adults. Currently the greatest limitations are the difficulties in diagnosis and the absence of optimal pediatric formulations. Although pediatric TB mortality is exceptional in our setting, there is a significant morbidity caused especially by extrapulmonary forms of the disease. Furthermore, although Spain is considered a low-incidence country, it is the Western European country with the highest number of cases. The role of the Primary Care pediatrician is essential in the initial management of these patients and their families, as well as in the ongoing follow-up and support throughout the course of the disease. |
Palabras clave: Tuberculosis pediátrica; Exposición; Infección tuberculosa latente; Enfermedad tuberculosa; Tratamiento de tuberculosis.
Key words: Pediatric tuberculosis; Exposure; Latent tuberculosis infection; Tuberculosis disease; Tuberculosis treatment.
Pediatr Integral 2026; XXX (2): 107 – 117
OBJETIVOS
• Conocer las formas clínicas y los métodos diagnósticos de la tuberculosis pediátrica.
• Detectar los factores de riesgo para adquirir una infección o enfermedad tuberculosa.
• Aprender a realizar una correcta anamnesis y exploración física dirigida.
• Realizar una adecuada orientación diagnóstica en el cribado inicial.
• Conocer los casos que deben recibir seguimiento en una unidad especializada.
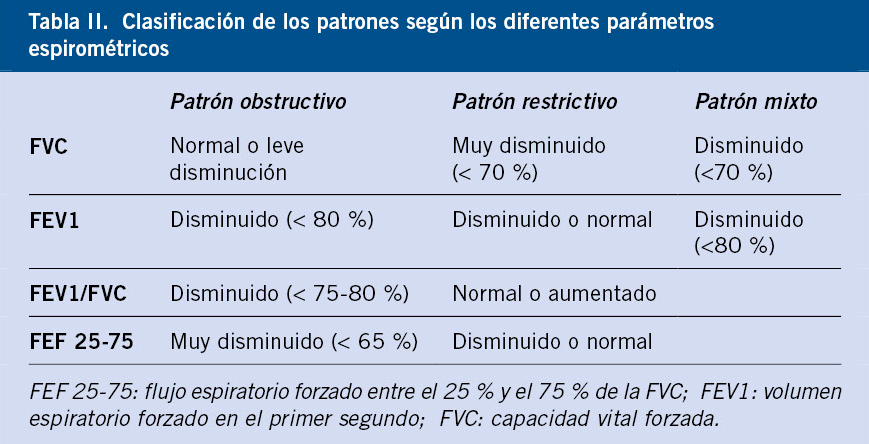
Tuberculosis pulmonar
https://doi.org/10.63149/j.pedint.121
Introducción
La tuberculosis es una infección causada por Mycobacterium tuberculosis que se transmite por vía respiratoria desde adultos bacilíferos; los niños rara vez contagian y, a menudo, no se confirma microbiológicamente. En pediatría, su diagnóstico es un “evento centinela” que indica transmisión reciente. Los niños procedentes o expuestos a entornos de alta endemia, así como los niños de menor edad y los inmunocomprometidos, presentan mayor riesgo de adquirir tuberculosis y de evolucionar a formas graves de la enfermedad.
La tuberculosis (TB) es una enfermedad infecciosa producida por Mycobacterium tuberculosis (MTB), bacilo ácido-alcohol resistente (BAAR). La infección se transmite por vía respiratoria, inhalando gotitas contaminadas procedentes de enfermos bacilíferos (baciloscopia positiva en esputo). Los niños no suelen ser transmisores, debido a su menor carga bacilar en secreciones respiratorias, lo cual, sumado a su incapacidad para expectorar, determina que hasta en la mitad de los casos no se alcance confirmación microbiológica(1). El diagnóstico de infección o enfermedad en un niño es siempre un “evento centinela” que refleja la transmisión reciente de MTB en la comunidad; aunque no lo demostremos, siempre hay un adulto cercano con enfermedad bacilífera. Todos los niños en contacto con MTB deberán ser diagnosticados adecuadamente en expuestos, infectados o enfermos. El desarrollo de una u otra situación dependerá de la intimidad del contacto con la fuente bacilífera, la cantidad de bacilos de la fuente, la duración de la exposición, la situación inmunológica y la edad del niño.
Tienen un mayor riesgo de adquirir la infección los niños inmigrantes que proceden de regiones de alta endemia o que conviven con adultos inmigrantes procedentes de estas regiones, así como los viajeros a zonas endémicas. Los niños, especialmente los más pequeños, y los pacientes inmunocomprometidos tienen más riesgo de progresión de infección a enfermedad tuberculosa y de presentar enfermedad grave(2).
Epidemiología
La tuberculosis es una emergencia global que causa 1,3 millones de muertes al año, siendo la primera causa de mortalidad infecciosa en la infancia y con especial impacto en menores de 5 años. Preocupan especialmente las formas multirresistentes y, aunque la incidencia en España disminuye, sigue siendo la más alta de Europa occidental, lo que justifica el cribado sistemático en niños inmigrantes procedentes de zonas de alta endemia.
La TB es considerada por la OMS una emergencia de salud global, falleciendo anualmente 1,3 millones de personas a causa de esta enfermedad, fundamentalmente en países de baja renta. Representa la primera causa de mortalidad por un único agente infeccioso en la infancia, especialmente en menores de 5 años. Por cada niño enfermo de TB, se estima que existen 10 niños infectados de forma latente, quienes, no habiendo desarrollado aún la enfermedad, son el reservorio de la TB de los próximos años. En general, la TB pediátrica afecta a lactantes y adolescentes, y es menos frecuente entre los 5-10 años. En el momento actual, existe una gran preocupación por el aumento de los casos de TB multirresistente (MDR), sobre todo en países de Europa del Este, donde supone un 16 % de los nuevos diagnósticos. La incidencia de TB resistente en niños no es bien conocida, pero se piensa que es similar a la población adulta. Mediante la estrategia “End TB”, la OMS pretende disminuir un 80 % la incidencia y un 90 % la mortalidad por TB para 2035(3).
España es el país de Europa occidental con mayor número de casos pediátricos, aunque la incidencia disminuye progresivamente(4). En la población pediátrica de nuestro país, la incidencia de la enfermedad es de 3 casos/100.000 niños(5).
Los factores que determinan la endemia en países desarrollados son fundamentalmente la situación de la infección por virus de la inmunodeficiencia humana (VIH) y el porcentaje de inmigrantes de países con alta prevalencia de TB. En las últimas décadas se ha incrementado el fenómeno de la inmigración, en ocasiones procedente de áreas con mayores tasas de resistencia a fármacos. En nuestro medio, el porcentaje de TB MDR en población general se sitúa en torno al 4 %, siendo superior en población inmigrante(6). Por todos estos motivos, está indicado realizar screening de TB a todo niño inmigrante procedente de zonas de alta endemia, para detectar precozmente la infección, fuentes de contagio, e interrumpir el ciclo de la transmisión.
Fisiopatología
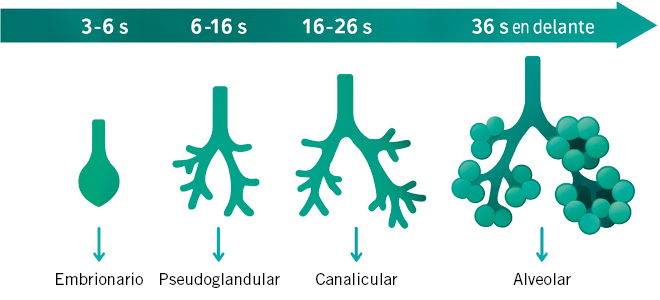
La tuberculosis pulmonar infantil comienza tras la inhalación de Mycobacterium tuberculosis, que se instala en los alvéolos y forma el complejo primario de Ghon; en la mayoría de los niños inmunocompetentes, la respuesta celular contiene la infección en forma latente. En lactantes y pequeños, la inmadurez inmunitaria favorece la diseminación hematógena y la aparición de formas graves, como miliar o meningitis tuberculosa.
La tuberculosis pulmonar infantil se produce tras la inhalación de aerosoles que contienen Mycobacterium tuberculosis, expulsados por un adulto con enfermedad bacilífera. Una vez en el pulmón, los bacilos alcanzan los alvéolos y son fagocitados por los macrófagos, donde pueden sobrevivir y replicarse gracias a sus mecanismos de evasión inmunitaria. En los días posteriores se forma el complejo primario de Ghon, constituido por la lesión pulmonar inicial y la afectación de los ganglios linfáticos regionales. En la mayoría de los niños, especialmente los inmunocompetentes, la respuesta inmune mediada por linfocitos T logra contener la infección en forma de latencia, aunque sin lograr su completa erradicación.
En los lactantes y niños pequeños, cuya inmunidad celular es inmadura, la contención del bacilo es menos eficaz, lo que facilita la diseminación temprana desde el foco pulmonar hacia el torrente sanguíneo y otros órganos. Esta vulnerabilidad explica la mayor frecuencia de formas graves en este grupo, como la tuberculosis miliar y la meningitis tuberculosa. En los niños mayores, la progresión hacia enfermedad pulmonar activa suele depender de factores, como la carga bacilar del caso índice, la intensidad y duración de la exposición, el estado nutricional y la presencia de comorbilidades o inmunosupresión.
Definición de estadios de la enfermedad
Exposición a tuberculosis
Consideramos exposición cuando: 1) existe contacto reciente (últimos 3 meses) y estrecho (>4 h diarias en el mismo habitáculo cerrado) con un paciente confirmado/sospechoso de TB bacilífera; 2) prueba de tuberculina (PT) y/o IGRA (Interferon Gamma Release Assays) negativo; y 3) ausencia de síntomas clínicos y radiografía de tórax normal.
Infección tuberculosa (ITB)
Consideramos ITB cuando: 1) PT/IGRA positivo; 2) ausencia de síntomas clínicos y radiografía de tórax normal, independientemente de que exista contacto conocido. En ausencia de contacto y sin factores de riesgo, el antecedente de vacunación Bacilo de Calmette-Guérin (BCG) con PT positiva e IGRA negativo se interpreta como efecto de la BCG, y estos casos no se consideran ITB.
Enfermedad tuberculosa
Consideramos enfermedad TB cuando se dan, al menos, dos de los siguientes: 1) clínica compatible; 2) hallazgos radiológicos compatibles; 3) exposición reciente o evidencia inmunológica de contacto (PT/IGRA positivo); 4) respuesta adecuada al tratamiento antituberculoso(7). El diagnóstico de certeza lo proporciona un cultivo o una PCR positiva para MTB, aunque, con frecuencia, en niños no obtenemos confirmación microbiológica (formas paucibacilares), realizando habitualmente un diagnóstico de sospecha. Los test inmunológicos (PT/IGRA) suelen ser positivos, aunque en formas iniciales o diseminadas pueden ser negativos. En caso de sospecha clínica, a pesar de test inmunológico negativo, deberemos instaurar tratamiento.
Clínica
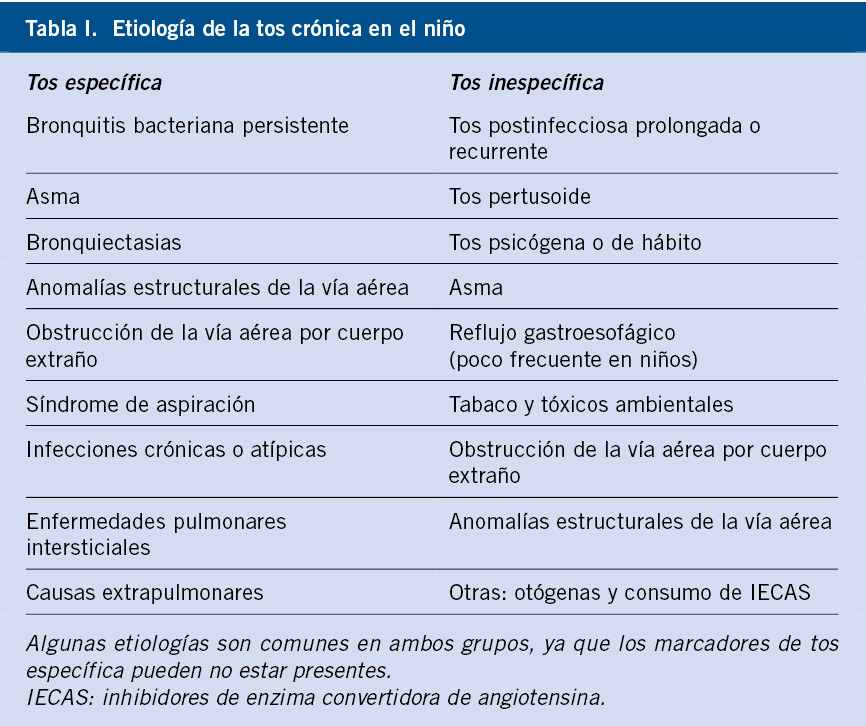
Los síntomas son inespecíficos y deben hacer sospechar la enfermedad cuando hay fiebre, tos prolongada o síndrome constitucional en niños expuestos a casos de TB o procedentes de zonas de alta endemia. Aunque la afectación puede ser multisistémica, la forma más frecuente es la pulmonar, con predominio ganglionar. La clínica respiratoria suele ser insidiosa y puede acompañarse de manifestaciones constitucionales o signos de gravedad, si bien muchos niños, en países de baja prevalencia, permanecen asintomáticos o con síntomas muy leves.
Los síntomas de la enfermedad son inespecíficos. Debemos sospecharla cuando aparezca una clínica larvada de síndrome constitucional, fiebre o tos de larga evolución, convivientes con tosedores crónicos o diagnosticados de TB o que provienen de zonas de alta endemia. En ocasiones, puede haber síntomas de afectación grave.
La TB puede afectar a múltiples sistemas, pero lo más frecuente, en la población pediátrica, es la TB pulmonar, con predominio de las formas ganglionares. Entre las extrapulmonares, las más frecuentes son las adenitis y la meningitis tuberculosa.
En la mayor parte de los niños, la TB pulmonar se debe a la progresión de una primoinfección TB en el primer año tras la infección, con afectación de los ganglios hiliares o mediastínicos, que puede extenderse al parénquima pulmonar, comprimir los bronquios adyacentes o afectar a la pleura, como consecuencia de una reacción de hipersensibilidad o por el vertido de caseum al espacio pleural. Los niños pequeños o inmunodeprimidos con TB diseminada presentan un patrón pulmonar característico que recuerda a las semillas de mijo (TB miliar). En niños mayores de 10 años, es más común la reactivación de una ITB antigua, superponible a la TB del adulto, con cavidades apicales posteriores.
Los síntomas de la TB pulmonar son superponibles a otras infecciones respiratorias, con tos, expectoración o dolor torácico, que se instauran de forma insidiosa y con mala respuesta a los tratamientos habituales. Habitualmente, se acompaña de síntomas constitucionales, como fiebre, sudoración nocturna y pérdida de peso. Las adenopatías intratorácicas grandes pueden ocasionar un cuadro de dificultad respiratoria con estridor y sibilancias, como consecuencia de la obstrucción bronquial. Los niños con afectación miliar pueden presentar hipoxemia. No obstante, es importante señalar que gran parte de los niños en un entorno de baja prevalencia, como España, se encuentran asintomáticos o con síntomas muy leves.
Diagnóstico
La tuberculosis pediátrica requiere una evaluación sistemática, que incluya anamnesis dirigida, exploración física y valoración de factores de riesgo y exposición. La prueba de tuberculina es el método inicial de cribado, complementado por IGRA en situaciones específicas para mejorar la rentabilidad diagnóstica. Las pruebas de imagen —radiografía, ecografía, TC o PET/TC— ayudan a definir la extensión y las complicaciones. El diagnóstico microbiológico mediante jugo gástrico, esputo inducido y técnicas moleculares es esencial, aunque limitado por la baja carga bacilar en niños. El diagnóstico diferencial debe considerar infecciones respiratorias comunes, procesos inflamatorios, neoplásicos y granulomatosos que pueden simular la TB. El pediatra de Atención Primaria es esencial en la detección inicial de la tuberculosis pediátrica, mediante una anamnesis cuidadosa, exploración física y pruebas básicas, derivando a unidades especializadas cuando existan dudas diagnósticas o una alta sospecha de enfermedad tuberculosa.
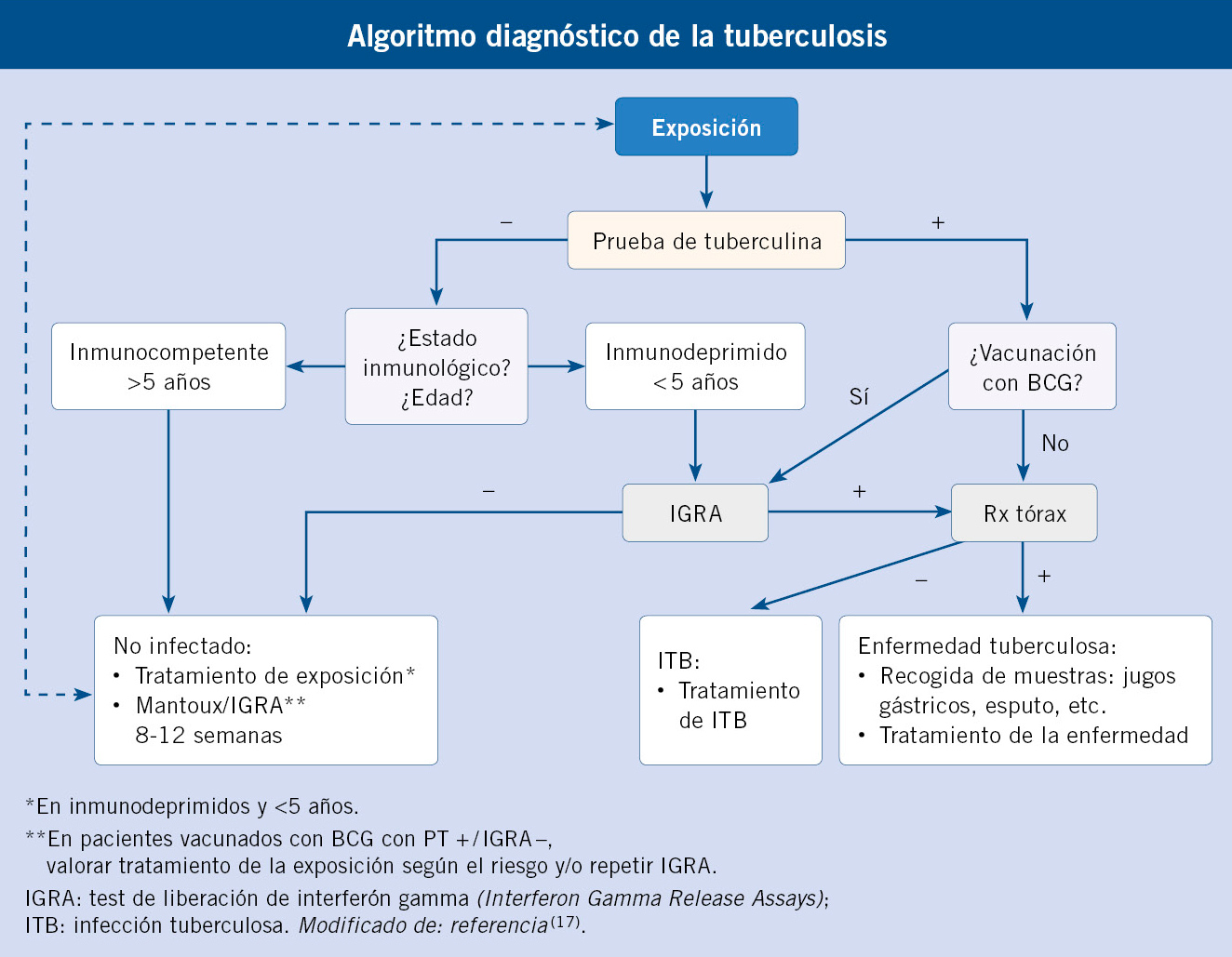
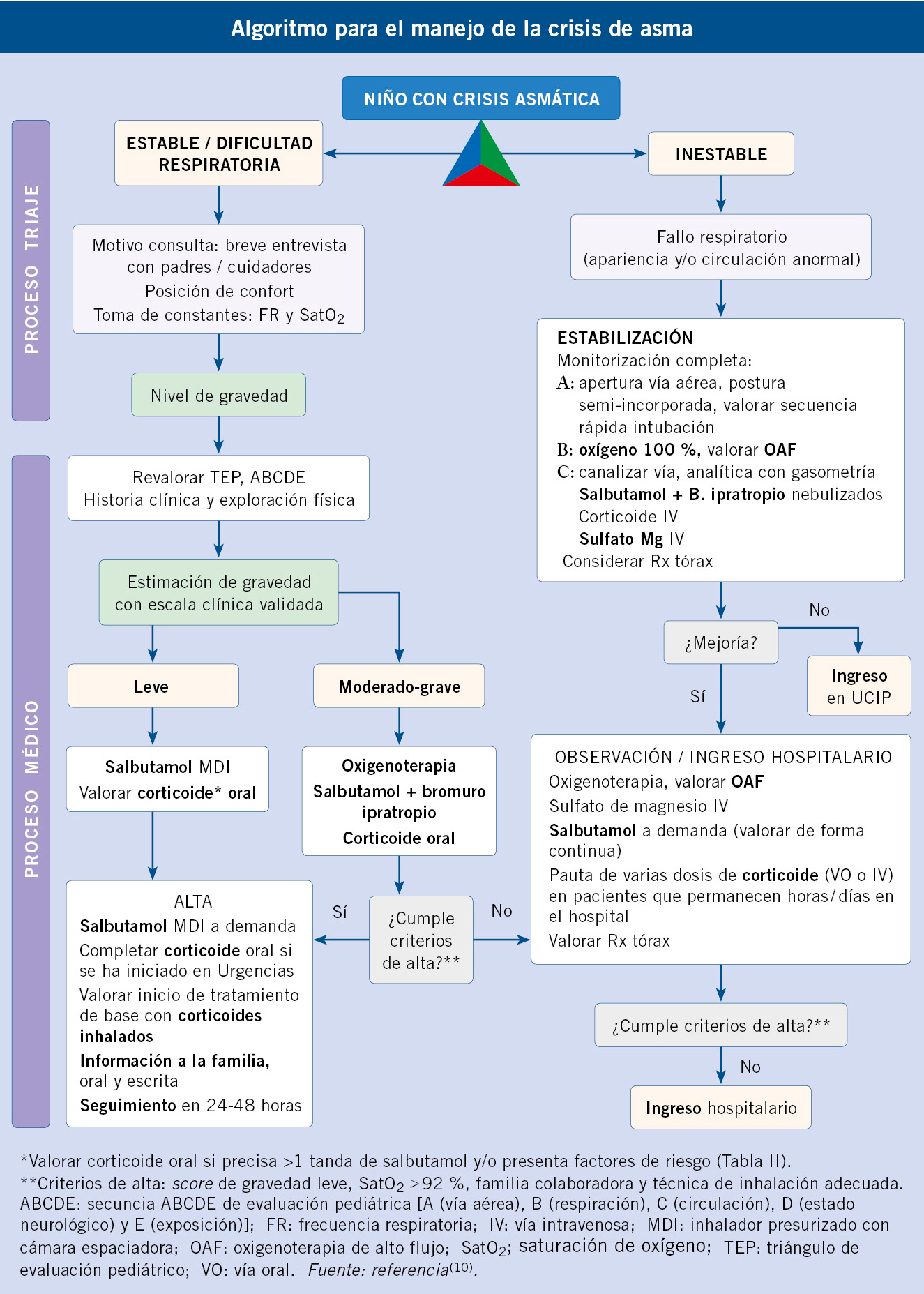
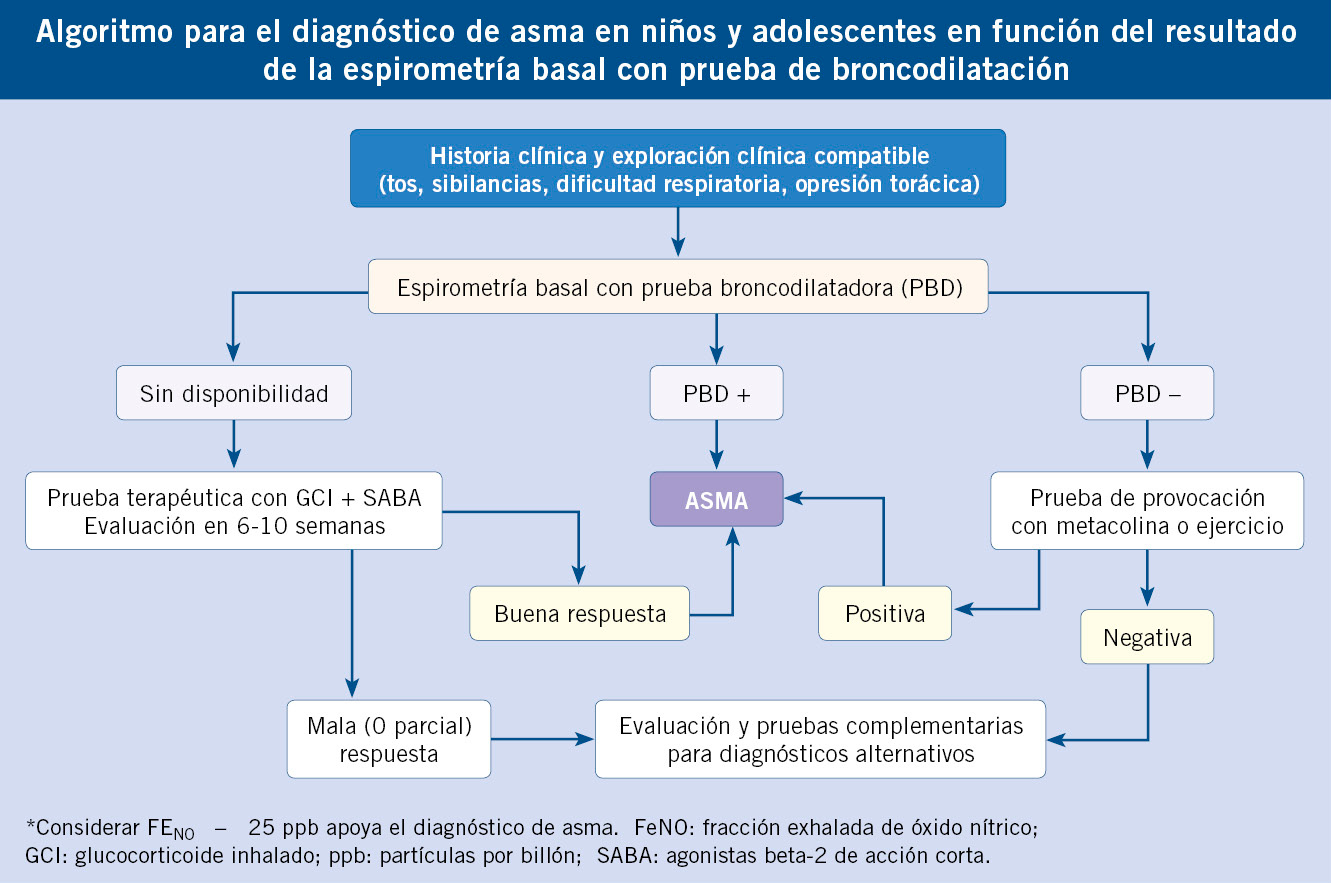
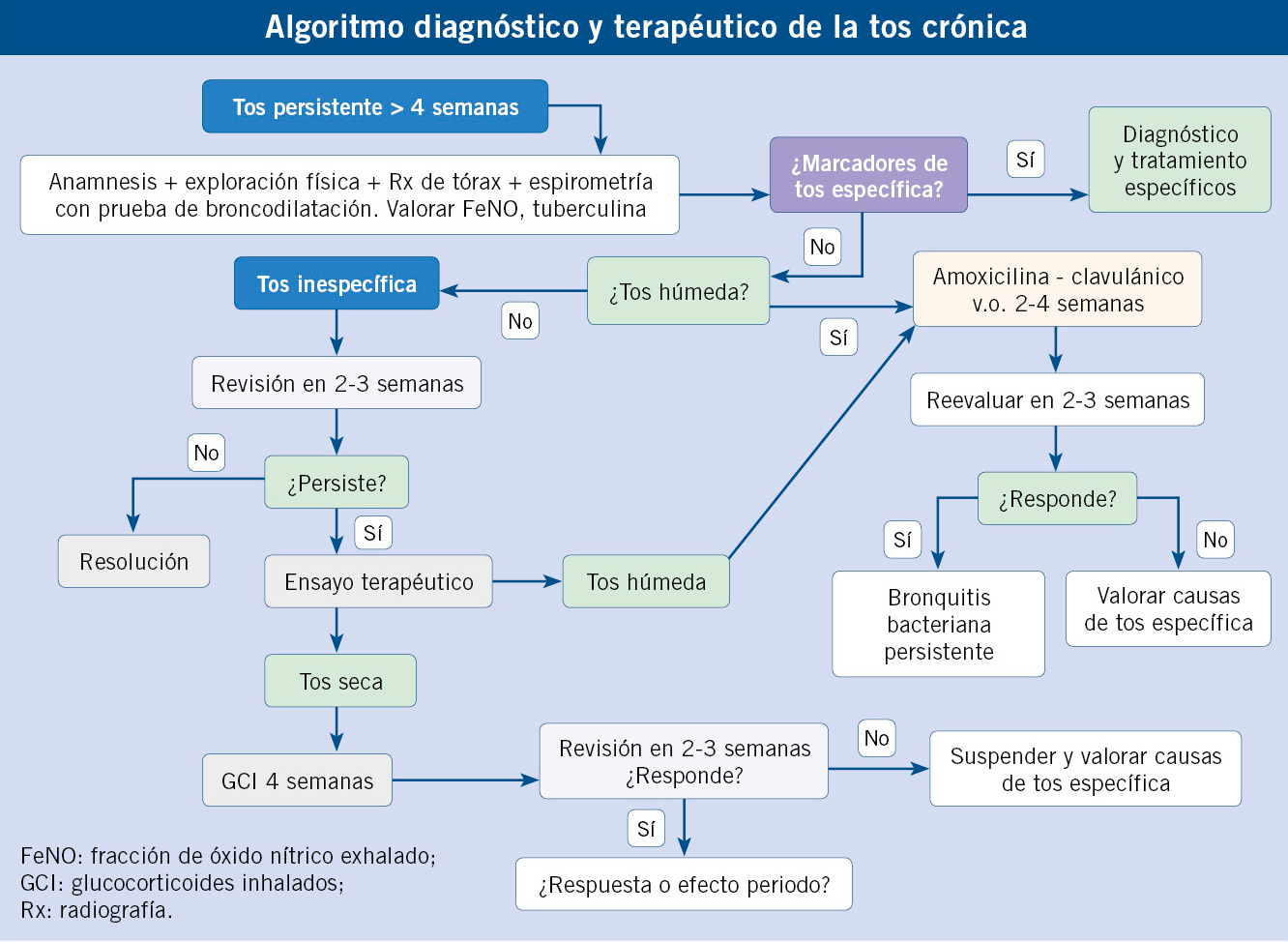
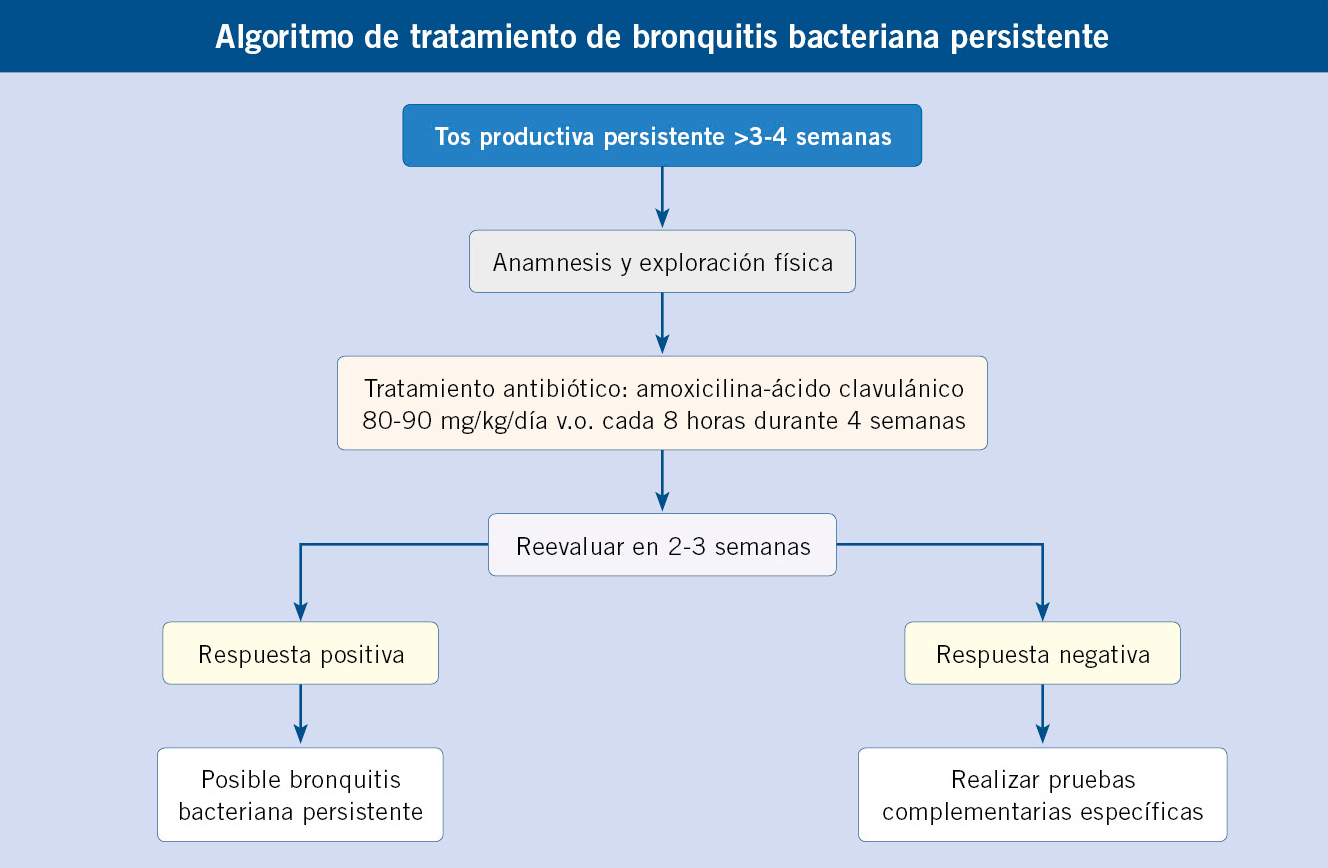
La evaluación diagnóstica que se debe seguir tras una exposición a TB se expone en el algoritmo al final del artículo.
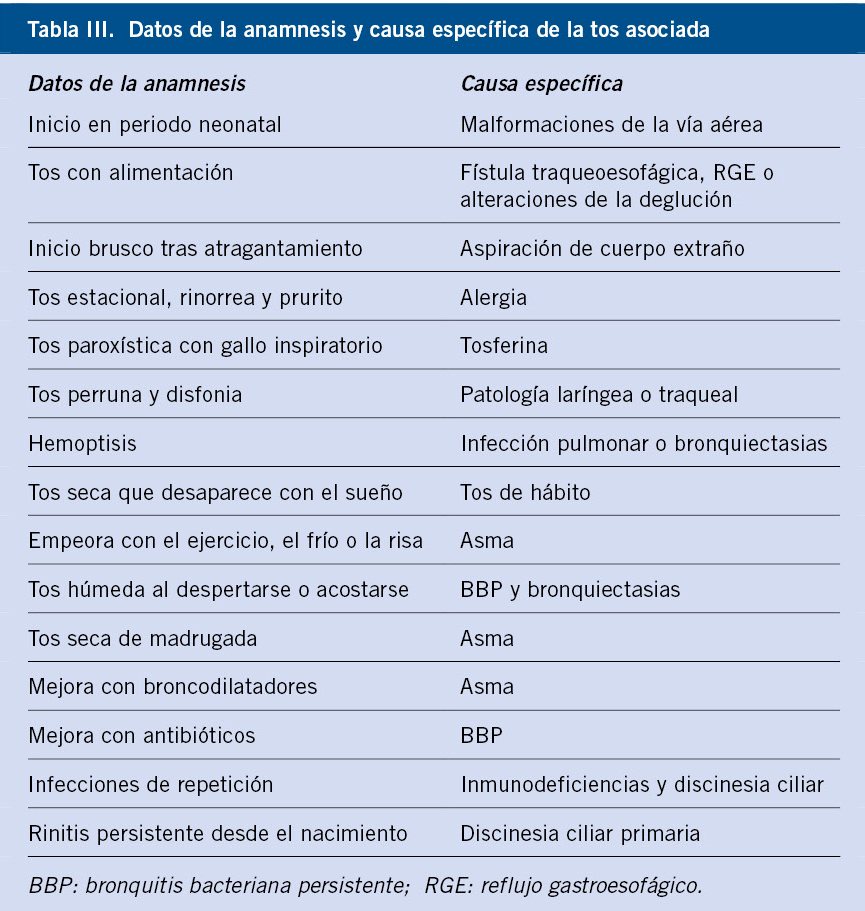
Anamnesis
• Buscar foco de contagio en el entorno habitual del niño. Si existe, confirmar el tiempo de exposición, fecha de la última exposición, si el contacto es bacilífero y el estudio de resistencias.
• Vacunación BCG y fecha. Número de dosis y cicatriz postvacunal.
• PT/IGRA previo, fecha de realización y resultado (milímetros de induración en 48-96 h).
• Existencia previa de cuadros febriles, adenopatías, síntomas constitucionales o respiratorios.
• Reportar inmunodeficiencias, enfermedades o terapia inmunosupresora.
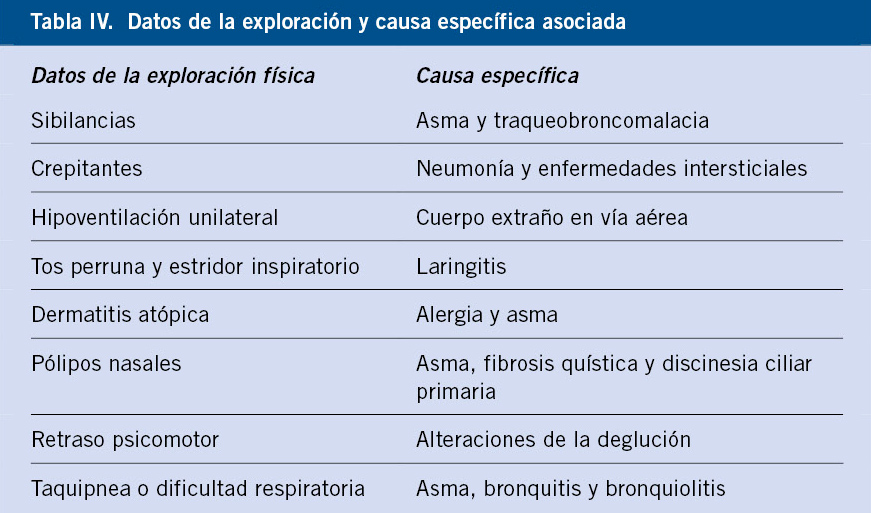
Exploración física
Habitualmente es normal, aunque es posible encontrar datos de alguna de las afectaciones pulmonares (sibilancias, hipoventilación) o extrapulmonares (afectación del VI par craneal, rigidez de nuca, artritis, adenitis, etc.).
Prueba de tuberculina (PT) o intradermorreacción de Mantoux
Es la prueba de elección para el cribado. El objetivo de la PT es identificar a los niños infectados por MTB, para: 1) diagnosticar los casos de enfermedad TB; 2) detectar precozmente los casos de infección para evitar su progresión a enfermedad; y 3) controlar a los niños expuestos, no infectados. Se necesita un periodo de tiempo entre 8-12 semanas después de la infección para que la PT se haga positiva, y refleja el desarrollo de inmunidad celular frente a MTB.
La prueba consiste en la administración intradérmica de tuberculina o PPD (derivado proteico purificado), compuesto con >200 antígenos comunes a MTB, BCG y otras micobacterias no tuberculosas (MNT). Si el niño ha tenido contacto previamente con el bacilo, se producirá una reacción de hipersensibilidad retardada, conocida como intradermorreacción de Mantoux. Su positividad solo indica infección; es necesario realizar pruebas complementarias para descartar enfermedad activa.
• Técnica: conservar la tuberculina a 4ºC preservada de la luz. Realizar una inyección intradérmica en la cara anterior del antebrazo con una aguja de calibre 26 con bisel corto hacia arriba: 0,1 mL/2 UI de PPD-RT23. Se debe producir una pápula de 6-10 mm.
• Lectura: debe leerse a las 72 horas, cuando se consigue la máxima induración, aunque es posible entre las 48 y 96 horas. Se mide el diámetro de induración máximo, transversal al eje mayor del brazo (p. ej.: 15 mm; no 15 x 10 mm), anotándose siempre en milímetros, con la fecha de lectura y la firma de la persona responsable. Si no hay induración, debe recogerse 0 mm de induración, no negativo. La vesiculación y la necrosis se consideran un resultado positivo.
• Interpretación:
1. Se considera positiva una induración ≥5 mm en:
a. Niños en contacto íntimo con el caso índice o sospechoso de TB.
b. Niños sospechosos de enfermedad clínica o radiológica.
c. Niños en situaciones de inmunodepresión o infección por el VIH.
d. Niños con conversión de la PT previamente negativa.
2. Se considera positiva una induración ≥10 mm en el resto de casos, incluido el niño inmigrante, viajero, y el cribado de niños sanos, independientemente de existir antecedente de BCG.
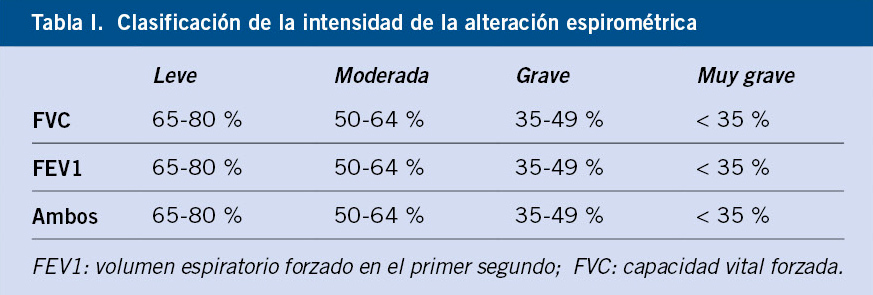
La PT puede tener falsos positivos y negativos (Tabla I). Aunque aún no están disponibles, existen nuevas pruebas intradérmicas basadas en los antígenos específicos de MTB (ESAT6 y CFP10), con mayor especificidad, que pueden ser una alternativa en el futuro(8).
Interferon-gamma Release Assays (IGRA)
Detectan la producción de interferón-gamma por las células T en contacto con los antígenos ESAT-6 (Early Secretory Antigenic Target-6) y CFP-10 (Culture Filtrate Protein-10). Dichos antígenos están presentes en el grupo MTB y, por lo tanto, en cepas salvajes de M. bovis, pero no en la cepa atenuada de la vacuna BCG, ni en la mayoría de micobacterias atípicas (aunque están presentes en M. kansasii, M. marinum, M. szulgai, M. flavescens). Como consecuencia, los IGRA son más específicos que la PT para diagnosticar la infección por MTB, ya que no presentan falsos positivos debidos a la vacunación con BCG ni a la mayoría de las MNT(9). Actualmente, existen dos IGRA disponibles en el mercado: el QuantiFERON®-TB Gold Plus y el T-SPOT®.TB.
Las recomendaciones para el uso de la PT y técnicas IGRA se incluyen en la tabla II.
Analítica general
Suele ser inespecífica. Discreta anemia, leucocitosis y VSG (velocidad de sedimentación globular) elevada (parámetro útil para seguir evolución). Se recomienda estudio de la función hepática previo a iniciar tratamiento.
Estudios radiológicos o de visualización
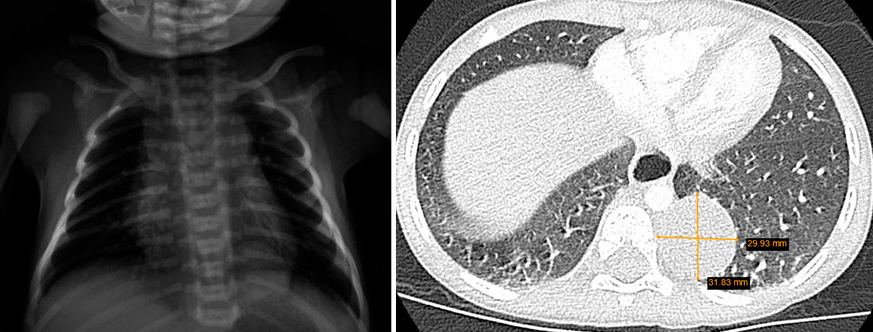
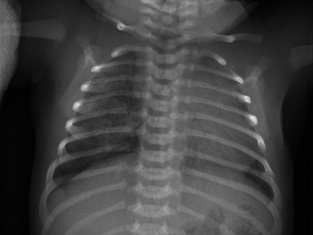
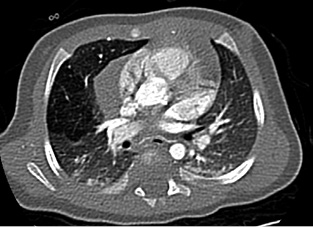
• Radiografía de tórax: no es patognomónica. Es posible encontrar formas adenopáticas, atelectasias, neumonías, cavitaciones (adolescentes), micronódulos (miliar) y cualquier otro patrón. Una radiografía normal no descarta TB.
• Tomografía computarizada (TC): se pueden visualizar adenopatías patológicas que miden >5-10 mm, con hipodensidad central y realce periférico del contraste. Se recomienda realizar TC en niños con hallazgos radiológicos equívocos, pacientes sintomáticos con radiografía normal, ante dudas diagnósticas en grupos de riesgo, para la valoración de complicaciones en TB endobronquial y en el seguimiento de casos complejos.
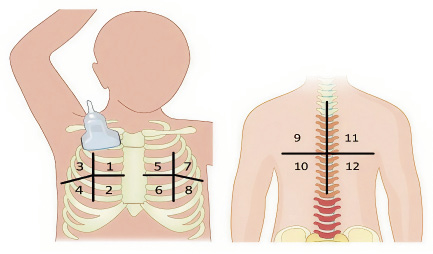
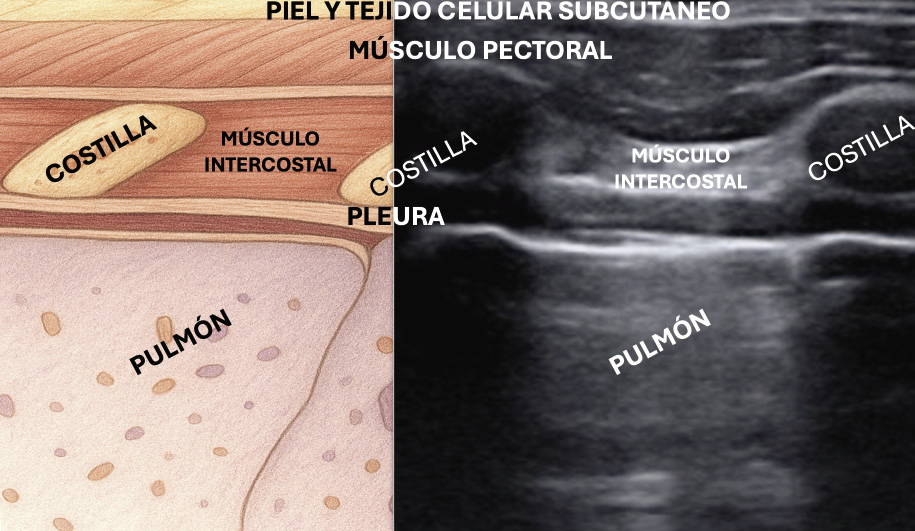
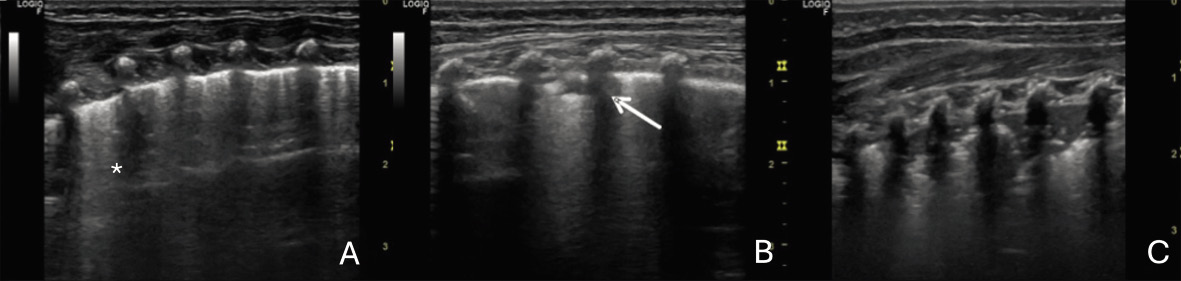
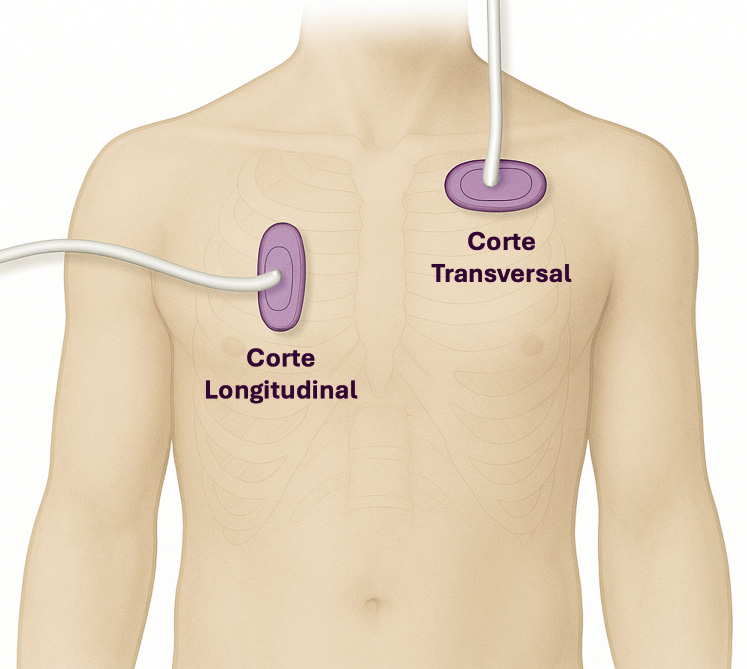
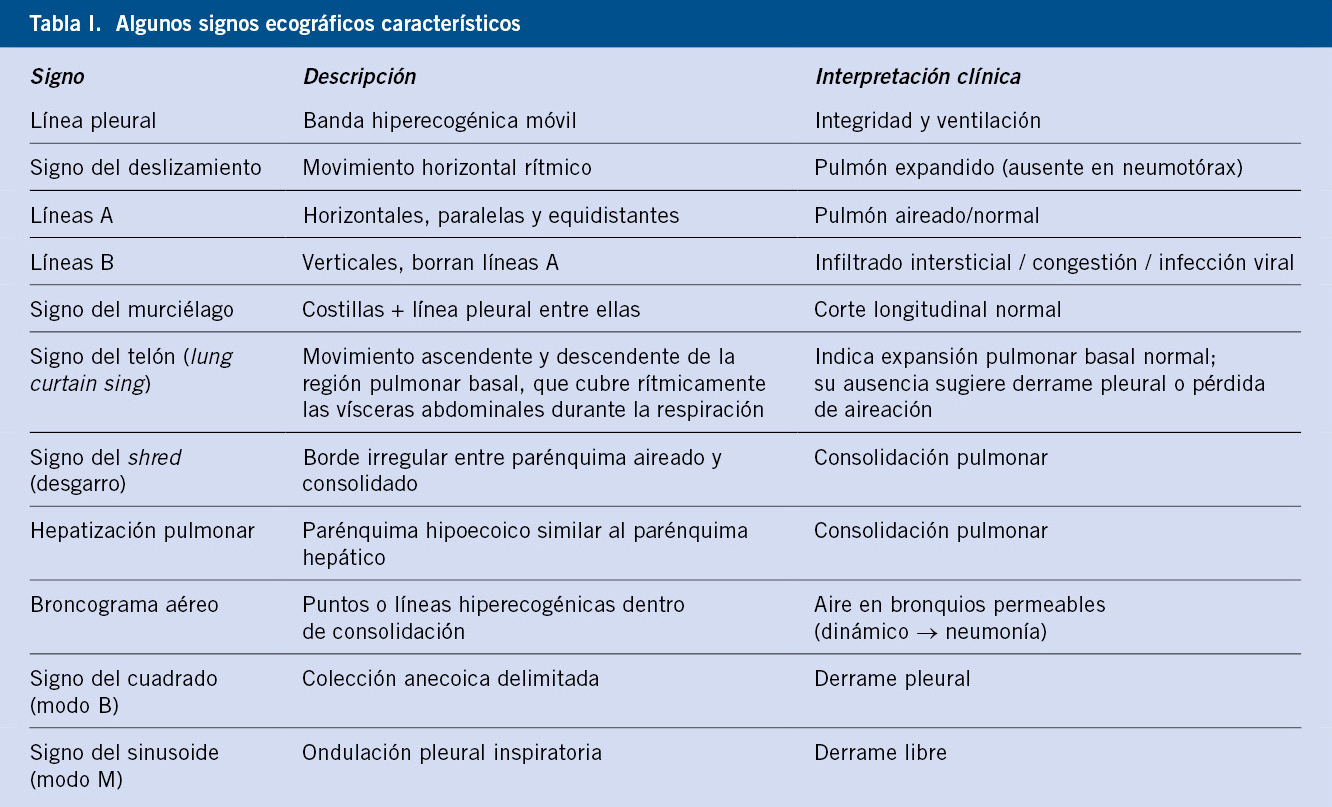
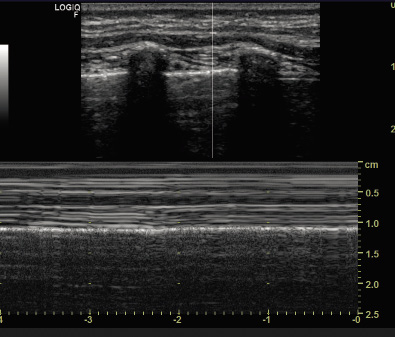
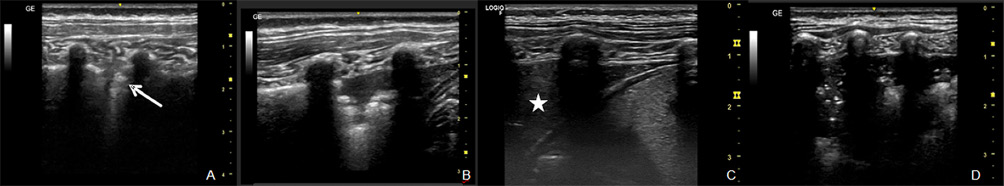
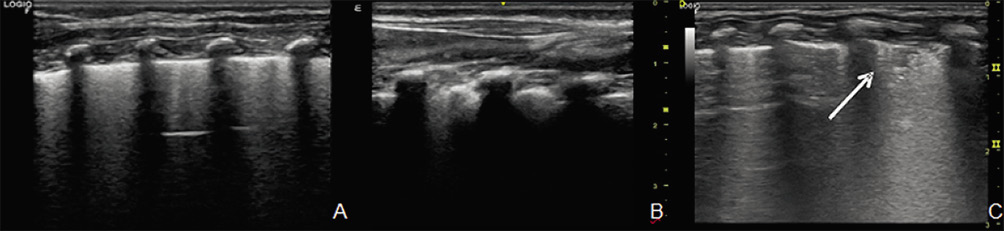
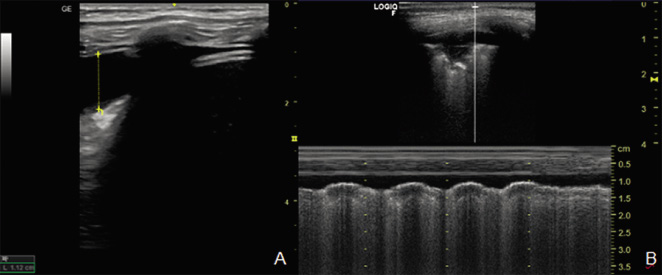
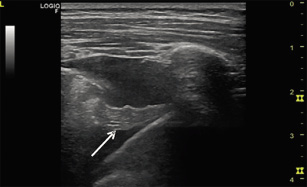
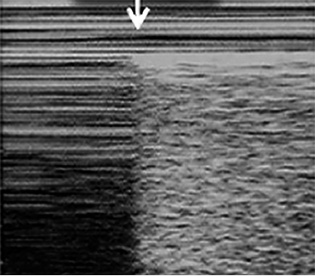
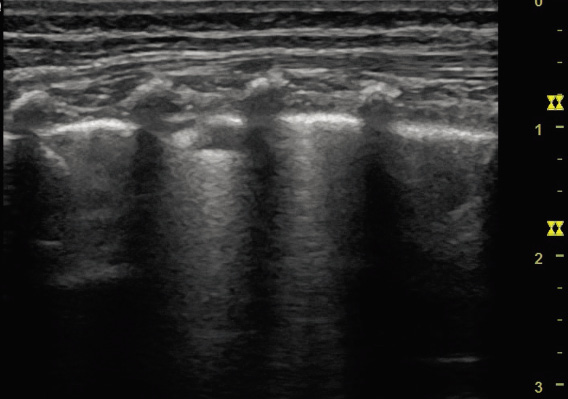
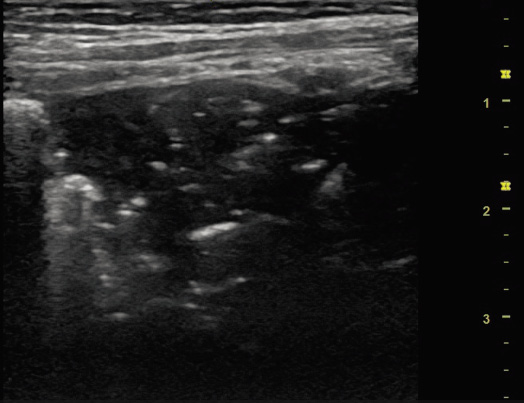
• Ecografía pulmonar: permite visualizar consolidaciones, cavitaciones y nódulos miliares, siempre que los cambios estén en contacto con la pleura. En manos expertas, tiene mayor sensibilidad que la radiografía para detectar linfadenopatías mediastínicas. También es útil en el diagnóstico del derrame pleural, adenopatías abdominales o lesiones focales esplénicas.
• Tomografía por emisión de positrones asociada a TC (PET/TC): permite diferenciar enfermedad de infección tuberculosa e imágenes residuales, evaluar la extensión de la enfermedad, monitorizar la respuesta al tratamiento e identificar focos de enfermedad candidatos a biopsia, pero presenta un grado de irradiación superior a la TC, por lo que su uso debe restringirse a casos seleccionados.
Estudios microbiológicos
Muestras
En niños sin capacidad de expectorar, la muestra de elección para el diagnóstico de TB pulmonar es el aspirado de jugo gástrico, recogido en ayunas a primera hora de la mañana en 3 días consecutivos a través de sonda nasogástrica (obtener mínimo 3-4 mL de jugo gástrico, inyectar 3 mL de agua estéril, aspirarla y añadirla a la muestra), o el esputo inducido, que tiene una sensibilidad similar y se obtiene administrando salbutamol inhalado y, posteriormente, 3-10 mL de suero salino hipertónico al 3 %, nebulizado durante 15 minutos. La mayor rentabilidad se obtiene realizando el mismo día esputo inducido y jugo gástrico.
En adolescentes o niños mayores con tos productiva, se recogerá esputo y, en pacientes intubados, aspirado bronquial o lavado broncoalveolar. Además, en niños pequeños, se recomienda el estudio de una muestra de heces para aumentar la rentabilidad diagnóstica. Puede estar indicada la realización de broncoscopia y lavado broncoalveolar para toma de muestras en determinados casos (dudas diagnósticas, inmunodeprimidos, evolución lenta, sospecha de TB resistente). Igualmente, si se sospecha un granuloma endobronquial por obstrucción bronquial (imagen de atelectasia pulmonar extensa), está indicada la realización de broncoscopia rígida para exéresis del granuloma y estudio anatomopatológico.
Técnicas
• Tinción: baciloscopia o visión directa de BAAR mediante fluorescencia con auramina o tinción de Ziehl-Neelsen. La sensibilidad en niños se encuentra entre 10-15 %. No es específica, sobre todo en pacientes con riesgo de infección por micobacterias atípicas.
• Cultivo: es la técnica de referencia. Permite identificar la especie y realizar estudios fenotípicos de resistencia a los fármacos antituberculosos, pero su sensibilidad es baja (30-50 %) y son necesarias entre 2 y 4 semanas para obtener el resultado definitivo.
• Técnicas moleculares, reacción en cadena de la polimerasa (PCR) y secuenciación masiva: aunque no reemplazan al cultivo como técnica de referencia, tienen una sensibilidad próxima a este, alta especificidad en niños y permiten obtener resultados en pocas horas. La técnica más extendida es Xpert®MTB/RIF Ultra (Cepheid, EE.UU.), que permite detectar simultáneamente la resistencia a rifampicina. Además, existen técnicas de secuenciación masiva, como el Deeplex®Myc-TB (Genoscreen, Francia), que permiten la identificación de especie, la detección de resistencias a fármacos antituberculosos y el rastreo filogenético para un mejor control de la transmisión poblacional.
• Métodos moleculares de detección de resistencias: la prueba de referencia para el estudio de la sensibilidad a los fármacos antituberculosos es el cultivo; sin embargo, se han desarrollado pruebas moleculares rápidas para la detección de mutaciones asociadas a resistencia, que tienen la gran ventaja de su rapidez, alta sensibilidad (90-97 % si la baciloscopia es positiva, 67 % si la baciloscopia es negativa) y especificidad (99 %). Además de Xpert®MTB/RIF Ultra, las más empleadas en nuestro medio son aquellas que detectan mutaciones de resistencia a isoniazida y rifampicina, como BD MAX®MDR-TB (BD, EE.UU.), Genotype®MTBDRplus (Hain Lifescience, Alemania) o FluoroType®MTBDR (Hain Lifescience, Alemania), y a fármacos de segunda línea, como Xpert®MTB/XDR (Cepheid, EE.UU.) o GenoType®MTBDRsl (Hain Lifescience, Alemania)(10).
Otros
• Estudio histológico de biopsia: granulomas caseificantes y necrotizantes.
• Adenosina-desaminasa (ADA): se consideran valores normales <40 U/L en líquido pleural y 1-4 U/L en líquido cefalorraquídeo. Su elevación es orientativa de TB, aunque no específica, ya que también puede aumentar en otros derrames (empiemas, linfomas). Posee un alto valor predictivo negativo, por lo que es excepcional que un derrame con ADA <40 U/L sea tuberculoso.
• Nuevas técnicas diagnósticas: en los últimos años se están desarrollando pruebas diagnósticas en muestras fácilmente accesibles, como técnicas moleculares en sangre capilar o biomarcadores en saliva y en orina, aún no disponibles en nuestro medio(11,12).
Diagnóstico diferencial
El diagnóstico diferencial de la tuberculosis pulmonar en niños es amplio debido a la inespecificidad de sus manifestaciones clínicas, que suelen solaparse con otras infecciones respiratorias frecuentes en la infancia. Deben considerarse patologías como las neumonías bacterianas comunes, especialmente por Streptococcus pneumoniae y Staphylococcus aureus, las infecciones virales persistentes (adenovirus, influenza, SARS-CoV-2), la infección por Mycoplasma pneumoniae y las bronquitis de curso prolongado. Las adenopatías hiliares o mediastínicas pueden confundirse con procesos como linfomas, infecciones fúngicas (histoplasmosis), malformaciones congénitas o enfermedades granulomatosas. En los casos con fiebre prolongada y afectación sistémica, deben valorarse entidades como la enfermedad de Kawasaki atípica, procesos autoinmunes o cuadros inflamatorios crónicos. La evaluación cuidadosa de la epidemiología, los factores de riesgo, la evolución clínica, la radiología y las pruebas inmunológicas o microbiológicas resulta esencial para orientar el diagnóstico y diferenciar la tuberculosis de otras causas más prevalentes.
Tratamiento
El manejo de la tuberculosis pediátrica incluye la profilaxis con isoniazida en niños expuestos sin infección —en menores de 5 años o inmunodeprimidos—, seguida de una nueva PT/IGRA a las 8-12 semanas para decidir la continuidad del tratamiento y adoptar medidas transitorias para reducir la transmisión. Los niños con infección tuberculosa deben recibir tratamiento preventivo con distintas pautas eficaces (6H/9H, 3HR o 4R), evitando la rifampicina en coinfectados por VIH y vigilando posibles hepatotoxicidades. La enfermedad tuberculosa requiere un régimen estándar de 6 meses (2HRZ(E)/4HR), con alternativas más cortas en casos no graves y ajustes en inmunodeprimidos o situaciones especiales, junto con un seguimiento estrecho de adherencia, toxicidad hepática y negativización microbiológica. La prevención se basa en el estudio de contactos, la vacunación BCG en grupos de riesgo y la mejora de determinantes sociales. El pediatra de Atención Primaria desempeña un papel esencial en la detección temprana, supervisión terapéutica y control de convivientes.
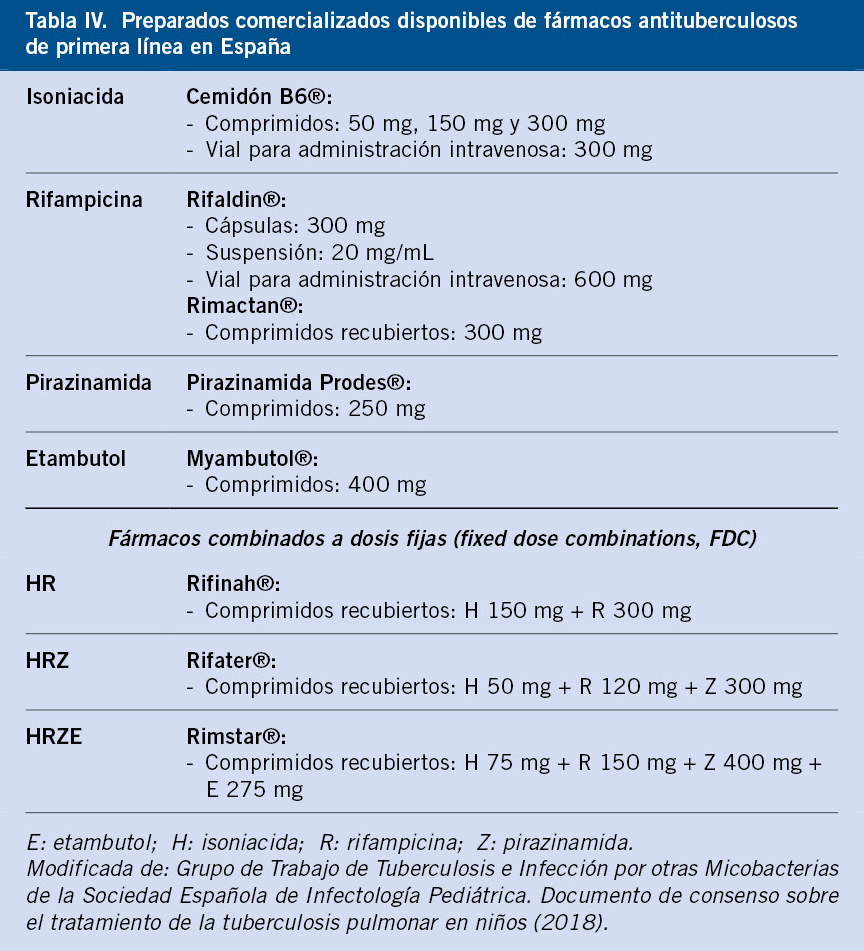
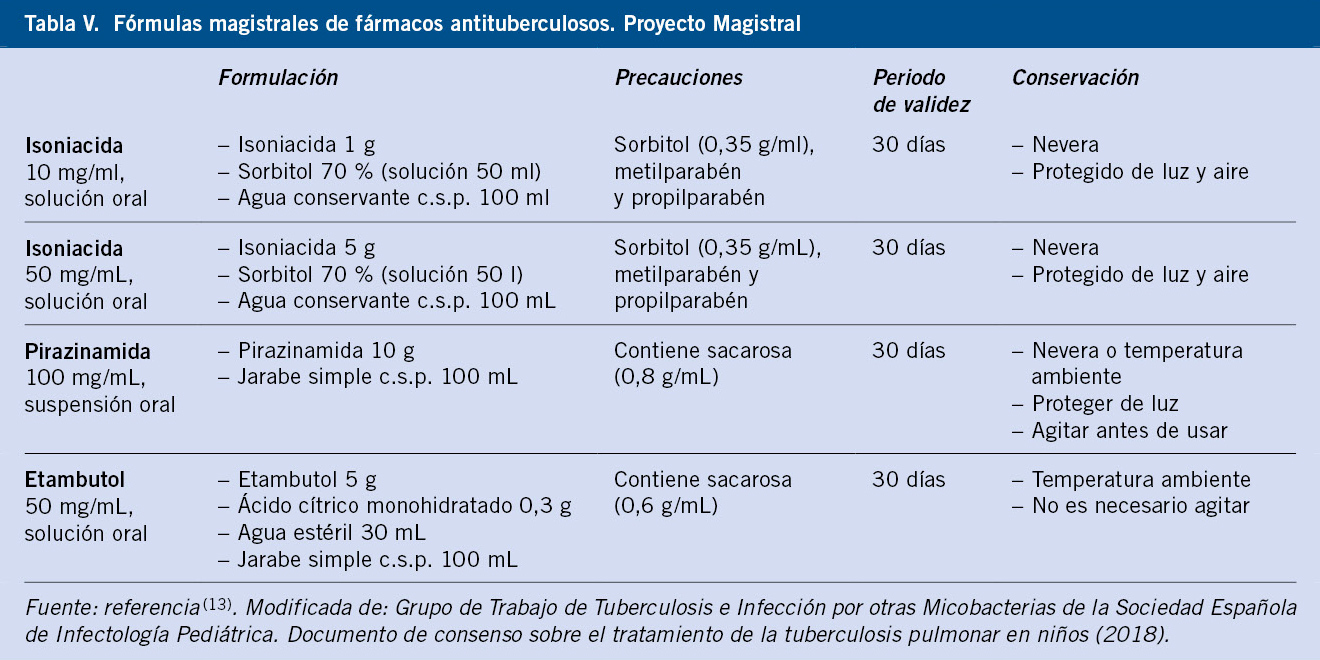
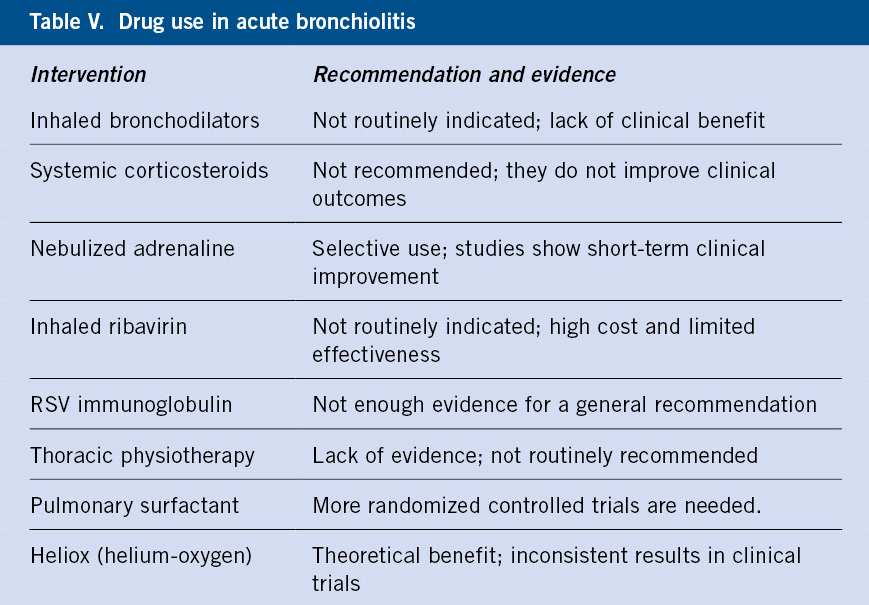
Exposición a TB sin infección (Tablas III-V)
Iniciar profilaxis con isoniazida en:
• Todos los niños menores de 5 años.
• Niños de cualquier edad con tratamiento inmunosupresor (uso prolongado de corticoides, anti-TNF-alfa, fármacos inmunosupresores, etc.) o comorbilidades del sistema inmunitario (VIH, insuficiencia renal crónica, tumores sólidos o hematológicos, inmunodeficiencias primarias, etc.).
Una vez transcurridas 8-12 semanas tras el último contacto de riesgo, se realizará nueva PT, independientemente de si recibió terapia o no. Se procederá según resultados:
• Si la segunda PT es < 5 mm (o IGRA negativo, si se hubiese realizado) en ausencia de clínica: retirar tratamiento preventivo, si se hubiese iniciado. En los niños infectados por VIH, dada la anergia, es prudente considerar a todos los expuestos como infectados y tratarlos como una ITB. Temporalmente, es importante intentar reducir la transmisión minimizando los contactos con los bacilíferos lo máximo posible según cada caso, habitualmente hasta completar 2 semanas de tratamiento adecuado. En recién nacidos de madres bacilíferas, se recomienda iniciar profilaxis con isoniazida durante, al menos, 12 semanas, tras descartar infección y enfermedad tuberculosa en el niño. Cuando la segunda PT/IGRA sea negativa a las 12 semanas, se puede interrumpir la profilaxis si la madre cumple bien el tratamiento o lo ha finalizado. Se recomienda repetir PT/IGRA a los 6 meses y al año. Se evaluará la conveniencia de la vacuna BCG. La lactancia materna no está contraindicada, salvo en la mastitis tuberculosa. Se recomienda extraer la leche y administrarla en biberón para evitar el contacto con el bebé en los siguientes casos: si la madre ha recibido menos de 2 semanas de terapia, si la madre sigue siendo bacilífera a pesar del tratamiento o si la cepa no es sensible a fármacos de primera línea.
• Si la segunda PT es ≥ 5 mm (o IGRA positivo, si se hubiese realizado): actuar según apartado ITB.
Tratamiento de la infección tuberculosa
Todos los niños y adolescentes diagnosticados de ITB deben recibir tratamiento para evitar el desarrollo de la enfermedad, siendo fundamental descartar enfermedad activa antes de iniciarlo. Existen varias pautas con eficacia similar(4):
• Isoniazida 6-9 meses (6H o 9H). En el paciente inmunocompetente se tiende a acortar a 6 meses.
• Isoniazida y rifampicina 3 meses (3HR). Especialmente recomendada en adolescentes o si se sospecha mala adherencia.
• Rifampicina 4 meses (4R). Esta pauta ha demostrado similar eficacia y seguridad a las pautas, mejorando la adherencia.
En niños coinfectados con VIH, no se recomiendan pautas con rifampicina; es un fármaco fundamental si desarrollara la enfermedad y podría quedar inutilizado. Además, la rifampicina interacciona con antirretrovirales, especialmente inhibidores de proteasas, disminuyendo sus niveles y aumentando la toxicidad de rifampicina.
El bajo riesgo de hepatotoxicidad en niños desaconseja realizar un control rutinario de transaminasas durante el tratamiento de ITB, salvo si aparece clínica compatible, enfermedad hepática de base o medicación hepatotóxica concomitante. En inmigrantes de países endémicos de hepatitis virales, VIH o esquistosomiasis, deben descartarse antes de iniciar tratamiento.
Tratamiento de la enfermedad tuberculosa
Régimen clásico
El régimen estándar de tratamiento de la TB es de 6 meses (2 meses HRZ(E) + 4 meses HR)(6). Dada la prevalencia de cepas resistentes a H en España (>4 %), debe asociarse E en la fase intensiva, si no se ha confirmado enfermedad por cepa sensible a fármacos de primera línea en el paciente o el caso índice.
En la primera fase, de inducción o bactericida, se produce una rápida disminución del número de bacilos, con mejoría clínica franca y disminución de la capacidad de contagio. En la segunda fase, de mantenimiento, tiene lugar la eliminación de bacilos en estado quiescente. Cuando se conozca la sensibilidad de la cepa y no existan resistencias, se pueden ajustar 3 fármacos en la fase de inducción (2 meses HRZ + 4 meses HR)(4). Este tratamiento consigue curación en >95 % de los casos, con escasos efectos adversos. Los fármacos deberán tomarse todos juntos y en ayunas. En pacientes con riesgo de incumplimiento, inmunodeprimidos o cepas resistentes, se recomienda tratamiento supervisado o directamente observado (TDO)(13).
Régimen corto en TB no grave(14)
En niños con TB no grave, se recomienda régimen corto de 4 meses (2 meses HRZ(E) + 2 meses HR), siempre que se cumplan los siguientes criterios:
• Edad mayor de 3 meses.
• TB no grave: TB ganglionar intratorácica sin obstrucción de vías respiratorias; TB pulmonar limitada a un lóbulo pulmonar, sin patrón miliar, sin cavernas, con derrame pleural no complicado; y TB ganglionar periférica.
• TB no bacilífera.
• No sospecha o evidencia de TB resistente.
Consideraciones y limitaciones a los regímenes cortos:
• Los niños y adolescentes que no cumplen los criterios de TB no grave deben recibir tratamiento estándar de 6 meses, o los regímenes recomendados para las formas graves de TB extrapulmonar.
• Los menores de 3 meses deben recibir siempre régimen de 6 meses.
• Los niños y adolescentes que han recibido tratamiento para la TB en los 2 años anteriores deben ser tratados con el régimen estándar de 6 meses (2 HRZ(E)/4 HR).
• En pacientes inmunodeprimidos, se recomienda tratamiento durante, al menos, 9 meses (idealmente 12 meses), con fase de inducción con cuatro fármacos hasta conocer la sensibilidad de la cepa en todos los niños. En los niños que viven con VIH y se encuentren en condiciones óptimas de su enfermedad de base, se seguirán las recomendaciones generales de los pacientes inmunocompetentes; no obstante, no deben recibir menos de 9 meses de tratamiento si la respuesta inicial o la recuperación inmunológica no son buenas. La rifampicina interfiere con los inhibidores de la proteasa, por lo que se debe valorar sustituirla por rifabutina; asimismo, puede interaccionar con no análogos de nucleósidos (efavirenz y nevirapina). Estos pacientes se deben derivar siempre a unidades de referencia para su manejo(15).
En España están disponibles (como medicamento extranjero) las formulaciones child-friendly en comprimidos dispersables de fármacos antituberculosos de primera línea para el tratamiento de la exposición a TB, de la ITB y de la enfermedad tuberculosa(16) (Tabla VI).
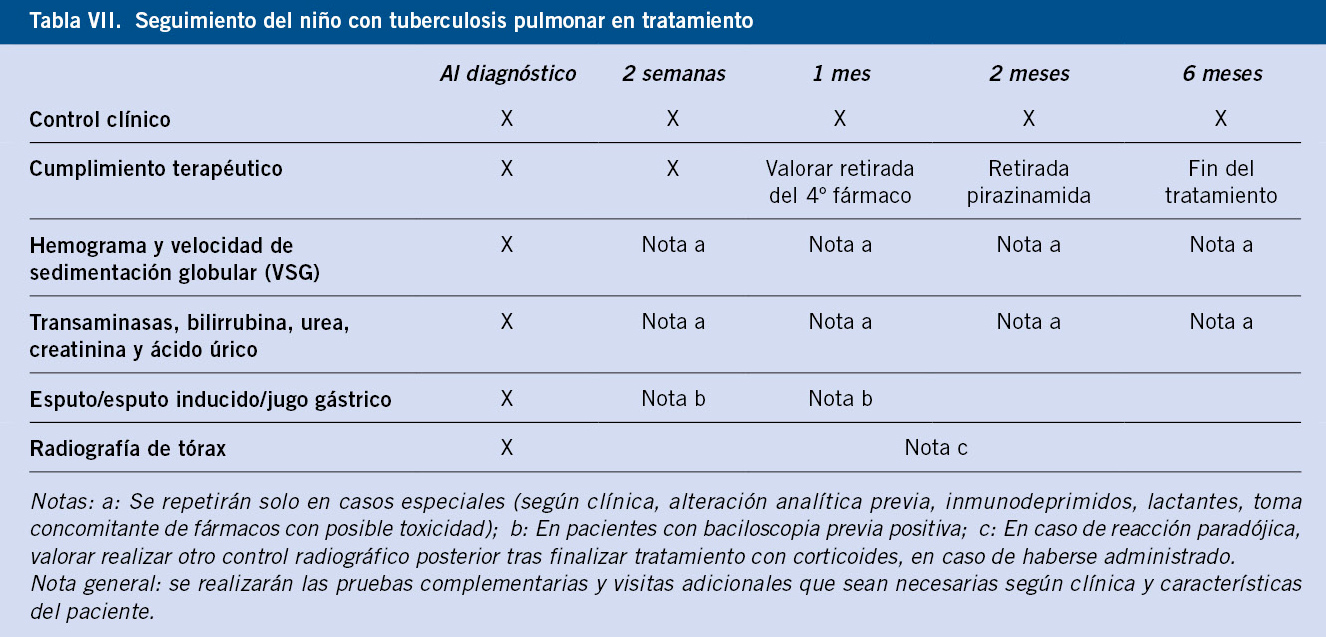
Seguimiento del niño con TB pulmonar (Tabla VII)
En el seguimiento del tratamiento de la TB en el niño es importante:
• Seguimiento de la adherencia, los problemas relacionados y la adecuación de la posología en cada visita: el mal cumplimiento es la causa más común de fracaso del tratamiento. En ocasiones, es posible utilizar el tratamiento directamente observado o la monitorización de los niveles plasmáticos de fármacos para monitorizar la adherencia.
• Evaluar la potencial toxicidad hepática: se recomienda el estudio y monitorización de la función hepática si aparecen signos o síntomas compatibles con hepatitis, si el paciente recibe otros fármacos potencialmente hepatotóxicos o si presenta otra patología que pueda cursar con hepatitis.
• En pacientes bacilíferos (habitualmente adolescentes): debe repetirse la baciloscopia periódicamente (cada 1-2 semanas) hasta comprobar su negativización, que permite finalizar el aislamiento respiratorio.
• Debe realizarse, al menos, un control clínico a las 2 semanas del inicio del tratamiento, a los 2 meses para pasar a fase de mantenimiento y, posteriormente, cada 2 meses hasta completar el tratamiento.
Criterios de ingreso hospitalario(17)
• <2 años.
• Formas pulmonares graves (derrames pleurales, atelectasias, etc.).
• Formas graves o diseminadas.
• Formas extrapulmonares, salvo ganglionares aisladas.
• Formas bacilíferas (adolescente con cavernas).
• Sospecha de enfermedad con resistencia a fármacos.
• Fracaso terapéutico previo (tras, al menos, 2 meses).
• Sospecha o riesgo de incumplimiento terapéutico.
• Inmunodeprimido.
• Recogida de muestras.
Tratamiento en unidades especializadas en TB
El tratamiento y seguimiento de niños inmunodeprimidos, con TB resistente, con formas complejas o con factores de riesgo de complicaciones, o con mala respuesta al tratamiento, se realizará en unidades expertas, con experiencia en esta patología(4).
Reacción paradójica
En los primeros 2 meses de tratamiento, puede aparecer reacción paradójica en un 5-10 % de los casos, caracterizada por un empeoramiento clínico-radiológico. En estos casos, se asociarán corticoides orales 2 mg/kg/día de prednisona o equivalente, durante 3-4 semanas, con descenso progresivo en 2 semanas(4).
Reacciones adversas
El efecto secundario más frecuente es la toxicidad hepática por isoniazida, rifampicina o pirazinamida, aunque más característicamente por isoniazida. En caso de hepatotoxicidad leve, se ajustará la dosis de isoniazida a 5 mg/kg/día. Si el paciente presenta sintomatología con transaminasas superiores a tres veces el límite normal o es asintomático con niveles superiores a cinco veces la normalidad, deberá interrumpirse el tratamiento y cualquier otro fármaco hepatotóxico. Deberá completarse el estudio etiológico de la hepatitis y monitorizar la función hepática. Cuando la hipertransaminasemia sea inferior al doble del límite normal y se hayan resuelto los síntomas clínicos, se reintroducirá inicialmente rifampicina y etambutol. Si la función hepática se mantiene estable a los 3-7 días, se puede reintroducir isoniazida y monitorizar tras 3-7 días. Nunca debe reintroducirse pirazinamida. Ante un nuevo empeoramiento de la función hepática, deberá diseñarse un nuevo régimen terapéutico en unidades de referencia. En cuanto al etambutol, el efecto secundario más frecuente es la neuritis óptica, que llevará a suspender el fármaco, aunque suele ser reversible.
Prevención
La prevención de la tuberculosis en niños combina estrategias destinadas a evitar la infección y a impedir su progresión a enfermedad. La identificación precoz y el estudio de contactos permiten detectar a los niños expuestos y ofrecer tratamiento preventivo cuando sea necesario, especialmente en menores de 5 años y en inmunodeprimidos. La vacunación con BCG sigue siendo clave en países de alta endemia y en grupos de riesgo, ya que reduce las formas graves, como la TB diseminada y la meningitis. Además, la mejora de las condiciones socioeconómicas, el adecuado acceso a los servicios sanitarios y el control de la transmisión en entornos comunitarios y escolares contribuyen significativamente a disminuir la incidencia(18-20).
Función del pediatra de Atención Primaria
La figura del pediatra de Atención Primaria es clave en la sospecha inicial de la TB pediátrica. Es fundamental que realice una buena anamnesis y exploración física, así como las pruebas de primer nivel disponibles (PT y radiografía de tórax). Si tras esta primera aproximación, existe una alta sospecha de enfermedad tuberculosa, el paciente debe ser remitido a unidades especializadas para completar el estudio, recoger muestras microbiológicas e iniciar el tratamiento.
El pediatra de Atención Primaria también desempeña un papel esencial en el seguimiento tras el inicio del tratamiento. Es fundamental monitorizar los efectos secundarios y asegurarse de una correcta adherencia, que es esencial para la recuperación del paciente y para frenar la transmisión. Este seguimiento también deberá realizarse en el caso de pacientes expuestos, en los que deberá confirmarse que no existe infección o enfermedad una vez transcurrido el periodo ventana (8-12 semanas). Por otro lado, el pediatra de Atención Primaria también puede implicarse en el estudio de contactos de la familia y de otros convivientes.
Conflicto de intereses
No hay conflicto de interés en la elaboración del presente manuscrito. Fuentes de financiación: PRM cuenta con financiación del Instituto de Salud Carlos III – Ministerio de Sanidad de España y Fondos Feder de la UE (Contrato Juan Rodés JR24/00015).
Bibliografía
Los asteriscos muestran el interés del artículo a juicio de las autoras.
1. Tebruegge M, Ritz N, Curtis N, Shingadia D. Diagnostic Tests for childhood tuberculosis: past imperfect, present tense and future perfect? Pediatr Infect Dis J. 2015; 34: 1014-9. Disponible en: https://doi.org/10.1097/inf.0000000000000796.
2. Marais BJ, Gie RP, Schaaf HS, Hesseling AC, Obihara CC, Starke JJ, et al. The natural history of childhood intra-thoracic tuberculosis: a critical review of literature from the pre-chemotherapy era. Int J Tuberc Lung Dis. 2004; 8: 392-402.
3. World Health Organization. Global Tuberculosis Report 2021. Geneva, Switzerland. Disponible en: https://www.who.int/teams/global-tuberculosis-programme/tb-reports.
4.** Baquero-Artigao F, Del Rosal T, Falcón-Neyra L, Ferreras-Antolín L, Gómez-Pastrana D, Hernanz-Lobo A, et al.; en representación de los Grupos de Trabajo en Tuberculosis de la Sociedad Española de Infectología Pediátrica y la Sociedad Española de Neumología Pediátrica. Update on the diagnosis and treatment of tuberculosis. An Pediatr (Engl Ed). 2023; 98: 460-9. Disponible en: https://doi.org/10.1016/j.anpede.2023.03.009.
5. European Centre for Disease Prevention and Control. Tuberculosis surveillance and monitoring in Europe 2021. Stockholm. Disponible en: https://www.ecdc.europa.eu/sites/default/files/documents/tuberculosis-surveillance-monitoring-Europe-2021.pdf.
6. Moreno-Pérez D, Andrés-Martín A, Altet Gómez N, Baquero-Artigao F, Escribano Montaner A, Gómez-Pastrana Durán D, et al. Diagnóstico de la tuberculosis en la edad pediátrica. An Pediatr (Barc). 2010; 72: 283.e1-e14.
7. Graham SM, Cuevas LE, Jean-Philippe P, Browning R, Casenghi M, Detjen AK, et al. Clinical case definitions for classification of intrathoracic tuberculosis in children: an update. Clinical Infectious Diseases. 2015; 61: S179-S187. Disponible en: https://doi.org/10.1093/cid/civ581.
8. Krutikov M, Faust L, Nikolayevskyy V, Hamada Y, Gupta RK, Cirillo D, et al. The diagnostic performance of novel skin-based in-vivo tests for tuberculosis infection compared with purified protein derivative tuberculin skin tests and blood-based in vitro interferon-release assays: A systematic review and meta-analysis. Lancet Infect Dis. 2022; 22: 250-64. Disponible en: https://doi.org/10.1016/s1473-3099(21)00261-9.
9. Martínez-Planas A, Baquero-Artigao F, Santiago B, Fortuny C, Méndez-Echevarría A, Del Rosal T, et al.; Spanish Pediatric TB Research Network (pTBred) and the European Nontuberculous MycoBacterial Lymphadenitis in childrEn (ENSeMBLE) Study. Interferon-Gamma Release Assays Differentiate between Mycobacterium avium Complex and Tuberculous Lymphadenitis in Children. J Pediatr. 2021; 236: 211-18.e2. Disponible en: https://doi.org/10.1016/j.jpeds.2021.05.008.
10. World Health Organization. The use of molecular line probe assays for the detection of resistance to second line anti-tuberculosis drugs. Policy guidance. Geneva, Switzerland. 2016. Disponible en: https://www.who.int/publications/i/item/9789241516136.
11. Mateos J, Estévez O, González-Fernández Á, Anibarro L, Pallarés Á, Reljic R, et al. High-resolution quantitative proteomics applied to the study of the specific protein signature in the sputum and saliva of active tuberculosis patients and their infected and uninfected contacts. J Proteomics. 2019; 195: 41-52. Disponible en: https://doi.org/10.1016/j.jprot.2019.01.010.
12. Nicol MP, Schumacher SG, Workman L, Broger T, Baard C, Prins M, et al. Accuracy of a Novel Urine Test, Fujifilm SILVAMP Tuberculosis Lipoarabinomannan, for the Diagnosis of Pulmonary Tuberculosis in Children. Clin Infect Dis. 2021; 72: e280-8. Disponible en: https://doi.org/10.1093/cid/ciaa1052.
13. Piñeiro Pérez R, Santiago García B, Rodríguez Marrodán B, Baquero-Artigao F, Fernández-Llamazares CM, Goretti López-Ramos M, et al.; Grupo de Trabajo del Proyecto Magistral de pTBred. Recomendaciones para la elaboración y administración de fármacos antituberculosos en niños. Segunda fase del Proyecto Magistral de la Red Española de Estudio de la Tuberculosis Pediátrica (pTBred). An Pediatr (Barc). 2016; 85: 323.e1-e11. Spanish. Disponible en: https://doi.org/10.1016/j.anpedi.2016.06.012.
14.** WHO consolidated guidelines on tuberculosis. Module 5: Management of tuberculosis in children and adolescents. Geneva: World Health Organization. 2022.
15. Documento de consenso sobre tratamiento antirretroviral en niños y adolescentes con infección por el virus de la inmunodeficiencia humana. Disponible en: https://www.sanidad.gob.es/ciudadanos/enfLesiones/enfTransmisibles/sida/publicaciones/2022/guias_TAR_ninos_enero_2022_def.pdf.
16. Noguera-Julian A, Buonsenso D, McKenna L, Seddon JA, Ritz N. Availability of fixed-dose, child-friendly formulations of first-line tuberculosis drugs in Europe. Eur Respir J. 2021; 58: 2101196. Disponible en: https://doi.org/10.1183/13993003.01196-2021.
17. Manual de Diagnóstico y Terapéutica en Pediatría, 7ª ed. Ed. Panamericana. 2025.
18. Mellado Peña MJ, Santiago García B, Baquero-Artigao F, Moreno Pérez D, Piñeiro Pérez R, Méndez Echevarría A, et al. Actualización del tratamiento de la tuberculosis en niños. An Pediatr (Barc). 2018; 88: 52.
19.** Turkova A, Wills GH, Wobudeya E, Chabala C, Palmer M, Kini-kar A, et al. Shorter Treatment for Nonsevere Tuberculosis in African and Indian Children. N Engl J Med. 2022; 386: 911-22. Disponible en: https://doi.org/10.1056/nejmoa2104535.
20. Ramos Amador JT, Berzosa Sánchez A, Callejas Caballero I, Illán Ramos M. Tuberculosis pulmonar en Pediatría. Pediatr Integral. 2021; 2: 76-90. Disponible en: https://www.pediatriaintegral.es/publicacion-2021-03/tuberculosis-pulmonar-en-pediatria/.
Bibliografía recomendada
– Baquero-Artigao F, Del Rosal T, Falcón-Neyra L, Ferreras-Antolín L, Gómez-Pastrana D, Hernanz-Lobo A, et al.; en representación de los Grupos de Trabajo en Tuberculosis de la Sociedad Española de Infectología Pediátrica y la Sociedad Española de Neumología Pediátrica. Update on the diagnosis and treatment of tuberculosis. An Pediatr (Engl Ed). 2023; 98: 460-9. Disponible en: https://doi.org/10.1016/j.anpede.2023.03.009.
Artículo de consenso y actualización en el diagnóstico y tratamiento de la TB pediátrica, que aúna la visión de pediatras expertos en su manejo.
– Turkova A, Wills GH, Wobudeya E, Chabala C, Palmer M, Kini-kar A, et al. Shorter Treatment for Nonsevere Tuberculosis in African and Indian Children. N Engl J Med. 2022; 386: 911-22. Disponible en: https://doi.org/10.1056/nejmoa2104535.
Primer ensayo clínico realizado específicamente en población pediátrica, que demuestra que los niños con tuberculosis no grave pueden tratarse eficazmente con un régimen más corto de 4 meses, en lugar de los 6 meses tradicionales. Esto supone un cambio potencial en la práctica clínica mundial, ya que acorta la duración del tratamiento sin comprometer la eficacia ni la seguridad, reduce el riesgo de abandono terapéutico, disminuye la carga para las familias y los sistemas sanitarios, y facilita la expansión de estrategias de tratamiento directamente observado.
| Caso clínico |
|
Motivo de consulta: contacto estrecho con paciente bacílifera diagnosticada de tuberculosis (TB) pulmonar. Anamnesis: varón de 13 meses, de origen español, remitido para estudio por contacto estrecho con su cuidadora, diagnosticada de tuberculosis pulmonar bacilífiera. El menor se encuentra asintomático. La cuidadora es una mujer de 35 años, procedente de Filipinas, que reside en España desde hace 2 años. Presenta tos con expectoración de 3 meses de evolución. En la radiografía de tórax se objetiva una caverna en lóbulo superior derecho. Se realiza estudio de esputo: baciloscopia positiva; PCR (Xpert Ultra): positivo (sin mutaciones de resistencia a R); y cultivo con cepa sensible. La paciente convive con su marido y sus hijos de 14 y 9 años. Antecedentes personales: se trata de un niño de 13 meses sano, sin enfermedades relevantes. Tomó medicación antirreflujo (ranitidina) hasta los 3 meses, actualmente sin tratamiento. Desarrollo psicomotor normal. Nacido en España, no vacunado de BCG. Exploración física por aparatos: sin alteraciones. Pruebas complementarias: se realiza en su centro de salud: prueba de tuberculina: 8 mm; y radiografía de tórax: adenopatía hiliar. Es remitido a una unidad especializada en TB para completar estudio: analítica con perfil hepático: normal; estudio de jugo gástrico: baciloscopia negativa; PCR (Xpert Ultra): positivo (sin mutaciones de resistencia a R); cultivo pendiente; PCR (Xpert Ultra) en heces: negativo. Juicio diagnóstico: enfermedad tuberculosa. Tratamiento: dado que cumple criterios de TB no grave y la cepa del caso índice es sensible, se puede realizar una pauta corta de tratamiento de 4 meses. Se inicia tratamiento con tres fármacos, ya que conocemos la sensibilidad de la cepa del caso índice: H+R+P 2 meses, seguido de H+R 2 meses. Se solicita a medicamentos extranjeros la dispensación de formulaciones bucodispersables para facilitar su administración. Debe tomar todos los fármacos juntos durante todos los días, por las mañanas, en ayunas. Indicamos a la familia que es posible que la medicación tiña los fluidos corporales de coloración naranja. También le indicamos que el caso índice debe estar aislado hasta cumplir, al menos, dos semanas de tratamiento y comprobar negativización de la baciloscopia. Seguimiento: se realiza seguimiento conjunto por parte de su pediatra de Atención Primaria y de la unidad especializada de TB. Se realizan visitas a las 2 semanas del inicio del tratamiento, a los dos meses y a los 4 meses. En cada visita se confirma la adecuada adherencia al tratamiento y se ajusta la dosis al peso. A los dos meses, se retira pirazinamida y se mantiene isoniacida y rifampicina hasta completar los 4 meses de tratamiento. Se realiza estudio de contactos en los convivientes de la cuidadora (marido y dos hijos).
|