|
| Temas de FC |
R. Ortiz de Lejarazu*, S. Tamames**
*Consejero científico y Director emérito. Centro Nacional de Gripe de Valladolid. **Dirección de Salud Pública, Consejería de Sanidad, Junta de Castilla y León
| Resumen
Los virus gripales de la gripe A tienen un reservorio animal muy extenso y los saltos de especie provocan gripe zoonótica que son fuente de las variantes pandémicas. Las epidemias estacionales de gripe están causadas por subtipos del virus A (H3 y H1) y linajes del tipo B (Victoria y Yamagata) que duran unas 10-12 semanas y ocurren de forma variable entre diciembre y marzo en países de clima templado. La gripe es una enfermedad sistémica y multiorgánica que se inicia en el tracto respiratorio superior, pudiendo progresar por vecindad al tracto respiratorio inferior o producir cuadros graves sistémicos mediados por citoquinas inflamatorias. |
| Abstract
Influenza A viruses have a very extensive animal reservoir, in whom host jumps cause zoonotic influenza and thereby being a source of pandemic variants. Seasonal influenza epidemics are caused by subtypes of virus A (H3 and H1) and type B lineages (Victoria and Yamagata) which last about 10-12 weeks between December and March in temperate climate countries. Influenza is a systemic and multiorgan disease that initiates in the upper respiratory tract, being able to progress by vicinity to the lower respiratory tract and/ or produce severe systemic pictures mediated by inflammatory cytokines. |
Palabras clave: Vacuna de gripe; Gripe; Pediatría; Virus.
Key words: Flu vaccine; Influenza; Pediatrics; Virus.
Pediatr Integral 2020; XXIV(8): 469 –478
Vacunas de gripe
La gripe es una gran desconocida en sus aspectos más básicos, aquellos que ayudan a comprender la génesis de las pandemias, las epidemias y las vacunas. La parte clínica, que es lo menos variable, ha tenido nuevos planteamientos patogénicos en la última década. La gripe debe considerarse como una infección respiratoria y sistémica causada por los virus gripales que infectan preferentemente a niños y jóvenes, y es causa de muerte de personas mayores y vulnerables. Entre estas últimas, están aquellas personas con patologías crónicas subyacentes o condiciones físicas determinadas (obesidad), que se han confirmado como de riesgo para complicaciones. La infección gripal puede acarrear en determinadas personas, un proceso grave y, a veces, mortal por agravamiento o descompensación de sus patologías o constantes vitales, inducido por una importante respuesta proinflamatoria con citoquinas específicas que impide el control del virus y favorece su extensión.
Aunque, en general, la infección gripal es una enfermedad autolimitada, leve o moderada en adultos y jóvenes sanos, a partir del año 2000, se puso de manifiesto que los niños y, especialmente por debajo de 2 años, constituyen un grupo de especial riesgo para la hospitalización por gripe(1,2). Así, la gravedad se concentra especialmente en los dos extremos de la vida, niños y personas mayores. Los niños en la gripe actúan además, como superdiseminadores, debido a la mayor carga viral y mayor duración de la excreción vírica; su vacunación selectiva ha demostrado modificar parcialmente el curso de las epidemias de gripe(3) y, también, efectos sobre la mortalidad específica por neumonía y gripe(4).
Por otra parte, existen factores víricos y del huésped no totalmente conocidos que pueden modificar su curso clínico, siendo característico de la gripe: su imprevisibilidad, variabilidad biológica, antigénica y genética, así como la epidemiológica (tiempo, virus, personas, geografía, etc.), de tal forma que las epidemias de gripe tienen distintos perfiles de gravedad general y poblacional anuales, lo que dificulta de forma especial los ensayos de fármacos y vacunas(5,6).
Desde la aparición, en diciembre de 2019, del coronavirus SARS-CoV-2 responsable de la pandemia de COVID-19, primera causada por un coronavirus, las comparaciones con la gripe fueron inevitables y, como se ha comprobado con el trascurso del tiempo, algunas de ellas no muy acertadas. Sin embargo, la sintomatología en los niños, puede facilitar la confusión clínica de COVID-19 y gripe. Otros factores, como los colegios y guarderías, elementos clásicos clave en la difusión de las epidemias de gripe, no parecen jugar idéntico papel para la difusión de la COVID-19; por lo que, bajo el principio de disminución de la carga de enfermedad, la vacunación de gripe en Pediatría, se ha empezado a considerar desde otra perspectiva.
Virus de la gripe
Los virus gripales tienen segmentos de ARN y están cubiertos por una membrana en la que se anclan tres glicoproteínas: hemaglutinina, neuraminidasa y M2.
Los virus de la gripe pertenecen a la familia Orthomyxoviridae, compuesta por virus de forma esferoide y unos 100-120 nm de tamaño, de simetría helicoidal y provistos de ARN monocatenario segmentado de polaridad negativa (precisan un intermediario de replicación positivo). Están cubiertos por una membrana de envoltura de naturaleza fosfolipídica, en la que se anclan dos tipos distintos de espículas de naturaleza glicoproteíca denominadas: hemaglutinina (H) y neuraminidasa (N). Ambas son antígenos dominantes del virus, especialmente la H de la que existen 18 tipos distintos por 11 de la N(7). Esta última tiene fármacos inhibidores (zanamivir, oseltamivir y peramivir). Además, en la superficie del virus hay canales iónicos que atraviesan la membrana de envoltura, formados por la glicoproteina M2 que juegan un papel importante en la replicación del virus dentro de la célula huésped y es diana farmacológica para los adamantanos (amantadina y rimantadina). El ARNmc está dividido en 8 segmentos que codifican las proteínas estructurales y no estructurales del virus (Fig. 1) y poseen, cada uno de ellos, su propia polimerasa sobre la que actúa el baloxavir marboxil, antiviral especifico frente a gripe de dosis única.
Figura 1. Estructura del virus de la gripe A.
Existen 4 tipos de virus de la gripe (A, B, C y D), aunque solo tres pueden infectar regularmente a los humanos (el D infecta principalmente al ganado) y solo dos de ellos tienen capacidad epidémica estacional (los virus de la gripe A y los de la B). Solo los virus del tipo A son capaces de generar pandemias.
Los virus de la gripe A se dividen en subtipos, según las dos glicoproteínas de la superficie del virus: hemaglutinina (H) y neuraminidasa (N). Existen 18 subtipos de hemaglutinina y 11 subtipos de neuraminidasa diferentes (de H1 a H18 y de N1 a N11, respectivamente). Si bien, existen potencialmente 198 combinaciones de subtipos de gripe A, solo se han detectado 131 subtipos en la naturaleza. Actualmente, circulan en el mundo los subtipos de virus de la gripe A(H1N1) y A(H3N2). Los subtipos de la gripe A pueden dividirse en diferentes “clados” y “sub-clados” genéticos, como consecuencia de la enorme variabilidad que experimentan y la presión biológica ejercida sobre ellos al circular en los humanos. Especialmente importantes son algunos del subtipo H3 (3C.2a1, 3C.2a1b y 3C.3a) con cepas que no hemaglutinan, de más difícil caracterización antigénica. Los de virus de la gripe B han evolucionado, desde finales de los años 70, en dos linajes divergentes y distintos, el B/Victoria y el B/Yamagata, que aunque comparten epítopos antigénicos comunes, la vacunación de uno de ellos no necesariamente ofrece protección cruzada contra el otro; de ahí, la razón de las vacunas tetravalentes de gripe.
La nomenclatura de las cepas de virus de la gripe humana se hace expresando: en primer lugar, el tipo de virus (A, B, C, etc.); seguido del lugar de procedencia o aislamiento (Valladolid, Brisbane, Phuket, etc.); número de laboratorio; y año de aislamiento. A continuación, entre paréntesis, se especifica el subtipo (H3N2, H1N1, etc.). En las cepas de virus del tipo B no hay subtipos y se añade el linaje al que pertenecen.
Las cepas incluidas en las vacunas anuales de gripe siguen dicha nomenclatura:
• A/Brisbane/02/2018 (H1N1).
• A/Kansas/14/2017 (H3N2).
• B/Colorado/06/2017 (B/Victoria/2/87 lineage).
• B/Phuket/3073/2013 (B/Yamagata/16/88 lineage).
La variabilidad de los virus de la gripe obedece a dos fenómenos distintos, uno es el reordenamiento genético con intercambio de genes entre dos virus parentales que infectan un mismo huésped, exclusivo de los virus A, que da lugar a las variantes mayores pandémicas; y el otro, es la deriva antigénica que ocurre tanto en el tipo A como en el B, consecuencia de la difusión estacional año tras año de las variantes mayores de unas personas a otras, que van seleccionando las cepas mutadas más adaptadas y capaces de infectar y resistir la inmunidad preexistente.
Reservorio
La gripe A tiene un reservorio animal muy extenso y los saltos de especie provocan gripe zoonótica, generalmente más letal y potencial fuente de las variantes pandémicas.
Los virus de la gripe A se caracterizan por tener múltiples hospedadores de diferentes especies animales. En general, se cree que son exclusivamente virus humanos, cuando en realidad, hay más cepas de gripe infectando a los animales que a humanos. Los virus de la gripe poseen la capacidad de franquear la llamada “barrera de especie”, por la cual virus de la gripe de aves o de otros animales (cerdos, caballos, focas) pueden transmitirse e infectar al hombre. Esta propiedad junto con la extrema variabilidad genética que poseen y la especial respuesta inmune de los humanos frente a ellos, configuran una trilogía que permite que la gripe sea una enfermedad que se distribuye entre huéspedes animales y humanos, lo que añade una dificultad adicional al desarrollo de vacunas erradicadoras de la enfermedad. La gripe tiene un reservorio animal muy extenso, sobre todo, en anátidas salvajes migratorias. El sistema inmunitario de las aves presenta una memoria inmunológica de corta duración frente a la gripe, lo que permite que una cepa de virus gripal pueda mantenerse durante mucho tiempo en poblaciones aviares por infecciones repetidas, incluso asintomáticas, con escasa presión biológica inmune, pudiendo transmitirse a otras aves o a otros animales con los que conviva, facilitando fenómenos de reordenamiento genético por infecciones dobles. Se puede decir que las aves constituyen el banco o reservorio genético de los virus de la gripe A.
En el reservorio animal, los virus de la gripe disponen de innumerables oportunidades para hacer reordenamientos genéticos, cuando se dan infecciones por más de un virus diferente en un mismo huésped. Estos reordenamientos originan virus nuevos por mezcla e intercambios entre los ocho segmentos de ARN que tiene cada virus. La respuesta inmune juega un papel muy importante; mientras que en las aves es de corta duración, pero de amplio espectro; en los seres humanos es muy específica y de larga duración. Este aspecto que parece una gran ventaja, tiene inconvenientes para la consecución de vacunas humanas de amplio espectro inmunitario (frente a muchas cepas de subtipos diferentes) e inmunidad de larga duración.
La hemaglutinina de los virus gripales humanos se une específicamente a receptores N-Acetil Neuramínico en posición α-2,6 (Neu.α-2,6) que se encuentran fundamentalmente en el epitelio respiratorio superior, mientras que los virus aviares usan el receptor Neu α-2,3 localizado preferentemente en el epitelio digestivo de las aves. A pesar de esta especificidad biológica, durante los últimos 30 años, han ocurrido varios brotes de diversa importancia en el ser humano causados por virus aviares, sobre todo, en el sureste asiático, por virus de los subtipos: A(H5N1), A(H7N9) y A(H9N2), algunos con tasas de mortalidad del 30 al 60%, según el subtipo.
Epidemiología
La gripe es una enfermedad estacional cuyas epidemias duran unas 10-12 semanas y ocurren de forma variable entre diciembre y marzo en países de clima templado.
La gripe humana es una enfermedad respiratoria estacional epidémica, de recurrencia anual, que se presenta en los países de clima templado durante los meses más fríos del año en ambos hemisferios. Las epidemias se caracterizan por un comienzo abrupto de casos que asciende exponencialmente hasta alcanzar el pico epidémico en cuatro o cinco semanas, descendiendo después a niveles no epidémicos de forma más paulatina. Sin embargo, la gripe se comporta de forma diferente en países con clima tropical y subtropical, mostrando un bajo, pero constante número de casos durante todo el año, sin mostrar picos epidémicos claros o estando estos ligados a la estación húmeda, tendiendo en estas zonas a una presentación de tipo endémica(8).
La recurrencia de las epidemias gripales está relacionada con: variabilidad del virus, memoria inmune y niveles de anticuerpos. La protección es de por vida para la cepa que origina una infección natural, pero la deriva antigénica del virus y la evanescencia parcial de anticuerpos, hacen que sean posibles las reinfecciones por otras cepas, variantes menores del mismo subtipo, en el trascurso del tiempo.
Patogenia
La gripe comienza infectando el tracto respiratorio superior, puede extenderse por vecindad al tracto respiratorio inferior o producir síntomas sistémicos mediados por citoquinas inflamatorias.
La infección gripal se inicia por la fijación del virus a los receptores mucoprotéicos de las células del epitelio columnar respiratorio, donde tiene lugar una intensa replicación en los dos o tres días siguientes y un periodo más largo en niños. Se eliminan grandes dosis infectantes por microgotas emitidas al hablar, estornudar o toser(9,10).
El virus difunde por contigüidad desde la mucosa a otros tejidos respiratorios, ocasionando un proceso inflamatorio con necrosis del epitelio ciliado del tracto respiratorio superior; pudiendo, en algunos casos, afectar al tracto respiratorio inferior (bronquios, bronquiolos y alvéolos), causando serias complicaciones. La infección gripal tiene también una repercusión sistémica importante, además de síntomas respiratorios, mediada por una liberación de citoquinas proinflamatorias que acuñó la expresión “tormenta citoquínica”. La incidencia mayor en los niños y la gravedad mayor en los ancianos, se relaciona con las experiencias antigénicas previas, la posible patología subyacente y el papel que juegan colegios y guarderías como factores de agregación que favorecen la difusión. Por tanto, en la gravedad de la gripe no solo influye el virus y la cepa causal, sino también los factores de riesgo presentes en los individuos infectados. Los individuos que desarrollan un cuadro grave no logran controlar adecuadamente la replicación celular del virus en el organismo, debido a defectos en la inmunidad innata inicial (Fig. 2). El cuadro grave que presentan se asemeja bastante al de sepsis, siendo importante el diagnóstico virológico de gripe a los 2-3 días de mala evolución de los casos pediátricos ambulatorios.
Figura 2. Respuesta inmunológica innata frente al virus de la gripe. Modificado de: Bermejo-Martin JF, et al. Crit Care. 2009; 13: R201.
Manifestaciones clínicas generales
El síndrome gripal clásico comienza por los síntomas sistémicos (fiebre de aparición brusca, cefalea y quebrantamiento general), seguido por síntomas respiratorios.
Los virus gripales producen el síndrome gripal, cuadro clínico más frecuente causado, tanto por los virus de la gripe A como por los de la B. Los virus C producen cuadros respiratorios de vías altas sin la repercusión sistémica de la gripe y, en general, más banales. Los D, cuadros en el ganado y escasos en humanos. Al inicio, las manifestaciones sistémicas predominan sobre las respiratorias. El espectro de signos y síntomas de la gripe es muy amplio, aunque los básicos son: fiebre franca de inicio brusco, cefalea, quebrantamiento general y síntomas respiratorios. Los síntomas pueden cambiar en función de edad, hábitos de la persona, procesos gripales sufridos anteriormente, virulencia de las cepas y enfermedades subyacentes. La vacunación no solo reduce la mortalidad y la hospitalización, sino que limita la duración de los síntomas y la intensidad de los mismos. La infección gripal puede producir también formas ambulatorias leves semejantes al resfriado común, bronquitis aguda o faringitis e infecciones inaparentes. Los niños menores de un año tienen un riesgo de hospitalización por gripe similar a los individuos mayores de 65 años, aunque la mortalidad es sensiblemente menor(2).
La gripe en niños y adolescentes
La gripe en niños es más frecuente, más transmisible y ocasiona fiebre más alta que en adultos. En los más pequeños puede ser inespecífica, presentar clínica gastrointestinal y presentar complicaciones o signos y síntomas de gravedad.
Aproximadamente 2-3 de cada 10 niños contraen la gripe cada año(11). Los niños son más susceptibles a la infección gripal y juegan un papel decisivo en la difusión de la enfermedad en el hogar y los colegios, eliminando más cantidad de virus(carga viral más alta) y durante un tiempo más prolongado (10-15 días) que los adultos(12).
La infección gripal en los niños y adolescentes ocasiona fiebre más elevada que en adultos. Los neonatos, a menudo, presentan síntomas poco específicos con apnea y rechazo del alimento, y cuadros respiratorios que puedan imitar, a veces, al crup o producir bronquiolitis. En casi la mitad de los niños menores de cuatro años, se aprecia somnolencia y letargia(13,14) (Tabla I).
En más del 20% de los niños hospitalizados, menores de cinco años, se pueden observar cuadros convulsivos y una mayor incidencia de otitis media (4-5%). En lactantes menores de seis meses, se dan: abdominalgias, vómitos y diarrea. El síndrome sistémico gripal puede ser especialmente intenso y postrante en niños pequeños, encontrándose la CPK elevada y la GOT discretamente elevada, como manifestaciones enzimáticas de la afectación muscular.
Complicaciones de la gripe
Dos terceras partes de los niños que sufren una hospitalización por gripe grave, no presentaban ningún factor de riesgo conocido previo.
Las complicaciones de la gripe se presentan en todas las edades; sin embargo, son más frecuentes en niños menores de dos años, además de las personas con: patologías crónicas subyacentes, inmunosupresión o edad avanzada(15). Algunas, como el síndrome de Reye, son exclusivas de niños y jóvenes. Las más frecuentes son las respiratorias y, entre las no respiratorias, se incluyen: manifestaciones cardiovasculares, musculares, nerviosas, renales, endocrinas, gastrointestinales y hemáticas.
Las complicaciones más frecuentes en niños son: otitis media, traqueobronquitis, laringotraqueitis y bronquiolitis. La bronquitis aguda es la complicación respiratoria más frecuente, especialmente en pacientes naïve. La más grave es la neumonía primaria viral, asociada a subtipos A (H3 y H1). La sintomatología gripal típica da paso a fiebre alta continuada, tos, disnea y cianosis con hipoxemia acusada. En las pruebas de imagen, aparecen infiltrados bilaterales difusos de localización peribronquial sin consolidación. El deterioro de la función pulmonar es rápido y la mortalidad elevada. La neumonía secundaria por sobreinfección bacteriana por: S. pneumoniae, H. influenzae y S. aureus, microorganismos más frecuentes, ocurre tras una pequeña remisión de la sintomatología gripal 11 a 14 días después del inicio del síndrome gripal. La forma bronconeumónica es la más frecuente y grave, y ha sido responsable de más del 80% de las muertes ocurridas en las pasadas pandemias de gripe. Una complicación típica de niños y adolescentes (2-18 años) es el síndrome de Reye; una encefalopatía acompañada de degeneración hepática grasa que cursa con una alta letalidad (10-40%). Se presenta como una complicación de la gripe B y, con menor frecuencia, de la gripe A. También, se ha asociado a otras infecciones víricas, sobre todo, a varicela. La incidencia tras la infección gripal se ha estimado en 0,3 a 0,8 casos por 100.000 menores de 18 años; existiendo formas leves más frecuentes. Otras complicaciones raras son: encefalitis y encefalopatía, Guillain-Barré, miositis, fracaso renal, síndrome de coagulación intravascular y síndrome hemofagocítico. El registro de casos graves del Sistema de Vigilancia de la Gripe en España (SVGE) muestra como, la hospitalización ha sido más alta cuando circula el nuevo virus H1N1 (1,4%) y menor cuando circula el subtipo H3 o el virus B (0,4-0,5%)(16). Los pacientes inmunodeprimidos pediátricos tienen una mayor persistencia y excreción del virus gripal, y sufren con mayor frecuencia neumonía primaria viral. En trasplantados, la mortalidad se asocia con el grado de neutropenia.
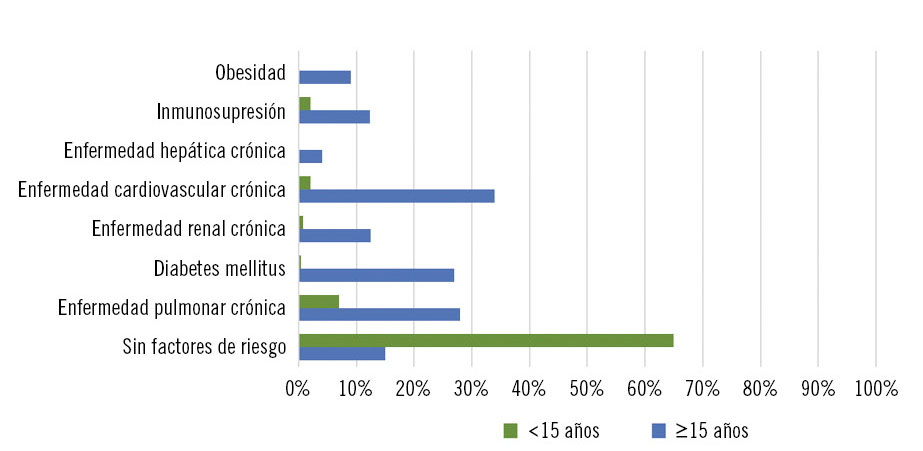
La gripe grave en niños y adolescentes se presenta, la mayoría de las veces, sin ningún antecedente de riesgo, haciendo que la hospitalización de estos individuos se demore en el tiempo, lo que añade mayor riesgo de muerte (Fig. 3).
Figura 3. Prevalencia de factores de riesgo por grupos de edad, de los casos graves hospitalizados con diagnóstico de gripe, temporada 2019-20. Modificado de: Sistema de Vigilancia de la Gripe en España (http://vgripe.isciii.es).
La capacidad de difusión de la gripe y su alta morbilidad pediátrica hace que sobrecargue los servicios sanitarios, especialmente los de Atención Primaria pediátrica. La gripe tiene repercusión también sobre la mortalidad y eleva los costes sociosanitarios directos e indirectos en Pediatría(1,17). Estados Unidos y Canadá han implementado la recomendación universal de vacunar con especial énfasis a los niños, recomendación que, en la mayor parte de Europa, no existe de forma real, a excepción del Reino Unido y Finlandia.
Tipos de vacunas frente a la gripe
Existen diferentes tipos de vacunas antigripales que aportan diferentes ventajas. La más significativa es la concordancia frente a los dos linajes B que ofrecen las vacunas tetravalentes.
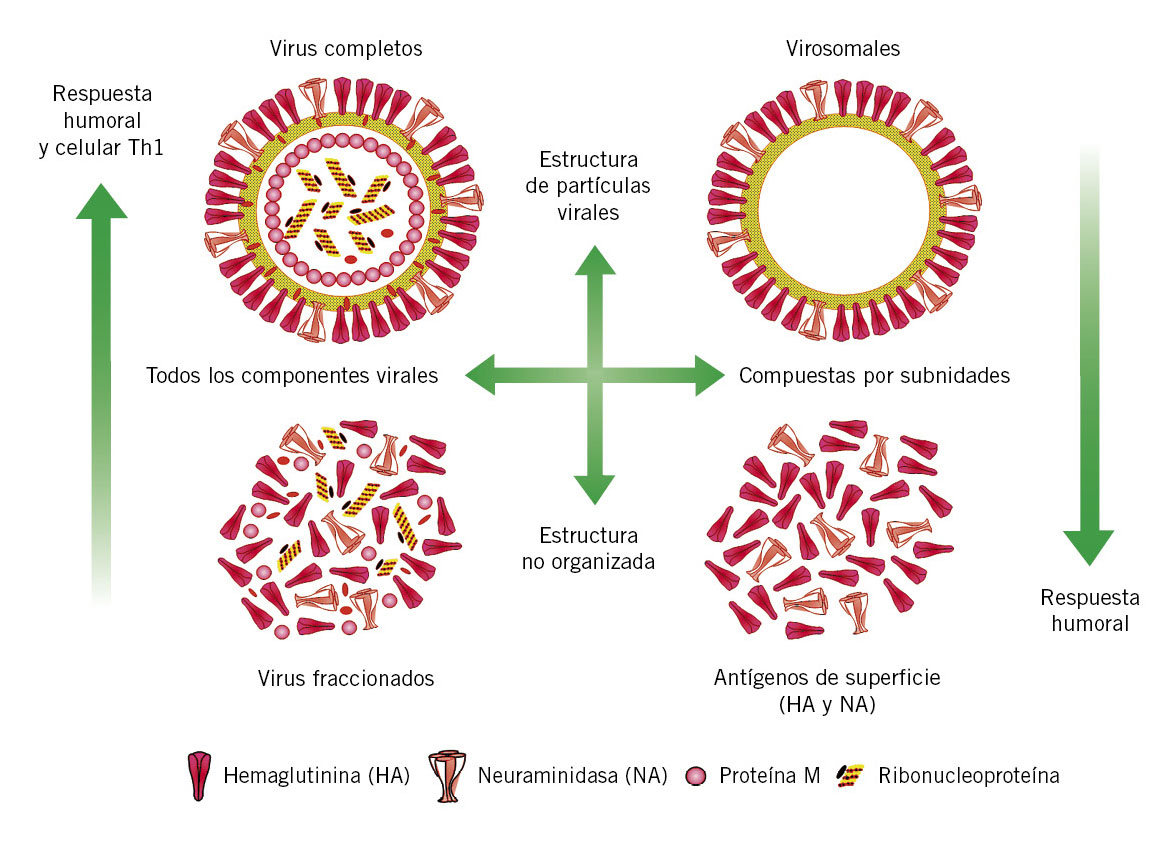
Existen diferentes tipos de vacunas frente a la gripe(18). En función de su composición, distinguimos vacunas de virus vivos atenuados y vacunas inactivadas que, a su vez, pueden ser de virus fraccionados o de subunidades (Fig. 4).
Figura 4. Inmunogenicidad y composición de las vacunas antigripales. Tomado de: Ortiz de Lejarazu R, Tamames S. Enferm Infecc Microbiol Clin. 2015; 33: 480-90.
El antígeno común a todas las vacunas antigripales es la hemaglutinina. Las vacunas de virus vivos atenuados se administran por vía intranasal y están autorizadas en España para su uso entre los 2 y 17 años, sin embargo, no están comercializadas. Su principal limitación es que no pueden administrarse en niños con inmunodeficiencias, además de presentar potenciales alérgenos en su composición. Reino Unido utiliza estas vacunas con éxito en su programa de inmunización infantil poblacional, logrando protección directa e indirecta frente a la gripe.
Las vacunas inactivadas continúan siendo las más extendidas en Europa. La mayoría de ellas se administran por vía intramuscular y algunas pueden administrarse por vía subcutánea profunda. Las vacunas trivalentes están siendo sustituidas por las tetravalentes. En la composición de las primeras, se incluyen solo tres cepas de virus gripales: A(H1N1), A(H3N2) y un linaje B, mientras las segundas incluyen dos subtipos de gripe A y dos linajes de gripe B, aumentando la concordancia entre la composición de la vacuna y los linajes circulantes del tipo B. Estas vacunas son especialmente adecuadas para la primo vacunación en Pediatría, ya que proporcionan un desafío inmune más completo.
Otro aspecto diferencial entre vacunas antigripales es su producción. La tecnología clásica de producción se basa en el cultivo viral en huevos embrionados de pollo. Las vacunas producidas en huevo autorizadas en España pueden emplearse a partir de los 6 meses de edad con la excepción de Influvac® e Influvac tetra® de Mylan, que están autorizadas a partir de los 3 años.
Actualmente, van tomando protagonismo sistemas de producción basados en células. Entre las ventajas de la producción en células destacan: la potencial flexibilización de la capacidad de producción y que se evitan los cambios que sufre el virus adaptado a huevo respecto a la cepa humana salvaje, lo cual podría redundar en una mayor concordancia entre la vacuna y la cepa circulante. Además, los sistemas de producción que no utilizan el cultivo en huevos embrionados, no conllevan presencia de proteínas de huevo en las vacunas y evitan el uso de antibióticos que es frecuente en las vacunas producidas en huevos embrionados. La presencia de antibióticos, generalmente aminoglucósidos en las vacunas, pueden suponer una contraindicación para su uso en alérgicos. No así, la presencia de proteínas del huevo, que constituyen un motivo de precaución en alérgicos a estas, pero no una contraindicación, ni siquiera con antecedentes de reacción anafiláctica. La vacuna producida en células comercializada en España, Flucelvax tetra®, está autorizada a partir de los dos años.
Otro sistema que presenta ventajas análogas al cultivo viral en células es la producción de antígenos, como expresión génica inducida por baculovirus recombinante en células de insecto. La tecnología de vacunas recombinantes es muy similar a la empleada en la vacuna de la hepatitis B. Sin embargo, la primera vacuna autorizada por la Agencia Europea del Medicamento con esta tecnología, Supemtek®, no tiene aún datos de seguridad y eficacia por debajo de 18 años.
Las vacunas inactivadas pueden acompañarse de mecanismos conducentes a aportar una inmunogenicidad reforzada. La administración intradérmica o el incremento de concentración (alta dosis) desde los habituales 15 µg de HA por subtipo viral a los 60 µg, son mecanismos no ensayados en población infantil. Los adyuvantes (MF59 y AS03) sí se han ensayado en menores de 18 años con resultados prometedores, aunque por el momento no existen en el mercado vacunas antigripales adyuvadas autorizadas en menores de 65 años. Fluad tetra® es una vacuna producida en huevos embrionados y adyuvada con MF59 que está autorizada, aunque no comercializada en España, con una indicación a partir de 65 años; lo interesante de esta vacuna es que ya presenta en su ficha técnica, datos de seguridad e inmunogenicidad en niños de 6 meses a 5 años, lo que podría augurar un futuro cambio de indicación.
Selección de cepas para las vacunas antigripales
La composición de las vacunas antigripales es publicada anualmente por la OMS, en base a la vigilancia virológica que desarrollan centros de todo el mundo.
Desde el año 1973, la Organización Mundial de la Salud (OMS) informa anualmente de las cepas de gripe que deben incluirse en la composición de la vacuna estacional antigripal de cada campaña de vacunación, de forma diferenciada para los hemisferios norte y sur en febrero y septiembre, respectivamente. Estas recomendaciones se basan en la vigilancia epidemiológica, virológica y clínica en todo el mundo, gracias a la información suministrada por parte de los 144 centros nacionales de gripe y los centros colaboradores de la OMS que forman la red GISRS (Global Influenza Surveillance and Response System) sobre las cepas circulantes de virus de la gripe y sus características antigénicas y genéticas(7).
Para la selección de las cepas, uno de los criterios fundamentales es que puedan convertirse en virus dominantes en la siguiente temporada de gripe. Además, las cepas seleccionadas deben poder replicarse fácilmente sin pérdida de sus características antigénicas. Desde 2018, se anuncian las cepas para fabricación en huevo y para cultivo celular, de forma diferenciada para cada subtipo de gripe A (H1) y (H3).
Este proceso está siendo permanentemente revisado y mejorado, y entre las futuras aproximaciones para una mejor selección de cepas, además del fortalecimiento de la vigilancia, se plantean el análisis de patrones dinámicos de movilidad de cepas, para aquilatar mejor la evaluación de las cepas dominantes en la siguiente temporada, y la incorporación de los patrones de anticuerpos existentes en diferentes poblaciones. Este último ingrediente tendría por primera vez en consideración, la susceptibilidad de la población a la cepa a seleccionar, priorizando la vacunación frente a cepas a las que una población determinada presente mayor susceptibilidad.
Eficacia, efectividad e impacto de la vacunación antigripal
La vacunación en niños es más eficaz que la de adultos y tiene un impacto mucho mayor, con un caso prevenido por cada 5 vacunados.
Existen diversas medidas del efecto protector de las medidas preventivas: eficacia analítica, eficacia clínica, efectividad e impacto de la vacunación.
Las pruebas de eficacia analítica de la vacunación antigripal deben realizarse cada año en alrededor de 200 sujetos sanos. En estos ensayos, se mide la respuesta inmune humoral frente a las cepas vacunales, con el fin de comprobar que las vacunas cumplen los requerimientos de la Agencia Europea del Medicamento (European Medicines Agency, EMA). En adultos, entre 18 y 59 años, se exige que las vacunas confieran títulos de Ac. anti-HA superiores a 1:40 en, al menos, el 70% de los vacunados, tasas de seroconversión de, al menos, el 40% de los vacunados y un incremento en el título de Ac. anti-HA de, al menos, 2,5. En mayores de 65 años, los requerimientos son ligeramente inferiores. Los criterios de la EMA están en revisión, ya que no se han definido criterios, por ejemplo, para niños ni para vacunas atenuadas, ni existen correlatos de inmunidad celular. A partir de 2017, se empezó a medir la efectividad vacunal mediante metodología de test negativo, sustituyendo a los criterios clásicos de eficacia serológica.
Es más adecuada e informativa la medición de la capacidad de prevenir eventos (casos, muertes, etc.) mediante ensayos clínicos (eficacia clínica) o mediante estudios observacionales (efectividad vacunal, EV). Los ensayos clínicos y los estudios observacionales de cohortes permiten, además, medir las incidencias de la enfermedad, por lo que se puede calcular el NNV o número necesario a vacunar, que es una medida ilustrativa del impacto de la vacunación.
Tanto la eficacia clínica como la efectividad de la vacuna antigripal (EV), tienen una alta variabilidad en función de aspectos relacionados con la vacuna, como: similitud entre las cepas vacunales y circulantes salvajes, tipo de vacuna, presencia de adyuvantes o vía de administración. Además, existen también 3 aspectos fundamentales no directamente relacionados con la vacuna en sí: el virus (su transmisibilidad, su virulencia, su comportamiento epidemiológico), el individuo (edad, comorbilidad, riesgo de exposición) y el objetivo de prevención perseguido (diagnóstico confirmado, enfermedad clínica, complicaciones o fallecimientos).
En relación con la prevención mediante vacunación frente a la gripe en niños sanos, la EV de las vacunas inactivadas es del 64% (IC95% 52-72), según la revisión de la Cochrane de 2018, lo que conlleva un NNV de 5, es decir, se prevendrá un caso de gripe por cada 5 vacunados. Las vacunas vivas atenuadas tienen una EV en niños que es globalmente del 78% (IC95% 59-89)(19).
Cuando se analiza la EV de las vacunas inactivadas en niños y adolescentes hasta 19 años por subtipo, se ha observado una mayor EV frente al subtipo A/H1N1 (69%), seguida de la EV frente al tipo B (56%) y, por último, la menor EV se observa frente al subtipo A/H3N2 (43%). Todos los grupos etarios presentan un patrón similar de EV, aunque en niños y adolescentes, las diferencias observadas son menos marcadas que en adultos (20-64 años), en los que la EV oscila entre el 73% para A/H1N1 y el 35% para A/H3N2.
La medición del efecto mediante herramientas clásicas no tiene en cuenta la protección de grupo o de rebaño. Pero en la vacunación antigripal infantil, es importante evaluar el impacto colectivo de los programas de vacunación, puesto que los niños son los que presentan mayores tasas de padecimiento de la enfermedad y, además, los principales transmisores, tanto en la gripe estacional como en la pandémica.
Indicaciones y estrategias de vacunación
La vacunación infantil tiene beneficios directos, de protección individual, e indirectos, por la disminución de la difusión del virus gripal.
En España, la principal estrategia es la de protección individual o directa en población especialmente vulnerable, es decir, la vacunación directa de personas que por sus patologías o tratamientos tienen más probabilidad de padecer la gripe o de que la gripe en ellos sea grave (riesgo elevado de hospitalización y muerte)(20).
Existe un extenso listado de indicaciones por patología, en los que se recomienda la vacunación antigripal por las autoridades sanitarias españolas a partir de los 6 meses de edad (Tabla II).
Dicho listado es actualizado anualmente por el Ministerio de Sanidad y existen ligeras variaciones por CC.AA. La variación más significativa es que muchas CC.AA. comienzan a vacunar a los mayores a los 60 años de edad, mientras que otras lo mantienen a los 65 años. Una indicación particular es la recomendación de vacunar a los niños y jóvenes entre 6 meses y 18 años que reciben tratamiento prolongado con ácido acetil salicílico, por la posibilidad de desarrollar un síndrome de Reye.
La OMS considera entre las personas con mayor riesgo de enfermedad grave por gripe a todos los niños menores de 5 años y países como: EE.UU., Canadá, Finlandia o Reino Unido, ya han incorporado la vacunación infantil por edad a sus campañas estacionales.
La vacunación de la embarazada es un caso especial de estrategia de protección directa, ya que responde a dos objetivos: protección de la propia mujer y del futuro recién nacido. Debido a su buen perfil de seguridad y a la constatación de la mayor gravedad de la gripe durante el embarazo, tanto la OMS como las autoridades sanitarias de la mayoría de los países, recomiendan la vacunación antigripal en cualquier trimestre del embarazo. Lejos de suponer un riesgo para la gestación, los abortos y las muertes fetales se observaron con menor frecuencia en mujeres vacunadas(21), con una EV de 40 y 45%, respectivamente. La EV para prevenir gripe confirmada en los recién nacidos de madres vacunadas es del 41% (IC 95%: 6-63) y su riesgo de hospitalización por síndrome gripal se redujo en un 39% (IC 95%: 16-55).
Las llamadas estrategias de «nido seguro» son estrategias complementarias que se basan en la protección indirecta de población especialmente vulnerable a través de la inmunización de sus contactos, de forma que estos no puedan ser una fuente de infección. Tanto la OMS como la mayoría de los países de nuestro entorno, incluida España, contemplan la necesidad de complementar así las estrategias de protección directa. La vacunación del personal sanitario es un tipo especial de estrategia de protección indirecta de población especialmente vulnerable. Estas estrategias son las primeras de las analizadas hasta ahora, que incluyen el concepto de la cadena epidemiológica en su construcción.
La mitigación de impacto y el control de epidemias es el objetivo más ambicioso que se puede plantear. Para ello, es necesario alcanzar la inmunidad de grupo mediante vacunación. Una posibilidad es la vacunación universal, que ya se recomienda en países como EE.UU., pero serían necesarias coberturas de más del 90% para conseguirlo.
Otro abordaje sería la vacunación infantil, ya que solo los niños son capaces de hacer despegar una epidemia de gripe. Esto justifica el mayor impacto que tendría la inmunización infantil, hasta llegar a proponerse que la estrategia de vacunación óptima consistiría en la vacunación de niños en edad escolar y de los adultos entre 30 y 39 años, ya que los niños son los principales responsables de la transmisión y sus padres sirven de puente al resto de la sociedad.
Una de las experiencias en este sentido mejor documentadas hasta la fecha, es la de Inglaterra, donde se comenzó la vacunación infantil de forma parcial en la temporada 2013-14. En la temporada 2014-15, las coberturas alcanzadas fueron del 57 y del 50% en primaria y secundaria, respectivamente. En las áreas donde se inició, como estudio piloto, la vacunación infantil, se constató un impacto beneficioso global e indirecto en la población infantil. En las áreas donde habían vacunado en primaria, se constató una reducción significativa de consultas médicas por: síndrome gripal, urgencias respiratorias, positividad en frotis, hospitalizaciones y mortalidad por causas respiratorias; la disminución de la mortalidad por todas las causas no fue significativa. En las áreas donde se vacunó en secundaria, el impacto fue pequeño. En Reino Unido, durante la temporada 2018-19, la tasa de incidencia semanal máxima fue superior en adultos (15-64 años) que en niños y adolescentes (<15 años), lo cual es un hito en la historia epidemiológica de la gripe.
En resumen, los niños menores de 5 años constituyen un grupo de riesgo en sí mismo, que debe ser vacunado. La vacunación de niños hasta la etapa educativa de primaria aporta además beneficios poblaciones, disminuyendo la difusión del virus gripal. Los adolescentes se benefician de la vacunación antigripal en la misma medida que los adultos jóvenes y debe prestarse especial atención a aquellos que tengan cualquier patología de riesgo o a quienes sean convivientes de personas con dichas patologías.
La pauta vacunal en niños es de una dosis completa que, con las vacunas actuales, debe repetirse cada año. En niños entre 6 meses y 9 años, la primera vez que se vacunan deben recibir dos dosis separadas por, al menos, 4 semanas.
Bibliografía
Los asteriscos muestran el interés del artículo a juicio de los autores.
1.** Neuzil KM, Mellen BG, Wright PF, Mitchel EF Jr, Griffin MR. The effect of influenza on hospitalizations, outpatient visits, and courses of antibiotics in children. N Engl J Med. 2000; 342: 225-31. doi: 10.1056/NEJM200001273420401. PMID: 10648763.
2.** Izurieta HS, Thompson WW, Kramarz P, Shay DK, Davis RL, DeStefano F, et al. Influenza and the rates of hospitalization for respiratory disease among infants and young children. N Engl J Med. 2000; 342: 232-9. doi: 10.1056/NEJM200001273420402. PMID: 10648764.
3.** Monto AS, Davenport FM, Napier JA, Francis T Jr. Modification of an outbreak of influenza in Tecumseh, Michigan by vaccination of schoolchildren. J Infect Dis. 1970; 122: 16-25. doi: 10.1093/infdis/122.1-2.16. PMID: 5433709.
4.** Reichert TA, Sugaya N, Fedson DS, Glezen WP, Simonsen L, Tashiro M. The Japanese experience with vaccinating schoolchildren against influenza. N Engl J Med. 2001; 344: 889-96. doi: 10.1056/NEJM200103223441204. PMID: 11259722.
5. Garten R, Blanton L, Elal AIA, Alabi N, Barnes J, Biggerstaff M, et al. Update: Influenza Activity in the United States During the 2017-18 Season and Composition of the 2018-19 Influenza Vaccine. MMWR Morb Mortal Wkly Rep. 2018; 67: 634-42. doi: 10.15585/mmwr.mm6722a4. PMID: 29879098; PMCID: PMC5991814.
6. Biggerstaff M, Kniss K, Jernigan DB, Brammer L, Bresee J, Garg S, et al. Systematic Assessment of Multiple Routine and Near Real-Time Indicators to Classify the Severity of Influenza Seasons and Pandemics in the United States, 2003-2004 Through 2015-2016. Am J Epidemiol. 2018; 187: 1040-50. doi: 10.1093/aje/kwx334. PMID: 29053783; PMCID: PMC5908755.
7.*** Ortiz de Lejarazu Leonardo R. Los virus de la gripe. Pandemias, epidemias y vacunas. Amazing Books SL; 2019. ISBN 978-84-17403-22-5.
8. Hirve S, Newman LP, Paget J, Azziz-Baumgartner E, Fitzner J, Bhat N, et al. Influenza Seasonality in the Tropics and Subtropics – When to Vaccinate? PLoS One. 2016; 11: e0153003. doi: 10.1371/journal.pone.0153003. PMID: 27119988; PMCID: PMC4847850.
9. Killingley B, Nguyen-Van-Tam J. Routes of influenza transmission. Influenza Other Respir Viruses. 2013; 7 Suppl 2: 42-51. doi: 10.1111/irv.12080. PMID: 24034483; PMCID: PMC5909391.
10. Brankston G, Gitterman L, Hirji Z, Lemieux C, Gardam M. Transmission of influenza A in human beings. Lancet Infect Dis. 2007; 7: 257-65. doi: 10.1016/S1473-3099(07)70029-4. PMID: 17376383.
11.*** Paget WJ, Balderston C, Casas I, Donker G, Edelman L, Fleming D, et al. Assessing the burden of paediatric influenza in Europe: the European Paediatric Influenza Analysis (EPIA) project. Eur J Pediatr. 2010; 169: 997-1008. doi: 10.1007/s00431-010-1164-0. Epub 2010 Mar 13. PMID: 20229049; PMCID: PMC2890072.
12.* Ortiz de Lejarazu Leonardo R, Pumarola Suñé T, Trilla García A. Gripe. En Medicina Interna de Farreras-Rozman. Ediciones Elsevier España SL.2020. 19ª edición. ISBN 978-84-9113-544-9.301:2372-2377.
13. Silvennoinen H, Peltola V, Vainionpää R, Ruuskanen O, Heikkinen T. Admission diagnoses of children 0-16 years of age hospitalized with influenza. Eur J Clin Microbiol Infect Dis. 2012; 31: 225-31. doi: 10.1007/s10096-011-1297-8. Epub 2011 Jun 4. PMID: 21643867.
14.* Rodrigo C, Méndez M. Clinical and laboratory diagnosis of influenza. Hum Vaccin Immunother. 2012; 8: 29-33. doi: 10.4161/hv.8.1.18924. Epub 2012 Jan 1. PMID: 22251993.
15. Rothberg MB, Haessler SD, Brown RB. Complications of viral influenza. Am J Med. 2008; 121: 258-64. doi: 10.1016/j.amjmed.2007.10.040. PMID: 18374680; PMCID: PMC7172971.
16. Centro Nacional de Epidemiología. Informe sobre la gravedad de la epidémica de gripe en la temporada 2013-14 y su comparación con las tres temporadas precedentes 2010-11 a 2012-13. Madrid, 2014. Acceso el 6 de diciembre de 2020. Disponible en:
18.*** Poehling KA, Edwards KM, Weinberg GA, Szilagyi P, Staat MA, Iwane MK, et al. New Vaccine Surveillance Network. The underrecognized burden of influenza in young children. N Engl J Med. 2006; 355: 31-40. doi: 10.1056/NEJMoa054869. PMID: 16822994.
19.*** Ortiz de Lejarazu R, Tamames S. Vacunación antigripal. Efectividad de las vacunas actuales y retos de futuro. Enferm Infecc Microbiol Clin. 2015; 33: 480-90. Spanish. doi: 10.1016/j.eimc.2015.06.011. Epub 2015 Jul 29. PMID: 26232121.
20. Jefferson T, Rivetti A, Di Pietrantonj C, Demicheli V. Vaccines for preventing influenza in healthy children. Cochrane Database Syst Rev. 2018; 2: CD004879. doi: 10.1002/14651858.CD004879.pub5. PMID: 29388195; PMCID: PMC6491174.
21. Ortiz de Lejarazu R, Tamames S. Capítulo 32 – Inmunología y vacunación frente a la gripe. En Inmunología pediátrica de Fariñas Ferrero. Ediciones Amazing Books. ISBN 978-84-17403-60-7. 2020.
22. Giles ML, Krishnaswamy S, Macartney K, Cheng A. The safety of inactivated influenza vaccines in pregnancy for birth outcomes: a systematic review. Hum Vaccin Immunother. 2019; 15: 687-99. doi: 10.1080/21645515.2018.1540807. Epub 2018 Nov 15. PMID: 30380986; PMCID: PMC6605784.
23. Arístegui Fernández J. Gripe en Pediatría. Pediatr Integral. 2015; XIX(10): 694-701.
Bibliografía recomendada
– Ortiz de Lejarazu Leonardo R. Los virus de la gripe. Pandemias, epidemias y vacunas. Amazing Books SL; 2019. ISBN 978-84-17403-22-5.
Un libro que aborda casi todos los aspectos de la gripe, a través de autores españoles con experiencia e investigación acreditada nacional e internacional sobre los virus de la gripe. Tiene cuatro capítulos dedicados a las vacunas y la vacunación de gripe, y numerosas figuras y tablas.
– Paget WJ, Balderston C, Casas I, Donker G, Edelman L, Fleming D, et al. Assessing the burden of paediatric influenza in Europe: the European Paediatric Influenza Analysis (EPIA) project. Eur J Pediatr. 2010; 169: 997-1008. doi: 10.1007/s00431-010-1164-0. Epub 2010 Mar 13. PMID: 20229049; PMCID: PMC2890072.
En seis temporadas analizadas en: Reino Unido, Países Bajos, Italia y España, el modelo atribuyó entre el 47 al 83% de la carga por enfermedad similar a gripe en Atención Primaria a la infección por el virus de la gripe, siendo el virus A (H3N2) el más importante, seguido por los virus B y A (H1N1). Las medias nacionales de la temporada de los países estudiados indicaron que, entre el 0,4 al 18% de los niños, consultaron a un médico por dicha causa.
– Poehling KA, Edwards KM, Weinberg GA, Szilagyi P, Staat MA, Iwane MK, et al. New Vaccine Surveillance Network. The underrecognized burden of influenza in young children. N Engl J Med. 2006; 355: 31-40. doi: 10.1056/NEJMoa054869. PMID: 16822994.
Uno de los primeros artículos en demostrar la carga de enfermedad por gripe en niños confirmada por laboratorio en EE.UU. La tasa media anual de hospitalización asociada a gripe fue de 0,9 por 1.000 niños, y la de consultas ambulatorias y a urgencias fue de 50/1.000 y 6/1.000 niños, respectivamente, en la temporada 2002-03, y 95/1.000 y 27/1.000 durante la temporada 2003-04, demostrando la importancia y la gravedad, ya que muchos de los cuadros no eran reconocidos como gripe.
– Ortiz de Lejarazu R, Tamames S. Vacunación antigripal. Efectividad de las vacunas actuales y retos de futuro. Enferm Infecc Microbiol Clin. 2015; 33: 480-90. Spanish. doi: 10.1016/j.eimc.2015.06.011. Epub 2015 Jul 29. PMID: 26232121.
Un artículo de revisión general y actualizado, que complementa lo expuesto en este artículo y añade más bibliografía básica para aquellos que quieran profundizar más en el tema.
| Caso clínico |
|
Niño de 3 años de edad, con historial conocido de alergia al huevo diagnosticada de forma empírica. La sospecha de alergia se estableció con la introducción del huevo, en concreto de la clara del mismo, en la alimentación complementaria, a los 11 meses de edad. La clínica de las reacciones alérgicas fue de urticaria sin angioedema. No se han realizado pruebas de provocación. En la historia clínica, consta como diagnosticado de asma, con episodios de exacerbación de presentación invernal que se tratan de forma aguda, pero no se ha establecido tratamiento preventivo. Parto eutócico, lactancia artificial y desarrollo dentro de parámetros normales. El núcleo familiar lo forman: el padre, la madre y el paciente. La madre está embarazada de 21 semanas y acude a consulta solicitando la vacunación de su hijo por indicación de la matrona.
|