 |
| Temas de FC |
T. Cueva Quiroz![]() , M. Cols Roig, R. Ayats Vidal, J. Costa Colomer
, M. Cols Roig, R. Ayats Vidal, J. Costa Colomer
Facultativos Especialistas. Servicio de Neumología Pediátrica.Hospital Sant Joan de Déu. Barcelona
| Resumen
La patología pulmonar crónica en los niños engloba un conjunto diverso de enfermedades respiratorias, que ocasionan daño pulmonar, inflamación y/o alteración del intercambio gaseoso, con potencial compromiso de la función pulmonar a largo plazo. Aunque el rango de gravedad es muy variable, en ocasiones pueden conllevar necesidad de soporte respiratorio y/o de trasplante pulmonar. Es importante conocer los signos y síntomas de estas enfermedades, detectarlas de forma precoz y realizar un tratamiento adecuado e individualizado del paciente. Habitualmente, el trabajo multidisciplinar es esencial para lograr un óptimo control de la enfermedad y mejorar la calidad de vida de estos niños. |
| Abstract
Chronic lung disease in children encompasses a diverse group of respiratory illnesses that cause lung damage, inflammation, and/or impaired gas exchange, with the potential for long-term impairment of lung function. Although the severity varies considerably, these conditions can sometimes lead to the need for respiratory support and/or lung transplantation. It is important to recognize the signs and symptoms of these diseases, detect them early, and provide appropriate and individualized treatment. A multidisciplinary approach is usually essential to achieve optimal disease management and improve the quality of life for these children. |
Palabras clave: Síndrome aspirativo crónico; Bronquiectasias; Neumopatías intersticiales; Displasia broncopulmonar; Neumopatía crónica infantil.
Key words: Aspiration syndrome; Bronchiectasis; Interstitial lung diseases; Bronchopulmonary dysplasia; Chronic lung disease infant.
Pediatr Integral 2026; XXX(2): 118 – 127
OBJETIVOS
• Reconocer el cuadro clínico, los factores de riesgo y la etiología de la patología pulmonar crónica infantil para poder detectarla de forma precoz y evitar el daño pulmonar progresivo.
• Conocer el abordaje diagnóstico y terapéutico de la patología pulmonar crónica infantil.
• Reconocer las complicaciones de la patología pulmonar crónica.
• Valorar el tratamiento en las agudizaciones respiratorias en el paciente con patología pulmonar crónica.
Neumopatía crónica
https://doi.org/10.63149/j.pedint.123
Introducción
La patología pulmonar crónica infantil representa un grupo de enfermedades que provocan un daño persistente en el tejido pulmonar y que requieren un abordaje multidisciplinar para optimizar el control de la enfermedad y mejorar la calidad de vida del niño.
Aunque son varias las enfermedades que pueden conllevar neumopatía crónica en la infancia, en este artículo vamos a desarrollar el estudio y tratamiento del síndrome aspirativo crónico (SAC), de las bronquiectasias no vinculadas a enfermedad de fibrosis quística, las enfermedades intersticiales infantiles y la displasia broncopulmonar.
Síndrome aspirativo crónico
Se considera síndrome aspirativo crónico (SAC) a la sintomatología respiratoria y/o al daño pulmonar objetivable ocasionados por el paso de productos procedentes de la orofaringe y/o del esófago de forma recurrente o continuada al pulmón(1).
La principal causa de SAC en la infancia es la disfagia en pacientes neurológicos (especialmente, con parálisis cerebral infantil), aunque también es posible en afectos por otras patologías predisponentes (Tabla I)(1-5) (Fig. 1).
Figura 1. TAC pulmonar de un paciente de 15 años con alteraciones pulmonares crónicas por antecedentes de síndrome aspirativo crónico por disfagia secundaria a enfermedad neurológica: asimetría de campos pulmonares caracterizada por pérdida de volumen a expensas de lóbulo inferior izquierdo. Bronquiectasias de morfología cilíndrica, multifocales, con predominio izquierdo, con tapones mucosos y opacidades centrolobulillares en lóbulo medio.
En el periodo neonatal y en el lactante, las aspiraciones pueden ocasionar apnea, bradicardia, estridor, accesos tusígenos (simulando un cuadro pertusoide) e incluso un episodio aparentemente letal. En el niño con integridad de los mecanismos defensivos de la vía aérea, se observan atragantamiento y/o tos con la ingesta o postprandial.
Los pacientes neurológicos y/o con cronicidad del SAC pueden presentar pérdida del reflejo tusígeno, por lo que deben sospecharse aspiraciones silentes ante la presencia de voz húmeda y/o respiración con ruido vibratorio, disfonía, distrés respiratorio y/o cianosis en relación con la ingesta, aun con la ausencia de atragantamiento o tos evidentes.
Los síntomas de la neumopatía secundaria a SAC (sibilancias, tos crónica, neumonías recurrentes, insuficiencia respiratoria), también deben situar el SAC en el foco diagnóstico(5). Por otro lado, es muy importante remarcar que la ausencia de complicaciones graves o neumonía previa no descarta el SAC(3).
El diagnóstico de SAC es un reto, siendo fundamental la sospecha clínica. La anamnesis debe considerar la edad del paciente, su patología basal, la presencia de síntomas de SAC y de sus causas.
La exploración física debe valorar la evolución pondoestatural, la anatomía facial y de vía aérea superior, la presencia de sialorrea, la integridad del reflejo tusígeno y la evaluación sistemática del acto de la deglución. A nivel respiratorio, la auscultación normal no descarta el diagnóstico. En caso de auscultación patológica, pueden apreciarse roncus, estertores, zonas hipofonéticas, espiración alargada y/o sibilancias. Las exploraciones complementarias deben planificarse según la sospecha etiológica, habitualmente de forma multidisciplinaria. Por ello, se aconseja planificar un algoritmo de estudio individualizado(1). Las pruebas que contribuyen al diagnóstico de SAC son(1-7):
• Pruebas de imagen pulmonar: la tomografía axial computarizada (TAC) torácica es más sensible que la radiografía simple. Cuando es posible la aplicación de protocolo con muy baja dosis, se obtiene buena información, disminuyendo substancialmente el nivel de irradiación. Los hallazgos característicos son: engrosamiento bronquial, atrapamiento aéreo, bandas parenquimatosas, opacidades centrolobulares en forma de árbol en gemación, ocupación de la luz bronquial, bronquiolectasias, bronquiectasias y/o atelectasias, aunque no son patognomónicos.
• Broncoscopia flexible (FBS) con lavado broncoalveolar (LBA): permite la evaluación anatómica de la vía aérea y la recogida de muestras broncoalveolares. En el caso de las hendiduras laríngeas grado I, suele ser necesario el palpado de la zona interaritenoidea con varilla metálica para poder apreciar la solución de continuidad existente. Cuando la causa es el reflujo gastroesofágico (RGE), puede observarse hipertrofia de la amígdala lingual, edema y/o eritema del espacio retroglótico y/o de aritenoides, así como lesión en cuerdas vocales. En la vía aérea inferior puede observarse la mucosa inflamada y aumento de secreciones. El LBA permite la identificación de microorganismos y estudiar el índice de macrófagos cargados de lípidos (IMCL). Este puede sugerir etiología aspirativa, pero es una técnica con elevada variabilidad interobservador, escasa sensibilidad y baja especificidad, por lo que debe interpretarse con prudencia.
• Esofagoscopia, con o sin toma de biopsias: es útil para el diagnóstico de RGE y de esofagitis eosinofílica. Para el diagnóstico de fístula traqueoesofágica (FTE), en ocasiones, es preciso realizar esofagoscopia con instilación de contraste, simultánea a la FBS, para constatar su permeabilidad.
• Videofluoroscopia de la deglución (VFSS): permite el diagnóstico de la disfagia y sugiere malformaciones anatómicas. Se realiza mediante grabación de una exploración fluoroscópica de la vía aérea y digestiva con proyección lateral, mientras el paciente realiza una ingesta protocolarizada de distintas texturas contrastadas. La irradiación es proporcional a la duración de la prueba.
• Videoendoscopia de la deglución (VEES) o fibroendoscopia de la deglución (FEES): es una exploración no irradiante que se realiza introduciendo un endoscopio con cámara de vídeo (VEES) o fibra óptica (FEES) por la nariz del paciente. Permite la visualización directa de la hipofaringe y la laringe durante la ingesta, la deglución salival, su coordinación con la respiración y la valoración de los reflejos protectores de la vía aérea. Se considera de elección para la aspiración salival y también es útil en el diagnóstico de la disfagia.
• Registro de pH-impedanciometría: es la técnica de elección para el estudio del RGE. Permite la detección del paso de contenido ácido, alcalino y de gas por el esófago. Sus limitaciones son la escasa accesibilidad y la ausencia de valores de normalidad en algunas edades pediátricas.
• La tinción alimentaria en pacientes portadores de traqueostomía se utiliza, aunque sin demasiada evidencia. El aspirado de contenido tintado por la cánula es altamente sugestivo de SAC, pero su ausencia no lo descarta.
En pacientes con alta sospecha de SAC, pero con normalidad de todas las pruebas realizadas, a veces, el diagnóstico solo puede realizarse ex juvantibus, objetivando la mejoría clínica una vez retirada la ingesta oral, substituyéndose por alimentación enteral(1).
El tratamiento primordial del SAC es eliminar la causa
En el tratamiento de la disfagia, deben establecerse medidas posicionales, instrumentación adecuada y definición de las texturas alimentarias toleradas. Debe valorarse la posibilidad de terapia conductual y/o rehabilitación de la musculatura motora orofacial. Cuando las medidas compensatorias no pueden garantizar el aporte calórico y/o evitar la aspiración, puede ser necesario un dispositivo para alimentación enteral (gastrostomía, gastroyeyunostomía o yeyunostomía). Puede disminuirse la secreción salival con medicaciones anticolinérgicas por vía oral (glicopirrolato, trihexifinidilo) o mediante parche cutáneo (escopolamina), vigilando la aparición de efectos adversos. Otras posibilidades son: la inyección de toxina botulínica en glándulas salivares y, en casos graves y refractarios, la escisión de glándulas salivales o la ligadura de sus conductos. Para el tratamiento del RGE, se aconsejan medidas posturales, espesamiento y/o fraccionamiento de las ingestas y evitar determinados alimentos (p. ej.: cafeína, cacao, picantes, grasas, bebidas gaseosas). Son efectivos los fármacos antiácidos, como los inhibidores de las bombas de protones o anti-H2, pero no evitan el RGE alcalino. Fármacos procinéticos, como el cisapride, la domperidona, la metoclopramida o la eritromicina, tienen efectos secundarios potencialmente graves y su evidencia es limitada, por lo que se desaconseja su uso. El tratamiento quirúrgico con funduplicatura de Nissen es el tratamiento de elección para pacientes con RGE patológico persistente y grave refractario. La alimentación por sonda transpilórica o gastroyeyunal puede ser una alternativa, en determinados casos(4,5). Si la lesión pulmonar está establecida, va a ser beneficioso instruir al paciente y a sus cuidadores en técnicas de drenaje de secreciones, usar antibióticos precozmente en caso de sospecha de infección pulmonar y optimizar las medidas higiénicas y de inmunización, para evitar infecciones respiratorias(5). En caso de bronquiectasias secundarias, deben considerarse los cuidados descritos en el siguiente apartado de este artículo.
Bronquiectasias no fibrosis quística (FQ)
Definición
Las bronquiectasias son dilataciones bronquiales anormales y persistentes, habitualmente observadas por TAC de tórax.
Existe aumento en la secreción de moco y, clínicamente, se manifiesta con tos productiva crónica y exacerbaciones respiratorias recurrentes. Si se detecta de forma precoz, se puede detener la progresión de la alteración de la función pulmonar; además genera una alta carga económica y un impacto negativo significativo en la calidad de vida de los pacientes y sus familiares(8,9).
Epidemiología y etiología
Son más prevalentes en los países en vías de desarrollo y, a escala mundial, son un factor importante de morbimortalidad respiratoria crónica(10). En Europa, las tasas de incidencia anual oscilan entre 0,2/100.000 en el Reino Unido y 2,3/100.000 en Irlanda(10).
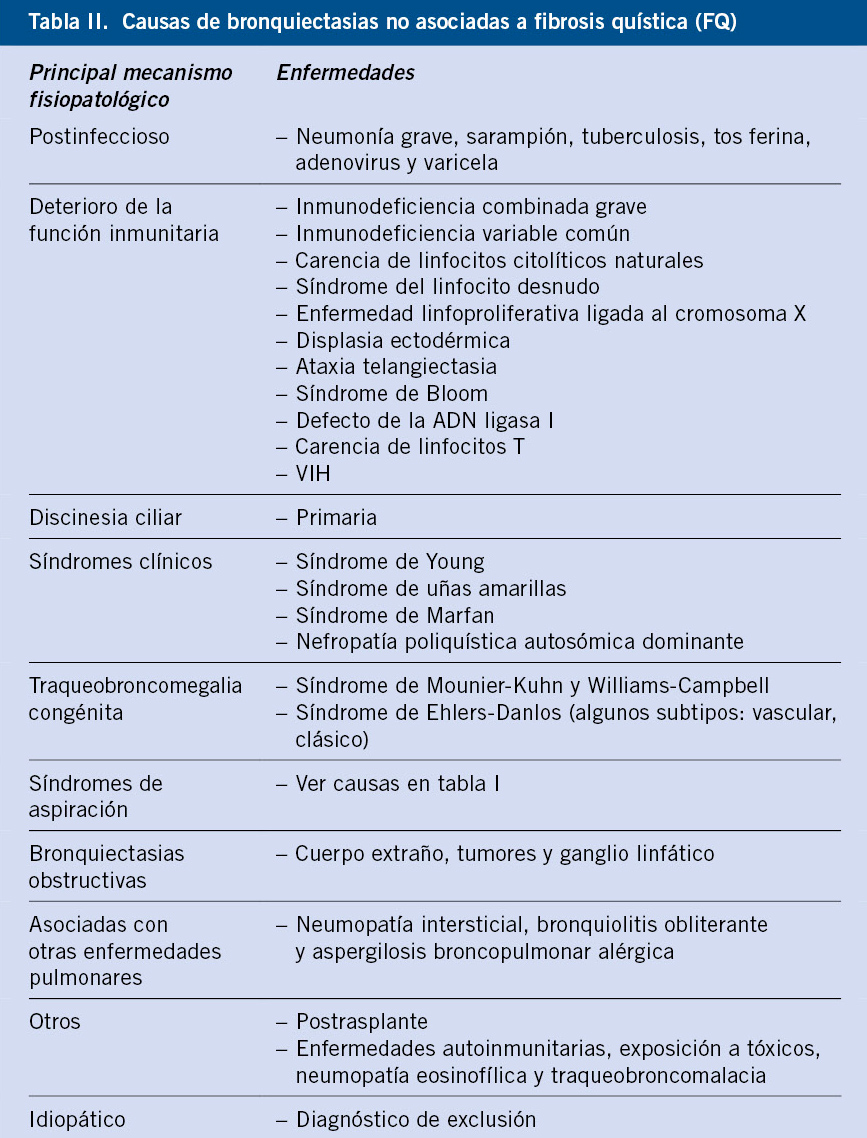
Existen múltiples causas, siendo la más frecuente la infección grave del tracto respiratorio. En la tabla II se identifica la etiología en las bronquiectasias no asociadas a FQ(9,14).
Clínica
La clínica depende de la gravedad y/o presencia de una enfermedad subyacente. Sospechamos bronquiectasias cuando el paciente presenta:
• Tos productiva crónica matutina (>4 semanas), que no responde a antibioticoterapia.
• Bronquitis bacteriana persistente (>3 episodios al año).
• Neumonías localizadas recurrentes.
• Hemoptisis.
• Hiperreactividad bronquial de difícil control.
• Acropaquias.
• Pacientes con auscultación patológica persistente (crepitantes) o cultivos para organismos inusuales (como Pseudomonas aeruginosa)(11).
También pueden estar presentes algunas comorbilidades, como hiperreactividad bronquial, reflujo gastroesofágico, patología cardiaca, trastorno del sueño y factores psicosociales(12).
Se define una exacerbación respiratoria, cuando un paciente presenta aumento de la tos (con o sin aumento de la cantidad de esputo y/o purulencia) durante ≥ 3 días, fiebre, fatiga, malestar, cambios en el comportamiento y/o apetito del niño. Los cambios en la auscultación y/o en las radiografías, aunque pueden ser importantes, no siempre están presentes y, por tanto, no son criterios obligatorios para considerar la exacerbación. La presencia de disnea y la hipoxemia orientan a una exacerbación respiratoria grave, independiente de su duración(13).
Diagnóstico
El diagnóstico confirmatorio de las bronquiectasias es radiológico y se realiza mediante una TCAR (tomografía computarizada de alta resolución), siendo esta la prueba de elección(13).
El estudio dirigido a determinar la causa subyacente de las bronquiectasias es determinante para poder valorar un tratamiento específico precoz y así mejorar el pronóstico de la enfermedad. Se describen, a continuación, exámenes obligatorios y exámenes adicionales, según sospecha etiológica(9,12).
Exámenes obligatorios
• TCAR: se utiliza el índice broncoarterial (BAR) pediátrico (definido por la relación entre el diámetro interno de la vía aérea y el diámetro externo de la arteria adyacente) > 0,8. Esta medida se relaciona con la edad y aumenta a medida que la bronquiectasia se agrava. También la morfología de las bronquiectasias varía según gravedad, siendo cilíndricas las más leves y evolucionando a varicosas y quísticas en casos graves.
Los hallazgos que encontramos en la TCAR son: imágenes de apariencia en anillo de sello, aumento del diámetro bronquial interno, falta de afilamiento normal de las vías respiratorias mientras avanzan hacia la periferia, presencia de vías respiratorias en la periferia del TCAR, engrosamiento de la pared bronquial, taponamiento mucoso o impactación, y perfusión en mosaico que refleja atrapamiento aéreo en los cortes espiratorios. En la fase aguda, también puede visualizarse un patrón en árbol en brote(9,13).
• Radiografía de tórax: es una prueba poco sensible. Puede ser normal en fases iniciales. Pueden presentarse en forma de engrosamientos peribronquiales, “signo de vías de tren”, que sería el bronquio dilatado visto longitudinalmente, atelectasias lineales y opacidades irregulares(9,12).
• Estudio de inmunodeficiencias: con hemograma, inmunoglobulinas (IgG total, IgA, IgM, IgE), respuestas vacunales a tétanos, difteria y neumococo, y estudio del complemento. Otras evaluaciones inmunológicas adicionales según valoración del inmunólogo pediátrico, a considerar de forma individualizada(9,12).
• Test del sudor: para el despistaje de fibrosis quística(9,12).
• Cultivo de secreciones: con el objetivo de conocer el estado de colonización del paciente. Se realizan en el seguimiento evolutivo, en caso de exacerbación y en el control posterior de un tratamiento erradicador(9,12).
• Espirometría: en los pacientes colaboradores (generalmente, en mayores de 5 años). La mayoría de los niños con cuadros leves de bronquiectasias presentan espirometrías normales, aunque, según causa subyacente y gravedad, pueden presentar desde patrón obstructivo a patrón restrictivo o mixto (en fases avanzadas)(9,12).
• Estudio de tuberculosis (prueba de Mantoux e interferón gamma) y de VIH, en pacientes en lugares con alta prevalencia(9,12).
Pruebas adicionales, según sospecha etiológica
• Si sospechamos aspergilosis broncopulmonar alérgica (ABPA): en un paciente con clínica que simula asma grave de difícil control y bronquiectasias centrales en el TCAR, se debe realizar IgE total, pruebas cutáneas y precipitinas para Aspergillus.
• Se debe descartar el SAC (según se ha descrito previamente).
• Se puede valorar realizar fibrobroncoscopia con análisis de lavado broncoalveolar.
• De forma individualizada, se puede considerar el estudio de discinesia ciliar primaria (óxido nítrico nasal, estudio genético y estudio de motilidad ciliar y microscopía electrónica), en pacientes con score de PICADAR >5 y/o bronquiectasias sin causa identificada tras un estudio exhaustivo(9,12).
Tratamiento
El abordaje adecuado consiste en tratar la etiología, valorar la microbiología, movilizar las secreciones retenidas en las bronquiectasias y disminuir la inflamación pulmonar, con el fin de reducir las exacerbaciones, optimizar la calidad de vida y prevenir el deterioro de la función pulmonar(12).
Técnicas de aclaramiento de secreciones mucosas de vía aérea
Tras el diagnóstico, los pacientes y sus progenitores (si el paciente no puede realizar tratamiento de forma autónoma) deben ser capacitados en técnicas de drenaje de secreciones mucosas adaptadas a su situación clínica y edad, para realizarlas de forma regular e intensificarlas en las agudizaciones(13).
Agentes mucoactivos
No se recomienda la DNA humana recombinante (DNasa rh), ni bromhexina(13). No se recomienda utilizar de forma rutinaria manitol inhalado ni solución salina hipertónica. Aunque la evidencia es limitada, las guías mencionan que el tratamiento con solución salina hipertónica al 6-7 % y el manitol se puede considerar en pacientes seleccionados, por ejemplo, pacientes con síntomas diarios, exacerbaciones frecuentes, dificultad para expectorar y/o baja calidad de vida. Siempre que se inicie este tratamiento, se debe realizar bajo supervisión médica la primera vez, y puede considerarse el uso de un beta-2 agonista de acción corta previamente, para prevenir la potencial broncoconstricción iatrogénica(9,12,13).
Antibióticos
En los pacientes con exacerbación respiratoria aguda, se recomienda tratamiento antibiótico, siendo de elección la antibioterapia orientada según las colonizaciones y/o cultivos previos de cada paciente, con duración del tratamiento más extensa que en la población general (habitualmente 14 días). En ausencia de cultivos previos, amoxicilina-ácido clavulánico (con dosis altas de amoxicilina) cubre la mayoría de bacterias colonizadoras de bronquiectasias no FQ pediátricas(9,10,13).
En exacerbaciones recurrentes
En los pacientes que presentan más de 1 exacerbación hospitalaria o ≥3 exacerbaciones no hospitalarias en los últimos 12 meses, se recomienda el uso de azitromicina a largo plazo (10 mg/kg/día) 3 veces por semana, durante, al menos, 6 meses. Antes de empezar el tratamiento, se recomienda descartar infección por micobacterias atípicas y repetir de forma anual. En caso de antecedentes familiares de arritmias, QT largo o eventos cardiacos agudos, se debería practicar ECG previo(9,10,13).
Antibióticos para erradicación
La evidencia es limitada en niños. Las recomendaciones en caso de aislamiento de P. aeruginosa, descritas en la guía de la ERS, se basan en estudios en adultos y en pacientes con FQ, abogan por el uso de antibióticos antipseudomónicos orales, endovenosos y/o nebulizados, según la situación clínica del paciente(9,13).
Terapias basadas en el asma
No se recomienda utilizar corticoides inhalados, beta-2 agonistas de acción corta o prolongada o antagonistas de los antileucotrienos de forma rutinaria, solo en caso de que exista asma bronquial confirmada y coexistente(12,13).
Otras terapias
Se recomienda fomentar el ejercicio físico, asegurar una buena evolución nutricional y niveles normales de vitamina D. Se aconseja seguir el programa de vacunación poblacional y completar con vacunación antigripal estacional anual y antineumocócica 23 valente. Debe formarse al paciente y a su familia en medidas higiénicas, fomentando el lavado frecuente de manos y evitando el contacto con las personas con cuadros respiratorios contagiosos, así como evitar la exposición al tabaco y a la contaminación ambiental(12,13).
Pronóstico y seguimiento
El pronóstico depende de la etiología, del diagnóstico y el tratamiento de forma precoz, de la alteración de la función pulmonar, de las exacerbaciones y de la colonización por P. aeruginosa(12).
Estos pacientes deben ser atendidos, con revisiones cada 3 a 6 meses, para valorar la función pulmonar y realizar cultivo de muestras respiratorias para orientar el tratamiento antibiótico empírico ante futuras exacerbaciones(9,13).
Neumopatías intersticiales
Introducción y definición
Las neumopatías intersticiales pediátricas constituyen un grupo heterogéneo y poco frecuente de enfermedades que afectan principalmente al tejido intersticial pulmonar, produciendo alteraciones en el intercambio gaseoso.
Estos grupos de enfermedades se conocen con el acrónimo chILD (child Intersticial Lung Disease)(15). Son 10 veces menos frecuentes en niños que en adultos(16). Un estudio reciente, en España, estimó una incidencia de 8,2 nuevos casos por millón de niños por año y una prevalencia promedio de 46,4 casos por millón de niños(17).
El diagnóstico de ChILD se define cuando cumple, al menos, 3 de los siguientes 4 criterios(18):
1. Síntomas respiratorios: tos persistente, taquipnea, disnea o intolerancia al ejercicio.
2. Signos clínicos de insuficiencia respiratoria: crepitantes o estertores en la auscultación, retracciones intercostales o acropaquias.
3. Hipoxemia.
4. Anomalías difusas del parénquima pulmonar en las radiografías de tórax o TAC pulmonar.
Etiología y clasificación
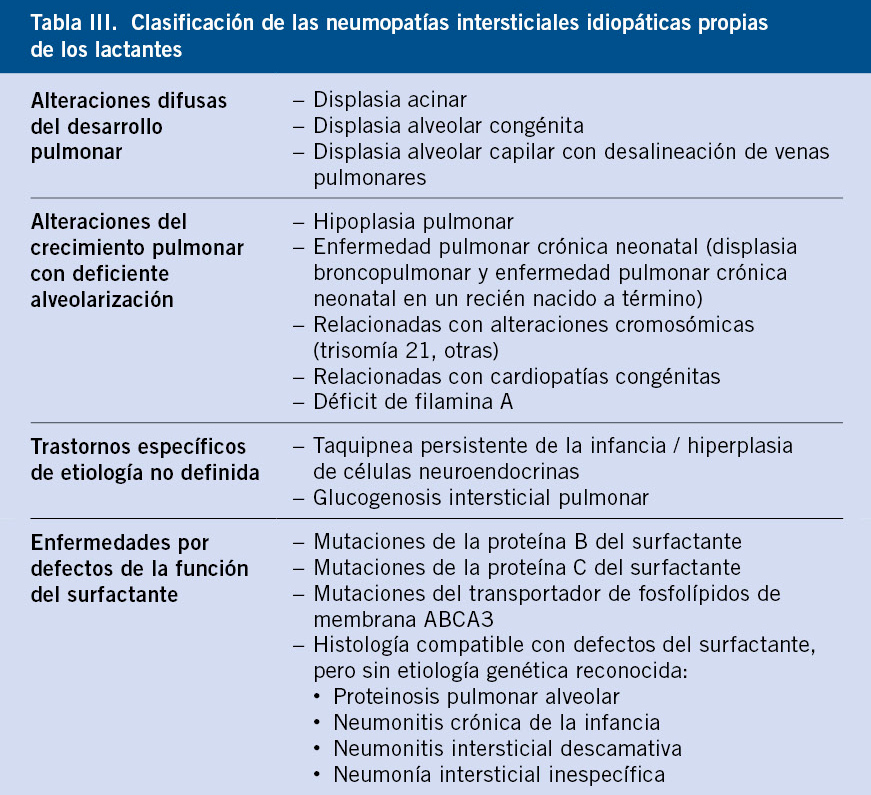
Su etiología es muy variada, incluyendo formas de origen genético, infecciosas crónicas o postinfecciosas, inflamatorias o autoinmunes, asociadas a trastornos sistémicos o multisistémicos, relacionadas con factores ambientales o tóxicos, fármacos o de causa desconocida. El consorcio americano ChILD propuso una clasificación, distinguiendo dos grupos: los trastornos específicos del recién nacido y del lactante (Tabla III), que son muy diferentes de los adultos; y los trastornos en niños mayores (Tabla IV), que se parecen más a los trastornos de los adultos, con las particularidades de una aparición temprana de la enfermedad, la influencia del desarrollo pulmonar y la práctica ausencia de fibrosis pulmonar idiopática en niños(19).
Sospecha clínica
En el neonato, se debe sospechar ante un distrés respiratorio agudo en el recién nacido a término, no explicable por otros motivos, y en prematuros que no respondan al tratamiento con surfactante o que evolucionen de forma no habitual. En los dos primeros años de vida, la clínica más frecuente es la taquipnea moderada, junto con retraso ponderal, rechazo de la ingesta, hipoxemia nocturna y/o diurna. Los niños mayores pueden presentar una clínica similar o debutar con disnea o cianosis con el esfuerzo, que progresa hasta presentarse en reposo. En la auscultación, es habitual detectar crepitantes y, ocasionalmente, algún sibilante, aunque puede ser normal. También pueden presentar acropaquias y deformidad de la caja torácica.
Ante una sospecha de chILD, requiere descartar otras causas de enfermedad pulmonar difusa más frecuentes, como fibrosis quística, inmunodeficiencias, cardiopatías congénitas, displasia broncopulmonar, infección pulmonar, síndrome aspirativo crónico o discinesia ciliar primaria.
Abordaje diagnóstico
El enfoque diagnóstico para las chILD incluye una combinación de antecedentes personales y familiares, exploración clínica, evaluación de la hipoxemia y pruebas de imagen torácica, que constituyen la piedra angular del diagnóstico.
Otras herramientas diagnósticas incluyen pruebas de función pulmonar, análisis de laboratorio específicos, broncoscopia con lavado broncoalveolar, ecocardiografía, pruebas genéticas y, si es necesario, como paso final, una biopsia pulmonar (Fig. 2)(18-20).
Figura 2. Investigaciones en el enfoque diagnóstico de las enfermedades pulmonares intersticiales infantiles.
• Historial médico: el inicio y las características de los síntomas pueden orientar a un diagnóstico específico. Una historia familiar detallada es importante. Los trastornos recesivos se observan con mayor frecuencia en casos de consanguinidad, mientras que los trastornos dominantes pueden manifestarse a lo largo de generaciones con penetrancia y expresividad variables. También se debería preguntar sobre los hábitos de vida y las posibles exposiciones ambientales que podrían estar relacionadas con la aparición o empeoramiento de la neumopatía.
• Pruebas de imagen: la radiografía de tórax muestra anomalías inespecíficas o puede ser normal. La TAC pulmonar es la prueba más sensible y los hallazgos más comunes asociados a chILD son: opacidades en vidrio deslustrado, nódulos y micronódulos, quistes aéreos, engrosamiento septal y atrapamiento aéreo. En la mayoría de los casos, los hallazgos son inespecíficos; sin embargo, ciertos patrones pueden indicar diagnósticos específicos, como opacidades en vidrio deslustrado en lóbulo medio, língula y regiones parahiliares/paramediastínicas, característica de la hiperplasia de células neuroendocrinas (Fig. 3).
Figura 3. A. Corte axial a la altura de la língula. B. Reconstrucción coronal. Áreas con patrón en vidrio deslustrado que afectan predominantemente al lóbulo medio y a la língula, mostrando el patrón de distribución típico de la hiperplasia de células neuroendocrinas de la infancia.
• Pruebas de función pulmonar: en general, suelen presentar un patrón restrictivo. En la hiperplasia de células neuroendocrinas se ha descrito un patrón obstructivo con hiperinsuflación. La bronquiolitis obliterante se caracteriza por un patrón obstructivo irreversible con atrapamiento aéreo. La medición de la capacidad de difusión pulmonar de monóxido de carbono (DLCO) suele estar disminuida, excepto en la hemorragia pulmonar, que está elevada(21). La prueba de marcha de 6 minutos puede ser útil en el seguimiento de niños en edad escolar.
• Ecocardiografía: es útil para descartar hipertensión pulmonar y excluir cardiopatías.
• Estudios analíticos: dependerán de la orientación clínica, incluyendo: estudios inmunológicos, autoinmunidad, hipersensibilidad y enfermedades sistémicas(19).
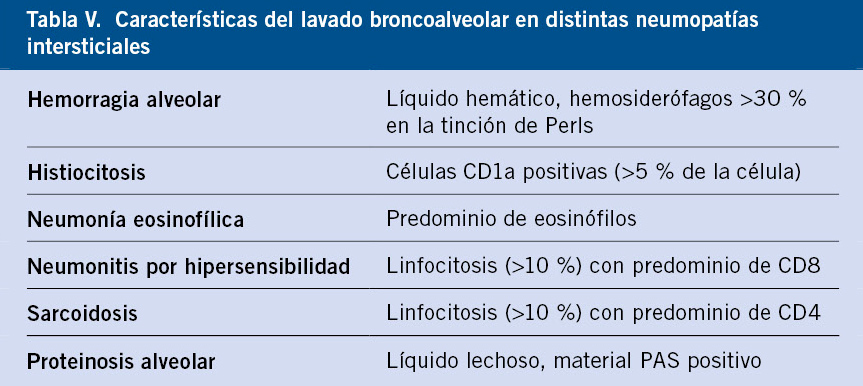
• Lavado broncoalveolar: es útil para descartar infecciones y orienta hacia algunas enfermedades (Tabla V).
• Biopsia pulmonar: está indicada cuando no se ha obtenido un diagnóstico con las exploraciones anteriores. Se realiza mediante minitoracotomía o videotoracoscopia, preferiblemente en dos áreas con diferente grado de afectación.
• Estudios genéticos: se recomienda para todos los niños con chILD sin causa identificada. Actualmente, solo se identifica la causa genética en un 20 % de los casos(22). Algunas de las mutaciones son: las relacionadas con el déficit de proteína del surfactante (déficit de proteína B, C y ABCA3); mutaciones en el gen NKX2-1 o TTF-1 (asociadas con neumopatía intersticial, hipotiroidismo y alteración neurológica); mutaciones causantes de proteinosis alveolar (CSF2RA, CSF2RB y MARS); deficiencia de GATA2 (asociadas a manifestaciones hematológicas, infecciones oportunistas y neumopatía intersticial); y mutaciones relacionadas con trastornos del desarrollo alveolar (gen filamina A y gen ACTA2) y con trastornos del desarrollo pulmonar, como el gen FOXF1(19).
Tratamiento
Las medidas generales son: corregir la hipoxemia, optimizar la nutrición, tratar las infecciones, promover la correcta inmunización (especialmente gripe y neumococo) y evitar irritantes pulmonares (tabaco, contaminación y alérgenos).
A nivel de tratamiento antiinflamatorio, en la mayoría de chILD, el abordaje más usado son los corticoides sistémicos, que pueden ser en forma de pulsos endovenosos de metilprednisolona (10-30 mg/kg/día) durante 3 días consecutivos, mensualmente durante 1-6 meses, o prednisolona oral a 1-2 mg/kg/día, ya sea solos o combinados con hidroxicloroquina (para ayudar a reducir el daño celular y la fibrosis)(19). La azitromicina (10 mg/kg/día, 3 días a la semana) puede ser útil en inflamación persistente sin fibrosis, en situación de infecciones respiratorias de repetición, bronquiectasias asociadas o algunas mutaciones del surfactante, como ABCA3. En las neumopatías intersticiales relacionadas con enfermedades del tejido conectivo o síndromes autoinflamatorios, pueden considerarse fármacos inmunosupresores, como micofenolato de mofetilo, azatioprina, rituximab o inhibidores de JAK. El trasplante pulmonar está reservado para casos graves refractarios(19,20).
Pronóstico
El pronóstico es muy variable y depende de varios factores: el tipo específico de chILD (algunas son autolimitadas o tratables, mientras que otras pueden ser crónicas, progresivas y letales); la edad de inicio (cuanto más temprana, suele tener peor pronóstico); la presencia de fibrosis progresiva en el TAC; la pérdida persistente de función pulmonar; la respuesta al tratamiento; y si tiene comorbilidades asociadas. Se asocian a mal pronóstico: trastornos del desarrollo y crecimiento pulmonar, los déficits de proteína B del surfactante y déficit de ABCA3 de presentación neonatal; y a buen pronóstico: la hiperplasia de células neuroendocrinas o la glucogenosis intersticial pulmonar (sin trastorno importante del desarrollo alveolar asociado).
Displasia broncopulmonar (DBP)
Definición y fisiopatología
La displasia broncopulmonar (DBP) es la complicación crónica a nivel pulmonar más frecuente del prematuro.
A pesar de afectar principalmente el sistema respiratorio, puede generar también alteraciones a nivel cardiovascular, de crecimiento y en el neurodesarrollo, con una pérdida de la calidad de vida en la edad pediátrica y en el adulto(23).
Desde su primera descripción en 1967, ha habido múltiples definiciones. Actualmente, la más utilizada es la propuesta en 2001 por el consenso del National Institute of Child Health and Human Development (NICHD), que establece el diagnóstico de DBP, como la necesidad de oxigenoterapia, al menos, durante 28 días. Este mismo consenso clasificaba la gravedad de la DBP según la FiO2 requerida a las 36 semanas de edad postmenstrual o al alta en los nacidos antes de las 32 semanas de gestación, o a los 56 días de vida en los nacidos a las ≥32 semanas. El NICHD realizó posteriormente un estudio prospectivo para determinar los principales factores de morbilidad en la DBP. A partir de este estudio, la clasificación utilizada actualmente para la gradación de la severidad de la DBP se basa en el tipo de soporte respiratorio requerido a las 36 semanas de gestación, independientemente de la FiO2(24) (Tabla VI).
A pesar de los avances médicos, la incidencia de DBP se ha mantenido estable a lo largo de los años. La explicación la encontramos en el aumento de supervivencia de los recién nacidos de muy bajo peso. Estos avances sí han representado un cambio en las características de la DBP. En la denominada “antigua DBP”, se observaba un predominio del componente enfisematoso y fibrótico secundario a una ventilación más agresiva y a las altas concentraciones de oxigenoterapia. A partir de los años 90, se observó un aumento de la supervivencia y cambios en las características de la DBP. Esto fue debido a la introducción de los corticoides prenatales, al uso de surfactante y a los cambios en la ventilación, con un mayor uso de la ventilación no invasiva y parámetros menos agresivos, permitiendo una hipercarbia permisiva. Esta “nueva DBP” se caracteriza por una simplificación alveolar y disregulación en la vascularización pulmonar, secundarias a la interrupción precoz del desarrollo del pulmón(25).
Manifestaciones pulmonares durante la infancia
Los niños nacidos pretérmino y con muy bajo peso, muy especialmente aquellos con diagnóstico de DBP, presentan una mayor morbilidad respiratoria durante los primeros años de vida.
Es habitual el ingreso hospitalario causado por infecciones de las vías aéreas inferiores asociadas a sibilancias, especialmente durante los 2 primeros años. Varios estudios reportan que aproximadamente el 50 % de los niños diagnosticados de DBP requieren ingreso durante el primer año de vida, por complicaciones a nivel respiratorio. Existe una mayor susceptibilidad a presentar complicaciones con relación a las infecciones virales, muy especialmente por virus respiratorio sincitial (VRS)(26).
La introducción de nirsevimab ha provocado una reducción muy significativa de ingresos por bronquiolitis por VRS en la población general, aunque no se disponen de datos específicos en la población con displasia broncopulmonar. Otros factores, como la exposición al humo del tabaco, pueden facilitar la aparición de complicaciones respiratorias en estos pacientes. Existen otras comorbilidades asociadas a la displasia broncopulmonar que pueden también empeorar la evolución respiratoria. Aproximadamente, el 60 % de los prematuros presentan reflujo gastroesofágico. La aspiración del contenido gástrico por este reflujo puede exacerbar la alteración a nivel pulmonar subyacente(27). Puede también existir un componente de traqueobroncomalacia que agrave los síntomas respiratorios, empeorando el estado con el uso de broncodilatadores.
La evolución, a lo largo de los años, acostumbra a ser hacia una mejoría, con un claro descenso de las hospitalizaciones por causa respiratoria a partir de los 3-4 años. A pesar de esta mejoría, manifestaciones respiratorias persisten a los 4-5 años en un porcentaje remarcable de pacientes(26).
Sintomatología asmática y evolución de la función respiratoria
Tal y como ya se ha comentado, los pacientes con antecedente de DBP presentan un mayor riesgo de padecer episodios de sibilancias durante los primeros años de vida y la edad escolar que el resto de población. Además, presentan también una menor tolerancia al ejercicio físico. Estos síntomas, habitualmente descritos como asthma-like, vienen condicionados por un patrón de obstrucción bronquial. Múltiples estudios muestran una disminución de FEV1 (Volumen Espiratorio Forzado en el primer segundo) en los escolares con antecedente de prematuridad y bajo peso al nacer, siendo más marcada esta afectación en los diagnosticados de DBP. Asimismo, se ha observado también una hiperreactividad bronquial, tanto al ejercicio como a la metacolina. Esto conduce a que, en múltiples ocasiones, se etiquete de forma poco precisa a estos pacientes como asmáticos. Hay que tener en cuenta que, a pesar de la naturaleza obstructiva de las dos entidades, la inflamación subyacente es diferente. En el asma, mayoritariamente la inflamación es eosinofílica, con valores elevados de óxido nítrico exhalado y, frecuentemente, con antecedentes de atopia. En la DBP no existen estos antecedentes y la inflamación es de naturaleza neutrofílica(27). Además, mientras la obstrucción bronquial en el asmático es reversible con el uso de betaadrenérgicos, en la DBP esta reversibilidad es parcial. La diferenciación de estas dos entidades es importante, ya que su historia natural y su manejo terapéutico no es el mismo.
Existen estudios que muestran que el patrón obstructivo en los casos de DBP persiste hasta la adolescencia, mientras que no existe esta alteración en los prematuros sin DBP. Por el contrario, no existen diferencias en la clínica asmática observada en los pretérminos con diagnóstico de DBP, sin DBP y en los nacidos a término(28).
Tratamiento
• Oxigenoterapia: no existe un consenso a partir de los estudios actuales que determine con exactitud la SatO2 mínima para evitar alteraciones en el desarrollo, una vez superadas las 36 semanas de edad gestacional corregida. Sí se conoce con certeza que saturaciones por debajo del 90 % deben evitarse. Asimismo, otro estudio mostró que no había diferencia en la evolución de los pacientes con saturaciones entre 91-94 % vs. 95-98 %. Las guías elaboradas por la American Thorax Society (ATS) y la European Respiratory Society (ERS) sugieren establecer, como objetivo, saturaciones >90 %. A pesar de esto, reconocen la necesidad de estudios para determinar el valor ideal de saturación entre 90-93 %(29).
• Diuréticos: no se ha observado un beneficio en tratamiento con diuréticos. Posteriormente, a las 36 semanas de edad gestacional corregida, únicamente se recomienda su uso de forma empírica de forma puntual en pacientes con episodios de edema. En los pacientes que reciben este tratamiento, se recomienda retirada progresiva, manteniendo dosis a pesar del aumento de peso(29).
• Corticoterapia inhalada: no se ha observado un beneficio en el uso de corticoides de mantenimiento en los pacientes con DBP. En casos de DBP grave con múltiples episodios de sibilancias en ingresos, se puede realizar una prueba de forma empírica, controlando de forma estrecha su efectividad y sus potenciales efectos adversos(29).
Implicaciones de la DBP en la edad adulta
Existe un número creciente de publicaciones reportando la afectación pulmonar en la edad adulta secundaria a la DBP. Por una parte, existe ya un amplio conocimiento en la persistencia de la obstrucción bronquial en las pruebas de función respiratoria.
Asimismo, cada vez hay una mayor certeza de casos de enfermedad pulmonar obstructiva crónica (EPOC) de aparición temprana con relación a la DBP. Estos casos se pueden ver favorecidos por la exposición a tóxicos, como el humo de tabaco, y por la presencia de factores genéticos(27).
Con los conocimientos actuales, podemos afirmar que la DBP no es únicamente una afectación de la edad pediátrica, sino que sus efectos se pueden observar a lo largo de toda la vida.
Por este motivo, es de gran importancia el papel del pediatra, realizando un seguimiento a lo largo de la infancia, estableciendo medidas preventivas a nivel higiénico y de hábitos tóxicos, así como llevando a cabo una adecuada transferencia de la información al médico de adultos.
Función del pediatra de Atención Primaria
• Identificar a los pacientes con signos de enfermedad respiratoria crónica (tos crónica, taquipnea, infecciones respiratorias recurrentes, auscultación patológica persistente).
• Identificar a los pacientes con factores de riesgo, como la prematuridad, la displasia broncopulmonar, inmunodeficiencias y aspiraciones.
• Realizar un seguimiento clínico, evolutivo y coordinar la derivación con el servicio de neumología pediátrica.
• Detectar las complicaciones y valorar la respuesta al tratamiento en las agudizaciones.
• Controlar que el calendario vacunal esté completo, incluyendo vacunación antigripal, antineumocócica, inmunización con anticuerpo monoclonal frente al virus sincitial respiratorio (VRS) y promover la evitación del humo de tabaco y de contaminantes ambientales. En determinados pacientes, se incentivará la realización habitual de fisioterapia respiratoria, incrementando su uso durante las agudizaciones.
• Educar a las familias sobre la higiene, prevención de infecciones, signos de alarma de exacerbaciones y el momento en el que deben acudir a urgencias.
Conflicto de intereses
No hay conflicto de interés en la elaboración del presente manuscrito ni fuente de financiación.
Bibliografía
Los asteriscos muestran el interés del artículo a juicio de los autores.
1. Boesch RP, Daines C, Willging JP, Kaul A, Cohen AP, Wood RE, et al. Advances in the diagnosis and management of chronic pulmonary aspiration in children. Eur Respir J. 2006; 28: 847-61. Disponible en: https://doi.org/10.1183/09031936.06.00138305.
2.** Cuestas G, Rodríguez V, Bellia P, Bellia G. Algoritmo para el manejo de la aspiración pulmonar crónica en pediatría. Arch Argent Pediatr. 2019; 117: 412-20.
3. Tanaka N, Nohara K, Ueda A, Katayama T, Ushio M, Fujii N, et al. Effect of aspiration on the lungs in children: a comparison using chest computed tomography findings. BMC Pediatrics. 2019; 19: 162. Disponible en: https://doi.org/10.1186/s12887-019-1531-6.
4. Pastor MD. Síndromes aspirativos. En: M. Cruz. Manual de Pediatría, 4ª ed. Madrid: Ergon; 2020. p. 1032-4.
5.*** Cols-Roig M. Síndrome aspirativo crónico en la edad pediátrica. En: García Ezquerra R y cols. Abordaje de la disfagia pediátrico-neonatal, 1ª ed. Barcelona: Elsevier; 2022. p. 151-7.
6. Duvallet C, Larson K, Snapper S, Iosim S, Lee A, Freer K, et al. Aerodigestive sampling reveals altered microbial exchange between lung, oropharyngeal, and gastric microbiomes in children with impaired swallow function. PLoS ONE. 2019; 14: e0216453. Disponible en: https://doi.org/10.1371/journal.pone.0216453.
7. Colombo JL, Halberg TK. Recurrent aspiration in children: lipid-laden alveolar macrophage quantitation. Pediatr Pulmonol. 1987; 3: 86-9. Disponible en: https://doi.org/10.1002/ppul.1950030209.
8. Faverio P, Franco G, Landoni V, Nadalin M, Negri D, Tagliabue A, et al. Therapeutic Management of Bronchiectasis in Children and Adolescents: A Concise Narrative Review. J Clin Med. 2024; 13: 4757. Disponible en: https://doi.org/10.3390/jcm13164757.
9.** Anne B, Chang, MBBS, FRACP, MPHTM. Bronquiectasias y enfermedad pulmonar supurativa. En: Robert W. Wilmott, Andrew Bush, y cols. Enfermedades respiratorias en niños. 9ª ed. Barcelona: Elsevier; 2019. p. 439-59.
10.** Tsouprou M, Koumpagioti D, Botsa E, Douros K, Moriki D. Utilization of Inhaled Antibiotics in Pediatric Non-Cystic Fibrosis Bronchiectasis: A Comprehensive Review. Antibiotics (Basel). 2025; 14: 165. Disponible en: https://doi.org/10.3390/antibiotics14020165.
11.** Chang AB, Bush A, Grimwood K. Bronchiectasis in children: diagnosis and treatment. Lancet. 2018; 392: 1196. Disponible en: https://doi.org/10.1016/s0140-6736(18)31554-x.
12. Lim AYL, Kantar A, Chang AB. Protracted bacterial bronchitis and non-CF bronchiectasis. En: Ernst Eber, Fabio Midulla. ERS (European Respiratory Society) handbook. Paediatric Respiratory Medicine. 2nd Edition. UK; 2021. p. 312-23.
13.*** Chang AB, Fortescue R, Grimwood K, Alexopoulou E, Bell L, Boyd J, et al. European Respiratory Society guidelines for the management of children and adolescents with bronchiectasis. Eur Respir J. 2021; 58: 1-29. Disponible en: https://doi.org/10.1183/13993003.02990-2020.
14. Lim M, Chan M, Widger J, Prentice B, Wales S, Stroil-Salama E, et al. Risk factors associated with severe non-CF bronchiectasis in children. International Journal of Infectious Diseases. 2020; 96: 46-53. Disponible en: https://doi.org/10.1016/j.ijid.2020.11.027.
15. Deutsch GH, Young LR, Deterding RR, Fan LL, Dell SD, Bean JA, et al. Diffuse lung disease in young children: application of a novel classification scheme. Am J Respir Crit Care Med. 2007; 176: 1120-8. Disponible en: https://doi.org/10.1164/rccm.200703-393oc.
16. Griese M. Chronic interstitial lung disease in children. Eur Respir Rev. 2018; 27: 170100. Disponible en: https://doi.org/10.1183/16000617.0100-2017.
17.** Torrent-Vernetta A, Gaboli M, Castillo-Corullón S, Mondéjar-López P, Sanz Santiago V, Costa-Colomer J, et al. Incidence and Prevalence of Children’s Diffuse Lung Disease in Spain. Arch Bronconeumol. 2022; 58: 22-9. Disponible en: https://doi.org/10.1016/j.arbres.2021.06.001.
18.** Bush A, Cunningham S, de Blic J, Barbato A, Clement A, Epaud R, et al. European protocols for the diagnosis and initial treatment of interstitial lung disease in children. Thorax. 2015; 70: 1078-84. Disponible en: https://doi.org/10.1136/thoraxjnl-2015-207349.
19.** Nathan N, Griese M, Michel K, Carlens J, Gilbert C, Emiralioglu N, et al. Diagnostic workup of childhood interstitial lung disease. Eur Respir Rev. 2023; 32: 220188. Disponible en: https://doi.org/10.1183/16000617.0188-2022.
20.*** Marczak H, Krenke K, Griese M, Carlens J, Seidl E, Gilbert C, et al. An update on diagnosis and treatments of childhood interstitial lung diseases. Breathe (Sheff). 2025; 2: 250004. Disponible en: https://doi.org/10.1183/20734735.0004-2025.
21. Ring AM, Carlens J, Bush A, Castillo-Corullón S, Fasola S, Gaboli MP, et al. Pulmonary function testing in children’s interstitial lung disease. Eur Respir Rev. 2020; 29: 200019. Disponible en: https://doi.org/10.1183/16000617.0019-2020.
22. Griese M, Seidl E, Hengst M, Reu S, Rock H, Anthony G, et al. International management platform for children’s interstitial lung disease (chILD-EU). Thorax. 2018; 73: 231-9. Disponible en: https://doi.org/10.1136/thoraxjnl-2017-210519.
23.** Gilfillan M, Bhandari A, Bhandari V. Diagnosis and management of bronchopulmonary dysplasia. BMJ. 2021; 375: n1974. Disponible en: https://doi.org/10.1136/bmj.n1974.
24. Jensen EA, Dysart K, Gantz MG, McDonald S, Bamat NA, Keszler M, et al. The Diagnosis of Bronchopulmonary Dysplasia in Very Preterm Infants. An Evidence-based Approach. Am J Respir Crit Care Med. 2019; 200: 751-9. Disponible en: https://doi.org/10.1164/rccm.201812-2348OC.
25.*** Enzer KG, Baker CD, Wisniewski BL. Bronchopulmonary Dysplasia. Clin Chest Med. 2024; 45: 639-50. Disponible en: https://doi.org/10.1016/j.ccm.2024.03.007.
26. Pérez G, Navarro M. Displasia broncopulmonar y prematuridad. Evolución respiratoria a corto y a largo plazo. An Pediatr (Barc). 2010; 72: 79.e1-e16.
27. Homan TD, Nayak RP. Short- and Long-Term Complications of Bronchopulmonary Dysplasia. Respir Care. 2021; 66: 1618-29. Disponible en: https://doi.org/10.4187/respcare.08401.
28. Pérez-Tarazona S, Rueda Esteban S, García-García ML, Arroyas Sánchez M, de Mir Messa I, Acevedo Valarezo T, et al. Respiratory outcomes of “new” bronchopulmonary dysplasia in adolescents: A multicenter study. Pediatr Pulmonol. 2021; 56: 1205-14. Disponible en: https://doi.org/10.1002/ppul.25226.
29.*** Duijts L, van Meel ER, Moschino L, Baraldi E, Barnhoorn M, Bramer WM, et al. European Respiratory Society guideline on long-term management of children with bronchopulmonary dysplasia. Eur Respir J. 2020; 55: 1900788. Disponible en: https://doi.org/10.1183/13993003.00788-2019.
30. Rodríguez Alonso A, Molina Amores C, Ruiz de Valbuena Maiz M. Patología pulmonar crónica. Pediatr Integral. 2021; 2: 101-8. Disponible en: https://www.pediatriaintegral.es/publicacion-2021-03/patologia-pulmonar-cronica/.
Bibliografía recomendada
– Cols-Roig M. Síndrome aspirativo crónico en la edad pediátrica. En: García Ezquerra R y cols. Abordaje de la disfagia pediátrico-neonatal, 1ª ed. Barcelona: Elsevier; 2022. p. 151-7.
Capítulo didáctico y práctico sobre la valoración clínica y el abordaje diagnóstico y terapéutico del paciente pediátrico con patología aspirativa crónica.
– Chang AB, Fortescue R, Grimwood K, Alexopoulou E, Bell L, Boyd J, et al. European Respiratory Society guidelines for the management of children and adolescents with bronchiectasis. Eur Respir J. 2021; 58: 1-29. Disponible en: https://doi.org/10.1183/13993003.02990-2020.
Guía completa y actualizada de la Sociedad Europea Respiratoria sobre el diagnóstico, manejo y el seguimiento del paciente pediátrico con bronquiectasias no asociadas a fibrosis quística; cuenta con las recomendaciones del grupo de trabajo.
– Marczak H, Krenke K, Griese M, Carlens J, Seidl E, Gilbert C, et al. An update on diagnosis and treatments of childhood interstitial lung diseases. Breathe (Sheff). 2025; 2: 250004. Disponible en: https://doi.org/10.1183/20734735.0004-2025.
Revisión actualizada sobre el enfoque diagnóstico y terapéutico para los pacientes pediátricos con neumopatías intersticiales.
– Duijts L, van Meel ER, Moschino L, Baraldi E, Barnhoorn M, Bramer WM, et al. European Respiratory Society guideline on long-term management of children with bronchopulmonary dysplasia. Eur Respir J. 2020; 55: 1900788. Disponible en: https://doi.org/10.1183/13993003.00788-2019.
Es una guía completa y actualizada sobre el manejo de los pacientes con displasia broncopulmonar; cuenta con las recomendaciones del grupo de trabajo.
| Caso clínico |
|
Paciente de 6 años que presenta infecciones respiratorias recurrentes y tos crónica. Antecedentes: recién nacido a término. Sin antecedentes perinatales de interés. Esquema vacunal incompleto. Sin alergias conocidas. Dermatitis atópica. Sin antecedentes familiares de asma o alergia respiratoria o alimentaria. Historia respiratoria: bronquiolitis aguda, de curso ambulatorio, a los 6 meses de vida. Desde los 2 años, inicia sibilancias recurrentes con desencadenante viral, de predominio en otoño-invierno, presentando 4-5 episodios anualmente. La mayoría de episodios son moderados, requiriendo corticoterapia oral. Ha precisado dos ingresos: el primero por infección por VRS, precisando oxigenoterapia de flujo convencional; y el segundo, en contexto de infección por rinovirus y neumococo, presenta bronconeumonía grave con atelectasia de lóbulo medio, con requerimientos de ventilación mecánica en unidad de cuidados intensivos pediátricos (UCIP). Tras el alta, había presentado 3 agudizaciones respiratorias que se resolvieron tras antibioticoterapia y permanece con tos productiva matutina y expectoración diurna intermitente en los últimos 4 meses. Niega tos seca nocturna. En ocasiones, presenta disnea de esfuerzo. Niega clínica de reflujo gastroesofágico o disfagia. Exploración física: SatO2: 97 %; frecuencia respiratoria: 26; buen estado general; abdomen: normal. Aparato respiratorio: buena ventilación pulmonar, crepitantes en base derecha. Aparato cardiovascular: ruidos cardiacos rítmicos, sin soplos. Examen neurológico: normal. Exploraciones complementarias: radiografía de tórax: infiltrado en lóbulo medio, engrosamientos peribronquiales. TAC tórax: se evidencian bronquiectasias quísticas en lóbulo medio con tractos de aspecto fibrocicatricial. No hay áreas de atrapamiento aéreo.
|







 Pulmonary tuberculosis
Pulmonary tuberculosis