 |
| Temas de FC |
F. Álvarez Caro![]() , M. García González, A. Méndez Sánchez
, M. García González, A. Méndez Sánchez
Unidad de Neumoalergia Infantil. Servicio de Pediatría. Hospital Universitario de Cabueñes. Gijón
| Resumen
El asma es una de las enfermedades crónicas más prevalentes en la infancia. El objetivo final del tratamiento del asma es lograr y mantener el control total de la misma. El tratamiento del asma se divide en el tratamiento de mantenimiento o de fondo y en el tratamiento de las exacerbaciones agudas. Para el primero, se dispone de un arsenal terapéutico que incluye: corticoides inhalados, broncodilatadores de acción larga, antagonistas de los receptores de leucotrienos, anticolinérgicos de acción prolongada y anticuerpos monoclonales. Un dato prioritario para alcanzar el objetivo final es la educación del niño y su familia, dado que la principal causa de mal control de la enfermedad es el incumplimiento terapéutico, bien por la administración insuficiente e inconstante, o bien por la mala técnica de administración de las terapias inhaladas. Los objetivos del tratamiento de una exacerbación aguda de asma son principalmente revertir la obstrucción y corregir la hipoxemia, disponiendo para ello de armas terapéuticas, como broncodilatadores de acción corta, corticoides sistémicos, anticolinérgicos de acción corta, oxigenoterapia y sulfato de magnesio, entre otros. |
| Abstract
Asthma is one of the most prevalent chronic diseases in childhood. The ultimate goal of asthma treatment is to achieve and maintain complete control. Asthma treatment is divided in maintenance treatment and treatment of acute exacerbations. For the former, several drugs are available such as inhaled corticosteroids, long-acting bronchodilators, leukotriene receptor antagonists, long-acting anticholinergics, and monoclonal antibodies. A priority for achieving this ultimate goal is educating patients and their families, given that the main cause of poor disease control is therapeutic noncompliance, either due to insufficient and inconsistent administration or poor administration technique for inhaled therapies. Treatment goals for an acute asthma exacerbation are primarily reversing bronchial obstruction and correcting hypoxemia. For this, several drugs may be used such as short-acting bronchodilators, systemic corticosteroids, short-acting anticholinergics, oxygen therapy, and magnesium sulfate among others. |
Palabras clave: Asma infantil; Tratamiento; Fármacos antiasmáticos; Educación sanitaria; Control.
Key words: Childhood asthma; Treatment; Anti-asthma drugs; Patient education; Control.
Pediatr Integral 2026; XXX (2): 99 – 106
OBJETIVOS
• Entender los distintos aspectos del tratamiento del asma infantil.
• Poder llevar a cabo el tratamiento de mantenimiento del niño asmático, independientemente de su gravedad.
• Poder llevar a cabo el tratamiento de una exacerbación asmática de acuerdo al nivel de gravedad de la misma.
• Conocer las distintas características y particularidades de los distintos tratamientos utilizados en el manejo agudo y crónico del asma.
Tratamiento de asma en pediatría
https://doi.org/10.63149/j.pedint.120
Introducción
El asma es un problema de salud pública, siendo un motivo muy frecuente de consulta, tanto en Atención Especializada como en Atención Primaria.
El asma es una de las enfermedades crónicas más frecuentes en la infancia, que genera mayor impacto económico y pérdida de calidad de vida(1,2), constituyendo un problema de salud a nivel global. En España, entre el 12-15 % de los niños y adolescentes son asmáticos(3), dependiendo su coste, entre otros factores, de la gravedad de la enfermedad. Hace ya más de una década, su coste total en Pediatría en España era de unos 532 millones de euros(4), representando los costes directos (costes sanitarios) el 60 % del total, y los indirectos (tiempo de cuidador) el 40 %(5). Estos datos hacen perentoria la necesidad de optimizar los recursos, tanto terapéuticos como no terapéuticos(5).
Todas las guías de consenso asumen que el objetivo fundamental del tratamiento es conseguir y mantener el control total de la enfermedad(1,2). Su éxito se fundamenta en el tratamiento farmacológico y en la educación sanitaria, junto con la inmunoterapia específica en caso de estar indicada(6).
Tratamiento de la crisis de asma
Ante un niño con crisis asmática, se debe clasificar la misma en función de la gravedad para instaurar el tratamiento adecuado.
El diagnóstico y tratamiento precoces son claves en el manejo de la crisis de asma. Sería deseable que todo asmático dispusiera de un plan de acción escrito que ayude a reconocer los síntomas e iniciar el tratamiento pertinente. Los objetivos del tratamiento de la crisis de asma son revertir la obstrucción bronquial, corregir la hipoxemia e, idealmente, prevenir las recurrencias(6).
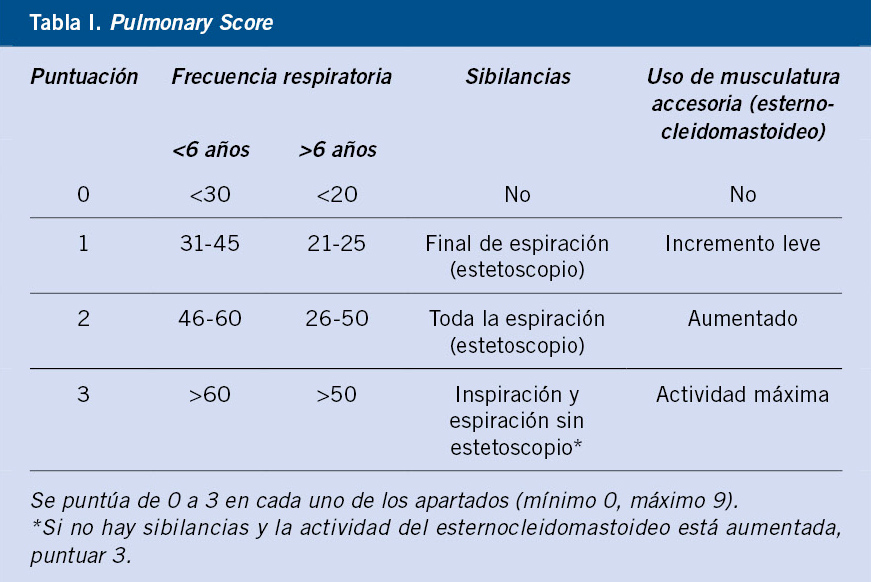
Aunque ninguna escala clínica está bien validada(7,8), el Pulmonary Score (Tabla I) es sencillo y aplicable a todas las edades(9).
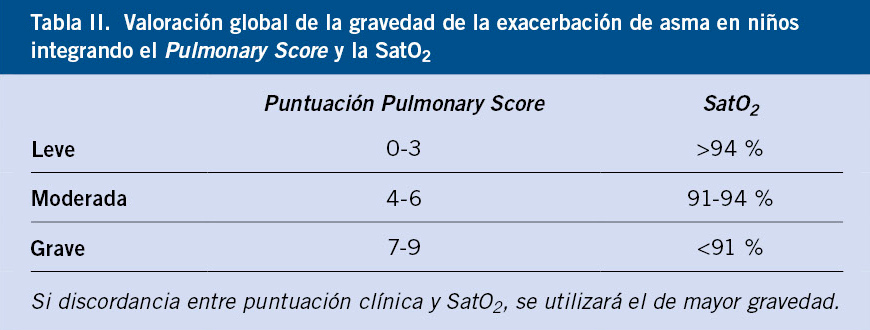
La combinación de síntomas con la saturación de oxígeno (SatO2) permitirá completar la estimación de la gravedad(1) (Tabla II). No está indicada la realización rutinaria de otras pruebas complementarias, como gasometría, analítica sanguínea, estudios microbiológicos o radiografía de tórax, salvo sospecha de complicaciones o formas graves.
De forma paralela a la valoración de la gravedad del asma, se debe completar la historia clínica, prestando especial atención a aspectos, como el tiempo de evolución, tratamiento administrado (dosis, periodicidad, tiempo de administración de última dosis, técnica inhalatoria), tratamiento de mantenimiento y existencia de enfermedades asociadas(10). Es importante identificar factores de riesgo de crisis asmática grave (Tabla III).
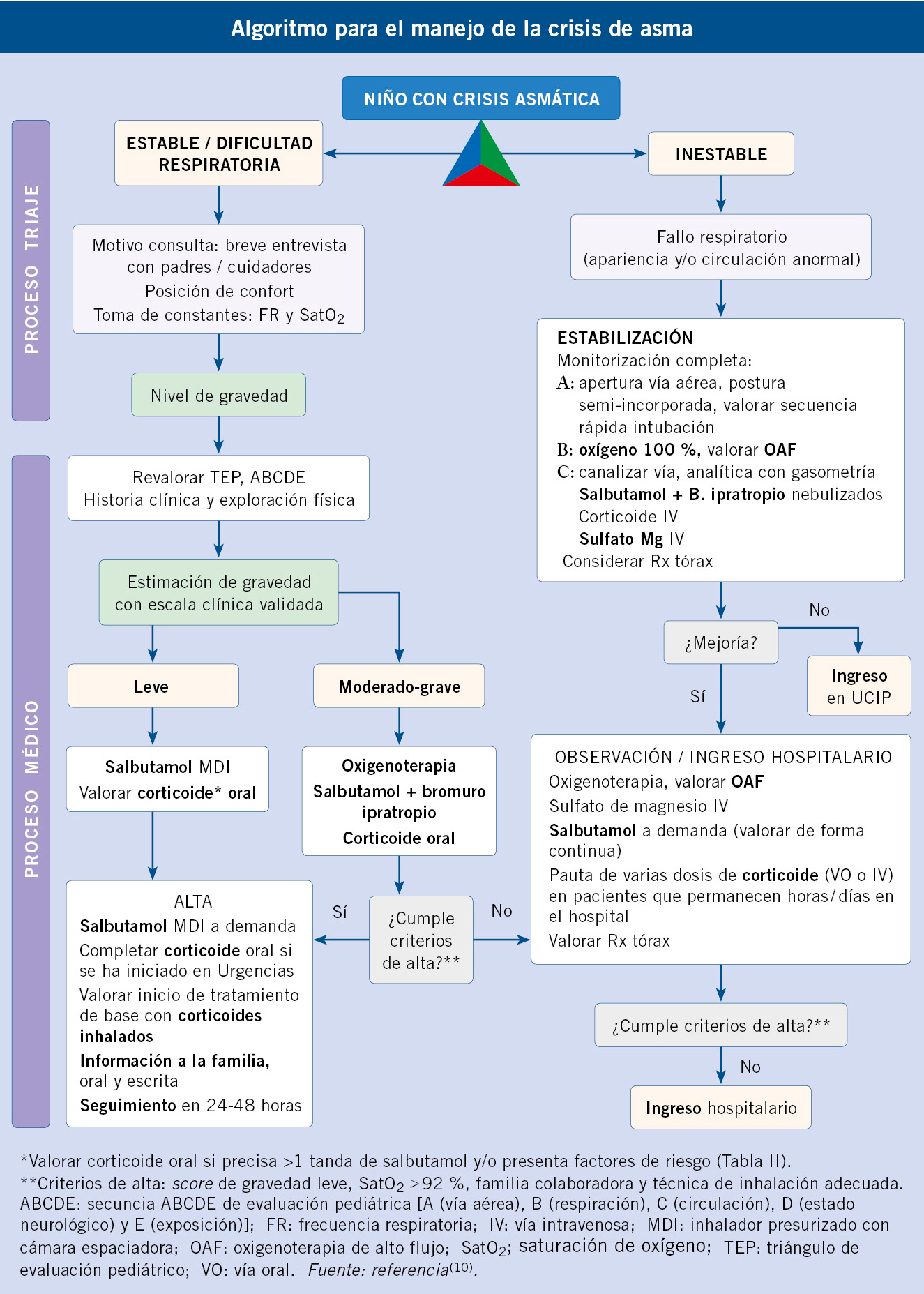
El manejo de la crisis de asma propuesto por la Sociedad Española de Urgencias de Pediatría se representa en el algoritmo al final del artículo(10).
Fármacos utilizados en las crisis de asma
• Oxígeno: se recomienda durante la estabilización de pacientes inestables, en crisis graves y en moderadas con gran trabajo respiratorio y/o hipoxemia. El objetivo es mantener SatO2 92 %.
• Agonistas B2 adrenérgicos inhalados de acción corta (SABA) (salbutamol): fármacos de primera línea. Se deben administrar, preferentemente, con inhalador presurizado y cámara espaciadora (MDI), ya que es tan efectivo como la vía nebulizada, con menos efectos secundarios y más coste-eficiencia. Se reserva la vía nebulizada para crisis graves y fallo respiratorio. La dosis de dispositivos presurizados en cámara espaciadora es de 2-4 pulsaciones en crisis leves, 6-8 en crisis moderadas y 10 en crisis graves. La dosis vía nebulizada es de 0,15 mg/kg (mínimo 2,5 mg, máximo 5 mg) o dosis estandarizadas de 2,5 mg para niños <20 kg y 5 mg para niños >20 kg(10). El tratamiento inicial suele realizarse con tres dosis de broncodilatador en la primera hora (cada 20 minutos).
• Corticoides sistémicos: indicados en crisis moderadas y graves, y en leves no respondedoras completas tras la primera dosis de salbutamol o con factores de riesgo (Tabla III). Se usan en pautas cortas (3-5 días). Se utilizan dosis de 1-2 mg/kg/día de prednisona o equivalente (máximo 60 mg/día). Es de elección la vía oral, siempre que sea posible(2). Una alternativa segura y eficaz es la dexametasona (dosis 0,6 mg/kg, máximo 12 mg), pudiendo repetir la misma a las 24 horas(10). Pautas cortas se pueden retirar bruscamente al no afectar al eje hipotálamo-hipófiso-suprarrenal. La vía intravenosa está indicada en casos de mayor gravedad o con intolerancia oral (metilprednisolona 1-2 mg/kg, máximo 125 mg/día)(10). En pacientes en tratamiento preventivo con corticoides inhalados, no deben retirarse, existiendo controversia sobre la utilidad de aumentar la dosis temporalmente ante la aparición de los primeros síntomas de exacerbación.
• Bromuro de ipratropio: indicado junto a SABA de rescate en forma de tres dosis sucesivas asociadas a las tandas iniciales de salbutamol(10). Se suele utilizar durante las primeras 48 horas de una crisis asmática grave. Utilizado de forma precoz, se ha asociado a disminución del número de hospitalizaciones. La dosis en dispositivos presurizados en <20 kg son 4 puff; si > 20 kg, hasta 8 puff. La dosis vía nebulizada en caso de <20 kg son 250 µg, y si >20 kg, 500 µg(11).
• Sulfato de magnesio: en pacientes con crisis graves o moderadas que no mejoran a pesar del tratamiento de rescate inicial (primeras 1-2 horas de atención). Una dosis única de 40 mg/kg (máximo 2 g) en perfusión intravenosa lenta ha demostrado reducir la tasa de hospitalización.
Tratamiento de mantenimiento del asma
La medicación de mantenimiento es aquella que se administra a diario y durante largos periodos de tiempo, con el objetivo de lograr el control de la enfermedad.
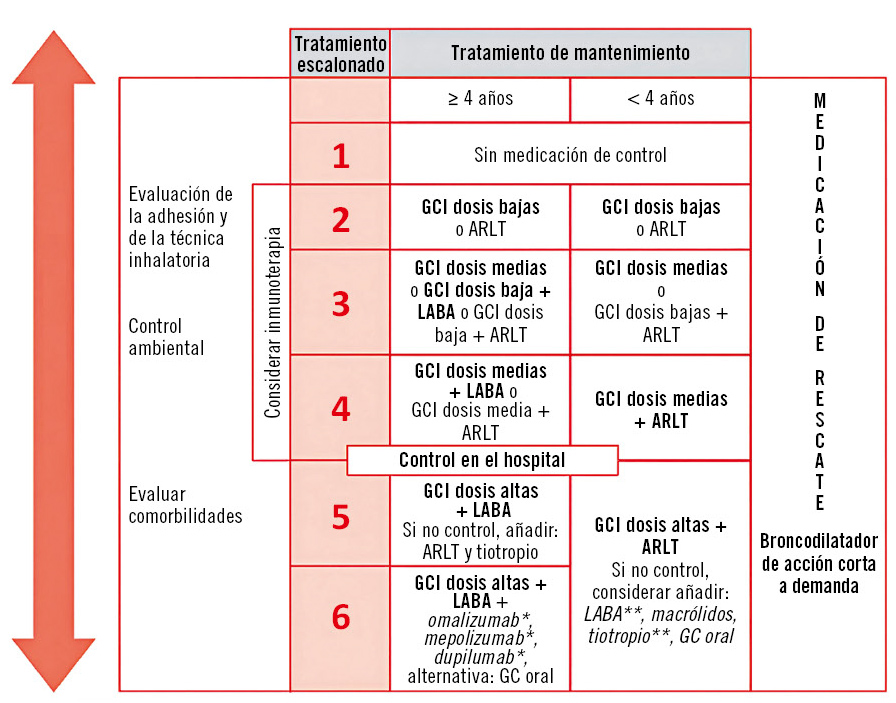
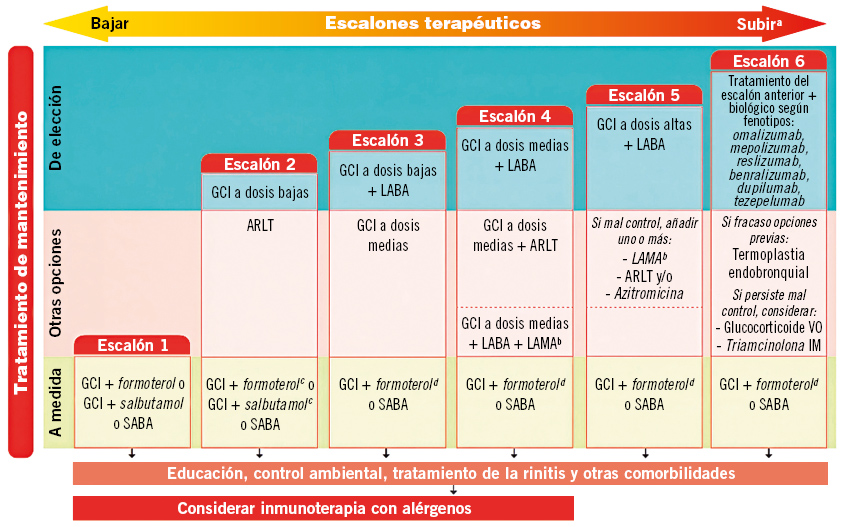
Se debe ajustar la misma de forma continua, en función del nivel de control, teniendo siempre presentes las medidas no farmacológicas y la adhesión terapéutica. El tratamiento de mantenimiento se iniciará en función del nivel de gravedad inicial, no necesariamente desde el primer escalón. En la figuras 1 y 2, se refleja el tratamiento escalonado en la edad pediátrica en función del nivel de control(1).
Figura 1. Tratamiento escalonado del asma en menores de 12 años. ARLT: antileucotrienos; GC: glucocorticoide; GCI: glucocorticoides inhalados; LABA: agonista B2 adrenérgico de larga duración. *A partir de 6 años. **Fuera de ficha técnica.
Fuente: referencia (1).
Figura 2. Tratamiento escalonado del asma a partir de los 12 años. ARLT: antileucotrienos; GCI: glucocorticoides inhalados; LABA: agonista B2 adrenérgico de larga duración.
Fuente: referencia(1).
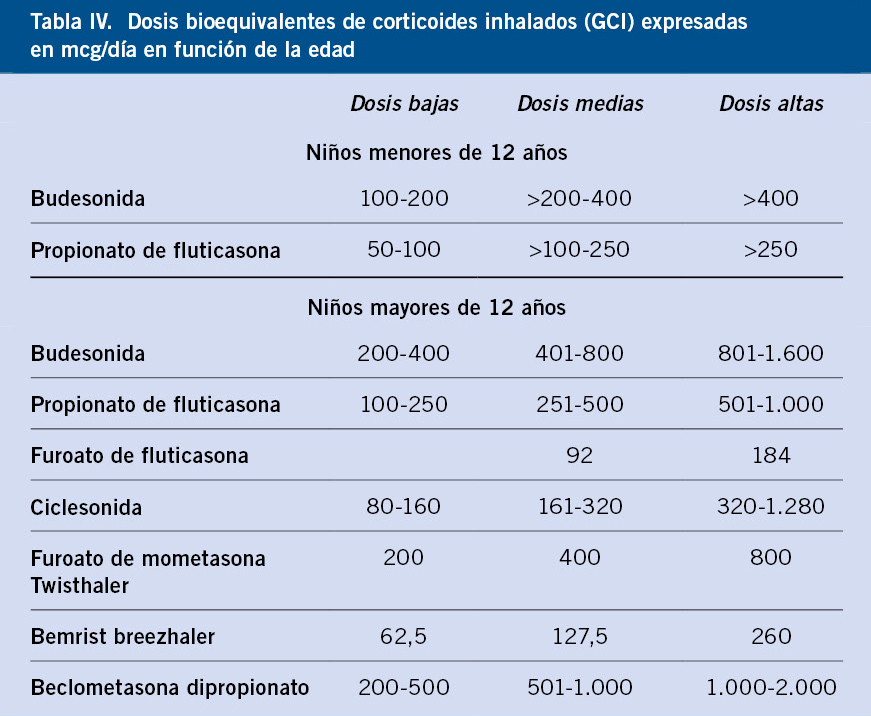
• Corticoides inhalados (GCI): tratamiento de elección a partir del escalón terapéutico 2, debido a su alta afinidad y selectividad por su receptor, su efecto antiinflamatorio local, su prolongada permanencia en el pulmón y su baja biodisponibilidad oral y sistémica. Actualmente, en España, se comercializan en forma de budesonida, fluticasona (propionato y furoato), beclometasona, ciclesonida y mometasona. Se debe utilizar siempre la mínima dosis eficaz necesaria para mantener el control y tener en cuenta la bioequivalencia entre los distintos GCI(6,12). Las dosis bioequivalentes de los mismos se recogen en la tabla IV. A partir de dosis medias-altas, es más efectivo añadir un segundo fármaco antes que seguir incrementando las dosis de ellos(6).
• Antagonistas de los receptores de leucotrienos (ARLT): el montelukast es el único fármaco de este grupo autorizado en España a partir de los 6 meses de vida. Se administra en dosis única diaria por vía oral, una hora antes o dos horas después de las comidas, pudiendo producir efectos secundarios, como dolor abdominal y alteraciones del sueño. En preescolares con asma, reducen de forma modesta los síntomas y la necesidad de corticoides orales(13,14). Se podría realizar un ensayo terapéutico para valorar eficacia, suspendiéndose en caso de no respuesta(13). Se precisa más evidencia para determinar si existe un fenotipo respondedor a ARLT(15). Si no existe control con GCI a dosis bajas, es más eficaz incrementar los GCI a dosis medias que asociar ARLT(16).
• Asociación de agonistas β2 adrenérgicos de acción larga (LABA) y GCI: los LABA deben asociarse siempre a un GCI, no recomendándose su uso en monoterapia ni como medicación preventiva ni como broncodilatador de rescate(1). En España existen las siguientes combinaciones: salmeterol/propionato de fluticasona (a partir de 4 años), formoterol/budesonida (a partir de 6 años), formoterol/propionato de fluticasona (a partir de 12 años), vilanterol/furoato de fluticasona (a partir de 12 años), indacaterol/furoato de mometasona (a partir de los 12 años) y formoterol/beclometasona (a partir de 18 años). Existen estudios que demuestran que, en niños a partir de 4 años con asma persistente no controlada con dosis bajas de GCI, es más eficaz añadir un LABA que doblar la dosis de GCI en el control clínico y la función pulmonar(17-19). Un tipo más novedoso de LABA son los ultra-LABA, como vilanterol o indacaterol, autorizados para pacientes >12 años en combinación con GCI. Dada su farmacocinética, que permite su dosificación en una única toma diaria, podrían suponer una ventaja para un mejor cumplimiento terapéutico y mejor control de la enfermedad, especialmente en adolescentes(20).
Dado el rápido inicio de acción del formoterol (5 minutos), en >12 años puede ser aplicable una estrategia de rescate con la combinación formoterol/budesonida en los distintos escalones del tratamiento(1), e incluso como terapia de rescate y mantenimiento con un único dispositivo (estrategia MART) en el escalón 2 del asma en adelante(1,21,22). Los resultados de los anteriores estudios podrían proporcionar evidencia indirecta para la posible indicación de las combinaciones de GCI a dosis bajas con formoterol, administrados exclusivamente a demanda en el tratamiento del escalón 2 en pacientes con baja adhesión terapéutica en los que fracasó una intervención educativa específica(1). Existen estudios que demuestran una disminución de exacerbaciones y de necesidad de glucocorticoides sistémicos en niños de 4-11 años tratados con formoterol/ budesonida de rescate y mantenimiento(23), si bien otros autores consideran que la evidencia es limitada en esta franja de edad(24).
• Antagonistas muscarínicos de acción prolongada (LAMA) (bromuro de tiotropio): se asocian a GCI y LABA(6). Indicado en niños >6 años con asma grave mal controlada, en tratamiento con GCI a dosis altas más LABA (escalón 5), siendo su dosis de 5 µg/día(25).
• Terapia biológica: indicada en asma grave no controlada (escalón 6) a partir de 6 años. El primero en desarrollarse fue el omalizumab (anti-IgE), para >6 años con asma alérgica grave por sensibilización a alérgeno perenne. Tanto mepolizumab (anti-IL5) como dupilumab (anti-IL4R/IL13) están autorizados para asma grave eosinofílica no controlada en >6 años. Y, finalmente, tezepelumab (antilinfopoyetina estromal tímica) está autorizado para niños >12 años con asma grave, tanto eosinofílica/alérgica como no eosinofílica (tanto en fenotipo Th1 como Th2).
• Inmunoterapia específica (ITE): cuando se usan extractos estandarizados biológicamente, en pacientes sensibilizados, adecuadamente seleccionados, ha mostrado efecto beneficioso, reduciendo síntomas, medicación de rescate y mantenimiento e hiperrespuesta bronquial(26). La ITE por vía subcutánea o sublingual es eficaz para el asma alérgica bien controlada (escalones 2 a 4), siempre que haya una sensibilización mediada por IgE frente a un aeroalérgeno común clínicamente relevante. No debe prescribirse en asma no controlada. Además, previene el desarrollo de nuevas sensibilizaciones y asma en niños con rinitis(27).
Sistemas de inhalación
Independientemente de la edad, la vía inhalada es la más adecuada para administrar la medicación en el tratamiento del asma.
Ningún tratamiento con medicación inhalada se puede realizar adecuadamente si el niño no usa los sistemas de inhalación de forma correcta. Es necesaria la revisión periódica de la técnica y se debe plantear el cambio de sistema, dependiendo de la edad, de la preferencia del niño mayor o cuando el asma no evolucione correctamente. En la tabla V se recomiendan los dispositivos de inhalación dependiendo de la edad(5).
Ajuste del tratamiento
Debe ajustarse en función del grado de control conseguido, aplicando cuando corresponda en cada caso los fármacos incluidos en cada escalón terapéutico.
Cualquier aumento debe entenderse como un ensayo terapéutico y ser revisado tras 2 o 3 meses. Si no se consigue la respuesta esperada, se deben considerar otras opciones o la derivación al especialista(6). Debe considerarse el descenso farmacológico, en ausencia de infecciones respiratorias o cambios ambientales, cuando los síntomas estén controlados y la función pulmonar haya permanecido estable durante, al menos, 3 meses. La reducción de los GCI un 25-50 % es factible y segura para la mayoría de los pacientes(6).
Control y gravedad del asma
Los términos control y gravedad del asma no son equivalentes, aunque estén íntimamente relacionados.
Tanto el control como la gravedad se asocian a los requerimientos de medicación que precisan los pacientes, siendo el asma grave aquella que precisa tratamiento en los escalones terapéuticos más elevados(1). Según el consenso nacional, se considera que un niño padece asma grave: si ha requerido dos o más ciclos de corticoides orales durante el último año; si requiere tratamiento con GCI a dosis medias (con otra medicación controladora) o dosis altas (con o sin otra medicación controladora); si no responde a un tratamiento convencional optimizado; si la enfermedad pone en peligro o deteriora de forma importante su calidad de vida; si consume (de manera justificada) recursos sanitarios regularmente; o si existen factores psicosociales o ambientales que impiden su control(6). Ante una sospecha de asma grave, debe diferenciarse si se trata de un asma de difícil control (ADC) o un asma grave refractaria al tratamiento (AGR). En el ADC se deben tratar en su caso factores que contribuyan a una mala respuesta terapéutica, como la falta de adherencia, factores ambientales perjudiciales o comorbilidades asociadas. En el caso del AGR, se debe considerar incluso la implementación de estrategias fuera de las recomendadas en las guías(6). Para medir el control, se valoran, entre otros parámetros, la ausencia de síntomas, el ejercicio y el uso de medicación de rescate. Es conveniente indicar que las escalas que valoran el control (cuestionario CAN o ACT) tienen menos utilidad en preescolares(6).
Educación en el asma
La educación del niño y su familia es un aspecto fundamental en el manejo de la enfermedad, dado que aumenta la calidad de vida, reduce el riesgo de exacerbaciones y el coste.
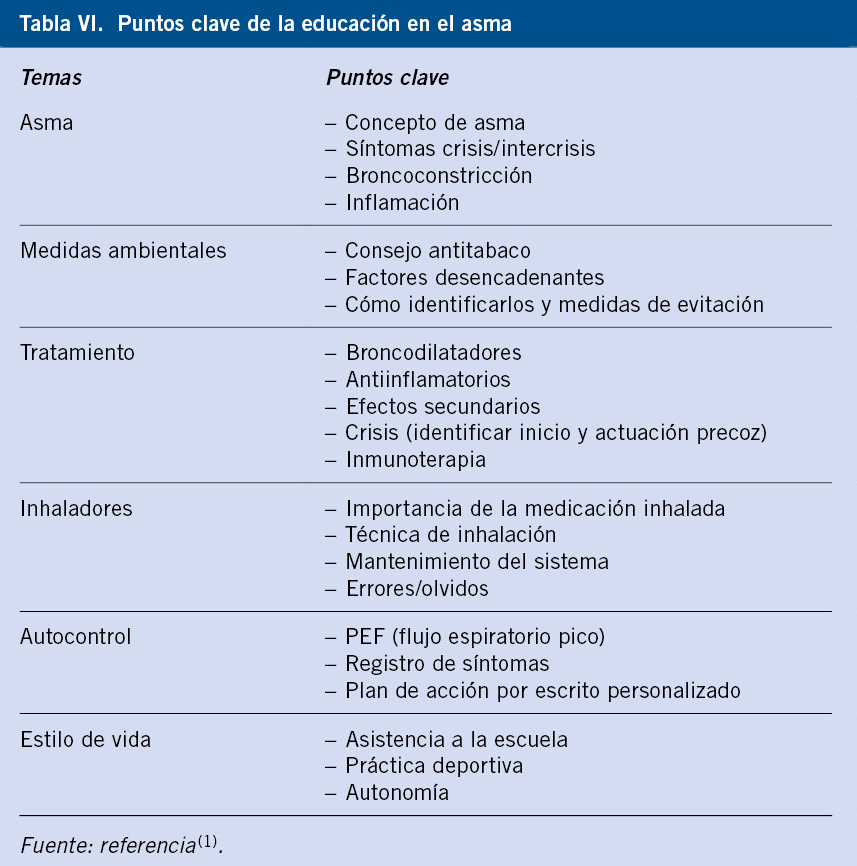
La educación en el asma proporciona conocimientos que facilitan el autocontrol, el manejo de las crisis y mejores condiciones para la práctica de deporte. Debe desarrollarse en todos los ámbitos sanitarios en los que el niño sea atendido. Se dirigirá fundamentalmente a la familia durante la primera infancia y, a partir de los 8-9 años, cuando el niño tenga la madurez suficiente, principalmente al propio paciente, con el objetivo de facilitar su autonomía y autocuidado(28). Los puntos clave de la educación se recogen en la tabla VI(1).
El pediatra de Atención Primaria y la enfermera del centro de salud, por su cercanía, accesibilidad y confianza, tienen un papel fundamental(5,12). Disponer de un pediatra accesible, que conoce el entorno sociofamiliar, hará que el centro de salud sea el escenario idóneo para dar respuesta a las necesidades educativas y de control. La intervención es más efectiva cuando está acompañada de planes de acción personalizados por escrito, que aborden el tratamiento de mantenimiento y de rescate(1), debiendo ir asociado a revisiones periódicas. Los planes de acción escritos, basados en la medición del PEF (flujo espiratorio pico), pueden utilizarse de forma individualizada, especialmente en pacientes con asma grave y baja percepción de los síntomas(29), pues de forma generalizada no aportan beneficios frente a los planes basados en la monitorización de los síntomas(30).
Función del pediatra de Atención Primaria
El pediatra de Atención Primaria es un actor fundamental, no solo en la educación sanitaria del niño y la familia del paciente asmático, sino también como prescriptor inicial de la mayoría de los tratamientos de mantenimiento. Asimismo, dada su cercanía y accesibilidad, juega un papel muy relevante en el control y seguimiento de los niños que reciben tratamiento de mantenimiento, especialmente en los escalones terapéuticos iniciales e intermedios. Por otro lado, tiene un papel protagonista en el manejo de la mayoría de las crisis asmáticas que no precisen asistencia hospitalaria, así como en la estabilización inicial de aquellas que sí lo precisen, pero se presenten en el ámbito ambulatorio.
Conflicto de intereses
No hay conflicto de interés en la elaboración del presente manuscrito ni fuente de financiación.
Bibliografía
Los asteriscos muestran el interés del artículo a juicio de los autores.
1.*** Guía Española para el Manejo del Asma 2025 (GEMA 5.4). Disponible en: https://www.gemasma.com/.
2.*** Global Initiative for Asthma. Global Strategy for Asthma Management and Prevention. 2025. Disponible en: https://ginasthma.org/.
3. Bercedo-Sanz A, Martínez-Torres A, Varela AL, Belinchón FJP, Aguinaga-Ontoso I, Díaz CG, et al. Prevalence and time trends of symptoms of allergic rhinitis and rhinoconjunctivitis in Spanish children: Global Asthma Network (GAN) study. Allergol Immunopathol (Madr). 2023; 51: 1-11. Disponible en: https://doi.org/10.15586/aei.v51i1.711.
4. Blasco Bravo AJ, Pérez-Yarza EG, Lázaro y de Mercado P, Bonillo Perales A, Díaz Vázquez CA, Moreno Galdó A. Coste del asma en Pediatría en España: un modelo de evaluación de costes basado en la prevalencia. An Pediatr (Barc). 2011; 74: 145-53.
5. Belinchón JP, Ortega Casanueva C, de Arriba Méndez S. Nuevo abordaje en el tratamiento del niño con asma. Pediatr Integral. 2021; 2: 67-75. Disponible en: https://www.pediatriaintegral.es/publicacion-2021-03/nuevo-abordaje-en-el-tratamiento-del-nino-con-asma/.
6. Torres Borrego J, Ortega Casanueva C, Tortajada-Girbés M. Tratamiento del asma pediátrica. Tratamiento de la crisis de asma. Protoc diagn ter pediatr. 2019; 2: 117-32.
7. Bekhof J, Reimink R, Brand PL. Systematic review: insufficient validation of clinical scores for the assessment of acute dyspnoea in wheezing children. Paediatr Respir Rev. 2014; 15: 98-112. Disponible en: https://doi.org/10.1016/j.prrv.2013.08.004.
8. Eggink H, Brand P, Reimink R, Bekhof J. Clinical Scores for Dyspnoea Severity in Children: A Prospective Validation Study. PLoS One. 2016; 11: e0157724. Disponible en: https://doi.org/10.1371/journal.pone.0157724.
9. Smith SR, Baty JD, Hodge D. Validation of the pulmonary score. An asthma severity score for children. Acad Emerg Med. 2002; 9: 99-104. Disponible en: https://doi.org/10.1111/j.1553-2712.2002.tb00223.x.
10.*** Paniagua Calzón N, Benito Fernández J. Diagnóstico y tratamiento de la crisis asmática en Urgencias. Protocolos Diagnósticos y Terapéuticos en Urgencias de Pediatría. Sociedad Española de Urgencias de Pediatría (SEUP) 4ª ed., 2024. Disponible en: https://seup.org/wp-content/uploads/2024/04/4_Asma_4ed.pdf.
11. Vézina K, Chauhan BF, Ducharme FM. Inhaled anticholinergics and short-acting beta(2)-agonists versus short-acting beta2-agonists alone for children with acute asthma in hospital. Cochrane Database Syst Rev. 2014; 7: CD010283. Disponible en: https://doi.org/10.1002/14651858.cd010283.pub2.
12. De Arriba Méndez S, Pellegrini Belinchón J, Ortega Casanueva. Tratamiento del niño asmático. Pedíatr Integral. 2016; 2: 94-102. Disponible en: https://www.pediatriaintegral.es/publicacion-2016-03/tratamiento-del-nino-asmatico/.
13. Brodlie M, Gupta A, Rodríguez-Martínez CE, Castro-Rodríguez JA, Ducharme FM, McKean MC. Leukotriene receptor antagonists as maintenance and intermittent therapy for episodic viral wheeze in children. Paediatr Respir Rev. 2016; 17: 57-9.
14. Castro-Rodríguez JA, Beckhaus A, Forno E. Efficacy of oral corticosteroids in the treatment of acute wheezing episodes in asthmatic preschoolers: systematic review with meta-analysis. Pediatr Pulmonol. 2016b; 51: 868-76. Disponible en: https://doi.org/10.1002/ppul.23429.
15. Hussein HR, Gupta A, Broughton S, Ruiz G, Brathwaite N, Bossley CJ. A meta-analysis of montelukast for recurrent wheeze in preschool children. Eur J Pediatr. 2017; 176: 963-9. Disponible en: https://doi.org/10.1007/s00431-017-2936-6.
16. Chauhan BF, Ben Salah R, Ducharme FM. Addition of anti-leukotriene agents to inhaled corticosteroids in children with persistent asthma. Cochrane Database of Systematic Reviews. 2013; 10: CD009585. Disponible en: https://doi.org/10.1002/14651858.cd009585.pub2.
17. Stempel DA, Szefler SJ, Pedersen S, Zeiger RS, Yeakey AM, Lee LA, et al. Safety of adding salmeterol to fluticasone propionate in children with asthma. N Engl J Med. 2016; 375: 840-9. Disponible en: https://doi.org/10.1056/nejmoa1606356.
18.*** Lemanske RF Jr, Mauger DT, Sorkness CA, Jackson DJ, Boehmer SJ, Martinez FD, et al. Step-up therapy for children with uncontrolled asthma receiving inhaled corticosteroids. N Engl J Med. 2010; 362: 975-85. Disponible en: https://doi.org/10.1056/nejmoa1001278.
19. Pitrez PM, Nanthapisal S, Castro APBM, Teli C, P G A. Managing moderate-to-severe paediatric asthma: a scoping review of the efficacy and safety of fluticasone propionate/salmeterol. BMJ Open Respir Res. 2023; 10: e001706. Disponible en: https://doi.org/10.1136/bmjresp-2023-001706.
20. Parimi M, Svedsater H, Ouratul A, Gokhale M, Gray MC, Hinds D, et al. Persistence and Adherence to ICS/LABA Drugs in UK Patients with Asthma: A Retrospective New-User Cohort Study. Adv Ther. 2020; 37: 2916-31. Disponible en: https://doi.org/10.1007/s12325-020-01344-8.
21. Soberaj DM, Weeda ER, Nguyen E, Coleman CI, White CM, Lazarus SC, et al. Association of inhaled corticosteroids and long-acting beta-agonists as controller and quick relief therapy with exacerbations and symptom control in persistent asthma: A systematic review and meta-analysis. JAMA. 2018; 319: 1485-96. Disponible en: https://doi.org/10.1001/jama.2018.2769.
22. O’Byrne PM, FitzGerald JM, Bateman ED, Barnes PJ, Zhong N, Keen C, et al. Inhaled Combined Budesonide-Formoterol as Needed in Mild Asthma. N Engl J Med. 2018; 378: 1865-76. Disponible en: https://doi.org/10.1056/nejmoa1715274.
23. Bisgaard H, Le Roux P, Bjâmer D, Dymek A, Vermeulen JH, Hultquist C. Budesonide/Formoterol Maintenance Plus Reliever Therapy. A new strategy in pediatric asthma. Chest. 2006; 130: 1733-43. Disponible en: https://doi.org/10.1378/chest.130.6.1733.
24. Bateman ED, Reddel HK, O’Byrne PM, Barnes PJ, Zhong N, Keen C, et al. As-needed budesonide-formoterol versus maintenance budesonide in mild asthma. N Engl J Med. 2018; 378: 1877-87. Disponible en: https://doi.org/10.1056/nejmoa1715275.
25. Rodrigo GJ, Neffen H. Efficacy and safety of tiotropium in school-age children with moderate-to-severe symptomatic asthma: A systematic review. Pediatr Allergy Immunol. 2017; 28: 573-8. Disponible en: https://doi.org/10.1111/pai.12759.
26. Abramson MJ, Puy RM, Weiner JM. Injection allergen immunotherapy for asthma. Cochrane Database Syst Rev. 2010; 8: CD001186. Disponible en: https://doi.org/10.1002/14651858.cd001186.pub2.
27. Kristiansen M, Dhami S, Netuveli G. Allergen immunotherapy for the prevention of allergy: A systematic review and meta-analysis. Pediatr Allergy Immunol. 2017; 28: 18-29. Disponible en: https://doi.org/10.1111/pai.12661.
28. Korta J, Valverde J, Praena M, Figuerola J, Rodríguez CR, Rueda S, et al. La educación terapéutica en el asma. An Pediatr (Barc). 2007; 66: 496-517.
29. Ohlmann A. Peak Flow versus Symptom Monitoring to Manage Childhood Asthma. Kaleidoscope. 2015; 5: 7.
30. Zemek RL, Bhogal SK, Ducharme FM. Systematic review of randomized controlled trials examining written action plans in children: what is the plan? Arch Pediatr Adolesc Med. 2008; 162: 157-63. Disponible en: https://doi.org/10.1001/archpediatrics.2007.34.
Bibliografía recomendada
– Guía Española para el Manejo del Asma 2025 (GEMA 5.4). Disponible en: https://www.gemasma.com/.
Guía de consenso nacional, que resume el tratamiento, diagnóstico y manejo en general del paciente asmático, incluyendo específicamente a la edad pediátrica.
– Global Initiative for Asthma. Global Strategy for Asthma Management and Prevention. 2025. Disponible en: https://ginasthma.org/.
Guía de consenso internacional, que establece recomendaciones de diagnóstico, seguimiento y, especialmente, tratamiento del paciente asmático, dividiendo la edad pediátrica asimismo por edades.
– Lemanske RF Jr, Mauger DT, Sorkness CA, Jackson DJ, Boehmer SJ, Martinez FD, et al. Step-up therapy for children with uncontrolled asthma receiving inhaled corticosteroids. N Engl J Med. 2010; 362: 975-85. Disponible en: https://doi.org/10.1056/nejmoa1001278.
Artículo de referencia con respecto al escalado terapéutico de los pacientes que no se controlan adecuadamente con corticoides en monoterapia, evaluando distintas opciones terapéuticas.
| Caso clínico |
|
Niño de 12 años de edad, que presenta síntomas compatibles con asma bronquial. Antecedentes familiares: madre con asma y rinitis alérgica; hermana de 8 años con dermatitis atópica. Antecedentes personales: alergia a huevo superada mediante inducción de tolerancia oral. Dermatitis atópica. Bronquiolitis VRS + a los 8 meses de vida, posteriormente sibilantes recurrentes, incluso en ausencia de procesos infecciosos. Ingreso a los 2 años por episodio disneizante en contexto de infección respiratoria viral por metaneumovirus. Enfermedad actual: recibe tratamiento con budesonida inhalada a 400 mcg diarios, a pesar de lo cual, en los últimos 6 meses ha presentado un aumento en la frecuencia y severidad de los síntomas, con 2 consultas en su centro de salud por exacerbaciones asmáticas (que precisaron corticoide oral) y 1 consulta en Urgencias (que precisó igualmente corticoide oral). Pruebas complementarias: prick test: D; Pteronyssinus: 12 mm; D. farinae: 9 mm; L. destructor: 5 mm, gramíneas, árboles, malezas, epitelio de perro, gato y hongos 0 mm. Espirometría basal: FEV1: 87 %; FVC: 95 %; FEV1/FVC: 92 %; PostB2: +15 % FEV1.
|



 Pulmonary tuberculosis
Pulmonary tuberculosis