|
| Regreso a las bases |
M. Mateos Polo
Médico Adjunto de Neonatología. Hospital Universitario de Salamanca
| Resumen
El cuidado y atención de los recién nacidos a término (sanos/enfermos), así como prematuros, han sufrido muchos cambios a lo largo de los años derivados de los avances del conocimiento científico. A medida que avanza la medicina basada en la evidencia, se afianza la importancia a la hora de crear, respetar y fomentar el vínculo madre/hijo tras el parto. Dicha unión, presenta efectos beneficiosos, tanto en la madre como el recién nacido. |
| Abstract
The care and attention of healthy and ill full-term newborns as well as of premature babies has undergone many modifications over the years derived from advance in scientific knowledge. As evidence-based medicine advances, the importance of respecting and promoting the mother-child bond after childbirth has strengthened. This union has beneficial effects on both, the mother and the newborn. |
Palabras clave: Recién nacido; Vínculo; Transición
Key words: Newborn; Mother-child bond; Transition.
Pediatr Integral 2024; XXVIII (3): 194 – 200
OBJETIVOS
• Conocer la fisiología de la adaptación neonatal al medio extrauterino.
• Saber los factores que pueden alterar la transición del recién nacido.
• En caso de transición anómala, actuar en función de los conocimientos científicos validados en la primera hora de vida.
Los primeros 60 minutos en la vida del recién nacido
Introducción
La adaptación a la secuencia de cambios que acontecen tras el nacimiento del recién nacido supone un reto para la medicina perinatal. Una transición a la vida postnatal sin complicaciones constituye un indicador de salud para la población infantil. Una vida fetal sin alteraciones, así como un periodo perinatal fisiológicamente normal, obtienen como resultado un lactante/niño sano.
El término “hora de oro” traducido del inglés “Golden hour” ha sido adoptado de la medicina de urgencias del adulto ante catástrofes(1). En ella, un adecuado manejo, basado en evidencias científicas y actuaciones protocolizadas, en la primera hora desde el accidente, disminuye la mortalidad y mejora el pronóstico a corto y largo plazo.
“Golden hour” en el periodo neonatal, engloba los primeros 60 minutos tras el nacimiento del recién nacido a término y pretérmino. El concepto “Golden hour” incluye todas aquellas intervenciones médicas basadas en la evidencia científica acerca del manejo del recién nacido a término como pretérmino, que mejoran su pronóstico a corto y largo plazo. Reynolds et al. fueron los primeros en implementar este concepto en los cuidados neonatales, demostrando el efecto beneficioso a corto y largo plazo de una actuación correcta en el momento del nacimiento(2).
Para entender la importancia de estos primeros 60 minutos, es necesario hacer un recuerdo de la fisiología que acontece en la transición del recién nacido a la vida extrauterina.
Fisiología fetal
Durante la vida intrauterina, el feto se desarrolla gracias al soporte nutricional, hemodinámico y de intercambio gaseoso que le facilita la circulación materna a través de la placenta, creciendo además en un entorno líquido y térmicamente estable. Esta situación cambia drásticamente en el momento del nacimiento, principalmente por tres fenómenos que inician una serie de cambios fisiológicos(3): 1) el inicio de la respiración espontánea (aireación pulmonar); 2) el colapso de las arterias umbilicales (ligadura del cordón umbilical); y 3) la transición térmica.
Inicio de la respiración espontánea
El pulmón fetal está lleno de líquido. Para conseguir vaciar el agua necesita un aumento de la presión transpulmonar que se produce durante el paso por el canal del parto y, sobre todo, al iniciar el llanto o respiración espontánea. Una vez que el agua abandona el alveolo, pasa al intersticio pulmonar y permanecerá allí las siguientes horas. En esta fase, existe la posibilidad de la reentrada del agua de nuevo al alveolo desde el intersticio. Esta situación es más probable en los casos de parto prematuro, de ahí la mayor incidencia de distrés respiratorio inmediato tras el parto, secundaria al colapso pulmonar(4). Este aspecto, unido al conocido déficit de surfactante del pulmón inmaduro, es la base de la suma importancia de la aplicación de presión positiva al final de la espiración (PEEP) o presión positiva continua de las vías respiratorias (CPAP) en el recién nacido prematuro para evitar el colapso pulmonar.
Cuando el agua se elimina del intersticio, la presión intersticial es negativa, así que se logra la expansión pulmonar completa en la espiración. Es en este momento donde se logra el equilibrio llamado homeostasis respiratoria(5).
Ligadura del cordón umbilical
Si pinzamos el cordón umbilical una vez iniciadas las respiraciones, se produce un aumento de las resistencias vasculares sistémicas que, junto a la disminución de las resistencias vasculares pulmonares, condiciona el cierre de los cortocircuitos fetales. El corazón izquierdo recibirá sangre de los pulmones y la bombeará al resto del organismo. De esta forma, se intentará evitar la caída del gasto cardiaco que se produce con el pinzamiento inmediato sin haber logrado la aireación pulmonar(6).
En los casos en los que el cordón se ha ligado con el pulmón no aireado, se producirá una pérdida de la precarga sanguínea izquierda junto con un aumento de las resistencias vasculares sistémicas y de la tensión arterial del feto, condicionando un aumento de la postcarga del corazón izquierdo.
Ambas situaciones son responsables de una caída del gasto cardiaco en los primeros minutos tras el pinzamiento del cordón, si no se acompaña de una adecuada aireación pulmonar(6).
Transición térmica
El recién nacido pasa de un medio líquido termoestable en su etapa fetal a un medio aéreo al nacer, lo cual favorece la pérdida de calor básicamente por mecanismos de evaporación y conducción. Se debe evitar tanto la hipotermia como la hipertermia, ya que ambos factores aumentan la morbimortalidad en el recién nacido.
Al igual que los órganos se ajustan rápidamente al enorme cambio de presión sanguínea y oxigenación, la termorregulación neonatal sustituye a la termoestabilidad intrauterina, con su inherente aumento en el consumo de oxígeno. La mejor forma de establecer normotermia y hacer una transición térmica adecuada es mediante el contacto piel con piel.
Respuesta del feto/recién nacido a una transición anómala
Existen situaciones patológicas (madre, feto, placenta) que pueden alterar la secuencia de cambios detallados previamente y comprometer la adecuada transición fetoneonatal. La hipoxia generada de dicho compromiso condiciona el mantenimiento de la vasoconstricción del lecho vascular pulmonar y la disminución del gasto cardiaco, acidosis e hipercapnia.
Los motivos que ocasionan una transición anómala son múltiples y relativamente frecuentes. A modo de resumen, los factores que pueden alterar la transición neonatal son los referidos en la tabla I(4):
Una vez conocidos dichos factores, surge la necesidad de crear intervenciones necesarias en el cuidado perinatal en esos primeros 60 minutos de vida que logran minimizar la aparición de complicaciones neonatales (Tabla II)(7-8).
A continuación, iremos desgranando, una a una, cada intervención.
Consenso antenatal/información y equipo de reanimación
Cuando se pueda, debe existir una anticipación, preparación y asignación de roles antes de una reanimación neonatal, en el recién nacido a término y pretérmino(9).
La anticipación permite obtener datos de la historia familiar/obstétrica de interés, así como una primera entrevista con la familia, sobre todo en aquellos casos de parto pretérmino. El ideal de la entrevista es que sea en ambiente de tranquilidad, con la gestante acompañada por su cónyuge/familia. La información debe ser clara, tanto del momento inicial de la reanimación como de porcentajes de morbimortalidad de nuestra unidad. Se deben aclarar dudas y preguntas. En los casos de amenaza de parto pretérmino, en los que no se produzca un parto de forma inmediata, se deben realizar entrevistas con intervalo de 7-10 días para informar de las variaciones del pronóstico. Es aconsejable ofrecer a la familia la posibilidad de conocer la unidad neonatal en la que permanecerá ingresado el recién nacido si se produce el parto prematuro.
Se recomienda la presencia de los padres en el momento de la reanimación neonatal. Cuando se pueda, se debe informar de las maniobras de reanimación que se han realizado y de su necesidad. Se ha visto beneficioso, tanto en la comprensión de la situación como en los casos de duelo por muerte perinatal.
En cuanto al equipo de reanimación, debe ser siempre de, al menos, dos reanimadores por cada recién nacido. En partos de bajo riesgo, al menos, un reanimador con conocimiento en reanimación cardiopulmonar (RCP) avanzada; en partos de riesgo, los dos reanimadores con conocimientos de RCP avanzada. Cada reanimador debe tener claro su papel dentro de la reanimación. La comunicación debe de ser constante y se ha de seguir el esquema de evaluación-intervención y respuesta a la misma de forma cíclica. Se aconseja la realización de debriefing tras la reanimación, así como listas de verificación o“check list”(10).
Retraso del pinzamiento del cordón umbilical
Fisiológicamente, se habla de pinzamiento precoz del cordón umbilical cuando el clampaje se produce habiendo aún circulación de sangre entre la placenta y el recién nacido (15 segundos del nacimiento). El pinzamiento tardío se produce cuando el clampaje del cordón se realiza una vez detenida la circulación placentaria (30 segundos-3 minutos de vida). La circulación placentaria contiene un volumen de sangre entre 110-115 ml/kg de peso fetal. De modo que un recién nacido a término sano recibiría entre 80-100 ml de sangre extra con la maniobra de pinzamiento tardío.
El pinzamiento tardío del cordón se ha asociado a varios beneficios clínicos, por lo que se recomienda desde hace años en aquellos partos no complicados(10).
En función de ello, la Guía de Reanimación Neonatal de la Sociedad Española de Neonatología (SENeo) recomienda el pinzamiento tardío del cordón (al menos, un minuto tras el nacimiento) en el recién nacido a término y prematuro de cualquier edad gestacional, nacidos vía vaginal o por cesárea, que no requieran reanimación inmediata(10).
El dilema surge en aquellos neonatos que precisan reanimación. En un intento de mantener los potenciales beneficios del pinzamiento tardío, se han descrito diversas alternativas como: inicio de ventilación con cordón íntegro, el ordeño del cordón desde la placenta al neonato sin pinzar, o el ordeño del cordón tras su pinzamiento.
En cuanto al ordeño del cordón, se asocia a oscilaciones del flujo cerebral y parece asociarse a una mayor incidencia de hemorragia intraventricular en menores de 28 semanas(10). Actualmente, NO se recomienda ninguna de esas medidas alternativas en la reanimación neonatal.
El grupo de RCP neonatal de la Sociedad Española de Neonatología (SENeo) de momento, prioriza la ventilación con presión positiva en aquellos neonatos que lo precisen, considerando la opción de estimulación y estabilización inicial con cordón integro si la situación clínica y el contexto madre/hijo lo permiten. El ordeño del cordón umbilical no se recomienda actualmente y está desaconsejado extensamente en menores de 28 semanas(10).
Prevención de hipotermia
El rango de temperatura óptima para cualquier neonato es aquel que minimiza el estrés fisiológico y el consumo metabólico. Dicha temperatura se encuentra entre 36,5ºC y 37,5ºC para recién nacidos a término y nos sirve de referencia para el recién nacido pretérmino.
La pérdida de calor es más importante en los primeros minutos de vida, puesto que nacen impregnados de líquido amniótico y unto sebáceo en un ambiente frío.
Pese a los avances en reanimación neonatal, hasta un 40-50 % de los neonatos presentan hipotermia en la primera hora de vida, lo que representa un factor de mortalidad independiente para dicha población. La hipotermia al ingreso es un fuerte predictor de mortalidad neonatal en prematuros(11).
La mejor forma de estabilizar la temperatura en el recién nacido a término o pretérmino tardío, que no necesita reanimación, es manteniendo el contacto piel con piel inmediato tras el nacimiento. Dicha medida es efectiva al estabilizar la temperatura corporal del recién nacido. Debe mantenerse de manera ininterrumpida, al menos, durante los primeros 60 minutos y aconsejable de 90-120 minutos desde el nacimiento. No se interrumpe para maniobras no prioritarias, como peso del recién nacido y/o administración de profilaxis oftálmica y hemorrágica del recién nacido.
En el recién nacido pretérmino, se describe un incremento de la mortalidad de hasta un 28 % por cada grado de temperatura inferior a la normalidad a su llegada a la Unidad de Cuidados Intensivos Neonatales(12). Después del nacimiento, existe una rápida pérdida de calor por conducción, evaporación, convención y radiación. El recién nacido prematuro es especialmente vulnerable a la pérdida de calor por los siguientes motivos:
• Carece de grasa subcutánea.
• Tiene mayor superficie corporal en relación al peso.
• Presenta un control vasomotor pobre, sobre todo en las primeras 24-48 h.
• Tiene un estrato córneo inmaduro.
Existen diferentes medidas a adoptar para prevenir la hipotermia en el recién nacido prematuro. Lo ideal es conseguir un ambiente térmico neutro y un nivel de humedad adecuado. Para evitar hipotermia del prematuro se debe mantener una temperatura en la sala de reanimación de, al menos, 26ºC y evitar corrientes de aire. Además, es necesario tener en cuenta las siguientes medidas(13):
• Calentar la cuna térmica antes del parto. Realizar la reanimación bajo fuente de calor radiante.
• Uso de envoltorio oclusivo o bolsa de polietileno para mantener la temperatura corporal.
• En lugar de secar el cuerpo del recién nacido, cubrirlo justo al nacer con la bolsa o envoltorio oclusivo de polietileno sobre la piel húmeda(13-14).
• No se debe retirar la bolsa hasta alcanzar una temperatura corporal normal (una vez introducido en la incubadora en la unidad neonatal).
• La incubadora de transporte deberá estar enchufada y caliente entre 36,5ºC y 38ºC.
Es importante evitar la hipertermia (temperatura por encima de 37,5ºC). Si sucediera, la primera medida a tomar es bajar la temperatura de la cuna de reanimación, preservando el calor de la bolsa de polietileno.
Soporte respiratorio
Ya que casi siempre que se requiere una reanimación neonatal, el origen de la parada es respiratorio, el soporte a dicho nivel es fundamental. Debe existir un adiestramiento constante en maniobras de ventilación para todas aquellas personas que trabajan en el entorno del recién nacido.
Distinguiremos entre ventilación con presión positiva y oxigenoterapia en la sala de partos.
Ventilación con presión positiva
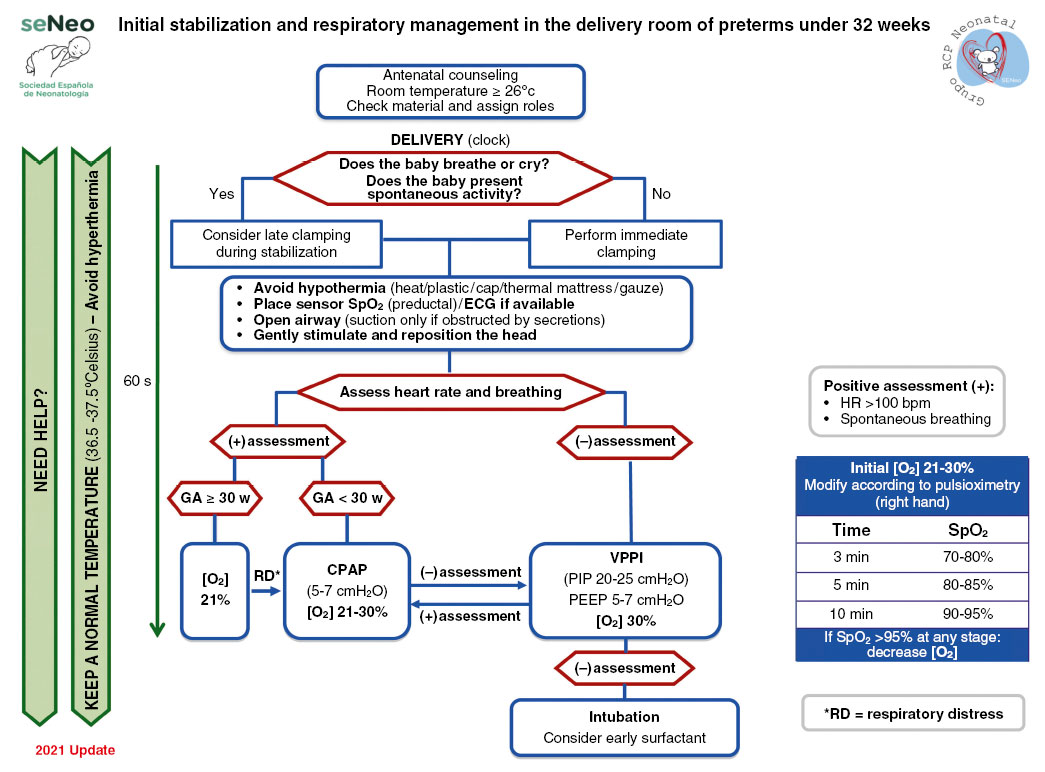
Ante un recién nacido en apnea o bradicardia en la sala de partos, es prioritario el establecimiento de una ventilación pulmonar adecuada. La guía de la Sociedad Española de Neonatología (SENeo) establece idealmente una ventilación con presión positiva con mezcla de gases calientes y humidificados, y de forma ininterrumpida durante 30 segundos(5). Se recomienda una frecuencia de 40-60 rpm con tiempos inspiratorios cortos de menos de 1 segundo, una PEEP de 5-7 cmH2O y una presión inspiratoria máxima (PIP) de 20-25 cmH2O en el recién nacido pretérmino y 25-30 cmH2O en el recién nacido a término, ajustando los parámetros lo más pronto posible según la respuesta de la frecuencia cardiaca(5). La aspiración de secreciones podría ser necesaria si no se logra una adecuada aireación. Hasta el momento, se desaconseja el uso de insuflaciones sostenidas, ya que no ha demostrado una clara evidencia en: reducción de mortalidad, displasia broncopulmonar o duración de la hospitalización, y sí un mayor riesgo de mortalidad en las primeras 48 horas(4).
Oxigenoterapia en sala de partos
En los años 90 aparecen las primeras publicaciones sobre reanimación con aire ambiente que demuestran que es tan eficaz como concentraciones de oxígeno al 100 %, además de disminuir la mortalidad y los efectos de la hiperoxia(19). En 2010 se produce un cambio en las recomendaciones a favor del uso de aire ambiente en el recién nacido (RN) mayor de 35 semanas, que se mantiene actualmente. De hecho, un reciente meta-análisis de la ILCOR (Comité Internacional de Enlace sobre Reanimación) concluye que la reanimación con FiO2 de 0,21 frente al 1 en recién nacidos por encima de las 35 semanas, se asocia a menor mortalidad sin encontrarse diferencias en la gravedad de la encefalopatía hipóxico-isquémica ni en el neurodesarrollo(14).
Paralelamente, aparecen publicaciones que comparan el uso de fracciones inspiratorias de oxígeno de 1 en grandes prematuros con FiO2 bajas sin evidenciarse ningún daño aparente; por lo que, desde el 2015, el ILCOR recomienda iniciar la reanimación en recién nacidos prematuros menores de 35 semanas con FiO2 bajas (0,21-0,3) y desaconseja FiO2 elevadas (0,65-1).
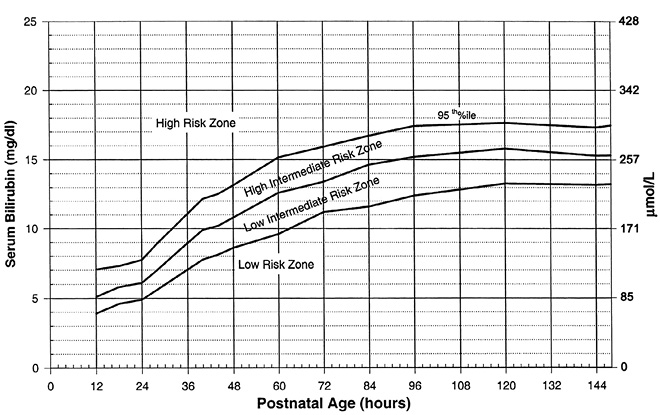
Por otro lado, se utilizará la pulsioximetría para el ajuste posterior de oxígeno para alcanzar una saturación por encima de p25 de las gráficas de Dawson, evitando saturaciones por encima de p90(15). Con la implementación del retraso del pinzamiento del cordón en 2020, un estudio elabora curvas de saturación en recién nacidos a término sanos en los que se realiza el pinzamiento tardío. Comparadas con las curvas de Dawson (pinzamiento precoz), encuentran saturaciones más altas en los primeros 5 minutos de vida(16). Aún no existe suficiente evidencia para recomendar otro tipo de gráficas de saturación diana diferentes a las curvas de Dawson, como las relacionadas con el pinzamiento tardío.
En caso de necesidad de compresiones torácicas, se recomienda aumentar FiO2 hasta 1 disminuyéndola posteriormente una vez recuperada la circulación espontánea(4).
Soporte cardiovascular
El parámetro fundamental para evaluar la respuesta a las maniobras de resucitación cardiopulmonar es la frecuencia cardiaca. La mejoría o mantenimiento de frecuencia cardiaca por encima de 100 lpm es el mejor indicador de respuesta favorable a la reanimación(4).
La forma inicial para medir dicho parámetro es el método auscultatorio(4). Se recomienda la monitorización con pulsioximetría en el recién nacido a término que precisa ventilación y en los prematuros por debajo de las 32 semanas inmediatas tras el nacimiento, durante la estabilización inicial. También, es aconsejable monitorización EEG si está disponible(4).
En aquellos casos en los que la frecuencia cardiaca se mantenga por debajo de 60 lpm, a pesar de una ventilación eficaz, estaría indicado el inicio de masaje cardiaco con frecuencia 3:1 (90 compresiones/30 ventilaciones por minuto) con independencia de la edad gestacional y siempre coordinado con la ventilación. La técnica de los dos pulgares con la mano envolviendo el tórax es la de elección. En los casos que se requieran comprensiones torácicas, se recomienda la intubación orotraqueal y aumento de FiO2 hasta 1(4).
La vía de elección para la administración de medicación es la vena umbilical. La indicación de canalización surge cuando la frecuencia cardiaca se mantiene por debajo de 60 lpm(4).
Si a pesar del masaje cardiaco no recupera frecuencia por encima de 60 lpm, estaría indicada la administración de adrenalina siempre diluida (1:10.000). La vía de elección para su administración es intravenosa, aunque también se puede administrar intratraqueal. La dosis intravenosa sería entre 0,1-0,3 ml/kg (0,01-0,03 mg/kg) de la adrenalina 1:10.000. En caso de administración intratraqueal, la dosis recomendada sería 0,5-1 ml/kg (0,05-0,1 mg/kg) de la adrenalina diluida(4).
Soporte nutricional precoz/inicio de lactancia materna/piel con piel tras el parto
Intraútero, la placenta proporciona el soporte nutricional necesario para las demandas de crecimiento fetales. Tras el nacimiento, se produce el clampaje y sección del cordón umbilical, por tanto, dichas necesidades han de ser proporcionadas de forma externa.
El inicio precoz de aporte de nutrientes es fundamental, tanto en el recién nacido a término como en el pretérmino. El objetivo fundamental es evitar el catabolismo desencadenado tras el parto. Para hablar del aspecto nutricional, distinguiremos entre el recién nacido a término y pretérmino.
Recién nacido a término
En el recién nacido a término, se prioriza el amamantamiento precoz tras el nacimiento. En aquellos casos que no precisan maniobras de reanimación cardiopulmonar, se coloca en piel con piel inmediatamente tras el parto y se permite que el recién nacido haga su primera toma de lactancia materna directa del pecho.
El método piel con piel (CPP) trata de evitar que se produzca separación entre madre e hijo tras el parto. Podemos distinguir entre contacto piel con piel (CPP) inmediato, si se realiza inmediatamente al nacimiento; o precoz, si se realiza en la primera media hora tras el parto(17).
La duración del CPP debe tener un tiempo mínimo de 60 minutos, aunque lo más recomendado es que este dure entre 90 y 120 minutos, o hasta que haya finalizado la primera toma(17).
• El método piel con piel, ofrece las siguientes ventajas(17):
– Permite una adecuada incorporación del recién nacido a su nuevo medio externo, ayudando a estabilizar la temperatura.
– Aumenta las posibilidades de éxito de la lactancia materna y mejora el vínculo afectivo.
– Favorece la colonización del recién nacido por gérmenes maternos.
Para una exitosa técnica de piel con piel es necesario seguir los siguientes pasos(17):
1. Informar a la madre durante el periodo de dilatación del contacto piel con piel y sus beneficios.
2. Mantener una temperatura adecuada en paritorio (25ºC).
3. Crear un entorno de confianza. Mantener un ambiente silencioso, con poca luz, permitir a la mujer estar acompañada y contar con el menor número de profesionales dentro del paritorio, sin entradas y salidas, manteniendo la puerta cerrada.
4. Descubrir el pecho de la madre en los últimos minutos del expulsivo.
5. Colocar al recién nacido inmediatamente después de nacer, desnudo, sobre el tórax o abdomen de la madre en contacto directo con la piel, en decúbito prono con la cabeza ladeada.
6. Secarlo, comprobando que respira, tiene buen tono y coloración. En caso de que el RN haya tenido que ser separado para su atención, se volverá a colocar en contacto piel con piel tan pronto como su estado lo permita.
7. Pinzamiento tardío del cordón umbilical.
8. Realizar el test de Apgar en contacto piel con piel sobre el pecho de la madre, así como la evaluación continua del bienestar del recién nacido.
9. Permitir el agarre espontáneo al pecho, dirigido por el RN.
10. Administración de vitamina K para la profilaxis de la enfermedad hemorrágica del RN y administración de la profilaxis oftálmica o conjuntivitis gonocócica neonatal una vez finalizada la primera toma o tras el tiempo mínimo recomendado de contacto piel con piel.
En cuanto a la instauración de la lactancia materna, todas las madres tienen derecho a recibir una información clara e imparcial que les permita tomar una decisión de cómo quieren alimentar y cuidar a sus hijos. La lactancia materna a demanda, es la mejor forma de alimentar a los niños, proporcionando grandes beneficios, tanto para la salud de la madre como del niño. Debemos explicar a la madre que la lactancia materna también ayuda al desarrollo cerebral de su hijo, le da protección inmunitaria, ayuda al establecimiento del vínculo madre-hijo, así como en la prevención de enfermedades de etapas posteriores de la vida (18).
Los profesionales sanitarios son responsables de fomentar y mantener la lactancia materna.
En las 2 primeras horas después del nacimiento, el RN está en alerta tranquila. La mayoría de RN sanos a término presentan comportamientos espontáneos de alimentación en la primera hora de vida. Por tanto, la iniciación de la lactancia materna se realizará preferentemente dentro de esa primera hora. Sin embargo, se recomienda respetar el proceso de adaptación de los RN y esperar a que sean ellos los que realicen un agarre espontáneo, lo que facilitará un agarre correcto al pecho(18).
No se sabe el tiempo máximo esperado hasta que el RN se agarre al pecho. Por ello, en RN sanos, asintomáticos y sin riesgo de hipoglucemia, se puede observar y esperar a que se agarren al pecho espontáneamente. En caso de que el RN no muestre signos de búsqueda o no encuentre el pezón de forma espontánea, antes de que finalice la primera hora, se ofrecerá ayuda a la madre con el agarre. Si a pesar de la ayuda no se consigue una primera toma, se informará a la madre sobre los signos precoces de hambre y cómo identificar signos y síntomas de alarma.
El fomento, instauración y apoyo a la familia en la lactancia materna es deber y buen hacer de todos aquellos que nos dedicamos a velar por la salud de los recién nacidos y lactantes sanos. La OMS, UNICEF y la AEP recomiendan la lactancia materna exclusiva hasta los 6 meses de vida, y complementada con otros alimentos hasta los 2 años(18).
Recién nacido pretérmino
En aquellos casos en los que la prematuridad permita el grado de madurez necesario para mantener el vínculo afectivo madre-hijo, se seguirán las mismas recomendaciones que para el recién nacido a término. Se debe prestar una atención más directa y continua durante su tiempo de estancia en paritorio. Así mismo, es frecuente que dicha población necesite un mayor apoyo por parte del personal de enfermería para lograr un correcto agarre e instauración de la lactancia materna(18).
En los casos en lo que la prematuridad implique ingreso en la Unidad de Cuidados Intensivos Neonatales, el inicio de aporte de nutrientes de forma precoz es uno de los pilares a establecer en esa primera hora de vida. Ante inestabilidad respiratoria y/o hemodinámica, es necesario asegurar aportes de glucosa de forma precoz en forma de suero glucosado, generalmente al 10 %. En casos de prematuridad inferior a 32 semanas y/o peso inferior a 1.500 gramos, el soporte nutricional se basa en la administración precoz de nutriciones parenterales estandarizadas para dicha población.
Aunque los aportes intravenosos son el pilar fundamental para evitar y/o paliar el catabolismo que se produce tras el nacimiento con altas necesidades metabólicas por parte del pretérmino, no debemos olvidar la administración de calostro materno precoz, incluso aplicado en mejillas de aquellos recién nacidos extremadamente pretérminos.
El calostro materno, la leche de los primeros días, es un alimento rico en proteínas, minerales y vitaminas, contiene elementos (leucocitos y anticuerpos) que protegen al niño frente a infecciones y alergias. Tiene efecto laxante, ayuda a expulsar el meconio y a prevenir la ictericia. Favorece el crecimiento, acelera la maduración del intestino y previene la alergia y la intolerancia a los alimentos(18)
Prevención de hipoglucemia
El recién nacido en riesgo de hipoglucemia (prematuro, con retraso de crecimiento intrauterino, bajo peso, hijo de madre con diabetes gestacional o pregestacional, asfixia perinatal, postérmino…) debe recibir aporte externo de glucosa en la primera hora de vida. El objetivo es mantener un valor de glucemia entre 50-100 mg/dl de manera constante para evitar complicaciones derivadas de la hipoglucemia. El manejo inicial de la hipoglucemia incluye el aporte precoz de calostro (18)/fórmula artificial (bajo deseo materno) o infusión de glucosa intravenosa en casos de persistencia de hipoglucemia a pesar de aporte oral o imposibilidad de aporte oral por patología concomitante.
Prevención de infecciones
Un pilar básico en la atención del recién nacido es la prevención de infecciones. En este sentido, nos vamos a centrar en las medidas a tomar en esos primeros 60 minutos de vida en el recién nacido prematuro.
La sepsis neonatal y la prematuridad son las dos causas más comunes de morbimortalidad neonatal. Las actuaciones en este sentido van dirigidas a la prevención primaria de infecciones nosocomiales derivadas de su estancia en unidades de cuidados intensivos neonatales.
El recién nacido prematuro debe ser manejado con estrictas medidas de asepsia desde su nacimiento, dadas sus características de inmunodeprimido. Todos aquellos procedimientos invasivos, como canalización umbilical, inserción periférica de catéter central, instilación de surfactante pulmonar, antibióticos y otras medicaciones intravenosas, deben hacerse bajo una estricta asepsia.
Al llegar a la unidad, hay que extraer un hemocultivo estéril y, valorar, al prescribir antibioterapia, los factores de riesgo perinatales de infección vertical (prematuridad, rotura prematura de membrana en pretérmino, fiebre materna y/o signos de corioamnionitis subclínica). En casos sintomáticos, es precisa la administración precoz de antibioterapia. Ante ausencia de sintomatología, pero con factores de riesgo, la medida a tomar es el inicio precoz de antibioterapia, así como la retirada precoz (36-48 horas) en casos de hemocultivo negativo(19).
Hasta ahora no existe ningún marcador sanguíneo ideal ni para instalar ni controlar infecciones en el recién nacido. La prueba “Gold Estándar” para la confirmación de la sepsis es el hemocultivo. La mejor manera de monitorizar al recién nacido es la vigilancia clínica estrecha(19).
Pruebas complementarias
El recién nacido prematuro se someterá a la mayoría de las pruebas complementarias en su primera hora de vida. Dentro de las pruebas se encuentra: realización de hemograma, bioquímica básica, gasometría, hemocultivo, cultivos de superficie y radiografía de tórax. Las últimas recomendaciones se inclinan hacia la individualización de dichas pruebas, así como la valoración de su rentabilidad y la necesidad de su precocidad. En la medida de lo posible, retrasar la realización de pruebas sanguíneas hasta la estabilización respiratoria y térmica.
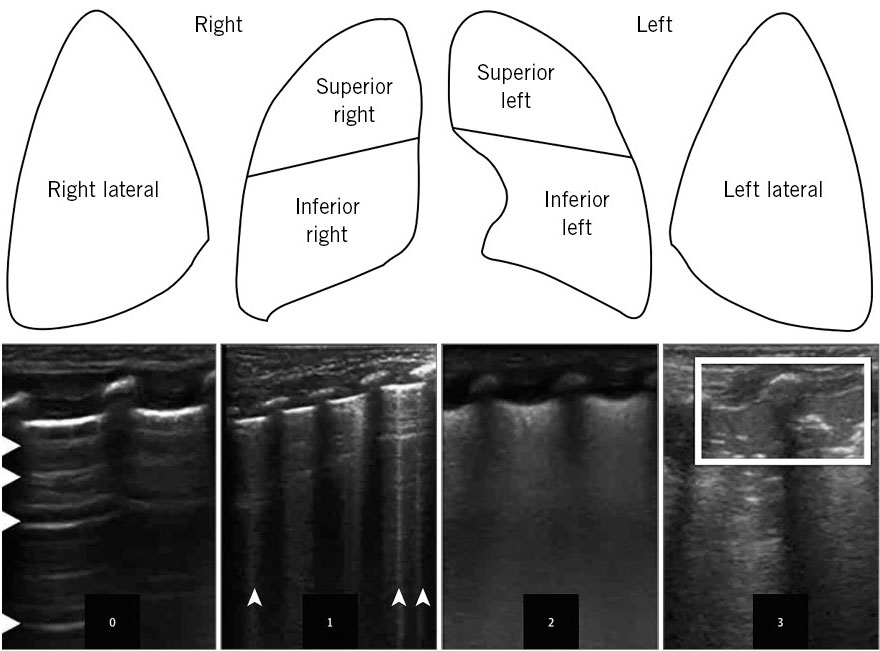
En cuanto a las pruebas de imagen, la tendencia se dirige a la ecografía pulmonar a pie de incubadora. La ecografía es una técnica inocua, fácil de realizar y accesible. Permite conocer los patrones pulmonares de normalidad y diagnosticar con rapidez la presencia de complicaciones importantes, como el neumotórax. La ecografía identifica patologías pulmonares, como el pulmón húmedo, la bronconeumonía, incluso es posible que ayude a la hora de decidir la necesidad de administración de surfactante.
Monitorización de constantes
El registro continuo de constantes cardiorrespiratorias es fundamental dentro de la “Golden hour”. Dentro del registro se debe incluir como mínimo: frecuencia cardiaca, frecuencia respiratoria, electrocardiograma, tensión arterial no invasiva y saturación de oxígeno. En casos de encefalopatía hipóxico-isquémica, se debe colocar el monitor de electroencefalograma integrado por amplitud (aEEG). La monitorización de saturación regional de oxígeno tiene utilidad en aquellos casos en los que exista compromiso de aporte de oxígeno a los órganos. Por ejemplo, casos de asfixia perinatal, cirugía cardiaca, hipotensión, enterocolitis…
Límites de viabilidad y comunicación con la familia
En los últimos años, la literatura refleja un aumento de la viabilidad de los prematuros más extremos. Esta tendencia es más acentuada en aquellos de menor edad gestacional (22-23 semanas), dado el cambio hacia una actitud más proactiva en este grupo en algunos países, como Reino Unido, EE.UU., Australia y Suecia. No parece describirse una clara mejoría en el pronóstico a largo plazo en esta población.
Las recomendaciones de la Sociedad Española de Neonatología abogan por un manejo proactivo a partir de las 24 semanas y cuidados paliativos hasta la 22+6/7. Los recién nacidos en la franja entre 23-23+6/7, considerada como zona gris, y la decisión de actuación activa o no, se debe basar en una deliberación conjunta del equipo médico y la familia.
Hipotermia terapéutica en casos de asfixia perinatal
La asfixia perinatal ha de ser sospechada en cualquier neonato con antecedente de estado fetal no tranquilizador, evento centinela o distocia de parto que, al nacimiento, precisa: reanimación avanzada, test de Apgar inferior o igual a 5 a los 5 minutos y/o pH de cordón inferior o igual a 7, y déficit de bases superior a 16(20).
La encefalopatía hipóxico-isquémica es el término que señala que el neonato presenta una alteración funcional del sistema nervioso central atribuida a una agresión hipóxico-isquémica.
La hipotermia terapéutica inducida está reconocida como medida de tratamiento eficaz, dentro de las primeras 6 horas de vida, en casos de encefalopatía hipóxico-isquémica moderada-grave. Existen escalas de evaluación y graduación de la gravedad de la encefalopatía hipóxico-isquémica. En nuestro entorno, la más utilizada es la Escala García-Alix(20).
La hipotermia inducida moderada (33,5ºC) durante 72 horas es la única intervención eficaz para disminuir secuelas en casos de encefalopatía hipóxico-isquémica moderada-grave(20).
La edad gestacional mínima en nuestro medio para la inclusión en la hipotermia son las 35 semanas. En casos seleccionados, se puede disminuir el límite hasta las 34 semanas.
Conclusiones
• La transición del feto a la vida extrauterina supone un reto para la medicina perinatal.
• Lo esperado es que dicho proceso suceda de manera natural sin necesidad de intervención externa por nuestra parte.
• Es necesario conocer la fisiología de la transición para entender el porqué de las posibles alteraciones.
• Existen numerosos factores que pueden alterar la transición.
• Actualmente, tenemos el conocimiento científico necesario dirigido a actuar en los primeros 60 minutos de vida del recién nacido, cuyo fin es mejorar el pronóstico a corto, medio y largo plazo, tanto del bebé como de su familia.
Conflicto de intereses
No hay conflicto de interés en la elaboración del manuscrito. Declaración de intereses: ninguno.
Bibliografía
1. Lerner EB, Moscati RM. The golden hour: scientific fact or medical “urban legend”? Acad Emerg Med Off J Soc Acad Emerg Med. 2001; 8: 758-60.
2. Reynolds RD, Pilcher J, Ring A, Johnson R, McKinley P. The Golden Hour: care of the LBW infant during the first hour of life one unit’s experience. Neonatal Netw NN. 2009; 28: 211-9.
3. Hooper SB, Kitchen MJ, Polglase GR. The physiology of neonatal resuscitation. Curr Opin pediatr. 2018; 30: 187-91.
4. Manual de reanimación neonatal, Sociedad Española de Neonatología. 4ª ed. Ergon; 2017. p. 272.
5. Hooper SB, Pas AB, Kitchen MJ. Respiratory transition in the newborn: a three-phase process. Arch Dis Child Fetal Neonatal. 2016; 101: 266-71.
6. Knol R, Brouwer E, Van der Akker T, DeKoninck P, van Geloven N, Polglase GR, et al. Physiological-based cord clamping in very preterm infants. Randomised controled trial of effectiveness of stabilisation. Resuscitation. 2020; 147: 26-33.
7. Sharma D. Golden 60 minutes of newborn’s life: Part 1: Preterm neonate. J Matern Fetal Neonatal Med. 2017; 30: 2716-27.
8. Sharma D, Sharma P, Shastri S. Golden 60 minutes of newborn’s life: Part 2: Term neonate. J Matern Fetal Neonatal Med. 2017; 30: 2728-33.
9. Brett J, Staniszewska S, Newburn M, Jones N, Taylor L. A systematic mapping review of effective interventions for communicating with, supporting and providing information to parents of preterm infants. BMJ Open. 2011; 1: e000023.
10. Zeballos Sarrato G, Ávila Álvarez A, Escrig Fernández R, Izquierdo Renau M, Ruiz Campillo CW, Gómez Robles C, et al; Grupo de Reanimación Neonatal de la Sociedad Española de Neonatología (GRN-SENeo). Guía española de estabilización y reanimación neonatal 2021. Análisis, adaptación y consenso sobre las recomendaciones internacionales. Anales de pediatría. 2022; 96: 145.e1-e9.
11. Laptook AR, Salhab W, Bhaskar B. Neonatal Research Network. Admission temperature of low birth weight infants: predictors and associated morbidities. Pediatrics. 2007; 119: e643-9.
12. Chang H-Y, Sung Y-H, Wang S-M, Lung H-L, Chang J-H, Hsu C-H, et al. Short- and Long-Term Outcomes in Very Low Birth Weight Infants with Admission Hypothermia. PloS One. 2015; 10: e0131976.
13. Oatley HK, Blencowe H, Lawn JE. The effect of coverings, including plastic bags and wraps, on mortality and morbidity in preterm and full-term neonates. J Perinatol. 2016; 36: S83-9.
14. Welsford M, Nishiyama C, Shortt C, Isayama T, Dawson JA, Weiner G, et al. Room Air for Initiating Term Newborn Resuscitation: A Systematic Review with Metaanalysis. Pediatrics. 2019; 143: e20181825.
15. Perlman JM, Wyllie J, Kattwinkel J, Atkins DL, Chameides L, Goldsmith JP, et al. Part 11: Neonatal resuscitation: 2010 International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science with Treatment Recommendations. Circulation. 2010; 122: S516-38.
16. Padilla Sánchez C, Baixauli Alacreu S, Cañada Martínez AJ, Solaz García Á, Alemany Anchel MJ, Vento M. Delayed vs Immediate Cord Clamping Changes Oxygen Saturation and Heart Rate Patterns in the First Minutes after Birth. J Pediatr. 2020; 227: e1.149-56.
17. WHO recommendations for care of the preterm or low-birth-weight infant. Guideline. 2022. Disponible en: https://www.who.int/publications/i/item/9789240058262.
18. Comité de Lactancia Materna de la Asociación Española de Pediatría. Recomendaciones sobre lactancia materna. 2012. Disponible en: https://www.aeped.es/sites/default/files/201202-recomendaciones-lactancia-materna.pdf.
19. Brady MT, Polin RA. Prevention and management of infants with suspected or proven neonatal sepsis. Pediatrics. 2013; 132: 166-8.
20. Blanco D, García-Alix A, Valverde E, Tenorio V, Vento M, Cabañas F. Neuroprotección con hipotermia en el recién nacido con encefalopatía hipóxico-isquémica. Guía de estándares para su aplicación clínica. Anales de Pediatría. 2011; 75: 341.e1-e20.





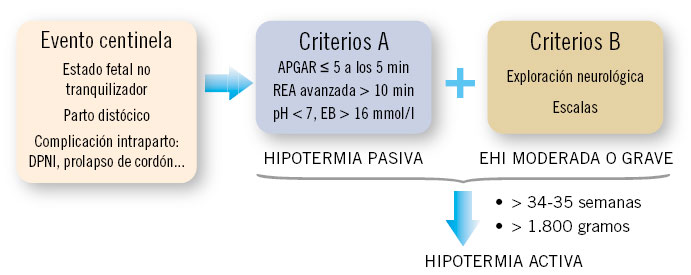









































































 La plagiocefalia posicional es una deformidad de la parte posterior del cráneo, que se aplana de forma asimétrica, es maleable y raramente está presente al nacimiento
La plagiocefalia posicional es una deformidad de la parte posterior del cráneo, que se aplana de forma asimétrica, es maleable y raramente está presente al nacimiento  Se produce como consecuencia de una fuerza mecánica prolongada aplicada sobre la cabeza, con un pico de incidencia entre los 3 y 4 meses de edad
Se produce como consecuencia de una fuerza mecánica prolongada aplicada sobre la cabeza, con un pico de incidencia entre los 3 y 4 meses de edad  Su prevalencia, difícil de determinar, ha aumentado en las últimas décadas con la recomendación del decúbito súbito como posición preferida para el sueño de los lactantes
Su prevalencia, difícil de determinar, ha aumentado en las últimas décadas con la recomendación del decúbito súbito como posición preferida para el sueño de los lactantes  Los factores de riesgo más frecuentes son: sexo masculino, ser primogénito, prematuridad, tortícolis congénita, dormir en supino y escasez de tiempo en prono (“tummy time”)
Los factores de riesgo más frecuentes son: sexo masculino, ser primogénito, prematuridad, tortícolis congénita, dormir en supino y escasez de tiempo en prono (“tummy time”)  Aunque no se puede concluir, con la evidencia científica existente en el momento actual, si tiene o no impacto en el neurodesarrollo, sí lo tiene a nivel estético y psicosocial
Aunque no se puede concluir, con la evidencia científica existente en el momento actual, si tiene o no impacto en el neurodesarrollo, sí lo tiene a nivel estético y psicosocial  El diagnóstico es clínico. La cabeza tiene forma de paralelogramo, ya que la oreja ipsilateral al lado que se aplana se desplaza anteriormente y se desarrolla una prominencia occipital contralateral
El diagnóstico es clínico. La cabeza tiene forma de paralelogramo, ya que la oreja ipsilateral al lado que se aplana se desplaza anteriormente y se desarrolla una prominencia occipital contralateral  La gravedad se puede medir mediante la diferencia diagonal transcraneal: grave, >12 mm; moderada, 10-12 mm; y leve, 3-10 mm
La gravedad se puede medir mediante la diferencia diagonal transcraneal: grave, >12 mm; moderada, 10-12 mm; y leve, 3-10 mm  La terapia de reposicionamiento consiste en cambiar la posición del bebé, de manera que rote la cabeza hacia el lado contrario de la parte aplanada cuando mire a lo que le pueda llamar la atención y favorecer el prono mientras esté despierto
La terapia de reposicionamiento consiste en cambiar la posición del bebé, de manera que rote la cabeza hacia el lado contrario de la parte aplanada cuando mire a lo que le pueda llamar la atención y favorecer el prono mientras esté despierto  Además, desde Atención Primaria, para combatir la tortícolis congénita, frecuentemente presente en cierto grado, se recomiendan ejercicios de estiramiento del cuello (“mentón a hombro” u “oreja a hombro”) para que realicen los padres y/o un fisioterapeuta
Además, desde Atención Primaria, para combatir la tortícolis congénita, frecuentemente presente en cierto grado, se recomiendan ejercicios de estiramiento del cuello (“mentón a hombro” u “oreja a hombro”) para que realicen los padres y/o un fisioterapeuta  Son criterios de derivación al especialista las formas graves y los mayores de 4 meses con formas leves/moderadas con empeoramiento a pesar de reposicionamiento y fisioterapia
Son criterios de derivación al especialista las formas graves y los mayores de 4 meses con formas leves/moderadas con empeoramiento a pesar de reposicionamiento y fisioterapia