|
| Temas de FC |
M. González-Valcárcel Espinosa*, R.C. Raynero Mellado*, S.M. Caballero Martín**
*Hospital Virgen de la Salud. Complejo Hospitalario Universitario de Toledo. **Hospital General Universitario Gregorio Marañón. Madrid
| Resumen
La hiperbilirrubinemia constituye uno de los diagnósticos más frecuentes en el período neonatal, agrupando un amplio número de etiologías, desde causas banales hasta motivos de consulta graves. La valoración visual de la coloración del recién nacido ha demostrado no ser eficaz a la hora de inferir la cifra de bilirrubina y, por tanto, la indicación del tratamiento; siendo importante, por ello, la cuantificación de esta por métodos cutáneos o séricos. La indicación terapéutica se realizará en función del resultado obtenido y las tablas de referencia ajustadas a la edad gestacional y días de vida. La fototerapia en espectro azul-verde (luz especial azul 425-475 nanómetros) es el tratamiento de elección para estos pacientes que, solo en determinados casos de cifras elevadas o de etiologías hemolíticas con ascenso rápido de bilirrubina, pueden requerir técnica invasiva de exanguinotransfusión. |
| Abstract
Hyperbilirubinemia is one of the most frequent diagnoses in the neonatal period; grouping a large number of etiologies, ranging from banal causes to serious reasons for consultation. Visual evaluation of the skin color of the newborn has proved to be ineffective when inferring the bilirubin level and therefore the indication of treatment. Hence the importance of quantifying it by cutaneous or serum methods. The therapeutic indication will be made based on the result obtained and the reference tables adjusted to the gestational age and days of life. Phototherapy in the blue-green spectrum (special blue light 425-475 nanometers) is the treatment of choice for these patients. An invasive exchange transfusion technique may only be necessary in certain cases of high bilirubin levels or hemolytic etiologies with rapid bilirubin rise. |
Palabras clave: Hiperbilirrubinemia; Fototerapia; Exanguinotransfusión; Ictericia neonatal.
Key words: Hyperbilirubinemia; Phototherapy; Exchange transfusion; Neonatal jaundice.
Pediatr Integral 2019; XXIII (3): 147 – 153
Ictericia neonatal
Definición
La ictericia se define como coloración amarillenta cutánea y aparece con motivos principalmente fisiológicos en un alto porcentaje de recién nacidos.
Se define la ictericia como: la coloración amarillenta de piel y mucosas por depósito a ese nivel de bilirrubina (Bb). Entre el 25-50% de todos los recién nacidos a término y un mayor porcentaje de prematuros desarrollan ictericia relevante desde el punto de vista clínico, alcanzando el pico máximo a las 48-72 horas en nacidos a término y a los 4-5 días en los pretérminos(1,2).
La elevación de la Bb se considera fisiológica en la mayor parte de los recién nacidos. Cifras máximas de Bb no conjugada de 12 mg/dl en recién nacidos a término y de 15 mg/dl en prematuros, podrían considerarse dentro de los límites no asociados a patología específica del metabolismo de la Bb(3,4).
Se considera ictericia patológica aquella que cumple los siguientes criterios(5):
• Aparece en las primeras 24 horas de vida.
• La cifra de Bb aumenta más de 0,5 mg/dL/hora.
• Cursa con Bb directa mayor de 2 mg/dL.
• Se eleva por encima del valor descrito con anterioridad (recién nacido a término [RNT] 12 mg/dl y recién nacido pretérmino [RNPT] 15 mg/dl).
Recuerdo fisiopatológico
En el ciclo del metabolismo de la Bb juega un papel importante el grupo hemo procedente de la degradación de los glóbulos rojos y el papel hepático en la conjugación y excreción de la Bb.
El porcentaje mayor de Bb proviene de la degradación del grupo hemo (80%). La Bb circula en la sangre como fracción indirecta/no conjugada (insoluble), libre o unida a albúmina hasta su llegada al hígado, donde sufre un proceso de conjugación a Bb directa/conjugada (soluble), siendo así captada por los lisosomas y el aparato de Golgi y excretada al intestino delgado desde la vesícula biliar. Las bacterias intestinales juegan un importante papel en la transformación a urobilinógeno y estercobilinógeno, modo en el cual se excreta en heces. Parte de la Bb vuelve al hígado mediante recirculación enterohepática(3,5,6) (Fig. 1).
Figura 1. Ciclo de la degradación del grupo hemo.
En el período neonatal, existen características específicas que alteran el normal metabolismo de la Bb. Existe: un mayor volumen de hematíes con menor vida media; una menor concentración de albúmina con menor afinidad por la Bb; un menor nivel de enzimas encargadas de la conjugación; y una ausencia de bacterias intestinales con menor conversión a urobilinoides. Todo ello hace más difícil la excreción de Bb(3,7).
Clasificación etiológica
La clasificación etiológica de la ictericia se divide en dos grandes causas, que dependen de si se encuentra elevada la fracción indirecta o directa de la Bb.
Aumento de bilirrubina indirecta(5,7)
• Fisiológica.
• Por aumento de producción de Bb: causas hemolíticas o hematomas.
- Con test de Coombs directo (CD) positivo (anticuerpos maternos sobre células del niño): isoinmunización (Rh, ABO, antiKell, antiDuffy y otros antígenos).
- Con test de CD negativo: déficit de enzimas eritrocitarias (déficit de glucosa 6 fosfato deshidrogenasa), alteraciones morfológicas de los hematíes (esferocitosis, eliptocitosis…) y hemoglobinopatías (talasemias).
- Reabsorción de sangre extravascular: cefalohematoma, hematoma subdural e ingesta de sangre materna en el momento del parto.
- Policitemia por clampaje tardío del cordón, transfusión feto-fetal y transfusión materno-fetal.
• Por alteración en la conjugación hepática de la Bb:
- Alteraciones hereditarias en el metabolismo de la Bb: síndrome de Crigler-Najjar I y II.
- Hiperbilirrubinemia neonatal familiar transitoria (síndrome de Lucey-Driscoll).
- Síndrome de Gilbert (existe también una alteración de la captación hepática).
- Estenosis pilórica.
- Hipotiroidismo y prematuridad.
• Por alteración en la circulación enterohepática de la Bb:
- Ictericia por lactancia materna en recién nacido bien hidratado: hiperbilirrubinemia de predominio indirecto y benigna, que se inicia en el 3-5º día de vida y puede ser prolongada (hasta 12 semanas).
- Ictericia de inicio precoz por problemas con la lactancia materna: inicio en la 1ª semana de vida a causa de hipogalactia o mala técnica de lactancia.
Aumento de bilirrubina directa: colestasis(5,8)
Bb directa mayor de 2 mg/dl y/o mayor del 20% de la Bb total:
• Infecciones: víricas (especial mención citomegalovirus) y bacterianas (sepsis, infección urinaria). Recordar infecciones connatales.
• Enfermedad biliar extrahepática: atresia biliar extrahepática y quiste de colédoco.
• Enfermedad biliar intrahepática: pobreza de conductos biliares intrahepáticos (síndrome Alagille y formas no sindrómicas) y bilis espesa.
• Enfermedad hepatocelular: enfermedades metabólicas y genéticas (déficit de alfa-1-antitripsina, fibrosis quística, hipotiroidismo, galactosemia, síndrome de Zellweger, enfermedades de depósito, Dubin-Johson y síndrome de Rotor).
• Iatrogénica: colestasis secundaria a nutrición parenteral (NPT) prolongada y antibióticos (ceftriaxona).
• Idiopática: hepatitis neonatal.
• Miscelánea: shock o hipoxia (infarto hepático).
Historia clínica y exploración física
La realización de una historia clínica detallada y una exploración física completa nos ayudará a descartar el origen no fisiológico de la ictericia.
Debemos realizar una exhaustiva historia clínica que deberá incluir(3,5,9):
• Antecedentes familiares de ictericia, anemia, esplenectomía o patología hepatobiliar de inicio precoz.
• Origen, raza y etnia de los familiares por el aumento fisiológico de Bb en grupos étnicos, como los indios americanos y asiáticos.
• Ictericia precoz en hermanos del paciente afecto o anemia grave sugerente de incompatibilidad de grupo con la madre.
• Valoración del embarazo, para descartar síntomas de infección connatal, así como el registro del uso de fármacos durante la gestación que pudieran interferir en la unión de la albúmina con la Bb (sulfonamidas).
• Valoración completa del momento del parto, para valorar posible distocia que asocie hemorragia o hematomas en el recién nacido.
• Valoración completa de la lactancia, pérdida de peso, número de deposiciones y su coloración, con el objeto de detectar de forma precoz una escasa ingesta.
• Como en cualquier otra patología, en la ictericia, es preciso una exploración completa y sistemática.
• La valoración de la coloración cutánea no resulta un marcador objetivo de la cifra real de Bb, no siendo útil para definir su gravedad.
• Valorar signos de deshidratación sugestivos de hipogalactia, que pudieran condicionar la aparición de hiperbilirrubinemia en el recién nacido.
• Descartar sintomatología de afectación del estado general o signos clínicos de infección/sepsis.
• Valorar los rasgos fenotípicos de los pacientes, debido a su alteración en algunos cuadros sindrómicos, citados previamente.
• Descartar la presencia en la exploración de hepatoesplenomegalia, sugestiva de patología concomitante: infecciones, hemólisis…
• Junto a la exploración física de los pacientes, es preciso valorar la coloración de las heces (acolia) y de la orina (coluria) que pudieran existir en aquellos pacientes con colestasis.
• Valorar signos de sangrado, desde petequias hasta grandes cefalohematomas, que puedan ser causantes de la hiperbilirrubinemia.
• Existen dos cuadros clínicos de importante gravedad, debidos a lesión neuronal secundaria al depósito de Bb que afecta especialmente: a los ganglios de la base (núcleo pálido), núcleos de pares craneales, núcleos cerebelosos, hipocampo y neuronas del asta anterior de la médula. No existe un nivel de Bb exacto que condicione la aparición de estas patologías, aunque cifras superiores a 25-27 mg/dl tienen mayor riesgo. La presencia de algunos factores concomitantes puede potenciar el efecto tóxico de la Bb: acidosis, hipoxia, convulsiones, edad gestacional y postnatal, velocidad de incremento sérico de Bb, concentración sérica de albúmina…
- Encefalopatía bilirrubínica aguda: 1) fase precoz, con hipotonía, letargia y mala succión; 2) fase intermedia, con estupor, irritabilidad e hipertonía (opistótonos e hiperextensión del cuello; 3) fase avanzada (daños irreversibles): opistótonos e hiperextensión del cuello más llamativa, llanto agudo, apnea, fiebre, coma, convulsiones y muerte.
- Kernícterus o forma crónica (depósito patológico de Bb en el cerebro): parálisis cerebral atetoide, disfunción auditiva, displasia ónico-dental, parálisis de la mirada hacia arriba y, con menor frecuencia, retraso intelectual. No siempre aparece precedida de la fase aguda.
Exploraciones complementarias
La cuantificación de cifras de Bb y sus fracciones directa e indirecta es el escalón inicial en los estudios complementarios del neonato con ictericia. La necesidad de otros estudios complementarios dependerá de la orientación diagnóstica de los pacientes.
• Herramientas utilizadas tradicionalmente, basadas en la valoración visual del color, como los icterómetros, han quedado en desuso por su escasa correlación con la cifra real de Bb en sangre.
• Bilirrubinómetros transcutáneos: son baratos y útiles para screening de los recién nacidos que precisan control analítico con Bb sérica menor de 14,6 mg/dL. Su medición no es valorable en los recién nacidos menores de 35 semanas y se ve afectada por la raza y el peso al nacimiento. No son útiles cuando el paciente se encuentra con fototerapia(9,10).
• Exámenes de laboratorio(11):
1. Cifra de Bb total y fracciones indirecta y directa.
2. Ante la sospecha de anemización que pudiera sugerir hemólisis: grupo sanguíneo, Rh, test de Coombs directo; hemograma completo con recuento de leucocitos, con hemoglobina y hematocrito; índices de eritropoyesis: reticulocitos (mayor de 6% en isoinmunización Rh) y número de hematíes nucleados por 100 leucocitos (mayor de 10 en isoinmunización Rh); extensión de sangre periférica y morfología del hematíe (anisocitosis y policromatofilia en enfermedad hemolítica grave); estudio de déficit de glucosa 6 fosfato deshidrogenasa (si es varón y raza de riesgo: asiática o mediterránea y/o ictericia de inicio tardío); iones, albúmina y proteínas totales; y carboxihemoglobina (COHb): buena correlación con la Bb sérica y evolución clínica por formación equimolar de COHb y Bb en el catabolismo del hemo. Tienen mayor necesidad de exanguinotransfusión, mayor incidencia de Kernícterus y mayor mortalidad si la COHb es mayor de 1,4%.
3. Si aparecen signos clínicos de letargia, apnea, inestabilidad térmica o mala succión, debe investigarse la presencia de enfermedad subyacente: vigilar signos que pudieran indicar sepsis clínica.
4. Predominio de Bb directa o ictericia que se prolonga más de 2 semanas, siendo los signos clínicos más frecuentemente asociados: coluria y acolia o hipocolia:
- Descartar causas metabólicas: estudios hepáticos (GOT-GPT-GGT-FA); estudio de coagulación; proteínas totales; déficit de alfa-1-antitripsina; estudio tiroideo (T3, T4, TSH); despistaje de metabolopatías (hipotiroidismo, galactosemia); sustancias reductoras de glucosa en orina (galactosemia); y aminoácidos en sangre y orina, y ácido pipecólico en orina (enfermedad de depósito peroxisomal o síndrome de Zellweger).
- Descartar causas infecciosas. Serología para: herpes, rubéola, toxoplasma, sífilis, hepatitis B y C, y echovirus; recoger orina para: CMV (rápido y menos falsos positivos y negativos); orina para: sedimento y cultivo (infección urinaria) y hemocultivo.
• Examen del color de las heces (> 3 deposiciones acólicas consecutivas) y coluria.
• Pruebas radiológicas: ante sospecha de obstrucción de vía biliar: colestasis.
1. Ecografía abdominal (hígado y sistema biliar).
2. Gammagrafía con radioisótopos: el ácido iminodiacético sustituido-Tecnecio-99 (HIDA) es captado por los hepatocitos y excretado en la bilis al intestino (permite diferenciar colestasis intrahepática de una obstrucción extrahepática). La captación es escasa en hepatopatías parenquimatosas, como la hepatitis neonatal, apreciándose excreción hacia la bilis y el intestino.
3. Colangiografía: visualización directa del árbol biliar intra y extrahepático utilizando un material radiopaco. Evalúa: causa, localización o extensión de una obstrucción biliar.
4. Biopsia hepática percutánea (corregir previamente la coagulopatía si existe, con plasma fresco congelado y vitamina K).
Tratamiento
La existencia de nomogramas de estratificación del riesgo de desarrollar ictericia patológica y de nomogramas de indicación terapéutica, es esencial en la elección y control de estos pacientes.
Vigilancia de pacientes de riesgo
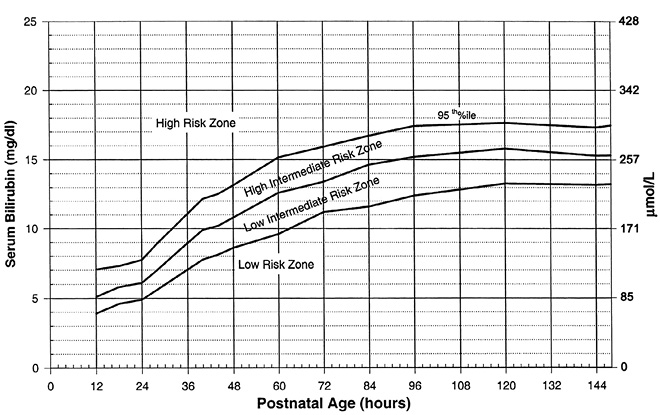
En el año 2004, la Academia Americana de Pediatría establece nomogramas predictivos de bilirrubinemia basado en la Bb sérica según las horas de vida en los recién nacidos ≥ 35 semanas de edad gestacional. Se define así el riesgo de presentar posteriormente hiperbilirrubinemia significativa en 3 niveles: riesgo alto (≥ percentil 95), riesgo intermedio (percentil 40-95) y riesgo bajo (< percentil 40). Hay que tener en cuenta que no describe la evolución natural de la hiperbilirrubinemia neonatal a partir de las 48-72 horas de vida. Precisarán control los pacientes que al alta tienen una cifra de Bb sérica ≥ percentil 95 (Fig. 2).
Figura 2. Nomograma de riesgo de hiperbilirrubinemia para RN ≥35 semanas de edad gestacional, según valores de Bb sérica específicos de cada hora (según Guía Práctica Clínica de la Academia Americana de Pediatría, Pediatrics, 2004).
El nomograma, junto con los factores de riesgo más frecuentemente asociados a hiperbilirrubinemia, puede ayudar en la valoración de cada caso. Dentro de los factores de riesgo a tener en cuenta, destacan: lactancia materna exclusiva, edad gestacional < 38 semanas, ictericia significativa en hijo previo y presencia de ictericia al alta. La utilización de los grupos de riesgo de desarrollar ictericia es de gran ayuda para una mayor vigilancia al alta de la planta de Maternidad en aquellos casos necesarios(1-3).
Medidas terapéuticas
Fototerapia(1,4,12)
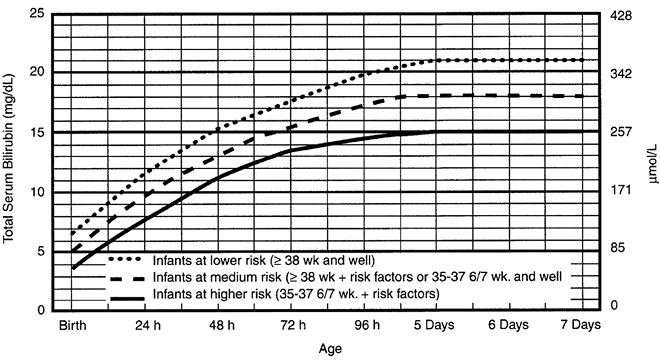
Debemos seguir las indicaciones de los nomogramas de tratamiento de hiperbilirrubinemia, según las indicaciones de la Academia Americana de Pediatría para el recién nacido mayor de 35 semanas (Fig. 3) y según la revisión de NICE y de la Academia Americana de Pediatría para el menor de 35 semanas (Tabla I).
Figura 3. Fototerapia para RN hospitalizados ≥ 35 semanas (según Guía Práctica Clínica de la Academia Americana de Pediatría, Pediatrics, 2004).
El mecanismo de acción de la fototerapia (FT) se produce por isomerización estructural, debida al efecto de la absorción de la luz por parte de la Bb y su transformación a lumirrubina con su posterior excreción. Es una reacción irreversible que ocurre en el espacio extravascular de la piel y se relaciona con la dosis de FT. En la FT simple, el rango se sitúa entre 6-12 μW/cm2/nm. La máxima eficacia de la fototerapia (descenso más rápido de la Bb sérica) se obtiene con la llamada fototerapia intensiva, en la cual se alcanzan valores superiores a 30 μW/cm2/nm en la longitud de onda 460-490 nm. Para ello, es preciso colocar la luz especial azul a 10-15 cm del RN, con máximo área de piel expuesta.
• Tipos de aparatos para administrar fototerapia(12,13):
- Lámparas halógenas: producen una mayor irradiación central con una menor irradiación en la periferia. Pueden generar una pérdida importante de calor.
- Lámparas fluorescentes: la luz más efectiva es la luz especial azul. Son las más utilizadas.
- Lámparas LED: son las lámparas de más reciente aparición y tienen la ventaja de permitir atenuar o aumentar la intensidad de la irradiación empleando un solo equipo. Así mismo, generan menor pérdida de calor que las lámparas convencionales.
- Mantas de fibra óptica: no deben utilizarse como primera línea de tratamiento para recién nacidos mayores de 37 semanas de edad gestacional.
• Controles a realizar durante el tratamiento con FT:
- Vigilar el estado de hidratación. Las pérdidas insensibles se incrementan. Aumentar la frecuencia de las tomas de lactancia materna y, si es preciso, pautar suplemento oral de fórmula. No dar aporte de glucosa oral.
- La FT solo debe interrumpirse durante las tomas y visitas de los padres. En los casos que se indica FT intensiva, no debe interrumpirse hasta que descienda el nivel de Bb sérica o se inicie exanguinotransfusión.
- Vigilancia de posibles efectos secundarios de este tratamiento: síndrome del niño bronceado, inestabilidad térmica y aparición de exantemas.
- Inicialmente, se indicará FT simple. Se indicará FT doble en el caso de: incremento sérico mayor de 0,5 mg/dl/hora de la cifra de Bb; fracaso en la reducción de la cifra de Bb a las 6 horas de inicio de la FT; o cifra de Bb que se encuentra 2,9 mg/dl puntos por debajo de indicación de exanguinotransfusión.
- Los controles analíticos tras su inicio se realizarán con un intervalo que dependerá de la cifra inicial de Bb y de los factores de riesgo existentes en cada paciente. La retirada de FT se realizará con cifras de Bb menores de 14 mg/dl, vigilando el posible efecto rebote.
Exanguinotransfusión(1,2,4)
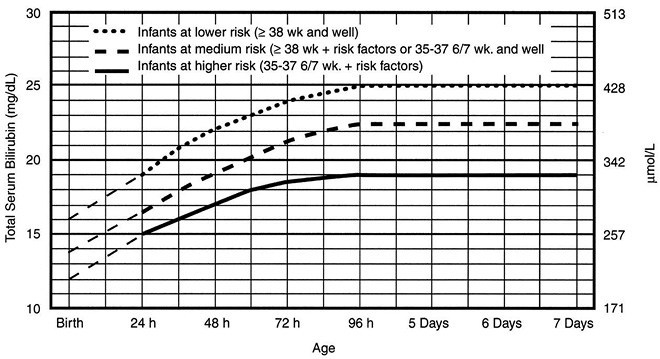
La exanguinotransfusión (EXT) elimina Bb de la sangre antes de que pase al espacio extravascular, elimina anticuerpos hemolíticos de la sangre y permite corregir la anemia. Existen nomogramas para su indicación, al igual que en el caso de la FT (Fig. 4 y Tabla II).
Figura 4. Exanguinotransfusión en RN ≥ 35 semanas (según Guía Práctica Clínica de la Academia Americana de Pediatría, Pediatrics, 2004).
• Características de la técnica:
- Monitorización de constantes: electrocardiograma, frecuencia cardiaca, tensión arterial y temperatura del paciente.
- Utilizar sangre total fresca anticoagulada con: citrato, irradiada, reconstituida con plasma fresco congelado y concentrado de hematíes, para obtener hematocrito final del 45-50%.
- Monitorizar calcio iónico durante el procedimiento, por riesgo de hipocalcemia e hipomagnesemia, glucosa y cifra de plaquetas, después del procedimiento.
- El tipo de sangre a utilizar dependerá de la etiología hemolítica o no de la ictericia y de la urgencia de uso. Se deben solicitar pruebas cruzadas al recién nacido y a la madre, para optimizar la búsqueda de anticuerpos que puedan estar causando la hemólisis.
- Vía de acceso: vena umbilical, canalizando solo lo necesario para que refluya bien.
- El volumen de intercambio será de dos veces la volemia (2 x 80 ml x kg). Se realizará en alícuotas de 10-15 ml en un tiempo máximo de 1,5-2 horas.
- Se administrará profilaxis con cefazolina durante 24 horas.
- Tras EXT, mantener FT y controlar Bb cada 4 horas. Mantener la canalización central 12-24 horas, por si fuera necesario repetir la EXT.
Tratamiento en pacientes con ictericia de etiología hemolítica(3,5,14)
• Isoinmunización Rh. Ocurre en fetos recién nacidos de madres Rh negativo sensibilizadas por parto, aborto, embarazo ectópico… Se producen anticuerpos anti-D tipo IgG que pasan al feto, siendo afectado si es Rh positivo. Otros anticuerpos que pueden causar enfermedad hemolítica son: anti-C, anti-Kelly, anti-Duffy…
La isoinmunización Rh es evitable con una adecuada profilaxis: gammaglobulina anti-D a las 28 semanas de gestación a todas las madres Rh negativo, con una segunda dosis dentro de las 72 horas siguientes al parto.
Está indicado tratamiento en el recién nacido, cuando:
- Seguir nomogramas de indicación de tratamiento indicados previamente.
- Considerar siempre en estos niños, fototerapia intensiva hasta obtener resultados analíticos. Mantener la FT hasta que la Bb total sérica sea menor de 14 mg/dL y vigilar posible rebote.
- EXT si hemoglobina en sangre de cordón menor de 12 mg/dL o Bb total sérica mayor de 5 mg/dL.
- Seguimiento en consulta, con controles de hemoglobina hasta los 3 meses de edad.
- Incompatibilidad ABO. Ocurre con madre grupo O e hijo de grupos A o B. Reviste menos gravedad que la isoinmunización Rh y, rara vez, afecta al feto. Generalmente, el RN presenta ictericia clínica a las 24-48 horas que responde bien a fototerapia, siendo raro que precise EXT. Se seguirán igualmente nomogramas de tratamiento.
Otras medidas de tratamiento(1,5,15)
• En caso de enfermedad hemolítica isoinmune sin respuesta a fototerapia intensiva (incremento sérico mayor de 0,5 mg/dl/hora o cifra de Bb que se encuentra 2-3 mg/dl por debajo de la indicación de exanguinotransfusión), valorar administrar inmunoglobulina intravenosa 0,5 g/kg en 4 horas y repetir a las 12 horas si precisa.
• En casos de colestasis secundaria a nutrición parenteral prolongada o pacientes con Crigler-Najjar tipo II, puede utilizarse fenobarbital a 5-8 mg/kg/día; como favorecedor de conjugación y excreción de Bb.
• En el caso de hiperbilirrubinemia directa, se individualizarán las medidas terapéuticas.
• El resto de los fármacos no han demostrado su eficacia.
Función del pediatra de Atención Primaria
• Vigilancia de los neonatos dados de alta desde las plantas de maternidad con factores de riesgo de ictericia. Dada la tendencia al alta precoz de los recién nacidos, es importante valorar en Atención Primaria o a nivel hospitalario aquellos pacientes con factores de riesgo de ictericia: lactancia materna exclusiva, prematuros tardíos (34-37 semanas de edad gestacional), presencia de cefalohematomas, raza asiática y cifra elevada de Bb en zona de alto riesgo.
• Vigilancia de los neonatos con clínica de ictericia mayor de 7 días de vida. Debemos recordar que los pacientes con lactancia materna exclusiva pueden presentar ictericia clínica hasta las los 40-60 días de vida sin repercusión clínica. No obstante, ante los cuadros de ictericia prolongada en periodo neonatal, se deberá realizar un diagnóstico diferencial, incluyendo: infección urinaria, hipotiroidismo, posibilidad de enfermedad hemolítica familiar, fibrosis quística y enfermedades metabólicas, como la galactosemia.
• Vigilancia de los neonatos que desarrollen signos de colestasis: ictericia junto a coluria/acolia. En estos casos, se orientará el diagnóstico hacia patología hepatobiliar, siendo necesaria una derivación del paciente al ámbito hospitalario, para completar el diagnóstico y el abordaje terapéutico que precise.
Bibliografía
Los asteriscos reflejan el interés del artículo a juicio del autor.
1.*** American Academy of Pediatrics. Clinical Practice Guideline. Subcommittee on Hyperbilirrubinemia. Management of hyperbilirrubinemia in the newborn infant less 35 or more weeks of gestation. Pediatrics. 2004; 114: 297-316.
2.*** Maisels MJ, Watchko JF, Bhutani VK, Stevenson DK. An approach to the management of hyperbilirubinemia in the preterm infant less than 35 weeks of gestation. Journal of Perinatology. 2012; 32: 660-4.
3.*** Sánchez-Redondo Sánchez-Gabriel MD, Leante Castellanos JL, Benavente Fernández I, Pérez Munuzuri A, Rite Gracia S, Ruiz Campillo CW, et al. Recomendaciones para la prevención, la detección y el manejo de la hiperbilirrubinemia en los recién nacidos con 35 o más semanas de edad gestacional. An Pediatr (Barc). 2017; 87: 243-98.
4.*** National Institute for Health and Clinical Excellence. Neonatal Jaundice. (Clinical guideline 98). 2010. www.nice.org.uk/CG98.
5.*** Caballero SM, González-Valcárcel M. Ictericia patológica en el recién nacido. En: Casado Flores J, Serrano González A. Urgencias pediátricas niño grave. Ergon. SA.; 2015. p. 1146-53.
6.** Omeñaca Teres F, González Gallardo M. Ictericia neonatal. Pediatr Integral. 2014; XVIII(6): 367-74.
7.** Stark A, Bhutani V. Hiperbilirrubinemia Neonatal. En: Cloherty JP, Stark AR (eds). Manual of neonatal care. 8 ed. Wolters Kluwer. 2017. p. 316-32.
8.* Johnson L, Bhutani VK. Guidelines for management of the jaundiced term and near-term infant. Clin Perinatol. 1998; 25: 555-74.
9.* Ratnavel N, Ives NK. Investigation of prolonged neonatal jaundice. Current Paediatrics. 2005; 15: 85-91.
10.* Yao TC, Stevenson DK. Advances in the diagnosis and treatment of neonatal hyperbilirrubinemia. Clin Perinatol. 1995; 133: 705-7.
11.* Vandborg PK, Hansen BM, Greisen G, Ebbesen F. Dose-Response Relationship of Phototherapy for Hyperbilirubinemia. Pediatrics. 2012; 130; e352.
12.* Capasso L, Parrella C, Borrelli AC, et al. Is it worthwhile using a transcutaneous bilirubinometer in the nursery? Early Human Development. 2012; 88S2: S25-S26.
13.* Dijk PH, Hulzebos CV. An evidence-based view on hyperbilirubinaemia. Acta Pædiatrica. 2012; 101: 3-10.
14* Kaplana M, Bromikera R, Hammermana C. Severe Neonatal Hyperbilirubinemiaand Kernicterus: Are These Still Problems in the Third Millennium? Neonatology. 2011; 100: 354-62.
15** Stokowski LA. Fundamentals of Phototherapy for Neonatal Jaundice. Advances in Neonatal Care. 2011; 11: S10-S21.
Bibliografía recomendada
– American Academy of Pediatrics. Clinical Practice Guideline. Subcommittee on Hyperbilirrubinemia. Management of hyperbilirrubinemia in the newborn infant less 35 or more weeks of gestation. Pediatrics. 2004; 114: 297-316.
Guía de diagnóstico y tratamiento de los recién nacidos mayores de 35 semanas con ictericia.
– Maisels MJ, Watchko JF, Bhutani VK, Stevenson DK. An approach to the management of hyperbilirubinemia in the preterm infant less than 35 weeks of gestation. Journal of Perinatology. 2012; 32: 660-4.
Guía de diagnóstico y tratamiento de los recién nacidos menores de 35 semanas con ictericia.
– Sánchez-Redondo Sánchez-Gabriel MD, Leante Castellanos JL, Benavente Fernández I, Pérez Munuzuri A, Rite Gracia S, Ruiz Campillo CW, et al. Recomendaciones para la prevención, la detección y el manejo de la hiperbilirrubinemia en los recién nacidos con 35 o más semanas de edad gestacional An Pediatr (Barc). 2017; 87(5): 243-98.
Revisión actualizada en el año 2017, sobre el manejo de la ictericia en los mayores de 35 semanas.
– Caballero Martín S, González-Valcárcel Espinosa M. Ictericia patológica en el recién nacido. En: Casado Flores J, Serrano González A. Urgencias y tratamiento del niño grave. Ergon. SA.; 2014. p. 178-79.
Estudio en profundidad sobre la etiología, fisiopatología, diagnóstico y tratamiento de la ictericia neonatal.
| Caso clínico |
|
Recién nacido pretérmino de edad gestacional 36 semanas, con antecedentes perinatales: madre 36 años, primípara, primigesta. Grupo Sanguíneo A Rh positivo. Sana. Padre 37 años, sano. No consanguineidad. Embarazo controlado. Serologías connatales (rubeola inmune, toxoplasmosis no inmune, VIH, VHB, VHC y lúes negativas). Exudado vaginorrectal no realizado. Ecografías connatales normales salvo en semana 34, peso fetal estimado en percentil 7 con doppler normal. Parto a las 36 semanas, vaginal, eutócico. Peso al nacimiento: 2.300 gramos. No precisó reanimación. pH de cordón: 7,30. Durante su estancia en planta de maternidad, presenta máxima pérdida ponderal del 10% con alimentación con lactancia materna exclusiva. Peso al alta: 2.070 gramos. Mantiene buen tránsito intestinal sin presentar vómitos y con exploración física dentro de la normalidad. Previo al alta, a las 48 horas de vida, se objetiva ictericia cutánea. Se realiza medición con bilirrubinómetro transcutáneo con cifra de 10 mg/dL. Se indica a los padres vigilancia en domicilio, tomas de lactancia materna frecuentes, vigilancia de diuresis (cambiar, al menos, 5-6 pañales con orina al día) y control en 24 horas en consulta hospitalaria de neonatología. En revisión en consulta, se objetiva buen estado de hidratación, peso: 2.040 gramos (-30 gramos) y se repite medición transcutánea de Bb de 15 mg/dL comprobándose medición sérica de 16,2 mg/dL (Bb directa de 0 mg/dL). Ante los hallazgos y la valoración de la cifra de Bb de los nomogramas de la AAP, se decide su ingreso para fototerapia simple en planta de neonatología y vigilancia de enganche y realización de tomas, para valorar necesidad de suplemento si es necesario. En control analítico a las 6 horas de inicio de tratamiento, descenso de cifras de Bb a 11 mg/dL, permitiendo retirada de fototerapia a las 12 horas de ingreso, con control posterior dentro de la normalidad. Presenta buena realización de tomas durante el ingreso con succión adecuada, siendo dado de alta a las 48 horas de este, con curva ponderal ascendente.
|