Pubertad precoz y retraso puberal
Introducción
Las alteraciones en la cronología de la pubertad pueden determinar trastornos no solo del desarrollo gonadal y genital, sino también, del crecimiento, de la composición y proporciones corporales, así como de los aspectos psicológicos y emocionales propios de la adolescencia.
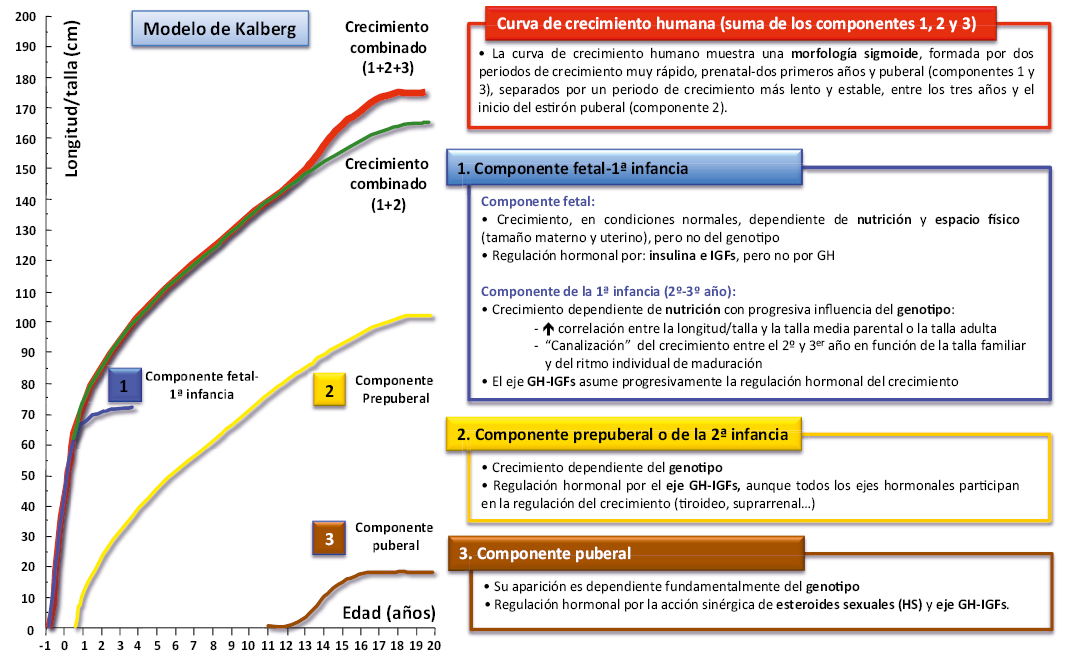
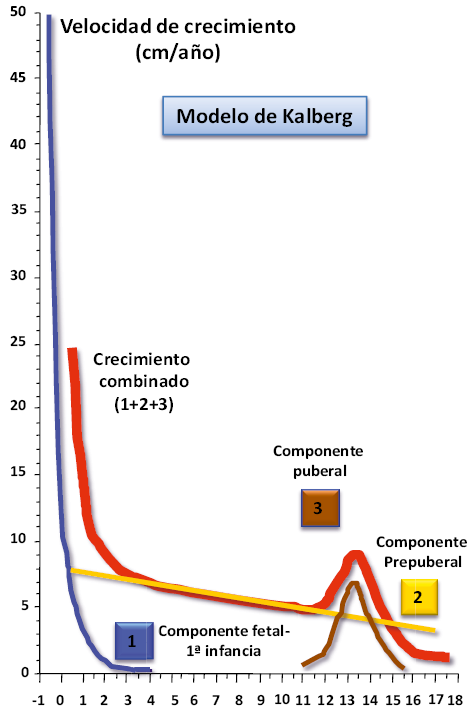
La pubertad es el periodo del desarrollo humano en el que tienen lugar los cambios biológicos y somáticos que marcan la diferencia entre la infancia y la edad adulta. Un proceso madurativo de límites muy imprecisos que, en condiciones normales, se inicia con la aparición de los caracteres sexuales secundarios y finaliza cuando se ha alcanzado la talla adulta, la maduración sexual completa y la capacidad reproductora. Este proceso conlleva no solo el desarrollo gonadal y genital, sino también, la aceleración del crecimiento, la modificación de la composición corporal y de las proporciones corporales, así como, cambios psicológicos y emocionales propios de la adolescencia. Por consiguiente, las alteraciones en la cronología de la pubertad pueden determinar trastornos en todos estos aspectos, cuya magnitud dependerá de la causa que las origine, del grado de adelanto o de retraso en su inicio y de la rapidez de su progresión.
Aspectos fisiopatológicos de la cronología puberal
La variabilidad en la edad de inicio puberal, entre individuos de condiciones de vida similares, es de unos 4-5 años. Esta variabilidad parece estar determinada por factores genéticos (˜50-80% de la variabilidad) y ambientales.
El eje hipotálamo-hipófiso-gonadal (HHG) se activa en la vida fetal, hacia la mitad de la gestación, y es posteriormente inhibido por el retrocontrol negativo de las hormonas placentarias, principalmente por el estradiol; por lo que, al nacimiento, el nivel sérico fetal de gonadotropinas es bajo. La desaparición de los esteroides placentarios después del nacimiento permite la reactivación del eje HHG, a partir aproximadamente de la 1ª semana de vida postnatal, y se mantiene activo durante los primeros meses de vida, lo que se conoce como mini-pubertad(1). La duración de esta actividad es variable, habitualmente hasta los 6-12 meses de vida, con un predominio de LH (hormona luteinizante) en los varones y de FSH (hormona folículo-estimulante) en las niñas; si bien, en ellas, la elevación de FSH suele persistir más tiempo, hasta los 2-3 años, a veces más. La secreción de gonadotropinas en la minipubertad provoca un cierto grado de estimulación gonadal. En los varones, la testosterona alcanza su pico de secreción alrededor de los 1-3 meses de vida, incrementando solo ligeramente el tamaño testicular y del pene; ya que, el aumento concomitante de los niveles de SHBG [proteína trasportadora de los esteroides sexuales (ES)] limita su actividad biológica. En las niñas, el incremento de gonadotropinas favorece el desarrollo folicular ovárico y la producción fluctuante de estradiol que puede traducirse en una telarquia del lactante que, con frecuencia, tiene también un carácter fluctuante. Después de la minipubertad, el eje HHG permanece quiescente, como consecuencia de una supresión activa de la secreción de GnRH (hormona hipotalámica liberadora de gonadotropinas), hasta que se aproxima el tiempo de la pubertad, momento en que se reactiva la secreción pulsátil de GnRH y, con ella, la de LH y FSH.
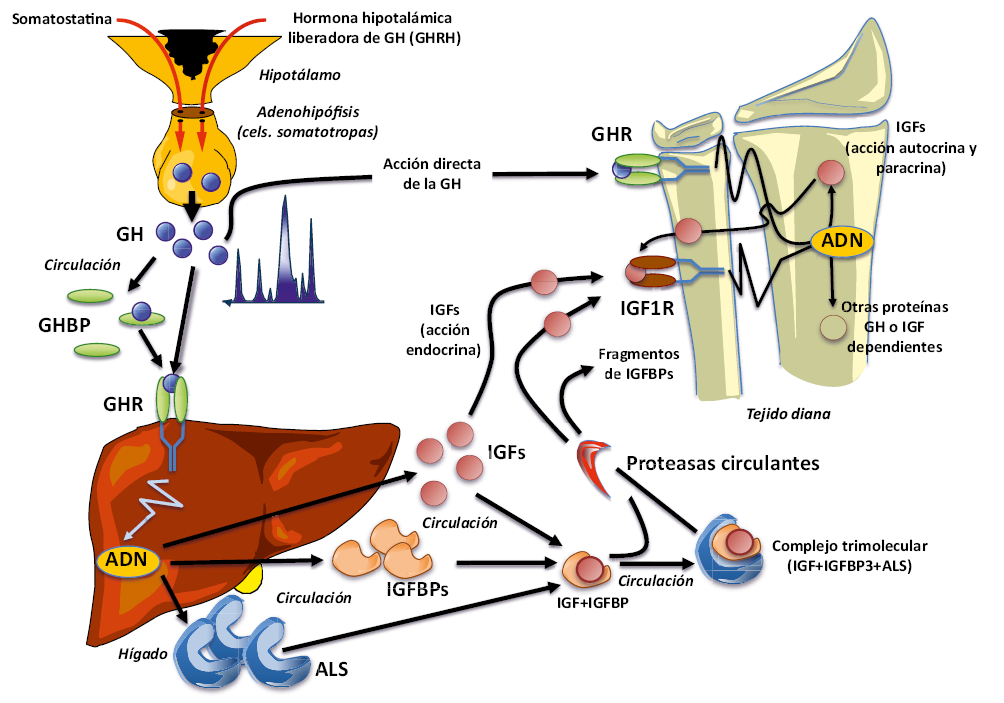
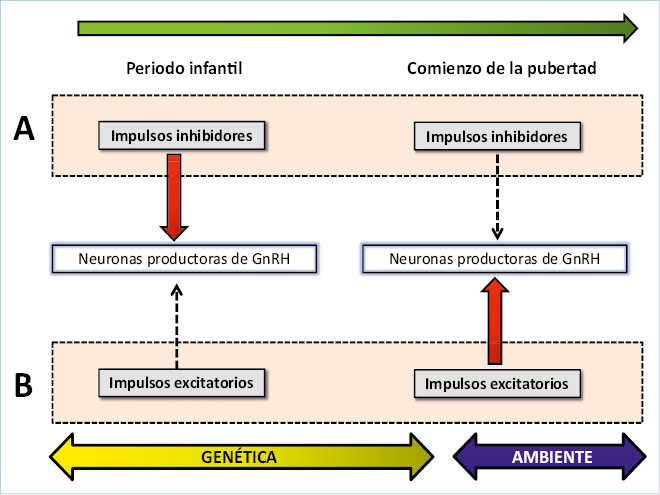
En la pubertad, LH y FSH son liberadas de forma pulsátil, inicialmente durante la noche y, posteriormente, a medida que la pubertad progresa, durante el resto del día, y actúan coordinadamente en la gónada para inducir la maduración de las células germinales (óvulos o espermatozoides) y la producción de ES, así como de otros péptidos gonadales, como es el caso, entre otros, de las inhibinas. La testosterona en el varón y el estradiol en la mujer son los principales responsables del desarrollo de los caracteres sexuales secundarios y ejercen un retrocontrol negativo en hipotálamo e hipófisis (Fig. 1), reduciendo la secreción de GnRH y LH; mientras que, las inhibinas controlan, en la hipófisis, la secreción de FSH a través de un asa de retrocontrol diferente.
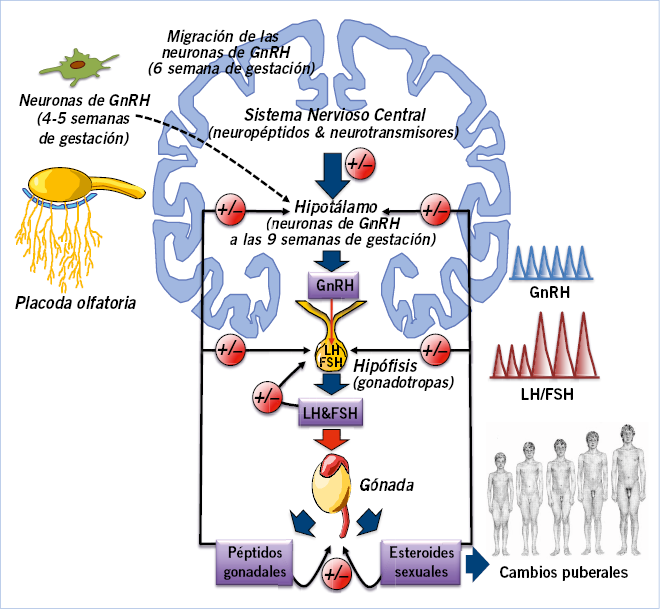
Figura. 1. Eje hipotálamo-hipófiso-gonadal (HHG). La hormona hipotalámica liberadora de gonadotropinas (GnRH) induce, en las células gonadotropas hipofisarias, la síntesis y liberación pulsátil de las gonadotropinas hipofisarias, LH (hormona luteinizante) y FSH (hormona folículo-estimulante), que actúan coordinadamente en la gónada para inducir la maduración de las células germinales (óvulos o espermatozoides) y la producción de esteroides sexuales (ES), así como de otros péptidos gonadales (inhibinas, activinas, folistatina…). ES y péptidos gonadales, así como otras hormonas circulantes (leptina…), ejercen a través de mecanismos de retrocontrol, acciones estimulantes e inhibidoras, a diferentes niveles del eje HHG, modulando su complejo funcionamiento; así, por ejemplo, los ES, principalmente la testosterona en el varón y estradiol en la mujer, además de ser los responsables finales del desarrollo de los caracteres sexuales secundarios, ejercen un retrocontrol negativo en hipotálamo e hipófisis, reduciendo la secreción de GnRH y LH.
Desde el punto de vista endocrinológico(2), el primer signo del inicio de la pubertad y, por tanto, de la reactivación del eje HHG es el incremento de la secreción pulsátil de GnRH. Las neuronas productoras de GnRH tienen su origen embriológico en el ectodermo oral y a partir de la sexta semana de vida intrauterina migran desde la placoda olfatoria a su localización normal en el hipotálamo, desde donde proyectan sus axones liberadores de GnRH hacia la eminencia media. Se ha demostrado que estas neuronas, independientemente de estímulos externos, poseen la capacidad de secretar GnRH en forma pulsátil, con autorritmicidad sincronizada y espontánea; sin embargo, la amplitud de los pulsos secretorios de GnRH, cuyo incremento es característico del inicio de la pubertad, está regulada por la acción de señales estimulantes (sistema glutaminérgico, noradrenérgico, dopaminérgico, kisspeptinas…) e inhibidoras (sistema gabaérgico, opiáceos endógenos…) que, en forma de neuropéptidos y neurotransmisores, actúan en el hipotálamo. La secreción de GnRH está, además, modulada por la interacción entre las neuronas que la producen y las células gliales circundantes, así como por el sistema nervioso central (SNC) que, a su vez, integra los efectos de muchos factores externos, que influirían en el momento de inicio puberal, como serían: nutrición, ejercicio, estrés o factores sociales y psicológicos, entre otros.
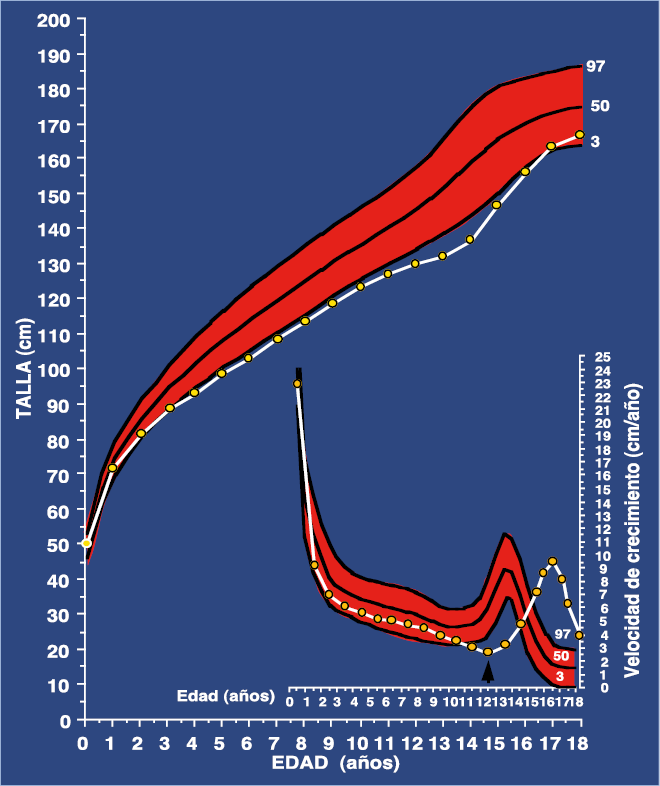
Desde el punto de vista clínico, el inicio de la pubertad lo marca la aparición y el desarrollo de los caracteres sexuales secundarios, que siguen una secuencia relativamente predecible y que fue categorizada en cinco fases o estadios por James Tanner a principios de la década de los sesenta (estadios de Tanner). En las niñas, la telarquia o aparición del botón mamario suele ser el primer signo de desarrollo puberal (estadio II, a una edad media de 10,5-11 años; intervalo de 8 a 13 años) y coincide, habitualmente, con el inicio del “estirón puberal”. En los varones, el inicio de la pubertad lo marca el incremento del volumen testicular, que alcanza o supera los 4 mL o, si no se dispone de un orquidómetro, una longitud mayor o igual a 25 mm (estadio II, a una edad media de 11,5-12 años; intervalo de 9 a 14 años). En los varones, a diferencia de las niñas, el estirón puberal no coincide con el inicio de la pubertad, sino que se inicia más tardíamente, aproximadamente un año después (12,5-13 años), en el estadio III, y cuando el volumen testicular ha alcanzado los 8-12 mL de volumen.
Los datos descritos corresponden a estudios longitudinales europeos llevados a cabo en la década de los sesenta del siglo pasado. Desde mediados del siglo XIX a mediados del siglo XX, en los países occidentales desarrollados, se ha observado una mejoría en el crecimiento, con mayores tallas adultas en ambos sexos, y una tendencia a una maduración más rápida, especialmente en mujeres, donde la edad de la menarquia se ha adelantado desde los 15-17 años a menos de 14 años(3). Ambos fenómenos, conocidos como: “tendencia secular del crecimiento y desarrollo”, muestran variaciones de magnitud entre diferentes países y se han atribuido, especialmente, a la mejoría en la nutrición, salud y condiciones generales de vida; no obstante, es objeto de debate si esta tendencia secular continúa o se ha estabilizado. En cualquier caso, la edad de inicio puberal muestra una variabilidad de unos 4-5 años entre individuos con condiciones de vida similares(4). Esta variabilidad parece estar determinada por factores genéticos (˜50-80% de la variabilidad) y ambientales(5,6):
• Factores familiares y étnicos. La influencia genética en la edad de inicio puberal ha sido plenamente demostrada mediante estudios familiares y de concordancia entre gemelos monocigóticos; no obstante, sus bases genéticas no han sido claramente establecidas. Se han identificado polimorfismos en determinados genes que parecen estar relacionados con el momento de la menarquia [receptor de andrógenos, receptor alfa de estrógenos, CYP17 o proteína transportadora de esteroides sexuales (SHBG), entre otros]. Más recientemente, mediante estudios de asociación del genoma completo (GWAS), se han identificado más de 100 loci relacionados con el momento de la menarquia(4); entre los más importantes, uno en 6q21 (región próxima a LIN28B) y otro en 9q31.2 (región intergénica). También, recientemente, se ha demostrado que mecanismos epigenéticos modulan la interrelación entre genética y ambiente para poner en marcha la pubertad(5). Las diferencias en la edad de inicio puberal entre razas y etnias, al igual que ocurre entre diferentes áreas geográficas, es, probablemente, un reflejo de la combinación de factores genéticos, socioeconómicos y ambientales, cuya influencia individual es difícil de establecer; no obstante, determinadas razas, como la negra, en condiciones de vida similares, parecen mostrar una tendencia a una maduración más temprana.
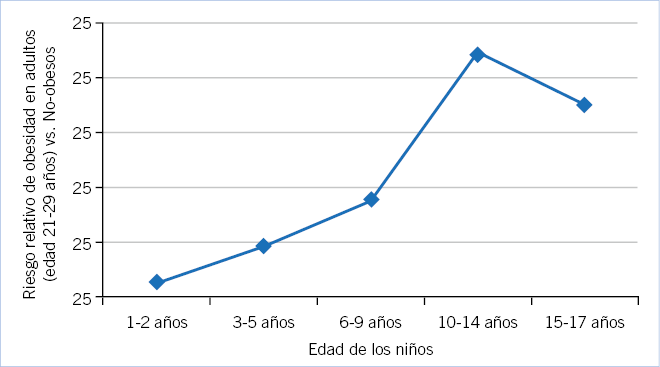
• Factores nutricionales y socioeconómicos. Una adecuada nutrición y un ambiente socioeconómico favorable se asocian a un desarrollo puberal más temprano; por el contrario, condiciones nutricionales o socioeconómicas desfavorables condicionan un desarrollo puberal más tardío. En este sentido, la nutrición parece ser uno de los principales factores determinantes del momento de inicio puberal, una interrelación probablemente mediada por la leptina liberada por los adipocitos; aunque, otras sustancias, como glucosa, insulina o ghrelina podrían también actuar como fuentes de información para el hipotálamo del estado nutricional. En los países en vías de desarrollo, la malnutrición calórico-proteica (marasmo) temprana, pero no la proteica (kwashiorkor) condicionan un retraso puberal. Fuera de estas situaciones extremas, la malnutrición crónica, en general, induce un retraso puberal en ambos sexos y es, probablemente, uno de los factores responsables del retraso puberal asociado a las patologías crónicas o a la amenorrea atlética. En el otro extremo, el exceso de grasa subcutánea y el aumento del índice de masa corporal (IMC) durante el periodo prepuberal se asocian con un incremento en el riesgo de presentar una pubertad temprana, especialmente en niñas, y podrían ser uno de los factores implicados en la aceleración puberal observada en algunos países occidentales con tasas crecientes de obesidad infantil en las últimas décadas.
• Ciclo luz-oscuridad y condiciones climáticas. Aunque algunos estudios sugieren un gradiente norte-sur en la edad de la menarquia (más tardía en las latitudes norte) y la posibilidad de un efecto inhibitorio de la luz mediado por la melatonina sobre el desarrollo puberal, los efectos de la luz, el clima y la latitud en humanos son inciertos.
• Estrés crónico. El estrés crónico parece ser capaz de inhibir el eje HHG y sería uno de los factores implicados en el retraso puberal asociado a: enfermedades crónicas, ejercicio físico intenso-competición o conflictos bélicos, entre otras potenciales situaciones de estrés; no obstante, en muchas de ellas, es difícil separar el componente de estrés de otros componentes, habitualmente presentes en estas situaciones, como sería el caso de la malnutrición.
• Condiciones de vida intrauterina. Algunos estudios indican, que los recién nacidos, especialmente las niñas, con bajo peso al nacimiento (PRN < 2.500 g) o pequeños para su edad gestacional (RNPEG), muestran una mayor incidencia de pubertad adelantada o precoz, sobre todo, si experimentan un rápido crecimiento de recuperación.
• Disruptores endocrinos. En las últimas décadas, la industrialización ha producido un incremento gradual, pero significativo, en el número y cantidad de contaminantes ambientales. Algunos de ellos son sustancias, naturales o de síntesis, que debido a su similitud estructural con determinadas hormonas, pueden tener efectos negativos sobre el sistema endocrino (disruptores endocrinos)(5,6). En algunos de ellos: fitoestrógenos, estrógenos naturales (tópicos o sistémicos), pesticidas, fungicidas, sustancias químicas industriales o ftalatos, entre otros, se ha demostrado que son agentes capaces de producir en humanos: pubertad adelantada/precoz, pubertad retrasada o, incluso, trastornos de la diferenciación sexual, dependiendo de su mecanismo de acción (estrogénico, androgénico, antiandrogénico o antiestrogénico) y momento de actuación.
• Adopción. Los últimos 30 años han puesto de manifiesto la importancia, como causa de adelanto puberal, de la adopción internacional. Entre un 15-30% de los casos de pubertad precoz central (PPC) idiopática corresponden a niños adoptados de otros países, habitualmente en vías de desarrollo(3). En todos los estudios, existe un claro predominio de niñas, lo que podría estar en relación con la clásica e inexplicada preponderancia femenina en lo que a la PPC idiopática se refiere. En el año 2010, se publicaron los primeros resultados del Registro Español de Pubertad Precoz(7), donde se observó un riesgo 25 veces mayor de desarrollar PPC idiopática entre niñas adoptadas de otros países respecto a la población nacida en España. Las causas que motivan el adelanto puberal en estas niñas son desconocidas, aunque se han sugerido distintos factores, entre ellos: traslado a un ambiente socioeconómico más favorable, mejoría nutricional, reducción de la situación de estrés crónico o reducción de la exposición a disruptores endocrinos que pudieran estar inhibiendo y madurando el eje HHG. Se ha postulado, también, que el adelanto puberal podría ser el resultado de la combinación de unas condiciones vitales adversas en la infancia temprana, asociadas a condiciones de opulencia en el periodo prepuberal tardío, dos condiciones opuestas que favorecerían el desarrollo puberal temprano(8).
La duración de la pubertad es, al igual que el momento de su inicio, muy variable. En las niñas, suele utilizarse como marcador de finalización puberal el inicio de las menstruaciones, aunque, en la mayoría de los casos, en el momento de la menarquia, ni se ha completado el desarrollo puberal (estadio IV de Tanner), ni se ha finalizado el crecimiento (crecimiento postmenarquia medio de 4-6 cm, rango entre 2-12 cm), ni se ha alcanzado plenamente la fertilidad (frecuentes ciclos anovulatorios). El intervalo desde el inicio de la pubertad a la menarquia es de 2,4 años ± 1,1 año (media ± 1 SDS). Se ha observado una correlación negativa entre el inicio de la pubertad y la aparición de la menarquia; de forma que, las niñas que inician la pubertad más temprano tardan algo más en tener la menarquia que las niñas que maduran más tardíamente.
En los varones, la finalización de la pubertad es aún más difusa que en las niñas. Suele considerarse que la pubertad se ha completado cuando se alcanza un volumen testicular de adulto (media de unos 20 mL), lo que se produce habitualmente, unos 3,2 ± 1,8 años (media ± 1 SDS) después del inicio de la pubertad(2). No obstante, el criterio es poco claro, dada la variabilidad normal del volumen testicular de un adulto. De hecho, algunos varones normales no superan los 12-15 mL de volumen testicular; mientras que, otros superan los 25-30 mL. Por otro lado, como en el caso de las mujeres, en ese momento, habitualmente, tampoco se ha finalizado el crecimiento ni se han desarrollado completamente los caracteres sexuales secundarios.
Pubertad precoz (PP)
Concepto
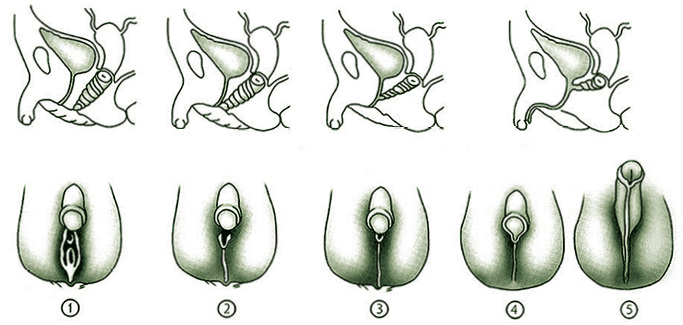
El concepto de pubertad precoz es arbitrario, pero suele definirse como: la aparición de los caracteres sexuales secundarios antes de los 8 años en las niñas y de los 9 años en los niños (˜2,5-3 SDS por debajo de la edad media para el sexo y población estudiada; Fig. 2)(9).

Figura 2. Concepto estadístico de pubertad precoz (inicio puberal alrededor de 2,5-3 SDS por debajo de la edad media para el sexo y población estudiada), retrasada(inicio puberal alrededor de 2-2,5 SDS por encima de la edad media para el sexo y población estudiada) y normal para ambos sexos, basado en los rangos normales de inicio de la pubertad (Marshall, WA, Tanner, JM. Arch Dis Child. 1969; 44: 291).
En los últimos años, los límites de edad que delimitan el inicio normal de la pubertad y, en consecuencia, el concepto de PP han sido objeto de debate, especialmente tras la publicación en 1997 del estudio PROS (Pediatric Research in Office Setting) sobre la edad de desarrollo puberal en EE.UU. Los resultados de este estudio sugerían un inicio puberal más precoz, especialmente en las niñas afroamericanas, e hicieron plantear la conveniencia de cambiar los límites de edad para la PP a antes de los 7 años en niñas caucásicas y a antes de los 6 años en afroamericanas(10). No obstante, los potenciales errores de la metodología empleada en este estudio, así como el hecho de que estudios similares en Europa no pusieran de manifiesto la misma tendencia, han hecho que, en la mayor parte de la comunidad científica internacional, los límites de edad para considerar una pubertad como precoz no se hayan modificado.
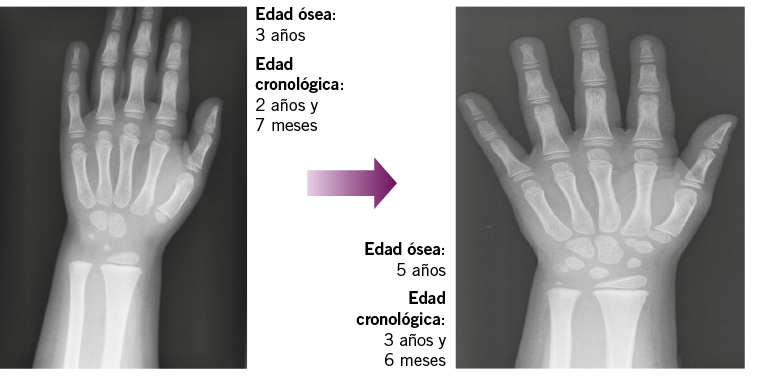
Unido al concepto de PP, estaría el de “pubertad adelantada” (PA), como: aquella que se inicia próxima a los límites inferiores de la normalidad. Tampoco existe un consenso internacional que establezca con claridad sus límites, pero podríamos situarlos entre los 8-9 años en las niñas y entre los 9-10 años en los niños. Al igual que la PP, la PA es mucho más frecuente en niñas y se considera habitualmente la expresión de uno de los extremos del rango normal de edad de desarrollo puberal; es decir, una variante de la normalidad, que puede ser familiar (“aceleración constitucional del crecimiento y de la pubertad”; ACCP) o esporádica, pero que no precisaría, en general, tratamiento. Los niños con esta variante normal de pubertad se caracterizan, clínicamente, por un patrón de crecimiento y desarrollo característico, que conlleva un crecimiento acelerado a partir de los 1-2 años de vida, con talla prepuberal por encima del carril correspondiente a su talla diana, aceleración de la edad ósea (1-3 SDS por encima de su edad cronológica), inicio puberal a una edad en los límites inferiores del rango normal y finalización temprana del desarrollo puberal y del crecimiento, alcanzando, habitualmente, una talla acorde con su contexto familiar.
Morbilidad asociada al adelanto puberal
Las consecuencias de una PP dependen en gran medida de su etiopatogenia, pero, incluso cuando no se encuentra una base orgánica, el desarrollo precoz de la pubertad conlleva una serie de riesgos potenciales (auxológicos y psicosociales). La PA, aunque en principio no se considera patológica y, por consiguiente, no requeriría tratamiento, conlleva un riesgo intermedio entre una PP y una pubertad normal. Este riesgo es mayor cuando la pubertad es rápidamente progresiva o afecta a poblaciones con mayor riesgo de afectación de la talla adulta o a pacientes con alteraciones cognitivas. Por ello, aunque no existen criterios que permitan establecer qué pacientes podrían beneficiarse, en algunos casos muy individualizados, la PA podría ser también susceptible de tratamiento.
Riesgos auxológicos
El desarrollo puberal precoz acelera el ritmo de crecimiento, pero más aún la maduración ósea; de forma que, aunque estos niños parezcan inicialmente altos, el cierre de los cartílagos de crecimiento y la finalización del crecimiento a una edad temprana conlleva un riesgo de modificación de las proporciones corporales (acortamiento de extremidades) y, especialmente, de pérdida de talla final(11). Esta pérdida puede ser muy variable, pero suele ser tanto mayor cuanto más precoz es el inicio puberal, mayor la edad ósea (EO), mayor el tiempo de evolución y mayor la rapidez de progresión de la EO y del desarrollo puberal. Además, existirían determinadas poblaciones de riesgo para una mayor afectación de la talla, como serían aquellos pacientes con:
• Talla baja en el momento del diagnóstico.
• Cuadro sindrómico asociado a talla baja.
• Antecedentes de RNPEG.
• Deficiencia asociada de hormona de crecimiento (GH).
• Patología oncológica con radioterapia craneal y, especialmente, cráneo-espinal.
• Antecedentes de adopción internacional.
En cualquier caso, la repercusión auxológica es muy difícil de predecir en un sujeto concreto; ya que, los métodos de predicción de talla adulta de que disponemos son inadecuados para este tipo de pacientes y existen mecanismos normales de compensación responsables de que no en todas las PP la talla final sea baja.
Riesgo psicosocial
Las consecuencias psicosociales y conductuales de presentar una PP han sido poco estudiadas y, además, pocas veces son tenidas en consideración a la hora de valorar a estos pacientes. En las niñas, donde mayoritariamente se han llevado a cabo estos estudios, se han descrito situaciones de estrés y de dificultad de adaptación ante los rápidos cambios físicos y psicológicos que se producen, rechazo por parte de sus compañeros y tendencia al aislamiento y a la depresión. Ambos sexos, pero sobre todo los varones, pueden mostrar un aumento de la líbido, con desarrollo de conductas masturbatorias o sexuales inadecuadas, especialmente si existe un cierto grado de retraso mental que limite su capacidad de control. En las niñas, se ha descrito también un inicio más precoz de las relaciones sexuales e, incluso, un mayor riesgo de abuso sexual. Las pacientes que han tenido una PP muestran en la adolescencia más problemas de conducta, incluso delictiva, menor competencia social y suelen alcanzar niveles educativos más bajos(12). Esta desadaptación social parece limitarse a la adolescencia y desaparece en la edad adulta. En cualquier caso, al igual que ocurre con los riesgos auxológicos, los riesgos psicosociales en un paciente concreto son difíciles de predecir.
Otros riesgos potenciales
Aunque los datos disponibles son todavía insuficientes para poder establecer conclusiones definitivas, las mujeres adultas con antecedentes de menarquia temprana parecen presentar un mayor índice de masa corporal (IMC), con incremento de grasa abdominal, mayores cifras de tensión arterial y de hemoglobina glicada, así como un peor perfil lipídico. Todos estos factores sugieren que estas mujeres tendrían un mayor riesgo cardiovascular y de diabetes y, por tanto, de morbimortalidad. También, se ha sugerido en los pacientes con PP un posible incremento en el riesgo de cáncer de mama y de testículo.
Clasificación y epidemiología
El incremento de ES, que es lo que determina la aparición y desarrollo de los caracteres sexuales secundarios, puede tener distinto origen (Tabla I), lo que permite clasificar la PP en:
• PP central (PPC). Conocida, también, como: PP verdadera o PP dependiente de gonadotropinas; ya que, el incremento de ES es el resultado de una reactivación normal, pero precoz, del eje HHG y, por ello, siempre es isosexual.
• PP periférica (PPP).Conocida, también, como: pseudopubertad precoz o PP independiente de gonadotropinas. La fuente de ES puede ser exógena o endógena, gonadal o extragonadal, pero, en cualquier caso, el desarrollo de los caracteres sexuales secundarios no es la consecuencia de la activación del eje HHG. Dependiendo del ES aumentado (andrógeno o estrógeno) y del sexo del niño, las manifestaciones clínicas puede ser isosexuales (apropiadas al sexo del niño) o contrasexuales (contrarias al sexo del niño).
• PP mixta (PPM). Se la conoce, también, como: PP combinada o PPC secundaria; ya que, resulta de una mezcla o combinación de una PPP y una PPC. La exposición prolongada a ES, provocada por una PPP, aceleraría el crecimiento, la EO y la maduración de los centros hipotalámicos implicados en el inicio del desarrollo puberal, causando la reactivación precoz del eje HHG y el desarrollo secundario de una PPC.
La PP es una patología infrecuente, con una incidencia difícil de establecer (1:5.000-10.000 niños)(2) y, al contrario de lo que ocurre con la pubertad retrasada, con un claro predominio en niñas (relación que oscila entre 3:1 y 23:1 según las series; 10:1 en el estudio español de 2010(7)). Más del 90% de los casos corresponden a formas de PPC y la gran mayoría son de etiología idiopática. En el caso de pacientes con trastornos o lesiones del sistema nervioso central (neurofibromatosis, hidrocefalia, mielomeningocele…), determinados síndromes (Beuren-Williams…) o, como ya ha sido comentado, procedentes de adopción internacional, la frecuencia de PPC es claramente superior a la del resto de la población.
Etiopatogenia y manifestaciones clínicas
Pubertad precoz central (PPC)
La PPC se debe a una reactivación precoz del eje HHG y se caracteriza clínicamente por un desarrollo precoz de los caracteres sexuales secundarios, que siempre son isosexuales y que siguen la secuencia normal de aparición, con aumento del tamaño y de la actividad de las gónadas.
La PPC se caracteriza clínicamente, en las niñas, por la aparición (telarquia) y desarrollo progresivo de la mama antes de los 8 años, que puede ser, inicialmente y durante unos meses, unilateral, y por el incremento del volumen testicular (=4 mL) en los varones antes de los 9 años, que es seguido, habitualmente y en ambos casos, por el desarrollo de la pubarquia y axilarquia. La EO se adelanta, habitualmente más de 2 SDS por encima de la edad cronológica y, en las niñas, la VC experimenta una rápida aceleración (estirón puberal) que coincide o incluso puede preceder a la aparición del botón mamario. En los varones, el estirón puberal es un fenómeno más tardío en el desarrollo puberal (estadio III-IV de Tanner) y no suele coincidir con el incremento inicial del volumen testicular; no obstante, en los casos de PPC, también tiende a adelantarse (finales del estadio II o principio del III)(13).
Es una patología con un claro predominio en niñas, en las que la etiología es habitualmente idiopática (Fig. 3); mientras que, en los niños son más frecuentes que en las niñas las causas orgánicas (40-90% en varones frente a un 8-33% en niñas)(9). El motivo de estas diferencias entre sexos es desconocida. Otro factor relacionado con la organicidad es la edad; de forma que, a menor edad de inicio puberal, mayor riesgo de organicidad.
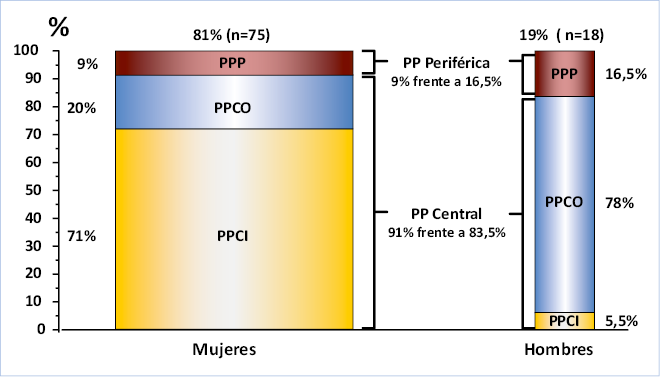
Figura. 3. Distribución por categorías diagnósticas en varones y mujeres con pubertad precoz (PP). La figura muestra los resultados, en porcentajes, de una serie de 93 pacientes recogidos entre 1971 y 1977 en Francia (JC Job y M Pierson. Endocrinología Pediátrica y Crecimiento. Barcelona: Editorial Científico-Médica 1983). PP: pubertad precoz; PPCI: pubertad precoz central idiopática; PPCO: pubertad precoz central de etiología orgánica; PPP: pubertad precoz periférica.
Dentro de las formas de PPC idiopática, alrededor de un 30% son familiares(2). Es probable que la mayoría correspondan a formas más o menos extremas de ACCP; no obstante, se han descrito situaciones de PPC familiares de base monogénica(14). Las primeras que se describieron fueron mutaciones activadoras en el sistema de las kisspeptinas, un grupo de péptidos que resultan del proceso proteolítico del producto del gen KiSS1 (1q32), secretados por neuronas de los núcleos arcuato y anteroventral del hipotálamo, y que se consideran como unos de los principales mediadores del inicio de la pubertad. Estos péptidos, en condiciones normales, incrementan su secreción antes del inicio de la pubertad y se unen a un receptor ligado a las proteínas G de la membrana de las neuronas productoras de GnRH, denominado GPR54 (GPR54 o KiSS1R, en 19p13.3), incrementando considerablemente la amplitud de los picos secretorios de GnRH. Se han descrito dos mutaciones activadoras en KiSS1, una en homocigosis y otra en heterocigosis, y una mutación activadora en el gen que codifica para su receptor (KiSS1R), todas ellas asociadas a una PPC hereditaria, aunque con expresividad familiar variable. Más recientemente, se han descrito, en varias familias con PPC familiar, mutaciones en heterocigosis, con pérdida de función en el alelo paterno, en el gen MKRN3 (15q11.2). El gen MKRN3 está localizado en la región crítica del síndrome de Prader-Willi y sometido a impronta genética (en condiciones normales, solo se expresa el gen de origen paterno) y codifica para una proteína relacionada con la ubiquitinación de proteínas, pero de funcionalidad incierta.
Dentro de las causas orgánicas de PPC, la más frecuente es el hamartoma hipotalámico(15), que puede encontrarse en un 2-28% de los casos de PPC (Fig. 4).

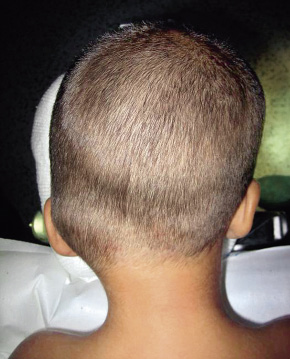
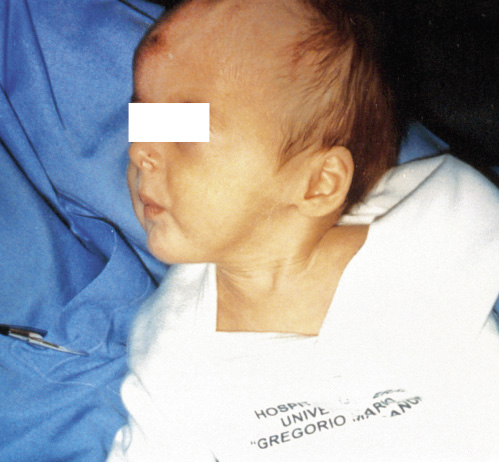
Figura. 4. Pubertad precoz central orgánica por hamartoma hipotalámico. Varón de 18 meses de edad con talla alta (+2 SDS), incremento de la velocidad de crecimiento, aumento del volumen testicular (6 mL de volumen) y del tamaño del pene, hábito atlético y aceleración de la edad ósea (4 años). Testosterona elevada (1,8 ng/mL; VN para la edad < 0,24) con test de LHRH de características puberales (cociente LH/FSH > 1 y pico de LH de 25 mUI/mL). En la RM craneal, se observa una masa retroquiasmática que cuelga del hipotálamo (flecha) y que corresponde al hamartoma hipotalámico. El paciente recibió tratamiento con triptorelina i.m. mensual con frenación completa del eje hipotálamo-hipófiso-gonadal y regresión parcial de los caracteres sexuales secundarios.
Estos tumores son malformaciones congénitas benignas formadas por tejido nervioso desorganizado en el que se incluyen neuronas productoras de GnRH. Aunque se ha especulado que estas neuronas podrían actuar como un generador ectópico de GnRH, el mecanismo responsable de la PPC no está plenamente aclarado. Típicamente, en la RM craneal, los hamartomas aparecen como una masa pedunculada que cuelga del hipotálamo, entre el tuber cinereum y los cuerpos mamilares, justo detrás del quiasma óptico. Pueden ser asintomáticos o asociarse a: PPC, crisis gelásticas (crisis comiciales de risa inmotivada), epilepsia secundariamente generalizada y alteraciones cognitivas y conductuales. La mayoría de estos tumores no crecen o lo hacen muy lentamente y responden al tratamiento habitual con análogos de GnRH; por lo que, la cirugía no suele estar indicada, salvo que condicionen una epilepsia intratable.
Otras múltiples alteraciones del sistema nervioso central (SNC), como: malformaciones, tumores, gliomas hipotalámicos o del quiasma en la neurofibromatosis tipo I, displasia septo-óptica, mielomeningocele e hidrocefalia, entre otras, pueden provocar una pubertad precoz (Tabla I). Se cree que estas lesiones alterarían las señales de inhibición tónica que recibe el hipotálamo, favoreciendo la reactivación del eje HHG.
La irradiación craneal, utilizada en el tratamiento de tumores del SNC o como tratamiento coadyuvante en otras patologías oncológicas, como la leucemia linfoblástica aguda, sobre todo cuando se administra a edades muy precoces, puede predisponer al desarrollo de una PA o PPC. Dosis bajas de radioterapia (18-24 Gy) a menudo se asocian a PPC en niñas; mientras que, dosis por encima de 25 Gy incrementan el riesgo de PPC en ambos sexos, con frecuente asociación a deficiencia de GH, combinación que puede ser especialmente negativa para la talla adulta del paciente. Por encima de los 30 Gy, es frecuente que tras una pubertad temprana/precoz desarrollen una deficiencia de gonadotropinas (hipogonadismo hipogonadotropo). Cuando se administran 50 o más Gy, no suele haber PP, sino una falta de desarrollo puberal secundaria a hipogonadismo hipogonadotropo(15). El diagnóstico de la PPC secundaria a irradiación craneal puede retrasarse o dificultarse debido a sus peculiaridades clínicas: la ausencia/disminución del estirón puberal, por la frecuente deficiencia asociada de GH, y, en el caso de los varones, el escaso o nulo incremento del volumen testicular por efecto de la quimioterapia recibida (hipogonadismo hipergonadotropo).
La neurofibromatosis, al igual que otros síndromes (Tabla I), en ausencia de gliomas del quiasma o hipotalámicos, presenta, también, con mayor frecuencia que la población normal PPC o PA.
Pubertad precoz periférica (PPP)
Es aquella PP en la que el incremento de ES responsable del desarrollo de los caracteres sexuales secundarios no es debido a una activación prematura del eje HHG. Por tanto, no es una verdadera pubertad, sino una pseudopubertad precoz, y los caracteres sexuales secundarios pueden, no solo perder su secuencia de aparición habitual, sino, en algunos casos, ser contrarios al sexo del paciente (contrasexuales).
Los ES implicados en el desarrollo de una PPP pueden ser andrógenos, estrógenos o una mezcla de ambos(2,13), y su origen exógeno (fuentes externas alimenticias, tópicas, orales o parenterales) o endógeno (suprarrenal o gonadal). El eje HHG no solo no está activado, sino que suele estar completamente inhibido por el exceso de ES circulantes, a través de los mecanismos normales de retrocontrol negativo. Las manifestaciones clínicas de la PPP dependen, fundamentalmente, del tipo de ES responsable:
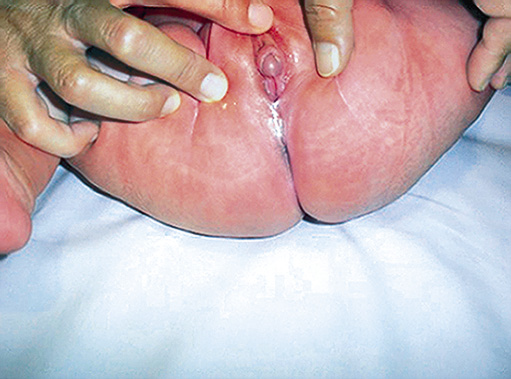
• En las niñas, la pérdida de la secuencia normal en la aparición de los caracteres sexuales secundarios supone que, por ejemplo, el primer signo de desarrollo puberal pueda ser una menstruación, sin un claro desarrollo mamario previo ni aceleración del crecimiento. El hallazgo de hiperpigmentación areolar precoz con desarrollo mamario todavía incompleto es sugerente de rápida y marcada elevación de los niveles séricos de estrógenos (Fig. 5).

Figura. 5. Pubertad precoz periférica secundaria a tumor ovárico secretor de estrógenos. Niña de 14 meses que consultó por telarquia bilateral de, aparentemente, solo 15 días de evolución, con aceleración de la velocidad de crecimiento (talla en +5 SDS) y sangrado vaginal dos días antes de la consulta. En la exploración, se observó una telarquia bilateral (T3 de Tanner) con hiperpigmentación areolar (dato clínico sugerente de alta concentración de estrógenos), sin pubarquia ni axilarquia. Los niveles de estradiol se encontraron muy elevados (230 pg/mL; VN prepuberales < 10). En la ecografía, masa ovárica izquierda de 30 x 20 mm, que se confirmó en la RM pélvica (flecha en la figura). El estudio anatomopatológico estableció el diagnóstico de quiste luteínico. Regresión posterior de los caracteres sexuales secundarios tras la cirugía.
La presencia de un sangrado vaginal en ausencia completa de telarquia es más sugerente de una causa local (agresión sexual, cuerpo extraño o tumor vaginal) que de una verdadera PP. Un acné severo, de rápida progresión y, especialmente, el agrandamiento del clítoris (virilización) debe hacernos sospechar la presencia de un tumor productor de andrógenos. El vello pubiano que aparece precozmente y progresa lentamente, en ausencia de telarquia ni de otros signos de virilización, no sugiere PP central ni periférica, sino un incremento leve de la producción suprarrenal de andrógenos, habitualmente una adrenarquia prematura aislada (hiperplasia suprarrenal congénita de presentación tardía o una variante de la normalidad).
• En el caso de los varones, es muy característico de la PPP, el desarrollo progresivo de signos de virilización, como sería el incremento del tamaño del pene, sin un aumento significativo del tamaño testicular. En algunos casos (testotoxicosis, restos adrenales testiculares, tumores productores de gonadotropina coriónica –HCG–, etc.) el volumen testicular puede incrementarse ligeramente (4-8 mL), pero, en cualquier caso, es un volumen inadecuado para el grado de desarrollo de los caracteres sexuales secundarios. Al igual que en las niñas, el vello pubiano moderado que aparece precozmente y progresa lentamente, en ausencia de agrandamiento testicular o del pene, no sugiere PP central ni periférica, sino adrenarquia prematura aislada. El desarrollo de signos feminizantes (ginecomastia marcada) es excepcional, pero puede producirse en el contexto de exposición a una fuente externa de estrógenos o en raros casos de tumores testiculares (tumor de células de Sertoli asociado al síndrome de Peutz-Jegher) o adrenales productores de estrógenos.
Las causas que pueden determinar una PPP quedan reflejadas en la tabla I. Las dos entidades nosológicas más características responsables de PPP son: el síndrome de McCune-Albright y la testotoxicosis.

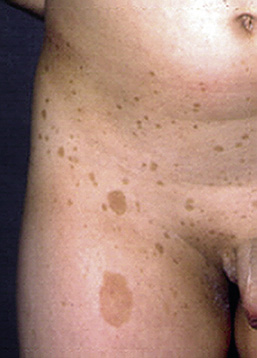
El síndrome de McCune-Albright (SMA) es una enfermedad rara, con una prevalencia estimada de 1:100.000-1.000.000, más frecuente en niñas, aunque puede darse en ambos sexos(16). Originalmente, fue definido clínicamente por la tríada de: displasia fibrosa poliostótica, manchas de color “café con leche” de bordes irregulares (“en costa de Maine”) y PPP, debida al desarrollo de quistes ováricos autónomos secretores de estrógenos. Posteriormente, se ha visto que otras endocrinopatías hiperfuncionantes pueden estar presentes, como: hipertiroidismo, gigantismo hipofisario, hipercortisolismo o raquitismo hipofosfatémico, entre otras. Se debe a una mutación activadora postcigótica en el gen de la subunidad alfa de la proteínas G de la membrana (GNAS1; 20q13.32), que se produce temprano en la embriogénesis y determina un mosaicismo que puede afectar, de forma variable, a tejidos endocrinos (gónadas, tiroides, adrenales, hipófisis y paratiroides) y no endocrinos (timo, bazo, páncreas, riñón, corazón, etc.). Debido a ello, la expresividad clínica puede ser, también, muy variable y el diagnóstico, en algunos casos, difícil.
La testotoxicosis o PP familiar del varón es una forma de PPP limitada a los varones, debida a una mutación activadora, de herencia autosómica dominante (esporádica o familiar) en el receptor de LH (LHCGR; 2p16.3), que ocasiona una activación autónoma de las células de Leydig. Suele ponerse de manifiesto a los 2-4 años de edad con la aparición de: signos puberales, virilización y aceleración del crecimiento que conduce a una talla final baja por cierre precoz de los cartílagos de crecimiento. En niñas, estas mutaciones no producen PPP; ya que, es necesaria la presencia de LH y FSH para la producción de estrógenos.
Los quistes foliculares ováricos secretan estrógenos de forma transitoria, lo que puede ocasionar desarrollo mamario y, en ocasiones, cuando la producción estrogénica cae, sangrado vaginal esporádico. Los quistes que producen esta sintomatología suelen ser relativamente grandes y pueden ser recurrentes, lo que puede acelerar la maduración ósea y favorecer el desarrollo de una PA o una PPC secundaria. Además, en los que alcanzan un mayor tamaño, puede favorecerse la torsión ovárica y la necesidad de tratamiento quirúrgico.
La exposición a ES exógenos (disruptores endocrinos) puede determinar una PPP iso o contrasexual, dependiendo de su acción hormonal y del sexo del paciente. Una de las hipótesis propuestas para explicar la alta incidencia de PA/PPC en niñas adoptadas de países en vías de desarrollo sería la de los disruptores endocrinos. En estas niñas se han encontrado frecuentemente niveles elevados de pesticidas derivados del DDT (diclorodifenildicloroetano), productos que siguen utilizándose en estos países como insecticidas en el ámbito rural. Según esta hipótesis, la exposición crónica a la actividad estrogénica de estos productos podría madurar el hipotálamo al tiempo que suprimiría su actividad. La eliminación de la exposición al migrar a países desarrollados, donde estos pesticidas están prohibidos, supondría el incremento de la liberación de GnRH y el inicio de la pubertad.
El hipotiroidismo primario severo y de larga duración puede, aunque raramente, presentarse como una PP (síndrome de Van Wyk-Grumbach) a través de mecanismos no completamente aclarados, pero que podrían afectar tanto a la hipófisis como a la gónada. Clínicamente, las niñas suelen presentar telarquia con galactorrea, por aumento concomitante de prolactina por acción de TRH (hormona hipotalámica estimulante de la secreción de TSH), y sangrados vaginales recurrentes; por su parte, los niños suelen mostrar incremento prematuro del volumen testicular. Estos signos puberales desaparecen con el tratamiento con L-tiroxina. La peculiaridad clínica de esta rara forma de PP es que, a diferencia de las demás, cursa con enlentecimiento del crecimiento y retraso de la EO.
La hiperplasia suprarrenal congénita, especialmente en su forma clásica, si está insuficientemente tratada, puede producir un PPP isosexual en el varón y contrasexual en la niña. De forma característica, en el varón, el tamaño testicular permanece prepuberal; no obstante, en algunos casos, pueden existir restos (habitualmente bilaterales) de tejido adrenal en los testículos y crecer por el efecto de la ACTH aumentada, requiriendo diagnóstico diferencial con una PPC o con tumores testiculares de otra extirpe anatomopatológica.
Tumores ováricos, testiculares o adrenales productores de ES, son causas raras de PPP iso o contrasexual. Los tumores ováricos (sobre todo los de células de la granulosa/teca) frecuentemente causan síntomas locales (dolor, distensión, ascitis, efecto masa, etc.) y suelen secretar estrógenos, aunque en ocasiones producen andrógenos y virilización. El diagnóstico en las formas típicas se basa en el hallazgo ecográfico de una masa sólida o sólido-quística en el ovario, con niveles séricos elevados de estradiol y suprimidos de LH/FSH (Fig. 5). Los tumores testiculares más frecuentemente asociados a PPP son los derivados de las células de Leydig, que suelen ser benignos en la infancia y presentarse con signos de virilización, incremento del tamaño de uno de los testículos (nódulo, frecuentemente palpable) y niveles séricos elevados de testosterona. Los tumores adrenales (adenomas y adenocarcinomas) suelen producir andrógenos (virilización) y cortisol (síndrome de Cushing); si bien, excepcionalmente pueden producir también estrógenos y feminización.
La resistencia generalizada a glucocorticoides es una rara enfermedad autosómica dominante, debida a mutaciones en el gen del receptor de los glucocorticoides (GCCR; en 5q31.3), que conlleva el aumento compensador de las concentraciones circulantes de la hormona adrenocorticotrópica (ACTH), lo que incrementa la producción de esteroides adrenales con actividad mineralocorticoide y/o androgénica, e incrementa la excreción urinaria de cortisol libre sin ninguna evidencia clínica de hipercortisolismo.
Tumores productores de gonadotropina coriónica (HCG), de efecto biológico similar a la LH, inducen en los niños la producción por las células de Leydig de testosterona y un incremento moderado del volumen testicular(15). En las niñas, estos tumores no producen PP; ya que, que es necesaria la presencia de ambas gonadotropinas, LH y FSH, para el desarrollo de los folículos ováricos. Los hepatoblastomas son los tumores más frecuentes productores de HCG, pero esta puede también ser producida, entre otros, por: pinealomas, germinomas intracraneales, coriocarcinomas o tumores de células germinales (testiculares o extratesticulares). El hallazgo de un tumor extratesticular de células germinales, especialmente mediastínico, obliga a descartar un síndrome de Klinefelter, donde la frecuencia de este tipo de tumores es 50 veces mayor que en el resto de la población. La presencia de marcadores tumorales alfa-fetoproteína y b-HCG) puede ser útil en el diagnóstico de este tipo de tumores.
Pubertad precoz mixta o combinada
Se habla de PP mixta o combinada, cuando una PPP desencadena secundariamente una PPC.
Niños expuestos a altos niveles séricos de ES como consecuencia de una PPP (hiperplasia suprarrenal congénita pobremente controlada, SMA…) pueden desarrollar una posterior PPC. Se ha especulado que los ES podrían “impregnar” el hipotálamo, causando la maduración del eje HHG y la puesta en marcha de la PPC; o bien que, el hipotálamo, acostumbrado a una inhibición por niveles muy elevados de ES, al disminuir estos como resultado de un tratamiento efectivo de la PPP, se reactivara, poniendo en marcha la PPC. En la mayoría de los casos, la PPC solo se inicia si la EO es superior a los 10 años.
Evaluación diagnóstica
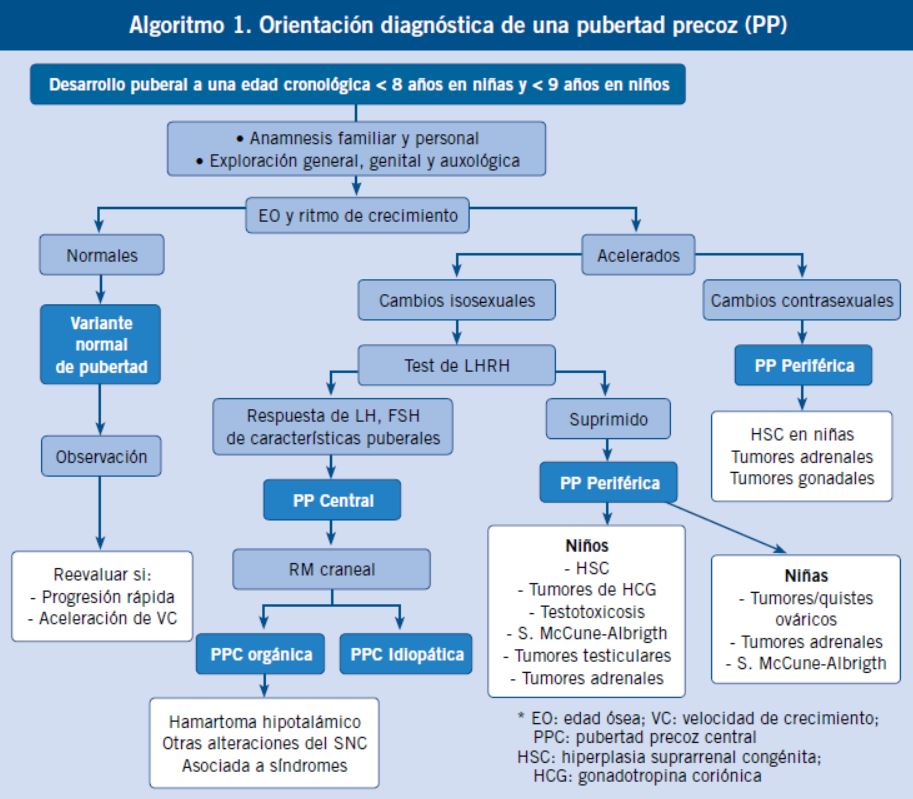
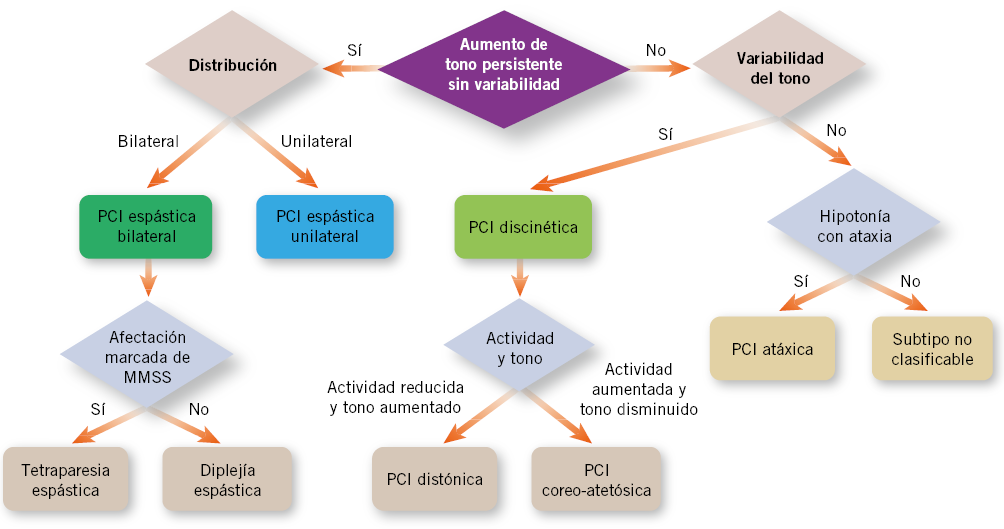
La aparición antes de los 8 años en las niñas y de los 9 años en los niños de los caracteres sexuales secundarios, puede ser la manifestación de una PP (central o periférica y de causa orgánica o idiopática), pero con más frecuencia se tratará de una variante normal, benigna y no progresiva, de pubertad, que no requerirá habitualmente tratamiento (Algoritmo 1). Por ello, un diagnóstico correcto puede evitar costosos y prolongados tratamientos no exentos de potenciales efectos secundarios. La evaluación diagnóstica de estos pacientes conlleva una anamnesis y exploración completas, con énfasis en determinados aspectos, y un número limitado de pruebas complementarias básicas(9).
Anamnesis detallada
Debe interrogarse sobre la edad y orden de aparición de los caracteres sexuales secundarios, así como sobre las características de su progresión (rápida, lenta, cíclica). En las niñas, la evolución cíclica de la telarquia es muy sugerente de quistes foliculares recurrentes. La aparición precoz de vello pubiano y/o axilar sin otros signos de virilización (clitoromegalia o aumento del tamaño del pene, hirsutismo, marcada aceleración de la EO, aumento de la masa muscular…) sugiere adrenarquia prematura (variante de la normalidad) y no PP, y puede acompañarse de otros signos de androgenización leve-moderada, como: aceleración de la EO de 1-2 años, olor corporal de características puberales, presencia de comedones o acné leve y aumento de grasa en el pelo. Deben recogerse y llevarse a la gráfica de crecimiento los datos de la evolución de la talla, el peso y, sobre todo, de la VC. Debe interrogarse, también, sobre posibles signos de hipertensión intracraneal (cefalea, vómitos o trastornos visuales) sugerentes de patología orgánica intracraneal. Los antecedentes familiares (padres, hermanos y familiares próximos) de PA o PP, así como de patologías hereditarias que puedan modificar el tempo normal de la pubertad deben ser recogidas (hiperplasia suprarrenal congénita, testotoxicosis, resistencia a glucocorticoides…).
Exploración física
Se deben recoger cuidadosamente los parámetros antropométricos (talla, peso y proporciones corporales), el estadio puberal de Tanner, así como otros datos sugerentes de desarrollo puberal, virilización o feminización: olor corporal, acné, ginecomastia, galactorrea, pigmentación areolar, estrogenización de la mucosa vaginal, leucorrea, volumen y simetría testicular, tamaño del clítoris, etc. Debe recogerse, también, la presencia, localización y características de manchas cutáneas sugerentes de neurofibromatosis o SMA.
Edad ósea (EO)
Suele ser la primera prueba complementaria a realizar ante la sospecha de una PP; ya que, en condiciones normales, el grado de desarrollo puberal se correlaciona mejor con la EO (r = 0,82) que con la edad cronológica (r = 0,72). Así, por ejemplo, en las niñas, el desarrollo mamario se inicia a una EO media de 10,75 años y la menarquia se produce a una EO media de 13 años, con una varianza para la EO que es la mitad de la correspondiente a la EC. Además, trastornos que aceleran la EO (hiperplasia suprarrenal congénita…) se asocian a PA y los que la retrasan (deficiencia de GH, hipotiroidismo, patología crónica…) a pubertad retrasada. En las PPC idiopáticas, la EO está típicamente acelerada al menos un 20% por encima de la edad cronológica (˜2 SDS) y, en el caso de las niñas, próxima, habitualmente, a los 10-11 años. Por el contrario, en las PP de causa orgánica, la aceleración de la EO es más variable y depende de la duración y grado de exposición previa a los ES. También, la EO es útil para realizar predicciones de talla adulta y valorar la posible repercusión de la PP sobre la talla final, tanto en el momento del diagnóstico como a lo largo del seguimiento del paciente; no obstante, hay que tener en consideración que la fiabilidad de estas predicciones, en condiciones normales es escasa y, en los pacientes con PP, cuando la EO está muy acelerada, todavía menor y con tendencia a sobrevalorar las expectativas de talla adulta.
Determinaciones hormonales
La presencia de niveles séricos elevados de estradiol o testosterona sería, lógicamente, lo primero a demostrar ante una sospecha de PP; sin embargo, su determinación puede no ser de mucha utilidad en las fases iniciales de la pubertad, ya que, se sitúan con frecuencia por debajo del límite de detección de los inmunoanálisis convencionales, especialmente en el caso del estradiol.
La determinación en suero de andrógenos suprarrenales o de sus precursores, especialmente: sulfato de dehidroepiandrosterona (SDHEA), ∆4-androstendiona y 17-OH-progesterona, puede ser de utilidad en aquellas situaciones clínicas sugerentes de incremento de andrógenos de posible origen adrenal, como sería el caso de tumores suprarrenales o de la hiperplasia suprarrenal congénita; en este último caso, puede ser necesaria la estimulación previa con ACTH (test de ACTH) para descartar formas de presentación tardía.
La prueba hormonal más importante en el diagnóstico de PP es la determinación de los niveles séricos de gonadotropinas (LH y FSH) tras estímulo con 100 µg/m2 de LHRH (test de LHRH) o con un análogo de GnRH (test de GnRHa)(17). Esta prueba nos permitiría distinguir, al menos teóricamente, una PPC (patrón de respuesta puberal: claro incremento de LH y FSH, con predominio de LH: cociente LH/FSH > 1) de una variante de la pubertad no progresiva (patrón de respuesta prepuberal: escaso o nulo incremento de LH y FSH con predominio de FSH: LH/FSH <1) y de una PPP (secreción de LH/FSH inhibida). No obstante, su interpretación no siempre es sencilla; ya que, los puntos de corte diagnósticos (pico de LH) no son claros y dependen en gran medida de la sensibilidad y fiabilidad del inmunoanálisis empleado. Con los inmunoanálisis más modernos, el punto de corte para una respuesta prepuberal de LH sería de alrededor de 5 mUI/mL. Por otra parte, en la situación más frecuente en la práctica clínica, como es el caso de las niñas con inicio de desarrollo mamario entre los 7 y 8 años (70% de las telarquias prematuras), la diferenciación entre una PPC idiopática (susceptible de tratamiento) y una telarquia prematura aislada (variante de la normalidad que no precisa tratamiento) puede ser muy difícil y, a veces, solo un seguimiento estrecho puede diferenciarlas (Tabla II). En estos casos, es frecuente el hallazgo de un patrón de respuesta de LH y FSH a LHRH intermedio entre lo que hemos denominado puberal y prepuberal (incremento moderado en los picos de secreción de LH y FSH con predominio de FSH o solo un claro incremento de FSH); de hecho, algunos autores consideran que estas formas de telarquia prematura de evolución variable (pueden regresar, mantenerse sin progresar o progresar lentamente) serían parte de un continuum en la activación del eje HHG y que entre un 15-20% de ellas terminan evolucionando hacia una PP.
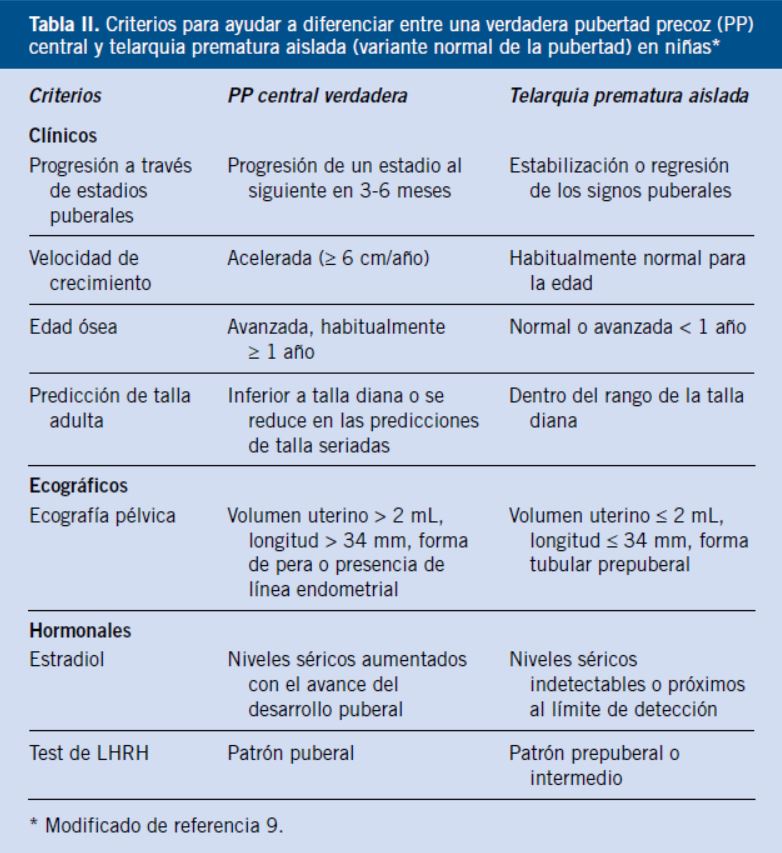
En los últimos años, la disponibilidad de inmunoensayos más sensibles y fiables para la determinación de gonadotropinas ha hecho que se plantee la posibilidad de determinar solo los niveles basales de gonadotropinas, en concreto de LH, para el diagnóstico o, al menos, el cribado de una PPC. Niveles basales de LH = 5 mUI/mL serían sugerentes de PPC, gonadotropín-dependiente; no obstante, el solapamiento en los resultados entre los pacientes prepuberales y aquellos que se sitúan en fases iniciales de la pubertad y la multiplicidad de inmunoanálisis utilizados, desaconsejan, al menos de momento, semejante práctica.
Pruebas de imagen
Una RM craneal, para evaluar la anatomía de la región hipotálamo-hipofisaria y descartar patología orgánica, debería realizarse si se demuestra una activación precoz del eje HHG, especialmente en varones, donde el riesgo de patología orgánica es claramente superior (40-90% en varones frente a un 8-33% en niñas)(9). En las niñas, cuando la pubertad se inicia entre los 6 y los 8 años y sin sintomatología neurológica, el riesgo de patología orgánica es muy escaso (2-7%) y se discute la conveniencia de realizar una RM craneal; no obstante, la mayoría de los centros continúa realizándola.
La ecografía abdómino-pélvica puede, además de descartar la presencia de tumoraciones (suprarrenales, ovario, hígado, etc.) responsables de una PPP, permitirnos, en el caso de las niñas, valorar el tamaño ovárico y uterino. Un volumen ovárico (longitud x anchura x altura x 0,5233) de <1 mL es claramente prepuberal, pero los límites para considerarlo puberal, varían entre 1 y 3 mL, según los autores. La presencia de pequeños quistes (<9 mm), en ocasiones múltiples (2 a 4), es un hallazgo frecuente y normal en niñas prepuberales (50-80%). Típicamente, no suelen producir cantidades significativas de estrógenos, aunque en ocasiones pueden elevar transitoriamente sus niveles séricos, determinando un desarrollo mamario transitorio. Un incremento del volumen (>2 mL), una relación cuerpo/cuello mayor de 1 o la presencia de línea endometrial, son signos sugerentes de niveles elevados de estrógenos circulantes y, por tanto, de inicio puberal.
La ecografía testicular puede ser de utilidad en varones con pubertad precoz periférica, especialmente si existe asimetría testicular, para detectar tumores o restos adrenales, en ocasiones no palpables.
Otros estudios
Dependiendo del caso y de los resultados previos, otros estudios pueden estar indicados: función tiroidea (hipotiroidismo en el síndrome de Van-Wyk-Grumbach o posible hipertiroidismo en el SMA), mapa óseo (lesiones de displasia fibrosa en SMA), marcadores tumorales (b-HCG, alfa-fetoproteína), estudios moleculares (detección de mutaciones conocidas), etc.
Tratamiento
El tratamiento de la PP central lo que pretende es, según los casos: revertir, detener o, al menos, enlentecer el desarrollo de los caracteres sexuales secundarios, conservar el potencial de crecimiento y evitar las consecuencias psicosociales y conductuales de una pubertad temprana.
Pubertad precoz central
En este caso, el tratamiento busca frenar o suprimir la activación del eje HHG. El tratamiento de elección son los análogos de GnRH (GnRHa) de liberación sostenida (depot). En los casos en los que exista una causa orgánica, deberá hacerse tratamiento etiológico si es posible, aunque este, rara vez tiene efecto sobre la evolución de la pubertad.
La administración de GnRHa de liberación sostenida produce, tras una breve estimulación de la liberación de gonadotropinas, una prolongada desensibilización de los receptores hipofisarios de GnRH, con inhibición de la secreción de LH/FSH y, como consecuencia, de la producción y liberación de ES. Los más utilizados son: la triptorelina depot, a la dosis de 80-100 µg/kg, y el acetato de leuprolerina, a la dosis de 150-200 µg/kg, que se administran, ambos, por vía intramuscular cada 25-28 días. Más recientemente, se han introducido preparados depot de una duración de 3 meses, pero la experiencia en su utilización en la PPC es menor y no se han aprobado en nuestro país para esa indicación(9). Tampoco han sido aprobados en Europa, los implantes subcutáneos de histrelina, un análogo de GnRH con efecto inhibidor de la secreción de LH y FSH superior a un año(9,18).
La utilización de los GnRHa en los casos de PPC idiopática con inicio a una edad próxima a los límites considerados normales es controvertida; ya que, los efectos beneficiosos del tratamiento sobre la talla final son, en la mayoría de los pacientes, escasos o nulos. Por ello, no existe un consenso internacional(19) y la indicación de tratamiento se establece de forma individualizada, teniendo en consideración factores psicosociales (repercusión psicológica, familiar, social y conductual) y auxológicos (expectativas de crecimiento, edad ósea, rapidez de progresión de la EO y de los caracteres sexuales secundarios). Tras el inicio de la terapia, la VC puede disminuir considerablemente; en estos casos, algunos estudios han sugerido que la adición de GH al tratamiento con GnRHa podría mejorar la VC y las expectativas de talla final; no obstante, no existen suficientes estudios controlados que demuestren la seguridad y eficacia de esta asociación, para poder establecer una clara indicación.
Otro aspecto controvertido sería el momento más adecuado para suspender el tratamiento con GnRHa. Aunque no existe consenso, en el caso de las niñas, se recomienda que se haga a una edad cronológica de ˜11 años y EO de ˜12-12,5 años; ya que, por encima de estas edades podría no solo no mejorar, sino incluso empeorar las expectativas de talla adulta. En los varones, la experiencia es muy escasa y suele recomendarse, sin mucha base científica, la suspensión del tratamiento alrededor de los 12 años de edad cronológica y de los 13-13,5 años de EO(17). Pocas semanas o meses después de la suspensión, la pubertad progresa y se recupera la respuesta puberal al estímulo con GnRH. En las niñas, la menarquia se produce, habitualmente, entre 6 y 18 meses después.
Los resultados del tratamiento con GnRHa sobre la talla final varían de unos pacientes a otros; aunque, en general, la mayoría de ellos alcanzan una talla final en el rango bajo de su talla diana y con escasos efectos secundarios locales (abscesos estériles, infecciones…) y generales (cefalea, sofocos…).
Pubertad precoz periférica
Los objetivos del tratamiento de la PPP son similares a los de la PPC; si bien, en este caso, los GnRHa son ineficaces y lo que se utilizan son fármacos que inhiben directamente la producción de ES o su acción sobre los órganos diana.
El tratamiento de la PPP será etiológico, en aquellos casos en los que sea posible: quirúrgico (extirpación del tumor ovárico, testicular, suprarrenal o productor de HCG), o médico (tratamiento con hidrocortisona en la hiperplasia suprarrenal congénita, quimioterapia en los suprarrenalomas malignos metastásicos, etc.). En el resto de los casos, el tratamiento será sintomático, con fármacos que, como: ketoconazol, acetato de ciproterona, espironolactona, flutamida, testolactona, letrozole y anastrozole, entre otros, son capaces, por diferentes mecanismos, de reducir o inhibir la producción de ES o de bloquear su acción en los órganos diana(18). En general, estos tratamientos no son demasiado eficaces, rara vez se alcanza con ellos una detención completa en el desarrollo de los caracteres sexuales secundarios y una adecuada talla final y, en algunos casos, sus efectos secundarios son importantes.
Pubertad retrasada (PR)
Concepto y morbilidad
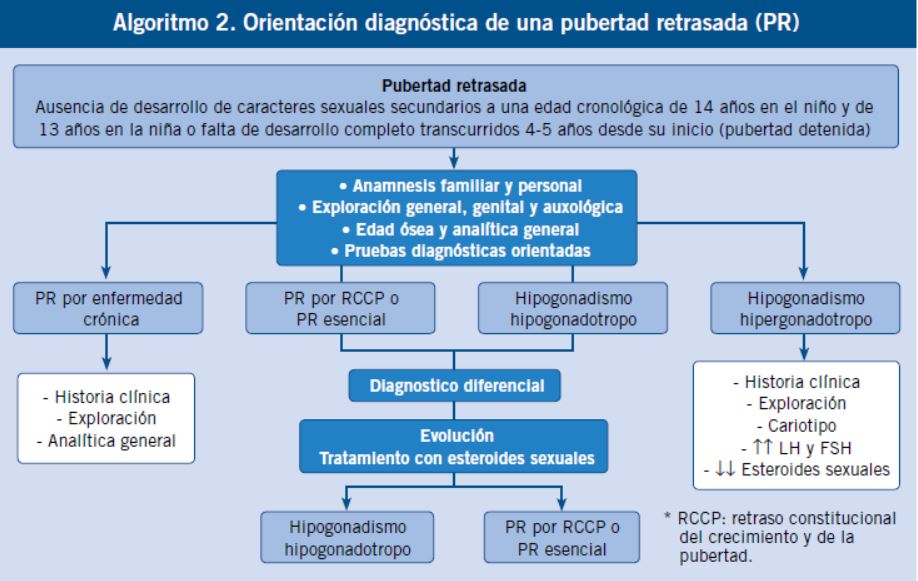
No existe un consenso internacional que establezca con claridad el concepto de pubertad retrasada; de hecho, el término engloba varios conceptos: pubertad retrasada propiamente dicha, pubertad detenida y ausencia de pubertad o infantilismo sexual(20).
Se considera la “pubertad retrasada”, cuando no se ha iniciado el desarrollo puberal a una edad 2-2,5 SDS por encima de la edad media de su aparición en la población de referencia(21,22). A efectos prácticos, la ausencia de telarquia en las niñas a una edad de 13 años y la ausencia de incremento del volumen testicular (=4 mL) a los 14 años (Fig. 2). Se habla de “pubertad detenida”, cuando la pubertad, iniciada tardíamente o no, no llega a completarse y transcurren más de 4-5 años entre su inicio y el desarrollo gonadal completo en los varones o la menarquia en las mujeres. Por último, se habla de “ausencia de pubertad” o “infantilismo sexual”, cuando la pubertad no llega a iniciarse.
La PR, especialmente en los varones, puede conllevar importantes repercusiones psicosociales que son, con frecuencia, el motivo por el que el paciente acude a la consulta. En una época de extremada sensibilidad y labilidad psicológica, donde la imagen corporal es muy importante para la autoestima del sujeto, la falta de desarrollo puberal y la talla baja, que frecuentemente acompaña al retraso puberal, les hace con frecuencia objeto de burlas y vejaciones por parte de sus compañeros de edad, al tiempo que son relegados de las actividades deportivas y sociales, especialmente de aquellas que conllevan una interrelación con el otro sexo. Como consecuencia, es frecuente que los pacientes desarrollen una mala imagen de sí mismos, baja autoestima, conductas depresivas y tendencia al aislamiento y a una cierta agresividad, alteraciones que, en ocasiones, pueden desembocar en fracaso escolar y en problemas familiares y sociales graves. Por otra parte, la PR puede tener, también, repercusiones físicas, sobre la masa ósea (masa ósea disminuida por el retraso en la aparición de los ES) y auxológicas: alteración de las proporciones corporales (extremidades más largas con relativo acortamiento del segmento superior) y pérdida de talla final. Por motivos desconocidos, un pequeño porcentaje de los pacientes con PR pueden no alcanzar una talla adulta adecuada a su contexto familiar(23).
Etiopatogenia y clínica
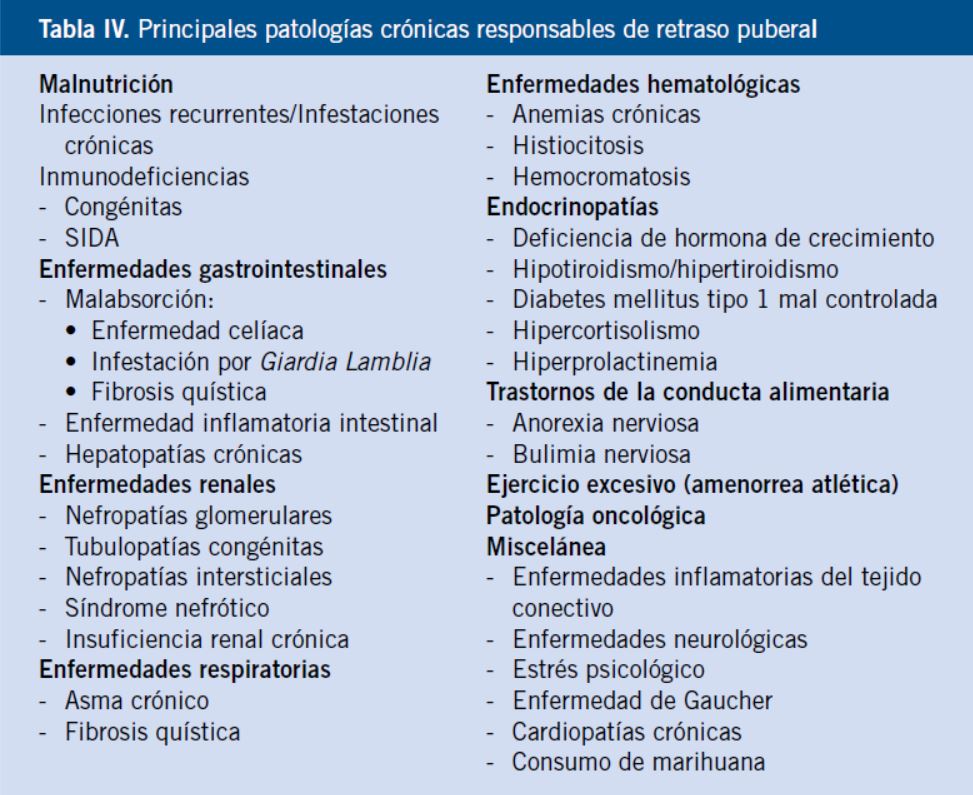
Las causas que pueden provocar una PR son múltiples; no obstante, pueden ser fácilmente divididas en cuatro categorías (Tabla III):
• Retraso puberal simple. Englobaría aquellos retrasos temporales en el inicio puberal de causa desconocida (idiopáticos) o debidos a factores constitucionales o genéticos (“retraso constitucional del crecimiento y de la pubertad” –RCCP–).
• Retraso puberal secundario a enfermedades crónicas. Serían el resultado de trastornos funcionales en el eje HHG secundarios a múltiples patologías crónicas o endocrinopatías (hipogonadismo hipogonadotropo funcional o transitorio).
• Hipogonadismos hipogonadotropos (HHipo). Serían aquellos pacientes que fracasan en su desarrollo puberal por anomalías en los mecanismos de control hipotálamo-hipofisarios de la pubertad.
• Hipogonadismos hipergonadotropos (HHiper). Serían aquellos pacientes que fracasan en su desarrollo puberal por fallo gonadal primario.
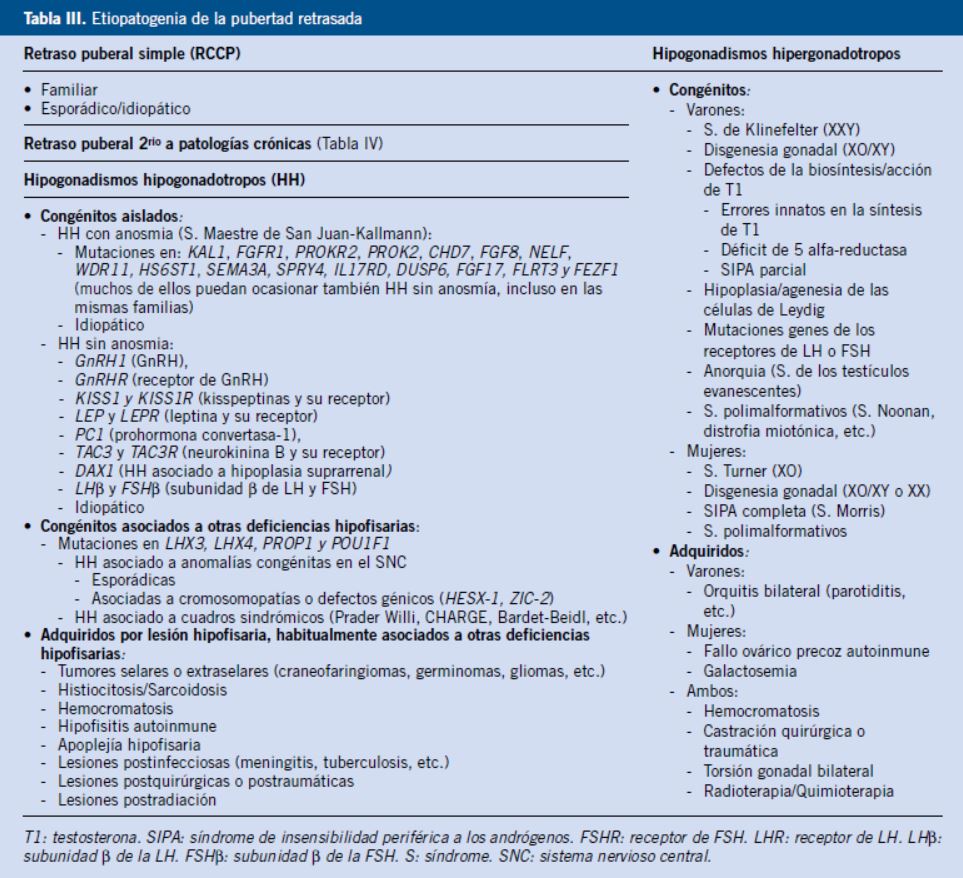
La PR es una situación frecuente, aunque su incidencia real es difícil de establecer. Estadísticamente, debería afectar, al menos, a un 2-3% de la población. También, debería tener una incidencia similar en ambos sexos, pero, y al contrario de lo que ocurre con la PP, se presenta especialmente en varones (˜70%). En ambos sexos, la causa más frecuente es el simple retraso en su inicio, de etiología familiar o idiopática, que representaría alrededor del 60% de los casos de PR en varones y del 30% en mujeres (Fig. 6).
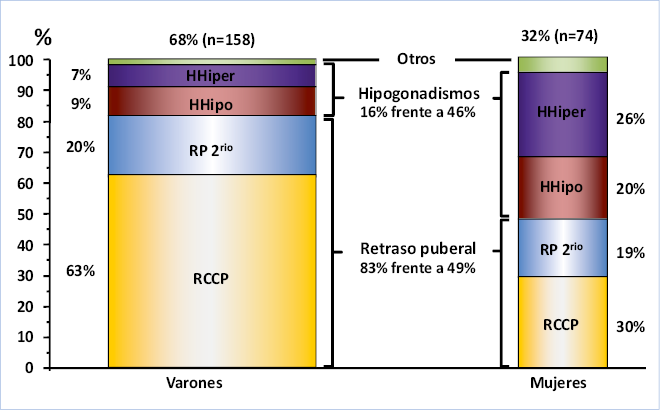
Figura. 6. Distribución por categorías diagnósticas en varones y mujeres con pubertad retrasada. La figura muestra los resultados, en porcentajes, de una serie de 232 casos, recogidos en Boston, EE.UU. (IL Sedlmeyer y MR Palmert. J Clin Endocrinol Metab 2002; 87: 1613-1620). RCCP: retraso constitucional del crecimiento y de la pubertad; RP2rio: retraso puberal secundario a patología crónica (hipogonadismo hipogonadotropo transitorio); HHipo: hipogonadismo hipogonadotropo permanente; HHiper: hipogonadismo hipergonadotropo permanente; Otros: etiología no clasificada claramente.
Es importante destacar, en las niñas, la gran importancia porcentual de los HHiper, ligada a la elevada incidencia del síndrome de Turner (45,X0 y sus variantes), que probablemente ha descendido en los últimos años como consecuencia de que muchas de estas anomalías cromosómicas terminan en interrupción voluntaria del embarazo, y, en ambos sexos, el incremento, en las últimas décadas, de los retrasos puberales secundarios a patología crónica, resultado de que los avances diagnóstico-terapéuticos han permitido que un mayor número de pacientes con patologías crónicas alcancen la edad puberal. Los hipogonadismos, dependiendo de la causa, de que sean parciales o totales, y del momento de su aparición, pueden determinar manifestaciones clínicas variables: retraso puberal, detención del desarrollo puberal, infantilismo sexual, ambigüedad genital, infertilidad, amenorrea secundaria, etc.
Retraso constitucional del crecimiento y de la pubertad
El retraso puberal simple de etiología idiopática o familiar (RCCP) es la causa más frecuente de PR y asociado o no a un componente de talla baja familiar, la causa más frecuente de talla baja en la infancia.
El RCCP es más frecuente en varones (Fig. 6), que llegan a consultar por este problema en proporciones de 9:1. Se considera una variante cronológica de la normalidad y, aunque puede presentarse de forma esporádica o idiopática, lo hace habitualmente en un contexto familiar de maduración tardía (60-90% de los casos). El patrón de herencia es sugerente de una herencia autosómica dominante. Serían niños normales con un patrón madurativo familiar más lento que la media de la población. El cuadro clínico se caracteriza por un hipocrecimiento de inicio postnatal, con un patrón de crecimiento característico, que se acompaña de un retraso en la maduración ósea y en el inicio de la pubertad de 2 a 4 años. Son niños que hasta los 12-18 meses de edad crecen normalmente. A partir de ese momento y hasta los 3-4 años (fenómeno de canalización del crecimiento), experimentan una caída en el ritmo de crecimiento que les lleva a situarse en un carril de crecimiento inferior al que les correspondería para su contexto familiar, con frecuencia próximo o por debajo del percentil 3. Cuando existe un componente familiar importante de talla baja, el hipocrecimiento puede ser muy severo, con tallas por debajo de –3 SDS. A partir de los 3-4 años, los niños crecen a un ritmo normal, aunque habitualmente por debajo del percentil 50 de VC, y tienden a mantener el percentil de talla. Cuando alcanzan la edad en la que habitualmente se produce la pubertad, se observa un nuevo periodo de desaceleración del ritmo de crecimiento, lo que se conoce como “depresión prepuberal de la VC”, que los aleja nuevamente de los percentiles normales hasta que se inicia el estirón puberal. Este se produce de forma normal, aunque tardíamente, y el pico de VC suele ser menor; de forma que, es un estirón menos aparente y se ganan menos centímetros que cuando este se produce a una edad media o temprana, compensándose así el mayor número de años de crecimiento. La talla final se alcanza también tardíamente y suele ser acorde con el contexto familiar, aunque, en alrededor del 15% de estos pacientes, por causas desconocidas, la talla final se sitúa por debajo de lo esperable para su contexto familiar.
Retraso puberal secundario a patología crónica
Prácticamente todas las enfermedades crónicas, si son lo suficientemente importantes en gravedad y duración, repercuten de un modo negativo sobre el crecimiento y la maduración (Tabla IV).
Los mecanismos fisiopatológicos que median el retraso puberal en las patologías crónicas son múltiples y varían dependiendo de la enfermedad y de la terapia empleada(24). En la mayoría de los casos, un cierto componente de malnutrición (exceso de pérdidas, disminución de ingesta o aumento de necesidades) suele estar presente, lo que condiciona unas modificaciones hormonales de adaptación que afectan, sobre todo, al eje GH-IGF-1 (resistencia parcial a la acción de la GH, retraso de crecimiento y de la maduración ósea) y al eje HHG (retraso puberal secundario a hipogonadismo hipogonadotropo funcional transitorio). Ambos fenómenos, el hipocrecimiento y la PR se consideran como mecanismos de adaptación a la escasez, absoluta o relativa, de nutrientes. Otros mecanismos fisiopatológicos implicados en la PR dependen de la enfermedad responsable, como son, entre otros: trastornos hidroelectrolíticos, hipoxia crónica, citoquinas inflamatorias, disfunciones hormonales, problemas psicopatológicos y tratamientos crónicos (corticoterapia, transfusiones repetidas, quimioterapia…).
En la mayoría de los casos, el cuadro clínico remeda clínica y hormonalmente al RCCP (hipocrecimiento con retraso de la maduración ósea y del inicio puberal con niveles bajos de gonadotropinas y ES). En otras ocasiones, cuando la enfermedad se manifiesta una vez iniciada la pubertad, puede condicionar una “pubertad detenida” (p. ej., anorexia nerviosa), con posterior progresión de los caracteres sexuales secundarios si la enfermedad mejora. Más raramente, algunas patologías crónicas, por la propia enfermedad (hemocromatosis, galactosemia) o por la terapia empleada (quimioterapia, radioterapia, cirugía), pueden a la larga determinar hipogonadismos hipo o hipergonadotropos definitivos con ausencia de desarrollo puberal.
Hipogonadismos hipogonadotropos (HHipo)
Los HHipo son responsables de alrededor del 10% de los retrasos puberales. Se caracterizan por niveles muy disminuidos o ausentes de las gonadotropinas circulantes, LH y FSH. Pueden ser debidos a defectos congénitos o adquiridos y presentarse aislados o asociados a otras deficiencias hormonales (Tabla III).
Los HHipo adquiridos son los más frecuentes y, en su mayoría, debidos a procesos tumorales o infiltrativos que afectan a la región hipotálamo-hipofisaria y que originan deficiencias hipofisarias múltiples(2). La causa más frecuente son los tumores, bien por invasión tumoral directa del área hipotálamo-hipofisaria, o bien como consecuencia de su extirpación quirúrgica o de la radioterapia aplicada para su tratamiento. El más frecuente de estos tumores en la infancia es el craneofaringioma, pero otros tumores, como: germinomas, gliomas o prolactinomas, pueden determinar manifestaciones clínicas similares. La dosis de radioterapia recibida por el hipotálamo o la hipófisis necesaria para producir un HHipo no está claramente establecida, aunque suele ser mayor de 40 Gy. Dosis de 30-55 Gy pueden determinar, inicialmente, una pubertad precoz o adelantada y, más adelante, por el efecto progresivo de la radiación, conducir a un HHipo. Procesos infiltrativos (histiocitosis, sarcoidosis, hemocromatosis), traumatismos craneales, procesos infecciosos o inflamatorios (hipofisitis autoinmune) que afecten al área hipotálamo-hipofisaria son otras posibles causas de HHipo. La hemocromatosis, por acúmulo de hierro en hipotálamo-hipófisis puede provocar un HHipo y por acúmulo gonadal un HHiper.
La prevalencia de HHipo congénitos se estima en alrededor de 1:10.000 personas y la mayoría son casos esporádicos, con un predominio en varones 3-5:1(25). Las formas familiares pueden heredarse con carácter autosómico dominante, recesivo o recesivo ligado al X. Los HHipo congénitos pueden presentarse aisladamente, asociados a otras deficiencias hipofisarias o en el contexto de otros cuadros sindrómicos complejos (Tabla III).
• HHipo congénitos aislados. Clásicamente y desde una visión clínica, estas formas de hipogonadismo se han clasificado como “HHipo congénitos con y sin alteraciones del olfato”; no obstante, esta diferenciación puede ser algo artificial, dado que el avance en los estudios genéticos ha puesto de manifiesto como, mutaciones en un mismo gen e incluso en una misma familia puede dar lugar a HHipo con y sin alteraciones del olfato.
La asociación de HHipo congénitos y alteración del olfato (anosmia o hipoosmia) secundaria a aplasia/hipoplasia de los bulbos olfatorios es lo que se conoce como síndrome de Maestre de San Juan-Kallmann o, simplemente, síndrome de Kallmann (SK). Este síndrome supone alrededor de un 15% de los HHipo y es cinco veces más frecuente en varones que en mujeres. La asociación de HHipo, por deficiencia de GnRH, y anosmia tiene su explicación en el origen embriológico común de las neuronas productoras de GnRH y de las neuronas olfatorias (Fig. 1). Los pacientes con SK pueden mostrar además de los trastornos del olfato, de los que frecuentemente no son conscientes, alteraciones muy variadas, entre ellas: agenesia renal unilateral, defectos atriales septales, ceguera para los colores, hipoacusia neurosensorial, sincinesias de los dedos, lesiones de línea media (labio-paladar hendido, agenesia de uno o más dientes y agenesia del cuerpo calloso), etc. Los casos esporádicos son los más frecuentes, más de dos terceras partes. En los casos familiares, las manifestaciones pueden ser muy variables entre los distintos familiares afectos: anosmia aislada, pubertad tardía, infertilidad, HHipo o pérdida temprana de la menstruación, entre otras. El primer gen responsable del SK, el gen KAL1 (Xp22.31), se descubrió en 1992 y codifica para una proteína, la anosmina, que facilita el crecimiento y la migración neuronal. Desde entonces, se han descrito, al menos, 16 genes diferentes asociados al síndrome (Tabla III) que serían responsables en conjunto de menos del 50% de los SK y con patrones hereditarios diferentes (autosómicos dominante, recesivo y ligado al X).
Las bases genéticas de los HHipo congénitos aislados sin anosmia (HHipo normoósmicos), al igual que ocurre con los SK, son solo parcialmente conocidas. Algunos de los genes que se han asociado a cuadros de HHipo sin anosmia son: GnRH1(GnRH), GnRHR (receptor de GnRH), KISS1 (kisspeptina) KISS1R (receptor de las kisspeptinas), LEP(leptina), LEPR (receptor de leptina), PC1 (prohormona convertasa-1), TAC3 (neurokinina B), TAC3R (receptor de TAC3), DAX1(miembro de la superfamilia de receptores nucleares huérfanos), LHβ (subunidad β de la LH) y FSHβ (subunidad β de la FSH). Las mutaciones en LEP, LEPR y PC1 cursan con obesidad de inicio temprano y las mutaciones en DAX1 se asocian a hipoplasia suprarrenal congénita. Sorprendentemente, alrededor del 10-20% de estas formas de HHipo aislado congénito, tanto con, como sin anosmia, pueden experimentar cierto grado de reversibilidad espontánea(25).
• HHipo asociados a otras deficiencias hipofisarias. Son debidas a anomalías congénitas en el desarrollo del SNC (displasia septo-óptica, holoprosencefalia, etc.) de base genética conocida o no, como sería el caso de algunas formas de displasia septo-óptica asociadas a mutaciones en HEX1, o a mutaciones en factores de transcripción implicados en el desarrollo de las diferentes líneas células hipofisarias: LHX3, LHX4, PROP1 y POU1F1 (Pit1). El gen más frecuentemente afectado es PROP1, cuyas mutaciones determinan una deficiencia combinada de: GH, Prl, LH, FSH, TSH y, frecuentemente, pero de forma más tardía, también de ACTH.
• HHipo asociados a cuadros sindrómicos. Determinados síndromes pueden asociar cuadros clínicos de HHipo, como es el caso de los síndromes de: Prader-Willi, CHARGE (cuando es por mutaciones en CDH7, se puede asociar anosmia), Laurence-Moon, Bardet-Biedl y 4H, entre otros.
Las manifestaciones clínicas de los HHipo son variables dependiendo de su etiopatogenia y momento de aparición (congénitos, infancia, pubertad o edad adulta), como sería el caso de: trastornos del olfato, rasgos sindrómicos, anomalías congénitas asociadas, síntomas debidos a otras deficiencias hipofisarias (GH, ADH, ACTH…), etc. En general, las formas congénitas, dado que la diferenciación sexual está controlada por la gonadotropina coriónica placentaria (HCG) y no por las gonadotropinas fetales, no presentan ambigüedad genital, aunque sí condicionan con frecuencia criptorquidia bilateral con micropene o una hipoplasia de labios menores, debido a su acción en la fase final de la gestación. Durante el periodo prepuberal, el crecimiento y la maduración ósea suelen ser normales, pero al llegar a la edad puberal, la ausencia de ES determina que no se desarrollen los caracteres sexuales secundarios (puede aparecer vello pubiano escaso por acción de los andrógenos suprarrenales) y se retrase el cierre de los cartílagos de crecimiento, lo que favorece el desarrollo de proporciones corporales eunucoides (aumento de las extremidades con incremento de la braza, >5 cm que la talla, y disminución del cociente segmento superior/segmento inferior). Algunos pacientes pueden iniciar la pubertad y no completarla (pubertad detenida) o completarla y desarrollar el hipogonadismo, posteriormente, en la edad adulta, manifestándose en forma de infertilidad y disfunción sexual.
Hipogonadismos hipergonadotropos (HHiper)
Este tipo de hipogonadismos son debidos a fallo gonadal primario y se caracterizan por niveles séricos elevados de gonadotropinas y disminuidos de ES. Pueden ser congénitos o adquiridos (Tabla III). La incapacidad de la gónada para producir adecuadas cantidades de ES e inhibina determina la falta de retroinhibición de estos sobre el hipotálamo y la hipófisis, incrementándose la secreción pulsátil de GnRH y, por tanto, de LH y FSH.
Las dos causas más frecuentes de HHiper congénito son dos cromosomopatías congénitas: el síndrome de Klinefelter y el síndrome de Turner.
• El síndrome de Klinefelter o síndrome de disgenesia de los túbulos seminíferos (47, XXY y sus variantes) es la causa más frecuente de hipogonadismo en el varón (1:500-1.000 niños nacidos vivos). La función de los túbulos seminíferos y de las células de Leydig está alterada y la espermatogénesis ausente. Dependiendo de los niveles de testosterona, la pubertad puede desarrollarse normalmente, retrasarse o empezar a una edad normal, aunque sin una adecuada progresión. Las manifestaciones clínicas son variables, pero la talla suele ser alta y en la pubertad y edad adulta los testes son pequeños y duros y la ginecomastia es frecuente. Otras anomalías asociadas incluirían: retraso mental variable, dificultades en el lenguaje, problemas de conducta, incremento en la incidencia de determinados tumores (cáncer de mama y tumores de células germinales de localización mediastínica, retroperitoneal y pineal) y alteraciones tiroideas, entre otras.
• El síndrome de Turner (45, X0 y sus variantes) es la causa más frecuente de HHiper en la mujer (1:2.500-3.000 niñas nacidas vivas). Sus manifestaciones clínicas resultan de la ausencia de genes que escapan a la inactivación del X. Estas niñas pueden presentar diferentes alteraciones y anomalías, incluyendo: hipocrecimiento, fallo gonadal, rasgos sindrómicos (pterigium colli, linfedema, tórax en coraza, hipoplasia areolar, cubitus valgo, alteraciones ungueales, acortamiento de metacarpianos, implantación baja del cabello y de las orejas, boca de pez, nevus múltiples, etc.), cardiopatía, malformaciones del sistema urinario, etc. Los síntomas más constantes son el hipocrecimiento (95%) y el fallo gonadal (90%). Pese a ello, un 30% son capaces de iniciar espontáneamente la pubertad, aunque solo un 2-5% llegan a completarla y a tener reglas espontáneas (menopausia precoz con amenorrea secundaria).
• Las causas adquiridas de HHiper son relativamente infrecuentes: torsión gonadal bilateral (testicular u ovárica), castración quirúrgica (tumores), traumatismos severos en el escroto y testículos, orquitis bilaterales (p. ej., parotiditis) y, en el caso de las mujeres, galactosemia o fracaso ovárico precoz de etiología idiopática o autoinmune. El tratamiento del cáncer, debido a la quimioterapia y radioterapia, con frecuencia aplicadas conjuntamente, es una causa creciente de HHiper adquirido.
Evaluación diagnóstica
Las causas que pueden provocar un retraso puberal son múltiples. Una valoración básica inicial incluiría: una cuidadosa historia médica, personal y familiar, una exploración física completa y una serie de pruebas complementarias (Algoritmo 2) que pueden variar en función de los hallazgos de la historia y exploración(20).
Anamnesis detallada
Una historia familiar de PR está presente en la gran mayoría de los casos de RCCP, pero también puede formar parte de la historia familiar en pacientes con HHipo. Un interrogatorio cuidadoso puede poner de manifiesto la presencia de síntomas sugerentes de patologías concretas (anosmia, infertilidad, galactorrea, hipotiroidismo, etc.) o de patologías crónicas inadvertidas, así como un exceso de ejercicio o un trastorno de la conducta alimentaria. Los antecedentes de criptorquidia, quimioterapia, radioterapia gonadal o craneal y la administración crónica o prolongada de medicamentos que puedan interferir en la función gonadal debe ser, también, recogida. La reconstrucción de la gráfica de crecimiento y peso puede ser de utilidad, junto con la los datos auxológicos parentales. El hipocrecimiento es un hallazgo habitual en: RCCP, malnutrición, patología crónica o Turner; mientras que, en la mayoría de las formas de HHipo la talla suele ser normal o incluso alta. Un bajo peso para la talla puede indicar trastornos nutricionales o enfermedad crónica inadvertida; mientras que: hipotiroidismo, exceso de glucocorticoides, deficiencia de GH o determinados síndromes (Prader Willi, Turner, etc.) suelen tener un claro o moderado incremento del peso para la talla.
Exploración física
Debe ser completa, analizando especialmente: talla, peso, signos de malnutrición o patología crónica, estigmas sindrómicos (Turner, Klinefelter…) y signos neurológicos sugerentes de patología intracraneal (fondo de ojo, campimetría y estudio del olfato pueden ser necesarios). Debe realizarse una cuidadosa valoración del estadio de desarrollo puberal; ya que, signos incipientes de desarrollo puberal pueden pasar inadvertidos para los pacientes o alteraciones en la secuencia normal de la pubertad pueden sugerir patología. En las niñas con desarrollo puberal normal, pero sin menarquia, deben descartarse causas anatómicas de amenorrea (himen imperforado, septum transverso vaginal o disgenesia mülleriana –síndrome de Rokitansky–), mediante una adecuada exploración ginecológica y ecográfica.
Edad ósea (EO)
El RCCP, la patología crónica, las endocrinopatías y los hipogonadismos presentan, habitualmente, un retraso de EO de 1 a 4 años. Una talla normal-baja, con ralentización reciente y EO inferior a 11 años en una niña y a 13 años en un varón es muy sugerente de retraso puberal simple; por el contrario, la ausencia de signos puberales a una EO de más de 11 años en las niñas y de más de 13 años en los niños es muy sugerente de hipogonadismo.
Otras pruebas complementarias
Su realización dependerá de la historia, exploración y EO.
• Analítica general. En pacientes en los que la historia clínica o la exploración física sugieran la presencia de patología crónica subyacente, debe realizarse una evaluación individual orientada a la sospecha clínica. Esta puede incluir: hemograma y bioquímica básica, marcadores de enfermedad celíaca, anticuerpos antitiroideos, TSH, T4 libre, prolactina y marcadores de deficiencia de GH (IGF-I, IGFBP-3). La sospecha de una deficiencia de GH puede obligar a realizar test de GH precedidos de la administración de ES (primación) para diferenciar una deficiencia real de GH de una deficiencia transitoria asociada a RCCP.
• Cariotipo. Su realización estaría indicada ante la presencia de estigmas sindrómicos o en el caso de: gonadotropinas elevadas, niñas con talla baja de etiología incierta o varones con testes pequeños e inadecuados para el grado de desarrollo puberal.
• RM craneal. Podría poner de manifiesto patología orgánica intracraneal, en área hipotálamo-hipofisaria, o anomalías de la vía olfatoria (agenesia de bulbos o nervios olfatorios).
• Ecografías pélvico-abdominales. Podrían poner de manifiesto malformaciones congénitas asociadas (renales en el SK) o anomalías vaginouterinas (agenesia o malformaciones uterinas, septum vaginal…), tamaño y morfología del útero y ovarios, localización de testes criptorquídicos, etc.
• Estudios hormonales. Un aspecto fundamental de la evaluación del retraso puberal, pero especialmente compleja, es la valoración del eje HHG. Los niveles séricos de testosterona y estradiol son de escasa utilidad en las fases iniciales de la pubertad; ya que, sus niveles séricos se sitúan, con frecuencia, por debajo del límite de detección de la mayoría de los inmunoanálisis. A partir de los 10-11 años de EO, a veces incluso antes, es frecuente observar en los HHiper niveles séricos elevados de LH y FSH basales o tras estímulo con GnRH. El diagnóstico de los HHipo completos también es sencillo cuando la EO supera, al menos en un año, la EO en la que habitualmente la pubertad se inicia. Se observan en este caso, niveles séricos disminuidos de LH y FSH tras estímulo con GnRH. El principal problema de diagnóstico diferencial se plantea entre el RCCP y el HHipo (sobre todo si es parcial, aislado e idiopático) cuando la EO del paciente está retrasada por debajo de las edades en que normalmente se inicia la pubertad. En estos casos, existe un considerable solapamiento entre la pobre respuesta de los pacientes con RCCP y la observada en pacientes con HHipo. Inhibina B y hormona antimülleriana, marcadores de la célula de Sertoli, pueden ser en ocasiones de utilidad para diferenciar HHipo y RCCP; ya que, la presencia de niveles séricos de inhibina B y hormona antimülleriana muy disminuidos o ausentes es más característico de los HHipo que de los RCCP. No obstante, en muchos casos, solo el tiempo y la evolución espontánea de la pubertad permitirán excluir o confirmar, definitivamente, el hipogonadismo(26).
• Estudios moleculares. Los pacientes con hipogonadismo y cariotipo normal, así como los hipogonadismos sindrómicos son candidatos para estudios moleculares más amplios. Estos deberían estar orientados, en función del diagnóstico y los hallazgos clínicos y hormonales, hacia genes concretos. En el caso de que las características clínicas del paciente no orienten hacia un diagnóstico concreto, se puede considerar, en colaboración con el genetista clínico, la posibilidad de realizar otros estudios genéticos más amplios: estudios de MLPA (Multiplex Ligation-dependent Probe Amplification), GWAS (Genoma-Wide Association Studies) o estudios de secuenciación de alto rendimiento (NGS: Next-Generation Sequencing). Este último tipo de estudios permite la secuenciación del genoma completo, de capturas selectivas (paneles de genes implicados en determinadas patologías), de regiones concretas o de todas las regiones codificantes y reguladoras conocidas de todo el genoma (exoma).
Tratamiento
Retraso constitucional del crecimiento y de la pubertad
El RCCP se considera una variante de la normalidad; por consiguiente, en la gran mayoría de los casos, una clara explicación al paciente y a los padres, junto con un adecuado control y apoyo psicológico, son suficientes. Solo aquellos casos en los que el retraso sea más severo y existan graves repercusiones psicológicas y sociales (depresión, baja autoestima, fracaso escolar, etc.) serán susceptibles de tratamiento.
En los varones, suele administrarse testosterona, a dosis baja, en forma de preparados depot de ésteres de testosterona (enantato o cipionato), en una inyección intramuscular mensual de 50-100 mg, y a partir de los 12-12,5 años de EO o de los 14 de edad cronológica(20). Por debajo de esa edad, rara vez es necesario desde el punto de vista psicológico y el riesgo de acelerar la EO y comprometer la talla definitiva es mayor. La testosterona acelera la VC, el desarrollo de los caracteres sexuales secundarios y favorece el desarrollo espontáneo de la pubertad. Se recomienda realizar ciclos de tratamiento de 3-6 meses, alternando con periodos similares de observación durante los cuales se vigila la progresión espontánea de la pubertad. Si tras 2-3 ciclos, la pubertad no se ha iniciado (aumento del volumen testicular), lo más probable es que nos encontremos ante un hipogonadismo hipogonadotropo.
En las niñas, la incidencia de RCCP es muy inferior a la de los varones y la experiencia menor. Se recomienda que el tratamiento no se inicie antes de los 13 años de edad cronológica y de los 11-12 años de EO y que se utilicen estrógenos (estradiol o etinil-estradiol) a dosis muy bajas, al objeto de no acelerar en exceso la maduración ósea y comprometer la talla final.
En pacientes con RCCP con malas expectativas de talla adulta, se ha sugerido la posibilidad de emplear otro tipo de tratamientos, como sería el caso de la GH; sin embargo, al menos con las pautas utilizadas, la GH no parece ser capaz de mejorar significativamente la talla final en estos pacientes. Otros estudios más recientes, sugerían que los inhibidores de la aromatasa de 3ª generación (letrozol y anastrozol) asociados a andrógenos podrían acelerar la VC, enlentecer la progresión de la maduración ósea y mejorar las expectativas de talla final y, todo ello, sin efectos secundarios reseñables; no obstante, los resultados disponibles a talla final, aunque todavía insuficientes para poder establecer conclusiones definitivas, no sostienen estos potenciales beneficios y sí posibles efectos secundarios, entre ellos: marcada elevación de los niveles séricos de testosterona, de repercusión incierta, desarrollo de anomalías vertebrales, disminución del colesterol HDL y aumento del hematocrito(27).
Retraso puberal secundario a patología crónica
El tratamiento y la prevención del retraso puberal en pacientes con patologías crónicas se basa en el tratamiento óptimo y precoz de la enfermedad de base, junto con una adecuada nutrición (aporte suficiente de macro y micronutrientes).
Las pautas para inducir y mantener el desarrollo puberal no difieren, en general, de las empleadas en el RCCP o en el hipogonadismo.
Hipogonadismos
En los hipogonadismos es necesario inducir o completar el desarrollo de los caracteres sexuales secundarios y posteriormente, establecer una pauta crónica de reemplazamiento de ES.
Disponemos de tres opciones terapéuticas para inducir la pubertad: administración pulsátil de GnRH, administración de gonadotropinas y administración de ES. La elección dependerá del diagnóstico (en los HHiper, la única opción son los ES), de los objetivos terapéuticos (incremento de volumen testicular, fertilidad…), de la disponibilidad (la terapia con GnRH está limitada a muy pocos centros en Europa) y de las preferencias del paciente.
Durante la infancia, en los varones con HHipo puede ser necesario tratamiento para resolver la criptorquidia y mejorar el micropene. La criptorquidia, sobre todo cuando es bilateral, puede tener consecuencias negativas para la fertilidad futura, por ello se recomienda su corrección quirúrgica temprana, preferiblemente entre los 6-12 meses de vida(25). En cuanto al micropene, puede ser tratado con pequeñas dosis de testosterona depot (25 mg/mes), 1-3 dosis, preferiblemente durante los primeros 6-12 meses de vida o con gonadotropinas (HCG y FSH). Estudios recientes sugieren que el tratamiento con gonadotropinas en este periodo de la vida podría tener, además, efectos beneficiosos sobre el desarrollo testicular y la futura fertilidad del paciente, aunque estos resultados son todavía muy preliminares para establecer conclusiones definitivas.
En la adolescencia y edad adulta, los objetivos del tratamiento son: conseguir un desarrollo puberal completo, con una secuencia y ritmo normal de aparición de los caracteres sexuales secundarios, lograr la mejor talla adulta posible, evitar la osteoporosis y las complicaciones cardiovasculares y psicosociales, y, en aquellos casos en que sea factible, adquirir y optimizar la capacidad reproductiva(28,29). Una propuesta aceptable sería, remedando el desarrollo puberal normal, inducirlo alrededor de los 11 años de EO en las niñas y de los 12 años en los varones e incrementar lentamente los niveles séricos de ES para conseguir el desarrollo puberal completo en un periodo de 3-4 años. Cuando la talla final está comprometida (deficiencia de GH, Turner), puede ser necesario retrasar la inducción de la pubertad, al objeto de lograr unas mejores expectativas de talla adulta.
En varones, la forma más sencilla de inducir el desarrollo puberal es la administración de testosterona, que puede ser por vía oral (no disponible en España), parenteral o transdérmica. En la práctica, suelen utilizarse preparados depot de testosterona de acción prolongada (enantato o cipionato) por vía intramuscular. La dosis inicial será de 25-50 mg cada 4 semanas y se incrementará en 50 mg, cada 6-12 meses, para, a lo largo de un periodo de 3-4 años, alcanzar la dosis de sustitución de un adulto, que oscilaría entre 200-250 mg cada 10-14 días. Un inconveniente de esta terapia es que el volumen testicular no aumenta ni se induce la fertilidad. En los niños con HHipo en los que se desee incrementar el volumen testicular, la terapia intramuscular o subcutánea con gonadotropinas o la administración pulsátil, mediante bomba, de bolos de GnRH, por vía subcutánea, puede ser una alternativa. Una vez completado el desarrollo puberal, la terapia de mantenimiento en los varones se realiza, habitualmente, con testosterona. Aunque en este caso, también puede administrarse por diferentes vías, las más utilizadas son: la intramuscular (200-250 mg de enantato de testosterona cada 10-14 días o 1.000 mg de undecanoato detestosterona c/2-3 meses) y la transdérmica (parches de testosterona); ya que, los preparados orales de testosterona (undecanoato de testosterona) no están comercializados en nuestro país. La fertilidad, en el adulto, requiere de la administración de gonadotropinas o de bolos de GnRH, por vía subcutánea, durante periodos prolongados para inducir la espermiogénesis.
En las niñas, la inducción de la pubertad se realizará con estrógenos y con dosis iniciales muy bajas; ya que, los estrógenos son un potente inductor de la fusión epifisaria. Los regímenes más habitualmente empleados incluyen la administración oral o transdérmica de estradiol. La vía transdérmica, con parches de composición matricial es la más recomendada, ya que tiene la ventaja sobre la vía oral, de una mayor biodisponibilidad, mejor tolerancia gastrointestinal y menor toxicidad hepato-biliar al evitar el paso inicial por el hígado. Estos parches matriciales, dependiendo del preparado, liberan 25, 50, 75 o 100 µg/día de estradiol, pero permiten su fragmentación y la administración de dosis más bajas y progresivamente crecientes de estradiol. La dosis inicial sería de 0,05-0,1 µg/kg, habitualmente 1/8 de parche de 25 µg que, de forma ideal, se aplicaría durante los primeros 3-4 meses solo por la noche (se pondría al acostarse y se retiraría por la mañana); posteriormente, el 1/8 de parche se mantendría durante todo el día (se cambian 2 veces/ semana) y las dosis se irían incrementando cada aproximadamente 6-12 meses, durante un periodo no inferior a 2-3 años, hasta alcanzar la dosis diaria de sustitución estrogénica de una mujer adulta, que correspondería habitualmente a unos 50 µg/día de estradiol. Una vez alcanzado un adecuado desarrollo mamario (T4-5) y uterino (útero en la ecografía de >35-40 mm, con línea endometrial visible), o bien, si produce un sangrado menstrual o pequeños manchados, debe añadirse un progestágeno cíclico, preferentemente micronizado para favorecer su absorción (200 mg/día, antes de acostarse, del 10 al 21 día de ciclo, en forma de cápsulas orales u óvulos vaginales) para la protección uterina y establecer ciclos menstruales regulares mensuales. Una vez completado el desarrollo puberal, es necesario establecer una terapia sustitutiva a largo plazo. Se podría seguir con la asociación de estrógeno transdérmico y progestágeno oral-vaginal, pero, en la mayoría de los casos, suele administrase una combinación continua o cíclica de estrógenos-progestágenos, habitualmente por vía oral o transdérmica. Una gran variedad de preparados combinados de estrógenos-progestágenos están disponibles en el mercado en forma de píldoras orales anticonceptivas y pueden ser empleados. Deben elegirse, si están disponibles, aquellos que contengan estrógenos naturales y, si no es posible, los de menor contenido estrogénico (15-20 µg de etinil estradiol). La opción a la vía oral es la administración transdérmica continua de estrógenos-progestágenos que, habitualmente, aportan una dosis diaria de 50 µg/día de estradiol. Los parches se cambian cada 3,5 días (dos por semana), durante 3 semanas, transcurridas las cuales se suspende una semana el tratamiento, durante la cual se produce la regla. La inducción de fertilidad, requiere, como en el caso de los varones, de la administración prolongada de gonadotropinas o GnRH.
Funciones del pediatra de Atención Primaria (AP)
El pediatra de Atención Primaria es el profesional que se enfrenta inicialmente a este tipo de situaciones y debe ser capaz de realizar un enfoque diagnóstico adecuado, diferenciar aquellas variantes normales del desarrollo de las que no lo son, orientar a los padres y al paciente y, en aquellos casos que considere necesario, derivar al paciente a un servicio de Endocrinología Pediátrica. Trasmitir a los padres una información veraz sobre la amplia variabilidad normal en el tempo de la pubertad, las escasas o nulas repercusiones que estas variaciones normales tienen sobre la talla adulta y la inconveniencia de llevar a cabo tratamientos, por innecesarios, contraindicados, es muchas veces suficiente para tranquilizar a los padres y a los pacientes. Por el contrario, derivar precozmente aquellos pacientes sospechosos de patología puede permitir el diagnóstico precoz de patologías orgánicas, potencialmente graves y que el tratamiento evite, o al menos minimice las repercusiones auxológicas y psicosociales de estas patologías.
Bibliografía
Los asteriscos reflejan el interés del artículo a juicio del autor.
1.** Kuiri-Hänninen T, Sankilampi U, Dunkel L. Activation of the hypothalamic-pituitary-gonadal axis in infancy: minipuberty. Horm Res Paediatr. 2014; 82: 73-80.
2. Nakamoto JM, Franklin SL, Geffner ME. Puberty. En: Kappy MS, Allen DB, Geffner ME, ed. Pediatric Practice Endocrinology. New York: Mc Graw Hill Medical; 2010. p. 257-98.
3.** Parent AS, Teilman G, Juul A, Skakkebaek NE, Toppari J, Bourguignon JP. The timing of normal puberty and the age limits of sexual precocity: variations around the world, secular trends and changes after migration. Endocr Rev. 2003; 24: 668-93.
4.** Day FR, Perry JR, Ong KK. Genetic Regulation of Puberty Timing in Humans. Neuroendocrinology. 2015 May 7 (artículo publicado electrónicamente previo a su publicación en papel). DOI: 10.1159/000431023.
5.** Parent AS, Franssen D, Fudvoye J, Gérard A, Bourguignon JP. Developmental variations in environmental influences including endocrine disruptors on pubertal timing and neuroendocrine control: Revision of human observations and mechanistic insight from rodents. Front Neuroendocrinol. 2015; 38: 12-36.
6. Özen S, Darcan S. Effects of Environmental Endocrine Disruptors on Pubertal Development. J Clin Res Ped Endo. 2011; 3: 1-6.
7.** Soriano-Guillén L, Corripio R, Labarta JI, et al. Central precocious puberty in children living in Spain: incidence, prevalence, and influence of adoption and immigration. J Clin Endocrinol Metab. 2010; 95: 4305-13.
8. Sloboda DM1, Hickey M, Hart R. Reproduction in females: the role of the early life environment. Hum Reprod Update. 2011; 17: 210-27.
9.** Carel JC, Léger J. Precocious puberty. N Engl J Med. 2008; 358: 2366-77.
10. Kaplowitz PB, Oberfield SE. Reexamination of the age limit for defining when puberty is precocious in girls in the United States: implications for evaluation and treatment. Drug and Therapeutics and Executive Committees of the Lawson Wilkins Pediatric Endocrine Society. Pediatrics. 1999; 104: 936-41.
11.** Carel JC, Lahlou N, Roger M, Chaussain JL. Precocious puberty and statural growth. Human Reprod Update. 2004; 10: 135-47.
12. Johansson T, Ritzzen EM. Very long-term follow-up of girls with early and late menarche. Endocr Dev 2005; 8: 126-36.
13. Barrio R, Carcavilla A, Martín M. Pubertad Precoz y Retrasada. Inf Ter Sist Nac Salud. 2006; 30: 95-107.
14. Bulcao Macedo D, Nahime Brito V, Latronico AC. New causes of central precocious puberty: the role of genetic factors. Neuroendocrinology. 2014; 100: 1-8.
15. Stephen MD, Zage PE, Waguespack SG. Gonadotropin-dependent precocious puberty: neoplastic causes and endocrine considerations. Int J Pediat Endocrinol. 2011; 2011: 184502. doi: 10.1155/2011/184502.
16.** Dumitrescu CE, Collins MT. McCune-Albright syndrome. Orphanet J Rare Dis. 2008; 3: 12.
17.** Soriano-Guillén L, Argente J. Pubertad precoz central: aspectos epidemiológicos, etiológicos y diagnóstico-terapéuticos. An Pediatr (Barc.). 2011; 74: 336-43.
18.** Fuqua JS. Treatment and outcomes of precocious puberty: An update. J Clin Endocrinol Metab. 2013; 98: 2198-207.
19.** Carel JC, Eugster EA, Rogol A, Ghizzoni L, Palmert MR, on behalf of the members of the ESPE-LWPES GnRH Analogs Consensus Conference Group. Consensus statement on the use of gonadotropin-releasing hormone analogs in children. Pediatrics. 2009; 123: e752-62.
20. Pozo J, Argente J. Ascertainment and treatment of delayed puberty. Horm Res. 2003; 60 (suppl 3): 35-48.
21.** Palmert MR, Dunkel L. Delayed puberty. N Engl J Med. 2012; 366: 443-53.
22. Villanueva C, Argente J. Pathology or normal variant: what constitutes a delay in puberty? Horm Res Paediatr. 2014; 82(4): 213-21.
23. Moreno L, Ibañez L. Pubertad retrasada. En: Cruz-Hernández, ed. Tratado de Pediatría (10ª edición). Madrid: Ergon S.A. 2011; p. 1.094-1.100.
24. Pozo J, Argente J. Delayed puberty in chronic illnes. Baillieres Best Pract Res Clin Endocrinol Metab. 2002; 16: 73-90.
25.*** Boehm U, Bouloux PM, Dattani MT, de Roux N, Dodé C, Dunkel L, et al. Expert consensus document: European Consensus Statement on congenital hypogonadotropic hypogonadism-pathogenesis, diagnosis and treatment. Nat Rev Endocrinol. 2015 (artículo publicado electrónicamente previo a su publicación en papel). doi: 10.1038/nrendo.2015.112.
26. Harrington J, Palmert MR. Clinical review: Distinguishing constitutional delay of growth and puberty from isolated hypogonadotropic hypogonadism: critical appraisal of available diagnostic tests. J Clin Endocrinol Metab. 2012; 97: 3056-67.
27. Shams K, Cameo T, Fennoy I, et al. Outcome analysis of aromatase inhibitor therapy to increase adult height in males with predicted short adult stature and/or rapid pubertal progress: a retrospective chart review. J Pediatr Endocrinol Metab. 2014; 27: 725-30.
28. Bouvattier C, Maione L, Bouligand J, Dodé C, Guiochon-Mantel A, Young J. Neonatal gonadotropin therapy in male congenital hypogonadotropic hypogonadism. Nat Rev Endocrinol. 2011; 8: 172-82.
29.** Barrio R, Roldán B, Martín Frías M. Inducción de la pubertad. Rev Esp Endocrinol Pediatr. 2015; 6 (Suppl): 39-44.
Bibliografía recomendada
- Parent AS, Franssen D, Fudvoye J, Gérard A, Bourguignon JP. Developmental variations in environmental influences including endocrine disruptors on pubertal timing and neuroendocrine control: Revision of human observations and mechanistic insight from rodents. Front Neuroendocrinol. 2015; 38: 12-36.
Una excelente y amplia revisión sobre los mecanismos genéticos y ambientales implicados en el inicio puberal y su interrelación. Amplia bibliografía que permite profundizar aún más en estos aspectos. Muy recomendable.
- Carel JC, Eugster EA, Rogol A, Ghizzoni L, Palmert MR, on behalf of the members of the ESPE-LWPES GnRH Analogs Consensus Conference Group. Consensus statement on the use of gonadotropin-releasing hormone analogs in children. Pediatrics. 2009; 123: e752-e762.
Este trabajo es el fruto de un reciente consenso de las principales sociedades internacionales de Endocrinología Pediátrica sobre un tema tan controvertido como es la utilización de los análogos de GnRH en niños. Además de su empleo en la pubertad precoz central (principal indicación de estos fármacos), se revisa su empleo en otras situaciones (talla baja, hiperplasia adrenal congénita…). El trabajo reúne las conclusiones de estos expertos a la luz de los datos disponibles en la literatura. La revisión corta, pero muy esclarecedora, es muy recomendable no solo para endocrinólogos infantiles, sino también, para todos los pediatras interesados en temas de pubertad y crecimiento.
- Boehm U, Bouloux PM, Dattani MT, de Roux N, Dodé C, Dunkel L, et al. Expert consensus document: European Consensus Statement on congenital hypogonadotropic hypogonadism-pathogenesis, diagnosis and treatment. Nat Rev Endocrinol. 2015 (artículo publicado electrónicamente previo a su publicación en papel). doi: 10.1038/nrendo.2015.112.
Una reciente publicación que recoge el consenso de un grupo de expertos europeos sobre diferentes aspectos de los hipogonadismos hipogonadotropos congénitos, con los más recientes conocimientos sobre sus bases genéticas y los aspectos diagnósticos y terapéuticos. Además, es posible descargársela libremente en la dirección http://www.nature.com/nrendo/journal/vaop/ncurrent/pdf/nrendo.2015.112.pdf.
| Caso clínico |
|
Motivo de consulta
Varón de 13 años y 6 meses de edad, que consulta por ausencia de desarrollo puberal.
Antecedentes familiares
Madre: 39 años, sana. Talla: 165,6 cm. Menarquia a los 13 años. G.A.V. 2.0.2. Padre: 41 años, sano. Talla: 185 cm. Desarrollo puberal normal. Una hermana de 4 años: sana. Resto de antecedentes familiares sin interés.
Antecedentes personales
Embarazo y parto normales (cariotipo intraútero: 46,XY). Periodo neonatal: normal. PRN: 2.720 g. LRN: 50 cm. Alimentación: sin intolerancias ni alergias alimentarias. Desarrollo psicomotor: normal. Enfermedades anteriores: diagnosticado a los 4 años de edad, de sarcoma cerebeloso (meduloblastoma atípico) y tratado con: cirugía (resección completa y válvula de derivación ventrículo-peritoneal), altas dosis de quimioterapia y, para consolidación del tratamiento, trasplante autólogo de progenitores hematopoyéticos. Resto de antecedentes personales: sin interés.
Exploración
Edad cronológica: 13 años y 6 meses. Talla: 153 cm (P25-50). Peso: 55 kg (P50-75). Exploración normal con genitales externos masculinos normales en estadio puberal I de Tanner (G1, P1, Aa) con testes en bolsas de 3 mL de volumen.
Pruebas complementarias
• Edad ósea: 13 años.
• Hemograma y bioquímica básica: normales.
• Función tiroidea (T4L y TSH): normal.
• Testosterona: 0,45 ng/mL (VN: 0,3-4).
• Test de LHRH para LH y FSH: niveles basales y tras estímulo de LH y FSH elevados.
- FSH basal: 78 UI/mL, pico de FSH: 134 mUI/mL.
- LH basal: 39 mUI/mL, pico de LH: 164 mUI/mL.
|
|
|