|
| Temas de FC |
G.M. Garnacho Saucedo
Servicio Dermatología. Unidad Dermatología Pediátrica. Hospital Universitario Reina Sofía, Córdoba
| Resumen
Los nevus melanocíticos son las neoplasias más comunes en el ser humano y cada vez son más frecuentes las consultas relacionadas con su benignidad o malignidad, así como sobre la necesidad o no de su extirpación. De forma general, atendiendo al momento de aparición, los nevus melanocíticos se dividen en nevus melanocíticos adquiridos (NMA) y nevus melanocíticos congénitos (NMC). Los NMA habitualmente comienzan a aparecer después de la primera infancia (a partir de los 2 años). Posteriormente, aumentan en tamaño y número durante el resto de la infancia y la adolescencia, con un pico máximo en la tercera-cuarta década de la vida. Los NMC son aquellos presentes en el momento del nacimiento o que aparecen antes de los dos años de vida. La incidencia del melanoma, el tipo de cáncer cutáneo de mayor mortalidad, continúa aumentando, aunque en la infancia sigue siendo raro. Los melanomas en menores de 20 años constituyen solo 1-3% de todos los melanomas, y en la etapa prepuberal el 0,3-0,4% del total. Se ha demostrado que la fotoprotección adecuada, sobre todo, durante la infancia y la auto-observación son las principales medidas para luchar contra el melanoma. |
| Abstract
Melanocytic nevi are the most common tumors in humans and the reasons for consultation on their malignancy or benignity are becoming more frequent. In general, considering the time of onset, melanocytic nevi are divided into acquired melanocytic nevi (AMN) and congenital melanocytic nevi (CMN). The AMN usually appear in early childhood (from 2 years old). Then they increase in size and number during the rest of childhood and adolescence with a peak incidence in the third to fourth decade of life. CMN are those present at birth or appear before two years of life. The incidence of melanoma, the skin cancer with the highest mortality, continues to increase day by day although still rare in childhood. Melanomas under 20 account for only 1-3% of all melanomas, and in the prepubertal the 0.3-0.4% of the total. It has been shown that adequate sun protection especially during childhood and self-observation are the main measures to fight melanoma. |
Palabras clave: Nevus melanocítico; Melanoma; Nevogénesis; Fotoprotección
Key words: Melanocytic nevi; Melanoma; Nevogenesis; Photoprotection
Pediatr Integral 2016; XX (4): 262-273
Trastornos de la pigmentación: lentigos, nevus y melanoma. Fotoprotección
Introducción
Las lesiones pigmentadas y, en especial, los nevus melanocíticos son las neoplasias más comunes en el ser humano.
La importancia de estas tumoraciones radica en los problemas estéticos que pueden originar (sobre todo, nevus melanocíticos congénitos gigantes que ocasionan una gran alteración estética), la posible asociación con otras malformaciones y, sobre todo, que pueden ser marcadores y, en ocasiones, precursores potenciales de melanoma. De forma general, atendiendo al momento de aparición, los nevus melanocíticos se dividen en: nevus melanocíticos adquiridos (NMA) y congénitos (NMC). Los NMA habitualmente comienzan a aparecer después de la primera infancia (a partir de los 2 años). Posteriormente, aumentan en tamaño y número durante el resto de la infancia y adolescencia, con un pico máximo en la tercera-cuarta década de la vida. A partir de este momento, comienza una lenta y progresiva involución; de tal forma que, en la vejez son escasos los nevus que podemos encontrar. Los NMC son aquellos presentes en el momento del nacimiento o que aparecen antes de los dos años de vida.
Epidemiología
Los nevus melanocíticos son muy frecuentes y la gran mayoría benignos. Entre un 0,2 y un 2,1% de los recién nacidos presenta un nevus melanocítico y, en la mayoría de los casos, de pequeño o mediano tamaño. La incidencia del melanoma, el tipo de cáncer cutáneo de mayor mortalidad, continúa aumentando, aunque en la infancia sigue siendo raro. Los melanomas en menores de 20 años constituyen solo un 1-3% de todos los melanomas, y en la etapa prepuberal el 0,3-0,4% del total. La predisposición de un individuo al desarrollo de nevus melanocíticos adquiridos parece estar relacionada con diferentes factores, entre los que se incluyen: el fototipo, la raza, la carga genética y la exposición a la luz ultravioleta. En los niños, tres factores se han visto claramente implicados en su desarrollo: la exposición solar intermitente, las quemaduras solares y la piel blanca escasamente protegida (fototipos I y II). Se ha publicado también la asociación de muchos nevus melanocíticos en niños con historia de leucemia y/o quimioterapia y, en estos casos, las lesiones suelen aparecer con más frecuencia en localizaciones acrales.
Etiopatogenia
Los nevus melanocíticos adquiridos son neoplasias benignas producidas por la proliferación de células névicas o nevocitos, melanocitos modificados que pierden su forma dendrítica y tienden a retener pigmento. Estas células se originan en la cresta neural y en la etapa fetal intraútero, migran desde allí a la piel. Existen diferentes teorías de la nevogénesis que tratan de establecer la exacta evolución de las células névicas en el proceso de formación de los nevus, sin existir ninguna definitiva. Según la actual teoría dual de la nevogénesis(1), surgida en el 2009, existiría dos vías complementarias: una endógena o constitucional y otra exógena. Tras su origen en la cresta neural, los melanocitos migrarían a la piel pudiendo llegar a la unión epidermodérmica o quedar “atrapados” en la dermis. Aquellos que quedan “atrapados” en la dermis dan lugar a nevus intradérmicos (clínicamente verrucosos) que permanecerán constantes a lo largo de la vida sin experimentar cambios y constituirían el componente endógeno. Sin embargo, aquellos que alcancen el compartimento epidérmico (más superficial) podrán multiplicarse y organizarse de dos maneras, formando nidos en la unión epidermodérmica y dermis papilar dando lugar a los nevus compuestos, o sin formar nidos distribuyéndose aisladamente por toda la unión epidermodérmica con un crecimiento lentiginoso (células aisladas en hilera) dando lugar a los nevus de la unión. Estos nevus con componente epidérmico constituirían la vía exógena, ya que representan verdaderos nevus adquiridos que se desarrollan en respuesta a factores externos como la exposición solar intermitente o los traumatismos. Se ha comprobado que la exposición solar intermitente provoca mutaciones BRAF en las células madres melanocíticas de la unión epidermodérmica, dando lugar a los nevus cuando estas células mutadas proliferan. A lo largo de su desarrollo podrán experimentar cambios e incluso malignizar.
Nuevas tecnologías
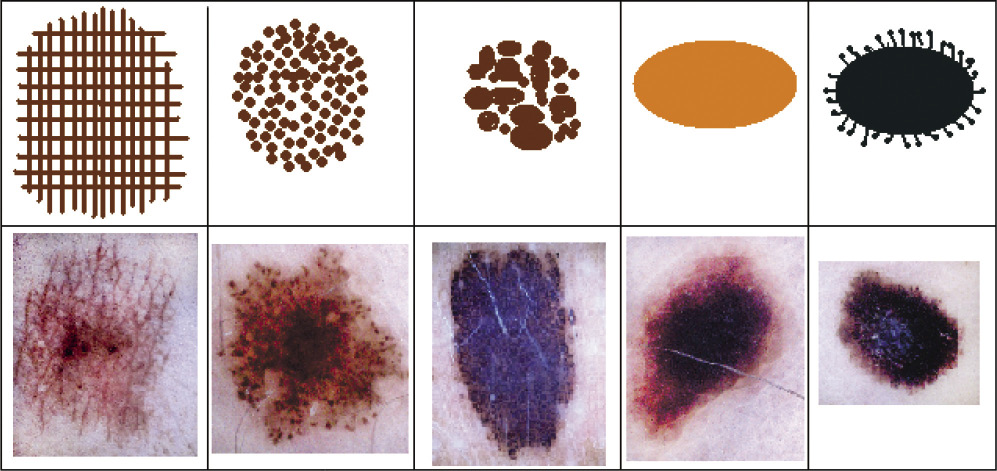
Estos nuevos conceptos han sido posibles gracias al desarrollo de nuevas tecnologías aplicadas al estudio de las lesiones melanocíticas, como la dermatoscopia o la microscopía confocal. La dermatoscopia o microscopía de epiluminiscencia es una técnica diagnóstica no invasiva que amplía la piel, de manera que hace visibles el color y la estructura de la epidermis, la unión dermoepidérmica y la dermis papilar. Con formación y experiencia, se ha demostrado que la dermatoscopia aumenta significativamente el diagnóstico clínico de las lesiones melanocíticas benignas y malignas de la piel, con una mejoría en el diagnóstico del melanoma del 10% al 27%, en comparación con los resultados obtenidos solo con la exploración clínica. De una forma resumida y breve, podemos decir que se establecen fundamentalmente 5 diferentes patrones dermatoscópicos, en los que podemos englobar las lesiones melanocíticas no acrales: reticular, globular, empedrado, homogéneo y estallido de estrellas (Fig. 1).
Figura 1. Patrones dermatoscópicos en lesiones melanocíticas no acrales: reticular, globular, empedrado, homogéneo y estallido de estrellas.
Todos estos patrones se correlacionan con una clínica y una histopatología determinada que iremos detallando.
Nevus melanocíticos adquiridos
Características clínicas y clasificación
La morfología(2) de los nevus es amplia y variada, existiendo: lesiones delgadas, parcialmente elevadas, cupuliformes, verrugosos, papilomatosos…, que pueden distribuirse ampliamente en cualquier localización de la superficie cutánea, mucosa y semimucosa.
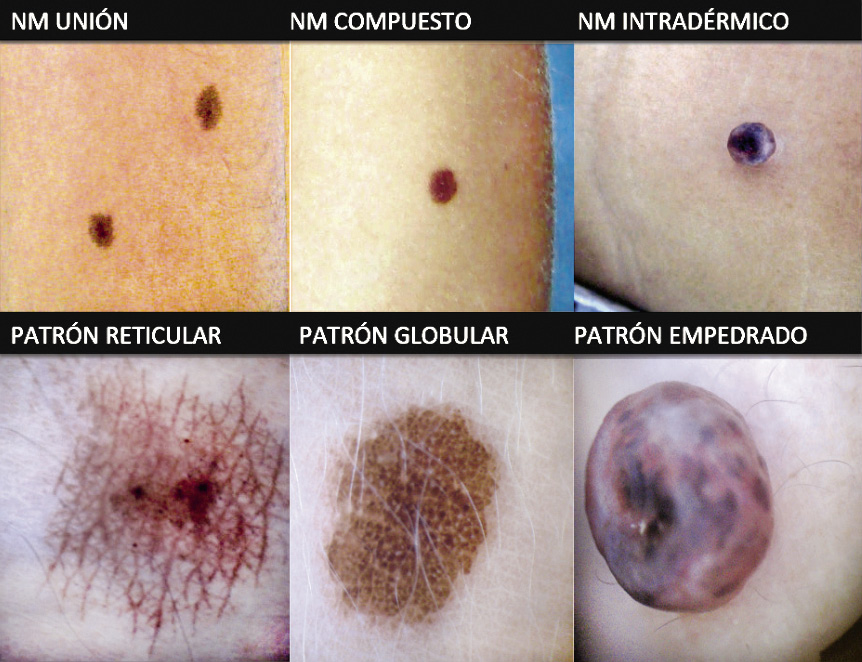
Clásicamente(3), atendiendo a la distribución de las células névicas a nivel histológico, según la teoría de la nevogénesis de Unna, se establecen tres categorías de nevus bien definidas (Fig. 2):
Figura 2. Nevus junturales o de la unión (lesiones planas, máculas), nevus compuestos (sobreelevadas) y nevus intradérmicos. Patrones dermatoscópicos correspondientes.
1. Nevus juntural o de la unión: clínicamente, se caracteriza por ser una mácula hiperpigmentada no palpable de tamaño y color variable. La superficie es lisa conservando las líneas habituales de la piel. La forma suele ser redondeada o elíptica, simétrica, de límites regulares y bordes netos. Histológicamente, están constituidos por células névicas agrupadas en nidos pequeños o melanocitos aislados en la unión epidermodérmica. Estos nevus son los más frecuentes en las etapas medias(4) de la vida. Son las lesiones más sometidas a estímulos externos (traumatismos, radiación ultravioleta, infecciones…) y, por tanto, pueden experimentar variaciones a lo largo del tiempo, dentro de las cuales se encuentra la transformación maligna. Dermatoscópicamente, se caracterizan por un patrón reticular y, en ocasiones, homogéneo que posteriormente evoluciona a reticular. Este retículo es la expresión de la importante actividad de la unión epidermodérmica en estas lesiones.
2. Nevus compuesto: puede variar clínicamente desde una pápula ligeramente elevada a una lesión verrugosa, existiendo casos con diferentes volúmenes dentro de una misma lesión. Suelen tener folículos pilosos, en ocasiones, prominentes. Son los más frecuentes en los niños(5). Es muy característico, que durante los últimos años de la infancia y principio de la adolescencia sufran un aumento en su grosor y pigmentación llamando la atención a los padres y motivando la visita médica para su evaluación. Histológicamente, están constituidas por células névicas agrupadas en nidos de mayor tamaño localizados en la unión epidermodérmica y, en ocasiones, en la dermis papilar. Dermatoscópicamente, el patrón predominante es el patrón globular con glóbulos de mayor o menor tamaño, expresión de los diferentes nidos o tecas a distintos niveles de profundidad. En ocasiones, podemos encontrar patrones mixtos globular-reticular y globular-homogéneo dependiendo de la localización de las tecas y su tamaño.
3. Nevus intradérmico: lesión cupuliforme, sésil, escasamente pigmentada con telangiectasias superficiales, especialmente las lesiones localizadas en la cara. Pueden presentar pelos terminales prominentes en la superficie. Histológicamente, se caracteriza por estar constituido por células que han perdido la agrupación y han disminuido su capacidad de producir pigmento. Se distribuyen en la dermis papilar y reticular formando regueros de células con tendencia a la maduración neuroide. Son nevus estables que suelen permanecer sin variaciones a lo largo de la vida. Son los más frecuentes en los últimos años de la vida. Dermatoscópicamente, suelen tener un patrón en empedrado, constituido por: glóbulos muy grandes, angulados, densos de diferentes formas y tamaños.
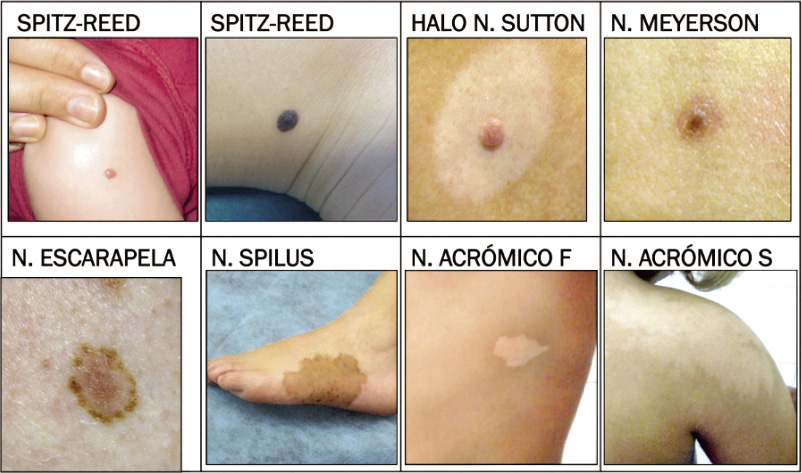
Además de los NMA comunes o vulgares comentados anteriormente, existen nevus con identidad propia (Fig. 3), con características especiales que los hacen diferentes al resto y constituyen una verdadera entidad independiente.
Figura 3. Figura resumen de los diferentes tipos de nevus especiales.
Entre ellos, encontramos los siguientes:
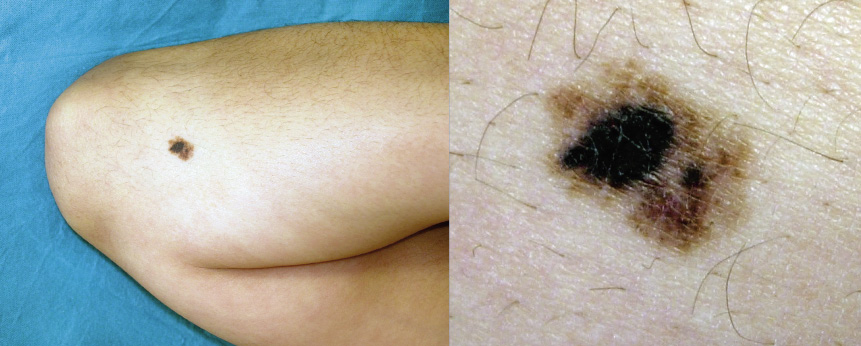
• Nevus de Spitz-Reed. Podría considerarse(6) un tipo de nevus compuesto que aparece con mayor frecuencia en los niños y adultos jóvenes, sobre todo, en las dos primeras décadas de la vida. Clínicamente, puede manifestarse de diferentes formas, siendo quizás la variedad más común, aquella caracterizada por una pápula o nódulo tumoral solitario, firme, redondeada, sin pelo, de superficie lisa y de color rojo o marrón rojizo. El color blanquea a la vitropresión, por la gran vascularización que posee, y muestra una pigmentación melánica residual que permite el diagnóstico diferencial con otras lesiones rojas como el granuloma piogénico o el xantogranuloma juvenil. Algunas lesiones, particularmente aquellas localizadas en las extremidades, son de color marrón oscuro intenso o incluso negro y son estas lesiones las que más alarman a médicos y pacientes por su diagnóstico diferencial con el melanoma. En ocasiones, adoptan una morfología atípica con diferentes tonos de color dentro de la misma lesión, superficie cutánea erosionada y bordes irregulares. Es de crecimiento rápido durante 3-6 meses, lo cual suele resultar bastante alarmante, y durante este tiempo puede sangrar debido al adelgazamiento de la epidermis, y causar prurito o dolor que suele ser transitorio, permaneciendo estable posteriormente. Se localiza preferentemente en: cara, sobre todo en mejillas, y en piernas, respetando siempre palmas, plantas y mucosas. La dermatoscopia es una técnica que ha mejorado mucho el diagnóstico de los nevus de Spitz, en concreto la variante pigmentada, recogiéndose cifras en la literatura que van de un 56% a un 93% de exactitud diagnóstica. Se han descrito dos principales patrones dermatoscópicos: globular y estallido de estrellas que suelen ser estadios evolutivos de una lesión en crecimiento. Su manejo es aún motivo de debate entre diferentes expertos. Muchos recomiendan su extirpación sistemática basándose en su comportamiento biológico incierto, existiendo casos de potencial agresivo con afectación de ganglios linfáticos regionales. Otros, sin embargo, abogan por “esperar y ver”, reservando la escisión quirúrgica para lesiones de formas muy atípicas o que experimenten cambios bruscos. En nuestra práctica clínica habitual, solemos extirpar todos los nevus de Spitz palpables (pápulas y nódulos), los que aparecen en niños mayores de 13 años peri puberales y los que son clínicamente atípicos. En cuanto a las lesiones planas de morfología típica en niños prepuberales, podría contemplarse la posibilidad de observación sin que este sea un hecho carente de discusión o polémica (Fig. 4).
Figura 4. Algoritmo de toma de decisiones en los nevus de Spitz. Gerardo Ferrara, Iris Zalaudek, Imma Savarese, Massimiliano Scalvenzi, Giuseppe Argenziano. “Pediatric Atypical Spitzoid Neoplasms: A Review with Emphasis on ‘Red’ (‘Spitz’) Tumors and ‘Blue’ (‘Blitz’) Tumors”. Dermatology 2010; 220:306–310.
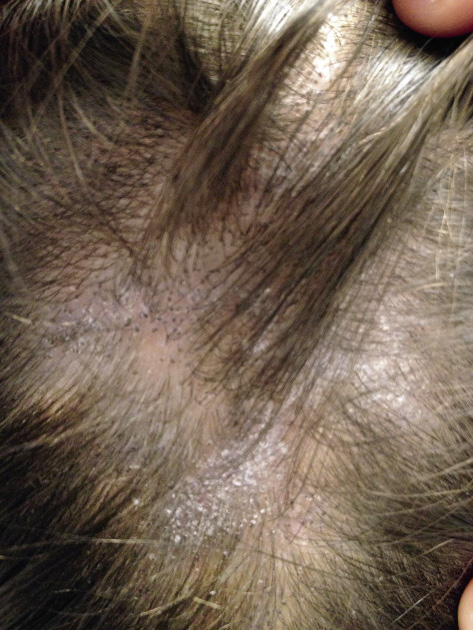
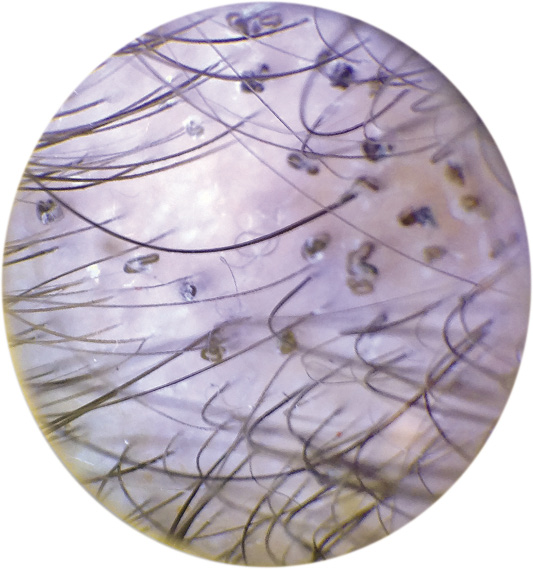
• Halo nevus de Sutton. Se caracteriza por ser un nevus rodeado de un halo simétrico y regular de piel despigmentada. Son lesiones muy frecuentes, sobre todo, en niños mayores y adolescentes con una media de edad de 15 años y sin diferencias entre sexos. Suelen localizarse en la parte alta de la espalda y hasta en un 25-50% de los pacientes son lesiones múltiples. El halo puede progresar hasta despigmentar por completo al nevus y hacerlo desaparecer en un periodo que oscila entre unos pocos meses a varios años. El área despigmentada residual tiende a recuperar el color normal con el paso del tiempo. En otras ocasiones, el nevus persiste. La causa de la pérdida espontánea de la pigmentación es desconocida, pero parece estar relacionada con una destrucción inmunológica de los melanocitos. Apoyando esta hipótesis, está el hecho de que algunos pacientes pueden desarrollar vitíligo. También, se ha demostrado su relación con el melanoma y los nevus atípicos, apareciendo abundantes halo nevus en pacientes con melanoma oculto, pero este hecho es propio de adultos y excepcional durante la infancia.
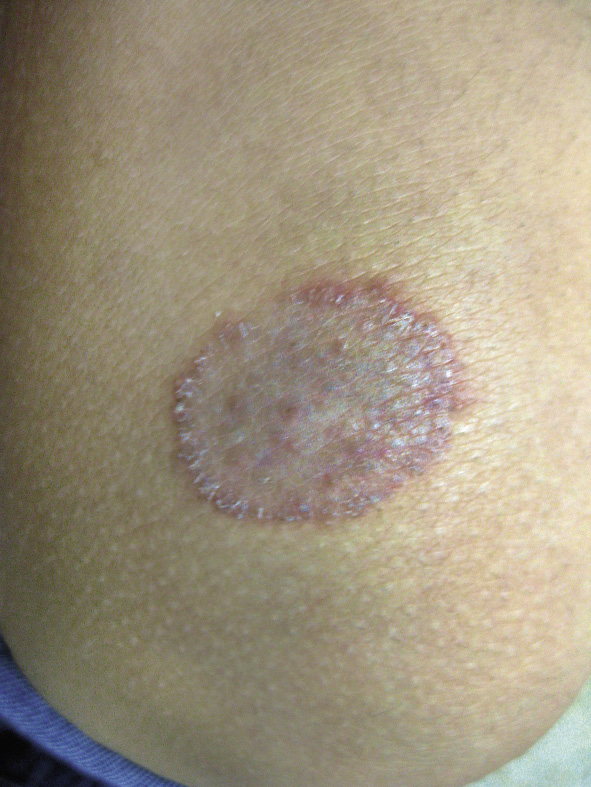
• Nevus de Meyerson. Consiste en un fenómeno benigno, por el cual una reacción inflamatoria eczematosa se desarrolla sobre y alrededor de un nevus melanocítico. Como todo eczema, se acompaña de prurito y descamación superficial. Es una lesión muy frecuente en niños con dermatitis atópica o psoriasis y el tratamiento consiste en tratar el eczema sin que exista la necesidad de extirpar el nevus.
• Nevus en diana o escarapela. Es un tipo morfológico de nevus típico de pacientes jóvenes y caracterizado por la existencia, dentro de la lesión, de tres zonas bien delimitadas: una zona central pigmentada, otra zona que la rodea más clara y otra externa nuevamente hiperpigmentada, siempre simétrica y de distribución regular del color. Por lo demás, es una lesión benigna sin mayor riesgo de malignización, por lo que únicamente requiere observación sin necesidad de extirpación.
• Nevus lentiginoso o moteado de Spilus. Se trata de la asociación de un acúmulo de nevus junturales lentiginosos o compuestos, agrupados sobre una mancha café con leche. En ocasiones, en fototipos altos puede no apreciarse el componente macular de base, y en otras circunstancias ser la única lesión existente. La lesión en su conjunto puede mostrar una forma redondeada y pequeña de escasos centímetros o ser muy extensa pudiendo alcanzar hasta los 20 cm de diámetro distribuyéndose en forma de cuadrantes. Suele ser adquirido, manifestándose por primera vez en las últimas etapas de la lactancia o primera infancia, pero en algunos casos son congénitos. En ocasiones, aparece primeramente la lesión macular de fondo, confundiéndose con una mancha café con leche y, posteriormente, se va cubriendo de lesiones melanocíticas superpuestas de escaso tamaño. Se presenta en poco menos que el 0,2% de los recién nacidos, en el 1 al 2% de los niños de edad escolar y en el 2% de los adultos, afectando por igual a ambos sexos y a todas las razas. Pueden aparecer en cualquier zona anatómica de la cara, tronco y extremidades, sin relación con la exposición solar. Persiste de forma indefinida. Existen varios casos asociados a melanoma, por lo que es importante su estrecho seguimiento y si aparecen cambios o atipias, proceder a su biopsia o extirpación.
• Nevus acrómico o despigmentado. Consiste en un área bien circunscrita y localizada de hipopigmentación de diferentes morfologías. Existe una forma segmentaria de distribución unilateral en cuadrantes o por las líneas de Blaschko, sin cruzar nunca de forma característica la línea media que denominamos mosaicismo hipopigmentado. El pelo dentro del nevus acrómico puede estar también despigmentado y los márgenes de la lesión pueden ser irregulares o serrados. Puede aparecer al nacimiento o en los primeros años de la vida, localizándose en cualquier región de la superficie corporal, siendo las más afectadas tronco y extremidades, sobre todo, espalda y nalgas, seguidas de tórax y abdomen, respetando: palmas, plantas y mucosas. Es importante destacar, que nunca van precedidas de un componente inflamatorio o lesión cutánea previa, pues de lo contrario estaríamos ante una lesión hipopigmentada residual y no de un nevus acrómico. Son más evidentes en verano y en los pacientes de piel oscura, siendo muy poco llamativos en los de piel clara durante el invierno. De la misma manera, pero en el sentido opuesto, podemos encontrar nevos hipercrómicos o hiperpigmentados. Aunque, en ocasiones, plantea difíciles diagnósticos diferenciales, se suele distinguir fácilmente de la esclerosis tuberosa segmentaria (asociada con frecuencia con otras máculas hipomelanóticas, con diferentes manifestaciones cutáneas y con un compromiso neurológico), del vitíligo (amelanótico y adquirido) y del nevus anémico (presentan enrojecimiento periférico frente a estímulos mecánicos como el frotado de la lesión).
Manejo clínico y signos de alarma
La mayoría de los motivos(7) de consulta de nuestra práctica diaria en relación a la patología melanocítica están relacionados con su apariencia cosmética, sintomatología reiterada (foliculitis subnévicas, irritaciones, prurito…) o dudas sobre su potencial de malignización. La mayoría de los nevus melanocíticos no precisan tratamiento y un buen seguimiento es más que suficiente para estar tranquilos y convencidos de su benignidad. En el pasado, muchos autores abogaban por la eliminación profiláctica sistemática de todas las lesiones pigmentadas de determinadas localizaciones: palmas, plantas y genitales, suponiendo un mayor riesgo de transformación maligna en estas zonas. Hoy día, se sabe que este hecho estaría injustificado y que la histología más atípica de estas lesiones es propia de su localización (continuamente sometida a traumatismos) sin que ello suponga un mayor poder de degeneración maligna. Podríamos realizar la extirpación profiláctica de lesiones únicas en las anteriores localizaciones, si se distribuyen en zonas de difícil acceso o visualización, que dificulten su control y seguimiento (sobre todo, en genitales) o lesiones aisladas en pacientes no colaboradores ni concienciados que incluso no acuden a las visitas, por su seguridad.
Aunque la posibilidad de malignización de un nevus adquirido es muy baja (tasa de transformación anual de un nevus en melanoma es de un 0,0005% para individuos menores de 40 años), ante cualquier duda o cambio brusco y sospechoso observado debe procederse a su extirpación y consiguiente estudio histológico. Existen una serie de cambios, en ocasiones, súbitos, que pueden sufrir los nevus sin que ello suponga malignización y que son importantes de conocer. En general, estos cambios no malignos suelen afectar a todos los nevus de un individuo o al conjunto de ellos que se hallan expuestos al mismo agente responsable de un cambio y al cabo de un tiempo (7 o 10 días) suelen volver a su situación basal. Un nevus puede cambiar en el color, en el tamaño y superficie, puede aparecer dolor, prurito, ulceración o sangrado y ser debido a causas fisiológicas o por agentes concretos, como es muy frecuente en la administración sistémica de glucocorticoides, o factores locales como: la exposición solar, los traumatismos, enfermedades ampollosas, foliculitis, traumatismos, trombosis en los pediculados, quistes epidérmicos…
A la hora de evaluar las lesiones pigmentadas de nuestros pacientes sería útil aplicar la conocida regla del ABCD(8), que habitualmente solemos ampliar a EFGHI como queda resumido en la Tabla I.
Hemos de considerar también, el número de lesiones o carga melanocitaria. Aunque un paciente tenga todos los nevus de morfología típica (ABCD) si posee un alto número (más de 50 o 100 nevus) tiene mayor riesgo de desarrollar melanoma por el simple hecho de que tiene más probabilidades por tener mayor número de lesiones. Estos pacientes deberán seguirse estrechamente en una unidad de lesiones pigmentadas de un servicio de dermatología, con dermatoscopia digital, ya que es muy difícil detectar cambios simplemente con la exploración física.
Es importante recoger en la historia clínica, los antecedentes familiares de cáncer, ya sea cutáneo o extracutáneo, (páncreas, vejiga, neoplasias hematológicas…) y, dentro de los cutáneos, melanoma o no melanoma, así como antecedentes personales y familiares de nevus displásicos confirmados histológicamente.
Teniendo en cuenta todos los factores expuestos con anterioridad, se consideran dos fenotipos de nevus melanocíticos, recogidos en la tabla II.
Diagnóstico diferencial
Los nevus deben diferenciarse de otras lesiones englobadas bajo los términos de hiperplasias melanocíticas epidérmicas y melanosis dérmicas circunscritas. En el primer grupo, el número de melanocitos es normal, pero estos son más grandes o contienen mayor cantidad de melanina y no existe riesgo de malignización. En el segundo grupo, los melanocitos se hayan profundos en la dermis, por lo que son de color azul característico. Sus características clínicas se resumen en la tabla III.
Nevus melanocíticos congénitos
Características clínicas y clasificación
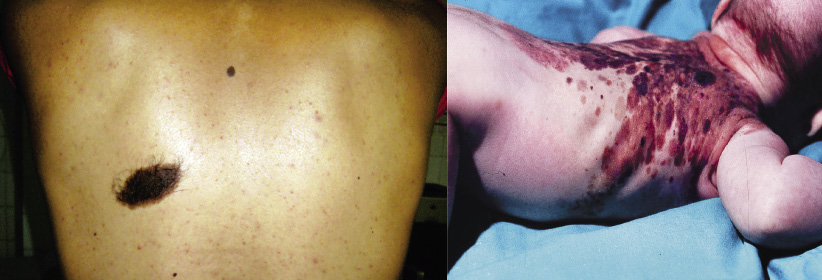
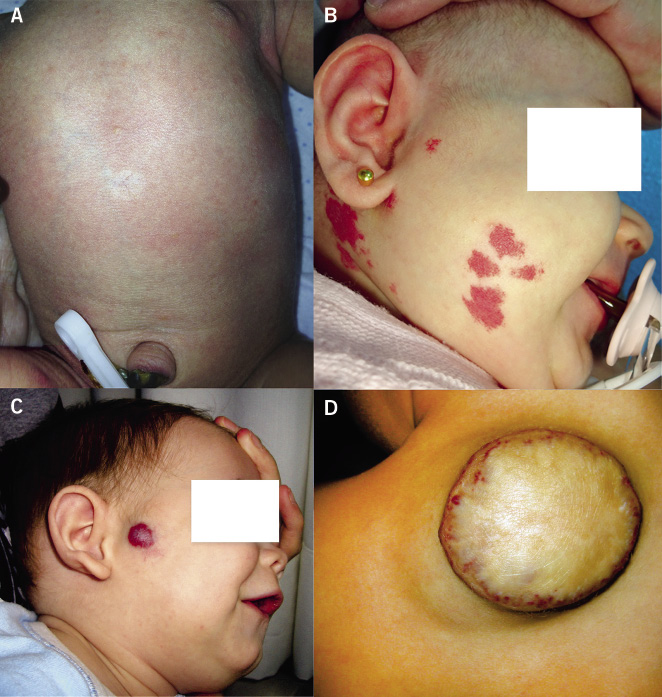
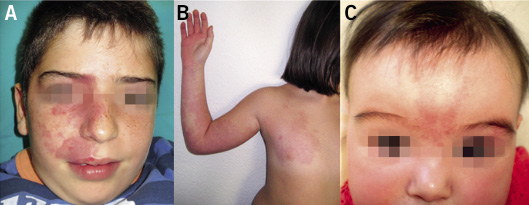
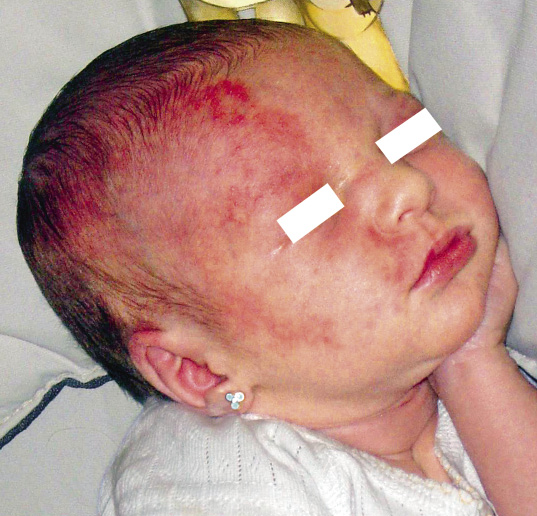
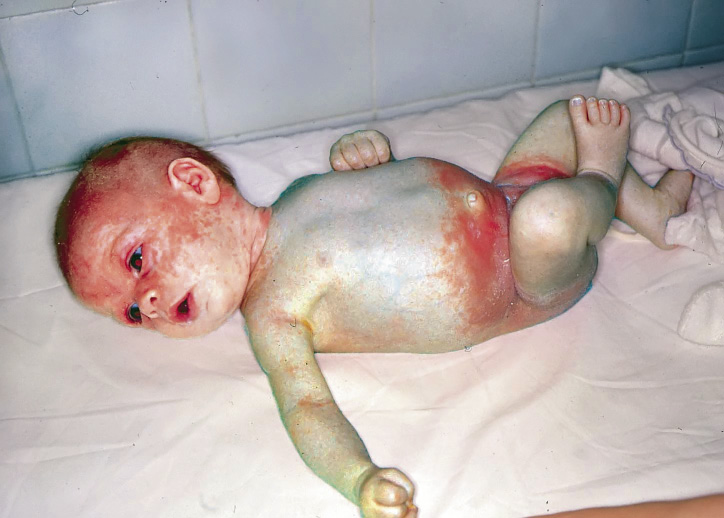
Clínicamente, se manifiestan como máculas de color marrón claro o rosado en el recién nacido. Durante los años siguientes, aumentan su tamaño, proporcionalmente al crecimiento del niño, se oscurecen y desarrollan pelos terminales. Tienden a engrosarse y arrugarse con el tiempo y pueden aparecer nódulos proliferativos generalmente benignos. En las lesiones grandes y gigantes, pueden ocurrir ulceraciones y erosiones sin que este hecho indique malignidad. Son frecuentes las variaciones en el color, lo que supone una dificultad adicional para su seguimiento y para apreciar cambios sugestivos de malignidad. Suelen localizarse, por orden decreciente, en: tronco, extremidades y cabeza, adoptando, en ocasiones, una morfología curiosa («en bañador», «en capelina», etc.). Además, presentan con frecuencia nevus melanocíticos «satélites» más pequeños en su vecindad. Se dividen clásicamente(9) en tres grupos, según el tamaño (Fig. 5) que alcanzarán en la edad adulta: pequeños (<1,5 cm de diámetro), medianos (1,5-20 cm de diámetro, son el grupo más numeroso, constituyendo el 70% de los nevus melanocíticos congénitos), grandes (>20 cm de diámetro o que midan la medida de la palma de la mano del paciente en la cara y cuero cabelludo o el doble de la palma de la mano en abdomen y tórax; son infrecuentes, presentándose en 1 de cada 20.000 nacidos vivos) y gigantes (>40-50 cm de diámetro. Nevus vestimentarios que, por su extensión, cubren toda una parte del cuerpo. Son los más raros, detectándose en 1 de cada 500.000 recién nacidos). Según la última clasificación(10) de consenso, también deben registrarse las siguientes características morfológicas de los NMC: coloración heterogénea, rugosidad en la superficie, nódulos dérmicos o subcutáneos e hipertricosis asociada.
Figura 5. Nevus melanocíticos congénitos mediano y gigante vestimentario en capellina.
Manejo clínico y signos de alarma
Los nevus melanocíticos congénitos, especialmente los gigantes, pueden asociarse a otras anomalías extracutáneas resumidas en la tabla IV(11).
Los dos problemas que generan los nevus melanocíticos congénitos, además de las asociaciones anteriores, son su potencial de malignización (directamente proporcional al tamaño) y la alteración estética, especialmente los gigantes. Los pacientes con nevus melanocíticos poseen un mayor número de melanocitos de lo normal y, por ello, presentan una probabilidad mayor de que alguno de ellos malignice. Se desconoce(12) la verdadera incidencia de la malignización y, aunque son muchos los trabajos que han intentado cuantificarla, los resultados no son homogéneos y tampoco aclaran la actitud terapéutica más adecuada que debemos seguir(13). Los últimos estudios sugieren que el riesgo de malignización es mucho más bajo del que se pensaba, en torno a un 0,7%-5%, y que afecta principalmente a lesiones de gran tamaño, nevus gigantes y los localizados en la línea media. La aparición de melanoma no siempre ocurre sobre el nevus congénito, sino que, en ocasiones, pueden aparecer sobre lesiones parcial o totalmente extirpadas e incluso alejadas de la lesión névica (músculos, peritoneo, fascia o SNC), y la extirpación radical de la lesión no elimina el riesgo de malignización. Por todo ello, la cirugía profiláctica está cada vez más en duda. Tras los últimos estudios y publicaciones, sobre todo, a partir del 2006, se observa que las etapas críticas de la malignización son: la edad escolar y la adolescencia, no los primeros años de la vida.
Como se deduce, no está todavía todo dicho sobre los nevus melanocíticos congénitos, ni se puede establecer aún un protocolo de seguimiento y tratamiento universal, sino que debemos enfrentarnos a cada paciente de forma individualizada, no olvidando que un buen seguimiento es imprescindible en todos los casos y considerando el riesgo de malignización, el resultado estético o funcional y simultáneamente el riesgo quirúrgico. En general, la actitud debería ser conservadora sin la extirpación rutinaria de todas las lesiones salvo que existan criterios clínicos o dermatoscópicos que así lo indiquen. Existen una serie de situaciones que podrían apoyar de forma relativa una extirpación profiláctica sin estar exenta de críticas y opiniones (Tabla V).
En los nevus de pequeño y mediano tamaño, la situación es más controvertida aún. Aunque algunos estudios sugieren que existe un mayor riesgo de degeneración, otros no lo indican. En cualquier caso, un abordaje multidisciplinar (pediatra, dermatólogo, radiólogo y cirujano plástico) y hacer a los padres partícipes de la toma de decisiones, mostrando los pros y contras de cada opción, facilitaría el manejo de estos pacientes y debe ser la actitud que hemos de perseguir.
Melanoma
El melanoma en la infancia(14) es raro, sobre todo, en la etapa anterior a la pubertad. La incidencia en niños y adolescentes menores de 15 años es de 1/millón. El melanoma supone el 15% de todos los cánceres entre los 15 y los 19 años y solo el 1,2% en los menores de 15 años.
Es un tema controvertido y del que aún queda mucho que aclarar, ya que no hay grandes series de casos. No se sabe mucho de sus factores pronósticos(15) ni comportamiento biológico. Puede aparecer de “novo” o sobre un nevus preexistente (más frecuente que en adultos), sobre todo, en los nevus melanocíticos congénitos grandes y gigantes. Los niños afectos de melanoma tienen un riesgo de desarrollar una segunda neoplasia que se estima en un 15%. Los factores de riesgo quedan recogidos en la tabla VI(16-18).
El melanoma infantil puede dividirse en cuatro grupos de edad:
1. Congénito (desde la fase intraútero hasta el nacimiento): cerca del 60% se desarrollan a partir de nevus melanocíticos congénitos medianos o gigantes. Un porcentaje pequeño lo constituyen casos de transmisión transplacentaria de un melanoma materno.
2. Infantil 1ª infancia (desde el nacimiento hasta el primer año de vida).
3. Infantil 2ª infancia (desde el primer año de vida a la pubertad).
4. Adolescente (tras la pubertad).
Habitualmente, el melanoma se presenta como una pápula o nódulo de rápido crecimiento, marrón oscuro o negro, aunque se pueden ver otros colores como rojo, azul o blanco. También existe la posibilidad de melanoma amelanótico, de color eritematoso y sin pigmento. Suelen ser lesiones asimétricas (Fig. 6), de bordes irregulares, coloración no homogénea en toda la lesión y grandes >10mm (criterios ABCD). Sangrado, prurito, ulceración, erosión y dolor pueden estar presentes y son cambios relevantes a tener en cuenta, sobre todo, si son recientes (en varias semanas o meses).
Figura 6. Melanoma de extensión superficial sobre nevus atípico en paciente de 13 años. Lesión asimétrica, de bordes irregulares con entrantes y salientes, coloración no homogénea y diámetro mayor de 6 mm.
Las localizaciones más frecuentes, al igual que en adultos, son: tronco y extremidades. Existen varias formas clínico-histológicas: melanoma de extensión superficial (forma más frecuente en la infancia. Suele tener lesión precursora o nevus previo), lentigo maligno melanoma (no existe en la edad infantil), melanoma nodular (forma más peligrosa, ya que su crecimiento es más rápido y se diagnostica tarde), melanoma lentiginoso acral (palmas, plantas o aparato ungueal) y otros (mucosas, amelanótico, desmoplásico, spitzoide, nevoide…).
El pronóstico del melanoma en niños, es superponible al melanoma que aparece en los adultos. El factor pronóstico más importante es el espesor tumoral o índice de Breslow, por lo que el único factor que aumenta la supervivencia hoy día es el diagnóstico precoz. El tratamiento es la cirugía del tumor primario con posterior ampliación de márgenes. En función del estadio el paciente, se podrá beneficiar de tratamiento adyuvante o paliativo con interferón alfa-2B y algunos regímenes de mono o poliquimioterapia. Actualmente, se están llevando a cabo diferentes ensayos clínicos con nuevas moléculas biológicas selectivas para el tratamiento del melanoma metastásico, que probablemente serán el futuro.
Fotoprotección
En los niños, tres factores se han visto claramente implicados en el desarrollo de nevus melanocíticos: exposición solar intermitente, quemaduras solares y piel blanca escasamente protegida (fototipos I y II).
Es por ello, de gran importancia, la educación a la población infantil en hábitos de exposición solar saludable (campañas) y su modificación de actitudes con respecto al sol, el bronceado y la fotoprotección(19) (tanto en lo que se refiere al uso de ropas y otras medidas físicas como la utilización de cremas protectoras).
Los fotoprotecores son aquellas sustancias que absorben y filtran la radiación UV. En la actualidad, también hay sustancias (vitamina C y E, carotenoides, polifenoles del té verde, flavonoides…) que actúan previniendo o reparando los daños inducidos por las radiaciones solares, lo que inactiva los radicales libres que se producen y que están involucrados en el envejecimiento, el cáncer de piel y la nevogénesis. Su uso correcto es fundamental para que sea efectivo. La mayor efectividad del fotoprotector se consigue aplicándolo de 15 a 30 minutos antes de la exposición solar y reaplicándolo cada 2 horas en las zonas fotoexpuestas o tras actividades físicas intensas que puedan eliminarlo de la piel (un secado enérgico puede eliminar hasta un 85% del producto). La reaplicación tras la inmersión en agua es necesaria siempre. El número del filtro solar (FPS) es un índice que significa el grado de protección que aporta una pantalla solar en el espectro entre 290 y 340 nm. Indica el tiempo durante el cual el producto nos protege en la exposición solar sin riesgo de tener quemaduras. Como depende de la cantidad de producto que se utilice, en muchas ocasiones, el valor del FPS verdadero o real no llega al 50 o incluso al 20% del indicado en la etiqueta del producto, por eso es tan importante insistir en que la cantidad de producto a aplicar sea la adecuada (regla del dedo). El FPS mide, sobre todo, la protección frente a UVB. En la Unión Europea, el método más usado para la medición del mismo es COLIPA.
Los fotoprotectores ante todo deben ser seguros, sobre todo, en la infancia. Los fotoprotectores químicos u orgánicos son muy variados. Lo ideal es utilizar aquellos que absorben radiación UVB y UVA como el Tinosorb M o Tinosorb S. Son filtros en general incoloros y cosméticamente muy aceptables, aunque presentan un mayor riesgo de reacciones alérgicas de contacto que las pantallas minerales o físicas.
Los fotoprotectores físicos, inorgánicos o minerales actúan como una barrera física. Se consideran muy seguros. Contienen pequeñas partículas de: dióxido de titanio, óxido de zinc, óxido de hierro, óxido de magnesio, mica, talco, caolín, ictamol o calamina. No son irritantes ni sensibilizantes, sin embargo, cosméticamente son algo peores, ya que la piel puede tornarse blanquecina al aplicarlos. Con las nuevas formulaciones micronizadas se ha mejorado enormemente este último aspecto y se ha eliminado la apariencia de “pasta blanca”. Se suelen usar combinaciones de varios para proporcionar estabilidad, seguridad y efectividad. Existen también fotoprotectores orales que podrían complementar a los tópicos como son: los betacarotenos, el polipodium leucotomos, las combinaciones de antioxidantes orales…, sin embargo, no hay estudios de eficacia en niños.
La FDA no recomienda la aplicación de fotoprotectores en niños menores de 6 meses, para evitar hipotéticos problemas de toxicidad secundarios a la mayor absorción de la piel del neonato. En mayores de 6 meses, los fotoprotectores que deben usarse deben tener un factor de protector mayor o igual a 25, deben proteger frente a las radiaciones UVA y UVB y, si fuese posible, infrarrojos y luz visible, deben ser lo más resistentes al agua posibles, al sudor, frotamiento y deben tener texturas lo más hidratantes y cosméticas posibles. No deben contener PABA (ácido paraaminobenzóico) ni benzofenonas, como la oxibenzona. Hay que aplicarlos generosamente, de 15 a 30 minutos antes de la exposición solar y reaplicarlos en las zonas fotoexpuestas de 15 a 30 minutos después de comenzada la exposición solar y, posteriormente, cada 2 horas o al bañarse, al frotarse con la toalla o al sudar excesivamente.
También es importante, entrenar a los pacientes y sus familias en la autovigilancia (detectar lesiones nuevas, cambios de lesiones preexistentes, signos de alarma…) y derivar a aquellos pacientes de especial riesgo a un servicio de dermatología(20), donde se pueda realizar un seguimiento más estrecho y controlado gracias a los nuevos avances en dermatoscopia y seguimiento digital dermatoscópico.
Bibliografía
Los asteriscos reflejan el interés del artículo a juicio del autor.
1.* Pellacani G, Scope A, Ferrari B, et al. New insights into nevogenesis: In vivo characterization and follow-up of melanocytic nevi by reflectance confocal microscopy. J Am Acad Dermatol. 2009; 61: 1001-13.
2.* Zalaudek I, Manzo M, Savarese I, Docimo G, Ferrara G, Argenziano G. The morphologic universe of melanocytic nevi. Semin Cutan Med Surg. 28: 149-56.
3.*** Schaffer J. Update on melanocytic nevi in children. Clinics in Dermatology. 2015; 33: 368-86.
4.** Westhafer J, Gildea J, Klepeiss S, et al. Age distribution of biopsied junctional nevi. J Am Acad Dermatol. 2007; 56: 825-7.
5.** Aguilera P, Puig S, Guilabert A, et al. Prevalence study of nevi in children from Barcelona. Dermatology. 2009; 218: 203-14.
6.** Ferrara G, Zalaudek I, Savarese I, et al. Pediatric Atypical Spitzoid Neoplasms: A Review with Emphasis on ‘Red’ (‘Spitz’) Tumors and ‘Blue’ (‘Blitz’) Tumors. Dermatology. 2010; 220: 306-10.
7.* Luelmo Aguilar J. Melanocyte nevus in childhood. An Esp Pediatr. 2001; 54: 477-83.
8.* Rubegni P, Cevenini G, Burroni M, et al. Objetive follow up of atypical melanocytic skin lesions: a retrospective study. Arch Dermatol Res. 2010; 302: 551-60.
9.*** Monteagudo B, Labandeira J, Acevedo A, et al. Prevalence and clinical features of congenital melanocytic nevi in 1000 spanish newborns. Actas Dermosifiliogr. 2011; 102: 114-20.
10. Price H, O´Haver J, Marghoob A, et al. Practical Application of the New Classification Scheme for Congenital Melanocytic Nevi. Pediatric Dermatology. 2015 (32); 1: 23-7.
11.* Shah K. The risk of melanoma and neurocutaneous melanosis associated with congenital melanocytic nevi. Semin Cutan Med Surg. 2010; 29: 159-64.
12.** Paradela S, Fernández-Torres R, Fonseca E. Controversial issues in congenital nevi. Actas Dermosifiliogr. 2009; 100: 548-61.
13.*** Price HN, Schaffer JV. Congenital melanocytic nevi when to worry and how to treat: facts and controversies. Clinics in Dermatology. 2010; 28: 293-302.
14.* Melinda Jen, Michael Murphy, Jane M. Grant-Kels. Childhood melanoma. Clinics in Dermatology. 2009, 27: 529-36.
15.*** Paradela S, Fonseca E, Pita-Fernández S, et al. Prognostic Factors for Melanoma in Children and Adolescents. Cancer. 2010, 15: 4334-44.
16. Psaty EL, Scope A, Halpern AC, Marghoob AA. Defining the patient at high risk for melanoma. International Journal of Dermatology. 2010, 49: 362-76.
17.* Avilés JA, Lázaro P, Fernández LP, et al. Phenotypic and Histologic Characteristics of Cutaneous Melanoma in Patients with Melanocortin-1 Receptor Polymorphisms. Actas Dermosifiliogr. 2011.
18.*** Nagore E, Botella-Estrada R, Requena C, et al. Clinical and epidemiologic profile of melanoma patients according to sun exposure of the tumor site. Actas dermosifiliogr. 2009; 100: 205-11.
19.*** Valdivielso M, Herránz JM. Actualización en fotoprotección infantil. An Pediatr (Barc.). 2010; 72: 282.e1-e9.
20.* Stratigos A, Katsambas A. The value of screening in melanoma. Clinics in Dermatology. 2009; 27: 10-25.
Bibliografía recomendada
– Antonio Torrelo. Nevus y trastornos del desarrollo. En: Antonio Torrelo. Dermatología en Pediatría General. Aula Médica. 2007. Madrid. Pág: 39-58.
Estupendo capítulo de libro, con conceptos claros y concisos sobre esta patología.
– Hernández A, Torrelo A. Recent data on the risk of malignancy in congenital melanocytic nevi: the continuing debate on treatment. Actas Dermosifiliogr. 2008; 99: 185-9.
Magnífica revisión y puesta al día de dos de nuestros más expertos dermatólogos pediátricos españoles.
– Cutaneous tumors and tumor syndromes. En: Amy Paller and Anthony Mancini. Hurwitz. Clinical pediatric dermatology. A textbook of skin disorders of childhood and adolescence. 3ª Edición. Elsevier. 2006.
Capítulo de monografía en lengua inglesa muy concisa, pero con buenos esquemas y guías de diagnóstico diferencial.
– Schaffer J. Update on melanocytic nevi in children. Clinics in Dermatology. 2015; 33: 368-86.
Maravillosa puesta al día en nevus melanocíticos congénitos y adquiridos, así como en melanoma.
– Valdivielso M, Herránz JM. Actualización en fotoprotección infantil. An Pediatr (Barc.). 2010; 72: 282.e1-e9.
Actualización completa y detallada y en español sobre fotoprotección en la infancia.
| Caso clínico |
|
Paciente de 10 años de edad, sin antecedentes personales ni familiares de interés, que consultaba por la aparición súbita de lesión pigmentada en la zona del talón de la planta del pie derecho de 24-48 horas de evolución. El paciente refería molestias en esa zona e incluso sangrado. A la exploración, el paciente, de fototipo III, presentaba escasos nevus en tronco y extremidades (<20) de características clínicas típicas: simétricos, bordes regulares, coloración homogénea y marrón uniforme (acorde con el fototipo) y diámetro escaso. Destacaban 3 lesiones en la planta del pie derecho. Dos de ellas (superior e inferior) las tenía desde hacía años, eran lesiones simétricas, de bordes regulares, coloración homogénea marrón en toda su superficie y diámetro 0,6 mm. La lesión nueva y por la que consultaba el paciente estaba cercana a la inferior, era algo asimétrica, bordes regulares y diferentes colores (marrón claro, oscuro y rojo).
|