|
| Temas de FC |
M. Güemes-Hidalgo*, M.T. Muñoz-Calvo**
*Departamento de Endocrinología. Great Ormond Street Hospital for Children. Londres. Reino Unido. **Servicio de Endocrinología. Hospital Infantil Universitario Niño Jesús. Profesora Asociada de Pediatría. Universidad Autónoma. Madrid
| Resumen
En la actualidad, la obesidad se considera un problema de salud pública mundial dado el aumento de su prevalencia, su continuidad en la edad adulta, los cambios en los estilos de vida de la población, la comorbilidad que se asocia y la baja percepción del riesgo por parte de la población. La prevalencia actual de obesidad infantojuvenil en nuestro país se estima en un 12,6%. Determinados sujetos pueden tener una mayor predisposición genética a aumentar de peso, y los genes pueden no expresarse totalmente hasta la etapa adulta. A continuación, se aborda: la etiopatogenia multifactorial, la comorbilidad, así como el abordaje diagnóstico, terapéutico y la prevención que debe iniciarse en edades precoces, ya que los hábitos de salud se establecen en la infancia y posteriormente será difícil modificarlos. El diagnóstico es fundamentalmente clínico. El tratamiento es multidisciplinar, actuando sobre el paciente y su entorno. El pediatra tiene un papel importante detectando los factores y poblaciones de riesgo, colaborando en el tratamiento y ejerciendo una acción preventiva educadora en los diferentes niveles: familiar, escolar, social y político. |
| Abstract
Obesity is considered a worldwide public health problem given its increasing prevalence, its continuation into adulthood, society ́s lifestyle changes, the associated comorbidities and society ́s low perception of its risk. Spain ́s current estimated prevalence among children and adolescents is 12.6%. Certain individuals have a higher genetic predisposition to gain weight, although the genes involved may not be fully expressed until adult age. This review includes the multifactorial pathogenesis, comorbidities, diagnostic and therapeutic approaches, and prevention strategies. The latter ought to be commenced in early ages as health habits are established during infancy, hence the difficulty in modifying these at a later stage. The diagnosis remains mainly clinical. The management requires a multidisciplinary intervention over the patient and their environment. The pediatrician has a significant role in identifying risk factors and at-risk individuals, participating in treatment and conducting preventive educational actions at different levels such as family, school, social and political. |
Palabras clave: Sobrepeso; Obesidad; Alimentación saludable; Actividad física; Prevención; Estrategias comunitarias; Infancia
Key words: Overweight; Obesity; Healthy eating; Physical activity; Prevention; Community strategies; Childhood
Pediatr Integral 2015; XIX (6): 412-427
Obesidad en la infancia y adolescencia
Introducción
En los últimos años, la obesidad ha ido aumentado de forma alarmante a nivel mundial, constituyendo un problema de salud pública.
Según la OMS (2015), la prevalencia de la obesidad (OB) en la población infantojuvenil va en aumento en todos los países, y los ascensos más rápidos se registran en los países de ingresos bajos y medianos. El número de lactantes y niños pequeños con sobrepeso (SP) u OB se incrementó en todo el mundo, de 31 millones en 1990 a 42 millones en 2013. Si la tendencia actual continúa y no se interviene, se llegará a los 70 millones en 2025. Ya en mayo de 2004, la 57ª Asamblea Mundial de Salud declaró a la OB como la epidemia del siglo XXI.
La OB infantojuvenil constituye un importante problema de salud debido no solo a su prevalencia ascendente, sino también a su persistencia en la edad adulta, su asociación con otras enfermedades, además del enorme impacto económico que supone(1). Cuando se inicia en la segunda década de la vida, es un factor predictivo de obesidad adulta y si continúa en el tiempo, se asocia con un mayor riesgo de enfermedad cardiovascular y de muerte(1,2).
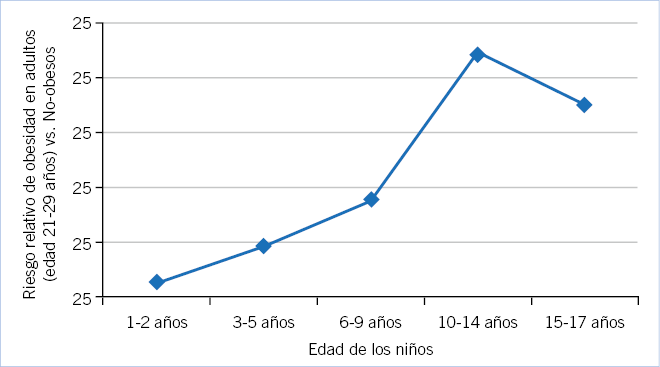
En la figura 1, puede observarse que, independientemente de la adiposidad de los padres; la probabilidad de que la OB infantil persista en la edad adulta, aumenta simplemente con la edad, con un agudo incremento en el periodo peri puberal(3).
Figura 1. Riesgo relativo de ser un adulto obeso (21-29 años) sobre la base de si se es obeso de niño, según las diferentes edades. Fuente: M Rosenbaum. Special Considerations Relative to Pediatric Obesity. Endotext [Internet]. www.endotext.org
La OB es el trastorno nutricional más frecuente en la población infantojuvenil y tiene su origen en una interacción genética y ambiental-conductual, siendo esta última la más importante, ya que establece un desequilibrio entre la ingesta y el gasto energético. El desarrollo del SP y posteriormente la OB, gira en torno a vivir en “la sociedad de la abundancia” donde junto a una importante oferta de alimentos hipercalóricos, coexisten cambios en los estilos de vida, como el sedentarismo, e inadecuados hábitos alimentarios, con una ingesta basada en las características organolépticas de los alimentos desconociendo sus características nutricionales.
En los últimos años, se han adquirido conocimientos en los mecanismos reguladores del peso y de la composición corporal descubriéndose nuevas hormonas, genes y vías reguladoras, pero el tratamiento de la OB sigue siendo uno de los problemas más difíciles de resolver en la práctica clínica. Los pilares del tratamiento son modificar la conducta alimentaria, estimular la actividad física y motivar al paciente; en la infancia se añade, además, la influencia familiar, ya que los niños aprenden por imitación y los hábitos que se establecen en la infancia tienden a mantenerse en la edad adulta. Es preciso un tratamiento multidisciplinar que puede ser coordinado por el pediatra quien, además de identificar las poblaciones y factores de riesgo, debe educar e instaurar medidas preventivas, y saber cómo abordar a los pacientes y sus familias. Serán precisas además, intervenciones en el ámbito escolar, sanitario y comunitario(1).
Concepto de sobrepeso y obesidad
En la práctica clínica, la estimación del contenido graso corporal se realiza determinando el Índice de Masa Corporal (IMC), a pesar de que aporta escasa información sobre los diferentes depósitos grasos corporales. El IMC se calcula dividiendo el peso (kilogramos) por la talla (metros) al cuadrado.
La OB consiste en el acúmulo de tejido graso en el organismo en relación con otros componentes corporales y suele ser el resultado de un balance energético positivo. Se acepta, que un niño presenta OB cuando su IMC sobrepasa en dos o más desviaciones estándar (DE) el valor medio de este parámetro estimado en individuos de la misma población, edad y sexo. Por el contrario, el concepto de SP hace referencia a aquellos individuos que presentan un exceso de tejido graso, pese a lo cual su IMC no sobrepasa +2 DE en idénticas condiciones a las anteriormente mencionadas(4).
Para la edad pediátrica, la International Obesity Task Force (IOTF) propone utilizar las gráficas de Cole et al. para definir el SP y la OB(5). Tomaron muestras representativas de poblaciones de EE.UU., Brasil, Reino Unido, Hong Kong, Singapur y Holanda y combinaron los datos. Se definieron los valores de IMC para cada sexo entre 2 y 18 años que se corresponden con los valores de 25 y 30 kg/m2 del adulto, equivalente a puntos de corte de SP y OB. Los niños y adolescentes con SP se corresponden con un percentil 85 y la OB con el percentil 95.
La Guía de Práctica Clínica para la Prevención y Tratamiento de la Obesidad Infanto-Juvenil(6), considera los criterios para definir el SP y la OB, los percentiles 90 y 97, respectivamente, específicos para edad y sexo, referido a los datos y curvas de Hernández et al., del año 1988.
El término “obesidad mórbida” se emplea, en ocasiones, para definir aquellos individuos con comorbilidades asociadas a OB. A menudo se usa de forma errónea para definir OB grave, con connotación negativa para el sujeto, por lo que se desaconseja su empleo.
Epidemiología
La prevalencia de SP y OB infantojuvenil en España sigue siendo muy alta (cercana al 40%), pero no ha crecido en los últimos 12 años. Se estima, actualmente, una prevalencia de obesidad del 12,6%, y de sobrepeso del 26,0% con ligero predominio en los varones y se asocia con clase social y nivel de estudios inferiores.
En los países occidentales, se ha señalado un rápido aumento de la prevalencia de OB en los últimos años, afectando por igual a ambos sexos, a todos los grupos de edad, a distintos grupos raciales, a familias con alto y bajo nivel económico, tanto en el medio rural como en el urbano.
La prevalencia de la OB infantil en nuestro medio es difícil de precisar. En parte, debido a los distintos criterios empleados en los diferentes estudios efectuados. El estudio enKid (utilizando las gráficas de Hernández et al.), desarrollado de forma multicéntrica entre los años 1998 y 2000, arrojaba cifras de prevalencia de OB del 12% para las niñas y del 15,6% en el caso de los niños, así como del 13% respecto al SP, si bien la distribución de los pacientes incluidos no era uniforme, predominando la franja infantil(2).
A través de los estudios: Paidos’84 donde el 4,9% de los niños de 6-12 años eran obesos, Ricardin-1995 y EnKid-1998-2000(2), se observa que se triplicaron las cifras y que el IMC medio aumentó un 0,7 kg/m2 y 2,7 kg/m2 en niños de 10 y 13 años, respectivamente. Todo ello condiciona que las expectativas de futuro para la población adulta sean muy negativas. Durante el periodo 1979-2001, el estudio GALINUT también demostró un incremento significativo de la media del IMC. El estudio AVENA (Alimentación y Valoración del Estado Nutricional en Adolescentes) desarrollado en varias ciudades españolas en el período 2000-2002, demostraba una prevalencia de SP más OB en adolescentes de 13 a 19 años del 25,69% y 19,13% en varones y mujeres, respectivamente(7). Según el estudio transversal español de crecimiento, realizado en 32.064 sujetos (16.607 varones y 15.457 mujeres), desde el nacimiento hasta la talla adulta, en una población caucásica española procedente de Andalucía, Barcelona, Bilbao y Zaragoza, realizado entre los años 2000 y 2004, afirmaban que en nuestro país y en cualquier edad en la infancia y la adolescencia, valores superiores a los de los percentiles 80 y 85, podrían utilizarse respectivamente para definir el SP en varones y mujeres, y que valores superiores al percentil 97 definirían OB en ambos sexos(8).
El Ministerio de Sanidad en el año 2006 publicó los datos nacionales correspondientes a la última Encuesta Nacional de Salud de España, en población de 2 a 17 años, donde observaban una prevalencia de OB del 8,9% y de SP del 18,7%.
En un reciente estudio realizado en 2012 sobre la prevalencia de la OB en la población infantojuvenil española entre los 8-17 años(9), se observa que la prevalencia de sobrepeso es del 26% y la de OB del 12,6%; 4 de cada 10 jóvenes sufren exceso de peso. En el grupo comprendido entre los 8 y los 13 años, el exceso de peso supera el 45%, mientras que para el grupo de 14 a 17 años, el exceso de peso es del 25,5%. La OB se asocia con las clases sociales más desfavorecidas y con menos estudios. Aunque la prevalencia sigue siendo muy alta, parece que no ha crecido en los últimos 12 años(9).
En Europa, la tasa de OB en niños y jóvenes ha aumentado considerablemente en las dos últimas décadas y, en la actualidad, son los países del sur de Europa los que expresan las cifras más elevadas, con tasas de sobrecarga ponderal entre el 20% y el 35%, frente al 10%-20% en países nórdicos(1,2). Estudios realizados en Estados Unidos, estiman que la prevalencia de OB en algunos grupos de edad de este colectivo se ha duplicado en relación con las tasas de los años setenta. En la población adolescente americana, se estima un aumento de la tasa del 5%(2).
En la figura 2, se recoge la prevalencia de SP y OB en la población infanto-juvenil (5-17 años) en diferentes países.
Figura 2. Porcentaje de sobrepeso y obesidad en niños de 5-17 años de edad de diferentes países. Fuente: The Organisation for Economic Co-operation and Development (OECD) (2011), Health at a Glance 2011: OECD Indicators, OECD Publishing. doi: 10.1787/health_glance-2011-en.
Etiología. Factores de riesgo
La identificación de factores genéticos y ambientales causantes del disbalance energético servirá para plantear estrategias preventivas.
La etiología de la OB es compleja y multifactorial. Se tendrán en cuenta factores individuales y biológicos (metabólicos y genéticos), así como los conocimientos, actitudes y comportamientos. Las influencias biológicas contribuyen entre un 30-70% en la determinación de la obesidad y las ambientales modulan su manifestación y el grado de OB. También, se considerará el balance energético positivo por una mayor ingesta de alimentos ricos en grasas, pobres en agua y fibra y el incremento del tamaño de las raciones. Igualmente, las causas que originan una disminución del consumo de energía que favorecen la inactividad física y el ocio. El ambiente económico, político y sociocultural facilitará las causas anteriores.
Los factores de riesgo (FR) de obesidad se exponen a continuación:
• Factores genéticos. Diversos estudios han encontrado asociación entre el IMC de los padres y de los hijos a partir de los 3 años. Si uno de los padres es obeso, el riesgo se triplica, si son ambos se multiplica por 15. También se hereda el patrón de distribución de la grasa, de la masa magra y otros FR cardiovascular. Es difícil diferenciar el origen genético y ambiental por la gran influencia de los estilos de vida similares entre padres e hijos.
• Exposición durante el periodo fetal. La hipótesis de Barker establece: que una agresión in útero produce una programación anormal del desarrollo de órganos y aparatos que se manifestará en etapas tardías de la vida(12). Ejemplo: la exposición al tabaquismo durante el embarazo y el sobrepeso en la infancia, se explica por la pérdida de apetito materno por la nicotina y una vasoconstricción y compromiso en la circulación útero-placentaria, además de exposición a mayores niveles de CO2, de esta forma disminuye el aporte de O2 al feto, se produce una afectación de su crecimiento y desarrollo, con impronta metabólica y efectos sobre su salud a corto, medio y largo plazo(10).
• Peso al nacimiento. Se ha observado una asociación positiva entre macrosomia (peso superior a 4 kg al nacimiento) y padecer OB en la infancia y edad adulta(11). También se ha observado una relación entre el bajo peso al nacimiento y el síndrome metabólico, observándose un mayor riesgo para la OB central. Los recién nacidos pequeños para la edad gestacional que ganan rápidamente peso durante los primeros meses de vida, son los que presentan más riesgo de desarrollar OB en la adolescencia tardía(11).
• Alimentación en el primer año de vida. Protección de la Lactancia materna (LM). Los lactantes alimentados con LM tienen menor riesgo de desarrollar OB que los alimentados artificialmente(11) y podría incrementarse con la duración de la LM. Además, son más capaces de autorregular su alimentación que los lactados con fórmula. Los lactantes en los que se introduce alimentación complementaria antes de los 4-6 meses de vida presentan una mayor ganancia ponderal y se asocia con menor duración de LM(11).
• Precocidad del rebote adiposo. En las curvas del IMC se ha identificado un crecimiento en el primer año de vida que decrece posteriormente llegando a valores mínimos entre los 5-6 años, momento en que se produce un nuevo aumento hasta la edad adulta. Esto se ha llamado “rebote adiposo” y cuando se produce precozmente antes de los 5 años de edad, conduce a una elevación rápida del IMC y se asocia con mayor riesgo de OB en la edad adulta(11).
• Etapa de la adolescencia y maduración sexual precoz. La adolescencia es una etapa de riesgo, ya que la probabilidad de que un niño obeso se convierta en adulto obeso aumenta del 20% a los 4 años de edad a un 80% en la adolescencia. Diferentes estudios han observado que la aparición precoz de la menarquía (< o igual a 11 años) incrementa el riesgo de OB en la época adulta.
• Sexo y edad. Diversos estudios han observado una prevalencia de obesidad superior en los varones. En el estudio Enkid, en los varones era del 15,6% y en mujeres del 12,0%, y también para el SP (14,3% vs.10, 5%, respectivamente). Por edades, la OB fue superior de los 6 a los 13 años(2,9).
• Nivel socioeconómico (NSC). El NSC elevado es un FR de OB en los países pobres y en los de transición. En el estudio Enkid(2), la OB fue mayor en niveles socioeconómicos y de instrucción más bajos (15,1 y 15,2%, respectivamente).
• Distribución geográfica. El medio rural parece ser un factor de protección de la OB en los países pobres y de transición nutricional, sin embargo, en estudios en países desarrollados se ha identificado como de riesgo.
• Estilos de vida:
- Tipo de Alimentación: En el estudio Enkid(2), se evidenciaron como factores protectores para la OB, además de la LM durante tres o más meses, el consumo de 4 o más raciones de frutas y verduras al día, un consumo graso menor del 35% del aporte energético total, el fraccionamiento de la ingesta diaria en 3 o más comidas al día y un estilo de vida activo.
Por el contrario, el consumo elevado de productos de bollería, refrescos azucarados y embutidos, un perfil dietético con un 38% o superior de la ingesta energética a partir de las grasas, la ausencia de la ración del desayuno y una baja actividad física, dedicando 3 o más horas al día a ver TV, aumentaba la probabilidad de ser obeso.
- Actividad física. La actividad física moderada se identifica como un factor protector de OB(11). A partir de la Encuesta Nacional de Salud(9) se estimó que los niños pasan una media de 2 horas y media al día viendo la TV, a lo que hay que sumar media hora adicional jugando con el ordenador o videojuegos.
- Sueño. Varios estudios han encontrado relación entre la menor duración del sueño y la OB infantil. En el estudio Enkid(2), la prevalencia de OB fue inferior en el grupo que dormía una media de 10 horas en relación con los que dormían menos de 7 horas. Por otro lado, el 47% de los niños obesos tienen problemas respiratorios del sueño moderados-intensos.
• Sociedad. Influencia de los medios de comunicación, la escuela, el barrio y la ciudad en que se vive. Estos dependen de políticas que afectan a la ordenación del sistema educativo, del mercado de la alimentación y de las condiciones sociosanitarias locales(12).
• Otros. Se investiga el posible papel de la flora microbiana intestinal, toxinas ambientales (“disruptores endocrinos”) y virus.
Clasificación
Dentro de los tipos de obesidad, la más frecuente es la exógena o poligénica, cuya etiología es multifactorial.
1. Obesidad exógena: es la más frecuente de las causas de OB, siendo la etiología multifactorial. La acumulación del exceso de energía en forma de tejido adiposo es debida a la existencia de una inadecuada nutrición, así como una disminución de la actividad física. Estos factores ambientales actuarían sobre una base poligénica que determinarían el desarrollo de un fenotipo obeso.
Se han descubierto unos 52 polimorfismos (variantes alélicas) asociados a rasgos de obesidad. El primero en descubrirse fue el gen FTO, relacionado con patrones de alimentación que conducen a un mayor aporte energético, con un efecto pequeño, pero acumulativo, sobre el IMC(13).
2. Obesidad monogénica: el hipotálamo es un órgano clave en el control del metabolismo energético. Por una parte, es responsable de la sensación de hambre y saciedad y, por tanto, del ingreso energético; y por otra parte, mediante la modulación del sistema nervioso simpático, interviene en la termogénesis adaptativa y, por tanto, en el gasto energético, ambas funciones son controladas por diferentes neuropéptidos. En el núcleo arcuato existen dos estirpes neuronales funcionantes antagónicas; por un lado, el neuropéptido Y que genera estímulos orexígenicos, y por otro la proopiomelanocortina (POMC), encargada de señales anorexigénicas. La leptina es una hormona derivada de los adipocitos cuyos niveles circulantes se correlacionan estrechamente con la cantidad de tejido graso corporal. La leptina ejerce su efecto homeostático, en parte actuando sobre hipotálamo generando POMC.
En la actualidad, se conocen, al menos, 20 enfermedades monogénicas, cuya manifestación fenotípica más importante es la instauración de una OB de comienzo temprano, por mutaciones en los genes de: leptina, receptor de leptina, POMC, receptor 4 de la melanocortina (MC4R) y prohormona convertasa 1 (PCSK1).
La deficiencia congénita de leptina (OMIM: 164160) genera OB de inicio temprano (durante los tres primeros meses de vida) junto a un hipogonadismo hipogonadotropo(14).
Las mutaciones en el receptor de leptina (OMIM: 164160) y de POMC (OMIM:176830) presentan OB de inicio antes de los 6 meses de vida con un peso al nacer normal. Las primeras, asocian: deficiencia de TSH, hormona de crecimiento e hipogonadismo hipogonadotropo(14).
Las mutaciones en el MC4R (OMIM: 155541) suponen la causa más frecuente de OB monogénica (2,6%). La mayoría de las mutaciones son heterocigotas, heredadas de forma dominante. Clínicamente cursan con OB e hiperfagia(15).
Las mutaciones en PCSK1 asocian: OB de inicio temprano, diarrea, homeostasis glucídica anormal, hipogonadismo hipogonadotropo y niveles altos de proinsulina y POMC(15).
3. Obesidad asociada a síndromes polimalformativos:entre los múltiples síndromes dismorfológicos pediátricos en los que se puede observar el desarrollo de un mayor o menor grado de OB a lo largo de su curso evolutivo, cabe destacar:
- Síndrome de Prader-Willi (OMIM: 176270):
La secuencia clínica que presentan los pacientes afectos de este síndrome puede comenzar ya a lo largo del periodo fetal, con la presencia de polihidramnios y la escasez, en número e intensidad, de los movimientos fetales. Tras el parto, destaca la intensa hipotonía que presentan estos pacientes y que llega a causarles dificultades para la succión, comprometiendo su ganancia ponderal durante los primeros meses de vida; y desde los 12 a 18 meses, se desarrolla una hiperfagia incontrolable(16). Son típicos, determinados rasgos fenotípicos como: ojos de forma “almendrada”, hipogonadismo hipogonadotropo, retraso mental e hipotonía muscular.
Se desconoce el mecanismo por el que se ocasiona la OB en estos pacientes, debido a la falta de expresión de copias paternas de genes improntadores en la región 15q11.2q13, fundamentalmente del gen SNRPN (small nuclear ribonucleoproten polypeptide N) (OMIM:182279) y también del gen NDN (OMIM:602117). Puede estar causado por delecciones en el cromosoma paterno, disomía uniparental materna o mutaciones que afecten a la impronta de la región.
- Síndrome de Alstrom (OMIM: 203800):
Los pacientes encuadrados en esta entidad nosológica comparten con aquellos afectos del síndrome de Bardet-Biedl: la presencia de defectos neuroftalmológicos, la presencia de OB y la instauración frecuente de diabetes mellitus tipo 2 (en la 2ª o 3ª década de la vida). Sin embargo, se distinguen por la ausencia de retraso mental y de las alteraciones digitales; así como, por la existencia del rasgo más distintivo de este síndrome, como es la presencia de miocardiopatía de inicio a muy temprana edad(17). En estos pacientes, es frecuente la aparición, a largo plazo, de alteraciones metabólicas, tales como: la hiperuricemia y la hipertrigliceridemia.
El gen considerado responsable de esta entidad se denomina ALMS1(2p13.1). (OMIM: 203800).
- Síndrome de Bardet-Biedl (OMIM: 209900):
Las características cardinales de este síndrome son: la existencia, prácticamente constante de retraso mental (más acusado en aptitudes verbales que manipulativas), alteraciones digitales (sobre todo polidactilia postaxial), distrofia retiniana y alteraciones renales, tanto funcionales como anatómicas. En estos pacientes, la OB (más acusada en el subtipo 4 y mucho menos en el subtipo 2), comienza a instaurarse en torno a los 2 o 3 años de vida.
Hay que señalar, que el síndrome de Laurence-Moon (OMIM: 245800), con el que compartió denominación desde el año 1925, se diferencia de este por la ausencia de alteraciones digitales y la presencia, prácticamente constante de paraplejia espástica y, de la característicamente descrita, retinitis pigmentaria.
En la actualidad, se conocen varios subtipos diferentes de este síndrome (asociados a mutaciones en diferentes localizaciones genéticas), algunos de los cuales se presentan debido a la asociación de mutaciones en diferentes locus cromosómicos, por lo que se les ha definido como ejemplo de una posible herencia trialélica(18).
En la tabla I, pueden verse la semiología clínica que indica que la obesidad puede ser el resultado de un síndrome genético.
4. Obesidad secundaria: las lesiones del SNC que afectan a la región hipotalámica pueden cursar con OB, ya sean secundarias a traumatismos, a tumores o a su tratamiento (gliomas, hamartomas, disgerminomas), a secuelas de infecciones o a cierto grado de hipertensión endocraneal crónica compensada (portadores de válvulas de derivación en las hidrocefalias).
Menos del 1% de los casos de OB infantojuvenil se deberán a etiología endocrinológica. Estas endocrinopatías pueden ser: el hipercortisolismo primario (síndrome de Cushing) o secundario al uso terapéutico de glucocorticoides, el hipotiroidismo, el déficit de hormona de crecimiento, el pseudohipoparatiroidismo tipo 1a y el hiperinsulinismo.
Determinados fármacos (antipsicóticos, antiepilépticos y esteroides) pueden producir OB.
Diagnóstico
El diagnóstico de la OB se realiza mediante una historia clínica detallada, investigando los antecedentes personales y familiares, encuesta nutricional con hábitos dietéticos, además de la exploración física y determinadas pruebas complementarias según la situación del paciente.
Historia clínica
Ante un paciente con sospecha de OB, nos interesa realizar una historia clínica detallada y conocer los antecedentes personales, tales como: la edad gestacional, el peso y la longitud al nacimiento, el tipo de lactancia, o la edad de introducción de los alimentos sólidos, así como conocer la edad del inicio de la ganancia ponderal y el grado de actividad física. Es importante conocer la distribución de las comidas a lo largo del día, el número de comidas fuera de las comidas principales y la presencia o no de ingesta compulsiva. Asimismo, en las adolescentes, se debe investigar la presencia de oligomenorrea o alteraciones del ciclo menstrual. El estilo de vida sedentario puede valorarse por parámetros, como las horas de ver televisión o jugando con ordenadores, fácilmente registrados con cuestionarios sencillos.
Entre los antecedentes familiares, es importante conocer la etnia y país de origen, el peso y el IMC de los padres y hermanos y los hábitos dietéticos de la familia, utilizando principalmente encuestas nutricionales. Se debe valorar la historia familiar de hipertensión arterial, dislipemia, enfermedad cardiovascular, diabetes mellitus tipo 2 y OB de distribución central.
Examen físico
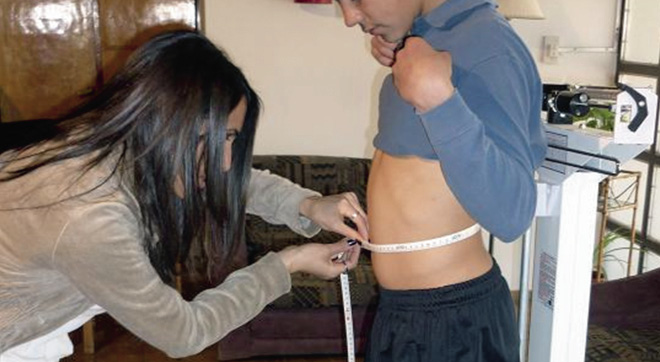
• Estudio auxológico: peso, talla, índice de masa corporal (IMC), perímetro de cintura (IDF 2004)
(Fig. 3).
Figura 3. Medida del perímetro de la cintura.
• Registro de la tensión arterial.
• Distribución de la grasa: obesidad abdominal.
• Rasgos dismórficos faciales: implantación del cabello y de los pabellones auriculares, paladar ojival o hendido, aplanamiento de la raíz nasal.
• Piel: acantosis nigricans, estrías, xantomas, hirsutismo.
• Desarrollo psicomotor.
• Presencia de alteraciones ortopédicas compensatorias (genu valgo), alteraciones de la marcha.
Pruebas complementarias
• Hemograma y bioquímica completa con transaminasas.
• Lipidograma: colesterol total, triglicéridos, C-HDL y C-LDL.
• Función tiroidea: T4 libre y TSH.
• Glucemia e insulina basal (cálculo de índice de sensibilidad para la insulina: HOMA: [glucosa (mmol) x insulina (microUI/ml)/22,5].
• Se debe realizar una sobrecarga oral de glucosa (SOG):
- Ante una obesidad moderada-grave.
- Si los niveles de glucemia son > 100 mg/dl.
- Si los niveles de insulina son > 15 microUI/ml.
- Antecedentes familiares de DM2 en 1º y 2º grado, etnia (hispana y afroamericana), hipertensión arterial, dislipemia y signos de resistencia a la insulina (acantosis nigricans, síndrome de ovario poliquístico).
Según la American Diabetes Association (ADA) 2015, se considera:
- Alteración de la glucemia en ayunas (AGA), cuando los niveles son > 100 mg/dl.
- Intolerancia a los hidratos de carbono: glucemia a las 2 horas de la SOG > 140 g/dl.
- Diabetes mellitus: glucemia en ayunas > 126 mg/dl o a las 2 horas de la SOG > 200 mg/dl, repetidas en dos ocasiones.
- Niveles de hemoglobina glicosilada como marcador de prediabetes: 5,7-6,4%, y diabetes > 6,5%.
• Rx de mano-muñeca izquierda: en general, los niños obesos presentan una edad ósea acelerada respecto a su edad cronológica, pero adecuada a la edad/talla del niño.
• El estudio de las concentraciones de adipoquinas y el estudio de las mutaciones monogénicas no están indicadas de forma sistemática
Comorbilidad asociada
Las consecuencias para la salud de la OB infantil incluyen numerosos problemas médicos que pueden verse en la tabla II. Además del riesgo de continuar padeciendo OB en la edad adulta (más riesgo a más edad y, especialmente, si se asocia con OB en los progenitores, el llamado fenómeno tracking), conviene tener presente que muchas de las complicaciones no se ponen en evidencia hasta pasadas algunas décadas.
Los factores nutricionales y los estilos de vida sedentarios, además de las enfermedades cardiovasculares, se relacionan con diabetes, tumores, osteoporosis y sus complicaciones.
Probablemente, los trastornos más frecuentes asociados a la OB infantil son los de tipo psicológico como: disminución de la autoestima, estigmatización y fracaso escolar. Ello les conduce a dificultades en: las relaciones amistosas entre pares, alteraciones del comportamiento, síntomas de depresión y ansiedad. Es difícil saber si estos trastornos psicológicos preceden a la OB o son consecuencia. Conocer esta diferencia es fundamental para planificar el tratamiento.
La OB y el SP pueden ser condiciones preexistentes, en algunos casos, de jóvenes que desarrollan trastornos del comportamiento alimentario, tales como: comer compulsivamente o hacer dieta de forma crónica. Aunque no se han encontrado evidencias que apoyen una relación estrecha entre bulimia o anorexia y OB, parece que hay riesgo de que una insistencia exclusiva en emplear la dieta como forma de mantener el peso y la imagen corporal, pueda contribuir al desarrollo de anorexia en niños con factores de riesgo psicológicos.
La OB se asocia con niveles de tensión arterial y triglicéridos elevados, niveles de C-HDL bajos, resistencia a la insulina y alteraciones vasculares e inflamatorias.
Hiperinsulinismo y resistencia a la insulina
En presencia de resistencia a la insulina, la célula beta pancreática incrementará la secreción de insulina y se producirá hiperinsulinismo. Si consigue compensar la resistencia insulínica, se alcanzará la normoglucemia, pero con los años este mecanismo compensador irá fallando y se producirá la intolerancia a los hidratos de carbono y la diabetes tipo 2. La hiperglucemia traerá como consecuencia glucotoxicidad con incremento del potencial aterogénico(19).
La determinación de la glucemia y la insulina en ayunas son necesarios para identificar las alteraciones de la homeostasis de la glucemia y reflejan fundamentalmente la secreción de insulina y la sensibilidad hepática y periférica. Además, tienen una alta especificidad y sensibilidad en identificar sujetos con resistencia a la insulina. La obesidad es el mayor factor de riesgo para el desarrollo de diabetes mellitus tipo 2 en los adolescentes(19).
Síndrome metabólico (SM)
Es el conjunto de alteraciones metabólicas y cardiovasculares que están relacionadas con la resistencia a la insulina y la OB abdominal, ejes centrales del síndrome que se desarrollaría en individuos metabólicamente susceptibles. Por ello y debido a que en las últimas décadas ha aumentado de forma importante su prevalencia, puede considerarse este síndrome un problema de salud pública de gran importancia, tanto en los países desarrollados como en algunos en transición económica y nutricional. Será abordado en el siguiente capítulo.
La OB infantojuvenil tiene asociados, además, unos costes económicos importantes. En España, representó el 7% del gasto sanitario en 2007. Padecer OB disminuye las expectativas de vida y aumenta el tiempo de estancia hospitalaria por cualquier proceso y en casi todas las edades.
Abordaje terapéutico
La base fundamental del tratamiento es la instauración de un programa multidisciplinar a largo plazo que asocie: educación nutricional, aumento de la actividad física y modificaciones de la conducta de la población.
En la actualidad, hay pocos ensayos aleatorios a largo plazo para poder determinar si las técnicas para prevenir y tratar la obesidad son eficaces. Las recomendaciones están basadas en consensos de expertos con experiencia clínica, observación de conductas que se asocian a la OB y evidencias científicas a corto plazo. Incluyen: medir el IMC y ver su evolución; evitar los factores de riesgo relacionados (intervenciones tempranas); utilizar intervenciones clínicas breves (mensajes educativos, centrados en el niño y la familia); establecer cambios a largo plazo centrados en la conducta que se asocia al riesgo de OB, en lugar de confiar exclusivamente en dietas y planes de ejercicio que tienden a establecer metas a corto plazo; e implementar un enfoque gradual en el control de peso para hacer frente a la OB en las diferentes edades y niveles de gravedad.
Dada la complejidad y variedad de los factores etiológicos involucrados en la génesis y mantenimiento de la OB y a las dificultades halladas hasta la fecha para lograr enfoques terapéuticos eficaces y resultados mantenidos, las recomendaciones propuestas se exponen a continuación.
En primer lugar, se debe realizar un correcto diagnóstico y asegurarse de que tanto el paciente como su familia desean iniciar el tratamiento, investigando la dinámica familiar. Se debe seguir el modelo de motivación al cambio de Prochaska y Diclemente(20). Según dicho modelo, las intervenciones se adaptarán en función del estadio en que se encuentre el paciente y la familia e incluyen 5 fases: Precontemplación: el individuo no considera la posibilidad del cambio. Contemplación: está considerando la posibilidad de cambiar, está planificando y comprometiéndose con el cambio. Acción: está realizando la conducta del cambio. Mantenimiento: sostener a largo plazo el cambio. El ciclo incluye la posibilidad de recaída, la que siempre debe ser anticipada para diseñar con el paciente como se enfrentará a ella.
La base del tratamiento de la OB es la instauración de un programa multidisciplinar a largo plazo que asocie: reorganización de los hábitos alimentarios, realización de actividad física y tratamiento conductual.
Reorganización de los hábitos alimentarios
Tiene como objetivo mejorar la sensibilidad a la insulina y prevenir o corregir las alteraciones metabólicas y cardiovasculares asociadas. Es importante corregir los errores como: la elevada ingesta de grasa a expensas de la disminución de los carbohidratos, la distribución de energía a lo largo del día, la selección de los menús y las técnicas culinarias. Si el paciente no responde a la corrección de los errores, se realizará una intervención nutricional.
En cuanto a la composición de la dieta, se aconseja una dieta equilibrada en la que el porcentaje de calorías aportadas por cada uno de los principios inmediatos sea: 50% en forma de hidratos de carbono, 30% de grasas y 20% de proteínas. Las proteínas deben ser de alto valor biológico. La grasa aportará ácidos grasos esenciales y vitaminas liposolubles, y favorecerá la sensación de saciedad. Asimismo, los alimentos con bajo índice glucémico ayudarán a controlar la sensibilidad a la insulina y las alteraciones lipídicas, así como asegurar un aporte extra de fibra que produce mayor sensación de saciedad y que disminuye la ingesta energética. Respecto a la ingesta de líquidos, la bebida habitual será la leche (requerimientos diarios) y el agua, evitando las bebidas azucaradas.
En los niños prepúberes, en general, se deben recomendar dietas normocalóricas, mientras se van desarrollando. No se recomiendan dietas hipocalóricas en menores de 2 años de edad. En OB moderada, será necesario una intervención nutricional con una dieta hipocalórica, calculada en función de la edad cronológica, no del peso. En obesidades graves, se utilizará dietas hipocalóricas llegando a restringir hasta un 20-25% de las calorías recomendadas al niño de la misma edad y sexo. Se distribuirá el total de las calorías en tres comidas principales y dos secundarias (media mañana y merienda), evitando periodos de ayuno prolongado, y evitando una ingesta rápida de comida, favoreciendo así la sensación de saciedad.
Existe otro grupo de dietas no aconsejable, tales como dietas muy restrictivas, sustitución por componentes líquidos o purificados de proteínas o dietas heterodoxas, donde no se aconseja su empleo en la edad pediátrica, debido a las posibles deficiencias nutricionales y complicaciones médicas asociadas.
Incremento de la actividad física
El ejercicio aumenta el gasto energético, mejora la sensibilidad a la insulina y disminuye la lipogénesis. Es útil para mantener la pérdida de peso y debe ser individualizado. Hay que estimular la realización de paseos diarios en niños que no tengan hábitos deportivos (ir al colegio andando o subir escaleras). Animarlos a que participen en deportes escolares y actividades deportivas durante el fin de semana. Es necesario que el ejercicio sea aceptado y forme parte de la vida diaria. Hay que evitar el sedentarismo, así como el uso de videojuegos y ver televisión demasiadas horas, en las que los niños tienen un consumo energético reducido y además, toman alimentos hipercalóricos. Asimismo, se aconseja la retirada de la TV y/o ordenador de las habitaciones de los niños y adolescentes, y limitar el tiempo dedicado a estos juegos.
Tratamiento conductual
Tanto el paciente como la familia deben tomar conciencia de las conductas que han conducido al exceso de peso, y deben ser capaces de introducir cambios en la alimentación y en los estilos de vida a medio y largo plazo. Se aconseja diseñar un plan de vida diario para toda la familia.
Los padres deberán aprender a controlar el entorno del hogar: tipos de alimentos que se compran, cómo se preparan, cómo se puede controlar el tiempo dedicado a la televisión, entre otros. El paciente irá aprendiendo a descubrir las situaciones, pensamientos o sensaciones que actúan de desencadenantes, incitándole a comer y también cómo se siente cuando cumple los objetivos. Se le darán pautas de comer sentado, masticar despacio, y no utilizar la comida para recompensas…
Se tendrán en cuenta los aspectos emocionales. Se evitaran las críticas o la estigmatización. Los profesionales deben utilizar la empatía y el estímulo. Con frecuencia son las sensaciones de tristeza o baja autoestima las que actúan como desencadenantes para ingerir alimentos. Se debe favorecer la imagen positiva de la alimentación, del ejercicio y del propio cuerpo ayudando a construir y reforzar la autoestima.
Es necesario proporcionar instrumentos para afrontar las situaciones estresantes o desencadenantes, mediante el entrenamiento en habilidades específicas para manejar el estrés, autoinstrucciones y formulación de objetivos. Se recomienda el apoyo psicológico con terapia conductual o cognitivo-conductual en menores y adolescentes (evidencia B). Hay que esperar recaídas, para las que se deben tener soluciones.
La entrevista motivacional, permite ayudar al paciente a descubrir sus deseos, emociones y motivaciones. Al centrarse en el paciente, permite que vaya descubriendo por sí mismo las barreras y dificultades, y lograr objetivos poco a poco, diseñando nuevas estrategias de superación adaptadas a cada situación.
Frente a la intervención paciente-profesional que con el tiempo aumenta el riesgo de fracaso terapéutico por desgaste de ambos, se perfila el tratamiento grupal que, aunque tienen algunas dificultades (perfiles de los profesionales a incluir, los contenidos adecuados a cada edad, el número de sesiones, el tiempo de seguimiento, etc.), parece que ofrece buenas expectativas.
Tratamiento farmacológico
La indicación del tratamiento farmacológico de la OB no debe utilizarse como terapia aislada, sino de forma complementaria a las terapias básicas de reeducación alimentaria, actividad física y tratamiento conductual.
El Comité de Expertos para la Prevención y Tratamiento de la Obesidad Infantil de la Academia Americana de Pediatría plantea su uso en la adolescencia, cuando no se hayan alcanzado los objetivos de pérdida de peso con los cambios en los estilos de vida y presenten comorbilidad severa.
Actualmente, solo está comercializado un fármaco con indicación aprobada para el tratamiento de la OB, el Orlistat(21). La sibutramina fue retirada del mercado en el 2010, por aumento del riesgo cardiovascular. La metformina no está indicada en la obesidad, pero sí en el tratamiento diabetes tipo 2 y en la alteración de la glucemia basal o la alteración de la tolerancia a la glucosa en pacientes con un IMC >35 kg/m2.
El Orlistat inhibe la acción de la lipasa pancreática y gástrica, lo que disminuye la absorción de grasa hasta en un 30%, con un perfil de seguridad favorable a pesar de efectos secundarios como: flatulencia, deposiciones grasas/oleosas y déficit de vitaminas liposolubles, en hasta un 50% de los pacientes(21). Es más eficaz cuando se asocia a control dietético y aumento de la actividad física. Su uso está permitido por la FDA a partir de los 12 años. El ensayo clínico con mayor número de sujetos y duración de seguimiento fue realizado en el año 2005 con Orlistat en una población de 539 adolescentes obesos durante 54 semanas, demostró una reducción significativa en el IMC y del perímetro de cintura(21). Es posible que mejore los FR cardiovasculares(22).
Tratamientos en fase de desarrollo
Actualmente, hay numerosos ensayos clínicos dirigidos a establecer la eficacia y la seguridad de diferentes sustancias, fármacos y hormonas neuroentéricas que participan de manera directa o indirecta en la regulación del peso corporal. La lorcaserina, fentermina, fentermina/topiramato y naltrexona/bupropion de liberación sostenida, son cuatro terapias adicionales para la pérdida de peso aprobadas para el manejo de OB en adultos, pero sin estudios en población adolescente(22).
La lorcaserina es un agonista del receptor de serotonina 5-HT2c que conduce a pérdida ponderal al aumentar la saciedad y disminuir el consumo de alimentos, posee beneficios sobre los FR cardiovasculares.
La fentermina es un simpatomimético que disminuye el apetito, estando aprobada por la FDA para duración breve en adultos, estando asociada a efectos adversos cardiovasculares. Su combinación con topiramato, también conduce a pérdida de peso significativa, así como la combinación del antagonista de opioides (Naltrexone) y el antidepresivo bupropion.
Otras medicaciones indicadas para otras condiciones médicas –distintas a la OB–, se ha visto que resultan efectivas para la pérdida de peso, como el bupropion, metformina, análogos de GLP-1 (glucagon-like-peptide-1), análogos de amilina y el topiramato.
Tratamiento quirúrgico
La Asociación Americana de Cirugía Pediátrica ha realizado unas recomendaciones para la práctica de Cirugía Bariátrica en adolescentes con OB mórbida (Tabla III). La sociedad Americana de Cirugía Bariátrica y Metabólica (ASMBS), recientemente, ha publicado la guía de práctica clínica para cirugía bariátrica pediátrica(23), recomendando un equipo multidisciplinar, incluyendo: cirujano bariátrico, pediatra especializado en obesidad, nutricionista, especialista en salud mental, especialista en la fisiología del ejercicio y un coordinador de salud, para evaluar el tratamiento óptimo para aquel niño candidato a cirugía bariátrica, basándose en la presencia de comorbilidades y fallo de otras intervenciones terapéuticas.
Las técnicas quirúrgicas más empleadas a nivel mundial en adolescentes y adultos son: el bypass gástrico mediante Y de Roux y la banda gástrica ajustable.
En un metaanálisis sobre adolescentes OB, la media de reducción de IMC fue de 17,8 a 22,3 kg/m2 con el bypass gástrico mediante Y de Roux, entre 1 a 6 años de seguimiento(24); mientras que fue de 10,6 to 13,7 kg/m2 en aquellos sometidos a banda gástrica, en estudios de 1-3 años de seguimiento. La banda gástrica mediante abordaje por laparoscopia, es una técnica restrictiva con colocación de una banda de silicona que circunda la parte proximal del estómago.
La gastrectomía en banda está en auge en adultos y adolescentes. Es una técnica menos compleja que la Y de Roux y con menor riesgo de déficit de micronutrientes y con disminución del IMC entre 32-37% en estudios en adolescentes(25).
La implantación endoscópica de un balón intragástrico por periodos máximos de 6 meses, produce una reducción ponderal leve y sus efectos secundarios más importantes son náuseas, vómitos, así como perforación o migración intestinal.
Recientemente, en 2015, la Canadian Task Force on Preventive Health Care (CTFPH)(26) ha dado una serie de recomendaciones con evidencia científica, para la vigilancia del crecimiento y la prevención y gestión del sobrepeso y la obesidad en los niños y adolescentes en AP. Recomienda intervenciones conductuales entre los 2 y 17 años y no recomienda ofrecer intervenciones farmacológicas o referir a los pacientes para intervenciones quirúrgicas, debido a la falta de datos que muestren efectividad y por los posibles daños potenciales. Aunque estadísticamente significativo, los beneficios clínicos de las intervenciones conductuales son pequeños y son necesarios datos a largo plazo para determinar si los beneficios se mantienen en el tiempo. En la tabla IV, pueden verse las recomendaciones sobre prevención y tratamiento del SP y OB según diferentes guías de práctica clínica.
Prevención
El mejor tratamiento de la obesidad infantil es la prevención, ya que es muy difícil tratar la obesidad una vez establecida.
Para luchar contra el SP y la OB infantil es fundamental la prevención primaria o universal, ya que es muy difícil tratar la enfermedad una vez establecida. Debe ser parte de una política nacional de salud pública para mejorar la alimentación y el ejercicio físico de la comunidad, disminuyendo el riesgo de enfermedades crónicas, mejorando la salud y la calidad de vida.
La intervención se basa en realizar consejos educativos a toda la población con especial enfoque hacia las familias, la población infantil y los distintos ámbitos sociales que les rodean: guardería, escuela, centros de salud, comunidad, ámbito legislativo y medios de comunicación(27) (Tabla V).
Los consejos forman parte del estilo de vida sana, que se adaptará a la edad del paciente, y las características socioculturales. El objetivo es promover y modelar actitudes positivas hacia la alimentación y la actividad física, sin centrarse en el peso corporal para evitar efectos adversos como los trastornos de la alimentación. Se realizará en los controles de salud programados y también de forma oportunista.
Se iniciará en la 1ª visita, con la promoción y apoyo a la lactancia materna. También se realizará intervención prenatal sobre factores relacionados con el peso elevado al nacimiento. El peso pregestacional y la ganancia de peso neta en el embarazo son las principales fuentes de información sobre las reservas nutricionales disponibles y el aporte nutritivo al feto(11). Se evitará culpabilizar y estigmatizar al paciente y las familias.
La prevención secundaria (cribado) se centrará en los niños con factores de riesgo para el SP y la OB. Aquí, es esencial la actuación médica identificando y dirigiendo a estos pacientes.
Aunque no existe suficiente evidencia para recomendar el cribado anual(6), dada la importancia del problema a prevenir, sí se recomienda monitorizar de forma periódica el peso, la talla y el IMC, que deben quedar reflejados no solo en la historia clínica, sino sobre las gráficas de crecimiento, para observar la tendencia. Además, hay suficiente evidencia que relaciona las técnicas de cribado con la detección de problemas de salud(6).
Una vez detectados los niños con FR, se debe evaluar: la alimentación, los conocimientos y actitudes hacia esta, la actividad física, así como los estilos de vida. El consejo se adaptará a la edad del paciente, aprovechando las actitudes y puntos fuertes(6).
La OMS y otros organismos, han llamado la atención sobre la necesidad urgente de poner en marcha planes de acción. En 2004, aprobó la Estrategia Global sobre Dieta y Actividad Física e instando a los estados miembros a la implantación de planes nacionales de actuación. Las estrategias de prevención frente a la OB infantil deben realizarse, como ya se ha comentado, a todos los niveles(27): familia, colegio, profesionales de la salud, industria, medios de comunicación y gobierno. En nuestro país, desde 2004, el Ministerio de Sanidad y Consumo lleva a cabo la estrategia NAOS (Nutrición, Actividad Física y Obesidad) con un programa específico dirigido de manera prioritaria a la intervención en el medio escolar, como es el Programa PERSEO (Programa Educativo de Referencia para la Salud, Ejercicio Físico y contra la Obesidad) realizado en diferentes provincias españolas entre los 6-10 años con resultados muy favorables.
Niño@s en movimiento es un programa multidisciplinario dirigido a niños de 7-12 años de edad con SP / OB y a su entorno familiar. Centra su atención en la salud general del niño, y no solo en el peso y la alimentación. También utiliza técnicas cognitivo-conductuales y afectivas. El estudio Evasyon es un programa educacional (nutricional y de actividad física) multidisciplinar, útil, dirigido específicamente a adolescentes con SP y OB, a partir de los resultados obtenidos del estudio AVENA. El programa Thao es un programa piloto nacional de prevención de la OB infantil que se realiza en el ámbito de los municipios, con acciones continuadas durante 4 años desde 2007. Dirigido a los niños escolarizados de 0 hasta 12 años, implicando a todos los actores en contacto con la población infantil.
Otras medidas adoptadas en nuestro país, incluyen el código de autorregulación de la publicidad de alimentos y bebidas (PAOS) y cambios en el etiquetado de los alimentos e información a los consumidores. El código PAOS pretendía proteger a los menores de 12 años de la presión excesiva de la publicidad de alimentos y bebidas, y ha sido muy positivo durante estos años también para garantizar el control y aplicación de las normas. Se revisó en 2013 para adaptar la publicidad en internet en menores de 15 años.
A nivel internacional, destacan: el proyecto HELENA (Healthy Lifestyle in Europe by Nutrition in Adolescence) y el proyecto HBSC (Health Behaviour in School-aged Children) o estudio sobre las conductas saludables de jóvenes escolarizados que se realiza cada 4 años; es un proyecto auspiciado por la OMS en el que participan más de 40 países occidentales.
Actividades del pediatra de Atención Primaria
El pediatra de AP tiene un papel esencial en la detección precoz, tanto del SP y OB como de los factores y poblaciones de riesgo, el tratamiento y la instauración de medidas de promoción y prevención en los diferentes ámbitos familiar, escolar y social.
La OB constituye un reto para los pediatras por: la alta prevalencia, la poca sensibilidad por parte de las familias hacia la enfermedad, la dificultad para conseguir cambiar los hábitos de forma permanente, la poca formación en técnicas de consejo y entrevista motivacional y la necesidad de controles y seguimiento a largo plazo, entre otras. Las actividades a realizar están basadas en las recomendaciones de las diferentes Guías de Práctica Clínica(6,26).
1. Detección precoz de poblaciones y factores de riesgo. Investigar factores personales: peso al nacer (elevado o bajo para la edad gestacional), ausencia de LM y rapidez en la ganancia de peso durante el primer año y el rebote adiposo precoz. Los periodos críticos para el desarrollo de OB en la edad pediátrica son: el primer año, antes de los 6 años y la adolescencia. Igualmente, los antecedentes familiares.
2. Promover y favorecer la LM. Se hará de forma general, con mensajes claros sobre su superioridad. Se propondrán alternativas al destete: en caso de enfermedad de la madre o el hijo, ingesta de fármacos, cirugía o el retorno de la madre al trabajo. La duración de la LM debe ser la que decida la familia. Se recomienda LM exclusiva los 6 primeros meses por sus grandes beneficios(6). Además de las curvas de crecimiento del estudio español, se dispone de las curvas de crecimiento de la OMS, basadas en lactantes amamantados. Se tendrá presente que la normalidad del peso es muy amplia y que los percentiles son descriptores estadísticos, y no indicadores de salud.
3. Favorecer una correcta alimentación en las diferentes edades. Respetando los mecanismos de saciedad del lactante, evitando pautas rígidas tanto en la LM como con fórmula artificial. La correcta introducción de la alimentación complementaria después de los 4 meses, adaptándola a la maduración psicomotriz del niño y favoreciendo las comidas tradicionales sobre las industriales. No se añadirá al biberón miel ni azúcar. La alimentación será equilibrada y variada, evitándose la sobrealimentación. El tamaño de las raciones se adaptará a la edad del niño. Se explicará a las familias que la velocidad de crecimiento y las necesidades nutricionales disminuyen a partir de los 18-24 meses. La alimentación del preescolar, escolar y adolescente puede verse en el nº 4 (mayo) de PI.
4. Evitar conductas que favorezcan una ganancia excesiva de peso. Como dedicar más de 2 horas/día a cualquier tipo de pantalla (con la TV se consume más cantidad y se asocia la influencia de los anuncios). Evitar comidas/bebidas con alto contenido en azúcares o grasas, picoteos, saltarse comidas o comidas rápidas, entre otras.
5. Recomendar conductas protectoras de una ganancia excesiva de peso. Alimentación saludable (pirámide nutricional) y comer en familia, incremento de la actividad diaria (juegos activos, usar escaleras, bici, tareas del hogar, caminar al colegio…) y una hora de actividad física vigorosa al día.
6. Diagnóstico de SP, OB, así como de las comorbilidades asociadas.
7. Comunicación al paciente y a la familia. Es importante, la forma de comunicar el diagnóstico al paciente y a la familia para el seguimiento y colaboración posterior. Expresiones negativas o estigmatizantes desencadenarán rechazo, mientras que una aproximación sensible con empatía, explorando conocimientos, actitudes y prácticas facilitará la colaboración.
Detectar los puntos fuertes o conductas saludables que servirán de apoyo para iniciar los cambios, así como las dinámicas familiares, estilos educativos y factores psicopatológicos que pueden ser el origen de la OB (ansiedad, depresión).
8. Tratamiento de la obesidad y seguimiento. La familia debe colaborar siempre, para no provocar rechazo. Esta llevará el peso del cumplimiento en los menores de 5 años. Entre los 5-10 años se le dará cierta responsabilidad vigilada y controlada al paciente. En la adolescencia, la familia tiene poca influencia y es el propio paciente el que debe controlarse.
9. Colaborar con otros profesionales, familias, escuelas y otros agentes sociales en actividades de promoción y prevención.
10. Derivar a la atención especializada. Si se asocian comorbilidades, sobre todo, si son del área de salud mental, obesidades extremas y por debajo de los 2 años, y si hay necesidad de intervención farmacológica o quirúrgica (Tabla VI).
Bibliografía
Los asteriscos reflejan el interés del artículo a juicio del autor.
1.** Speiser PW, Rudolf MC, Anhalt H, Camacho-Hubner C, Chiarelli F, Eliakim A, et al. Consensus statement: Childhood obesity. J Clin Endocrinol Metab. 2005; 90: 1871-87.
2.*** Serra Majem L, Ribas L, Aranceta J, Pérez C, Saavedra P. Epidemiología de la obesidad infantil y juvenil en España. Resultados del estudio enKid (1998-2000). En: Serra Majem L, Aranceta Bartrina J (eds.). Obesidad infantil y juvenil. Estudio enKid. Barcelona: Masson, S.A.; 2001. p. 81-108.
3.** Rosenbaum M. Special Considerations Relative to Pediatric Obesity. Endotext [Internet]. www.endotext.org. Última actualización: 8 Abril, 2013.
4.** Cali AM, Caprio S. Obesity in children and adolescents. J Clin Endocrinol Metab. 2008; 93(11 Suppl 1): S31-6.
5.*** Cole T, Bellizi M, Flegal K, Dietz WH. Establishing a standard definition for child overweight and obesity worldwide: international survey. BMJ 2000; 320: 1240-43.
6.*** Grupo de trabajo de la guía sobre la prevención y el tratamiento de la obesidad infantojuvenil. Centro Cochrane Iberoamericano, coordinador. Guía de práctica clínica sobre la prevención y el tratamiento de la obesidad infantojuvenil. Madrid: Plan de Calidad para el Sistema Nacional de Salud del Ministerio de Sanidad y Política Social. Agència d´Avaluació de Tecnología i Recerca Mèdiques; 2009. Guía de práctica clínica: AATRM N.º 2007/25.
7.** Moreno LA, Mesana MI, Fleta J, Ruiz JR, González-Cross M, Sarria A et al. Overweight, obesity and body fat composition in spanish adolescents. The AVENA Study. Ann Nutr Metab 2005; 49: 71-6.
8.** Carrascosa A, Fernández JM, Fernández C, Ferrández-Longás A, López-Siguero JP, Sánchez E, et al.; Grupo Colaborador Español. Spanish cross-sectional growth study 2008. Part II. Height, weight and body mass index values from birth to adulthood. An Pediatr (Barc). 2008; 68: 552-69.
9.* Sánchez-Cruz JJ, Jiménez-Moleo JJ, Fernández-Quesada F, Sánchez MJ. Prevalencia de obesidad infantil y juvenil en España en 2012. Rev Esp Cardiol. 2013; 66(5): 371-76.
10.** Rankinen T, Zuberi A, Chagnon YC, Weisnagel SJ, Argyropoulos G, Walls B, et al. The human obesity gene map: The 2005 update. Obesity. 2006; 14: 529-644.
11.** Lama More RA, Alonso Franch A, Gil-Campos M, Leis Trabazo R, Martínez Suárez V, et al., y Comité de Nutrición de la AEP Obesidad Infantil. Recomendaciones del Comité de Nutrición de la Asociación Española de Pediatría Parte I. Prevención. Detección precoz. Papel del pediatra. An Pediatr (Barc). 2006; 65: 607-15.
12.* Canadian Institute for Health Information. Obesity in Canada. Identifying Policy Priorities. 2003: 23-6. En: https://secure.cihi.ca/free…/CPHI_proceed_e.pdf.
13.** Kissileff H, Thornton M, Torres M, Pavlovich K, Leibel R, Rosenbaum M. Maintenance of reduced body weight in humans is associated with leptin-reversible declines in satiation. Amer J Clin Nutr. 2012; 95: 309-17.
14.** Farooqi IS, Wangensteen T, Collins S, Kimber W, Matarese G, Keogh JM, et al. Clinical and molecular genetic spectrum of congenital deficiency of the leptin receptor. N Engl J Med. 2007; 356: 237-47.
15.** Lubrano-Berthelier C, Dubern B, Lacorte JM, Picard F, Shapiro A, Zhang S, Bertrais S, Hercberg S, Basdevant A, Clement K, Vaisse C. Melanocortin 4 receptor mutations in a large cohort of severely obese adults: prevalence, functional classification, genotype phenotype relationship, and lack of association with binge eating. J Clin Endocrinol Metab. 2006; 91: 1811-18.
16.* Goldstone AP, Holland AJ, Hauffa BP, Hokken-Koelega AC, Tauber M; speakers contributors at the Second Expert Meeting of the Comprehensive Care of Patients with PWS. Recommendations for the diagnosis and management of Prader-Willi syndrome. J Clin Endocrinol Metab. 2008; 93: 4183-97.
17.* Li G, Vega R, Neims K, Gekakis N, Goodnow C, McNamara P, et al. A role for Alsmtröm syndrome protein, alms1, in kidney ciliogenesis and cellular quiescence. PLOs Genet. 2007; 3: 9-20.
18.* Abu Safieh L, Aldahmesh M, Shamseldin H, Hashem M, Shaheen R, Alkuraya H, et al. Clinical and molecular characterization of Bardet-Biedl syndrome in consanguineous populations: The power of homozygosity mapping. J Med Genet. 2010; 47: 236-41.
19.* Rosenbaum M, Fennoy I, Accacha S, Altshuler L, Carey D, Holleran S, Rapaport R, Shelov S, Speiser P, Ten S, The ROAD Project Study Group. Ethnic differences in clinical and biochemical type 2 diabetes mellitus risk factors in children. Obesity (Silver Spring). 2013; 21(10): 2081-90.
20.* Resnicow K, McMaster F, Bocian A, et al. Motivational interviewing and dietary counseling for obesity in primary care: an RCT. Pediatrics. 2015; 135: 649.
21.** Chanoine JP, Hampl S, Jensen C, Boldrin M, Hauptman J. Effect of orlistat on weight and body composition in obese adolescents: a randomized controlled trial. JAMA. 2005; 293: 2873-83.
22.*** Boland CL, Harris JB, Harris KB. Pharmacological Management of Obesity in Pediatric Patients. Annals of Pharmacotherapy. 2015, Vol. 49(2) 220-32.
23.*** Michalsky M, Reichard K, Inge T, Pratt J, Lenders C. ASMBS pediatric committee best practice guidelines. Surg Obes Relat Dis. 2012; 8: 1-7.
24.* Treadwell JR, Sun F, Schoelles K. Systematic review and meta-analysis of bariatric surgery for pediatric obesity. Ann Surg. 2008; 248(5): 763-76.
25.** Alqahtani AR, Antonisamy B, Alamri H, Elahmedi M, Zimmerman VA. Laparoscopic sleeve gastrectomy in 108 obese children and adolescents aged 5 to 21 years. Ann Surg. 2012; 256(2): 266.
26.*** Canadian Task Force on Preventive Health Care. Recommendations for growth monitoring, and prevention and management of overweight and obesity in children and youth in primary care. CMAJ, 2015: 187(6).
27.** Barlow SE, Expert Committee. Expert committee recommendations regarding the prevention, assessment, and treatment of child and adolescent overweight and obesity: summary report. Pediatrics. 2007; 120 Suppl 4: S164-S192.
Bibliografía recomendada
- Scottish Intercollegiate Guidelines Network (SIGN). Management of obesity. A national clinical guideline. 2010.
Guía de Práctica Clínica que provee evidencia para la prevención y el tratamiento de la obesidad en la consulta clínica dirigido a niños, jóvenes y adultos. Se focaliza en la prevención primaria para individuos con peso saludable y/o sobrepeso para evitar o retrasar el inicio de la obesidad.
- Canadian Task Force on Preventive Health Care. Recommendations for growth monitoring, and prevention and management of overweight and obesity in children and youth in primary care. CMAJ, 2015: 187(6).
Recoge la información de todas las guías previas y la evidencia científica actual.
- Grupo de trabajo de la guía sobre la prevención y el tratamiento de la obesidad infantojuvenil. Centro Cochrane Iberoamericano, coordinador. Guía de práctica clínica sobre la prevención y el tratamiento de la obesidad infantojuvenil. Madrid: Plan de Calidad para el Sistema Nacional de Salud del Ministerio de Sanidad y Política Social. Agència d´Avaluació de Tecnologia i Recerca Mèdiques; 2009. Guía de práctica clínica: AATRM N.º 2007/25.
Guía de Práctica Clínica de gran interés para la prevención y el tratamiento de la obesidad en España
- Martos-Moreno GA y Argente J. Obesidades pediátricas: de la lactancia a la adolescencia. An Pediatr (Barc). 2011; 75(1): 63.e1-63.e23.
Actualización de la obesidad desde la infancia a la adolescencia. Los autores resaltan la ausencia de una definición universalmente aceptada para la misma y señalan que es preciso un cambio de la mentalidad de los pediatras en el abordaje de estos pacientes, haciéndose necesaria la consideración de distintas «obesidades» o enfermedades diferentes que convergen en un mismo rasgo fenotípico, el aumento del peso corporal.
- Lama More RA, Alonso Franch A, Gil-Campos M, Leis Trabazo R, Martínez Suárez V, Moráis López A, Moreno Villares JM, Pedrón Giner MC y Comité de Nutrición de la AEP Obesidad Infantil. Recomendaciones del Comité de Nutrición de la Asociación Española de Pediatría Parte I. Prevención. Detección precoz. Papel del pediatra. An Pediatr (Barc). 2006; 65: 607-15.
Consenso nacional que revisa la epidemiología y los períodos de riesgo en la edad pediátrica. Reconoce el importante papel del pediatra de Atención Primaria y ofrecen pautas de estilo de vida saludable teniendo en cuenta la oferta dietética y la actividad física a lo largo de la infancia, con el objetivo de conseguir una prevención del sobrepeso y obesidad.
- Aranceta Bartrina J. Obesidad infantil: Nuevos hábitos alimentarios y nuevos riesgos para la salud. Análisis de sus causas. En: Díaz Méndez C, Gómez Benito C (coord.). Alimentación, consumo y salud. Colección Estudios Sociales, nº 24. Barcelona: Obra Social Fundación “La Caixa”, 2008: pp. 216-46.
Estudio de referencia sobre los nuevos hábitos alimentarios de la población española, las causas y los problemas que conlleva para la salud
- Carrascosa A, Fernández JM, Fernández C, Ferrández-Longás A, López-Siguero JP, Sánchez E, et al.; Grupo Colaborador Español. Spanish cross-sectional growth study 2008. Part II. Height, weight and body mass index values from birth to adulthood. An Pediatr (Barc). 2008; 68: 552-69.
Estudio transversal español de crecimiento, realizado en 32.064 sujetos (16.607 varones y 15.457 mujeres), desde el nacimiento hasta la talla adulta, en una población caucásica española procedente de Andalucía, Barcelona, Bilbao y Zaragoza, realizado entre los años 2000 y 2004.
| Caso clínico |
|
Motivo de consulta Niño de 9 años y 6 meses que consulta por exceso de peso desde siempre, más exacerbado en el último año. Anamnesis Dieta rica en grasas con escasas verduras y frutas. A menudo, realiza tentempiés de patatas fritas, golosinas, bollería industrial y refrescos azucarados en casa. La familia no realiza las comidas juntos, sino que realizan numerosos picoteos a lo largo del día, cada uno cuando quiere. Actividad física limitada exclusivamente a las 2 horas semanales de clase de educación física obligatoria en la escuela. En el último año, el paciente permanece la mayor parte del tiempo recluido en su cuarto jugando videojuegos al llegar de la escuela, y los padres creen que tiene bajo estado de ánimo. Antecedentes familiares Padre: talla 165 cm; peso: 112 kg; IMC: 41 kg/m2; desarrollo puberal normal; diabetes mellitus tipo 2 en tratamiento con antidiabéticos orales; hipercolesterolemia en tratamiento con estatinas. Madre: talla 150 cm; peso: 65 kg; IMC: 29 kg/m2; menarquía a los 12 años; hipertensión arterial en tratamiento médico; antecedente de diabetes gestacional en los 2 últimos embarazos. G-A-V: 3-0-3. Abuela materna diabetes tipo 2. Dos hermanos mayores con sobrepeso. Sin otros antecedentes de interés. Antecedentes personales Embarazo controlado, normal. Parto a las 40 semanas, cesárea por no progresión de parto debido a macrosomía. PRN: 4.500 g; LRN: 50 cm. Periodo neonatal normal. Pruebas metabólicas normales. Lactancia materna once meses, sin intolerancias alimentarias. Desarrollo psicomotor normal. Inmunizaciones correctas. Enfermedades anteriores: nada que reseñar. Medicaciones: ninguna en la actualidad. Exploración física Peso: 53 kg (+4,4 DE); talla: 130 cm (-0,77 DE); IMC: 31,3 kg/m2 (+5,6 DE). T.A.: 110/60 mmHg. Buen estado general. Coloración normal de piel y mucosas. Sin rasgos dismórficos. Obesidad generalizada, sin estrías ni acantosis. Sin bocio. ACP: normal. Abdomen: blando, depresible, sin visceromegalias. Genitales externos masculinos normales, pene embebido en grasa, 5 cm de longitud desde la sínfisis del pubis. Tanner I (genitales 1, pubarquia 1, axilarquia 1). Estudios complementarios Hemograma: fórmula y recuentos normales. Bioquímica general: normal. Hormonas tiroideas: normales. Glucemia en ayunas: 98 mg/dl. Insulina en ayunas: 9 mcU/l, HOMA-IR: 2.17. Lipidograma: CT: 210 mg/dl (vn: 120-200); Triglicéridos: 120 mg/dl (vn: < 100); C-HDL: 40 mg/dl (vn: 35-75); C-LDL: 140 mg/dl (vn: 60-130); C-VLDL: 30 mg/dl (vn: 5-23); C-LDL/C-HDL: 3,5 (vn: <2,2). Edad ósea: 8 años para una edad cronológica de 9 años y 6 meses. |