 |
| Temas de FC |
A. Montesdeoca Melián*, M. Castillo de Vera**
*Pediatra de AP. CS Guanarteme. Las Palmas de Gran Canaria. Las Palmas. **Pediatra de AP. CS El Doctoral. Santa Lucía de Tirajana. Las Palmas
| Resumen
El aumento de las infecciones producidas por especies bacterianas resistentes a antimicrobianos, tanto en medio hospitalario como en la comunidad, representa un problema sanitario de primer orden en todo el planeta. La lucha contra las resistencias a antimicrobianos, hoy en día, se plantea con un abordaje más amplio, donde la interacción de la salud animal, humana y ambiental debe tenerse en cuenta. La decisión de si iniciar o no un tratamiento antibiótico, conlleva una reflexión que implica un gran número de variables que el pediatra de Atención Primaria conjuga para aportar el tratamiento más apropiado. Aunque habitualmente se realiza un abordaje empírico, el espectro antimicrobiano y la duración del tratamiento son cuestiones primordiales en la prevención de aparición de resistencias. En este trabajo se abunda en todas estas cuestiones y se proponen opciones concretas para el tratamiento empírico de las infecciones más frecuentes en el ámbito de la Pediatría de Atención Primaria. |
| Abstract
The increase in infections caused by antimicrobial resistant bacterial species, both in hospital and community settings, represents a major health problem worldwide. The fight against antimicrobial resistance nowadays takes a broader approach, where the interaction of animal, human and environmental health must be taken into account. The decision of whether or not to initiate antibiotic treatment involves a large number of variables that the primary care paediatrician combines to provide the most appropriate treatment. Although an empirical approach is usually used, the antimicrobial spectrum and the duration of treatment are key issues in preventing the emergence of resistance. This paper explores all these issues and proposes specific options for the empirical treatment of the most frequent infections in the primary care setting. |
Palabras clave: Resistencias a antimicrobianos; Tratamiento empírico; Espectro; Tratamiento diferido.
Key words: Antimicrobial resistance; Empirical treatment; Spectrum; Deferred treatment.
Pediatr Integral 2023; XXVII (6): 321 – 330
OBJETIVOS
• Subrayar el papel que juega el pediatra de Atención Primaria en la lucha contra las resistencias bacterianas a antimicrobianos.
• Recordar las bases para una elección razonada del tratamiento antibiótico óptimo en Pediatría.
• Resaltar la importancia que tiene, en la práctica diaria, utilizar las pautas más cortas posibles
en el tratamiento de las infecciones comunitarias más comunes, siempre que estén refrendadas
por la evidencia científica.
• Actualizar el tratamiento empírico recomendado en la actualidad para las infecciones más frecuentemente atendidas en el ámbito de la Atención Primaria.
• Ofrecer al pediatra información clara, práctica y completa sobre los tratamientos recomendados para cada entidad, así como sobre las alternativas posibles en caso de alergia, resistencias o desabastecimiento de fármacos.
Uso racional de antibióticos en Pediatría
PARTE I
Introducción
Es en Atención Primaria donde más prescripciones de antibióticos se hacen. Seguir las recomendaciones y guías clínicas facilita la labor del pediatra y optimiza el uso de estos fármacos.
Solo en el año 2019, la Organización Mundial de la Salud (OMS) cifraba en 1.270.000 las muertes ocasionadas como consecuencia de las resistencias bacterianas a antibióticos(1), convirtiéndose en una de las diez mayores amenazas para la salud global. Desde hace más de una década, las naciones europeas trabajan juntas en acciones coordinadas, siguiendo la estrategia denominada One Health, donde se pone de manifiesto la fuerte relación existente entre la salud humana, la salud animal y la salud ambiental. Para conseguir frenar el avance de los microorganismos resistentes a antimicrobianos serán necesarias acciones que involucren a distintos actores en los tres eslabones de la cadena.
Centrándonos en la Pediatría y más concretamente en la de Atención Primaria (AP), el reto pasa por disminuir y adecuar el uso de los antibióticos. En las temporadas de máxima presión asistencial y de mayor circulación de virus respiratorios, aumenta también la demanda de antibióticos por parte de la población para tratar procesos agudos que los pediatras de AP manejaremos, la mayor parte de las veces, de forma empírica, sin exploraciones complementarias. Es decir, en los pocos minutos que dura la consulta, debemos generar la confianza y seguridad suficientes, como para que nuestro paciente no reciba un tratamiento antimicrobiano que, en la mayoría de los casos, no necesitará, aunque ello desemboque, en ocasiones, en situaciones conflictivas con los familiares. Si bien queda mucho trabajo de concienciación por hacer en nuestra sociedad, pues todavía la mayoría de la población no comprende plenamente lo que implica administrar un antibiótico innecesariamente a un niño, cierto es que, en los últimos años, empieza a notarse una cierta tendencia al cambio. Cada día más padres y madres dudan de la necesidad de administrar un tratamiento antibiótico a sus hijos. Solo entendiendo las razones que hacen que la población demande antimicrobianos, podremos combatir su abuso. Por citar solo algunas:
• Factores culturales heredados en nuestro país (miedo a las infecciones invasoras).
• La impaciencia por esperar a la resolución espontánea de procesos víricos.
• La necesidad de una cura rápida por cuestiones de diversa índole (antepuestos a la salud).
• Los crecientes compromisos sociales de niños de corta edad.
• La falta de conciliación de la vida familiar y laboral de los padres.
• Los bulos.
• Las negligencias médicas maximizadas.
• La desconfianza hacia el sistema sanitario.
• El menosprecio hacia el pediatra de AP.
• La creencia de que cada síntoma necesitará de un fármaco para mejorar.
En este trabajo intentaremos comentar, de forma resumida, los pasos que un pediatra de AP sigue (o debería seguir), habitualmente casi sin percatarse, antes de tomar la decisión de iniciar un tratamiento antibiótico en un paciente. El uso inapropiado de antibióticos: genera una exposición innecesaria a posibles efectos adversos del fármaco, contribuye al incremento de las resistencias (en el propio paciente y en la comunidad), genera costes y cimenta la falsa creencia en la población sobre la habitual necesidad de su uso para obtener la curación. Para el tratamiento de las infecciones más frecuentemente encontradas en la consulta del pediatra de AP, existe investigación de calidad que permite un uso apropiado de antimicrobianos basado en evidencia científica, de la cual emanan recomendaciones generales, guías de práctica clínica o posicionamientos de sociedades pediátricas. El tratamiento correcto de las infecciones más frecuentes es de vital importancia, pues su incorrecto manejo conllevará un perjuicio para un gran número de pacientes. Conviene resaltar que el manejo empírico de algunas infecciones puede ir cambiando con el paso de los años conforme varía la epidemiología, lo cual nos obliga a mantenernos actualizados. Ello es debido a la participación de múltiples factores: mejora en las condiciones de vida, impacto tras la inclusión de vacunas conjugadas infantiles con indicación sistemática (pueden hacer variar el patrón de resistencia de determinadas bacterias), circulación de nuevos patógenos o ya conocidos, pero con especiales características (resistencias o virulencia), épocas en las que haya una gran circulación de virus respiratorios (como hemos observado tras la pandemia de COVID-19), etc. Asumiendo el uso mayoritariamente empírico de los antibióticos en AP, es fundamental conocer el patrón de resistencias de los aislamientos bacterianos locales. Para ello, los laboratorios de microbiología de referencia de cada zona deben dar a conocer esta información anualmente, desagregada por tramos de edad, tipo de infección y procedencia de la muestra.
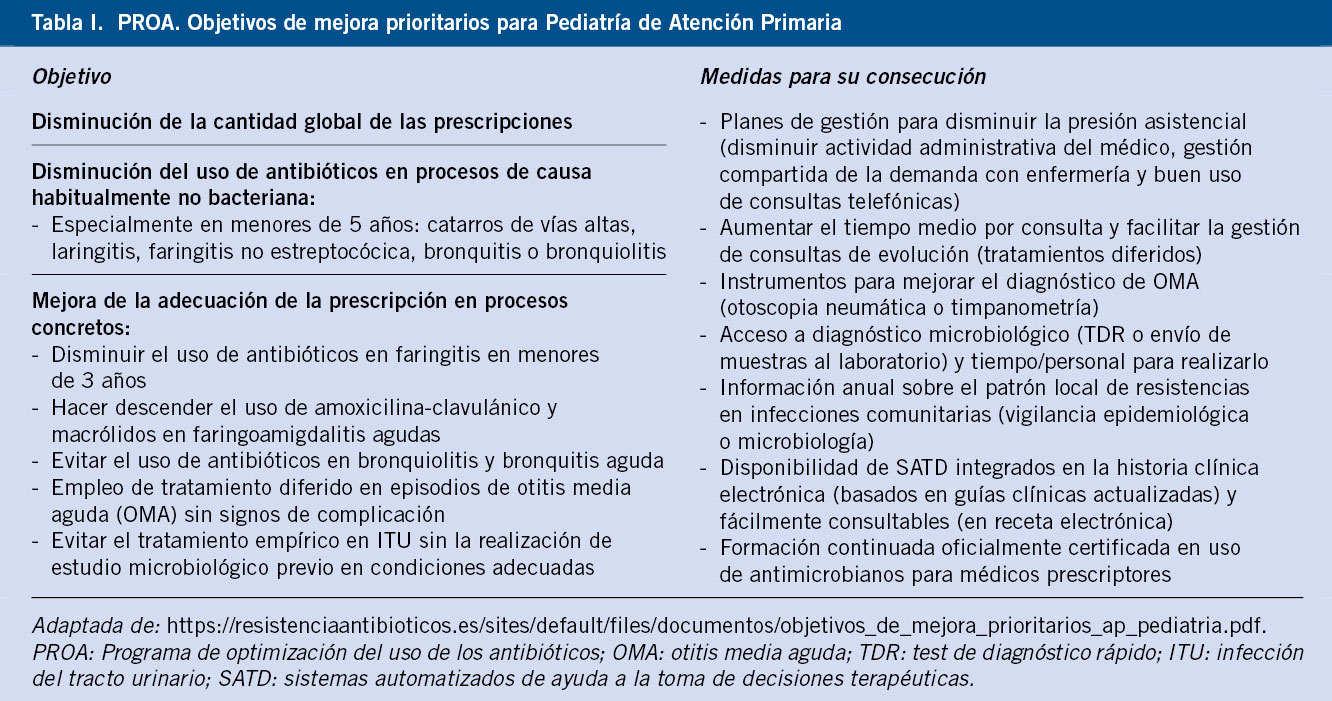
Estos datos resultan básicos para adecuar el tratamiento empírico de las infecciones más comunes, esforzándonos siempre por elegir la opción con menor espectro antimicrobiano. Entre todas las acciones que actualmente se están llevando a cabo para promover un uso racional de los antibióticos y la lucha contra las resistencias bacterianas, cabe destacar la labor de los equipos PROA (Programas de Optimización del uso de los Antibióticos) comunitarios o de AP, integrados en el Plan Nacional contra la Resistencia a los Antibióticos (PRAN) y que constan de unas líneas de acción y objetivos sujetos a normativa y certificación por parte del Ministerio de Sanidad(2). En su línea estratégica II, se definen unos objetivos de mejora, prioritarios para Pediatría de Atención Primaria, que se resumen en la tabla I.
En varias partes del texto de los PROA comunitarios, se hace referencia a la utilidad de los test de diagnóstico rápido (TDR) y de cómo pueden ayudar a disminuir la prescripción de antibióticos. Queremos enfatizar en la importancia que tiene disponer de algunos de ellos en las consultas de AP, pues representan un instrumento de gran ayuda al clínico; ahora bien, entendemos que su uso debería enfocarse a los casos en los que el resultado haga variar el manejo del paciente (tanto en el tratamiento como en las recomendaciones). Tan importante es saber cuándo utilizarlos como saber cuándo no, pues su uso indiscriminado puede tener efectos perniciosos (p. ej.: el uso del TDR para S. pyogenes en el manejo del lactante febril sin foco).
En la segunda parte de este trabajo, comentaremos esquemáticamente el tratamiento recomendado en nuestro país para las infecciones más comunes que se abordan desde una consulta de Pediatría de Atención Primaria, haciendo uso de bibliografía recientemente publicada.
Factores que influyen en la elección de un antibiótico
La elección del tratamiento antimicrobiano dependerá de varios factores relacionados con: el individuo (y su entorno), el microorganismo, la localización de la infección y el propio fármaco.
Lo primero que cabe plantearse es: ¿este paciente necesita un antibiótico para curarse? En la inmensa mayoría de los casos en Pediatría de AP, la respuesta será “no”, y solo condiciones específicas que podamos diagnosticar microbiológicamente en el acto (p. ej., la faringoamigdalitis estreptocócica), síndromes de muy posible origen bacteriano (p. ej., la celulitis periorbitaria) o la evolución desfavorable de un proceso que habitualmente es viral (p. ej., una sinusitis aguda), nos harán cambiar esa respuesta.
Frecuentemente, la prescripción de un antibiótico de forma empírica se realiza aplicando un protocolo consensuado o por conceptos fijados en nuestra memoria, sin que haya un aprendizaje razonado. Para la inmensa mayoría de los casos, esta actuación “semiautomática” resulta válida, pero conviene no olvidar que, cuando elegimos un antimicrobiano con una pauta posológica determinada, en realidad deberíamos tener en cuenta todos y cada uno de los factores que se enumeran en la tabla II.
La realización de análisis microbiológico no está siempre indicada, ya sea por: la facilidad para predecir el agente causal, la inaccesibilidad del lugar anatómico sin causar trauma, la baja rentabilidad del cultivo bacteriológico, la alta posibilidad de contaminación u otras razones. Sin embargo, el conocimiento del microorganismo causante de la infección permite realizar un tratamiento mucho más dirigido y con menos probabilidades de fracaso, al tiempo que podremos razonar opciones terapéuticas, si el curso de la enfermedad no es satisfactorio. Otra máxima a recordar es que, si la evolución no es la esperada con el tratamiento empírico, no hay definidas alternativas (como sí las hay p. ej., en la otitis media aguda que no responde a la amoxicilina) y aparecen complicaciones, debemos intentar obtener un aislamiento microbiológico que guíe nuestra terapia y no seguir empecinándonos en el empirismo. En ocasiones, ocurre que, a pesar de iniciarse un tratamiento supuestamente válido por los datos in vitro que conocemos del microorganismo, la evolución no es buena, momento en el que hay que plantearse: si el paciente cumple el tratamiento y la posología adecuada, si se requiere otro tipo de abordaje terapéutico (p. ej., cirugía) o si pudiera haber factores que hagan fracasar al antibiótico pese a ser el correcto (p. ej., inmunodeficiencia).
La falta de suministro o disponibilidad de antibióticos en formulaciones adecuadas para su administración a niños pequeños no suele ser habitual en nuestro país, pero en los últimos meses, todo el continente europeo se ha visto afectado en mayor o menor medida por problemas de este tipo. Ello nos ha forzado a usar tratamientos alternativos subóptimos, unas veces con mayor espectro antimicrobiano del deseado y otras con formulaciones farmacéuticas que impedían hacer un cálculo preciso de la dosis (sobres o comprimidos para adultos), lo cual expone a los pacientes a infra o sobredosificación, con todo lo que ello puede acarrear. Afortunadamente, los fármacos utilizados con mayor frecuencia (amoxicilina, fenoximetilpenicilina) tienen en general un amplio margen de seguridad, con lo que, si no existen alternativas, puede tenderse a prescribir dosis altas de estos antibióticos antes de optar por alternativas con mayor espectro (cefalosporinas) o mayor porcentaje de resistencias (macrólidos).
Tendencia a acortar tratamientos en infecciones adquiridas en la comunidad
Existe una tendencia generalizada a acortar la duración de los tratamientos de las infecciones más comunes diagnosticadas en la comunidad.
Hasta hace poco tiempo, se enfatizaba (y así incluso se le transmitía a los padres) en el cumplimiento total del tratamiento antibiótico, a pesar de que el paciente se recuperara en la mitad de tiempo. Es probable que muchos de esos niños no cumplieran hasta el final el tratamiento, pero aun así se hacía esta recomendación por miedo al fracaso terapéutico. En la actualidad, se tiende más bien a lo contrario. La administración innecesariamente prolongada de antimicrobianos contribuye a la selección de bacterias resistentes, por lo que existe una tendencia global al acortamiento de los tratamientos en infecciones adquiridas en la comunidad en pacientes inmunocompetentes, siempre y cuando se demuestre no inferioridad con respecto a los tratamientos estándar.
Muchas infecciones que tratamos en consulta reciben prescripciones de 7-10 días. Esta duración del tratamiento obedece a hábitos históricos y no se sustenta sobre una base científica; por ello muchos investigadores, ante la creciente preocupación por la emergencia de resistencias bacterianas, se han propuesto cambiar los estándares de tratamiento en infecciones, como la neumonía y la otitis media aguda (OMA)(3) o, desde hace más tiempo, la infección del tracto urinario (ITU)(4).
Parte II
En esta segunda parte del artículo, desarrollaremos por separado las infecciones bacterianas más prevalentes en Pediatría de AP, centrándonos principalmente en aquellos aspectos de interés a la hora de elegir qué antibiótico reúne las mejores características para su empleo de manera empírica.
Faringitis aguda
La penicilina oral es el tratamiento de elección de la faringitis producida por el estreptococo betahemolítico del grupo A.
La mayoría de faringitis agudas son causadas por virus. La principal bacteria implicada es el Streptococcus pyogenes o estreptococo betahemolítico del grupo A (EbhGA) con un 15 % del total, especialmente en niños entre 3-13 años, donde puede alcanzar el 30 % en época epidémica, la cual suele ocurrir entre el final del invierno y el comienzo de la primavera en climas templados(5). Las faringitis por EbhGA son muy raras por debajo de los 2-3 años. A cualquier edad, la presencia de conjuntivitis, rinorrea, afonía, estridor, tos y/o diarrea son hallazgos sugestivos de origen vírico de la infección(6). También lo son, la presencia a la exploración de vesículas en boca o úlceras en el paladar. En aquellos casos en que no están presentes estos síntomas y/o datos exploratorios excluyentes, el diagnóstico de presunción de faringitis por EbhGA en un porcentaje elevado de casos, no se correlaciona con una prueba de confirmación microbiológica positiva, incluso cuando lo hacen profesionales experimentados/as en este campo. La prueba microbiológica de elección en Atención Primaria es el test de detección rápida de antígeno estreptocócico. En la tabla III se recogen las indicaciones para su realización.
El tratamiento de elección será penicilina vía oral (fenoximetilpenicilina potásica o fenoximetilpenicilina benzatina). La dosificación sería: en <27 kg de peso, 250 mg cada 12 horas; y en ≥27 kg, 500 mg cada 12 horas. La toma debe separarse de las comidas (1 h antes o 2 h después) para favorecer su absorción. Como alternativa, en niños más pequeños, se puede pautar amoxicilina que tiene mejor sabor y cuya absorción no se modifica con la ingesta de alimentos. La pauta es de 50 mg/kg/día con una dosis máxima de 1 g/día.
Se puede dar en toma única o repartirla en 2 dosis(7). El tratamiento, a pesar de la baja incidencia de fiebre reumática en nuestro medio, tiene como fin último su prevención. Por ello, con la evidencia actual, su duración será de 10 días. La penicilina-benzatina en dosis única intramuscular, debe quedar limitada a quienes no toleren la vía oral o en el caso de que no pueda asegurarse el cumplimiento terapéutico. La dosificación es la siguiente: <27 kg 600.000 UI y ≥27 kg 1.200.000 UI. En alergia a betalactámicos no mediada por IgE o reacción retardada no grave, debe emplearse una cefalosporina de primera generación (cefadroxilo 30 mg/kg/día cada 12 h, dosis máxima 2 g/día). En caso de alergia mediada por IgE inmediata o retardada grave, la elección debe ser un macrólido. Para evitar cepas con fenotipo M resistente a macrólidos de 14 y 15 átomos de carbono, se prefiere elegir los de 16 átomos de carbono como josamicina (30-50 mg/kg/día cada 12 h, dosis máxima 1 g al día) o diacetil-midecamicina (35-50 mg/kg/día cada 12 h, dosis máxima 1,2 g al día). En caso de faringitis recurrente (nuevo episodio de faringitis en un periodo menor a un mes tras realizar correctamente el tratamiento antibiótico), en la que su cuadro clínico orienta a una nueva faringitis estreptocócica, habría que valorar la participación de bacterias productoras de betalactamasas, como favorecedoras de la recurrencia. En este caso, el tratamiento de elección sería una cefalosporina de primera generación como cefadroxilo, teniendo como alternativas, en caso de no disponer del mismo o no tolerancia: amoxicilina-clavulánico (4:1), cefuroxima (es suficiente con 5 días de tratamiento en este caso) o macrólidos (valorar siempre las resistencias locales).
Otitis media aguda (OMA)
Antes de la introducción de la vacuna antineumocócica conjugada, las bacterias implicadas con mayor frecuencia en la etiología de la OMA eran: Streptococcus pneumoniae (35 %), Haemophilus influenzae no tipificable (HiNT, 25 %), Streptococcus pyogenes (3-5 %), Staphylococcus aureus (1-3 %) y Moraxella catarrhalis (1 %). La vacunación universal con vacuna antineumocócica conjugada 13 valente (VNC13) ha tenido un impacto mayor de lo esperado en la prevención de otitis media aguda; HiNT y Streptococcus pneumoniae siguen siendo las principales bacterias implicadas, pero, en muchos estudios, HiNT ocupa ya el primer lugar, mientras que Moraxella catarrhalis ha pasado a ocupar el tercero. Las resistencias de Streptococcus pneumoniae a la penicilina (resistencia generalmente salvable con aumento de dosis) se siguen manteniendo entre el 15-30 %(8). El 80 % de las OMA se resuelven de manera espontánea. El tratamiento antibiótico tiene como fin reducir la duración de la sintomatología y evitar el desarrollo de complicaciones, tanto a corto plazo (mastoiditis) como a medio-largo (desarrollo de otitis media crónica). La Academia Americana de Pediatría (AAP) en su Guía de Práctica Clínica para la OMA, situó en 6 meses la edad mínima para conducta expectante y observación clínica antes de iniciar tratamiento antibiótico(9). Sin embargo, en diferentes estudios realizados, la conducta expectante entre 6-24 meses fracasa con frecuencia por diferentes motivos, por lo que será necesario individualizar cada caso. Las indicaciones de tratamiento antibiótico en el momento del diagnóstico son: menores de 6 meses, presencia de otorrea, OMA unilateral grave (Tabla IV), OMA bilateral, inmunodepresión o imposibilidad de seguimiento.
El tratamiento de elección es amoxicilina a 80 mg/kg/día cada 8 horas, dosis máxima 3 g/día. Si existen factores de riesgo o sospecha de infección por H. influenzae (menores de 6 meses, pauta incompleta de vacunación, presencia de conjuntivitis purulenta, recurrencia, o tratamiento antibiótico en los últimos 30 días), emplearemos amoxicilina-clavulánico (8:1) a 80 mg/kg/día de amoxicilina cada 8 horas, dosis máxima 3 g/día. En niños menores de 2 años, la duración del tratamiento debe ser de 7-10 días. También se recomienda este tiempo de tratamiento a cualquier edad con: OMA supurativa, historia de OMA de repetición, otitis media crónica o cirugía relacionada con hipoacusia asociada (adenoidectomía, drenaje transtimpánico o miringotomía). En el resto se podría limitar a 5 días. Es recomendable, sobre todo, en pautas de tratamiento de 5 o 7 días, un control clínico que valore la respuesta adecuada al tratamiento antes de su suspensión(10). En alérgicos a amoxicilina IgE mediada o retardada grave, el tratamiento sería con macrólidos, preferentemente azitromicina (10 mg/kg/día cada 24 h 3 días, dosis máxima 500 mg/día), por su posología, duración y biodisponibilidad. También puede emplearse claritromicina (15 mg/kg/día cada 12 h, dosis máxima 1 g/día). En alergia no inmediata leve, la elección sería cefuroxima (30 mg/kg día cada 12 h). La duración del tratamiento con claritromicina y cefuroxima sería la misma que para amoxicilina.
Otitis externa aguda
Otitis externa aguda difusa (OEAd)
Las bacterias implicadas principalmente son: Pseudomonas aeruginosa y Staphylococcus aureus. Podemos encontrar también Proteus mirabilis, estreptococos de los grupos D y G y anaerobios. La presencia de hongos es menos frecuente en la edad pediátrica, destacando Candida spp. y Aspergillus spp. No está indicada la toma de muestra para cultivo de forma rutinaria, pero debe recogerse siempre en: otitis externa grave (dolor intenso, canal completamente ocluido por edema, eritema periauricular, fiebre y/o linfadenopatía), otitis externa recurrente, inmunodepresión, cirugía reciente del pabellón auditivo o mala respuesta al tratamiento. El tratamiento de elección para las otitis externas difusas leves o moderadas es tópico. Cuando se encuentre cerumen, restos de piel descamada o exudado en gran cantidad, se debe limpiar el conducto antes de iniciar el tratamiento. A la hora de elegir tratamiento, debemos tener en cuenta lo siguiente(11):
• No existen diferencias entre: antibióticos (quinolonas o no), antisépticos (alcohol de 70º boricado, violeta de genciana al 2 %) y soluciones acidificantes (ácido acético 2 %).
• No hay estudios que determinen un mayor beneficio al asociar corticoides al antibiótico tópico, comparándolo con el empleo de este último solo.
• Existe suficiente evidencia de ototoxicidad de aminoglucósidos, antisépticos y soluciones acidificantes, por lo que estos no deberían emplearse en: portadores de tubos de timpanostomía, perforación timpánica o pacientes en los que no se pueda visualizar la membrana timpánica (otorrea, estrechez del conducto auditivo externo -CAE- por edema, etc.).
Ciprofloxacino ótico sería la opción más recomendable para el tratamiento. Proporciona una excelente cobertura contra Pseudomonas aeruginosa y aceptable para Staphylococcus aureus, y no produce ototoxicidad. La ficha técnica permite su uso por encima del año de vida. Dependiendo de la forma de presentación del fármaco, su posología será de 4 gotas o 1 vial cada 12 horas durante 7 días(10). En relación a los aminoglucósidos, neomicina es eficaz contra Staphylococcus aureus, mientras que tobramicina y gentamicina cubren también a Pseudomonas aeruginosa. Su principal problema es la ototoxicidad como ya se comentó. La polimixina B cubre solo a Pseudomonas aeruginosa. En las OEAd graves y en inmunocomprometidos, debe asociarse tratamiento sistémico y derivarse para valoración por otorrinolaringología (ORL). También deben ser valorados por ORL, quienes no presenten mejoría tras 7 días de tratamiento. En caso de otomicosis, está indicada la limpieza del CAE con retirada de todo el material contenido en el mismo. Se puede emplear clotrimazol 1 %, antisépticos y agentes acidificantes, como el ácido acético al 2 %(11).
Otitis externa aguda circunscrita o localizada
Se llama así a la presencia de un forúnculo en el tercio externo del conducto auditivo y es producido por Staphylococcus aureus. El tratamiento de elección sería una cefalosporina de primera generación, cefadroxilo o cefalexina, prefiriéndose la primera por su posología. La pauta de cefadroxilo es de 30 mg/kg/día cada 12 horas, dosis máxima 2 g/día. Amoxicilina-clavulánico (4:1) a 40 mg/kg/día cada 8 horas, dosis máxima 3 g/día y cefuroxima a 20-30 mg/kg/día cada 12 horas, dosis máxima 2 g/día, pueden ser alternativas cuando no se disponga o no se tolere cefadroxilo. Cloxacilina, que podría ser de entrada el antibiótico de elección, presenta varios problemas que lo relegan a un papel secundario: su posología cada 6 horas, su mal sabor, su absorción errática cuando ingiere con alimentos (debe tomarse 1 h antes o 2 h después) y su baja biodisponibilidad, disminuyen su efectividad y dificultan el cumplimiento terapéutico. En alergia mediada por IgE o tardía grave a betalactámicos, emplearemos azitromicina 10 mg/kg/día durante 3 días, dosis máxima 500 mg/día.
Sinusitis aguda
Las bacterias implicadas con mayor frecuencia en la sinusitis aguda en Pediatría son similares a las que se encuentran en la OMA, por lo que las pautas de tratamiento antibiótico de ambas coinciden, si bien la duración en esta última suele ser más prolongada (10 días). Ante la existencia de estudios con resultados contrapuestos, en caso de optar en niños mayores de 2 años por una conducta expectante o prescripción diferida, estas deben ir acompañadas de un seguimiento clínico estrecho para vigilar la posible aparición de complicaciones(8).
Bronquitis bacteriana persistente
La bronquitis bacteriana persistente clínica se define como: una infección de las vías respiratorias inferiores que se caracteriza por la presencia de tos húmeda o productiva de más de 4 semanas de duración en ausencia de otro diagnóstico que pudiera ser la causa de la misma. Afecta, sobre todo, a niños menores de 6 años. El síntoma principal es la tos húmeda, que suele presentarse en forma de accesos, que no responde a tratamiento broncodilatador y que puede acompañarse puntualmente de dificultad respiratoria. La exploración física es habitualmente normal.
Los principales agentes etiológicos son: Haemophilus influenzae no tipable, Streptococcus pneumoniae y, con menor frecuencia, Moraxella catarrhalis. Frecuentemente, se aísla más de uno. Es criterio excluyente del diagnóstico la existencia de una infección concomitante por Bordetella pertussis o Mycoplasma pneumoniae.
El tratamiento de elección es amoxicilina-clavulánico (8:1) a dosis de 80 mg/kg/día de amoxicilina cada 8 h, con una dosis máxima de 3 g/día durante un mínimo de 14 días. En ocasiones, es necesario mantener el tratamiento entre 4-6 semanas. En caso de alergia tardía no grave a betalactámicos, el tratamiento de elección sería cefuroxima (30 mg/kg/día cada 12 h, dosis máxima 500 mg/día) con igual duración. En alergia a betalactámicos mediada por IgE o tardía grave, el tratamiento de elección sería claritromicina (15 mg/kg/día cada 12 h, máximo 1 g/día durante un mínimo de 14 días)(12).
Neumonía adquirida en la comunidad
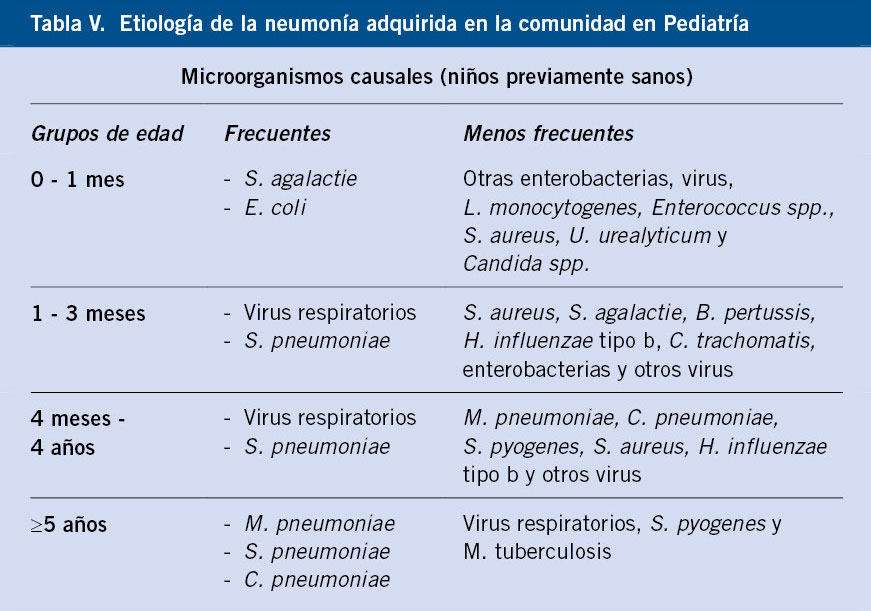
Los virus son la causa más común en menores de 4 años. La bacteria implicada con mayor frecuencia es Streptococcus pneumoniae. En menores de 5 años, ocupa el primer lugar con casi el 30 % del total. En mayores de 5 años, Mycoplasma pneumoniae es la bacteria aislada con mayor frecuencia. En la tabla III, se recogen los principales microorganismos causantes de neumonía adquirida en la comunidad en niños sanos(13).
Sospecha de neumonía típica(14,15)
Entendemos por neumonía típica, aquella que presenta un cuadro de inicio brusco con: fiebre (≥39ºC), tos productiva y exploración compatible (auscultación con crepitantes localizados y/o hipoventilación). Las guías clínicas vigentes indican que puede prescindirse de la realización de radiografía de tórax para el diagnóstico en niños previamente sanos con un primer episodio de neumonía que no presenten criterios de gravedad. El tratamiento, en la mayoría de las ocasiones, será empírico; los microorganismos causales pueden consultarse en la tabla V.
En los últimos años se han llevado a cabo múltiples investigaciones buscando acotar la duración del tratamiento de la neumonía no complicada en niños. La OMS(16) hace años que recomienda disminuir a 3-5 días el tratamiento de la neumonía adquirida en la comunidad en niños de 2 a 5 años, pero los criterios definitorios de neumonía no se corresponden exactamente con los empleados en países de alto Índice de Desarrollo Humano (IDH). Varios metaanálisis(17) aportan evidencia suficiente como para recomendar esta duración en menores de 5 años, también en países de alto IDH(18). Tanto es así, que varios grupos de expertos sugieren que las guías de tratamiento deberían cambiar en favor de acortar el tratamiento de la neumonía no complicada en niños de 6 meses a 5 años(19). En niños de edad <5 años, el tratamiento de elección será amoxicilina 80 mg/kg/día cada 8 h, dosis máxima diaria 6 g, 5 días. Hay que señalar que la duración del tratamiento vendrá condicionada por un seguimiento que confirme la buena evolución del cuadro clínico, siendo innecesaria la realización de exploraciones complementarias de ningún tipo para confirmar la curación. En menores de 5 años correctamente vacunados de Haemophilus influenzae tipo B, el tratamiento de elección es el mismo, mientras que en no vacunados, deberá ser amoxicilina-clavulánico (8:1) a 80 mg/kg/día de amoxicilina, dosis máxima diaria 3 g/día con igual duración. Si tras 48-72 h de tratamiento, no hubiera una respuesta adecuada al tratamiento y no existieran criterios de ingreso hospitalario, se puede asociar un macrólido. En alergia a betalactámicos mediada por IgE o tardía grave, el tratamiento de elección sería un macrólido, de elección azitromicina (10 mg/kg/día, dosis máxima diaria 500 mg durante 3 días) y, como alternativa, claritromicina (15 mg/kg/día cada 12 h, máximo 1 g/día,
5 días). En caso de reacción alérgica tardía no grave, pautaríamos cefuroxima (30 mg/kg/día cada 12 h, dosis máxima 1 g/día, 5 días).
Sospecha de neumonía atípica
El cuadro se caracteriza por: un inicio insidioso, poca afectación del estado general, fiebre menor de 39ºC, tos y, a la auscultación, estertores crepitantes difusos que se pueden acompañar de sibilancias bilaterales. En menores de 5 años, la causa más probable es la viral (especialmente en menores de 2 años). Si sospechamos etiología bacteriana, el antibiótico de elección es azitromicina (10 mg/kg/día, dosis máxima diaria 500 mg durante 3 días). Como alternativa, podemos emplear claritromicina (15 mg/kg/día cada 12 h, máximo 1 g/día durante 5 días).
Gastroenteritis aguda
La gastroenteritis aguda es viral en el 80 % de los casos. Rotavirus es el patógeno más frecuente, siendo la primera causa en menores de 2 años, a pesar del importante descenso acontecido tras la introducción de la vacuna. Otros virus causantes de diarrea aguda son: norovirus, sapovirus, astrovirus, enterovirus y adenovirus entéricos. Campylobacter spp. es el agente etiológico más frecuente en mayores de 5 años. Los agentes bacterianos aislados más frecuentemente en población infantil sana en nuestro medio son: Campylobacter jejuni y Salmonella spp. En el caso de la diarrea del viajero, el patógeno más frecuente es Escherichia coli enterotoxigénica. Los cuadros clínicos de gastroenteritis aguda suelen ser autolimitados, tanto si son de causa viral como bacteriana. El tratamiento antibiótico no suele acortar la duración del proceso y, en ocasiones, puede favorecer la persistencia en el tiempo del estado de portador, como ocurre con Salmonella spp. Las indicaciones de antibioterapia son, por tanto, muy limitadas (Tabla VI)(20).
Infección del tracto urinario (ITU)
Escherichia coli es el principal agente etiológico de ITU en Pediatría (60-80 %).
La ITU es una de las infecciones bacterianas más frecuentes en la edad pediátrica. Escherichia coli es la causa más frecuente, con una prevalencia de entre 60-80 % en los diferentes estudios epidemiológicos realizados en nuestro país. El segundo lugar en frecuencia lo ocupa Proteus mirabilis (6-10 %) y el tercero Klebsiella pneumoniae (3-5 %). Otras enterobacterias implicadas son: Klebsiella oxytoca, Enterobacter cloacae, Citrobacter spp., Serratia marcescens y Morganella morganii. Entre las bacterias grampositivas destacan: Enterococcus spp. (en lactantes <3 meses y niños con enfermedad nefrourológica) y Staphylococcus saprophyticus en mujeres adolescentes con infección de orina no complicada(21). El tratamiento antibiótico empírico (Tabla VII) debe iniciarse de manera inmediata una vez recogida una muestra adecuada para cultivo (“al acecho” o sondaje en niños/as no continentes y chorro miccional medio en continentes), con el fin de minimizar las posibles complicaciones.
La elección se hará en función de las resistencias locales y las características del paciente que pudieran determinar cambios en su etiología. Se debe evitar el empleo de antibióticos con resistencias ≥15 %. La mayoría de tratamientos serán domiciliarios y vía oral. Se recomienda hacer un control clínico a las 48 horas. Escherichia coli es generalmente sensible a cefalosporinas de segunda (cefuroxima) y tercera generación (cefixima, ceftibuteno), debiendo decantarnos por el primer grupo, si la sensibilidad existente así lo permite. También suele ser sensible a fosfomicina, la cual podremos usar solo en cistitis, dada la baja biodisponibilidad alcanzada por la misma en el tracto urinario alto. En niñas mayores de 12 años con cuadro de cistitis, se puede utilizar fosfomicina trometamol 3 g en dosis única, debiendo administrarse durante 2 días en caso de ITU recurrente. En el resto, utilizaremos fosfomicina cálcica (100-200 mg/kg/día cada 8 h, dosis máxima 1,5 g/día). En los últimos años, se han incrementado las resistencias de Escherichia coli a amoxicilina-clavulánico, por lo que debemos evitar de entrada el uso de este antibiótico (en cualquier caso, como ya comentamos, se tendrán en cuenta las resistencias locales existentes). En menores de 3 meses y población con antecedentes de enfermedad nefrourológica, la tinción de Gram puede orientar hacia la presencia de cocos grampositivos en la muestra. En este caso la amoxicilina sería el tratamiento empírico de elección. La duración del tratamiento antibiótico (excepto para fosfomicina trometamol) será entre 3-5 días para las cistitis y 7-10 días para las ITU de vías altas.
Infecciones cutáneas
En las infecciones cutáneas, en las que sospechemos la presencia de Staphylococcus aureus, no debemos utilizar amoxicilina como tratamiento (bacteria productora de betalactamasas).
Las bacterias más implicadas en las infecciones cutáneas son Staphylococcus aureus y Streptococcus pyogenes, sin embargo, las características del paciente o el contexto clínico-epidemiológico pueden favorecer la implicación de otras especies y la necesidad de tomar muestras para estudio microbiológico. Este deberá plantearse también ante lesiones muy extensas, la presencia de complicaciones o afectación sistémica.
El tratamiento en las infecciones cutáneas habituales es frecuentemente empírico. Las infecciones cutáneas localizadas, superficiales, se pueden tratar con antisépticos o antibióticos tópicos. Los más empleados, dado su espectro de acción, son la pomada de mupirocina o la crema o pomada de ácido fusídico. La pauta habitual de ambos será cada 8 horas, con una duración entre 5-7 días. En caso de encontrarnos con lesiones con complicaciones, extensas, diseminadas y/o con afectación sistémica o del estado general, está indicada la vía oral. La duración del tratamiento puede variar en función del tipo y características de la lesión, pero habitualmente oscila entre 5-10 días. En infecciones en las que se sospeche la presencia de Staphylcoccus aureus, se deberá tener en cuenta la producción de betalactamasas por parte de esta a la hora de elegir el tratamiento (amoxicilina no puede ser antibiótico de elección en este caso). El tratamiento de elección sería una cefalosporina de primera generación como cefadroxilo o cefalexina, siendo preferible la primera por su menor número de tomas diarias. La pauta de cefadroxilo es de 30 mg/kg/día cada 12 horas, dosis máxima 2 g/día. Amoxicilina-clavulánico (4:1) a 40 mg/kg/día cada 8 horas, dosis máxima 3 g/día, y cefuroxima a 20-30 mg/kg/día cada 12 horas, dosis máxima 1 g/día, pueden ser alternativas cuando no se disponga o no se tolere cefadroxilo.
Se debe sospechar la presencia de SARM (Staphylococcus aureus resistente a meticilina) ante mala respuesta al tratamiento, procedencia de América, Asia o el este de Europa, o convivencia con portadores conocidos. En caso de precisar antibioterapia oral, emplearíamos clindamicina, 10-30 mg/kg/día cada 6 horas, dosis máxima 1,8 g/día (no hay presentación en suspensión), o cotrimoxazol, especialmente en pacientes procedentes de zonas de alta resistencia a clindamicina o la necesidad de una presentación en solución que permita la toma del tratamiento. La pauta es de 6-12 mg/kg/día de trimetropim cada 12 horas, dosis máxima 320 mg/día)(22).
En las infecciones producidas por Streptococcus pyogenes, el antibiótico de elección será penicilina o amoxicilina. Cefadroxilo y amoxicilina-clavulánico se emplearán en caso de sospechar asociación con Staphylococcus aureus. En caso de alergia mediada por IgE o tardía grave a betalactámicos, podemos emplear macrólidos de 16 átomos de carbono, como josamicina (30-50 mg/kg/día cada 12 h, dosis máxima 1 g/día) o midecamicina (35-50 mg/kg/día cada 12 h, dosis máxima 1 g/día). También puede utilizarse clindamicina, 10-30 mg/kg/día
cada 6 horas, dosis máxima 1,8 g/día (no hay presentación en suspensión).
Función del pediatra de Atención Primaria
En la lucha contra las resistencias bacterianas a antimicrobianos, la figura del pediatra de Atención Primaria resulta clave, pues tendrá en su mano la decisión de si iniciar o no tratamiento antibiótico en cada caso, elegir el fármaco más adecuado atendiendo a múltiples factores y mantenerlo el tiempo preciso, ni más, ni menos.
La concienciación sobre el sobreuso de antibióticos en el ámbito de la Atención Primaria es fundamental y el pediatra es uno de los mayores prescriptores de este tipo de fármacos, junto a los odontólogos y los médicos de familia.
La presión asistencial, la insistencia de los familiares o el tiempo medio por consulta, juegan en contra del abuso de antimicrobianos en este ámbito. Desde los órganos de gestión, siguiendo las líneas marcadas por los PROA comunitarios, debe facilitarse la actividad profesional del pediatra, si lo que pretendemos es hacer todo lo posible por disminuir la expansión de las resistencias bacterianas.
Conflicto de intereses
No hay conflicto de interés en la elaboración del manuscrito. Declaración de intereses: ninguno.
Bibliografía
Los asteriscos muestran el interés del artículo a juicio de los autores.
1. Global antimicrobial resistance and use surveillance system (GLASS) report 2022. Geneva: World Health Organization; 2022. Disponible en: https://apps.who.int/iris/rest/bitstreams/1483639/retrieve.
2. Agencia Española de Medicamentos y Productos Sanitarios. Plan Nacional frente a la Resistencia a los Antibióticos. Programas de Optimización de uso de los antibióticos. Disponible en: https://resistenciaantibioticos.es/es/lineas-de-accion/control/programas-de-optimizacion-de-uso-de-los-antibioticos-proa.
3. Principi N, Autore G, Argentiero A, Esposito S. Short-term antibiotic therapy for the most common bacterial respiratory infections in infants and children. Front Pharmacol. 2023; 14: 1174146.
4. Fitzgerald A, Mori R, Lakhanpaul M, Tullus K. Antibiotics for treating lower urinary tract infection in children. Cochrane Database Syst Rev. 2012; (8): CD006857.
5.** de la Flor i Brú J. Infecciones de vías respiratorias alta-1: faringitis aguda y recurrente. Pediatr Integral. 2022; XXVI: 340-7. Disponible en: https://www.pediatriaintegral.es/publicacion-2022-09/infecciones-de-vias-respiratorias-altas-1-faringitis-aguda-y-recurrente-2022/.
6.** Piñeiro Pérez R, Álvez González F, Baquero Artigao F, Cruz Cañete M, de la Flor i Brú J, Fernández Landaluce A, et al. Actualización del documento de consenso sobre el diagnóstico y tratamiento de la faringoamigdalitis aguda. An Pediatr (Barc). 2020; 93: 206.e1-e8.
7. Lennon DR, Farrell E, Martin DR, Stewart JM. Once-daily amoxicillin vs twice-daily penicillin V in group A B-heamolytic streptococcal pharyngitis. Arch Dis Child. 2008; 93: 474-8.
8.*** López Martín D, Piñeiro Pérez R, Martínez Campos L, Ares Álvarez J, de la Calle Cabrera T, Jiménez Huerta I, et al., y Grupo colaborador del consenso de otitis media aguda y sinusitis en Pediatría. Actualización del documento de consenso sobre etiología, diagnóstico y tratamiento de la otitis media aguda y sinusitis. Anales de Pediatría. 2023; 98: 362-72.
9. Leiberthal AS, Carroll AE, Chonmaitree T. Clinical practice guideline: the diagnoses and management of acute otitis media. Pediatrics. 2013; 131: e964-9.
10. de la Flor i Brú J. Infecciones de vías respiratorias altas-2: Otitis media (etiología, clínica y diagnóstico; complicaciones y tratamiento); otitis media aguda de repetición y otitis media crónica; otitis externa. Pediatr Integral. 2022; XXVI: 353-68. Disponible en: https://www.pediatriaintegral.es/publicacion-2022-09/infecciones-de-vias-respiratorias-altas-2-otitis-2022/.
11. Maté Cano I, Ordóñez Sáez O, Romero-García A. Otitis externa. En: Guía-ABE. Infecciones en Pediatría. Guía rápida para la selección del tratamiento antimicrobiano empírico. Disponible en: https://www.guia-abe.es.
12. Busquets Monge RM, Castillo Corullón S, Aguilar Fernández AJ. Tos húmeda: bronquitis bacteriana persistente, enfermedad supurativa bronquial y bronquiectasias. Protoc diagn ter pediatr. 2017;1:15-29
13.** Úbeda Sansano I, Croche Santander B, Hernández Merino A. Neumonía. En: Guía-ABE. Infecciones en Pediatría. Guía rápida para la selección del tratamiento antimicrobiano empírico. Disponible en: https://www.guia-abe.es.
14.* Andrés Martín A, Escribano Montaner A, Figuerola Mulet J, García García ML, Korta Murua J, Moreno-Pérez D, et al. Documento de consenso sobre la neumonía adquirida en la comunidad en los niños. SENP-SEPAR-SEIP. Arch Bronconeumol. 2020; 56: 725-41.
15.*** Li Q, Zhou Q, Flórez ID, Mathew JL, Shang L, Zhang G, et al. Short-Course vs Long-Course Antibiotic Therapy for Children With Nonsevere community-acquired pneumonia: A systematic review and meta-analysis. JAMA Pediatr. 2022; 176: 1199-207.
16. World Health Organization. Revised WHO classification and treatment of childhood pneumonia at health facilities. 2023. Disponible en: https://apps.who.int/iris/bitstream/handle/10665/137319/9789241507813_eng.pdf;jsessionid=79B4F0183FB32C3C57ED7F65D2B5478B?sequence=1.
17. Li Q, Zhou Q, Florez ID, Mathew JL, Shang L, Zhang G, et al. Short-course vs long-course antibiotic therapy for children with nonsevere community-acquired pneumonia: A systematic review and meta-analysis. JAMA Pediatr. 2022; 176: 1199-207. Disponible en: https://jamanetwork.com/journals/jamapediatrics/article-abstract/2798514.
18. Kuitunen I, Jääskeläinen J, Korppi M, Renko M. Antibiotic Treatment Duration for Community-Acquired Pneumonia in Outpatient Children in High-Income Countries-A Systematic Review and Meta-Analysis. Clin Infect Dis. 2023; 76: e1123-8. Disponible en: https://doi.org/10.1093/cid/ciac374.
19. BMJ Publishing Group Ltd and Royal College of Paediatrics and Child Health (2023). Short courses of antibiotics for community acquired pneumonia. Arch Dis Child. 2023; 108: 52. Disponible en: http://dx.doi.org/10.1136/archdischild-2022-325186.
20. Albert de la Torre L. Gastroenteritis aguda (v.4.0/2019). Guía_ABE. Infecciones en Pediatría. Guía rápida para la selección del tratamiento antimicrobiano empírico. Disponible en: https://www.guia-abe.es.
21.*** González Rodríguez JD, Justa Roldán MJ. Infección de las vías urinarias en la infancia. Protoc diagn ter pediatr. 2022; 1: 103-29.
22.** Conejo Fernández AJ, Martínez Chamorro MJ, Couceiro JA, Moraga Llop FA, Baquero Artigao F, Álvez F, et al. Documento de consenso SEIP-AEPAP-SEPEAP sobre la etiología, el diagnóstico y el tratamiento de las infecciones cutáneas bacterianas de manejo ambulatorio. An Pediatr (Barc). 2016; 84: 121.e1-e10.
Bibliografía recomendada
- Piñeiro Pérez R, Hijano Bandera F, Álvez González F, Fernández Landaluce A, Silva Rico JC, Pérez Cánovas C, et al. Documento de consenso sobre el diagnóstico y tratamiento de la faringoamigdalitis aguda. An Pediatr. 2011; 75: 342.e1-e13.
Documento de consenso sobre el diagnóstico y tratamiento de la faringoamigdalitis aguda.
- López Martín D, Piñeiro Pérez R, Martínez Campos L, Ares Álvarez J, de la Calle Cabrera T, Jiménez Huerta I, et al., y Grupo colaborador del consenso de otitis media aguda y sinusitis en Pediatría. Actualización del documento de consenso sobre etiología, diagnóstico y tratamiento de la otitis media aguda y sinusitis. Anales de Pediatría. 2023; 98: 362-72.
Actualización del documento de consenso sobre etiología, diagnóstico y tratamiento de la otitis media aguda y sinusitis.
- Úbeda Sansano I, Croche Santander B, Hernández Merino A. Neumonía. En: Guía-ABE. Infecciones en Pediatría. Guía rápida para la selección del tratamiento antimicrobiano empírico. Disponible en: https://www.guia-abe.es.
Guía rápida para la selección del tratamiento antimicrobiano empírico.
- Andrés Martín A, Escribano Montaner A, Figuerola Mulet J, García García ML, Korta Murua J, Moreno-Pérez D, et al. Documento de consenso sobre la neumonía adquirida en la comunidad en los niños. SENP-SEPAR-SEIP. Arch Bronconeumol. 2020; 56: 725-41.
Documento de consenso sobre la neumonía adquirida en la comunidad en los niños.
- Conejo Fernández AJ, Martínez Chamorro MJ, Couceiro JA, Moraga Llop FA, Baquero Artigao F, Álvez F, et al. Documento de consenso SEIP-AEPAP-SEPEAP sobre la etiología, el diagnóstico y el tratamiento de las infecciones cutáneas bacterianas de manejo ambulatorio. An Pediatr (Barc). 2106; 84: 121.e1-e10.
Documento de consenso SEIP-AEPAP-SEPEAP sobre la etiología, el diagnóstico y el tratamiento de las infecciones cutáneas bacterianas de manejo ambulatorio.
| Caso clínico |
|
Eva, de 4 años, no tiene antecedentes personales destacables, incluyendo alergias, y se encuentra correctamente vacunada según calendario oficial de su comunidad autónoma. Consultan sus padres, porque presenta un cuadro clínico que se inició hace 5 días con rinorrea y tos, especialmente nocturna. En los últimos 4 días, ha comenzado de forma brusca, con fiebre de hasta 39,6ºC, con dos picos diarios, rechazo parcial del alimento, decaimiento y, desde esta mañana, dolor torácico localizado en flanco izquierdo. También presenta dolor abdominal continuo y un vómito aislado, sin diarrea. Tolera líquidos y algunos sólidos. No hay otros convivientes sintomáticos. En la exploración física, presenta buen estado general, sin alteraciones de coloración de piel y mucosas. La frecuencia cardiaca es de 110 lpm, la respiratoria de 32 rpm, la satO2 medida por pulsioximetría es de 97 % y la exploración ORL no revela alteraciones. A la inspección no muestra uso de musculatura accesoria ni tiraje, pero en la auscultación destaca la presencia de hipoventilación y estertores crepitantes, localizados en el lugar donde la niña se queja de dolor costal (base izquierda). El resto del examen físico es normal.
|






 Meningitis and meningoencephalitis
Meningitis and meningoencephalitis