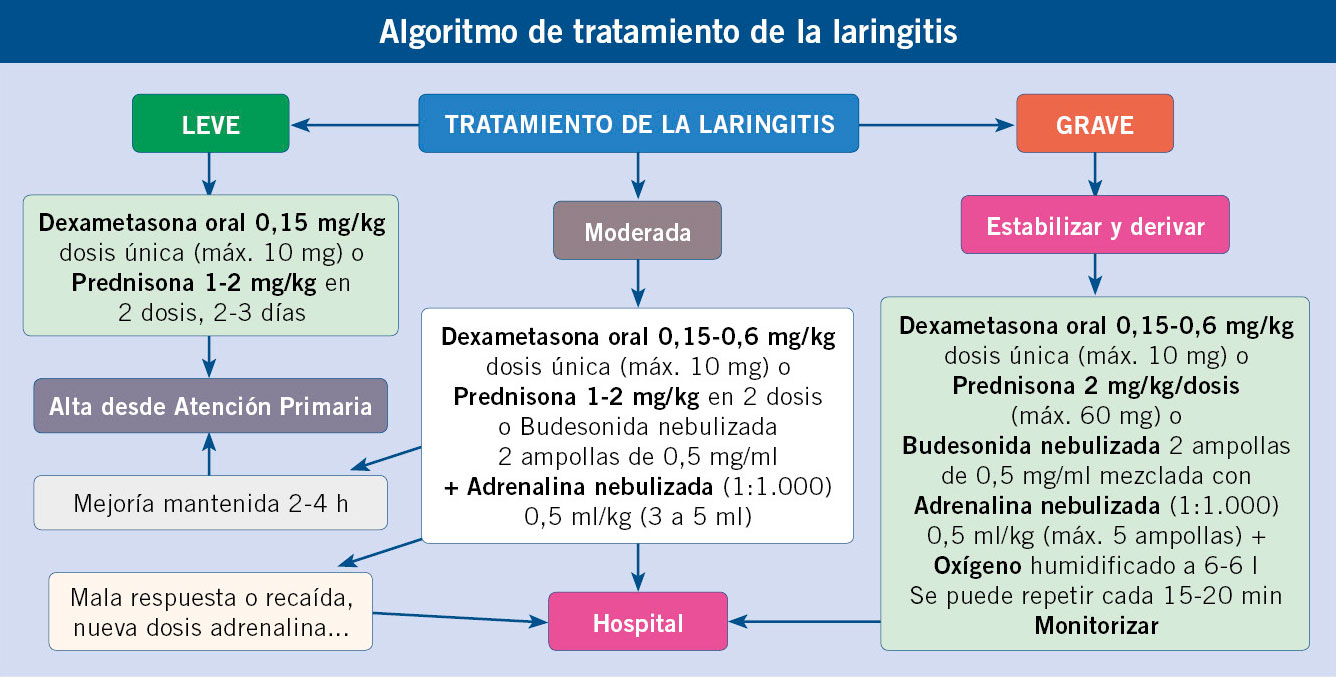
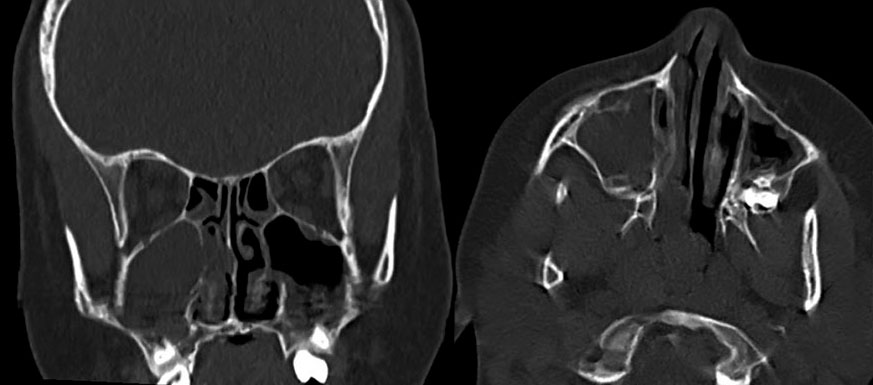
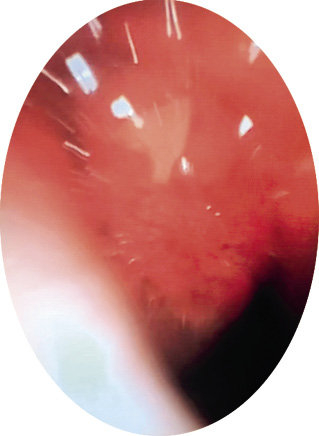
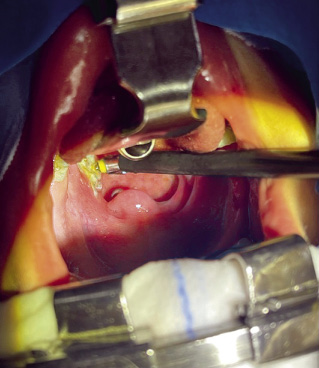
Infecciones de vías respiratorias altas-2: otitis media (etiología, clínica y diagnóstico; complicaciones y tratamiento); otitis media aguda de repetición y otitis media crónica; otitis externa
Otitis media (etiología, clínica y diagnóstico; complicaciones y tratamiento)
Introducción y epidemiología
La importancia epidemiológica de la otitis media en Pediatría de AP viene dada por su frecuencia, por el consumo de recursos sanitarios que comporta y, posiblemente, por sus repercusiones potenciales en el desarrollo y aprendizaje del niño.
La otitis media aguda (OMA) es el diagnóstico más frecuente en una consulta de AP después del resfriado común y de los controles de salud del niño sano. Un 80% de niños de 3 años han experimentado, al menos, un episodio, y un 33% han sufrido 3 o más ataques. El pico de incidencia está entre los 6-18 meses. Esta patología genera un gran número de visitas espontáneas y controles, y un gasto incalculable derivado de la utilización, muchas veces innecesaria, de fármacos, derivaciones y procedimientos quirúrgicos.
Definiciones
Hay que delimitar exactamente los distintos cuadros clínicos y saber con precisión a qué entidad nos estamos refiriendo.
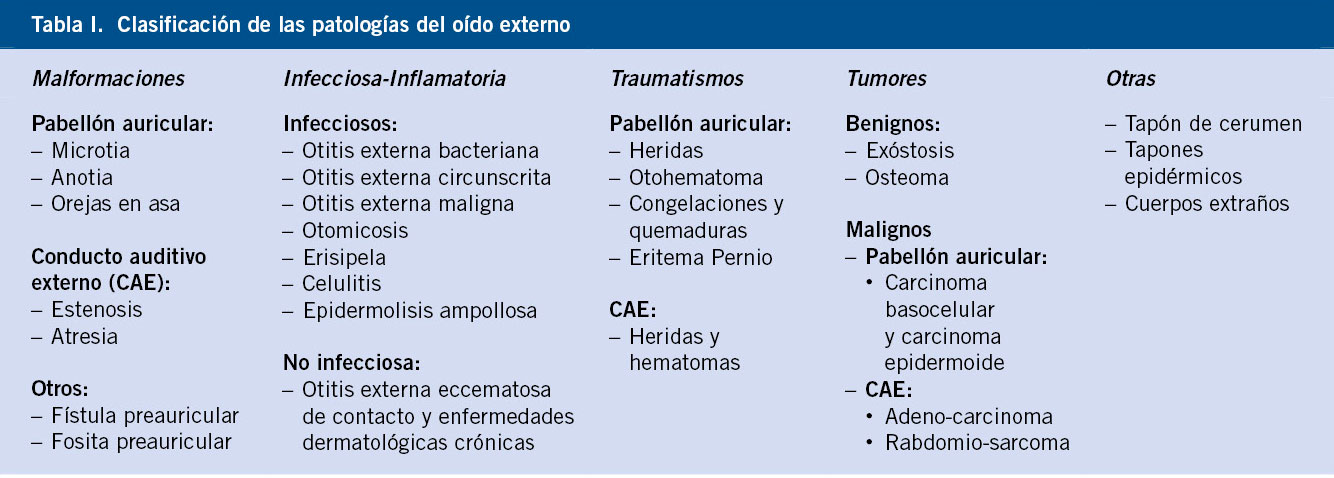
Es muy conveniente clarificar los términos con los que nos referiremos a las distintas variantes de esta enfermedad, dado que existe una gran confusión en la utilización de los mismos(1) (Tabla I).

Se define como otitis media: la inflamación de la mucosa del oído medio, acompañada generalmente de la presencia de líquido en dicha cavidad. El oído medio es una cavidad aérea en la que la existencia de cualquier líquido (sea exudado, trasudado, pus o sangre) es siempre patológica.
Si hay sintomatología clínica aguda atribuible a esta presencia de líquido hablamos de otitis media aguda (OMA).
Si no hay sintomatología clínica aguda, la otitis media recibe el nombre de otitis media secretora, con efusión, exudado o derrame (OME). Suele ser un evento evolutivo post infección aguda y, generalmente, se relaciona con la presencia en oído medio de citoquinas y otros mediadores de la inflamación. Cursa con una hipoacusia de transmisión de una media de 50 dB.
Esta situación se ha conocido clásicamente como “otitis serosa”, término en desuso actualmente, dado que presupone la esterilidad de dicho derrame, cuando en realidad se cultivan gérmenes en un 20-30% de ocasiones, con mayor prevalencia de virus. Usando técnicas de PCR, se encuentran gérmenes con mucha mayor frecuencia. Estos gérmenes pueden estructurarse recubriendo la mucosa de oído medio en forma de película o biofilm, sustancia mucoide de matriz polisacárida que protege a las bacterias de la actividad antibiótica y las esconde del sistema inmunitario.
Si el derrame dura más de 3 meses y es bilateral, recibe el nombre de otitis media con derrame crónica (OMEC). Si el derrame es solo unilateral, debe durar más de 6 meses para ser catalogado de crónico.
Hablamos de otitis media persistente en dos situaciones:
• Cuando persiste la sintomatología aguda (otalgia y/o fiebre) más allá de 48-72 horas en el curso de un tratamiento antibiótico (fracaso terapéutico).
• Cuando se presenta un nuevo episodio agudo antes de 14 días de la finalización del tratamiento antibiótico por un episodio anterior (OMA recidivante). En estas dos situaciones es más probable que se cultive el mismo germen aislado en la timpanocentesis inicial. A partir de este límite, un nuevo episodio agudo supone más frecuentemente una reinfección o recurrencia por otro germen que una recidiva por el mismo, y debe considerarse un ataque diferenciado del anterior(2).
Si un niño experimenta 3 o más episodios de OMA en 6 o menos meses, o 4 en 12 o menos meses, siempre que el último se haya producido en los 6 meses recientes, diremos que sufre de otitis media aguda de repetición (OMAR).
Etiología
En nuestro medio, la OMA debe ser considerada fundamentalmente una enfermedad causada por neumococo y secundariamente por Haemophilus influenzae no tipable. Otros gérmenes (Moraxella, estreptococo, estafilococo) tienen una importancia secundaria.
Conocer la flora bacteriana causante de OMA obliga a hacer estudios en los que se cultive la secreción de oído medio obtenida por timpanocentesis. No son útiles los cultivos de exudado obtenidos en el conducto auditivo externo a partir de OMA supurada con perforación, que mostrarán invariablemente flora saprofita y, especialmente, pseudomonas. La mayor parte de estos estudios provienen de EE.UU.(3), y muestran coincidencia en el orden de frecuencia de las bacterias responsables: neumococo, Haemophilus influenzae (HI) no capsulado (con incidencia similar en todas las edades) y Moraxella catarralis. A mucha distancia, Streptococcus pyogenes y estafilococo. Alloiococcus otitidis causa hasta un 9% de casos de OMA. Otro patógeno emergente es Turicella otitidis. Los escasos estudios análogos realizados en España muestran la casi total ausencia de Moraxella, por lo que a efectos prácticos de plantear un tratamiento empírico, se considerarán únicamente neumococo y HI. Estreptoco se aísla más frecuentemente en otorreas espontáneas y en mayores de 5 años, y estafilococo (con creciente incidencia de meticilina resistentes adquiridos en la comunidad/MARSA) en otorreas en niños portadores de drenajes. En ambientes con altas coberturas de vacunación antineumocócica conjugada, se ha producido un desplazamiento en las frecuencias etiológicas, con mayor importancia de HI(4). Hasta un 30% de cultivos presentan ausencia de bacterias. En muchos de ellos, se aíslan diversos virus respiratorios, algunos de los cuales parece claro que inducen a la sobreinfección bacteriana posterior (rinovirus, virus respiratorio sincitial, adenovirus, influenza), pero el papel etiológico primario de los mismos podría suponer un 10% de todos los casos(5,6). Es muy frecuente la asociación bronquiolitis VRS-otitis media. La coinfección virus-bacteria es un factor añadido de riesgo de fracaso terapéutico en un tratamiento antibiótico, dado que los virus favorecen la adhesión bacteriana al epitelio respiratorio y alteran la farmacocinética de los ATB. Es interesante resaltar la frecuente asociación entre VRS y HI, y entre virus de la gripe y neumococo.
Patogenia
La infección vírica de la rinofaringe favorece la disfunción de la trompa de Eustaquio, fenómeno que combina la presencia de presiones negativas en oído medio con la dificultad en el drenaje de las secreciones hacia la rinofaringe.
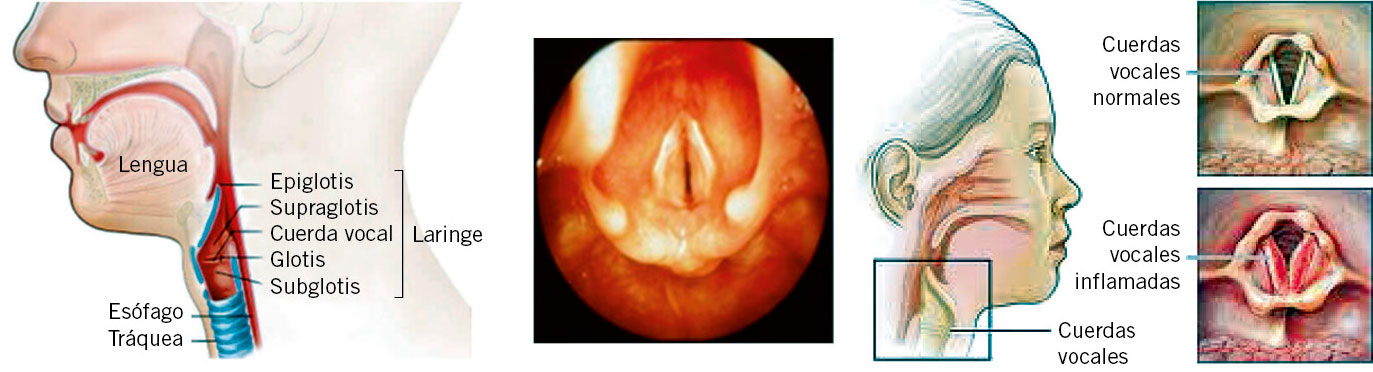
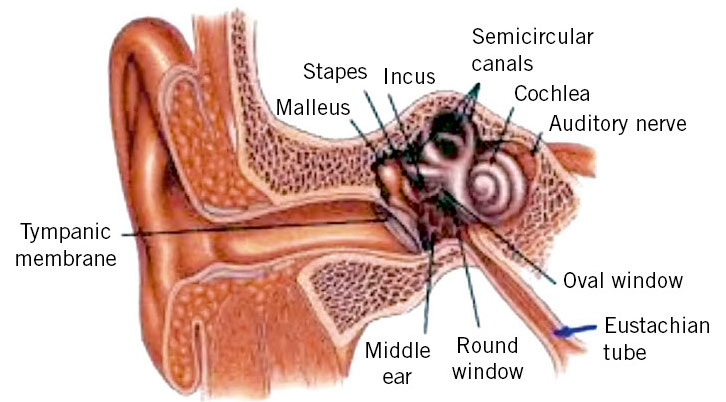
La OMA es una enfermedad relacionada con el resfriado común, del que es complicación habitual. Es mucho más frecuente en los 3 primeros años de vida (con un pico claro entre los 6-20 meses), época en la que se producen la mayor parte de infecciones respiratorias, muy especialmente en niños escolarizados. Para entender la patogenia de la otitis media, hay que conocer el funcionamiento de la trompa de Eustaquio. Su principal función (Fig. 1) es la ventilación del oído medio con aire que proviene de la nasofaringe, ya que el equilibrio de presiones aéreas entre el conducto auditivo externo y el oído medio favorece una correcta audición.
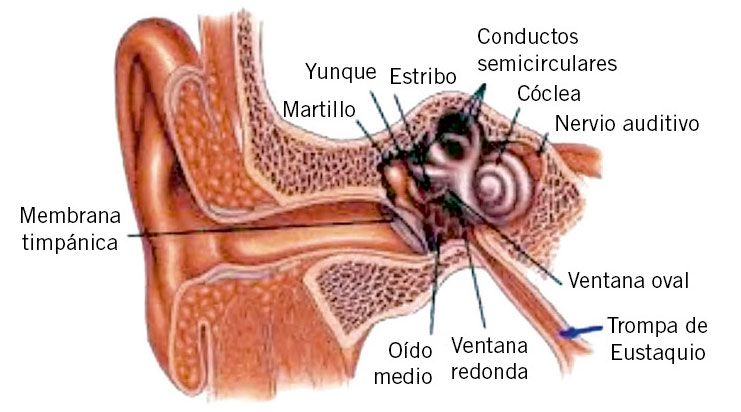
Figura 1. Anatomía de la trompa de Eustaquio.
Este equilibrio se consigue con la abertura intermitente de la trompa en cada movimiento de deglución, por acción del músculo tensor del velo palatino. Esta función es menos eficaz en niños que en adultos, por inervación insuficiente, lo que comporta mayor frecuencia de presiones negativas en oído medio. Ello justificaría el lloro del lactante durante los cambios de presión en un vuelo: la presión positiva del aire abre la trompa y reequilibra la presión en oído medio. Las otras dos funciones importantes de la trompa son la protección del oído medio de secreciones provenientes de la nasofaringe (que durante la deglución pueden penetrar hasta el istmo o estrechez que separa la parte cartilaginosa de la parte ósea de la trompa, pero no hasta el oído medio), y el drenaje de las secreciones de la mucosa del oído medio hacia la nasofaringe. La obstrucción de la trompa por moco comporta el inicio de un complejo mecanismo de inflamación en oído medio. La infección vírica de vías respiratorias altas provoca, además, toxicidad sobre el epitelio respiratorio, causante de discinesia ciliar en la trompa de Eustaquio (disfunción de la trompa de Eustaquio, también conocida como ototubaritis, DTE), con alteración del aclaramiento normal de secreciones. Los registros timpanométricos muestran DTE en un 75% de casos de resfriado común. El acúmulo de moco en la trompa, con la obstrucción resultante, comporta absorción de O2, CO2 y otros gases, por la rica vascularización de oído medio, lo que genera presión negativa en oído medio, con resultado neto de trasudado de líquido a partir de la mucosa, aspiración de secreciones nasofaríngeas y facilidad para la sobreinfección bacteriana de las mismas. Este fenómeno está favorecido el primer año de vida por la conformación rectilínea de la trompa y su menor longitud y, a cualquier edad, por el tabaquismo pasivo o activo y la rinitis alérgica. Sin DTE, no hay otitis media.
Clínica
La otalgia o sus equivalentes en lactantes (irritabilidad, tracción del pabellón) es el signo capital y de mayor especificidad. La OMA puede acompañarse de otros síntomas (fiebre, vómitos, diarrea) totalmente inespecíficos (Tabla II).

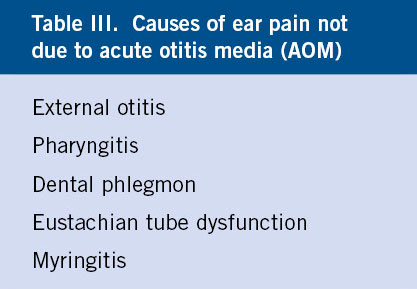
La OMA aparece habitualmente a los pocos días del inicio de un resfriado común, pero no es excepcional que lo haga súbitamente, sin signos catarrales previos aparentes o cuando la infección respiratoria ya parecía haberse resuelto. El síntoma de mayor especificidad es la otalgia, en ausencia de la cual o de sus equivalentes no debería diagnosticarse OMA. Sin embargo, su presencia tampoco es patognomónica de OMA (Tabla III) y puede ser debida a: otitis externa, dolor irradiado a partir de una faringitis, flemón dentario, DTE con presión negativa en oído medio o miringitis.
Es más frecuentemente de aparición nocturna, dado que el cambio de posición del niño al acostarse favorece una mayor presión del derrame sobre la membrana timpánica. Puede ser muy intensa y es un frecuente motivo de consulta nocturna a los servicios de urgencia. La fiebre es inconstante (30-60%), pero puede ser elevada, especialmente en lactantes. Otro síntoma, menos específico, pero de alto valor predictivo, es la irritabilidad en lactantes que, en ocasiones, tiran de los pabellones auriculares hacia abajo o se los frotan con las manos. Se considera equivalente a la otalgia. Los vómitos y/o diarrea, en niños de menos de 3 años, acompañan frecuentemente a la OMA, pero son totalmente inespecíficos. Cuando la membrana timpánica se perfora, se visualiza la secreción, que puede ser purulenta o sanguinolenta. La perforación suele seguirse de disminución o desaparición del dolor. La abundante irrigación de la membrana timpánica favorece una rápida cicatrización, a veces, en 24-72 horas, que puede condicionar un nuevo acúmulo de secreciones y la reaparición de la sintomatología aguda. La hip oacusia en niños mayores es un signo que acompaña frecuentemente a la OMA y, si es de corta evolución, tiene gran especificidad. Si bien, se consideró clásicamente que la OMA neumocócica tenía una presentación más aguda y la causada por HI solía ser de inicio y evolución más lentos, en la actualidad, se considera que el cuadro clínico no permite hacer valoraciones diferenciales en cuanto a la etiología.
oacusia en niños mayores es un signo que acompaña frecuentemente a la OMA y, si es de corta evolución, tiene gran especificidad. Si bien, se consideró clásicamente que la OMA neumocócica tenía una presentación más aguda y la causada por HI solía ser de inicio y evolución más lentos, en la actualidad, se considera que el cuadro clínico no permite hacer valoraciones diferenciales en cuanto a la etiología.
Diagnóstico
Es difícil, dado que la sintomatología puede ser muy inespecífica, la otoscopia se realiza frecuentemente en condiciones subóptimas y su interpretación es muy subjetiva.
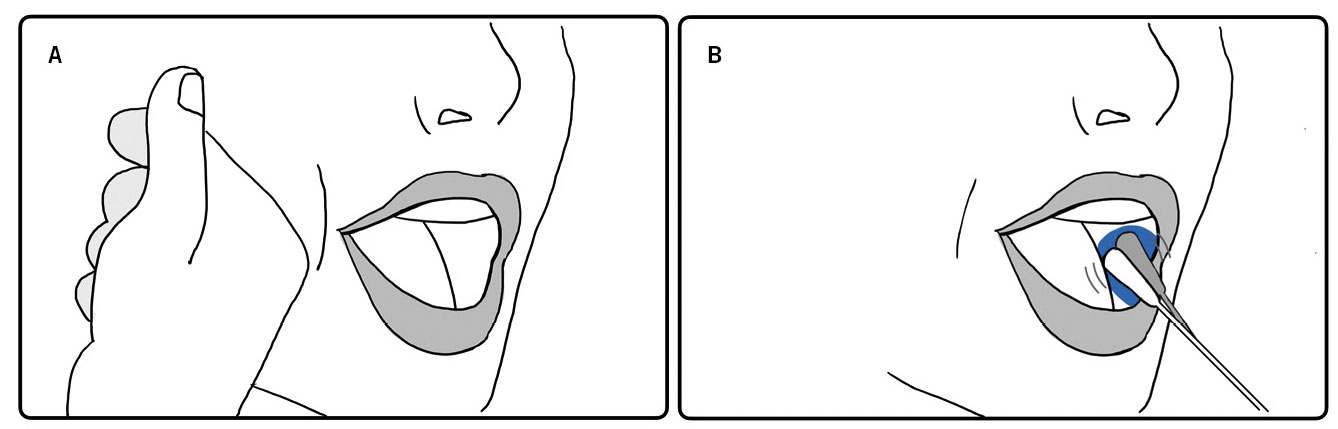
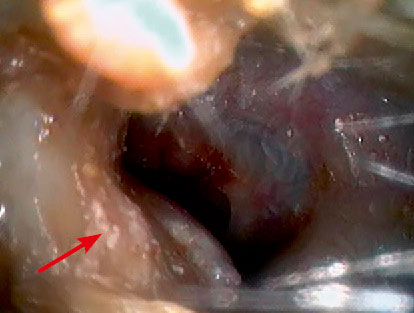
Pese a ser uno de los más frecuentes que hace un pediatra de AP, el diagnóstico de OMA es difícil, puesto que depende de la combinación de una sintomatología clínica, en ocasiones inespecífica, y de la adecuada visualización e interpretación de las anomalías en la membrana timpánica mediante la práctica de la otoscopia. La otoscopia es una exploración difícil y de valoración subjetiva, por lo que hay que practicarla en las mejores condiciones, con la correcta inmovilización del niño, utilizando el espéculo más ancho que permita el conducto auditivo, con ausencia o poca cantidad de cerumen y utilizando una fuente de luz adecuada, puesto que cuando se utilizan otoscopios portátiles, unas pilas medianamente gastadas muestran imágenes de hiperemia timpánica. La presencia de cerumen obstructivo (posible causa de tos crónica) es uno de los problemas más frecuentes que encuentra el pediatra de AP para realizar una otoscopia correcta. La limpieza directa con curetas (metálicas o de plástico) se hace a ciegas, con el riesgo de provocar heridas en el conducto auditivo. El lavado directo sin reblandecimiento previo suele ser doloroso, habitualmente ineficaz y debe hacerse con absoluta certeza de la integridad timpánica. El reblandecimiento pre-lavado requiere de varios días, lo que lo invalida como método para el diagnóstico del cuadro agudo. Las curetas con fuente de luz incorporada (Fig. 2) permiten una extracción guiada y la visualización inmediata de la membrana timpánica en más del 50% de casos en que el cerumen lo impedía inicialmente.

Figura 2. Cureta luminosa para la extracción guiada de cerumen.
Es fundamental hacer un breve recordatorio de aspectos básicos de la otoscopia (Tabla IV):

• La membrana timpánica normal es ligeramente cóncava y presenta un color gris perla o rosado pálido, siendo ligeramente transparente y permitiendo una cierta visualización de las estructuras de oído medio.
• Es de valoración especialmente difícil en el periodo neonatal, por la estrechez del conducto y la opacidad de la membrana timpánica.
• La hiperemia aislada sin otros signos acompañantes (abombamiento, matidez, coloración azul o amarilla) no tiene ningún valor, especialmente si el niño llora, y puede significar simplemente miringitis (inflamación de la membrana timpánica), que frecuentemente acompaña a un proceso catarral vírico, sin derrame asociado en oído medio. La miringitis puede ser una fase inicial de la OMA, por lo que el niño que la presente debe ser seguido evolutivamente, u observarse en la fase de resolución de una OMA. La forma ampollosa (miringitis bullosa) es una forma de presentación de OMA, con la misma etiología, aunque en este caso un posible agente etiológico adicional es Mycoplasma pneumoniae.
• La no visualización del triángulo luminoso no tiene ningún valor.
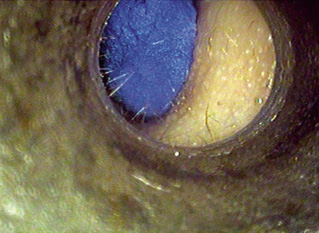
• El color azul o amarillo son sugestivos de otitis media. El tímpano azulado se visualiza más frecuentemente en OME, y el amarillo en OMA, pero esta regla no es patognomónica.
• La hiperemia asociada a matidez es sugestiva de otitis media.
• Las placas blancas en la membrana suelen traducir procesos crónicos o cicatriciales (timpanoesclerosis).
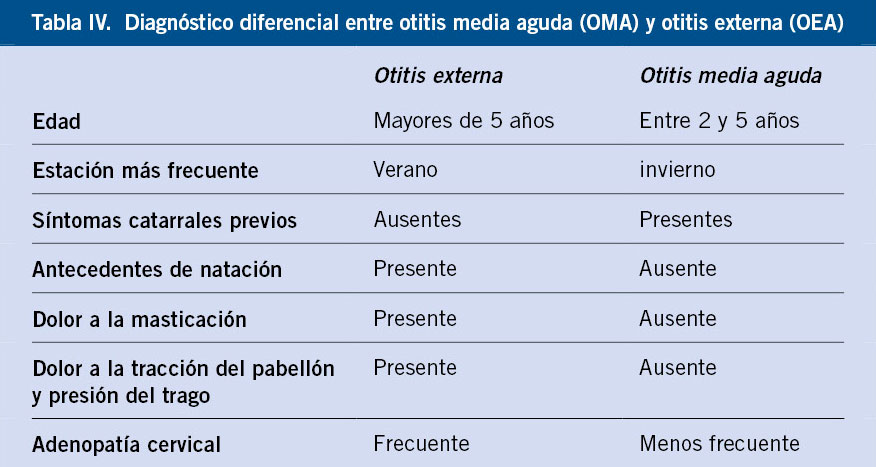
• La retracción timpánica marcada indica presión negativa en oído medio y es sugestiva de OME.
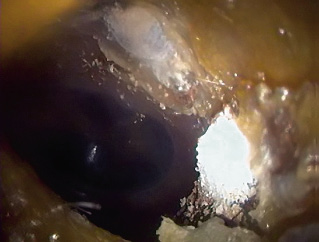
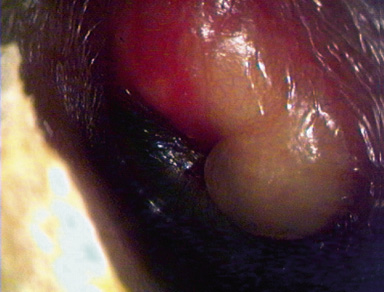
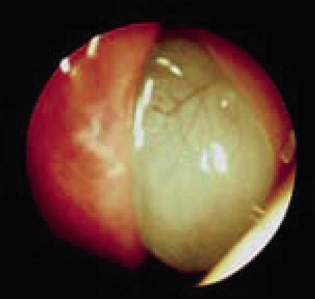
• Son casi patognomónicos de OMA el abombamiento timpánico (Fig. 3) (excepcionalmente presente en OME) y la presencia de una supuración aguda procedente de oído medio. El abombamiento se considera el signo otoscópico con mayor valor predictivo positivo de OMA.
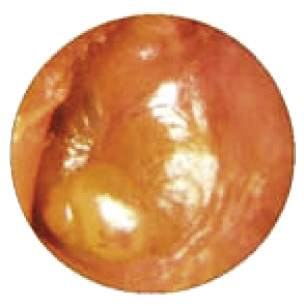
Figura 3. Abombamiento timpánico.
• Los clásicos signos “del trago” o “del pabellón” no tienen valor en el diagnóstico de OMA. En cambio, son muy sugestivos de otitis externa.
• Si estos signos otoscópicos se acompañan de sintomatología clínica aguda, y fundamentalmente de otalgia o su equivalente de irritabilidad en lactantes, se hará el diagnóstico de OMA.
La otoscopia neumática, extensamente descrita en la literatura internacional, es poco utilizada en nuestro medio, ni siquiera por los especialistas. Su posible valor estaría en mejorar la sensibilidad de la otoscopia visual en la detección de OME, acercándose a los resultados de técnicas objetivas, como la impedanciometría. La técnica es muy sencilla, puesto que se trata de adaptar un insuflador de goma a la toma de aire que tienen muchos otoscopios (Fig. 4).
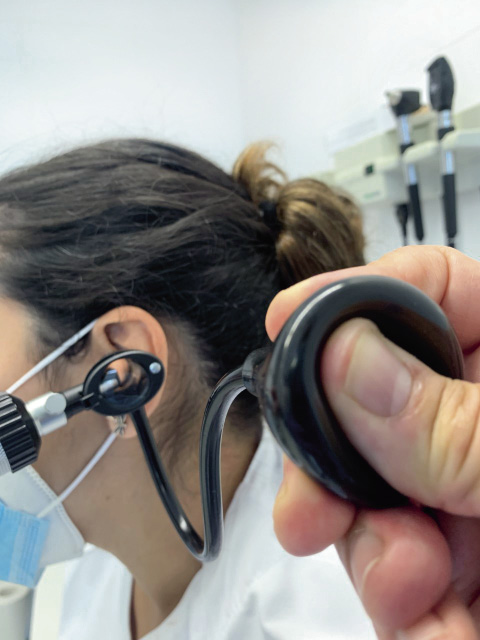
Figura 4. Otoscopia neumática.
Con el espéculo más ancho que permita el conducto del niño, se aplica presión negativa (introducción del insuflador totalmente colapsado en el conducto auditivo y dilatación posterior del mismo, que debe mostrar aproximación de la membrana timpánica hacia el examinador), y luego positiva (contracción del insuflador, que debe mostrar alejamiento de la membrana timpánica del examinador), observando la movilidad de la membrana timpánica. La disminución o abolición de la movilidad a la aplicación de presión negativa es sugestiva de presión negativa en oído medio. La disminución o abolición de la movilidad a la aplicación de presión positiva es sugestiva de OME. Estos cambios se observan fundamentalmente en el cuadrante póstero-superior. Al igual que en la otoscopia convencional, es preciso que el conducto esté limpio de cerumen para una adecuada valoración. La combinación de los hallazgos obtenidos con otoscopia visual y la valoración de la movilidad timpánica aumenta la sensibilidad, especificidad y valores predictivos positivo y negativo en el diagnóstico de otitis media, pero sigue sin presentar la correlación suficiente con los resultados obtenidos con técnicas de detección objetiva de exudado en oído medio. La otoscopia neumática sigue siendo una exploración de valoración subjetiva y se necesita experiencia para poder obtener información adecuada, y un grado de sujeción del niño aún mayor, puesto que la duración y la ligera molestia de la exploración es algo mayor, pero la inocuidad y nulo coste de la técnica la hace muy recomendable en la habitual ausencia en las consultas de AP de métodos de detección objetiva de OME.
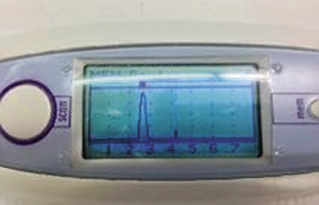
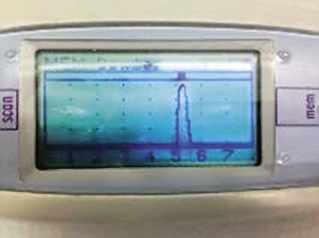
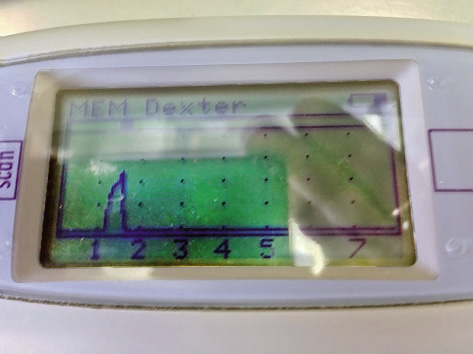
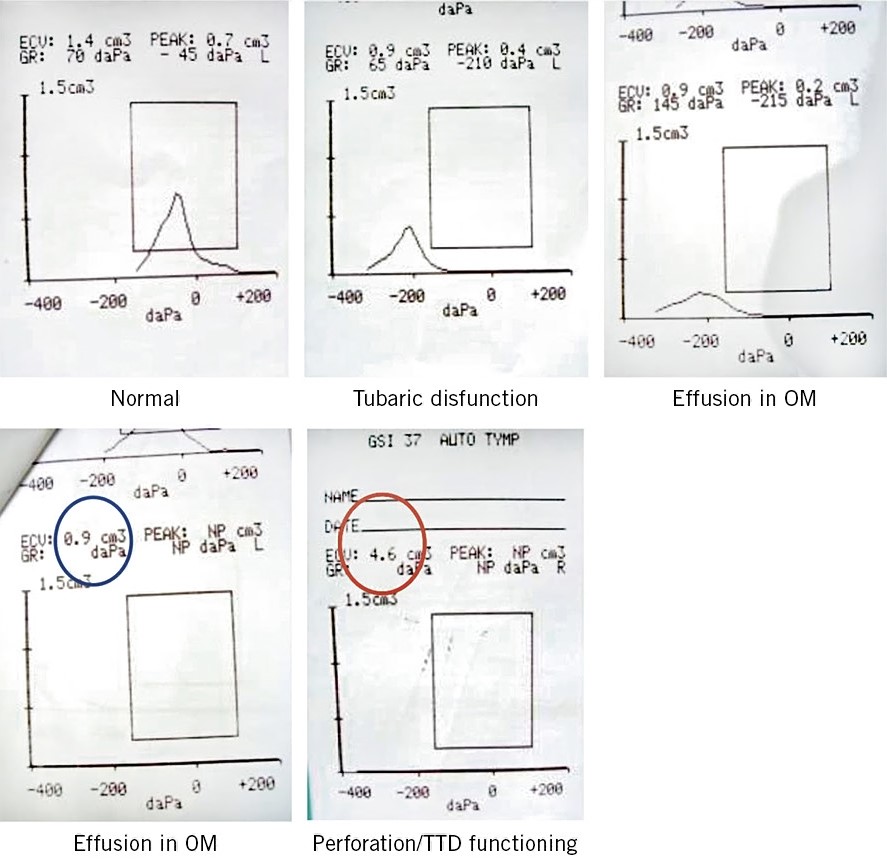
Por la frecuencia del diagnóstico de otitis media, las condiciones, a veces precarias en las que este se produce, y las repercusiones en Salud Pública que comporta errar en el mismo (generalmente por exceso), es necesario que el pediatra de AP pueda disponer en sus consultas de técnicas de detección objetiva de exudado en oído medio. La timpanometría/impedanciometría es una técnica no invasiva validada que permite predecir la presencia de dicho exudado con una sensibilidad y especificidad que la aproxima al patrón de oro en el diagnóstico, que es la timpanocentesis, técnica invasiva que debe reservarse a situaciones muy seleccionadas. Debemos describir brevemente la timpanometría, ya que consideramos imprescindible que el pediatra de AP se familiarice con su uso e interpretación en la consulta diaria(7). La timpanometría se basa en la transferencia de energía acústica de un medio aéreo con poca resistencia (impedancia) a un medio líquido con gran impedancia (cóclea). Si en el oído medio hay líquido que aumenta la resistencia al paso del sonido, se producirá un rebote de energía sonora nuevamente hacia la membrana timpánica, situación que será registrada por el aparato. El timpanómetro aplica automáticamente, en una sola exploración, diferentes presiones que modifican la rigidez de la membrana timpánica. Los cambios pueden verse en una curva llamada timpanograma (Fig. 5), con 3 registros básicos: normal, con una curva picuda y centrada; DTE (curvas desplazadas hacia la izquierda); y OME (curvas planas o indetectables).
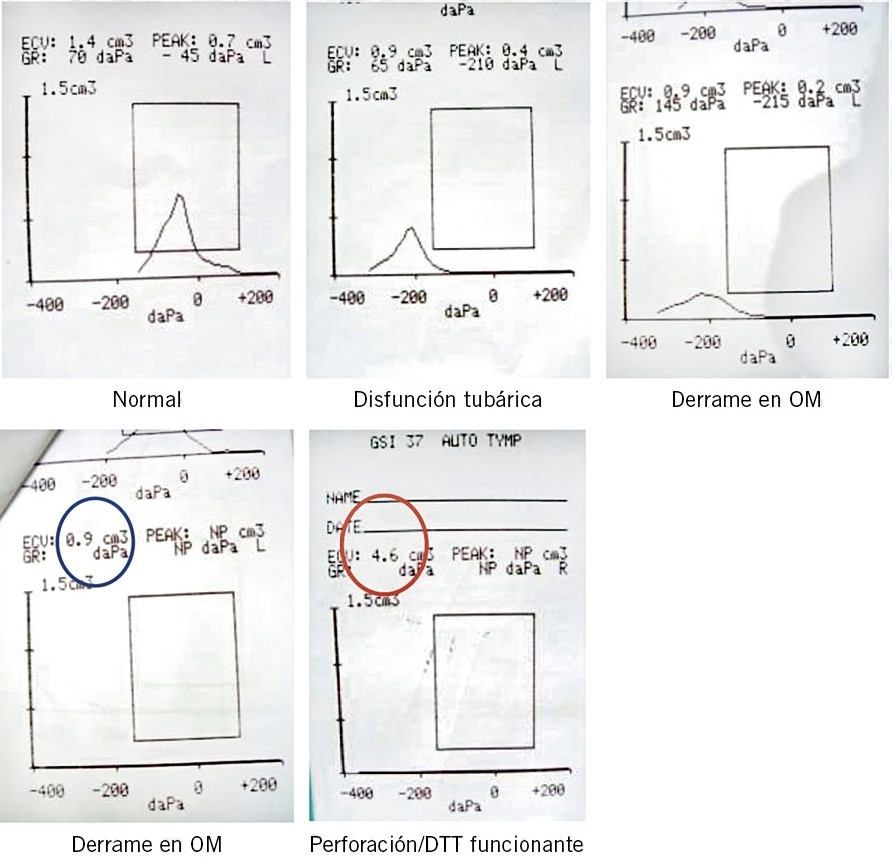
Figura 5. Curvas de timpanograma. OM: otitis media. DTT: drenaje transtimpánico.
Además, el timpanómetro nos da información sobre las presiones en oído medio, lo que nos permite valorar la presencia de DTE (presiones negativas en oído medio, causa frecuente de otalgia, en muchas ocasiones, asociada a un resfriado común, no acompañada de exudado de oído medio y, por tanto, no susceptible de ser tratada con ATB) y sobre el volumen del conducto auditivo externo (CAE). Cuando hay perforación, se produce una continuidad de cavidades entre oído medio y CAE, con un registro de volumen aumentado (>1 ml hasta los 7 años y superior a 2 ml en mayores de 7 años) y diagnóstico de perforación timpánica. Este dato es de extraordinario valor para: detectar pequeñas perforaciones no visibles otoscópicamente, valorar la funcionalidad de los drenajes transtimpánicos (el niño portador de drenajes funcionales debe presentar volúmenes equivalentes a una perforación) y hacer el diagnóstico diferencial, clínicamente no siempre sencillo, entre una otitis media supurada (volumen alto al haber perforación y continuidad entre oído medio y oído externo) y una otitis externa con otorrea (volumen normal, al no haber perforación ni continuidad). La timpanometría nos permite también diferenciar entre miringitis asociada a un proceso catarral (hiperemia de la membrana timpánica, con otalgia intensa, posiblemente con presión negativa en oído medio o DTE, pero sin derrame asociado) y OMA. Una curva totalmente plana, registro muy frecuente en OME, nos indica derrame en oído medio y presión negativa (DTE). La timpanometría ofrece resultados fiables a partir de los 7 meses de vida, puesto que la distensibilidad del conducto auditivo externo en menores de esta edad disminuye algo su sensibilidad, pero se mantiene su especificidad. Los timpanómetros modernos son muy manejables, de poco peso, portátiles, no mucho mayores que un otoscopio convencional, lo que permite incluso su transporte en un maletín de urgencias, y la exploración es rápida, pudiendo optar por imprimir el registro obtenido, o bien visualizarlo e interpretarlo en directo en la pantalla del aparato. Las gráficas obtenidas son de valoración sencilla, fácilmente interpretables con una mínima formación previa, y el examen es totalmente indoloro, siendo muy bien aceptado, tanto por los niños como por sus padres. La timpanometría objetiva la presencia de derrame de oído medio, pero no permite diferenciar entre OME y OMA, diferenciación que debe basarse en la interpretación de la clínica.
Complicaciones
Con la excepción de la mastoiditis, el resto de complicaciones agudas descritas en relación con OMA son excepcionales en la actualidad. El déficit auditivo es la complicación más frecuente a medio y largo plazo.
Las complicaciones graves en la fase aguda (petrositis, laberintitis, parálisis facial, meningitis, absceso cerebral…) se han reducido drásticamente desde la utilización general de ATB en la OMA. Únicamente, la mastoiditis se observa con alguna frecuencia en la actualidad. Debe sospecharse mastoiditis siempre que se presente enrojecimiento, tumefacción y dolor en región mastoidea. La sospecha debe confirmarse derivando al niño al hospital para practicar estudios de imagen. Se especuló que la reducción en el uso de ATB en OMA se ha acompañado de un leve aumento en la frecuencia de mastoiditis, pero estudios más recientes(8) parecen descartar esta hipótesis.
La complicación más frecuente es el déficit auditivo, prácticamente universal en la fase aguda (25 dB de pérdida media, equivalente a llevar tapones) y, habitualmente, reversible una vez alcanzada la curación. Después de un episodio de OMA, un 40% de pacientes presentan OME a las 4 semanas y un 10% a los 3 meses, con repercusión funcional variable, que no depende de la consistencia del fluido, por lo que hay que asegurar un adecuado control evolutivo después del tratamiento que constate la desaparición del derrame. La duración del derrame no parece tener relación con la eficacia del tratamiento antibiótico en la esterilización del mismo.
El pediatra de AP debe vigilar la posible aparición de complicaciones en otitis crónica: la retracción de la membrana timpánica que se observa cuando la presión en oído medio es permanentemente negativa, puede acompañarse de colesteatoma, masa de epitelio estratificado que invade la cadena osicular, con adhesión de los huesecillos (otitis adhesiva) o discontinuación/desarticulación entre los mismos, que genera pérdida auditiva potencialmente irreversible. Puede sospecharse ante una perforación crónica, con o sin supuración asociada, o cuando se observe una masa blanquecina retrotimpánica. En caso de sospecha, debe derivarse el paciente al especialista.
Más frecuente es observar timpanosclerosis, parches blancos en la superficie de la membrana timpánica, secundarios a cicatrices post drenaje transtimpánico o en niños afectos de OMA de repetición. Es conveniente valorar la audición en estos niños, aunque generalmente es un hallazgo sin repercusión funcional.
Derivación hospitalaria
La OMA es una patología de manejo inicial exclusivo del pediatra de AP. La derivación debe hacerse únicamente ante sospecha de mastoiditis o de complicaciones neurológicas, y cuando sea imperativo el conocimiento exacto del germen causante o en situaciones de fracaso terapéutico en que la timpanocentesis ejerce un papel diagnóstico y terapéutico en la resolución de la otalgia.
La OMA es una enfermedad de manejo prácticamente exclusivo por el pediatra de AP. Se procederá a la derivación hospitalaria ante la obligación de practicar timpanocentesis en las siguientes situaciones (Tabla V):

• Obligación de conocer con precisión el germen causante: inmunodeprimidos primarios o secundarios y OMA en el periodo neonatal, frecuentemente producida por gram negativos y gérmenes oportunistas.
• Cuando haya clínica persistente (dolor y/o fiebre) pese a una pauta antibiótica standard correcta (ATB de 1ª línea, ausencia de mejoría y cambio a las 72 horas por ATB de 2ª línea y nuevo fracaso terapéutico). En este caso, la timpanocentesis tiene tanto valor diagnóstico como terapéutico, al aliviar un dolor persistente y su realización debe considerarse una emergencia. No es razonable pautar un tercer ATB, como es práctica común, si las opciones manejadas anteriormente eran correctas, con la posible excepción del uso de ceftriaxona que analizaremos posteriormente.
• Cuando haya sintomatología neurológica: derivar ante la sospecha de complicaciones poco frecuentes, tales como: petrositis, meningitis, laberintitis y parálisis facial.
• Ante la sospecha de mastoiditis.
Tratamiento
El tratamiento de la OMA debe empezar por una correcta analgesia. La utilización o no de ATB debe fundamentarse en un correcto diagnóstico de OMA (con la presencia de dolor o su equivalente en lactantes) y en no tratar otoscopias positivas, sino la combinación de clínica específica y signos otoscópicos sugestivos, preferentemente confirmados con otoscopia neumática y, si es posible, con timpanometría. La amoxicilina a altas dosis es el tratamiento de 1ª elección. Cefuroxima es la mejor opción si se utiliza una cefalosporina. Los macrólidos no deben utilizarse, salvo en caso de alergia anafiláctica a la penicilina. Ceftriaxona puede ser una opción a considerar en caso de precisarse la vía parenteral o como último recurso previo a la derivación hospitalaria.
Analgésicos
Es el primer paso obligado (¡a veces, olvidado!) en el manejo de la OMA. La utilización de paracetamol a 15 mg/kg/dosis cada 4-6 horas (límite 60 mg/kg/día en lactantes y 90 en mayores de 1 año) suele ser suficiente. El ibuprofeno a 10 mg/kg/dosis cada 6 horas (límite 60 mg/kg/día) es una opción razonable, especialmente si no hay aceptación del paracetamol. Hay menos experiencia pediátrica con el metamizol magnésico, que debería reservarse a casos de no respuesta a los anteriores. La supuesta ventaja de utilizar analgésicos que tengan acción antiinflamatoria motiva que algunos pediatras (y muchos padres) prefieran ibuprofeno, pero tal ventaja no ha sido demostrada concluyentemente en ningún estudio. En caso de fracaso terapéutico, es útil asociar codeína (0,5-1 mg cada 4 horas) al paracetamol, pero nunca en menores de 12 años. Es recomendable, en las primeras 24 horas, pautar el analgésico a dosis fijas, para seguir posteriormente según necesidad. La utilización de calor local puede ser útil. No deben utilizarse analgésicos tópicos, puesto que no mejoran los resultados obtenidos con analgesia general, dificultando en cambio la otoscopia posterior.
Antibióticos
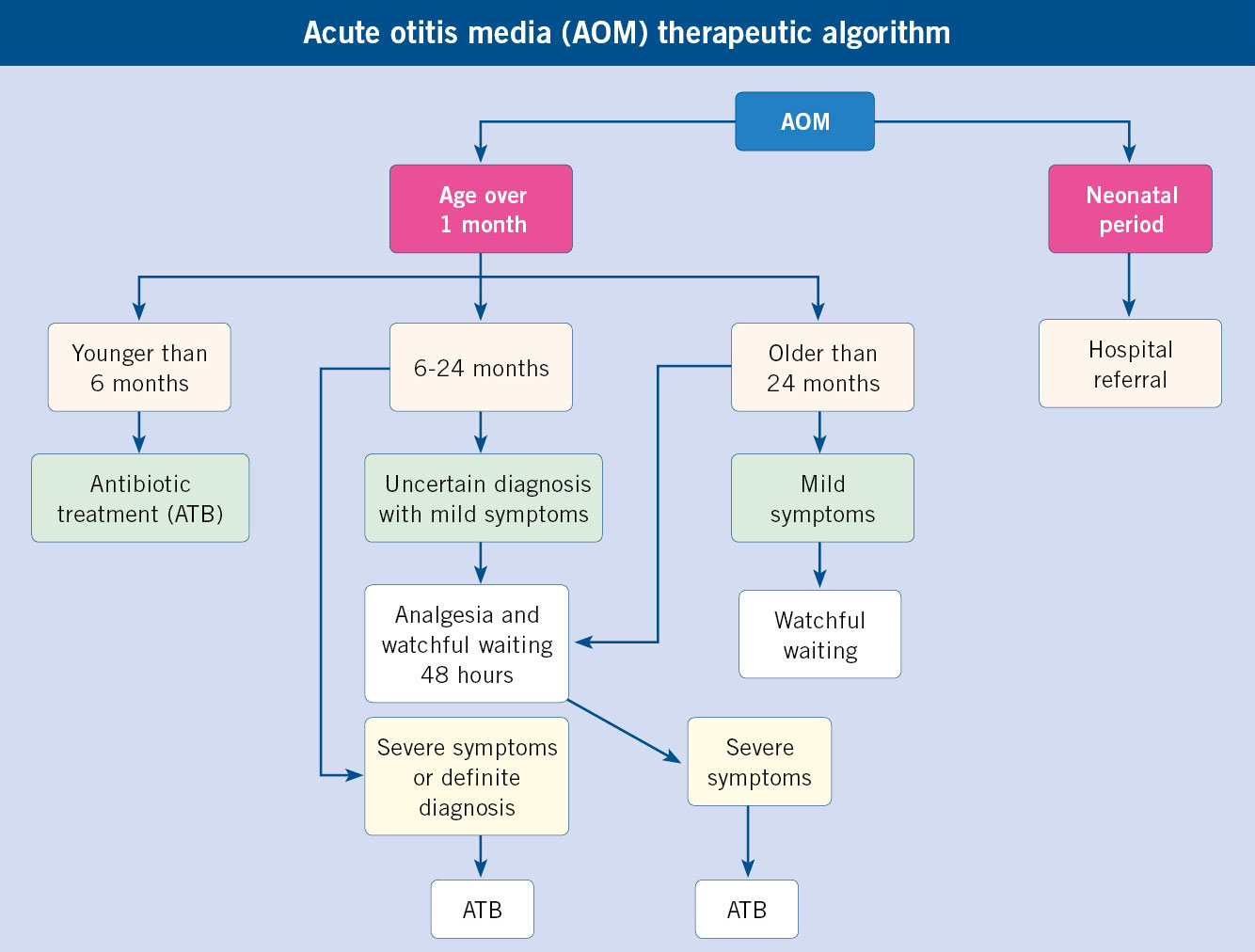
El tratamiento ATB de la OMA ha sido siempre un tema controvertido. Varios metaanálisis han coincidido en concluir que, si bien la mayor parte de OMA se resuelven espontáneamente, el tratamiento ATB tiene un efecto significativo, aunque modesto en la mejora de la sintomatología aguda (desaparición de la fiebre y otalgia). Según diferentes estudios habría que tratar entre 8 y 17 casos de OMA con ATB para obtener una mejora sintomática en uno (número necesario de tratamientos para obtener mejora en 1 caso o NNT). Recientemente, y con criterios diagnósticos más restrictivos, que tienden a diferenciar más claramente OMA de OME, la NNT se reduce hasta 3, potenciando el valor real de los ATB. En la actualidad, se considera que la principal utilidad de la utilización de ATB está en la prevención de complicaciones a corto (mastoiditis) y largo plazo (otitis media crónica con hipoacusia de transmisión y posible retraso del lenguaje y del rendimiento escolar), pese a que esta complicación está siendo actualmente puesta en entredicho. La llamada “pauta holandesa”, nombre que se debe al hecho de que la conducta observacional se empezó a aplicar en Holanda, consistente en la observación durante 2-3 días sin tratamiento antibiótico inicial con una segunda valoración para tomar una decisión definitiva, o en algunos casos, con la –a nuestro parecer– poco recomendable prescripción “diferida” de ATB (“y si no mejora en 3 días, empiece a darle…”), que presupone una capacidad de valoración evolutiva e interpretación de los síntomas por parte de los padres que muchas veces no se da, se ha relacionado inicialmente con un ligero aumento en el número de mastoiditis en los países en que se aplica masivamente. La valoración del impacto real de este hecho está siendo objeto de discusión, y no parece confirmarse en estudios recientes. Ciertamente, en los países que tratan las OMA con la “pauta holandesa” (Holanda, Escandinavia…) o “watchful waiting”/”esperar y ver”, hay una tasa de resistencia de neumococo ante la penicilina muy inferior a aquellos en que la OMA es tratada sistemáticamente. Por otra parte, se ha llamado la atención sobre las conclusiones de los metaanálisis que valoran el efecto de los ATB en la evolución de la OMA. En muchos de los trabajos analizados, no hay criterios claros en la definición de la OMA. Es muy probable que muchos casos incluidos en estos trabajos sean en realidad OME, en las que el efecto del ATB es mucho menor o nulo, condicionando una marcada similitud con el grupo control de no tratados. Pensamos que el objetivo del pediatra de AP debe estar en tratar auténticas OMA y no otoscopias positivas (diferenciación no siempre fácil) y, sobre todo, en evitar los ATB en patología respiratoria primariamente viral (resfriado común, la mayor parte de faringitis, laringitis, bronquitis aguda, bronquiolitis, neumonitis). Son necesarios más estudios que determinen definitivamente qué factores están relacionados con la resolución espontánea y ausencia de complicaciones para dejar las OMA inicialmente sin tratamiento ATB. No hay datos concluyentes al respecto, pero con las evidencias actuales parece razonable suponer que en niños mayores de 2 años, con una clínica leve (otalgia leve y fiebre inferior a 39ºC) y sin factores de riesgo generales (enfermedad crónica, inmunodeficiencia…) o locales (perforación timpánica con supuración, antecedentes de OMAR, procedimientos quirúrgicos relacionados con patología del oído medio, como timpanostomía, drenajes transtimpánicos, adenoidectomía) y OMA unilateral, el riesgo de no tratar inicialmente con ATB una OMA es menor, y probablemente pueda asumirse con seguridad. En la guía de práctica clínica de la Academia Americana de Pediatría (AAP)(9), se reduce esta edad mínima de inicio de la conducta observacional hasta los 6 meses, considerando esta posibilidad como una alternativa al tratamiento ATB entre los 6 y 24 meses cuando la clínica sea leve y la OMA unilateral, y tratando con ATB cuando la clínica sea grave (fiebre >39ºC u otalgia intensa) o la OMA sea bilateral (Tabla VI).

Se ha demostrado que la presencia de OMA bilateral se relaciona con mayor frecuencia que la unilateral con: presencia de bacterias en el exudado de oído medio, especialmente HI, mayores signos inflamatorios timpánicos, menor edad y mayor persistencia de la sintomatología sin tratamiento ATB. Estudios que valoran el seguimiento de las conductas de observación inicial muestran que solo 1/3 de casos recurren al ATB de rescate.
Una vez planteada la necesidad del tratamiento ATB, la duración del mismo también es motivo de controversia. Clásicamente, se han tratado durante 10 días, por extrapolación del tratamiento de la faringitis estreptocócica. Sin embargo, el estreptococo supone menos del 5% de la etiología de la OMA. Hay estudios que demuestran resultados clínicos semejantes con pautas de 3, 5, 7 y 10 días. En cambio, hay más dudas sobre el efecto de tratamientos cortos en la prevención de recidivas y secuelas a largo plazo. Dado que estas secuelas son más frecuentes en niños de menos de 2 años, que están poco representados en los estudios de pautas cortas, la recomendación actual está en tratar durante 10 días a estos niños, y a los de cualquier edad con OMA supurativa (con perforación timpánica), historia de OMA de repetición, otitis media crónica o procedimientos quirúrgicos relacionados con hipoacusia de transmisión (adenoidectomía, drenaje transtimpánico, miringostomía) y reducir la duración a 5-7 días para niños mayores sin factores de riesgo.
Valoración actual de ATB potencialmente utilizables en OMA
Vamos a referirnos únicamente a los más utilizados en nuestro medio. La efectividad de un ATB en el tratamiento de la OMA depende fundamentalmente de la susceptibilidad de los patógenos causantes al mismo y de la capacidad del fármaco de alcanzar niveles suficientes en oído medio para erradicar el otopatógeno. Esta capacidad está directamente relacionada con el tiempo que el ATB está por encima de la concentración inhibitoria mínima (CIM). Este tiempo está determinado para los betalactámicos en el 40% del intervalo de dosificación.
Amoxicilina; amoxicilina+ácido clavulánico (A+C)
La amoxicilina, sola o en asociación con el ácido clavulánico, debe ser considerada como el tratamiento de 1ª elección, por su espectro de actividad, seguridad, tolerancia y coste. Sus concentraciones inhibitorias mínimas (CIM) ante neumococo son las más bajas de todos los ATB orales utilizables en Pediatría y su penetración en oído medio solo es igualada por la ceftriaxona. El ácido clavulánico es un betalactámico que, por sí solo, tiene una escasa actividad antibacteriana y una capacidad inductora de resistencias poco significativa. Su función es la inhibición competitiva, irreversible y suicida de las betalactamasas, restituyendo a la amoxicilina su espectro inicial, que fue perdiendo progresivamente, primero frente a estafilococo y, posteriormente, frente a HI y otros gérmenes productores de betalactamasas. Siguiendo este concepto, debemos considerar que, en la actualidad, disponemos de dos amoxicilinas: una de espectro más reducido, que a nivel de OMA presenta actividad adecuada frente a neumococo sensible a penicilina (CIM < 2 ng/ml), y a altas dosis frente a neumococo con sensibilidad intermedia (CIM 2-8 ng/ml) e incluso algunas cepas de neumococo resistente (>8 ng/ml), y frente a Streptococcus pyogenes, pero inactiva ante HI productor de betalactamasas, Moraxella catarralis (100% productor de betalactamasas, pero de escasa presencia en nuestro medio) y staphylococcus aureus. La otra amoxicilina, asociada a ácido clavulánico, extiende su actividad a los gérmenes productores de betalactamasas. La preferencia por una u otra vendrá dada por la situación epidemiológica. Se han empezado a describir HI resistentes a la asociación A+C, por un mecanismo de alteración de proteínas fijadoras de penicilina similar al del neumococo resistente, y no por producción de betalactamasas. El impacto de este fenómeno por ahora parece poco relevante. En nuestro medio, hay pocos estudios de timpanocentesis y cultivo del exudado de oído medio. Los datos disponibles permiten suponer una frecuencia del 25% de HI como agente causante de OMA en la era prevacunal, pero el aumento de las coberturas de vacunación antineumocócica parece desplazar la frecuencia etiológica hacia el predominio de HI.
Algunos autores han defendido la inocuidad y resolución espontánea de las OMA producidas por HI no capsulado, como argumento para recomendar tratar únicamente el neumococo. Sin embargo, hay estudios que muestran el importante papel de HI en la producción de recidivas y secuelas crónicas y, contrariamente a la creencia común, el cuadro clínico no es diferenciable del producido por neumococo. Algunos autores proponen la utilización inicial de la asociación A+C en cuadros graves (fiebre superior a 39ºC y/o otalgia severa), pero la mayor intensidad de los síntomas no está relacionada con la etiología por HI. Sea cual sea la amoxicilina escogida, deberá utilizarse a dosis no inferiores a 80 mg/kg/día, (máximo 3 g al día) fraccionada en 2-3 tomas y administrada previamente a la ingesta de alimento, con lo que mejora sensiblemente la tolerancia. No es preciso usar una pauta estricta de cada 8 horas. El fraccionamiento de la dosis total en 3 tomas de intervalos irregulares ofrece los mismos resultados. La utilización de dosis altas está especialmente indicada en niños menores de 2 años escolarizados y en los que han recibido recientemente un betalactámico. En otras circunstancias puede ser correcto iniciar un tratamiento con dosis convencionales (40-50 mg/kg/día). En la práctica actual, la dosificación alta de entrada se ha convertido en la norma general, pero no hay estudios que cuantifiquen la tasa de fracasos terapéuticos en ambas circunstancias. La sistematización de vacunas antineumocócicas conjugadas comporta una disminución de la prevalencia de serotipos resistentes a la penicilina, por lo que es probable que las recomendaciones de dosificación se modifiquen a la baja en un futuro próximo. En EE.UU., se han aprobado presentaciones destinadas a su administración en 2 tomas, pero existe poca experiencia pediátrica al respecto y dudas sobre su capacidad de erradicación de neumococo en oído medio, al presentarse datos contradictorios sobre el tiempo en que se mantienen niveles superiores a la CIM en el intervalo entre dosis. La asociación con ácido clavulánico en su formulación actual de 8:1 facilita alcanzar estas dosis sin aumentar los efectos secundarios gastrointestinales, más frecuentemente dependientes del ácido clavulánico que de la amoxicilina. El ácido clavulánico aumenta el peristaltismo del intestino delgado y produce más frecuentemente diarrea. Sin embargo, estos efectos se minimizan con la administración previa a comidas, con la ingesta de yogurt o probióticos y, raramente, obligan a suspender el tratamiento.
Cefuroxima axetil
Tiene la mayor actividad antineumocócica de todas las cefalosporinas orales, pero tanto en potencia como en penetración en oído medio es muy inferior a la amoxicilina. Es una opción a considerar en las frecuentes historias de dudosas alergias a la penicilina con antecedentes de clínica no anafiláctica en las que se prefiera utilizar un betalactámico a un macrólido, en aquellos pacientes no conocidos o no habituales en nuestra consulta, catalogados anteriormente, probablemente de manera errónea, como “alérgicos a la penicilina”. Es un antibiótico poco aceptado por los niños por su sabor. Hay que saber que las alergias cruzadas entre penicilinas y cefalosporinas son mucho menos frecuentes que lo que se creía, y lo son más en cefalosporinas de primera (17%) que en las de segunda y tercera (que son las que se utilizarían en OMA, con un 0,5%).
Cefixima
Tiene pobre actividad frente neumococo con sensibilidad intermedia o resistente a la penicilina. En cambio, tiene la mejor actividad frente a HI de todos los ATB orales, por lo que puede ser una buena opción, dada su tolerancia y comodidad posológica, cuando se sospeche fuertemente su presencia, como en el síndrome OMA-conjuntivitis purulenta homolateral.
Ceftriaxona
Su potencia antineumocócica y su excelente penetración en oído medio, la convierten en una opción muy interesante en el tratamiento inicial a dosis única (50 mg/kg), indicación aprobada por la FDA, o bien en 3 dosis sucesivas cada 24 horas ante la sospecha de neumococo resistente a la penicilina, en situaciones de fracaso terapéutico, como último paso previo a la derivación para timpanocentesis. Dada su alta vida media, estas 3 dosis también pueden ser administradas a días alternos o incluso cada 3 días, si fuese necesario. En cualquier caso, su uso debe ser individualizado y fuertemente restringido a situaciones muy especiales. Es una opción a valorar, especialmente en casos de marcada intolerancia a la vía oral.
Claritromicina
En comodidad posológica y tolerancia, es inferior a azitromicina.
Azitromicina
Debe considerarse tratamiento de 1ª elección de OMA en niños con alergia anafiláctica a la penicilina. Sin embargo, no debe ser tratamiento de 1ª elección en otras circunstancias pese a su comodidad posológica, puesto que se ha mostrado claramente inferior a amoxicilina en la capacidad de erradicación de neumococo y haemophilus de oído medio. La pauta de 3 días y la de 5 se han mostrado con eficacia similar, por lo que parece más recomendable utilizar la pauta corta. El creciente uso de macrólidos en los años 90 comportó un marcado aumento de neumococo y Streptococcus pyogenes resistentes. Una política de ATB más contenida en los últimos años, ha empezado a revertir esta tendencia. Al contrario que en la resistencia de neumococo a betalactámicos, el aumento de dosis no significa mejorar la actividad.
Clindamicina
30-40 mg/kg/día. Es una opción a considerar en niños con alergia anafiláctica a la penicilina que hayan experimentado un fracaso terapéutico con macrólidos, pero no hay presentación pediátrica.
Control evolutivo y fracaso terapéutico
El paciente debe ser controlado si no mejora a las 72 horas, tanto si se ha utilizado un antibiótico como si se ha decidido una conducta expectante. La lenta resolución de las anomalías otoscópicas aconseja diferir el control a varias semanas después del diagnóstico.
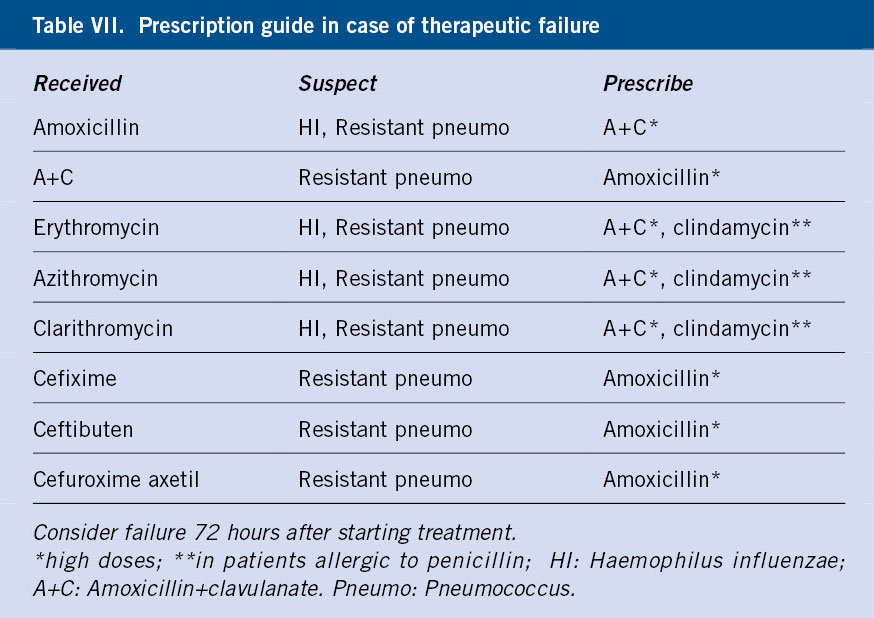
La creciente incidencia de gérmenes resistentes comporta un aumento de los fracasos terapéuticos. Debe considerarse esta situación, cuando a las 72 horas de un tratamiento ATB, el niño sigue con dolor y/o fiebre. Esta situación se da en un 15% de ocasiones. En este caso, se escogerá un ATB de 2ª línea según la opción inicial y la sospecha del germen implicado (Tabla VII).
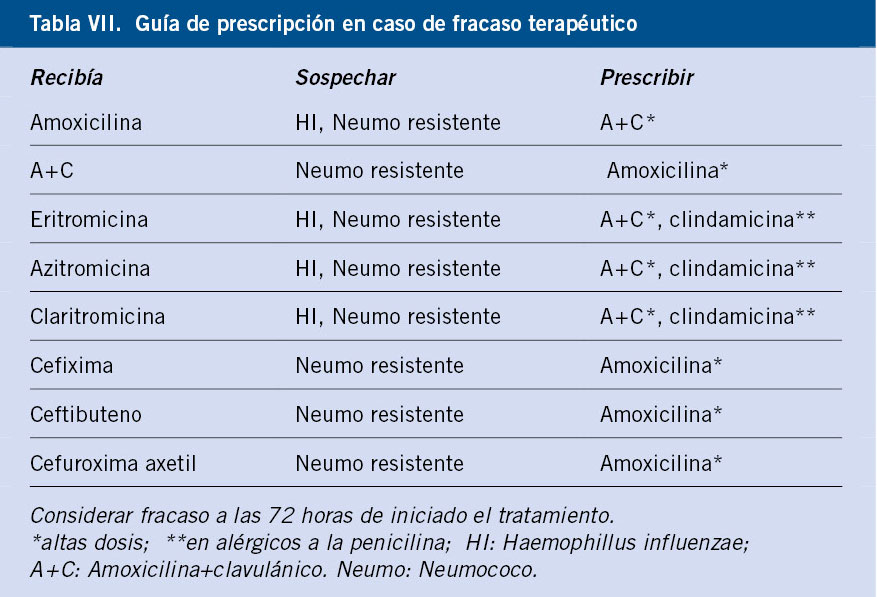
Si no se produce respuesta en 48 horas y siempre individualizando el caso, deberá derivarse al paciente para proceder a timpanocentesis (que aliviará el dolor) y cultivo del exudado. Las dificultades de coordinación con el nivel especializado que muchos pediatras tienen en nuestro medio, comporta que, en muchas ocasiones, estos niños acaben recibiendo inadecuadamente un tercer ATB, por lo que en este punto, podría considerarse el uso siempre muy selectivo y restrictivo de ceftriaxona. El control posterior de la desaparición de la OME deberá hacerse no antes de las 3-4 semanas del final del tratamiento. En niños mayores con OMA esporádica leve y sin factores de riesgo, es planteable incluso la posibilidad de no hacer ningún control si la evolución clínica es favorable.
Otitis media aguda con supuración
La OMA supurada debe tratarse siempre con ATB y recibir el mismo manejo terapéutico que la OMA con membrana timpánica integra, salvo en la duración del tratamiento antibiótico, que debe ser de 10 días.
La perforación de la membrana timpánica con evacuación de exudado purulento y eventualmente de sangre es tan común en la evolución de la OMA, que debe considerarse una forma de presentación clínica más que una complicación. Generalmente, el dolor desaparece después de la perforación. El manejo terapéutico deberá hacerse siguiendo el mismo algoritmo de actuación de la OMA sin supuración, puesto que la presencia de supuración no tiene ninguna implicación en cuanto a la sospecha del germen implicado, aunque en este caso aumenta el aislamiento de Streptococcus pyogenes y estafilococo. Un inicio muy agudo con otalgia intensa y supuración rápida se relacionó clásicamente como muy sugestivo de neumococo, pero esta evolución es compatible con HI y otros gérmenes. El tratamiento ATB deberá prolongarse siempre durante 10 días, independientemente de la edad del niño. No hay suficiente documentación que avale el tratamiento inicial con ciprofloxacino ótico, que en cambio es una excelente opción ante fracaso terapéutico y en otitis medias supurativas crónicas (superiores a dos meses), que antes eran subsidiarias de ingreso para tratamiento parenteral antipseudomónico. Mycobacterium tuberculosis es una rara causa de OM supurativa crónica. En las otitis medias supurativas crónicas hay afectación concomitante de las celdas mastoideas y debe descartarse siempre la presencia de colesteatoma. El colesteatoma es una tumoración benigna del oído medio formada a partir de restos epiteliales. Hay que sospecharla ante una coloración blancuzca opaca en membrana timpánica, la presencia de un pólipo, restos caseosos o supuración maloliente persistente. Deberá remitirse siempre al ORL para cirugía. Deberá hacerse un seguimiento de la perforación timpánica para constatar su cierre, y derivar al especialista aquellas que no lo hayan hecho en 3 meses, para seguimiento estrecho y valorar la necesidad de practicar una plastia. Algún estudio reciente parece mostrar superioridad de la asociación de antibiótico sistémico con ciprofloxacino tópico en relación a las 2 opciones por separado, pero estos datos deberán confirmarse.
Otitis media aguda de repetición (OMAR) y otitis media crónica con exudado (OMEC)
Definiciones
Se define como OMAR: la presencia de 3 o más episodios de OMA en 6 o menos meses, o 4 o más en 12 o menos meses, siempre que el último de los episodios se haya producido en los últimos 6 meses. Se define como OMEC: la presencia de exudado bilateral más de 3 meses o unilateral más de 6 meses. Frecuentemente, coexisten ambas entidades.
Se considera que un niño sufre de otitis media aguda de repetición cuando presenta 3 o más episodios en un plazo igual o inferior a 6 meses o 4 o más en un plazo inferior a 12 meses, siempre que el último se haya producido en los últimos 6 meses. Esta frecuencia se ha correlacionado significativamente con la aparición de secuelas a medio y largo plazo (OMEC) y/o hipoacusia de transmisión. Cuando una otitis media con efusión, exudado o derrame bilateral persiste más de 3 meses, o de 6 meses si es unilateral, hablamos de OMEC. Frecuentemente, coexisten ambas patologías (OMAR con OMEC).
Epidemiología
La otitis media aguda de repetición y la otitis media crónica con exudado son los problemas crónicos más frecuentes en la consulta del pediatra de AP.
Un 80% de niños menores de 3 años han tenido como mínimo un episodio de OMA, y un 33% han tenido 3 o más ataques. La OMAR no suele ser la única manifestación de problemas inmunológicos importantes y los estudios complementarios no están indicados en estos niños, salvo si hay otras infecciones concomitantes de repetición u otros signos clínicos que sean sospechosos de inmunodeficiencia. Es probable que ciertos problemas inmunológicos leves y madurativos puedan manifestarse únicamente como OMAR. Se ha demostrado en estos niños, un nivel de IgA significativamente inferior a niños sin OMAR. Un grupo relevante de estos niños tiene respuestas de Ac frente a las vacunaciones habituales significativamente inferiores a niños sin OMAR. Se discute el posible papel del déficit de subclases de IgG2. En algunos estudios, la administración de gammaglobulina a niños pequeños con OMAR mostró cierto beneficio. Se ha comunicado que los niños con OMAR presentan respuestas no protectoras frente a algunas inmunizaciones comunes, beneficiándose de la inmunidad de grupo en ambientes con altas coberturas vacunales(10). Independientemente de los problemas creados por los episodios agudos, el pediatra de AP debe tener como objetivo fundamental en el manejo de esta patología, preservar la audición en la fase decisiva de aprendizaje del lenguaje. Se sugiere en abundantes estudios, que la OMAR y la OMEC en los primeros años de vida tienen un efecto adverso significativo: en la comprensión del lenguaje, en el habla, en la lectura e incluso en la adquisición de funciones motoras groseras, que se mantiene hasta los 9 años de edad. Estudios de seguimiento hasta los 18 años de edad, muestran mayor frecuencia de trastorno de déficit de atención e hiperactividad a los 15 años, menor coeficiente intelectual a los 13 y mayores dificultades de lectura a los 11-18 años en niños con OMEC en los primeros años de vida. En otros estudios, se han cuestionado estos resultados, en base a supuestos defectos metodológicos. Un estudio multicéntrico, con un control estricto de las distintas y múltiples variables, demostró que no hay diferencias significativas en adquisición de lenguaje, aprendizaje o desarrollo psicomotor o social a los 3 años, entre niños con OMEC a los que se practique drenaje transtimpánico precoz o tardío. La confusión de estos datos obliga a que el pediatra los maneje con precaución y valore al niño con OMAR y/o OMEC como un niño de riesgo para un posible problema de audición-aprendizaje, pero que quizá sea más conservador en su tratamiento de lo que ha sido generalmente práctica habitual.
Otitis media aguda de repetición
Determinados factores favorecen su presencia (Tabla VIII): sexo masculino, hermano con antecedentes de OMAR, primer ataque de OMA antes de los 4 meses, inmunodeficiencia primaria o secundaria, lactancia artificial, asistencia a guardería con más de 6 niños en el grupo, tabaquismo pasivo, uso del chupete más allá de los 6 meses, presencia de fisura palatina aparente u oculta (úvula bífida), síndrome de Down y sensibilización a alérgenos.

Conducta
Antes de abordar un posible caso de OMAR, el pediatra de AP deberá ser muy cuidadoso en etiquetar así a un paciente, dado que pocas veces el diagnóstico se establece basándose en una correcta documentación de los distintos episodios de OMA, confundiendo en realidad OME con OMA. Los diagnósticos hechos sin métodos de detección objetiva de exudado en oído medio son poco fiables sin la presencia de clínica u otoscopia muy específicas (otalgia, abombamiento timpánico). En muchas ocasiones, se cataloga como OMA cualquier cuadro catarral o febril sin focalidad en el que la otoscopia sugiera OME.
El paso inicial es la eliminación de factores predisponentes cuando sea posible: plantear a los padres la posibilidad de retirada, al menos, temporal, de la guardería, evitar el tabaquismo pasivo, la exposición a alérgenos, vacunar de la gripe en el periodo indicado (con la reducción de hasta el 40% de episodios de OMA en el periodo epidémico en niños que van a guardería en algunos estudios, y sin diferencias significativas en otros) y restricción preventiva del uso del chupete en niños mayores de 6 meses a los momentos de conciliación del sueño, con retirada absoluta a partir de los 10 meses (reducción de hasta un 33% de ataques de OMA en algún estudio). La vacuna antineumocócica conjugada 13-valente ha mostrado una reducción significativa en el número de episodios. Algunos estudios mostraron que los chicles de xilitol tienen un efecto beneficioso significativo, pero a dosis poco realistas (5 chicles al día, dado que 3 no son efectivos, y durante todo el periodo epidémico de infecciones respiratorias). El pediatra de AP debe descartar también patología asociada a la OMAR, como: las inmunodeficiencias, que solo se manifestarán con OMAR sin otras patologías en casos excepcionales; la discinesia ciliar primaria; y la (excepcional) neoplasia de cavum. Sin embargo, es probable que el niño con OMAR presente alteraciones en la respuesta inmune, tanto innata como adaptativa a los otopatógenos que causan OMA. Se ha demostrado que la presencia de una flora variada en nasofaringe concretamente la de Corynebacterium spp y Dolosigranulum, es un factor protector para el desarrollo de OMAR(11).
Si bien, abundante literatura demostró que la OMAR se podía manejar adecuadamente en AP con profilaxis antibiótica durante un periodo de tiempo de 3 (primavera-verano) a 6 meses (otoño-invierno), lo que reducía significativamente el número de episodios (1,04/niño/año con placebo a 0,28/niño/año con ATB), esta práctica se ha ido abandonando ante el problema creciente de inducción de resistencias antibióticas. Cuando está presente una clínica de obstrucción nasal persistente, debida con casi toda seguridad a hipertrofia de las vegetaciones adenoideas, es razonable la derivación especializada de entrada, para la práctica de adenoidectomía. La adenoidectomía asociada a drenajes es también recomendable en un hipotético segundo tratamiento quirúrgico en niños, que después de la primera expulsión de los mismos mantienen su patología(12), independientemente de su tamaño, debido al beneficio de eliminar un foco de infección crónica asociada a la generación de biofilms y a la inflamación de vegetaciones que altera la función de la trompa de Eustaquio. De no existir la clínica obstructiva, la derivación o no al especialista se individualizará en función de la época del año (es recomendable la abstención en periodo estival), de la presencia o no de OMEC y/o clínica compatible con hipoacusia de transmisión, y de la posibilidad o no que tenga el pediatra de AP de documentar objetivamente en su consulta la presencia de exudado en oído medio (impendanciometría) y su repercusión funcional (otoemisiones acústicas, audiometría en niños mayores). Se ha comunicado que hay una relación entre OMAR y niveles bajos (<30 ng/ml) de vitamina D y se ha sugerido(13) que la suplementación con 1.000 ui/día de vitamina D durante 4 meses reduce significativamente el número de episodios. Faltan más estudios para hacer una recomendación en este sentido. La posición en decúbito prono para dormir se relaciona con mayor riesgo de OMAR.
Otitis media crónica con exudado
Se define como otitis media crónica con exudado: la presencia de una otitis media con derrame bilateral de más de 3 meses de duración o con derrame unilateral de más de 6 meses de duración.
Si bien el líquido puede ser trasudado o exudado, el niño con OME o con OMEC puede experimentar reagudizaciones (OMA) y el cultivo obtenido por timpanocentesis muestra, en un porcentaje elevado de casos, el crecimiento de los mismos gérmenes causantes de OMA. La OMEC se asocia siempre a hipoacusia de transmisión de variable repercusión funcional y, en algunas ocasiones, a hipoacusia sensorial reversible (por presión y rigidez sobre la membrana de la ventana redonda) o permanente (por diseminación de la infección o los productos de la inflamación a través de la membrana de la ventana redonda, por el desarrollo de una fístula perilinfática en la ventana redonda o por laberintitis supurativa). La otoscopia visual no es lo bastante sensible para detectar muchos casos de OME y, en consecuencia, de OMEC. Son signos otoscópicos sugestivos de OME: la hiperemia asociada a matidez, la coloración amarillenta y la coloración azulada de la membrana timpánica. Esta última está especialmente asociada a OMEC. La visualización de una retracción en la membrana timpánica, en la que los huesecillos de oído medio se verán muy marcados, es muy sospechosa de presión negativa en oído medio (DTE) y se correlaciona con OMEC. Si bien, la otoscopia neumática mejora la sensibilidad de la otoscopia visual, requiere de experiencia para interpretar los resultados y también es una exploración de interpretación subjetiva. En una OMEC observaremos inmovilidad de la membrana timpánica, tanto en la aplicación de presión negativa como en la positiva. Solo la impendaciometría tiene una sensibilidad y especificidad cercanas a la timpanocentesis. Lamentablemente, el pediatra de AP no suele disponer de esta técnica.
Podemos llegar al diagnóstico de OMEC por 3 caminos (Tabla IX):

• Seguimiento de OMA en el que la OME no se resuelve en 3 meses (bilateral) o 6 meses (unilateral).
• OME detectada en un control rutinario de salud, cuyo seguimiento en 3 meses (bilateral) o 6 meses (bilateral) nos lleva al diagnóstico de OMEC (llamada “de novo”).
• OMEC diagnosticada en un niño que consulta por hipoacusia de larga evolución o clínica asociada compatible (retraso del lenguaje, retraso escolar).
El diagnóstico de OMEC, sea de sospecha por otoscopia visual o neumática, o preferentemente por confirmación con técnicas objetivas de detección de exudado de oído medio (impedanciometría), debería comportar una derivación especializada, para valorar la repercusión funcional, puesto que el drenaje transtimpánico asociado o no a adenoidectomía, según la presencia o no de clínica de obstrucción nasal asociada, constituye el tratamiento de elección de la OMEC con hipoacusia de transmisión superior a 30 dB. En la práctica de nuestro medio, las relaciones de colaboración entre ambos niveles y la saturación asistencial de los especialistas de referencia comporta la dificultad de que esta derivación sea productiva, con lo que el pediatra de AP retiene muchos casos en los que la clínica parece ser de menor relevancia o no hay aparente afectación auditiva o alteración en el rendimiento escolar. La valoración objetiva de la repercusión funcional de la OMEC no suele estar disponible para muchos pediatras de AP hasta los 6 años, edad en la que un niño normal colabora en una audiometría convencional. Sin embargo, el impacto de esta patología se produce a edades muy inferiores. La posibilidad de que el pediatra de AP pudiese disponer en su consulta de un detector de otoemisiones acústicas, que permite descartar hipoacusia de transmisión o sensorial significativas, con el nivel de corte de 30 dB, sería un avance muy significativo en el manejo ambulatorio de esta patología(14).
La intervención es bien tolerada y durante el tiempo en que los drenajes permanecen en oído medio (6-18 meses), el niño mejora significativamente su audición y disminuyen las reagudizaciones. Los especialistas no suelen hacer seguimiento de estos niños post-intervención, pero es obligada una valoración auditiva después de la misma. Un pequeño porcentaje presenta otorrea persistente, que presenta buena respuesta al ciprofloxacino tópico. En guías de práctica clínica, se recomienda que la actitud inicial ante una OMEC sea más conservadora y que la derivación para cirugía parece especialmente indicada (Tabla X) en casos de: fisura palatina, retracción o atelectasia de la membrana timpánica, sospecha de colesteatoma, afectación bilateral, sospecha de retraso de lenguaje o del desarrollo psicomotor en general, trastornos del espectro autista o síndromes congénitos asociados a retrasos del desarrollo o del lenguaje(15).

Se han publicado diversos estudios en los que se utiliza tratamiento médico antes de proceder a la cirugía. Se obtuvieron buenos resultados con la utilización de antibióticos durante un mes a dosis terapéuticas, asociados a corticoides orales en la última semana. Sin embargo, los beneficios obtenidos eran a corto plazo y, en cualquier caso, la agresividad de esta pauta comporta la necesidad de individualizar el caso antes de utilizarla muy puntualmente. Sin embargo, un intento terapéutico con una tanda de ATB durante 2 semanas, si no se han utilizado recientemente, parece un intento razonable antes de la cirugía y es utilizado comúnmente por muchos pediatras. En cualquier caso, ante la alta tasa de resolución espontánea de la OME en verano, es práctica común dejar pasar esta estación antes de cualquier abordaje quirúrgico.
Es frecuente la utilización en OMEC de terapias con descongestionantes nasales, mucolíticos o antihistamínicos, solos o en asociación. Ningún estudio controlado ha demostrado beneficio alguno con su uso. Es probable que los antihistamínicos ejerzan algún efecto beneficioso sobre la OME en pacientes con alergia asociada, pero no se han hecho estudios al respecto.
Otorrea en el niño portador de drenajes transtimpánicos (DTT)
Es una frecuente complicación que debe ser tratada con ciprofloxacino tópico.
La otorrea ocurre en un 20-50% de los niños portadores de drenajes. La otorrea aguda debe considerarse como un episodio más de OMA. Al contrario, la ausencia de otorrea en un portador de DTT funcional anula la posibilidad de OMA. Los gérmenes responsables son los mismos que en niños no intervenidos, debiendo considerar asimismo la flora que proviene del conducto auditivo externo (Pseudomona aeruginosa, estafilococo dorado y Proteus mirabilis). Hay un creciente aislamiento de estafilococo resistente a la meticilina, adquirido en la comunidad (MARSA). La utilización de ciprofloxacino tópico es de primera elección, pues se ha mostrado tan eficaz como amoxicilina/clavulánico y superior en erradicación bacteriológica, con pocos efectos secundarios locales y sin inducción de resistencias. En casos recidivantes o persistentes, se ha ensayado con éxito la combinación de ambos tratamientos, tópico y sistémico. Estudios recientes sugieren que la asociación de uso tópico de ciprofloxacino con corticoides es superior al ciprofloxacino solo. El fracaso del tratamiento tópico hace aconsejable la práctica de un cultivo, dado que las quinolonas aumentan levemente el riesgo de sobreinfección fúngica.
Otitis externa
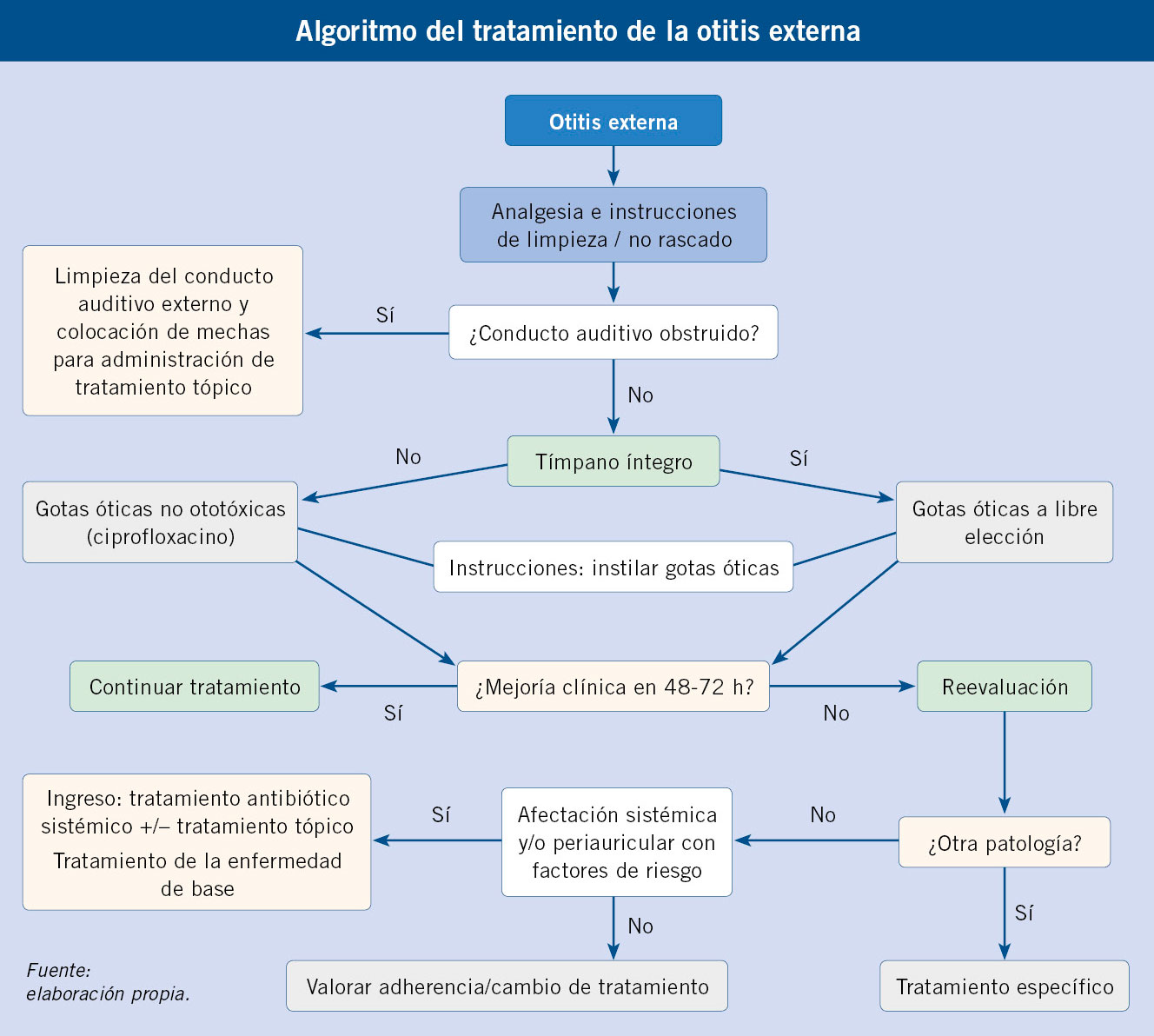
La otitis externa se produce generalmente por exceso de humedad en el conducto auditivo. Las normas higiénicas y un tratamiento antibiótico local serán suficientes en la mayoría de casos.
La otitis externa es la inflamación y/o infección del conducto auditivo externo. En la práctica del pediatra de AP es importante conocer: la otitis aguda externa difusa, la otitis aguda externa circunscrita o forúnculo del conducto auditivo y la miringitis ampollosa o bullosa.
Otitis aguda externa difusa (“otitis de las piscinas”)
La humedad persistente en el conducto auditivo: altera los mecanismos inmunitarios locales, disminuye la actividad antimicrobiana del cerumen, el espesor de la capa de queratina del epitelio, aumenta el pH, macera la piel y aparecen microfisuras. Sin embargo, la sequedad extrema, la ausencia total de cerumen (que actúa contra la humedad) o el tapón de cerumen impactado (que retiene agua) también son factores predisponentes a la otitis externa. La etiología puede ser bacteriana, generalmente por Pseudomona (80%), que sobrecrece en ambiente húmedo, y estafilococo (epidermidis y aureus), pero también por enterobacterias (Proteus mirabilis), difteroides o citrobacter, micótica (cándidas en inmunodeficientes y Aspergillus en diabéticos) o vírica: herpes simple y varicela-zóster (síndrome de Ramsay-Hunt). La otitis externa difusa aparece también como frecuente complicación de la otorrea en portadores de drenaje transtimpánico(16).
Clínica
La clínica se caracteriza fundamentalmente por el dolor, precedido, a veces, de prurito, con los clásicos signos del trago y del pabellón muy positivos. Suele ser unilateral. Habitualmente, hay disociación clínico-otoscópica, puesto que el niño tiene un dolor muy superior a los escasos o nulos signos inflamatorios que pueden visualizarse en fases iniciales. El dolor intenso se debe a la inervación del conducto auditivo externo por 4 pares craneales. Posteriormente, aparecen hiperemia de intensidad variable de la piel del conducto auditivo externo y estrechamiento hasta del 50% de la luz del mismo, con dificultades para visualizar la membrana timpánica. Es frecuente la hipoacusia y no es rara la supuración. La fiebre no es común y, cuando aparece, suele traducir infección mixta estafilococo-Pseudomona. Puede acompañarse de adenopatías preauriculares.
El diagnóstico diferencial con la OMA no siempre es fácil, especialmente cuando hay supuración que impide la visualización de la membrana timpánica. El dolor suele mejorar cuando hay perforación en la OMA y, en cambio, empeora con la otorrea en otitis externa. En caso de duda, el timpanómetro es un aliado imprescindible, al verificarnos si existe o no perforación timpánica con la valoración del volumen de oído externo. Los signos del trago y del pabellón son propios de la otitis externa y no de la OMA. En la OMA suele haber un antecedente catarral y es más frecuente la fiebre. La otitis externa es más propia del verano. Si la otitis externa cursa con edema periauricular, debe diferenciarse de la mastoiditis, en la que suele haber un episodio previo de OMA, hipoacusia, dolor a la presión de la apófisis mastoidea y ausencia de signo del trago. En la otitis externa se conserva el surco postauricular, que puede borrarse en la mastoiditis.
Tratamiento
El tratamiento fundamental es el analgésico, puesto que el dolor es el signo capital. La utilización de paracetamol o ibuprofeno a dosis adecuadas suele ser suficiente. Es útil el calor local. En casos más importantes, se obtiene buena respuesta con la asociación de paracetamol y codeína, que no debe utilizarse en menores de 12 años. Si hay mucho material orgánico y exudado, debe procederse a una limpieza del conducto auditivo con cureta o irrigación, y si no es posible hacerlo en la consulta, el paciente debe ser remitido al especialista ORL. De no hacerse esta limpieza, el ATB tópico no va a contactar con la pared del conducto y el tratamiento va a fracasar. Si el conducto está permeable, hay que administrar ATB local. Clásicamente, se han utilizado preparados que asocian aminoglucósidos (neomicina, polimixina o colistina) con corticoides, a razón de 2 gotas, 4 veces al día durante 7 días. No hay estudios que comparen la ventaja adicional de la utilización de corticoides con respecto al uso solo de ATB. Para el uso de estos preparados clásicos, hay que tener la certeza de que la membrana timpánica no está perforada, lo que puede ser difícil si hay secreción, de no disponer de un timpanómetro, puesto que se ha descrito ototoxicidad en raras ocasiones. Estos preparados llevan propilenglicol y ácido acético, que resultan irritantes y pueden causar eczema de contacto. Por otra parte, se han descrito reacciones de sensibilización a los aminoglucósidos tópicos. El ciprofloxacino ótico es igualmente eficaz y, pese a que su coste es muy superior, parece la opción más recomendable en la actualidad, por su mejor tolerancia, dosificación más cómoda (2 veces al día) y ausencia de efectos secundarios y sensibilización. El niño con la habitual otitis externa leve puede seguir bañándose, siempre que no bucee en el curso del tratamiento.
Pese a su teórica banalidad, la otitis externa no está exenta de potenciales complicaciones, por lo que el pediatra de AP deberá derivar toda otitis externa con fiebre, que requerirá de cultivo de la secreción y probable tratamiento parenteral, y siempre que no se obtenga mejoría con 7 días de tratamiento local.
La prevención de las recidivas es fundamental en el niño practicante de natación. Hay que educarle para que proceda al secado cuidadoso del conducto después del baño, utilizando la punta de la toalla, puesto que la humedad es el principal caldo de cultivo para el sobrecrecimiento de Pseudomona. Es muy útil en casos recidivantes, la instilación de unas gotas de ácido acético (vinagre común de cocina) diluido al 50% en agua, en el conducto auditivo externo al salir de la piscina, dado que la reducción del pH en el conducto auditivo impide la proliferación bacteriana, especialmente de Pseudomona. Se han comercializado recientemente secadores eléctricos para conducto auditivo externo, pero un secador de pelo convencional muestra también su utilidad. La utilidad del uso de tapones es controvertida.
Otitis aguda externa circunscrita (forúnculo del conducto auditivo externo)
Causada por estafilococo dorado, debe recibir tratamiento inicial sistémico con cloxacilina o ATB con actividad antiestafilocócica, asociado a analgesia suficiente. Si el cuadro es grave o no responde al tratamiento en 3 días, deberá derivarse al ORL para proceder a drenaje.
Miringitis
La miringitis es la inflamación de la membrana timpánica. Es frecuente observar hiperemias timpánicas con otalgia en el curso de cuadros víricos de vías altas, sin presencia de exudado de oído medio. Una vez más, el timpanómetro nos ofrecerá el diagnóstico diferencial entre simple miringitis y OMA. Estas formas catarrales no deben recibir tratamiento antibiótico, aunque debe vigilarse su evolución, dado que pueden evolucionar hacia OMA. La visualización de bullas timpánicas (que hay que diferenciar de la presencia de niveles líquidos retrotimpánicos, propios de formas crónicas de otitis media con exudado) asociada a un intenso dolor, es diagnóstica de miringitis bullosa o ampollosa. La miringitis ampollosa es una forma de otitis media con participación de la membrana timpánica, que si bien anteriormente se consideró debida a Mycoplasma pneumoniae, se ha demostrado que es causada más frecuentemente por los gérmenes habituales productores de OMA (neumococo, Haemophilus…). El tratamiento inicial será idéntico al de la OMA. El fracaso terapéutico deberá hacer considerar la posibilidad de instaurar un macrólido con actividad frente Mycoplasma. La miringitis por Mycoplasma raramente cursa sin afectación concomitante del tracto respiratorio inferior (traqueobronquitis, neumonía).
Otitis externa necrotizante (“otitis externa maligna”)
Es la infección del cartílago y el hueso del conducto auditivo externo. Es una rara entidad que debe ser conocida por el pediatra de AP dado su carácter potencialmente grave. Afecta a lactantes, diabéticos e inmunodeprimidos. Es causada habitualmente por Pseudomona y se caracteriza por: fiebre, mal estado general, toxicidad, necrosis del conducto auditivo, extensión a oído medio e interno, parálisis facial y afectación del SNC. Puede diagnosticarse en fase inicial, con la visualización de tejido de granulación en la zona de transición cartílago-hueso del conducto auditivo externo. Ante su sospecha, el niño debe derivarse urgentemente al hospital para tratamiento quirúrgico. Sin tratamiento, la mortalidad se eleva hasta el 80%.
Conflicto de intereses
No hay conflicto de interés en la elaboración del manuscrito. Declaración de intereses: ninguno.
Bibliografía
Los asteriscos reflejan el interés del artículo a juicio del autor.
1.** Pichichero ME. Otitis media. Pediatr Clin N Am. 2013; 60: 391-407.
2.* Kaur R, Casey JR, Pichichero ME. Relationship with original pathogen in recurrence of acute otitis media after completion of amoxicillin/clavulanate. Pediatr Infect Dis J. 2013; 32: 1159-62.
3.* Pichichero ME. Ten-year study of acute otitis media in Rochester, NY. Pediatr Infect Dis J. 2016; 35: 1027-32.
4.*** Pumarola F, Mar ès J, Losada I, Minguella I, Moraga F, Tarragó D, Ulla G, et al. Microbiology of bacteria causing recurrent acute otitis media (AOM) and AOM treatment failure in young children in Spain: Shifting pathogens in the post-pneumococcal conjugate vaccination era. International Journal of Pediatric Otorhinolaryngology. 2013; 77: 1231-6.
5.* Nokso-Koivisto J, Marom T, Chonmaitree T. Importance of viruses in acute otitis media. Curr Opin pediatr. 2015; 27: 110-5.
6.** Chonmaitree T, Ruohola A, Hendley JO. Presence of viral nucleic acids in the middle ear. Acute otitis media pathogen or bystander? Pediatr Infect Dis J. 2012; 31: 325-30.
7.* De la Flor J, Parellada N. Correlació d’otoscòpia visual, otoscòpia pneumàtica i timpanometria en la detecció de disfunció de trompa d’Eustaqui i d’exudat d’oida mitjana. Pediatr Catalana. 2003; 63: 62-8.
8.** Anthonsen K, Hostmark K, Hansen S, Andreasen K, Juhlin J, Homoe P, et al. Acute mastoiditis in children: a 10 year retrospective and validated multicenter study. Pediatr Infect Dis J. 2013; 32: 436-40.
9.*** Leiberthal AS, Carroll AE, Chonmaitree T. Clinical practice guideline: the diagnoses and management of acute otitis media. Pediatrics. 2013; 131: e964-9.
10.* Pichichero ME, Casey JR, Almudevar A. Nonprotective responses to pediatric vaccines occur in children who are otitis-prone. Pediatr Infect Dis J. 2103; 32: 1163-8.
11.* Folino F, Fattizzo M, Roggiero L, Oriano M, Aliberti S, Blasi F, et al. Nasopharyngeal microbiota analysis in healthy and otitis-prone children. Pediatric Infect Dis J. 2021; 40: 16-21.
12.* Kujala T, Alho OP, Luotonen J, Kristo A, Uhari M, Renko M, et al. Tympanostomy with and without adenoidectomy for the prevention of recurrences of acute otitis media. Pediatr Infect Dis J. 2012; 31: 565-9.
13.* Marchisio P, Consonni D, Baggi E, Zampiero A, Bianchini S, Terranova L, et al. Vitamin D supplementation reduces the risk of acute otitis media in otitis-prone children. Pediatr Infect Dis J. 2013; 32: 1055-60.
14.* Balatsouras DG, Kokoutsis G, Ganellis P. Transiently evoked otoacoustic emissions in children with otitis media with effusion. Int J Otolaryngol. 2012; 2012: 269203.
15.** Rosenfeld RM, Schwartz SR, Pynnonen MA. Clinical practice guideline: tympanostomy tubes in children. Otolaryngol Head Neck Surgery. 2013; 149: S1-S35.
16.** Rosenfeld RM, Schwartz SR, Cannon CR. Clinical practice guideline: acute otitis externa. Otolaryngol Head Neck Surg. 2014; 150: S1-S24.
Bibliografía recomendada
– American Academy of pediatrics. Swimmer’s ear/acute otitis externa. En: Kimberlin DW, Brady MT, Jackson MA, Long SS. Red Book: 2015 Report on the Committee on infectious diseases. 30th ed. Elk Grove Village IL: American Academy of Pediatrics; 2015. p. 218.
– Arnold DH, Spiro DM. Otitis media with effusion. En: Bajaj L, Hambidge SJ, Kerby G, Nyquist AC. Berman’s pediatric decision making. 5ª ed. Elsevier. Philadelphia; 2011. p. 128-31.
Guía actualizada en un texto de algoritmos pediátricos.
– Boyce TG, Balakrishnan K. Otitis externa and necrotizing otitis externa. En: Long SS, Prober CHG, Fischer M. Principles and practice of pediatric infectious diseases. 5ª ed. Elsevier. Phidalephia; 2017. p. 223-5.
– Casey JR, Bluestone CHD. Otitis media. En: Cherry JD, Harrison JG, Kaplan SL, Steinback WJ, Hotez PJ. Textbook of pediatric infectious diseases. Saunders Elsevier. 8ª ed. Philadelphia; 2018. p. 149-69.
– Friedman EM, Carrillo M. Otitis externa. En: Cherry JD, Harrison JG, Kaplan SL, Steinback WJ, Hotez PJ. Textbook of pediatric infectious diseases. Saunders Elsevier. 8ª ed. Philadelphia; 2018. p. 144-9.
– Haddad J, Dodhia SN. External otitis (otitis externa). En: Kliegman RM, St. Geme III JW. Nelson textbook of pediatrics. 21ª ed. Elsevier. Philadelphia; 2020. p. 3414-7.
– Hullegie S, Venekamp R, van Dongen T, Hay AD, Moore MV, Little P, et al. Prevalence and antimicrobial resistance of bacteria in children with acute otitis media and ear discharge. Pediatr Infect Dis J. 2021; 40: 756-62.
– Kerschner JE, Preciado D. Otitis media. En: Kliegman RM, St. Geme III JW. Nelson textbook of pediatrics. 21ª ed. Elsevier. Philadelphia; 2020. p. 3418-31.
Completa y actualizada revisión en el libro de texto de Pediatría general más consultado en el mundo. 15 páginas de obligada lectura para el pediatra de AP.
– Pelton SI. Otitis media. En: Long SS, Prober CG, Fischer M. Principles and practice of pediatric infectious diseases. 5ª ed. Philadelphia: Elsevier; 2017. p. 216-23.
Lo fundamental en otitis media, condensado en 7 imprescindibles páginas de un tratado de enfermedades infecciosas pediátricas. Ideal para pediatras de AP con poco tiempo para la lectura.
– Pichichero ME. Ten-year study of the stringently defined otitis-prone child in Rochester, NY. Pediatr Infect Dis J. 2016; 35: 1033-9.
– Spiro DM, Arnold DH. Acute otitis media. En: Bajaj L, Hambidge SJ, Kerby G, Nyquist AC. Berman’s pediatric decision making. 5ª ed. Elsevier. Philadelphia; 2011. p. 124-7.
Guía en un texto de algoritmos pediátricos.
– Schwartz SR, Coggins R, Gagnon L, Hackell JM, Hoelting D, Hunter LL, et al. Clinical Practice Guideline: Otitis Media with Effusion Executive Summary (Update). Otolaryngology–Head and Neck Surgery. 2016; 154: 201-14.
– Wald ER, De Muri, GP. Antibiotic recommendations for acute otitis media and acute bacterial sinusitis. Conundrum no more. Pediatr Infect Dis J. 2018; 37: 1255-7.
– Pichichero ME. Otitis media. Pediatr Clin N Am. 2013; 60: 391-407.
Revisión sucinta de los conceptos más importantes de la enfermedad.
– Chonmaitree T, Ruohola A, Hendley JO. Presence of viral nucleic acids in the middle ear. Acute otitis media pathogen or bystander? Pediatr Infect Dis J. 2012; 31: 325-30.
Interesante artículo de controversia sobre el papel real de los virus en la etiología de la OMA.
– De la Flor J, Parellada N. Correlació d’otoscòpia visual, otoscòpia pneumàtica i timpanometria en la detecció de disfunció de trompa d’Eustaqui i d’exudat d’oida mitjana. Pediatr Catalana. 2003; 63: 62-8.
Trabajo realizado en el ámbito de la AP con una muestra amplia de pacientes, en el que se demuestra la necesidad de objetivar al máximo la detección de exudado de oído medio.
– Kujala T, Alho OP, Luotonen J, Kristo A, Uhari M, Renko M, et al. Tympanostomy with and without adenoidectomy for the prevention of recurrences of acute otitis media. Pediatr Infect Dis J. 2012; 31: 565-9.
Excelente trabajo en el que se demuestra que el primer abordaje quirúrgico del niño con OMEC/OMAR debe basarse solo en el drenaje transtimpánico, salvo si hay una clínica obstructiva nasal relevante.
| Caso clínico 1 |
|
Un niño de 3 años, sin antecedentes valorables, acude a la consulta con un cuadro clínico de otalgia derecha de pocas horas de evolución, en el curso de un proceso catarral que se inició hace 5 días. La madre le ha administrado una dosis de paracetamol, que ha eliminado el dolor. A la exploración física, observamos un niño afebril, con buen estado general, faringe hiperémica, moco claro en cavum y rinorrea acuosa. El signo del trago es negativo. La otoscopia neumática nos muestra una intensa hiperemia de la membrana timpánica izquierda, sin presencia de abombamiento ni de exudado en conducto auditivo externo. La movilidad de ambas membranas a la presión positiva y negativa está abolida. La timpanometría muestra una curva izquierda totalmente plana.
|
|
| Caso clínico 2 |
|
Acude a la consulta un niño de 5 años sin antecedentes de interés, con un cuadro clínico de fiebre de 3 días de duración, acompañado de un cuadro catarral de larga evolución y otalgia intensa. El examen físico muestra una faringe congestiva, moco espeso en cavum, rinitis, otoscopia con marcada hiperemia y coloración amarillenta de la membrana timpánica. Con el diagnóstico de OMA se inicia tratamiento con amoxicilina a dosis de 80 mg/kg/día. Al tercer día, el niño acude de nuevo al no experimentar ninguna mejoría, pese a un cumplimiento y aceptación de la vía oral adecuados y se prescribe un antibiótico de 2ª línea. 48 horas después el niño permanece febril y sigue con otalgia.
|
|
| Caso clínico 3 |
|
Se trata de un niño de 2 años y medio, asistente a guardería. Es un paciente habitual de nuestra consulta, con frecuentes procesos catarrales y antecedentes de 7 episodios de OMA bien documentados en un periodo de 11 meses. Su último proceso agudo fue hace 3 meses. Al coincidir con el periodo estival, se decidió una conducta expectante. El niño ha recibido diversas tandas de tratamiento antibiótico en los últimos meses, frecuentemente en fines de semana en servicios de urgencia. El motivo de consulta actual es que la madre está preocupada por el lenguaje del niño. No es capaz de juntar dos palabras y su vocabulario es muy restringido. En las revisiones de los 18 meses y de los 2 años, el cuestionario de detección precoz del autismo M-CHAT fue normal. Se adjunta un informe escolar en el que se describe una conducta poco participativa. El examen físico no muestra hallazgos significativos, salvo la presencia de una otoscopia con tímpanos de coloración azulada, ligera retracción timpánica, otoscopia neumática con inmovilidad total de ambas membranas timpánicas y timpanograma completamente plano. Estos mismos hallazgos se documentan varias veces en la historia desde el último episodio de OMA.
|
|