Novedades en probióticos: evidencias, indicaciones y seguridad
Psicobióticos
Probióticos específicos que podrían mejorar algunos trastornos psiquiátricos, tales como: depresión, ansiedad, síndrome de intestino irritable y otros.
Término introducido en 2013 por Ted Dinan, catedrático de Psiquiatría de la Universidad de Cork (Irlanda). Inicialmente, lo define como: aquellos organismos vivos que, cuando se consumen en cantidades adecuadas, producen un beneficio en la salud de pacientes con trastornos psiquiátricos(2). Recientemente, se amplía su definición a aquellos probióticos, prebióticos y otras estrategias que, al actuar sobre el eje microbiota-intestino-cerebro, pueden conferir beneficios para la salud mental. Se incluye así a los prebióticos, pero también el ejercicio físico y la dieta, que afectan a las comunidades bacterianas en el intestino e influyen en el estado de ánimo y en la cognición(3).
El principal problema de esta nueva versión es que se apoya, principalmente, en estudios realizados in vitro y en animales, por lo que los científicos muestran cautela a la hora de valorar cualquier resultado que pueda parecer prometedor. La comunidad científica reconoce el término de psicobiótico, pero lo limita a aquellos probióticos con posibles efectos positivos en personas con patologías psiquiátricas. La depresión, la ansiedad y el síndrome del espectro autista son las tres enfermedades que, a priori, se podrían beneficiar más de los avances en este nuevo campo de estudio. También se ha estudiado en el síndrome del intestino irritable, donde se han reportado beneficios positivos para varios organismos, incluido Bifidobacterium infantis, y en el síndrome de fatiga crónica.
Se ha demostrado que algunas bacterias intestinales de los géneros Lactobacillus y Bifidobacterium segregan o modulan sustancias neurotransmisoras como GABA, acetilcolina o serotonina, implicadas en la regulación de muchos procesos fisiológicos y neurológicos, cuya disfunción se relaciona con la ansiedad o la depresión.
Posibles mecanismos de acción
Se barajan varias posibilidades:
• Que los microorganismos actúen directamente sobre el sistema nervioso entérico, encargado de controlar el aparato digestivo mediante la producción de neurotransmisores (serotonina, ácido gamma-amino-butírico), que a su vez se comunica con el SNC.
• Que regulen el sistema inmunitario intestinal, el cual produce citoquinas que modulan SNC.
• Que produzcan metabolitos que alteren la actividad de la barrera hemato-encefálica en el cerebro.
Los microorganismos podrían utilizar una o varias de estas vías y, a la vez, para producir efectos beneficiosos en la salud mental. Hay diversos trabajos que apoyan este tipo de acciones.
En un estudio en ratas modificadas con depresión, se observó que podía revertirse la patología administrando Bifidobacterium infantis. Los resultados muestran que se incrementan los niveles de triptófano en plasma y de metabolitos como la dopamina en la cortical, y se reducen las concentraciones de serotonina en la corteza frontal, disminuyendo los síntomas de la depresión(4).
En otro estudio, se analizaron las heces de 55 individuos, tanto con depresión como sin ella, encontrando un incremento de bacterias fecales en los pacientes con depresión(5).
En un artículo de revisión de 2015, sobre el potencial de los psicobióticos en la salud mental, se analizaron los únicos 10 estudios que cumplían los siguientes requisitos: realizarse en humanos, con sistema de doble ciego, asignación aleatoria y donde se comparasen los efectos de psicobióticos y placebos. No se encontraron pruebas concluyentes de los efectos psicológicos de los probióticos.
En 2016, un nuevo estudio examinó el impacto de ciertos probióticos en personas con depresión. Se proporcionó placebo o bacterias a dos grupos de 20 pacientes durante 8 semanas. Quienes consumieron las bacterias mejoraron su grado de depresión, según el inventario de depresión de Beck (BDI). Los resultados demuestran efectos beneficiosos significativos relacionados con la mejoría metabólica en cuanto al mantenimiento inalterado de los niveles de glucosa, disminución de la resistencia a insulina, disminución de los marcadores oxidativos, con incremento del glutatión total en plasma. Sin embargo, los probióticos que usan no están bien caracterizados: indican la especie (Lactobacillus acidophilus, Lactobacillus casei y Bifidobacterium bifidum), pero no la cepa(6).
Otra investigación realizada con la bacteria Bifidobacterium longum 1714, arrojó resultados prometedores. Durante 4 semanas, 22 varones tomaron placebo. A continuación, ingirieron el probiótico durante otras 4 semanas. Se analizó su respuesta al estrés, así como su actividad cerebral y cognitiva, con diferentes cuestionarios y electroencefalografías. El consumo de la bacteria se asoció a una disminución del estrés y a una mejora de la memoria(7).
En un estudio reciente, a 81 pacientes (36,5 ± 8,03 años) diagnosticados de depresión mayor y divididos en tres grupos similares, se les administra durante 8 semanas una mezcla de probióticos (Lactobacillus helveticus y Bifidobacterium longum), un prebiótico (galactooligosacárido) y un placebo, respectivamente. Se evaluaron los cambios en pacientes con trastorno depresivo mayor (TDM) mediante BDI, como resultado primario, así como las relaciones quinurenina/triptófano y triptófano/aminoácidos de cadena ramificada, como resultados secundarios. Se concluye que 8 semanas de suplementos probióticos a estos pacientes mejoró el BDI en comparación con el grupo placebo, así como los parámetros neuroquímicos mencionados, y no se observó ningún efecto significativo en el grupo al que se le administró prebióticos(8).
Paraprobióticos
Probióticos muertos o fantasmas con similares acciones y efectos que los probióticos vivos. Constituyen una nueva esperanza para ser utilizados en pacientes más vulnerables sin riesgos.
El término paraprobiótico (probióticos fantasma) se ha propuesto para definir células microbianas no viables (intactas o rotas) o extractos de células no fragmentados con composición química compleja que, cuando se administran (por vía oral o tópica) en cantidades adecuadas, confieren un beneficio para el consumidor humano o animal.
La inactivación de probióticos se puede conseguir por varios métodos, incluido el uso de: calor, productos químicos (p. ej., formalina), rayos gamma o ultravioleta, y sonicación (sonoporación, inactivación de material biológico por ultrasonidos). Los diferentes métodos de inactivación pueden afectar los componentes estructurales de la célula de manera diferente e influir en su actividad inmunomoduladora. El tratamiento térmico parece ser el método de elección para la inactivación de cepas probióticas en la mayoría de los estudios(9,10).
En cuanto a los mecanismos de acción de los probióticos inactivados por calor o muertos, aun siendo poco conocidos, son similares a la de los probióticos vivos, pero con algunas particularidades. Como posibles inconvenientes señalar:
• Capacidad reducida para la adhesión a la mucosa, que incluye las propiedades adhesivas de BoPA, una lipoproteína de la superficie celular identificada en Bifidobacterium (B.) bifidum. Sin embargo, se ha demostrado que para la cepa Propionibacterium freundereichii se obtiene una mayor capacidad de adhesión después de la inactivación por calor(11). En estudios preclínicos con lactobacilos viables y muertos, la alteración de la adhesividad a la mucosa producida por el calor ha hecho que se distribuyan de diferente forma, observándose las bacterias vivas en las placas de Peyer y en la lámina propia, mientras que las destruidas por el calor estaban en la luz y eran eliminadas rápidamente, pero mantenían la capacidad de inhibición del patógeno a la mucosa por exclusión competitiva, mejorando la barrera intestinal(12).
• Menor capacidad para ejercer efecto antiinflamatorio, sin embargo en las cepas inactivadas por calor Lactobacillus (L.) casei, Shirota o L. fermentum se ha demostrado eficacia para modular la respuesta inflamatoria al regular: la IL-10 (una anti-citocina inflamatoria), la B-defensina humana y otras citocinas proinflamatorias; también para Bifidobacterium (B.) breve y B. bifidum aumenta la capacidad de secreción de IL-10.
• Los extractos de la pared celular, el ácido lipoteicoico, el ADN bacteriano y las proteínas de la capa de superficie (S) pueden tener efectos inmunomoduladores por varios mecanismos, incluidos aumento de la producción de IgA salival, modulación de las respuestas de células T del huésped y expresión génica. Los probióticos vivos e inactivados tuvieron efectos comparables sobre la inmunidad innata. En cuanto a la respuesta fagocítica de B. lactis HN019 vivo y muerto en células de sangre periférica, solo las bacterias viables aumentaron la actividad fagocítica de las células peritoneales(13). En cuanto a la inmunidad adaptativa, la mayoría de estudios observan más beneficios con el uso de probióticos viables(14), pero algunos muestran que ambas formas tienen efectos similares sobre el fenotipo y las funciones de las células dendríticas mieloides humanas(15).
Resumiendo, la evidencia de los estudios preclínicos y clínicos sugiere que en algunas situaciones, dependiendo del mecanismo de acción, los efectos probióticos no dependen de la viabilidad celular.
Como posibles, ventajas cabe señalar que los paraprobióticos mejoran la seguridad y su vida útil es más larga. Los probióticos muertos tuvieron varias respuestas biológicas, incluidas: los efectos antiinflamatorios, la atenuación de la colitis, la reducción de la producción de IL-8, la estimulación del sistema inmunitario intestinal y la estimulación de la producción de IL-6, en estudios preclínicos. Por lo tanto, los microbios muertos podrían modular los efectos antiinflamatorios tan efectivamente como los probióticos vivos(16).
En una revisión sistemática de ensayos de bacterias, en las que se compararon microbios modificados (paraprobióticos) con placebo, o con la misma cepa probiótica, o con terapia estándar, para la prevención o tratamiento de diversas enfermedades, no se aprecia diferencia significativa entre los probióticos y los microbios modificados en el 86% de los ensayos de prevención y en el 69% de los tratamientos. La incidencia de eventos adversos fue comparable para microbios modificados, probióticos y otros controles. En general, hubo alguna evidencia de que los microbios modificados pueden ser útiles para algunas condiciones, por ejemplo, el L. acidophilus modificado como adyuvante en el tratamiento de la diarrea aguda. Sin embargo, esta revisión incluye limitaciones, tales como: la heterogeneidad de la metodología y las cepas evaluadas, y sus pequeños tamaños de muestra(10).
Otra publicación reciente realiza una revisión sistemática de los efectos, tanto de los probióticos como de los paraprobióticos, como posibles candidatos en la prevención y tratamiento de diversas enfermedades virales, dado la interacción de los mismos con el sistema inmunitario de la mucosa, produciendo inmunomodulación, tanto innata como adquirida, así como el papel en la producción de IFN tipo 1 (interferones tipo 1) implicado en los procesos de eliminación viral y en la regulación de las citocinas inflamatorias, que está mediada por receptores de reconocimiento de patrones, como los receptores tipo Toll y el gen I-inducible por ácido retinoico. Los estudios han comenzado a dilucidar los efectos inmunoestimuladores de las bacterias del ácido láctico y han informado de su capacidad para contribuir a la prevención de infecciones virales, incluida la gripe, así como en el tratamiento de la infección por Helicobacter pylori (17).
En este mismo artículo, se demuestra como L. lactis JCM 5805, utilizando células dendríticas derivadas de la médula ósea murina obtenida de varios tipos de modelos experimentales de ratones, es el estimulador más potente de la producción de IFN tipo 1 (IFN-α), que juega un papel importante en la mediación de la respuesta inmune antiviral al inducir la actividad citotóxica de las células asesinas naturales, lo que contribuye a la defensa del huésped contra la infección viral. Llegan a la conclusión de que, aun siendo necesaria una investigación más detallada, se espera que los probióticos y/o paraprobióticos se encuentren entre las opciones coadyuvantes racionales para el tratamiento y la profilaxis de las infecciones virales(17).
Hay varios estudios que demuestran el efecto de los paraprobióticos en la reducción de grasa corporal total, el IMC, otros parámetros antropométricos como modificaciones y regulación del metabolismo lipídico, de la glucosa y del síndrome metabólico. En un estudio hecho en Japón con voluntarios sanos, que incluía sujetos con sobrepeso y obesidad con un índice de masa corporal (IMC) con un rango de 25 o más, pero menos de 30 kg/m2, a los que se dividió en dos grupos de 98 y 99 pacientes (grupo prueba y control, respectivamente), se les administró dosis de 200 mg en forma de leche de Lactobacillus amylovorus CP1563 fragmentado, obtenido de muestras fecales, cultivado, lavado e inactivado por calor y liofilizado al grupo prueba, y similar preparado placebo al grupo control. Se realizaron registros de todas las ingestas y actividad física durante 16 semanas, y medidas antropométricas y de demás parámetros analíticos a las 4-8-12 semanas, momento en el que se terminó con la dosis de paraprobióticos, y a las 16 semanas. Aunque se necesitan más ensayos clínicos e investigaciones sobre los mecanismos de acción, los resultados de este estudio sugieren que el consumo de alimentos que contienen CP1563 fragmentado durante 12 semanas por sujetos obesos de clase I mejora: las mediciones antropométricas, los marcadores relacionados con el metabolismo de los lípidos y de la glucosa, sin ningún efecto adverso, previene el síndrome metabólico y las complicaciones.
El mecanismo de acción de estos fragmentos de Lactobacillus amylovorus CP1563 (CP1563) es el mismo que realizan los agonistas en el receptor activado por proliferador de peroxisoma (PPAR) α y γ. Algunos fármacos agonistas del PPARα (fibratos) reducen la concentración de triglicéridos y aumentan la concentración sérica de colesterol HDL. El PPARγ se expresa altamente en adipocitos y regula la diferenciación de los mismos, el almacenamiento de lípidos y el metabolismo de la glucosa. Los agonistas farmacológicos del PPARγ (glitazonas) mejoran la resistencia a la insulina y se usan ampliamente en el tratamiento de la dislipemia. Los agonistas farmacológicos (glitazars) de doble PPAR (PPARα/γ) ejercen efectos positivos sobre el metabolismo de los lípidos y la glucosa, y se han desarrollado recientemente como agentes prometedores para el tratamiento de la diabetes mellitus tipo 2 con dislipemia. La activación PPARα del CP1563 fragmentado también fue significativamente mayor que la de las células intactas y se correlacionó inversamente con el tamaño de la trituración, es decir, la longitud de los fragmentos(18).
Otro estudio utilizó la cepa de B. animalis subsp lactis inactivada por calor, en ratas Wistar de 6 semanas de vida durante 12 semanas, que siguieron dos tipos de dietas, la estándar y la dieta de cafetería (hipercalórica, rica en grasa que induce la aparición de síndrome metabólico). No se observaron cambios en el peso, pero las ratas que toman la B. animalis inactiva: disminuye la adiposidad y aumenta la sensibilidad a la insulina y mejora la dislipemia(19).
Postbióticos
Sustancias simples o complejas, producto de los probióticos con efectos similares a los mismos y sin los riesgos de estos en el caso de uso en pacientes comprometidos.
Se definen como sustancias solubles generadas del metabolismo de los probióticos y liberadas al medio extracelular, con actividad beneficiosa sobre la salud(20).
Este concepto hace referencia no solo a moléculas más simples producidas por los probióticos al interaccionar con las células intestinales, como factores solubles o secretados (denominados genéricamente metabolitos bacterianos bioactivos), sino también a moléculas más complejas y sobrenadante libre de células. Entre los metabolitos bacterianos bioactivos se encuentran: ácidos orgánicos (acetato, acetil acético, butirato y propionato); aminoácidos como: triptófano, taurina, histamina; otras proteínas y polisacáridos extracelulares como: espermina y bacteriocinas; y en las más complejas, componentes como: fracciones microbianas, proteínas funcionales, polisacáridos secretados, lisados celulares, ácido teicoico, muropéptidos derivados del peptidoglucano, estructuras de tipo pili y fragmentos celulares. Por ello, en algunas publicaciones, se incluyen los paraprobióticos, comentados previamente, como un tipo más de postbióticos(21,22).
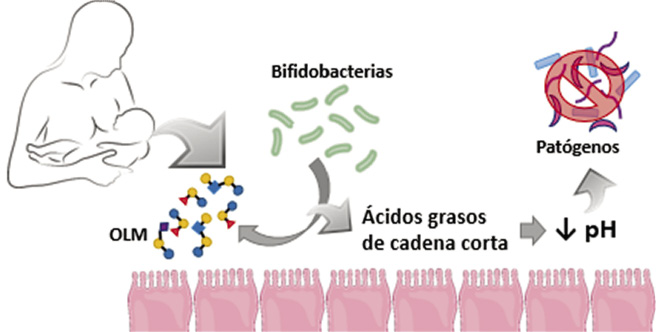
En cuanto a los mecanismos de acción, los postbióticos tienen el mismo que los probióticos e igual capacidad, debido a la presencia de metabolitos secundarios sin una célula viva. Pueden reducir el pH intestinal e inhibir la proliferación de patógenos oportunistas en la alimentación y en el intestino de los animales. Los postbióticos obtenidos de Lactobacillus plantarum exhiben acción inhibitoria sobre diversas bacterias patógenas, incluidas: Listeria monocytogenes, Salmonella Typhimurium, Escherichia coli y Enterococos resistentes a la vancomicina(23).
En pollos de engorde en condiciones normales, la suplementación postbiótica mejora el rendimiento del crecimiento y la salud, al promover el estado inmune y el buen estado intestinal a través de la mejora de las vellosidades intestinales y el aumento de la población de bacterias de ácido láctico, y la reducción de la población de Enterobacteriaceae y el pH fecal(24).
Tsilingiri, et al. propusieron la utilización de postbióticos en el tratamiento y prevención de enfermedades intestinales, como la enfermedad inflamatoria intestinal(20). Los sobrenadantes de cultivo de Lactobacillus casei y Lactobacillus paracasei, cepas aisladas de la leche materna humana que tienen bioactividad de citotoxicidad y apoptosis contra las células del cáncer cervical, tienen el potencial de ser fármacos antitumorales naturales(25).
El uso de moléculas postbióticas se ha convertido en una estrategia prometedora para tratar muchas enfermedades inflamatorias, ya que estas moléculas imitan los efectos terapéuticos útiles de los probióticos y evitan el riesgo de administrar microorganismos vivos a un huésped con un sistema inmunitario deteriorado. Ha resultado ser así en varios estudios que utilizan modelos de ratón de enfermedades inflamatorias, como: colitis, artritis, asma, gota y neumonía. Los resultados enfatizan las complejas interacciones entre el huésped y los metabolitos modulados por microbiota, lo que constituye un área interesante de investigación futura(26).
Los mecanismos moleculares subyacentes a los efectos de los postbióticos parecen estar mediados por una interacción entre el huésped y los productos microbianos. Estos, al interaccionar con el sistema inmunitario del huésped, pueden desencadenar una respuesta antiinflamatoria. Aunque dichos mecanismos no son bien conocidos, una posible acción de inmunomodulación por postbióticos en humanos, podría derivarse de un experimento in vitro que muestra la respuesta innata de los macrófagos a Lactobacillus casei no viable. Se observó un aumento en la expresión de citocinas proinflamatorias y una mejora de la transcripción de receptores tipo Toll (TLR-2, TLR-3, TLR-4 y TLR-9) y se presume que los compuestos postbióticos de Lactobacillus spp pueden ejercer actividad de inmunomodulación aumentando los niveles de citocinas asociadas a Th1 (respuesta tolerogénica), reduciendo las citocinas asociadas a Th2 (respuesta proinflamatoria).
Los experimentos con ratones con fórmula infantil fermentada que contiene postbióticos derivados de Bifidobacterium breve C50 y Streptococcus thermophilus 065 han demostrado una supervivencia y maduración prolongadas de las células dendríticas, e indujeron una alta producción de IL-10 a través de TLR-2, lo que sugiere funciones de regulación inmunitaria. Además, se ha demostrado que los postbióticos de estas cepas mejoran la función de barrera epitelial y estimulan la respuesta Th1 en modelos de ratón, destacando la participación de componentes postbióticos en la función inmune del huésped.
Los postbióticos, a diferencia de los probióticos, no necesitan, para mantener su eficiencia, de la necesaria colonización, para la cual es preciso mantener los microorganismos viables y estables en el producto a una dosis alta. Esto facilita la entrega de los ingredientes activos en la ubicación deseada en el intestino, mejora la vida útil y puede simplificar el embalaje y el transporte. Los postbióticos también se pueden usar en situaciones en las que es más difícil controlar y mantener las condiciones de producción y almacenamiento, como en los países en desarrollo. Además, se ha sugerido que el uso de postbióticos podría ser una alternativa atractiva para otros “bióticos” en pacientes críticos, niños pequeños y recién nacidos prematuros(21).
Los avances recientes en la comprensión de los efectos biológicos de los postbióticos y los mecanismos relacionados, algunos de ellos comentados aquí, indican que pueden ser una estrategia preventiva eficaz prometedora contra la enterocolitis necrotizante, al tiempo que evitan el riesgo de administrar microorganismos vivos a los recién nacidos prematuros, que podrían translocarse y causar infección. Sin embargo, se necesitan más datos de ensayos que investiguen la eficacia, y se deben abordar los problemas relacionados con su régimen óptimo, y el inicio y duración del tratamiento(27).
Principales indicaciones de probióticos en Pediatría
En el tratamiento de la gastroenteritis aguda en niños, coadyuvante de la erradicación del Helicobacter pylori. En la prevención de: la diarrea aguda e infecciones comunes de guarderías, la diarrea asociada a antibióticos, la diarrea nosocomial, la enterocolitis necrotizante y las enfermedades alérgicas. Y en el tratamiento y prevención de: el cólico del lactante, los trastornos funcionales gastrointestinales ligados al dolor abdominal y la enfermedad inflamatoria intestinal. También se valoran las precauciones y posibles efectos secundarios del uso de probióticos, sobre todo, en pacientes comprometidos.
A pesar del uso cada vez más extendido de los probióticos, los estudios publicados hasta la fecha tienen gran diversidad en su diseño y muestran, en muchas ocasiones, resultados no concluyentes, originando una importante dificultad para el desarrollo de guías definitivas de tratamiento que faciliten un uso racional de los mismos.
En esta revisión, se repasan las últimas recomendaciones y pautas del uso de probióticos en la prevención y tratamiento de diferentes patologías, principalmente intestinales, y solo de niños, basadas en los diferentes documentos de consenso de los paneles de expertos de distintas sociedades científicas expuestos en los dos últimos años. Se hace referencia también a los cambios efectuados con respecto a las guías previas y se analizan las precauciones y posibles efectos secundarios de dichos probióticos, sobre todo, al ser utilizados en pacientes con cierto compromiso orgánico.
Todos los probióticos han de cumplir una serie de características fundamentales:
• Ausencia de virulencia bajo cualquier circunstancia, lo que les ha permitido ser catalogados como organismos: Generally Regarded As Safe (GRAS) por la Food and Drug Administration de EE.UU. y Qualified Presumption of Safety (QPS) por la European Food Safety Authority.
• Ser capaces de atravesar los tramos altos del tubo digestivo manteniendo su supervivencia, tener capacidad de adherencia y de colonización del epitelio intestinal para seguir los efectos sobre la salud deseados: de tipo inmunomodulador, efectos sobre la barrera intestinal y capacidad de influir en algún proceso metabólico.
• Verificación mediante ensayos clínicos de las expectativas derivadas de que sus propiedades demostradas in vitro se cumplen tras su administración en humanos.
Se debe tener en cuenta que los efectos clínicos de los probióticos se consideran cepa-específicos y dosis dependientes, a valorar a la hora de interpretar la evidencia científica y realizar sus indicaciones en la práctica clínica. Las recomendaciones de las sociedades científicas se basan en meta-análisis y revisiones sistemáticas publicadas sobre los beneficios encontrados en el empleo de cepas específicas a dosis determinadas, en patologías concretas(1,28).
En las diferentes guías, se hace referencia a niveles de evidencia según el Centro Oxford para Medicina Basada en la Evidencia:
1. Revisión sistemática de ensayos aleatorizados o ensayos de n=1.
2. Ensayo aleatorizado o estudio observacional con efecto dramático (significativo).
3. Estudio de cohorte controlado no aleatorizado/de seguimiento*.
4. Serie de casos, estudios de control de casos, o estudios controlados históricamente*.
5. Razonamiento basado en un mecanismo.
*Una revisión sistemática suele ser mejor que un estudio individual(29).
En el tratamiento de la gastroenteritis aguda en niños
Ya se recoge en la Guía Práctica de la Organización Mundial de Gastroenterología: probióticos y prebióticos (WGO Practice Guideline: Probiotics and Prebiotics) del 2011. El Lactobacillus rhamnosus GG, a dosis de 1010–1011 UFC, dos veces por día durante 5-7 días muestra evidencia 1 a, refrendado por 1 metaanálisis de ECAs, recomendación ESPGHAN/ESPID; y el Saccharomyces boulardii, cepa de S. cerevisiae CNCM I-745, a dosis de 250-750 mg/día, durante 5-7 días, con igual evidencia, en 2 meta-análisis de ECAs, recomendación ESPGHAN/ESPID(30,32).
En la guía de 2017, dichos probióticos siguen manteniendo la misma evidencia e indicación. Se añade con evidencia 2, el L. reuteri DSM 17938 a dosis de 108 a 4 × 108 UFC/día, habitualmente 5-7 días; y con el mismo grado de evidencia, formulaciones multicepa que incluyen diferentes combinaciones de: Lactobacillus acidophilus-rhamnosus 573L/1, 573L/2, 573L/3 a dosis de 1,2 × 1010 UFC dos veces al día, durante 5 días, con efecto solo en diarrea rotavirus, o bien Lactobacillus helveticus R0052 y L. rhamnosus R0011; o con un mayor número de probióticos asociados, Lactobacillus delbrueckii var. bulgaricus, L. acidophilus, Streptococcus thermophilus, Bifidobacterium bifidum (cepas LMG-P17550, LMG-P 17549, LMG-P 17503 y LMG-P 17500) a dosis de 109 UFC, 109 UFC, 109 UFC y 5 × 108 UFC, respectivamente(29). Recomendación ESPGHAN, ESPID, AAP: puede emplearse como tratamiento adyuvante a las soluciones de rehidratación(32).
Conviene observar que, si bien la eficacia de los probióticos no está estrictamente relacionada con la etiología, es probable que la mayor eficacia se ejerza en la gastroenteritis viral en lugar de la bacteriana, siendo la originada por el rotavirus la más estudiada. El norovirus es un agente etiológico emergente, y los datos sobre la eficacia de L. rhamnosus GG, S. boulardii y otros probióticos contra este virus son limitados.
No hay datos claros sobre la eficacia de los probióticos en pacientes con cólera, aunque existen pruebas débiles de que los probióticos pueden tener algún efecto preventivo. Además, hay poca evidencia con respecto a la eficacia y seguridad de los probióticos en niños desnutridos(31).
En la prevención de la diarrea aguda e infecciones comunes de guarderías
En la guía WGO del 2011 para la prevención de las infecciones gastrointestinales comunes adquiridas en la comunidad, se recomienda, con igual grado de evidencia 1b, el L. casei DN-114 001 en leche fermentada 1010 UFC, una vez por día; el B. lactis Bb-12 o L. reuteri ATCC 55730 107 UFC/g polvo de fórmula o L. casei Shirota en leche fermentada 1010 UFC, una vez al día(30).
En la guía WGO de 2017, se habla, en general, de prevención de infecciones de niños que asisten a guarderías, del uso del LGG sin especificar ni cepa ni dosis con evidencia 1, relegando a evidencia 2 a los probióticos: L. reuteri DSM 17938 a dosis de 108 UFC/día durante 3 meses y al L. casei DN-114001 y el L. casei Shirota a igual dosis que las previamente referidas(29).
En sus comentarios, se limitan a mencionar que “en la prevención de la diarrea de adultos y niños, hay pruebas de que ciertos probióticos pueden ser eficaces en algunos contextos en particular”(29).
La ESPGHAN considera que la mayoría de los estudios que investigaron el uso de probióticos para prevenir las infecciones del tracto respiratorio superior, también investigaron el efecto de los mismos sobre el riesgo de contraer infecciones gastrointestinales, pero la evidencia sobre estas últimas fue aún más débil.
Las cepas probióticas más estudiadas fueron Lactobacillus rhamnosus GG (LGG) y Bifidobacterium (B). animalis subsp. Lactis (BB-12). LGG se examinó en tres estudios con un total de 1.375 niños que recibieron dosis de 108 a 109 UFC/día. Todos los estudios informaron de efectos positivos en la reducción de la incidencia de infecciones respiratorias, no así la otra cepa investigada B. animalis subsp. lactis BB-12, que mostró escaso efecto.
Se concluye que, si se consideran los probióticos para la prevención de infección respiratoria del tracto superior en niños que asisten a guarderías, durante los meses de invierno, solo se debe considerar LGG. Sin embargo, la evidencia es limitada, y no hay evidencia convincente para recomendar el uso de probióticos para prevenir infecciones gastrointestinales en guarderías(32).
En la prevención de la diarrea asociada a antibióticos (DAA)
En WGO de 2011, se recomienda S. boulardii, cepa de S. cerevisiae, a dosis de 250 mg, dos veces por día con evidencia 1 a, basada en, al menos, dos meta-análisis de ECAs bien diseñados. También los siguientes probióticos con menor grado de evidencia 1 b: L. rhamnosus GG 1010 UFC, una o dos veces al día; el Bifidobacterium lactis Bb12 + Streptococcus thermophiles 107 + 106 UFC/g de fórmula; y el L. rhamnosus (cepas E/N, Oxy y Pen), 2 × 1010, dos veces al día. Sin embargo, hay un estudio en adultos hospitalizados que muestra que L. casei DN-114 00 es eficaz para evitar la DAA y diarrea provocada por C. difficile(30).
En la WGO de 2017, se continúa recomendando con evidencia 1: el Saccharomyces boulardii CNCM I-745, a dosis de 5×109 UFC/cápsula o 250-500 mg dos veces al día y el Lactobacillus rhamnosus GG a dosis de 1010 UFC/cápsula dos veces al día. Con igual evidencia, en adultos, además se indica la combinación: Lactobacillus acidophilus CL1285 y L. casei (Bio-K+ CL1285) ≥ 1010 UFC/día o yogur con Lactobacillus casei DN114, L. bulgaricus, y Streptococcus thermophilus ≥ 1010 UFC/día(29).
El Grupo de trabajo ESPGHAN sobre prebióticos y probióticos aconseja el uso de LGG o Saccharomyces (S). boulardii para la prevención de DAA. Del mismo modo, una recomendación de 2017 para los niños de la región de Asia y Pacífico, apoyó el uso de LGG o S. boulardii para la prevención de la DAA(31,32).
En cinco estudios que cubren 445 niños se mostró que, en comparación con placebos o ningún tratamiento, la administración de LGG redujo el riesgo de DAA de 23% a 9,6% (RR 0,48, IC 95%: 0,26-0,89) y el número necesario para tratar fue de 8 (IC 95%: 6-40). En un estudio que abarcaba 1.653 niños, la administración de S. boulardii redujo el riesgo del 20,9% al 8,8% en 6 ECAs (RR 0,43, IC del 95%: 0,30 a 0,60) y el número necesario para tratar fue de 9 (IC del 95%: 7 a 12). Por otra parte, S. boulardii redujo el riesgo de diarrea asociada con Clostridium difficile en 2 ECAs (RR 0,25; IC del 95%: 0,08 a 0,73), en otro estudio que abarcaba 579 niños.
Desde un punto de vista práctico:
• Con el fin de evitar DAA, LGG o S. boulardii debe ser considerado.
• S. boulardii debe también tenerse en cuenta para evitar diarrea asociada a C. difficile.
• Actualmente, no se recomiendan otras cepas de probióticos, cepas individuales o combinadas.
• No se dispone de datos de seguridad sobre el uso de probióticos para prevenir la DAA en niños gravemente enfermos y, por tanto, su uso debe someterse a un escrutinio especial(32).
Prevención de la diarrea nosocomial
En las guías de 2011, se recomendaban con evidencia 1 b el L. rhamnosus GG a dosis de 1010-1011 UFC, dos veces por día, y la combinación B. lactis Bb12 + S. thermophiles, 108 + 107 UFC/g de fórmula en polvo30. En las guías de 2017, se da evidencia 1 al LGG pero se rebaja la evidencia a 2 de la combinación anteriormente mencionada(29).
La ESPGHAN sobre prebióticos y probióticos recomienda que para prevenir la diarrea nosocomial se considera el LGG, y debe usarse a una dosis de, al menos, 109 UFC/día, mientras dure la estancia hospitalaria. No hay recomendaciones para prevenir las infecciones respiratorias de vías altas en niños hospitalizados(32). Del mismo modo, se ha recomendado en 2017, para los niños de la región de Asia y Pacífico(31).
Tratamiento y prevención del cólico del lactante
Ya en la guía WGO del 2011, aparecía el L. reuteri DSM 17938, 108 UFC/día administrado durante 21-30 días con evidencia 1 b para el tratamiento del cólico del lactante(30). Un meta-análisis de 2014 incluyó 3 ECAs y descubrió que, en comparación con los placebos, la administración de L. reuteri DSM 17938 redujo los tiempos de llanto en el día 21 en 43 minutos (diferencia media 43 min/día, IC 95%: 68 a 19), pero principalmente en lactantes amamantados exclusiva o predominantemente (diferencia media 57 min/día, IC 95%: 67 a 46). Otros estudios con cepas LGG y mezclas de probióticos no tenían efecto(32).
En la última guía WGO de 2017, en base a este meta-análisis, se mantiene dicha recomendación apoyada ahora con evidencia 1: L. reuteri DSM 17938 es la única cepa que se muestra eficaz en el tratamiento del cólico infantil en lactantes amamantados. La dosis de L. reuteri DSM 17938 para el tratamiento debe ser de, al menos, 108 UFC/día, durante 21-30 días; y para la prevención, se establece igual evidencia y la misma dosis, pero prolongada durante 3 meses(29). Sin embargo, para la ESPGHAN la evidencia es limitada y excluye recomendaciones específicas(32).
Tratamiento coadyuvante de la erradicación del Helicobacter pylori
En las guías WGO de 2011, se recomendaba el L. casei DN-114 001 en leche fermentada 1010-1012 UFC diariamente, durante 14 días, administrado conjuntamente con la triple terapia omeprazol, amoxicilina y claritromicina en ciclo de 7 días con evidencia 1 b(30).
En la guía de 2017, se añade al anterior el Saccharomyces boulardii CNCM I-745 a dosis de 500 mg/día en dos tomas, durante 2-4 semanas, pero se rebaja el grado de evidencia a 2 con ambos probióticos, dado que no hay evidencias que apoyen la eficacia de un probiótico por sí solo, sin antibióticos concomitantes, en la erradicación del Helicobacter pylori(29).
Una revisión sistemática y un meta-análisis de 11 ECAs, que incluyeron un total de 2.200 participantes (de los cuales 330 eran niños), encontró un aumento en la tasa de erradicación de H. pylori con la adición de S. boulardii al tratamiento con antibióticos. El 80% de los pacientes en el grupo de S. boulardii logró la erradicación de H. pylori en comparación con el 71% de los pacientes en el grupo control. Además, S. boulardii redujo el riesgo general de diarrea relacionada con la terapia antibiótica. Sin embargo, dado que el número de niños incluidos en los estudios fue limitado, se precisan ensayos adicionales(33).
Un documento de consenso internacional, desarrollado después de la V Conferencia de Consenso de Maastricht/Florencia, en 2016, concluyó que ciertos probióticos (como Lactobacilli y S. boulardii) muestran resultados favorables como tratamiento adyuvante en la infección por H. pylori para reducir los efectos secundarios, con una mejora en la adherencia al tratamiento antibiótico(34).
No obstante, los autores resaltan la gran heterogeneidad de las publicaciones incluidas, tanto en: la población a estudio (niños y adultos), los métodos diagnósticos, las terapias de erradicación y las cepas empleadas, por lo que la calidad de la evidencia no se puede considerar adecuada como para establecer una recomendación, aunque sí pueda ser útil para los pacientes en los que no se haya logrado la erradicación(31).
Tratamiento y prevención de trastornos funcionales gastrointestinales ligados al dolor abdominal
La guía WGO de 2011 proponía el L. rhamnosus GG 1010-1011 UFC, dos veces al día, con evidencia 1 a y al L. reuteri DSM 17938 108 UFC, dos veces al día, con evidencia 1 b efectivo para el alivio de algunos síntomas de los trastornos intestinales funcionales(30).
En WGO de 2017, se mantienen dichas recomendaciones, administrando dichos probióticos de 4-8 semanas con evidencia 1; y da cierta utilidad al VSL#3* administrando 1 sobre/día en niños de 4-11 años de edad, 1 sobre/12 h para los de 12-18 años, durante 6 semanas, con evidencia 3.
(*VSL#3: Lactobacillus plantarum, Lactobacillus casei, Lactobacillus acidophilus, Lactobacillus delbrueckii subsp. bulgaricus, Bifidobacterium infantis, Bifidobacterium longum, Bifidobacterium breve y Streptococcus salivarius subsp. Thermophilius)(29).
En conclusión, hay alguna evidencia de que los probióticos podrían disminuir la intensidad del dolor en niños con problemas funcionales de trastornos de dolor abdominal y solo dos probióticos (LGG y L. reuteri DSM 17 938) demuestran ser efectivos en más de 2 ECAs. Sin embargo, es difícil interpretar los resultados, ya que incluyen diferentes protocolos de estudio, duraciones de intervenciones, resultados primarios y tipo de dolor. Debido a las limitaciones de la evidencia disponible y la falta de pautas estandarizadas, no se puede proporcionar ninguna recomendación sobre el uso de probióticos para el tratamiento o prevención de trastornos funcionales gastrointestinales asociados a dolor abdominal en niños(32).
Prevención de la enterocolitis necrotizante (ECN)
En la WGO de 2011, se recomendaba Infloran®: B. bifidum NCDO 1453,+ L. acidophilus NCDO 1748, 109 UFC para cada cepa, dos veces al día, con evidencia 1 b, y con igual evidencia también otras combinaciones: L. acidophilus +B. infantis 108 UFC para cada uno, dos veces al día, u otras como B. infantis, B. bifidum, S. thermophilus 109 UFC para cada uno, una vez al día(30).
En la guía WGO de 2017, establece que “las sociedades científicas no han dado indicaciones claras sobre qué cepa o cepas de probióticos se debería recomendar”, aunque se reconoce que producen reducción del riesgo de ECN y mortalidad en lactantes con peso al nacer <1.500 g. De hecho, se pronuncian al respecto con similares argumentos a los de 2011: “hay ensayos clínicos que muestran que la suplementación probiótica reduce el riesgo de enterocolitis necrotizante de los recién nacidos prematuros. Las revisiones sistemáticas de los ensayos controlados aleatorizados también han demostrado una reducción del riesgo de muerte en grupos tratados con probióticos. Para impedir la muerte de un prematuro por cualquier causa, el número necesario a tratar (NNT) con probióticos es de 20”(29).
Las siguientes cepas han resultado NO ser efectivas: Saccharomyces boulardii CNCM I-745, Bifidobacterium breve BBG-001, Bb12(29).
La ESPGHAN no llega a pronunciarse sobre el tema(32). Existe un debate dentro de la comunidad científica sobre el uso de probióticos para la prevención de la ECN. Varios estudios informan que los probióticos reducen tanto la incidencia de ECN, como de mortalidad asociada a ECN, en recién nacidos prematuros y varios meta-análisis han confirmado estos resultados(31).
En 2014, se realizó un extenso meta-análisis que incluyó 24 ensayos. Encontraron que la suplementación con probióticos enterales redujo significativamente la incidencia de ECN grave (estadio II o más) (20 estudios, 5.529 neonatos) y mortalidad (17 estudios, 5.112 neonatos). No hubo evidencia de una reducción significativa de la sepsis nosocomial (19 estudios, 5.338 recién nacidos). Los ensayos incluidos no informaron de infección sistémica con el organismo probiótico suplementario. Dicha revisión concluye que el uso de probióticos reduce la aparición de ECN y la muerte en bebés prematuros que nacen con un peso inferior a 1.500 gramos. No hay datos suficientes con respecto a los beneficios y los posibles efectos adversos en los lactantes con mayor riesgo que pesan menos de 1.000 gramos al nacer(35).
En 2016, se incorporaron 13 ensayos (n = 5.033), encontrando reducción en la incidencia de ECN grave y mortalidad por todas las causas. No se mostró mayor incidencia de sepsis achacable al probiótico en los cultivos. Y, aunque concluyen que los bebés prematuros se benefician de los probióticos para prevenir la ECN grave y la muerte, la heterogeneidad de los organismos y los regímenes de dosificación estudiados, evitan que se haga una recomendación de tratamiento específico de especie(36).
Ante estos resultados, la Cochrane Neonatal Review Group apoya un cambio en la práctica clínica mediante el uso sistemático de probióticos en prematuros, excepto en aquellos de muy bajo peso para la edad gestacional (<1.000 g), debido a la falta de datos específicos en este grupo de alto riesgo, mientras que el Grupo de Nutrición y Metabolismo Neonatal de la SENeo considera que el uso de probióticos debería tenerse en cuenta en el prematuro ≤32 semanas de gestación o <1.500 g, incluidos los menores de 1.000 g, si bien su uso, en especial en los recién nacidos con menos de 1.000 g, debe someterse a una estrecha monitorización. La suplementación debe indicarse precozmente, en cuanto el neonato inicia la nutrición enteral y mantenerse hasta alcanzar una edad gestacional corregida de 36-37 semanas o hasta el alta(37).
Tratamiento y prevención de la enfermedad inflamatoria intestinal (EII)
Hay escasas evidencias sobre las recomendaciones del uso de probióticos en la edad pediátrica.
En las guías de 2011 solo aparecía, con evidencia 1 b, la siguiente recomendación al respecto en edad pediátrica: el uso de mezcla VSL#3, 4 a 9 x 1011 UFC, 2 veces al día, para el tratamiento de la colitis ulcerosa levemente activa, junto al tratamiento con salicilatos, mejorando las tasas de inducción, remisión y mantenimiento al año de seguimiento frente a placebo.
Para los adultos, sí que recogía más experiencia y se recomendaba con igual evidencia 1 b, Escherichia coli Nissle 1917, 5 × 1010 bact. viables, dos veces al día, para el mantenimiento y la remisión en la colitis ulcerosa. El VSL#3, 2 a 9 × 1011 UFC, dos veces al día, tanto para el tratamiento como para la prevención y mantenimiento de la remisión de la colitis o pouchitis ulcerosa de actividad leve(30).
En las guías WGO de 2017 para la edad pediátrica, la evidencia es más modesta, tipo 2, y se recomiendan tanto E. coli Nissle 1917 como el VSL#3 a igual dosis y pauta que las referidas para la inducción a la remisión de la colitis ulcerosa.
En adultos con pouchitis o reservoritis (una complicación que puede aparecer con el tiempo en pacientes colectomizados), la mezcla VSL#3 se mostró con mayor evidencia 1 en mantenimiento de la remisión que en el tratamiento de la pouchitis activa, en la que mostró menor evidencia 2.
En la colitis ulcerosa, E. coli Nissle 1917 y VSL#3 mostraron evidencias más modestas, tanto en el mantenimiento de la remisión 2, como en la inducción de dicha remisión 3, respectivamente(29).
En resumen: con respecto a la pouchitis, hay buena evidencia de la eficacia de VSL#3 para prevenir el episodio inicial y las recaídas adicionales después de la inducción de la remisión con antibióticos. En general, las pautas concluyen que los probióticos se recomiendan para pacientes con pouchitis de actividad leve o como terapia de mantenimiento para aquellos en remisión. Para la colitis ulcerosa, las pautas sugieren que E. coli Nissle puede ser tan eficaz como la mesalazina para mantener la remisión de la colitis ulcerosa, y que VSL#3 tiene eficacia en la inducción y el mantenimiento de la remisión de la colitis ulcerosa leve a moderada. Para la enfermedad de Crohn, las directrices señalan que los probióticos son menos efectivos, como se informó en una revisión sistemática de la Cochrane, que concluyó que no hay evidencia que indique un efecto beneficioso de los probióticos en el mantenimiento de la remisión en la enfermedad de Crohn(31).
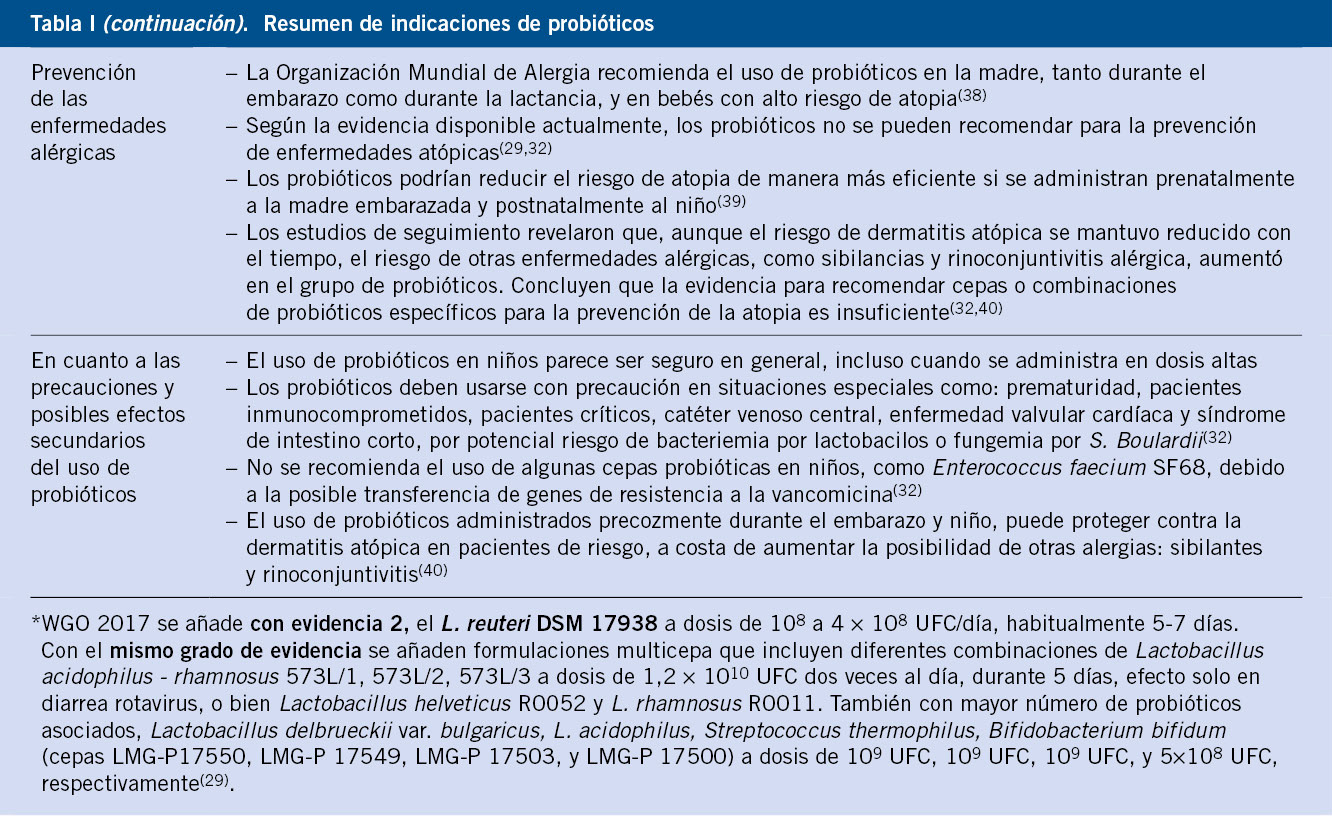
Prevención de las enfermedades alérgicas
En la guía WGO de 2011, no aparece ninguna recomendación específica de uso de probióticos para la prevención de las alergias, pero sí especifica que solo unos pocos estudios han evidenciado alguna utilidad en el tratamiento de un subgrupo de pacientes con eczema atópico. También que se conoce poco sobre la eficacia en la prevención de la alergia alimentaria(30).
En la guía de 2017 para la dermatitis atópica, especifica que “todavía no hay ninguna indicación clara en cuanto a qué probióticos utilizar”. Sin embargo, el beneficio neto de los probióticos durante el período perinatal previniendo enfermedades alérgicas, ha llevado a una recomendación de la Organización Mundial de Alergia sobre el uso de probióticos durante: el embarazo, la lactancia materna y el destete en familias con alto riesgo de enfermedad alérgica(29,38).
Aunque la Organización Mundial de Alergia recomienda el uso de probióticos en la madre, tanto durante el embarazo como durante la lactancia, y en bebés con alto riesgo de atopia, la ESPGHAN considera que no existe aún suficiente evidencia de calidad para recomendar rutinariamente su empleo en este apartado, principalmente debido a la heterogeneidad de los diferentes estudios analizados, en las cepas empleadas, el modo de administrarlas y la dosis y duración de la suplementación.
El meta-análisis más reciente comprendió 17 ECAs, que cubrieron a 4.755 niños, y mostró que el uso de probióticos, en general, disminuye el riesgo de dermatitis atópica, especialmente si se usa una combinación de probióticos. Sin embargo, no se encuentran diferencias significativas en términos de prevención del asma, sibilancias o rinoconjuntivitis. El análisis agrupado mostró que los probióticos podrían reducir el riesgo de atopia de manera más eficiente si se administran prenatalmente a la madre embarazada y postnatalmente al niño(39). Los estudios de seguimiento revelaron que, aunque el riesgo de dermatitis atópica se mantuvo reducido con el tiempo, el riesgo de otras enfermedades alérgicas, como sibilancias y rinoconjuntivitis alérgica, aumentó en el grupo de probióticos. Concluyen que la evidencia para recomendar cepas o combinaciones de probióticos específicos para la prevención de la atopia es insuficiente(32,40).
En cuanto a la posibilidad de utilizar probióticos para acelerar la tolerancia oral en niños con alergia a proteínas de leche de vaca (APLV), dos estudios, uno llevado a cabo en 2012 y otro en 2017, por los mismos autores, y ampliando la primera muestra de 55 a 220 lactantes (110 reciben fórmula hidrolizada y 110 la misma, suplementada con Lactobacillus GG), encuentran que en términos de adquisición de tolerancia, a los 12, 24 y 36 meses, fue mayor en los niños suplementados, tanto en casos de APLV IgE como no IgE mediada(41).
Los probióticos y prebióticos han demostrado estar relacionados con patologías que están fuera del espectro normal de la enfermedad gastrointestinal. Las nuevas evidencias sugieren que la microbiota intestinal puede tener efecto sobre afecciones no gastrointestinales, estableciendo así un vínculo entre esas afecciones y el tracto gastrointestinal. Muchos estudios han demostrado que los probióticos pueden reducir la vaginosis bacteriana, la cistitis, reducir los patógenos orales y las caries dentales, y reducir la incidencia y duración de las infecciones comunes del tracto respiratorio superior, incluidas las otitis. También, se están probando probióticos y prebióticos para la prevención de algunas manifestaciones del síndrome metabólico, incluyendo: exceso de peso, diabetes tipo 2 y dislipemias, alteraciones del estado de ánimo, como la ansiedad, etc.; pero están fuera del objetivo de esta revisión, que se ha centrado en el uso en aquellas patologías pediátricas en las que más evidencia se ha encontrado.
Precauciones y posibles efectos secundarios del uso de los probióticos
El uso de probióticos, debido al conocimiento de sus potenciales beneficios para la salud, mantiene un crecimiento exponencial, dando lugar a una gran variedad de productos comerciales denominados genéricamente nutracéuticos; es decir, de origen natural, beneficiosos para la salud, con propiedades biológicas activas y capacidad preventiva y/o terapéutica definida. Dichos productos también se utilizan como complemento en los llamados alimentos funcionales(1). Los productos probióticos están llegando al mercado en una amplia gama de formas diferentes. Por ejemplo, se agregan a los alimentos o se proporcionan como suplementos envasados en: cápsulas, píldoras, suspensiones, bolsitas de polvo, aerosoles y granulados. Estos productos se rigen por normativas, tanto europeas como americanas, diferentes, que en general deben ofrecer al consumidor información fiable sobre sus posibles efectos beneficiosos para la salud y la ausencia de virulencia “bajo cualquier circunstancia”, lo que les permite ser catalogados como organismos Generally Regarded As Safe (GRAS) por la Food and Drug Administration de EE.UU. y Qualified Presumption of Safety (QPS) por la European Food Safety Authority. Estos criterios son significativamente menos estrictos que los de origen medicamentoso o medicamentos. La administración de estos probióticos en población sana se ha demostrado, a lo largo de los años, como segura, reflejo de ello ha sido el escaso número de complicaciones publicadas. Sin embargo, el uso creciente en un amplio abanico de patologías, ha hecho reconsiderar el posible riesgo de complicaciones en algunas de ellas(29).
Los problemas de seguridad no se han establecido para la mayoría de probióticos, y los datos solo se han generado como resultados secundarios. Es importante señalar que faltan estudios que evalúen la seguridad como resultado primario del estudio. La mayoría de los efectos adversos informados se basaron en informes de casos o series de casos, y se deben realizar ECAs diseñados adecuadamente para evaluar este problema. Todo ello ha generado dudas sobre la calidad y la seguridad de dichos productos al ser aplicados en pacientes más vulnerables de presentar efectos secundarios indeseables(32).
En 2011, la Agencia de Investigación y Calidad de la Salud de EE.UU. publicó un informe sobre la seguridad de los probióticos, basado en una revisión sistemática de 622 ECAs, concluyendo que:
1. La mayoría de las cepas probióticas que se estudiaron deberían considerarse generalmente como seguras, pero la evidencia que abordaba adecuadamente la seguridad era limitada.
2. Los efectos adversos eran más frecuentes en pacientes con problemas de salud.
3. No hay evidencia concluyente de que el uso de una mezcla de diferentes cepas probióticas tuviera más eventos adversos que el uso de una única.
4. Los efectos a largo plazo del uso de cepas probióticas es desconocido(42).
En general, los efectos secundarios del uso de probióticos pueden ser potencialmente importantes como: infecciones sistémicas, actividades metabólicas nocivas, estimulación inmunológica en poblaciones susceptibles, síntomas gastrointestinales y la transferencia de genes que codifican características bacterianas potencialmente peligrosas, como la resistencia a los antimicrobianos. Además, pueden aparecer otros que incluyen efectos metabólicos, como la producción de d-lactato con acidosis láctica, la desconjugación de las sales biliares y los efectos inmunomoduladores a corto y largo plazo. Estos últimos son particularmente relevantes para el uso neonatal y la transferencia de material genético como los plásmidos que codifican la resistencia antimicrobiana de las bacterias probióticas a las bacterias más patógenas. Finalmente, también hay efectos adversos limitados a síntomas gastrointestinales leves, como: calambres abdominales, náuseas, diarrea, flatulencia y alteración del gusto, aunque los estudios no describieron ninguna diferencia en comparación con el placebo.
Las especies o cepas de Bifidobacterium, Lactobacillus y Saccharomyces son con las que mayoritariamente se informan de efectos adversos, dado que estas son las más utilizadas, en particular para el LGG y para el S. boulardii. También hay mayores preocupaciones de seguridad sobre el uso de probióticos si otras especies que pertenecen a los mismos géneros son patógenas (Streptococcus, Bacillus y Enterococcus)(32).
Los mayores riesgos específicos del uso de probióticos son:
Septicemia
Los pacientes que potencialmente corren un riesgo de diseminación séptica son: los inmunocomprometidos, prematuros y enfermos oncológicos debilitados. Los factores de riesgo menores son: la presencia de un catéter venoso central, barrera intestinal deteriorada, síndrome de intestino corto, administración de probióticos por yeyunostomía, administración concomitante de antibióticos de amplio espectro (resistencia a los probióticos), la patogenicidad conocida de las cepas probióticas y enfermedad valvular cardíaca(32).
Se estima que el riesgo de desarrollar bacteriemia por lactobacilos ingeridos es inferior a uno por un millón de los que lo ingieren, y los factores de riesgo asociados son: la existencia de inmunosupresión, de comorbilidades subyacentes graves o de hospitalizaciones, tratamiento antibiótico o intervenciones quirúrgicas previas (especialmente en pacientes con síndrome de intestino corto), cirugía cardiaca y parálisis cerebral.
El riesgo de desarrollar fungemia por Saccharomyces boulardii se estima en uno por 5,6 millones de consumidores. El riesgo de fungemia asociado con S. boulardii aumenta en pacientes críticos, los que están en unidades de cuidados intensivos, usan ventilación mecánica o catéteres venosos centrales, aquellos tratados con antibióticos de amplio espectro, o los que están inmunosuprimidos o son recién nacidos prematuros. Las guías de práctica clínica no recomiendan el uso de S. boulardii en pacientes con infecciones por C. difficile en estado crítico.
Pancreatitis severa en adultos
Sobre todo, cuando además hay isquemia intestinal, la administración de un preparado multiespecie (Lactobacillus acidophilus, Lactobacillus casei, Lactobacillus salivarius, Lactococcus lactis, Bifidobacterium bifidum y Bifidobacterium lactis) se relacionó con mayor mortalidad. Por lo tanto, se contraindica su uso en estas circunstancias(32).
Efecto sobre el sistema inmune
Hay varios estudios que han valorado la posibilidad de prevenir enfermedades alérgicas, administrando diferentes probióticos desde antes del nacimiento a embarazadas, y desde o poco después del nacimiento al niño. Se ha visto que, si bien, tienen un efecto protector sobre la dermatitis atópica durante un tiempo, el riesgo de otras enfermedades alérgicas, como sibilantes y rinoconjuntivitis alérgica aumentó en el grupo de prueba, como ya se ha comentado(40). Aunque no hay estudios a largo plazo que hayan probado los efectos de los probióticos sobre el sistema inmune, sí que parecen tener algún efecto sin que se conozcan los mecanismos exactos.
El riesgo de reacciones alérgicas por la ingesta de probióticos en pacientes alérgicos a las proteínas de la leche o el huevo, es relativamente frecuente y depende no del probiótico en sí, sino de los excipientes o componentes de la matriz de encapsulación. Martín-Muñoz, et al. en 2012(43), revisan los contenidos de trazas de proteínas de leche de vaca y huevo en diferentes productos comercializados con probióticos (7 suplementos dietéticos y 4 preparados farmacéuticos), encontrando contaminación y trazas de huevo en 3, y de proteínas de leche de vaca en 10, con valores de hasta 2,5 mg/kg en 3 de ellos, y algunos sin clara advertencia de su existencia en el etiquetado. Dado que las alergias a las proteínas de leche de vaca y al huevo son dos de las alergias alimentarias más comunes, el uso de probióticos en estos pacientes debe limitarse a los productos que no contengan alérgenos alimentarios y reflejar claramente dicha circunstancia en el etiquetado(29).
La transferencia de resistencia a los antimicrobianos
La posibilidad de transferencia de resistencia antimicrobiana desde los probióticos a bacterias patógenas se ha comprobado en algunas cepas: Lactobacillus, es naturalmente resistente a la vancomicina; LGG no tiene plásmidos que contengan resistencia a antibióticos; Lactobacillus reuteri ATCC 55730 tenía un rasgo de resistencia transferible para tetraciclina y lincomicina y, por lo tanto, fue reemplazado por una nueva cepa, L. reuteri DSM 17938(44); y no se recomienda el uso del Enterococcus faecium SF68 en la gastroenteritis aguda en niños, debido a la posible transferencia de genes resistentes a la vancomicina(32).


Bibliografía
Los asteriscos muestran el interés del artículo a juicio del autor.
1.*** Hernández A, Coronel C, Monge M, Quintana C. Microbiota, prebióticos, probióticos y simbióticos. Pediatría integral. 2015; XIX(5): 337-54.
2. Dinan TG, Stanton C, Cryan JF. Psychobiotics: A Novel Class of Psychotropic Biol Psychiatry. 2013; 74: 720-6.
3. Sarkar A, Lehto SM, Harty S, Dinan TG, Cryan JF, Burnet PWJ. Psychobiotics and the Manipulation of Bacteria–Gut–Brain Signals Trends. Neurosci. 2016; 39: 763-81.
4. Desbonnet L, Garrett L, Clarke G, Bienenstock J, Dinan TG. The probiotic bifidobacteria infantis: an assesment of potential antidepressant properties in the rat. Journal of psychiatric research. 2008; 43: 164-74.
5. Naseribafrouei A, Hestad K, Avershina E, Sekelja M, Linløkken A, Wilson R, et al. Correlation between the human fecal microbiota and depression. Neurogastroenterology and Motility: the official journal of the European Gastrointestinal Motility Society. 2014; 26: 1155-62.
6. Akkasheh G, Kashani-Poor Z, Tajabadi-Ebrahimi M, Jafari P, Akbari H, Taghizadeh M, et al. Clinical and metabolic response to probiotic administration in patients with major depressive disorder: A randomized, double-blind, placebo-controlled trial. Nutrition. 2016; 32; 315-20.
7. Allen AP, Hutch W, Borre YE, Kennedy PJ, Temko A, Boylan G, et al. Bifidobacterium longum 1714 as a translational psychobiotic: modulation of stress, electrophysiology and neurocognition in healthy volunteers. Transl Psychiatry. 2016; 6: e939.
8. A. Kazemi, Ali Noorbala AA, Eskandari M, Azam K, Eskandari MH, Djafaria K. Effect of probiotic and prebiotic vs placebo on psychological outcomes in patients with major depressive disorder: A randomized clinical trial. Clinical Nutrition. 2019; 38: 522e-28.
9. Taverniti V, Guglielmetti S. The immunomodulatory properties of probiotic microorganisms beyond their viability (ghost probiotics: proposal of paraprobiotic concept). Genes Nutr. 2011; 6: 261-74.
10.*** Zorzela L, Ardestani SK, McFarland LV, Vohra S. Is there a role for modified probiotics as beneficial microbes: a systematic review of the literature? Benef. Microbios. 2017; 8: 739-54.
11. Ouwehand AC, Tölkkö S, Kulmala J, Salminen S, Salminen E. Adhesion of inactivated probiotic strains to intestinal mucus. Lett Appl. Microbiol. 2000; 31: 82-6.
12. Maldonado C, Perdigón G. Role of viability of probiotic strains in their persistence in the gut and in mucosal immune stimulation. J. Appl. Microbiol. 2004; 97: 673-81.
13. Perdigón G, de Macías ME, Álvarez S, Oliver G, de Ruiz Holgado AA. Effect of Perorally Administered Lactobacilli on Macrophage Activation in Mice. Infectar Immun. 1986; 53: 404-10.
14. Ibnou-Zekri N, Blum S, Schiffrin EJ, von der Weid T. Divergent Patterns of Colonization and Immune Response Elicited from Two Intestinal Lactobacillus Strains That Display Similar Properties In Vitro Patrones. Infectar Immun. 2003; 71: 428-36.
15. Mohamadzadeh M, Olson S, Kalina WV, Ruthel G, Demmin GL, Warfield KL, et al. Lactobacilli activate human dendritic cells that skew T cells toward T helper 1 polarization. Proc Nat. Acad Sc. EE.UU. 2005; 102: 288-305.
16. Adams CA. The probiotic paradox: live and dead cells are biological response modifiers. Nutr Res Rev. 2010; 23: 37-46.
17. Osamu K, Akira A, Sazaly A, Naoki Y. Probiotics and Paraprobiotics in Viral Infection: Clinical Application and Effects on the Innate and Acquired Immune Systems. Current Pharmaceutical Design. 2018; 24: 710-7.
18. Nakamura F, Ishida Y, Aihara K, Sawada D, Ashida N, Sugawara T, et al. Effect of fragment lactobacillus amylovorus CP on 1563 on lipid metabolism in overweight and mildly obese individuals: randomized controlled trial. Microbial Ecology in health & Disease. 2016; 27: 303-12.
19. Caimari A, Del Bas JM, Boque N, Crescenti A, Puiggròs F, Chenoll E, et al. Heat-kulled Bifidobacterium animalis subsp Lactis CECT 8145 invres lean mass and ameliorates metabolic syndrome in cafeteria-fed obese rats. J Funtional Foods. 2017; 38: 251-63.
20. Tsilingiri K, Barbosa T, Penna G, Caprioli F, Sonzogni A, Viale G, et al. Probiotic and postbiotic activity in health and disease: comparison on novel polrised ex-vivo organ cluture model. Gut. 2012; 61: 1007-15.
21. Wegh CAM, Geerlings SY, Knol J, Roeselers G, Belzer C. Postbiotics and their Potential Applications in Early Life Nutrition and Beyond. Int J Mol Sci. 2019; 20: 46-73.
22. Aguilar-Toalá J, García-Varela R, García H, Mata-Haro V, González-Córdova A, Vallejo-Córdoba B, et al. Postbiotics: An evolving term within the functional foods field. Trends Food Sci Technol. 2018; 75: 105-14.
23. Kareem KY, Loh TC, Foo HL, Akit H, Samsudin AA. Effects of the postbiotic and inulin diet on growth performance, expression of IGF1 and GHR mRNA, fecal microbiota and volatile fatty acids in broilers. BMC Vet Res. 2016; 12: 163.
24. Merzza HA, Chwen LT, Ling FH, Samsudin AA, Mustapha NM, Zulkifli I, et al. Efects of Feeding Diferent Postbiotics Produced by Lactobacillus plantarum on Growth Performance, Carcass Yield, Intestinal Morphology, Gut Microbiota Composition, Immune Status, and Growth Gene Expression in Broilers under Heat Stress. Animals. 2019; 9: 644.
25. Chuah L, Ling FH, Teck Chwen L, Noorjahan Banu MAN, Alitheen NBM, Yeap SK, Mutalib NEA, et. al. Postbiotic metabolites produced by Lactobacillus plantarum strains exert selective cytotoxicity effects on cancer cells. Complemento BMC Altern Med. 2019; 19: 114.
26. Thomaz VA, Fukumori C, Marcantonio FC. New insights into therapeutic strategies for gut microbiota modulation in inflammatory diseases. Clin Transl Immunology. 2016; 5: e87.
27. Mosca F, Gianni ML, Rescigno M. Can Postbiotics Represent a New Strategy for NEC? Advances in Experimental Medicine & Biology. 2019; 1125: 37-45.
28. Espín JB. Probióticos: luces y sombras. En: AEPap (ed.). Curso de Actualización Pediatría. 2018. Madrid: Lúa Ediciones 3.0; 2018. p. 191-200.
29.*** Guarner F, Sanders ME, Eliakim R, Fedorak R, Gangl A, Garisch J, et al. World Gastroenterology Organisation Global Guidelines. Probiotics and prebiotics 2017. Acceso el 1 de diciembre de 2019. Disponible en: http://www.worldgastroenterology.org/guidelines/global-guidelines/probiotics-and-prebiotics.
30. Guarner F, Khan AG, Garisch J, Eliakim R, Gangl A, Thomson A, et al. World Gastroenterology Organisation Global Guidelines. Probiotics and prebiotics 2011. Acceso el 1 de diciembre de 2019. Disponible en: http://www.worldgastroenterology.org/guidelines/global-guidelines/probiotics-and-prebiotics.
31. Cameron D, Seng Hock Q, Kadim M, Mohan N, Ryoo F, Sandhu B, et al. Probiotics for gastrointestinal disorders: proposed recommendations for children of the Asia-Pacific region World J Gastroenterol. 2017; 23: 7952-64.
32.*** Hojsak I, Fabiano V, Pop TL, Goulet O, Zuccotti GV, Cullu F, et al. Guidance on the use of probiotics in clinical practice in children with selected clinical conditions and in specific vulnerable groups. Acta Paediatr. 2018; 107: 927-37.
33. Szajewska H, Horvath A, Kołodziej M. Systematic review with meta-analysis: Saccharomyces boulardii supplementation and eradication of Helicobacter pylori infection. Aliment Pharmacol Ther. 2015; 41: 1237-45.
34. Malfertheiner P, Megraud F, O’Morain CA, Gisbert JP, Kuipers EJ, Axon AT, et al. Management of Helicobacter pylori infection-the Maastricht V/Florence Consensus Report Intestino. 2017; 66: 6-30.
35. AlFaleh K, Anabrees J. Probiotics for prevention of necrotizing enterocolitis in preterm infants. Evidence-Based Child Health. 2014; 9: 584-671.
36. Sawh SC, Deshpande S, Jansen S, Reynaert CJ, Jones PM. Prevention of necrotizing enterocolitis with probiotics: a systematic review and meta-analysis. Peer J. 2016; 4: e24-29.
37. Narbona E, Uberos J, Armadá MI, Couce ML, Rodríguez G, Sáenz de Pipaone M. Grupo de Nutrición y Metabolismo Neonatal, Sociedad Española de Neonatología: recomendaciones y evidencias para la suplementación dietética con probióticos en recién nacidos de muy bajo peso al nacer. An Pediatr (Barc). 2014; 81: 397e1-8.
38. Fiocchi A, Pawankar R, Cuello-García C, Ahn K, Al-Hammadi S, Agarwal A, et al. World Allergy Organization-McMaster University Guidelines for Allergic Disease Prevention (GLAD-P): World Allergy Organization J. 2015; 8: 4.
39. Zuccotti G, Meneghin F, Aceti A, Barone G, Callegari ML, Di Mauro A, et al. Probiotics for prevention of atopic diseases in infants: systematic review and meta-analysis. Allergy. 2015; 70: 1356-71.
40. Peldan P, Kukkonen AK, Savilahti E, Kuitunen M. Perinatal probiotics decreased eczema up to 10 years of age, but at 5-10 years, allergic rhino-conjunctivitis was increased. Clin Exp Allergy. 2017; 47: 975-9.
41. Berni Canani R, Di Costanzo M, Bedogni G, Amoroso A, Cosenza L, Di Scala C, et al. Extensively hydrolyzed casein formula containing Lactobacillus rhamnosus GG reduces the occurrence of other allergic manifestations in children with cow’s milk allergy: 3 year randomized controlled trial. J Allergy Clin Immunol. 2017; 139: 1906-13.
42. Hempel S, Newberry S, Ruelaz A, Wang Z, Miles JN, Suttorp MJ, et al. Safety of probiotics used to reduce risk and prevent or treat disease. Evid Rep Technol Assess (Full Rep). 2011; 200: 1-645.
43. Martín-Muñoz MF, Fortuni M, Caminoa M, Belver T, Quirce S, Caballero T. Anaphylactic reaction to probiotics. Cow’s milk and hen’s egg allergens in probiotic compounds. Pediatr Allergy Immunol. 2012; 23: 778-84.
44. Rosander A, Connolly E, Roos S. Removal of antibiotic resistance gene-carrying plasmids from Lactobacillus reuteri ATCC 55730 and characterization of the resulting daughter strain, L. reuteri DSM 17938. Appl Environ Microbiol. 2008; 74: 6032-40.
Bibliografía recomendada
– Hernández A, Coronel C, Monge M, Quintana C. Microbiota, prebióticos, probióticos y simbióticos. Pediatría integral. 2015, XIX(5): 337-54.
En este artículo, se revisan diferentes aspectos sobre la flora gastrointestinal o microbiota, desde el momento de su adquisición, antes, durante y tras el nacimiento, composición y distribución de la misma en diferentes nichos o tramos intestinales. Se realiza un recordatorio anatomo-histo-fisio-inmunológico de la barrera intestinal y se analizan las funciones de la microbiota y el microbioma: 1) Mejora de dicha barrera mediante diferentes mecanismos. 2) La función metabólica, mediante la cual la flora comensal degrada los restos carbonados y proteicos no digeridos en el intestino delgado. 3) Una de las funciones más importantes es la inmunomodulación, dado que la microflora actúa modulando la respuesta tolerogénica de homeostasis intestinal Th2, frente a la proinflamatoria Th1.
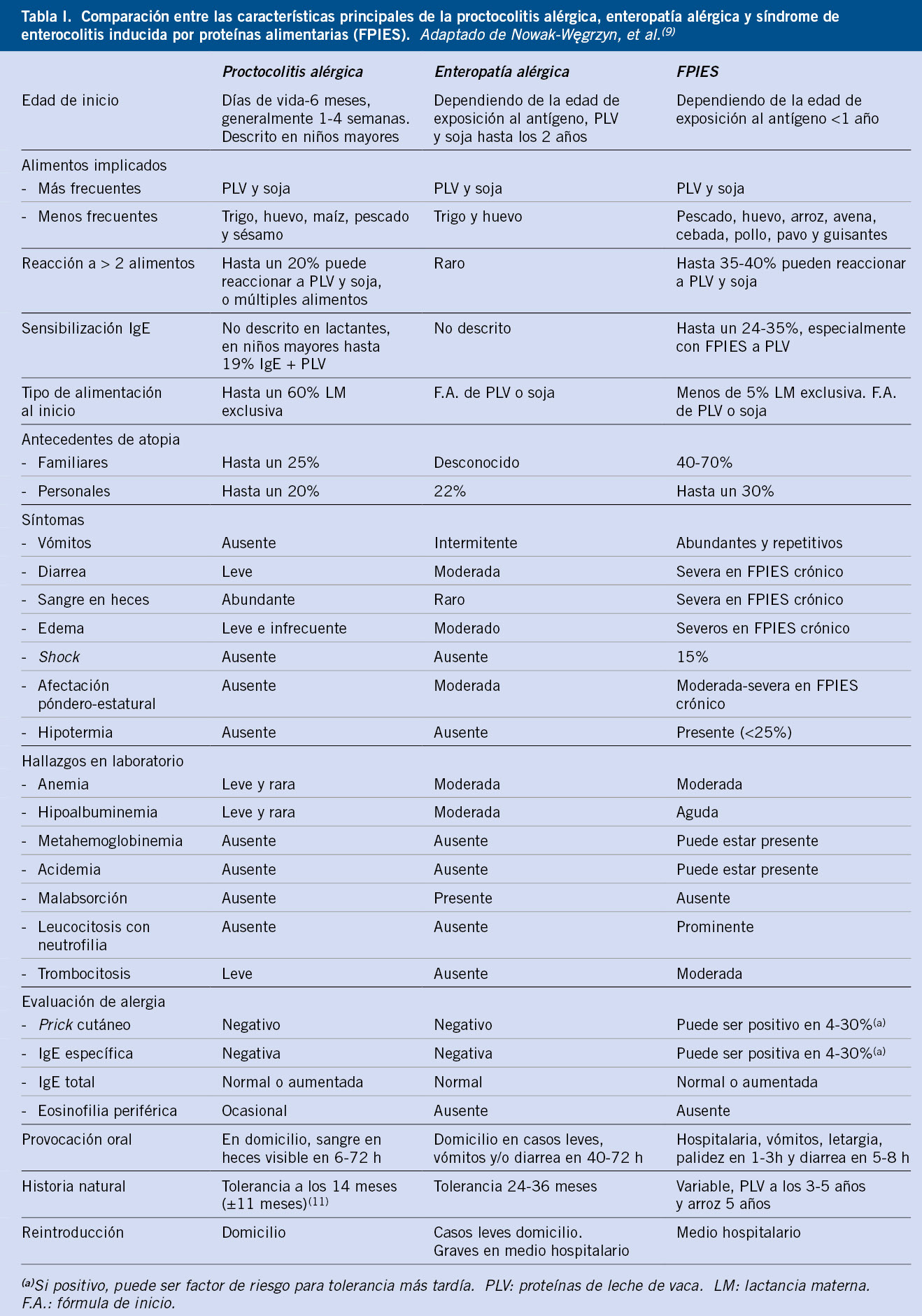
También, se valoró la composición, dosificación, mecanismos y efectos beneficiosos de los prebióticos, probióticos y simbióticos, así como las normativas generales por las que se rigen dichos productos bioterapéuticos, considerados comercialmente como nutracéuticos y con normativas más laxas que los medicamentos propiamente dichos. Se incluye una somera tabla de usos e indicaciones en Pediatría (Tabla I), según el consenso de WGO publicado en 2011.
– Zorzela L, Ardestani SK, McFarland L V, Vohra S. ¿Is there a role for modified probiotics as beneficial microbes: a systematic review of the literature? Benef Microbios. 2017; 8: 739-54.
Interesante revisión donde se realiza un estudio sistemático y un meta-análisis del uso de probióticos modificados (muertos por calor o sonicados), los llamados paraprobióticos, valorando la eficacia y seguridad para prevenir y tratar diversas enfermedades, dado el potencial riesgo del uso de probióticos vivos para el tratamiento o prevención de determinadas patologías en pacientes comprometidos. Se efectúa una amplia búsqueda en diferentes bases de datos. Se incluye un total de 40 ensayos (n = 3.913): 14 ensayos para la prevención de enfermedades (15 brazos con probióticos modificados y 20 brazos control), y 26 ensayos para el tratamiento de diversas enfermedades (29 brazos con probióticos modificados y 32 brazos control). El objetivo primario fue el análisis de la eficacia para prevenir o tratar la enfermedad, y el resultado secundario fue la incidencia de eventos adversos.
Se obtuvo los siguientes resultados: los probióticos modificados (paraprobióticos) se compararon con placebo (44%) o con la misma cepa probiótica viva (39%) o solo con terapias estándar (17%). Los microbios modificados no fueron significativamente más o menos efectivos que los probióticos vivos en el 86% de los ensayos preventivos y el 69% de los ensayos de tratamiento. Las cepas probióticas modificadas fueron significativamente más efectivas en el 15% de los ensayos de tratamiento. Las tasas de incidencia de eventos adversos fueron similares para los probióticos modificados y vivos, y otros grupos de control, pero muchos ensayos no recopilaron datos de seguridad y homogeneidad comparables adecuados, por lo que no se pudo llegar a conclusiones firmes de indicación para el tratamiento de enfermedades específicas, precisando una ampliación de estudios y ensayos.
Todo ello, rompe con la premisa de viabilidad para asegurar un efecto de dichos probióticos y abre un nuevo camino de investigación en la utilización de sustancias, bien secretadas por los propios probióticos (postbióticos) o bien los propios probióticos desvitalizados o incluso fragmentados con el menor riesgo, en cuanto a translocación o fungemia, que potencialmente podrían tener los probióticos cuando se usan en pacientes comprometidos.
– Guarner F, Sanders ME, Eliakim R, Fedorak R, Gangl A, Garisch J, et al. World Gastroenterology Organisation Global Guidelines. Probiotics and prebiotics. 2017. Acceso el 1 de diciembre de 2019. Disponible en: http://www.worldgastroenterology.org/guidelines/global-guidelines/probiotics-and-prebiotics.
Esta nueva guía de la Organización Mundial de Gastroenterología (WGO) es renovación de la ya previamente publicada en 2011. Realiza un repaso de las diferentes patologías, tanto en adultos como en edad pediátrica, de las indicaciones de los probióticos, con grado de evidencia y dosis; además, aporta unas tablas resumen muy prácticas. Es de necesaria lectura y manejo como herramienta a la hora de hacer una adecuada prescripción de dichos probióticos.
– Hojsak I, Fabiano V, Pop TL, Goulet O, Zuccotti GV, Cullu F, et al. Guidance on the use of probiotics in clinical practice in children with selected clinical conditions and in specific vulnerable groups. Acta Paediatr. 2018; 107: 927-37.
Esta revisión de las sociedades europeas resume las recomendaciones y las directrices científicamente acreditadas sobre el uso de probióticos en niños con condiciones clínicas seleccionadas, y proporciona puntos de práctica.
La Asociación Europea de Pediatría, la Unión de las Sociedades y Asociaciones Nacionales Europeas de Pediatría (EPA/UNEPSA) convocó a un panel de expertos europeos independientes para examinar la suplementación con probióticos.
Se realizaron búsquedas en las bases de datos de PubMed y Cochrane Library hasta septiembre de 2017 respecto a directrices, recomendaciones y documentos de posición relevantes que cubriesen las indicaciones clínicas pediátricas que se seleccionaron, recuperando las pruebas de alta calidad más recientes. Determinaron qué cepas probióticas específicas eran efectivas para prevenir: la diarrea asociada a antibióticos y nosocomial, tratar la gastroenteritis aguda y el cólico infantil en los lactantes. El panel decidió no incluir alimentos que contuviesen probióticos, prebióticos y simbióticos, porque estaba fuera del alcance de ese documento. También excluyeron el uso de bacterias vivas para prevenir la enterocolitis necrotizante en bebés prematuros.
Se recomienda especial precaución para ciertos grupos, incluidos los bebés prematuros, los pacientes inmunocomprometidos y los pacientes críticos.
| Caso clínico |
|
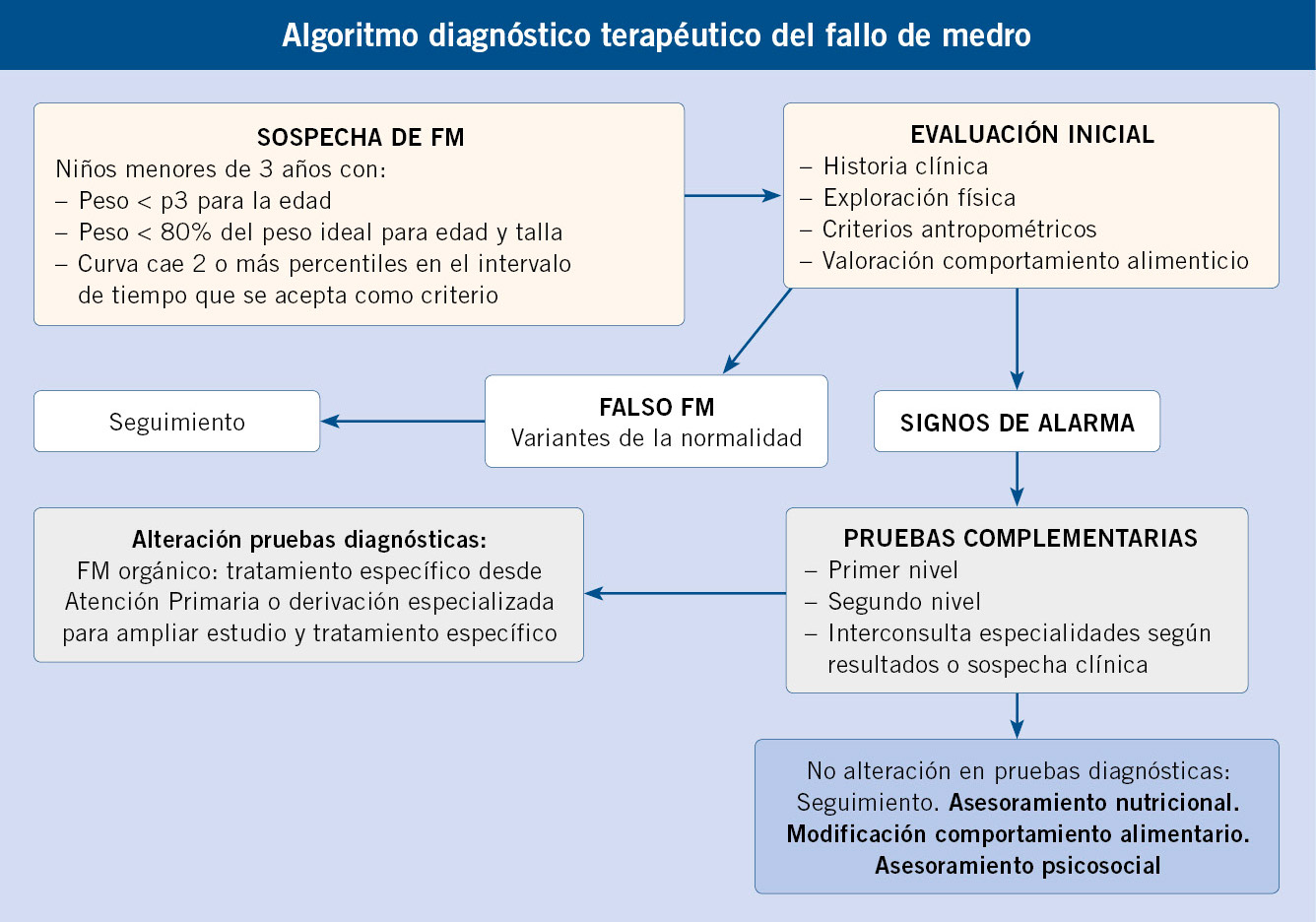
Niño de 4 años y 2 meses, conocido de consulta, que acude por cuadro de disconfort, dolor abdominal recidivante de tipo cólico, que puede prolongarse varias horas. En ocasiones, se acompaña de vómitos y abundante flatulencia que suele causar alivio. Su madre lo ha relacionado en principio con la toma de leche, aunque ha probado a dar hidrolizados, tanto de leche de vaca como a base de soja, e incluso ha probado, por indicación hospitalaria, una leche altamente hidrolizada a base de aminoácidos esenciales. Todo le sienta igual de mal, también otros alimentos proteicos (pescado, carne de res y pollo) y verduras (habichuelas verdes y bubango). En ocasiones, le ha producido dicho malestar, en otras los come sin problemas. Ha retirado sistemáticamente uno por uno estos alimentos durante 3-4 semanas sin que hubiera respuesta positiva, incluso ha hecho dieta exenta de FODMAPs sin resultados. No ha tenido problemas con el huevo y, actualmente, toma yogures normales, que parece tolerar mejor que la leche. En cuanto al hábito intestinal, tiene periodos de estreñimiento (Bristol 1-2), otros de heces más flojas sin llegar a ser líquidas (Bristol 5-6), y mucha flatulencia maloliente. Nunca ha tenido deposiciones sanguinolentas ni reacciones alérgicas en piel, a pesar de que presenta una leve atopia.
Su desarrollo póndero-estatural ha sido correcto, aunque en percentiles bajos de talla y peso (Pc 10 de peso y Pc 3 de talla), pero la talla diana está dentro de la talla genética y el desarrollo psicomotor ha sido adecuado en todo momento.
A la exploración: peso: 15 kg (Pc 15; -1,04 DE); talla: 97 cm (Pc 3; -1,96 DE), IMC (Pc 14,96; -0,05 DE). Buen estado general con normocoloración de piel y mucosas, doble pliegue palpebral y lengua geográfica, piel algo seca, sin descamación ni eritemas. Adecuado trofismo de cabello y dientes caducos sin caries ni alteraciones del esmalte. Resto de exploración por órganos y aparatos, sin hallazgos llamativos.
Exámenes complementarios realizados: RAST y prick test a PLV negativos, prueba de provocación APLV superada (aunque su madre sigue evitando darle mucha leche, porque nota que le sienta mal).
Estudios de hemograma, proteína C reactiva, VSG, bioquímica sanguínea: glucemia con perfil hepático, renal, iones (Ca, P, Zn, Cl, Na), ferritina, inmunoglobulinas, vitamina B12, ácido fólico, hormonas tiroideas TSH y T4L, todo dentro de límites normales. Serología de enfermedad celiaca: Ac antitransglutaminasa y antipéptido deaminado de gliadina, resultó negativa. Orina A/S, Ca/cr, citratos: normales. Heces: coprocultivo y parásitos, negativos. Determinación de grasa en heces (Van de Kamer), pH fecal, sustancias reductoras en heces, Ag de Helicobacter pylori y Calprotectina en heces: todo negativo. Electrolitos en sudor dentro de la normalidad. Ecografía abdominal, sin hallazgos anormales.
|
|
|










































































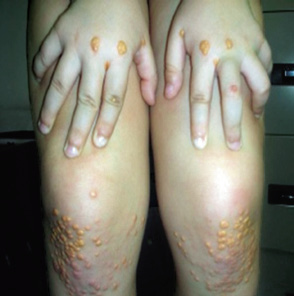
 El término carotinemia hace referencia a una condición médica consistente en la coloración anaranjado- amarillenta de la piel debida a una elevada concentración sérica de betacarotenos.
El término carotinemia hace referencia a una condición médica consistente en la coloración anaranjado- amarillenta de la piel debida a una elevada concentración sérica de betacarotenos. La causa más frecuente es la ingesta excesiva de alimentos ricos en betacarotenos. Estos son, sobre todo, frutas y verduras de colores amarillo, naranja, rojo y verde, aunque también se encuentran en otros alimentos como la leche (incluida la leche materna).
La causa más frecuente es la ingesta excesiva de alimentos ricos en betacarotenos. Estos son, sobre todo, frutas y verduras de colores amarillo, naranja, rojo y verde, aunque también se encuentran en otros alimentos como la leche (incluida la leche materna). Otras posibles etiologías son: hipotiroidismo, diabetes mellitus, hiperlipidemias, anorexia nerviosa, errores congénitos del metabolismo y enfermedades renales y hepáticas.
Otras posibles etiologías son: hipotiroidismo, diabetes mellitus, hiperlipidemias, anorexia nerviosa, errores congénitos del metabolismo y enfermedades renales y hepáticas. El diagnóstico es clínico, cobrando especial importancia la realización de una encuesta dietética detallada.
El diagnóstico es clínico, cobrando especial importancia la realización de una encuesta dietética detallada. En la exploración física, se objetiva coloración anaranjada-amarillenta, sobre todo en palmas y plantas, punta de la nariz, frente y pliegues nasolabiales.
En la exploración física, se objetiva coloración anaranjada-amarillenta, sobre todo en palmas y plantas, punta de la nariz, frente y pliegues nasolabiales. Solo deben realizarse pruebas complementarias en aquellos casos donde se tenga una alta sospecha de otra etiología diferente a la dietética.
Solo deben realizarse pruebas complementarias en aquellos casos donde se tenga una alta sospecha de otra etiología diferente a la dietética. El principal diagnóstico diferencial debe plantearse con la ictericia, distinguiéndose de esta por la falta de coloración en esclerótica y mucosa oral (aunque sí en paladar) y por la intensificación de la coloración con luz artificial.
El principal diagnóstico diferencial debe plantearse con la ictericia, distinguiéndose de esta por la falta de coloración en esclerótica y mucosa oral (aunque sí en paladar) y por la intensificación de la coloración con luz artificial. No se asocia a hipervitaminosis A, ya que la cantidad de betacarotenos que se transforma diariamente en vitamina A es reducida.
No se asocia a hipervitaminosis A, ya que la cantidad de betacarotenos que se transforma diariamente en vitamina A es reducida. La carotinemia de origen dietético es benigna y no precisa de tratamiento farmacológico.
La carotinemia de origen dietético es benigna y no precisa de tratamiento farmacológico. Si se desea eliminar la coloración anaranjado- amarillenta de la piel, debe disminuirse la cantidad de alimentos ricos en betacarotenos, consiguiendo la normalización de la piel en el plazo de varias semanas-meses.
Si se desea eliminar la coloración anaranjado- amarillenta de la piel, debe disminuirse la cantidad de alimentos ricos en betacarotenos, consiguiendo la normalización de la piel en el plazo de varias semanas-meses.