Hipertensión arterial sistémica
Introducción
El término de hipertensión arterial es cada vez más común en nuestra sociedad, así como su identificación como factor de riesgo cardiovascular; sin embargo, no todo el mundo traslada esta preocupación a los niños. La prevención de las enfermedades cardiovasculares no queda limitada a la edad adulta, sino que debe iniciarse en la edad pediátrica.
El término de hipertensión arterial sistémica (HTA) es cada vez más común en nuestra sociedad, así como su identificación como factor de riesgo cardiovascular; sin embargo, no todo el mundo traslada esta preocupación a los niños. Las guías elaboradas en conjunto de la Sociedad Europea de Hipertensión (ESH) y de la Sociedad Europea de Cardiología (ESC) para el manejo de la HTA, publicadas en 2003 y 2007, no incluyen, lamentablemente, ninguna sección dedicada a la HTA en niños y adolescentes(1). En 2009, se publican las primeras recomendaciones de la ESH para el manejo de la HTA en niños y adolescentes y, en 2016, se actualizan las nuevas guías clínicas(2).
La prevención de las enfermedades cardiovasculares no queda limitada a la edad adulta, sino que debe iniciarse en la edad pediátrica. La HTA es la mayor causa de morbimortalidad en muchos países, por sus consecuencias sobre el sistema cardiovascular y los accidentes cerebrovasculares(3). En los últimos años, se han desarrollado varios métodos computarizados para la estimación del riesgo cardiovascular total. El modelo Systematic COronary Risk Evaluation (SCORE) se ha desarrollado basándose en grandes cohortes de estudios europeos. Este modelo permite estimar el riesgo de muerte por enfermedad cardiovascular, no solamente por enfermedad coronaria, en 10 años, según: edad, sexo, hábitos de consumo de tabaco, colesterol total y presión arterial sistólica. La versión electrónica e interactiva del SCORE, llamada Heart-SCOREestá disponible en: www.heartscore.org(4).
Se ha demostrado que la HTA en la infancia es un factor de riesgo independiente para la hipertensión en la edad adulta y está asociada con marcadores precoces de enfermedad cardiovascular (hipertrofia ventricular izquierda, espesor de la íntima-media, complianza arterial, ateroesclerosis y disfunción diastólica)(5).
La HTA en niños, supone un reto diagnóstico para el pediatra de Atención Primaria, por el reconocimiento clínico difícil (niños asintomáticos) y por la amplia variabilidad de los valores normales de tensión arterial según edad, sexo y talla, que hace complicado recordar y precisar de tablas para consultar. El resultado final es un infradiagnóstico de la HTA en niños, dejando pasar un tiempo de evolución importante en la repercusión clínica (daño en tejidos y órganos), que determina el pronóstico en la edad adulta. La OMS considera lesión de órgano diana de la HTA a cinco regiones: cardiaca (hipertrofia ventricular izquierda, insuficiencia cardiaca), renal (necrosis arteriolar, insuficiencia renal), cerebral (hemorragia cerebral, encefalopatía hipertensiva), vascular (isquemia) y retina (retinopatía hipertensiva)(2).
El primer paso para el pediatra en Atención Primaria es pensar en la HTA en niños; en segundo lugar, identificarla en los controles de salud, así como sus factores de riesgo (familia con HTA, obesidad, enfermedades asociadas a HTA secundaria); y, en tercer lugar, una vez diagnosticada, saber la actitud a seguir. La Academia Americana de Pediatría recomienda que la HTA debe ser buscada activamente por el pediatra en Atención Primaria a partir de los 3 años de edad en todas las revisiones de salud del niño. En pacientes de riesgo (cardiopatía, nefropatía, síndrome de apnea-hipopnea del sueño, neurofibromatosis, esclerosis tuberosa…), la vigilancia deberá ser más estricta y precoz(6). Especial interés se debe prestar a niños y adolescentes con antecedente de prematuridad y su mayor riesgo de desarrollar HTA(7).
Epidemiología
Los datos epidemiológicos en población pediátrica son muy variables según estudios en diferentes países, la prevalencia global de HTA en Pediatría se estima en un 2% y la incidencia en 0,4-0,6/100 pacientes/año.
En términos generales, la prevalencia de la HTA en la población adulta se sitúa alrededor de un 30-45% de la población general, con un marcado aumento a edades más avanzadas(1). En España, el Estudio ERICE, publicado en 2008, estima la prevalencia y la distribución geográfica de los principales factores de riesgo cardiovascular en la población española adulta e investiga la existencia de diferencias geográficas. Dicho estudio confirma una alta prevalencia de HTA en la población española, con un 38%. Este aumento de la prevalencia de la HTA se acentúa en edades avanzadas, llegando hasta un 74% en mujeres y un 66% en varones. Mientras la presión arterial diastólica aumenta hasta la mediana edad y luego empieza a declinar, la presión arterial sistólica sigue incrementándose con la edad y adopta un patrón lineal. El incremento de la presión arterial sistólica con la edad es más marcado en las mujeres, sobre todo, a partir de los 65 años, lo que explica la mayor prevalencia de HTA sistólica aislada en estas que en los varones ancianos(8).
La prevalencia global de HTA en Pediatría se estima en un 2%; sin embargo, los datos en población pediátrica son muy variables según estudios en países diferentes, existen diferentes aspectos que dificultan su conocimiento real en los estudios realizados (tamaño muestral, edades de la población estudiada, método de medición de la presión arterial…). Uno de los trabajos más significativos es el de Kit et al, usando datos de National Health and Nutrition Examination Survey (NHANES) en Estados Unidos, que detectó una prevalencia global de HTA de 1,7% y de pre-HTA de 6,9%(9).
En Europa, las prevalencias varían según diferentes estudios de diferentes países, Suiza: 2,2%, Hungría: 2,5%, Polonia: 4,9%, Turquía: 9% y Portugal: 13%
En España, las publicaciones son escasas, el estudio realizado por Aguirre et al, en población pediátrica y área rural, muestra una prevalencia global de HTA del 4,4% y, como dato significativo, de esa población de niños hipertensos, el 57,14% eran obesos (índice de masa corporal > percentil 97) y el 28,57% presentaban sobrepeso (IMC entre percentil 85-95); es decir, solo el 14,29% de los niños hipertensos tenía normopeso(10).
Diferentes estudios internacionales muestran la relación sobrepeso-hipertensión. La obesidad es un factor de riesgo para la HTA (riesgo relativo de 3,26) y la prevalencia de HTA en niños y adolescentes con sobrepeso asciende a un rango de 27-47%.
El mecanismo mediante el cual la obesidad puede provocar HTA está dado por acumulación de grasa visceral, la cual se asocia con insulino-resistencia y aumento de la actividad del sistema renina-angiotensina. El hiperinsulinismo secundario a la insulino-resistencia aumenta la reabsorción de sodio a nivel renal y aumenta el tono simpático. Además, estudios experimentales han evaluado que la leptina también aumentaría el tono simpático. Todos estos factores influyen en la elevación de la presión arterial.
Datos procedentes del Estudio Español de Crecimiento 2008 muestran que la tasa de sobrepeso en la población de niños, adolescentes y adultos jóvenes de 4 a 24 años se ha incrementado aproximadamente un 10% en los últimos 20 años; estimándose que, en la actualidad, el 20% de los niños y adolescentes jóvenes varones y el 15% de las niñas y adolescentes jóvenes mujeres presentan sobrepeso, y que el 5% de esta población y en este rango de edad presentan obesidad de acuerdo con los criterios internacionales definidos por Cole en 2000(11).
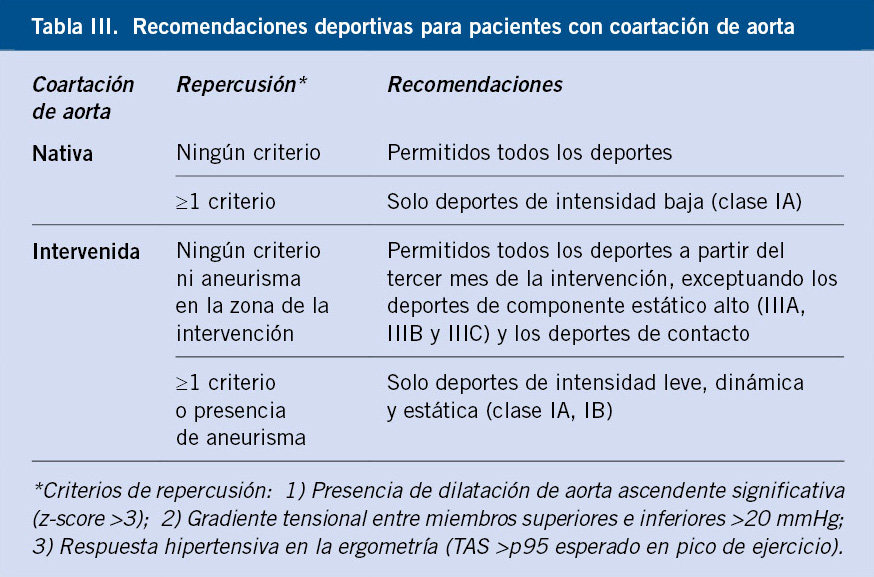
En referencia a la incidencia de HTA, estudios de seguimiento en población general entre 10 y 19 años, presentan una progresión de normotensión a HTA de 0,4-0,6/100 pacientes/año. Las tasas de incidencia son superiores en grupos de riesgo, siendo de 4/100 pacientes/año en adolescentes con diabetes mellitus tipo 2, y 1,3/100 pacientes/año en pacientes intervenidos correctamente de coartación de aorta. Con la monitorización ambulatoria de la presión arterial (MAPA), se ha estimado una incidencia de HTA enmascarada de 7/100 pacientes/año(2).
Definición y conceptos importantes
Los valores de normalidad de la presión arterial están condicionados por la edad cronológica, el sexo y la talla.
La presión arterial (PA) varía con la edad, aumentando con esta. Estos cambios de la PA tienen su base en el crecimiento y desarrollo corporal; por lo tanto, los valores de normalidad deben tener en cuenta, además de la edad y el sexo, el tamaño corporal, en concreto, la talla. El tamaño corporal se debe indicar con la talla y no con el peso, pues aunque la PA aumenta con toda claridad con la obesidad, su relación con el peso es de tipo causal.
En condiciones normales, la presión arterial sistólica aumenta de forma rápida durante el primer mes de vida, enlenteciéndose este aumento hasta los cinco años. Entre esta edad y el inicio de la pubertad, la presión arterial sistólica y diastólica aumentan a un ritmo anual de 1-2 mmHg y 0,5-1 mmHg, respectivamente, con mínimas diferencias entre varones y mujeres. Entre los 13 y los 18 años, la presión arterial vuelve a presentar un incremento en sus valores, siendo este más evidente en los varones que en las mujeres, que llegan a alcanzar cifras de presión arterial más elevadas, como consecuencia de su desarrollo puberal más tardío y mayor masa corporal. Por este motivo, los valores de normalidad tienen que considerar conjuntamente la edad, sexo y tamaño corporal, siendo la talla el indicador de maduración que mejor correlaciona con la edad esquelética.
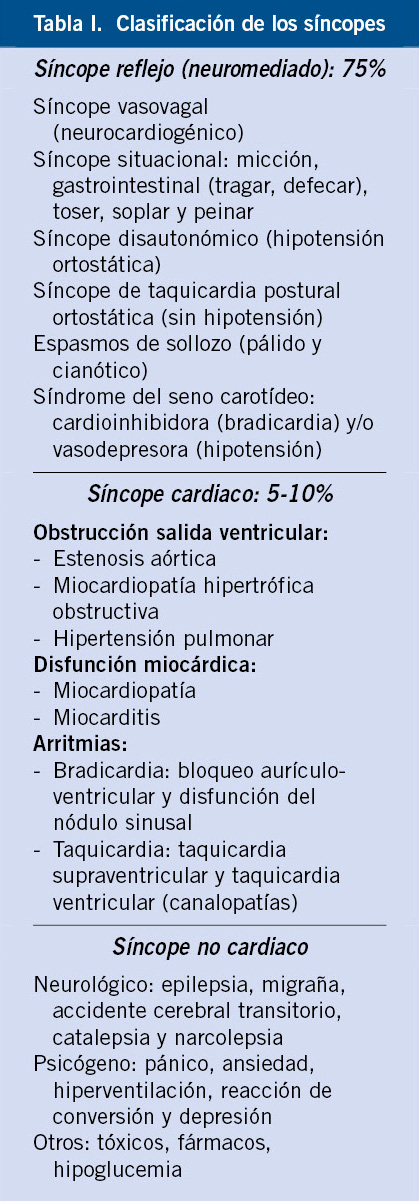
Por lo tanto, la definición más aceptada de HTA en Pediatría es la propuesta por la Academia Americana de Pediatría, en el año 2004. Se define HTA en niños y adolescentes cuando los valores de PA sistólica y/o diastólica (PAS y/o PAD) se encuentran de forma repetida, en tres o más ocasiones separadas, igual o por encima del percentil 95 específico para la edad, el sexo y la talla, según las tablas de normalización.
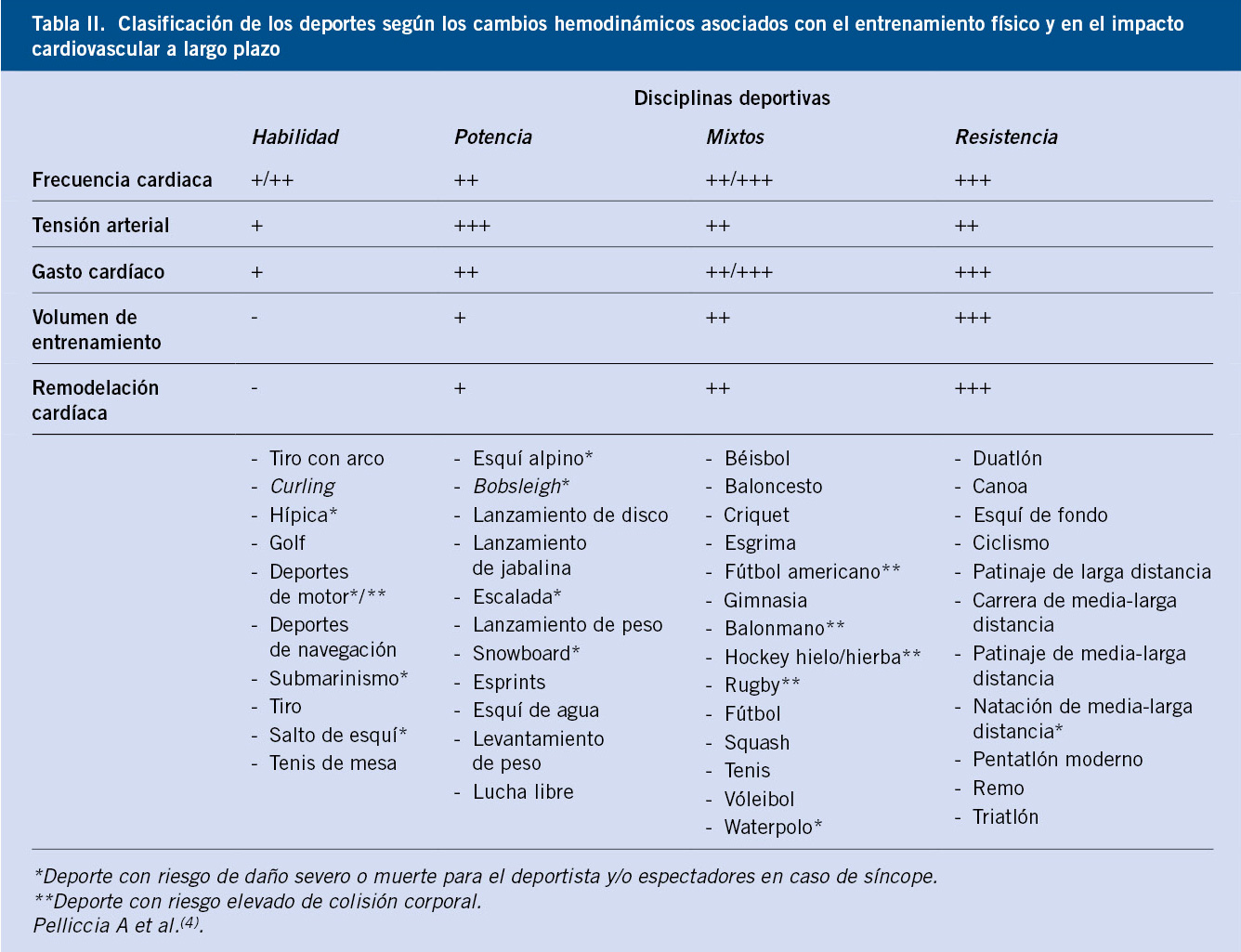
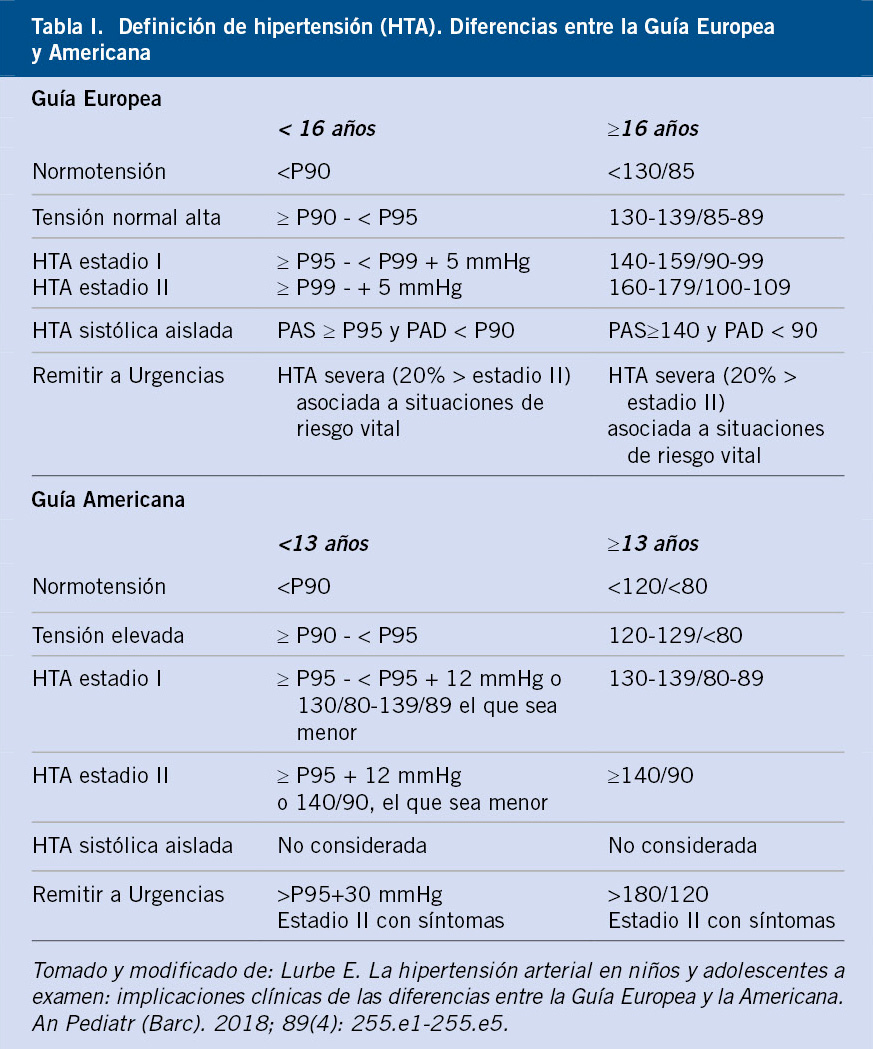
Los valores de normalidad de la PA más aceptados internacionalmente son los de la Task Force for Blood Pressure in Children publicados en 1987, que se correlacionan con la edad cronológica, el sexo y el percentil de talla para cada caso en particular, y validados por la 4ª Comunicación de la Academia Americana de Pediatría en 2004 (National High Blood Pressure Education Program Working Group on High Blood Pressure in Children and Adolescents) (Tablas I y II)(8).

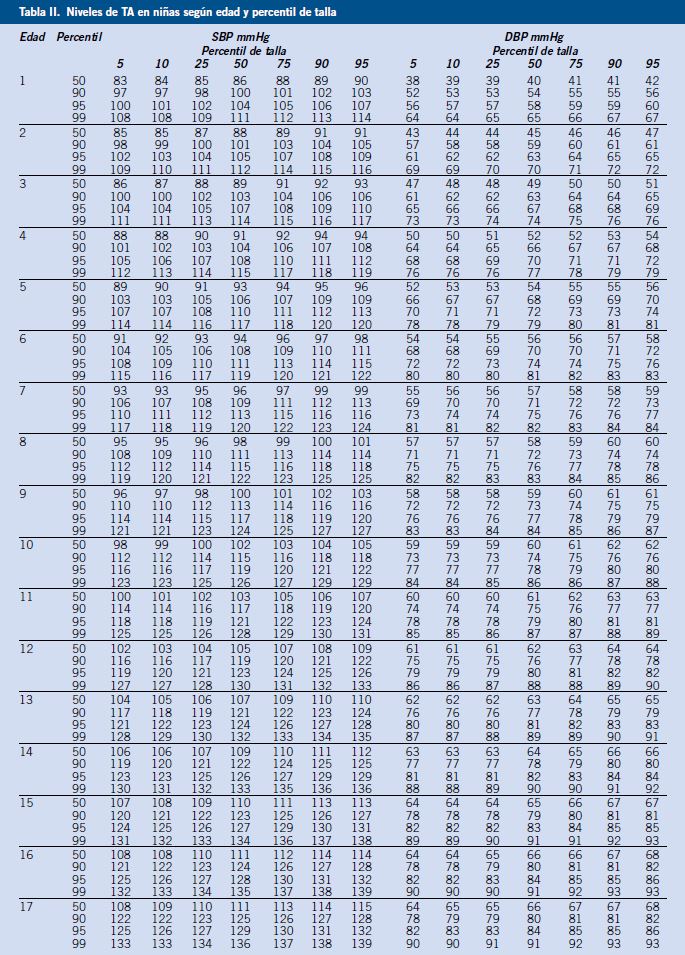
Clasificación de los valores de PA y conceptos importantes:
1. PA normal (normotensión): PAS y/o PAD < percentil p90.
2. PA alta-normal (antes llamada prehipertensión): PAS y/o PAD valor entre percentiles p90 y p95, o si >120/80 mmHg, incluso si es < p90 en adolescentes.
3. HTA (hipertensión): PAS y/o PAD ≥ percentil p95. Estadios HTA:
– HTA estadio 1: PAS y/o PAD > percentil p95 y hasta 5 mmHg por encima de percentil p99. En adolescentes > 140/90 mmHg.
– HTA estadio 2: PAS y/o PAD ≥ 5 mmHg por encima del percentil p99.
4. Crisis HTA: un valor 30% superior al percentil 95, o aunque el valor no sea >30%, si su aparición ha sido de forma rápida y brusca, o si se acompaña de síntomas.
5. Urgencia hipertensiva: HTA estadio 2, sin objetivarse daño de órgano diana (requiere tratamiento oral/sublingual).
6. Emergencia hipertensiva: HTA estadio 2, si se objetiva daño de órgano diana, es un riesgo vital (requiere tratamiento intravenoso).
En la población infantil en nuestro país, el estudio RICARDIN permite conocer los percentiles p95 de PAS y PAD, para cada talla, en edades comprendidas entre 6 y 18 años. Pero para edades inferiores, no se dispone de datos en España, por lo que se deben tomar como referencia los estudios americanos, con el problema que esta extrapolación supone(12).
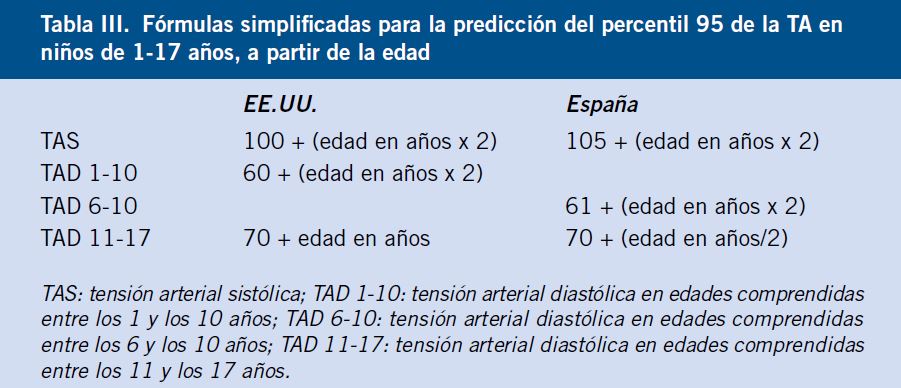
A efectos prácticos, existen unas fórmulas para la predicción del percentil p95 de la PA en niños a partir de una determinada edad. Los valores obtenidos son solo orientativos y con ellos no se puede tomar la decisión de iniciar un tratamiento antihipertensivo (Tabla III).
En la población adulta, los valores normales de presión arterial sistólica (PAS), presión arterial diastólica (PAD) y de HTA, siguiendo los criterios de la Sociedad Europea de Hipertensión (ESH) y de la Sociedad Europea de Cardiología (ESC), son los siguientes(1):
1. PA óptima: PAS <120 mmHg y PAD <80 mmHg.
2. PA normal: PAS 120-129 mmHg y/o PAD 80-84 mmHg.
3. PA normal-alta: PAS 130-139 mmHg y/o PAD 85-89 mmHg.
4. HTA de grado 1: PAS 140-159 mmHg y/o PAD 90-99 mmHg.
5. HTA de grado 2: PAS 160-179 mmHg y/o PAD 100-109 mmHg.
6. HTA de grado 3: PAS ≥180 mmHg y/o PAD >110 mmHg.
7. Hipertensión sistólica aislada: PAS ≥140 mmHg y PAD ≤90 mmHg.
Medición de la presión arterial
El método de elección para la medición de presión arterial es el auscultatorio y se debe seleccionar correctamente el tamaño adecuado del manguito. La monitorización ambulatoria de la presión arterial (MAPA) es clave para la confirmación del diagnóstico.
La medida de la PA es una de las exploraciones médicas más repetidas e importantes y, pese a su aparente sencillez, es una de las que se realiza de forma menos fiable y con escaso cumplimiento de las recomendaciones. Las dificultades para medir la PA en un sujeto, especialmente en niños, y que hacen que resulte poco reproducible, derivan de tres aspectos:
1. Variabilidad: la PA se modifica por múltiples situaciones propias y ajenas al paciente, desde la temperatura ambiente, hasta el estado físico y emocional.
2. Limitaciones: la precisión de la medición de la PA depende del observador, del lugar de realización, de la técnica empleada (auscultatorio, oscilometría), de la arteria seleccionada…
3. Iatrogenia: si la mayoría de los sujetos experimentan una reacción de alerta a la medición de la PA y que puede alterarla (“hipertensión de bata blanca”), en los niños esta modificación iatrogénica es aún más evidente. La determinación de la PA sería más real, si esta se realiza no solo en la consulta del médico (un entorno artificial), sino también durante las actividades diarias habituales (un entorno más natural).
Métodos de medición de la presión arterial
• Método auscultatorio: precisa esfingomanometro de presión y estetoscopio, es el método de elección.
• Método oscilométrico (“Dinamap”): método más sencillo, sobre todo, en lactantes; sin embargo, precisa calibración y que esté homologado. Toda medición anómala de la PA por este método, precisa comprobación por método auscultatorio. La medición de la PA por oscilómetro es superior a la realizada por esfingomanómetro.
• Monitorización ambulatoria de presión arterial (MAPA): este método permite una medición de la PA en el medio habitual y en las condiciones cotidianas del individuo, su uso en Pediatría es todavía limitado, pero cada vez resulta más valiosa para el correcto diagnóstico y el tratamiento de la HTA.
Técnica de medición de la presión arterial por auscultación
1. Condiciones del paciente: esperar 3-5 minutos para que el paciente esté tranquilo, con la máxima relajación física y emocional posible.
2. Posición del paciente: brazo derecho, libre de ropa, en decúbito supino o sentado con el manguito a la altura del corazón.
3. Equipo: esfingomanómetro de mercurio, manguitos (diferentes tamaños) y estetoscopio en correctas condiciones.
4. Manguito adecuado: la longitud del manguito debe cubrir el 80-100% del perímetro del brazo, y la anchura del manguito el 40-50% del perímetro del brazo. Se deben dejar libres la fosa antecubital y el hueco axilar (Tabla IV).

5. El manguito se hincha lentamente hasta una presión 20-30 mmHg superior a la presión arterial sistólica esperada o hasta que se deje de palpar el latido de la arteria radial.
6. Colocar la membrana del estetoscopio en la fosa antecubital, no debajo del manguito, y desinflar lentamente a un ritmo de 2-3 mmHg/segundo. La PAS se corresponde con el inicio del latido arterial (fase I de Korotkoff) y la PAD con la desaparición del latido (fase V de Korotkoff).
Recordad que, en la primera medición, la PA suele ser más alta que la verdadera PA, se recomienda realizar la medición 3 veces y obtener el valor medio.
La monitorización ambulatoria de la presión arterial (MAPA)
La monitorización ambulatoria de la presión arterial (MAPA) es una técnica de medición de la PA mediante un aparato automático portátil, que realiza numerosas mediciones (una medición cada 20 minutos durante el día, y cada 30 minutos por la noche) en el medio habitual y en las condiciones cotidianas del individuo. Esta técnica ha sido introducida para el estudio y valoración de la HTA en adultos durante la década de los años 1980; sin embargo, su incorporación en Pediatría ha sido más reciente, tras adaptar, comprobar su buena tolerancia y disponer de valores de referencia. Aunque existen estudios de MAPA en todas las edades, incluido lactantes, lo habitual de forma práctica es realizarla a partir de los 4 o 5 años.
El aparato utilizado consta de varios componentes (el manguito de presión adecuado, la grabadora de memoria y el soporte informático) que deben estar homologados y validados según protocolos internacionales (www.dableducational.org)(13).
La medición de la PA se obtiene promediando los valores obtenidos durante las 24 h o en aquellos periodos que puedan tener mayor significado fisiológico, como los periodos de actividad y su comportamiento durante el sueño. Generalmente, la división de período diurno engloba las medidas realizadas entre las 9,00 y las 20,00 h, y las nocturnas entre las 24,00 y las 6,00 h, desechando así los períodos del dormir y el despertar (de 20,00 a 24,00 h y de 6,00 a 9,00 h) por una mayor variabilidad.
En la práctica clínica, se calculan las siguientes medidas en la MAPA:
• Media aritmética de la PA sistólica (PAS) y diastólica (PAD) de las 24 h y de los períodos diurno (actividad) y nocturno (descanso).
• Índice de carga sistólica y diastólica: porcentaje de lecturas por encima de los valores de referencia (percentil 95 de Soergel). Respecto a la carga, en adultos tiene una clara asociación con la función cardíaca. En niños, el valor es arbitrario, considerando mayor riesgo cardiovascular las cargas por encima del 25%. Parece claro que por encima del 50% hay mayor prevalencia de hipertrofia de ventrículo izquierdo con significación estadística.
• Ritmo circadiano: porcentaje de descenso nocturno de la PA. Se calcula el descenso nocturno mediante la siguiente fórmula: (media sistólica día – media sistólica noche)/media sistólica día × 100; igual con diastólica. Existe un descenso nocturno (ritmo circadiano) de la PA que de forma arbitraria se establece en un 10%. Con esto, se distingue al paciente dipper (paciente con descenso tensional en período de sueño igual o superior al 10% para la presión arterial sistólica y/o para la diastólica) del nondipper (paciente con descenso tensional en período de sueño inferior al 10 % para la presión arterial sistólica y/o para la diastólica). En adultos nondippers existe mayor riesgo de daño de órganos diana, con aumento de la masa ventricular y morbilidad cardiovascular, datos que, aunque con menos experiencia, parecen extrapolables a la población pediátrica. La HTA nocturna aislada o la falta de descenso nocturno son anomalías frecuentes: en la HTA secundaria, en la insuficiencia renal crónica, en la nefropatía IgA, en pacientes diabéticos, en la apnea obstructiva del sueño y en el crecimiento intrauterino retardado.
Las ventajas del uso de MAPA son las siguientes:
1. Confirma el diagnóstico de HTA y analiza su severidad.
2. Permite identificar los casos de “HTA de bata blanca”: presencia de una PA casual elevada en presencia del profesional sanitario, pero con MAPA normal (falsos positivos de HTA).
3. Permite identificar los casos de “HTA enmascarada”: presencia de una PA casual normal, pero con MAPA alterada (falsos negativos de HTA). La HTA enmascarada se asocia a mayor frecuencia cardíaca, mayor índice de masa corporal y a la existencia de HTA en los padres. Al igual que en adultos, los niños con “HTA enmascarada” presentan hipertrofia de ventrículo izquierdo, con un índice de masa ventricular izquierda elevada, y un riesgo de morbilidad cardiovascular similar a los niños con HTA confirmada. Por tanto, los niños con “HTA enmascarada” deben tomarse como HTA con riesgo de daño de órganos diana y, por tanto, susceptible de iniciar tratamiento.
Etiología
En Pediatría, la HTA secundaria es más frecuente que la HTA esencial, especialmente cuanto menor sea la edad del niño y cuanto mayor sean sus valores de PA. No obstante, la HTA esencial puede estar infradiagnosticada en niños.
Desde el punto de vista etiológico, la HTA se divide en HTA primaria o esencial e HTA secundaria. En Pediatría, la HTA secundaria es más frecuente; no obstante, la HTA esencial puede estar infradiagnosticada en niños y su prevalencia ser mayor, asociada en parte a la “epidemia de obesidad pediátrica” de nuestra sociedad.
1. HTA primaria o esencial: es la más frecuente en el adulto (90%) y adolescente (80%). Existen fuertes evidencias de que la HTA esencial del adulto tiene sus orígenes en la infancia, con una base genética y determinados factores ambientales. La HTA primaria a menudo está en relación con otros factores de riesgo cardiovascular que se interrelacionan entre sí y que se agrupan en el síndrome metabólico: hipertrigliceridemia, descenso de las lipoproteínas de alta densidad (HDL), resistencia a la insulina, hiperinsulinismo, obesidad truncal e hipertensión arterial(11).
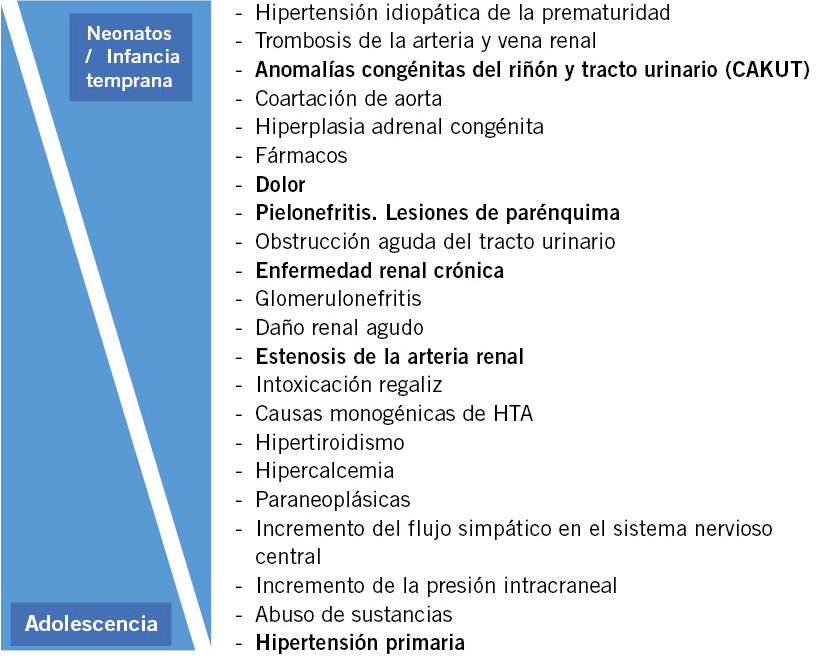
2. HTA secundaria: es la más frecuente en Pediatría, especialmente cuanto menor sea la edad del niño y cuanto mayor sea el valor de la medición de la PA. Las causas de HTA pueden ser: renal y/o renovascular (75-80%), cardiovascular (5%) o endocrinológica (5%), y su incidencia depende de la edad (Tabla V).

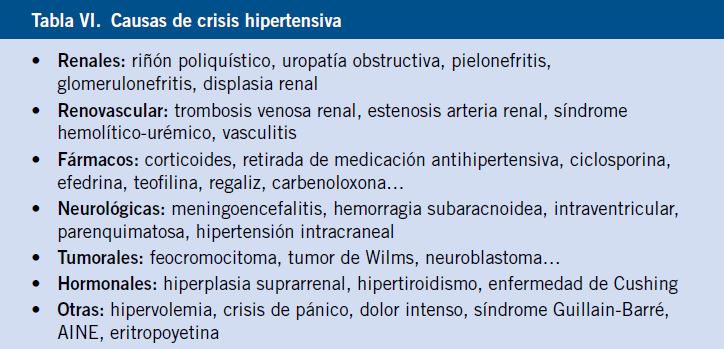
No obstante, recientes estudios resaltan la importancia de causas pulmonares en la etiología de la HTA secundaria, tales como la displasia broncopulmonar y el síndrome de apnea del sueño(14, 15). En las crisis de HTA, la etiología también puede ser variada: renovascular, neurológica, tumoral, hormonal, farmacológica… (Tabla VI).
Valoración del daño orgánico (órganos diana)
En todo niño con HTA, deben ser valorados los posibles daños sobre órganos diana (cardiovascular, renal, neurológico, oftalmológico).
Es importante investigar la lesión de órganos que potencialmente puede ocurrir en la HTA. La OMS considera lesión de órgano diana de la HTA a cinco regiones: cardiaca (hipertrofia ventricular izquierda, insuficiencia cardiaca, cardiopatía isquémica), renal (necrosis arteriolar, insuficiencia renal), cerebral (hemorragia cerebral, infarto cerebral, encefalopatía hipertensiva), vascular (isquemia, disección de aorta) y retina (retinopatía hipertensiva).
Corazón
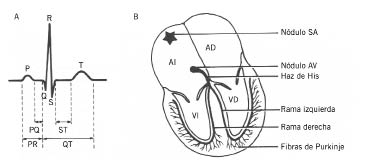
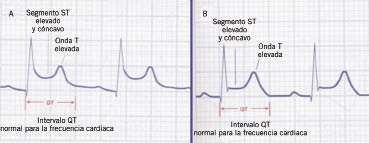
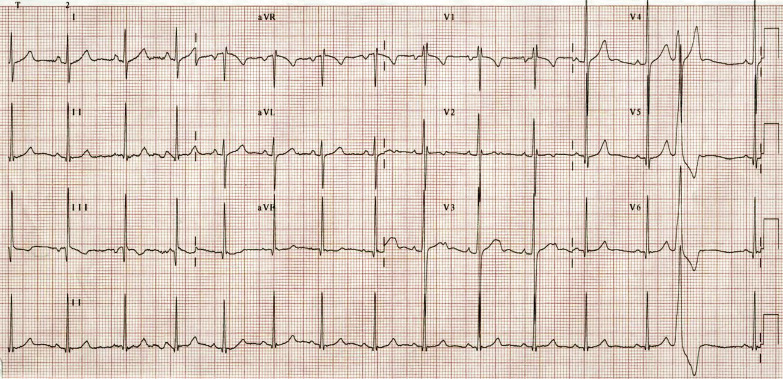
El electrocardiograma (ECG) es una prueba complementaria importante para la evaluación inicial y de la evolución de pacientes hipertensos. El ECG de superficie no es una prueba exclusiva de la medicina hospitalaria, también está disponible en los centros de salud. El ECG en Pediatría tiene unas características propias, que puede mostrar registros patológicos que realmente no lo son, como la presencia de onda T negativa en V1, el bloqueo incompleto de rama derecha, el patrón de repolarización precoz o el ECG del deportista. El reto del pediatra es saber realizar una interpretación básica del ECG y reconocer un registro normal de uno patológico.
El ECG en la HTA detecta la hipertrofia del ventrículo izquierdo y, además, permite valorar la presencia de isquemia, trastornos de la conducción y arritmias.
Crecimiento ventrículo izquierdo:
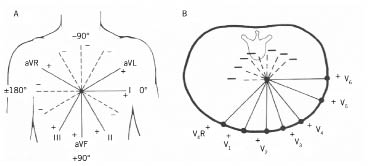
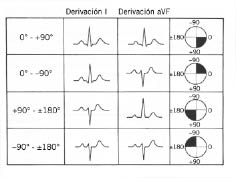
1. Desviación del eje del QRS a la izquierda (eje QRS mayor de -30º).
2. Aumento del voltaje de onda R en V5-V6 con onda S profunda en V1-V2.
3. Índice de Sokolow (onda S en V1 + onda R en V6) mayor de 35 mm.
4. Índice de Lewis (onda R en DI + onda S en DIII – onda R en DIII – onda S en DI) mayor de 17 mm.
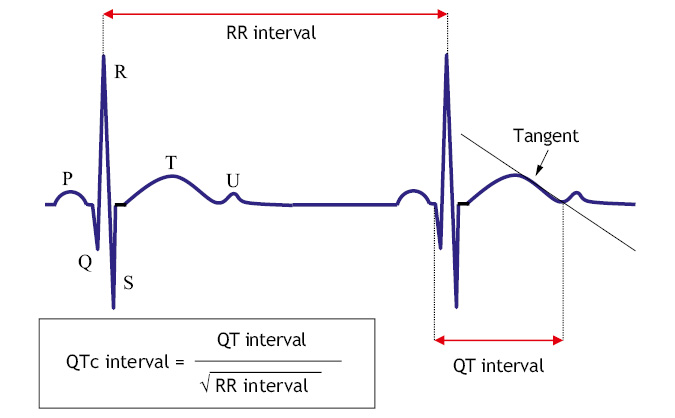
5. Retardo del tiempo de deflexión intrinsecoide en V5-6 (intervalo entre vértice de onda q, hasta pico de onda R) mayor de 0,045 s.
6. Desviación del plano de transición del QRS a la derecha en precordiales.
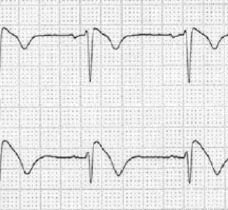
7. Signos de sobrecarga sistólica del ventrículo izquierdo (ondas T negativas en V5-6).
La ecocardiografía es sin duda más sensible que el ECG para identificar y cuantificar la hipertrofia ventricular izquierda, ayuda a clasificar con mayor precisión el riesgo global del paciente hipertenso y sirve de guía para el tratamiento. En la ecocardiografía, se debe valorar la masa del ventrículo izquierdo, el grosor de la pared y la función diastólica, mediante el Doppler en el flujo de la válvula mitral.
Vasos sanguíneos
El endotelio vascular regula la homeostasis local y el tono vascular. El óxido nítrico es una de las moléculas sintetizadas por el endotelio con función ateroprotectora (vasodilatador, antiagregante plaquetario, antioxidante, inhibidor de la proliferación de las células musculares lisas e inhibidor de la expresión de las moléculas de adhesión).
La disfunción endotelial predispone a la inflamación, la vasoconstricción y el incremento de la permeabilidad vascular, y se considera en la actualidad una de las primeras manifestaciones de la enfermedad vascular y la arteriosclerosis.
Los primeros cambios de la disfunción endotelial en niños con HTA pueden ser valorados por ecocardiografía de alta resolución con la medición del grosor de la íntima media de la arteria carótida.
La disfunción endotelial también puede ser valorada por la disminución de la vasodilatación, mediante ecografía vascular de alta frecuencia. Con esta técnica no invasiva, se valora la vasodilatación en la arteria braquial mediada por flujo tras la oclusión por presión con manguito de esfingomanómetro durante 5 minutos.
Riñón
El daño renal puede ser valorado por la disminución del filtrado glomerular (fórmula de Schwartz) y el aumento de la excreción urinaria de albumina (cociente albumina/creatinina en orina > 30 mg/g) o proteinuria (cociente proteínas/creatinina en orina > 300 mg/g, proteinuria en orina 24 h > 200 mg/m2/día)(2). La microalbuminuria se asocia con la progresión de la nefropatía y un mayor riesgo cardiovascular y, su asociación a la elevación de la proteína C reactiva se correlaciona con un mayor riesgo de hipertrofia del ventrículo izquierdo en niños con HTA esencial.
Cerebro
La encefalopatía hipertensiva es un síndrome de HTA severa con disfunción cerebral y daño neurológico. La clínica se caracteriza por: cefalea global de aparición temprana, náuseas, vómitos en proyectil, alteraciones visuales, confusión mental y convulsiones. Es importante la valoración por neurología pediátrica y la realización de electroencefalografía. En casos de emergencia, un TC y, ante la sospecha de pequeños infartos cerebrales silentes o microhemorragias, la resonancia magnética es el método de elección.
Recientemente, se ha descrito el síndrome de encefalopatía posterior reversible. Se trata de una entidad clínico-radiológica de presentación aguda en la HTA severa, asociado a: inmunosupresión, enfermedades hematológicas, vasculitis, conectivopatías o enfermedad renal. Su identificación y tratamiento de la HTA es clave para evitar el daño cerebral permanente(16).
Ojos
La HTA puede alterar el fondo de ojo y las lesiones vasculares se clasifican en cuatro grados (Keith, Wagener y Barker). En las fases tempranas de la HTA pueden presentar lesiones vasculares en pequeñas arterias (estrechamiento de las arteriolas). Sin embargo, en niños, es raro encontrar retinopatía grado 3 (hemorragias y exudados) o grado 4 (edema de papila), que son complicaciones de la HTA grave.
Clínica
La mayoría de los niños con HTA están asintomáticos o presentan una clínica anodina. El pediatra debe reconocer estos síntomas, especialmente los asociados a la crisis hipertensiva y afectación de órganos diana.
La mayoría de los niños con HTA están asintomáticos (más del 60%) o presentan una clínica anodina, poco específica, y cuando aparece, suele ser una HTA secundaria y/o grave (crisis hipertensiva)(17).
• Clínica general: epistaxis, cefalea, trastornos del sueño y fatiga crónica; en niños pequeños, fallo de medro, vómitos o irritabilidad.
• Crisis HTA: cefalea intensa, alteraciones visuales, mareos, náuseas, vómitos, crisis convulsiva, focalidad neurológica, parálisis nervio facial, dolor torácico, palpitaciones e insuficiencia cardiaca.
Es importante realizar una buena historia clínica del niño buscando factores de riesgo de HTA, tanto en los antecedentes personales (peso al nacimiento, prematuridad con canalización de vasos umbilicales, displasia broncopulmonar, apneas del sueño, infecciones urinarias…), como en los antecedentes familiares (HTA, obesidad, síndrome metabólico), revisar el tipo de alimentación (calorías, ingesta de sal) y el nivel de actividad física o sedentarismo. En los pacientes adolescentes hipertensos, no se debe olvidar investigar el posible consumo de tabaco, alcohol, drogas (cocaína, anfetaminas), esteroides anabolizantes, contraceptivos orales…(2)
Exploración física
La exploración física en niños con HTA suele ser normal, pero no debe dejar de realizarse para un correcto enfoque diagnóstico.
La exploración física en niños con HTA suele ser normal, pero no por ello se debe menospreciar una correcta exploración física. La exploración física debe comenzar con recoger correctamente los datos de peso, talla e índice de masa corporal, así como sus respectivos percentiles.
Una vez que se confirma la HTA, se debe tomar la PA en ambos brazos y en una pierna. Normalmente, la PA en piernas es 10-20 mmHg superior a la de la PA en brazos. Una disminución de la PA en piernas, respecto a la PA en brazos, debe hacernos sospechar una coartación de aorta, sobre todo si la diferencia es mayor de 20 mmHg.
Una correcta exploración física nos puede orientar en el enfoque diagnóstico de una HTA secundaria(2):
• Taquicardia: hipertiroidismo, feocromocitoma, neuroblastoma, HTA primaria.
• Pulsos femorales menores que pulsos braquiales: coartación de aorta.
• Retraso en el crecimiento: enfermedad renal crónica.
• Obesidad: HTA primaria, síndrome de Cushing, síndrome metabólico.
• Alteraciones faciales y cervicales: cara de luna llena (síndrome de Cushing), cara de duende (síndrome de Williams), cuello corto-pterigium coli-implantación baja del pelo (síndrome de Turner), bocio (hipertiroidismo).
• Alteraciones de la piel: palidez-enrojecimiento-sudoración (feocromocitoma), acné-hirsutismo-estrías (síndrome de Cushing), manchas café con leche (neurofibromatosis), adenomas sebáceos (esclerosis tuberosa), rash malar (lupus eritematoso sistémico).
• Ojos: cambios en la retina, estudio del fondo de ojo (HTA severa).
• ORL: hipertrofia adenoidea (apneas del sueño).
• Abdomen: masa (tumor de Wilms, neuroblastoma, feocromocitoma), palpación renal (enfermedad renal poliquística, displasia renal multiquística, hidronefrosis).
• Genitales: ambiguos o virilización (hiperplasia adrenal congénita).
• Extremidades: artritis (lupus eritematoso sistémico), debilidad muscular (hiperaldosteronismo, síndrome de Liddle), edemas (enfermedad renal, insuficiencia cardiaca).
• Auscultación: soplo interescapular (coartación de aorta), soplo epigástrico o en flancos (estenosis arteria renal), roce pericárdico (lupus eritematoso sistémico, uremia), taquicardia- ritmo de galope (insuficiencia cardiaca).
Pruebas complementarias
Las pruebas complementarias tienen el objetivo de identificar las posibles causas y, también, posibles complicaciones de la HTA.
Las pruebas complementarias tienen el objetivo de identificar las posibles causas y, también, posibles complicaciones de la HTA. Una vez confirmada la HTA en un niño, se debe iniciar un estudio para intentar identificar las posibles causas de la HTA, así como valorar las posibles complicaciones (daños en órganos diana).
• Análisis sanguíneo: hemograma, glucosa (si obesidad, insulina, hemoglobina A1C), perfil lipídico (triglicéridos, colesterol total, HDL, LDL), creatinina, urea, ácido úrico, sodio, potasio y calcio.
• Análisis de orina, sistemático de orina, proteinuria, microalbuminuria, iones en orina y urocultivo, según clínica.
• Ecografía-Doppler renal.
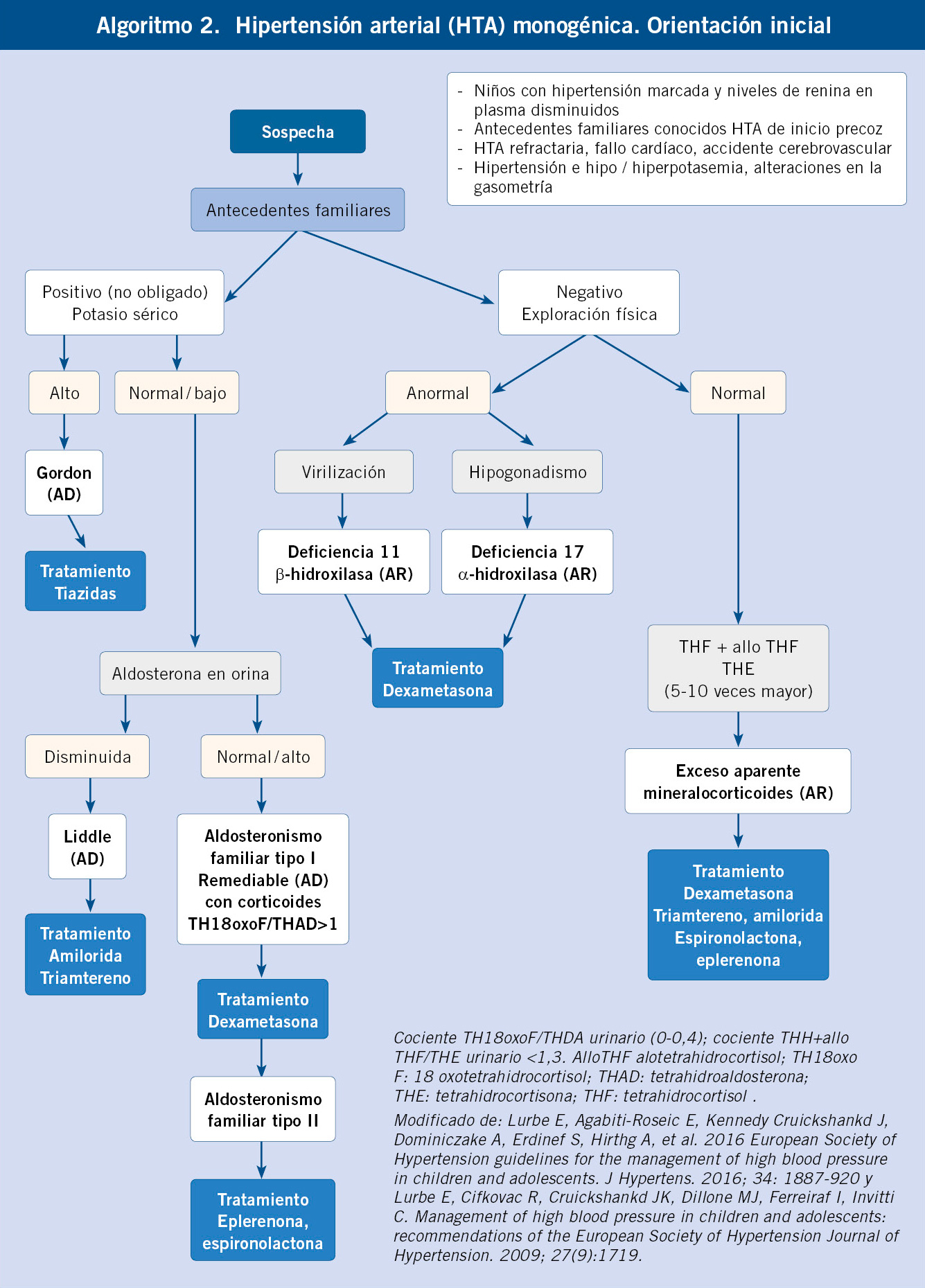
• Determinación de renina y aldosterona plasmática, y mejor calcular el índice aldosterona/renina (confirmar que sean las mismas unidades, si > 30, sospecha de hiperaldosteronismo primario), aunque esta prueba está muy condicionada por las circunstancias de la extracción y posible medicación y, en caso de resultado positivo, se precisan pruebas para confirmar (test de infusión salina, test de fludrocortisona, test de captopril)(18).
• Determinación de catecolaminas y metabolitos en sangre y orina.
• Determinación de esteroides en sangre y orina.
• Determinación de la función tiroidea: TSH, T4L.
• Estudios complementarios según caso clínico: isótopos, angio-TC, angio-RMN, arteriografía, DMSA, C3, ANA, ANCA, anti-DNA, biopsia renal, estudio apnea obstructiva del sueño…
• Estudios para valoración del daño en órganos diana: corazón (radiografía de tórax, ECG, ecocardiografía), retina (fondo de ojo) y cerebro (TAC-RMN cerebral).
Manejo y tratamiento
El tratamiento de la HTA en niños, se basa en tratamiento no farmacológico (hábitos saludables) y tratamiento farmacológico.
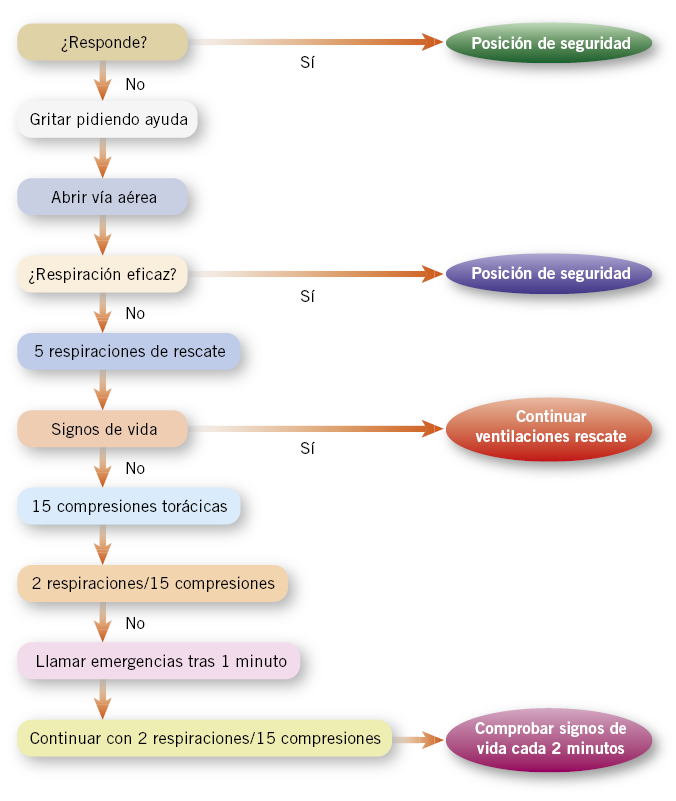
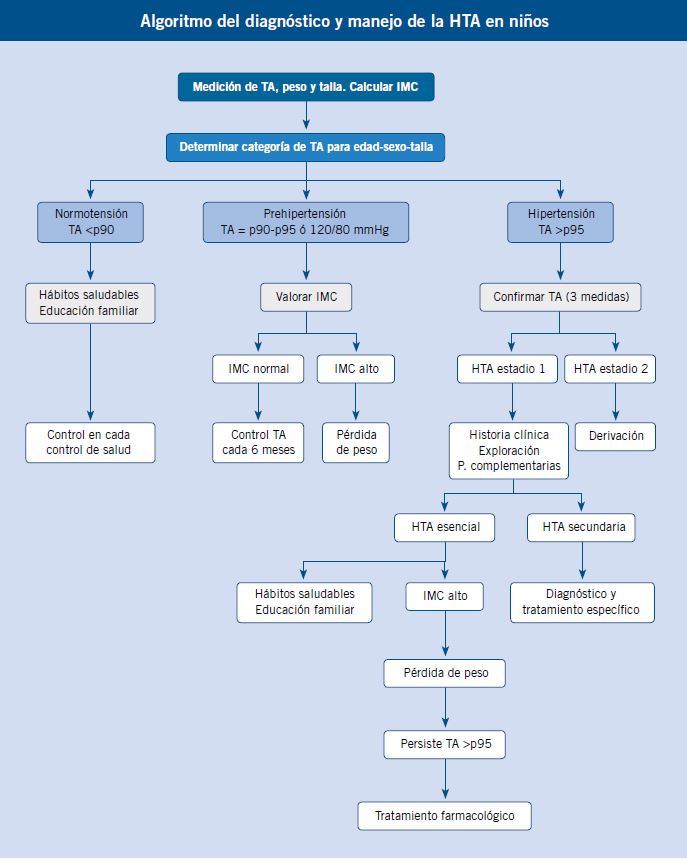
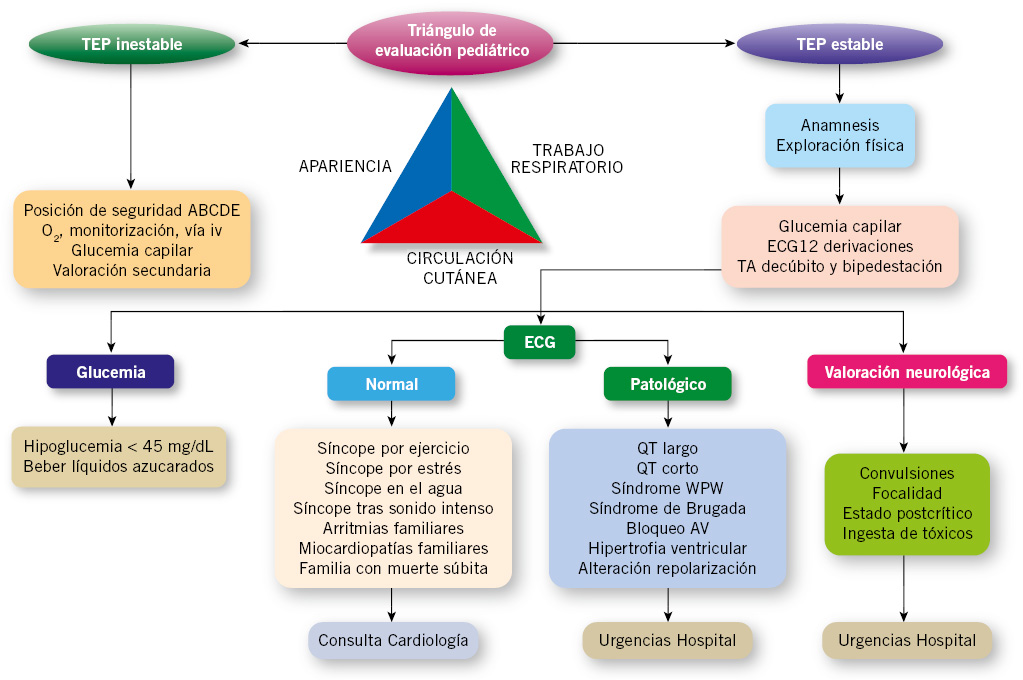
Una vez diagnosticado un niño con HTA, el siguiente paso es saber qué hacer con él (iniciar tratamiento o no, derivar a Pediatría hospitalaria, pruebas complementarias, controles periódicos…). En el algoritmo, se muestra, a modo orientativo, el manejo práctico que un pediatra de Atención Primaria puede seguir en un Centro de Salud.
El tratamiento de la HTA está basado en dos pilares básicos(5):
1. Tratamiento no farmacológico: estilos de vida saludables.
2. Tratamiento farmacológico.
Tratamiento no farmacológico
La prevención y promoción de la salud es una doctrina en Pediatría, especialmente en el ámbito extrahospitalario. Sin embargo, la prevención de la HTA, una patología prevalente en la edad adulta, a partir de la atención al niño, se considera una cuestión de futuro y, por lo tanto, lejana y poco atractiva en una sociedad que busca resultados inmediatos. Los hábitos saludables que se deben aconsejar para la prevención y tratamiento de la HTA en niños, son:
• Pérdida de peso en caso de obesidad: la obesidad es uno de los factores más determinantes de la elevación de los valores de PA. La pérdida de peso no solo disminuye los valores de PA, sino que también, disminuye la sensibilidad de la PA a la sal (disminuye la hiperactividad adrenérgica) y otros factores de riesgo cardiovascular (disminuye la hiperinsulinemia, la resistencia a la insulina y la dislipidemia).
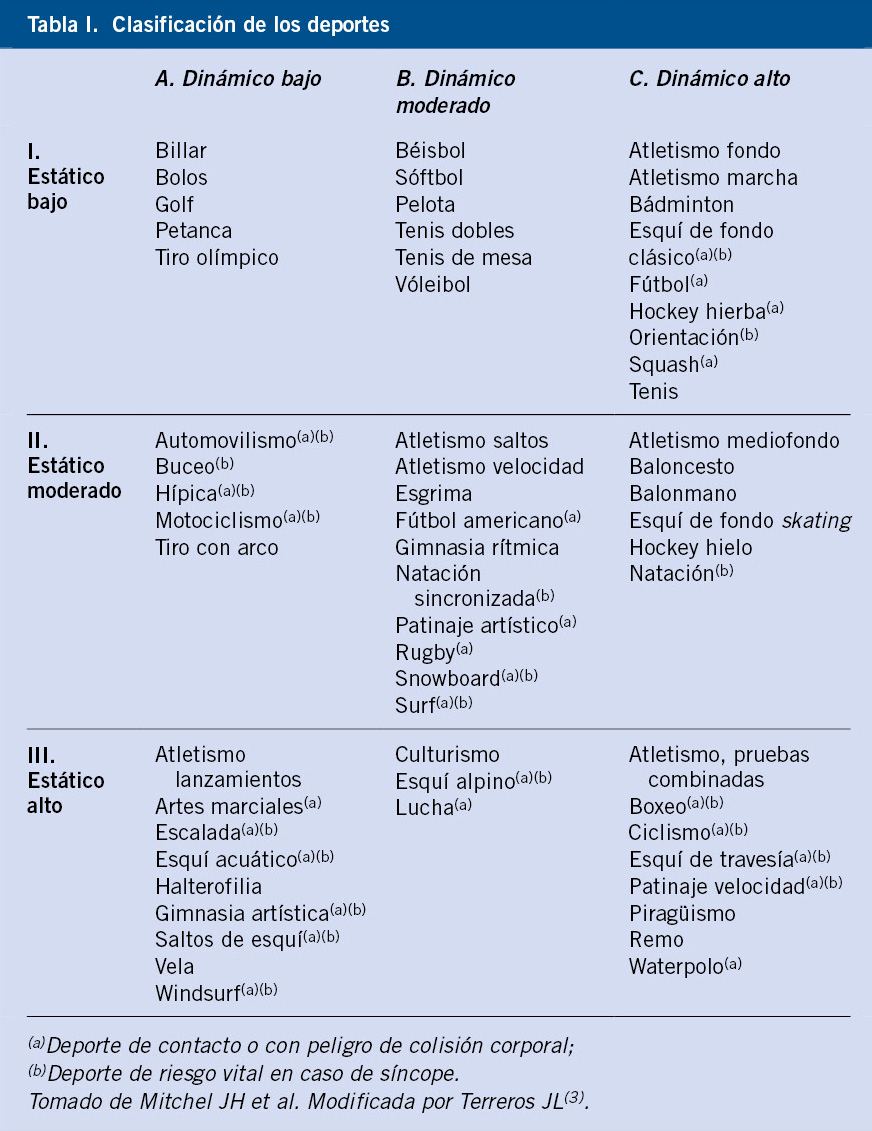
• Ejercicio físico y evitar el sedentarismo: es aconsejable realizar una actividad física de forma regular que, a su vez, sea placentera para el niño. Son recomendables los ejercicios dinámicos o isotónicos (p. ej.: correr, nadar), evitando los ejercicios estáticos isométricos (p. ej.: levantar pesas) que producen elevación brusca de la PA. El ejercicio físico es beneficioso por producir un aumento del gasto calórico (evita la obesidad) y por aumentar la vascularización periférica de los territorios musculares, por lo tanto, reduce las resistencias periféricas (disminuye los valores de PA). Nuestra sociedad ha potenciado el sedentarismo en los niños, con determinadas costumbres y actividades (ver televisión o películas, y el inagotable mundo de los juegos electrónicos) que limitan el ejercicio físico deseable y que, por lo tanto, deben tener un uso controlado y limitado. Existen trabajos que demuestran que, tras tres meses de ejercicio físico con entrenamiento controlado, la PA desciende 7-12 mmHg en la PA sistólica y 2-7 mmHg en la PA diastólica(19).
• Restricción de la sal: la sal, no solo aumenta la PA por la retención hídrica, también altera la función endotelial de los vasos al reducir la síntesis de óxido nítrico (vasodilatador). Una ingesta elevada de sal conlleva un aumento de la PA y, aunque una restricción moderada de sodio no se acompaña de un descenso efectivo de los niveles de PA, sí parece aconsejable el mantener una ligera restricción salina para un mejor control tensional. Una dieta con ingesta de sal máxima de 3 g/día produce un descenso de la PAS y PAD de 1,2/1,3 mmHg, respectivamente(20).
• Dieta equilibrada en cantidad y calidad: el pediatra debe fomentar nuestra tan socorrida dieta mediterránea (verdura, fruta, fibra, grasas monoinsaturadas, así como el aceite de oliva y grasas poliinsaturadas, como el pescado de mar) y evitar las dietas hipercalóricas con alto contenido de azúcar (bebidas azucaradas) y grasas saturadas (carnes, embutidos, patés, repostería industrial, snacks…), que está provocando una auténtica epidemia de obesidad infantil en nuestra sociedad. El consumo de bebidas azucaradas en adolescentes se asocia a un aumento de la PA sistólica(21).
Tratamiento farmacológico
Las indicaciones de tratamiento farmacológico de la HTA en niños, son:
• HTA sintomática.
• HTA secundaria.
• HTA con daño en órganos diana.
• HTA en diabetes tipo 1 y tipo 2.
• HTA no controlada con tratamiento no farmacológico.
El objetivo del tratamiento de la HTA en niños es “normalizar” la PA por debajo del percentil p95 y evitar el daño en los órganos diana, con los mínimos efectos secundarios y el mínimo coste.
En adultos, la mayoría de los pacientes hipertensos precisan medicación para el resto de sus vidas y aceptan su prescripción para evitar las consecuencias de una HTA no controlada. Sin embargo, en niños, existe siempre la preocupación de los posibles efectos secundarios de una medicación a largo plazo sobre el crecimiento y desarrollo.
El tratamiento en Pediatría de la HTA debe ser individualizado, dependiendo de la etiología si es reconocida, de los valores de la PA y de la historia del paciente.
Frente a los tratamientos más clásicos de la HTA en niños, como los diuréticos y los betabloqueantes, han surgido nuevos fármacos, como los inhibidores de la enzima de conversión de la angiotensina (IECA), los calcioantagonistas y los bloqueantes de los receptores de la angiotensina II (ARA II), cuyo perfil de seguridad y eficacia en niños es muy adecuado y los convierte en tratamiento hipertensivo de primera línea. En algunos casos, el tratamiento no es solo farmacológico, sino también quirúrgico, como por ejemplo, en la coartación de aorta, que será más grave cuanto más precoz sea la sintomatología llegando a convertirse en una urgencia médica.
El arsenal de fármacos disponibles para el tratamiento de la HTA en niños es muy amplio. A continuación, se citan los fármacos más usados en el tratamiento de la HTA, detallando la posología de los que pueden ser usados en Atención Primaria(2):
• Diuréticos: tiazidas y afines (hidroclorotiazida, clortalidona), diuréticos de asa (furosemida, ácido etacrinico, torasemida) y ahorradores de potasio (espironolactona, amiloride, eplerenona).
– Hidroclorotiazida: 0,5-3 mg/kg/día, c/12-24 h, v.o. (adulto: 12,5-100 mg/día).
– Furosemida: 1-4 mg/kg/día, c/12-24 h, v.o. (adulto: 20-80 mg/día).
– Espironolactona: 1-3 mg/kg/día, c/12-24 h, v.o. (adulto 50-100 mg).
• Beta-bloqueantes: atenolol (cardioselectivo), metoprolol, bisoprolol y propranolol.
– Atenolol: 0,5-2 mg/kg/día, c/12-24, v.o. (adulto: 50-100 mg/día).
– Propranolol: 0,5-2 mg/kg/día (máx. 4 mg/kg/día), c/6-8 h, v.o. (adulto: 80-320 mg/día).
• Alfa1-bloqueantes: doxazosín y prazosín.
– Doxazosín: 1 mg/día, c/24 h (máx. 4 mg).
– Prazosín: 0,05-0,1 mg/kg/día, c/8 h (máx. 0,5 mg/kg).
• Alfa2-bloqueantes: fentolamina y fenoxibenzamina.
• Alfa y beta bloqueante: labetalol y carvedilol.
– Labetalol: 1-3 mg/kg/día, c/12 h, (máx. 1.200 mg).
– Carvedilol: 0,1 mg/kg/dosis, c/12 h, (máx. 12,5 mg).
• Antiadrenérgicos centrales: clonidina y alfametildopa.
– Clonidina: 0,2 mg/kg/día, c/12 h, (máx. 2,4 mg).
• Vasodilatadores: hidralazina, diazóxido, minoxidil, nitroglicerina y nitroprusiato.
– Hidralazina: 0,75 mg/kg/día, c/6 h, (máx. 200 mg).
– Minoxidil: 0,2 mg/kg/día, c/8-24 h, (máx. 50-100 mg).
• Inhibidores de la enzima de conversión de la angiotensina (IECA): captopril, enalapril y lisinopril.
– Captopril: dosis inicial 0,25/kg, 0,5-6 mg/kg/día, c/8-12 h, v.o. (adulto: 6,25-25 dosis, c/8-12 h).
– Enalapril: 0,1-0,5 mg/kg/día, c/12-24 h, v.o. (adulto: 5-40 mg/día).
• Bloqueantes de los receptores de la angiotensina II (ARAII): losartán e irbesartán.
– Losartán: edad >6 años, dosis inicial 0,7 mg/kg/dosis, c/24 h, v.o. (max. 50 mg), subir hasta 1,4 mg/kg/dosis, c/24 h, v.o. (máx. 100 mg) (adulto: 50-100 mg/día).
– Irbesartán edad 6-12 años, 75-150 mg/día, c/24 h, v.o. (adulto: 150-300 mg/día).
• Antagonistas del calcio: nifedipino, amlodipino, verapamil y diltiazem.
– Nifedipino acción retardada: 0,25-0,5 mg/kg/día (máx. 3 mg/kg/día), c/12-24 h, v.o. (adulto 20-120 mg).
– Amlodipino: 0,06-0,3 mg/kg/día, c/24 h, (máx. 25-10 mg).
Recomendaciones de fármacos antihipertensivos
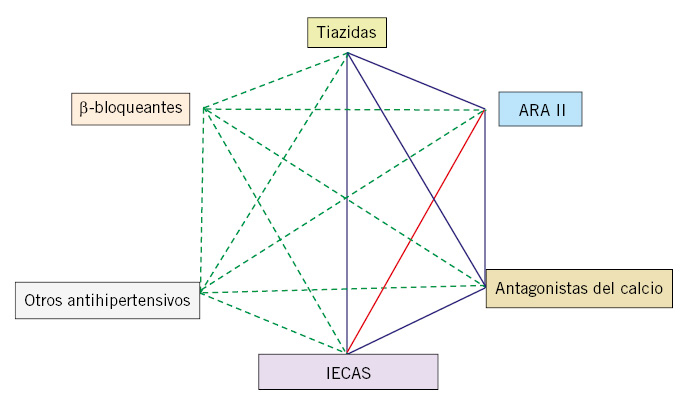
A la hora de elegir un fármaco para el tratamiento de la HTA, deberemos tener en cuenta las recomendaciones y contraindicaciones de cada grupo de fármacos(2):
• Diuréticos ahorradores de potasio:
– Recomendado: hiperaldosteronismo.
– Contraindicados: insuficiencia renal crónica y deportes de competición.
• Diuréticos tipo tiazida:
– Recomendado: insuficiencia renal crónica e HTA inducida por corticoides.
– Contraindicados: diabetes y deportes de competición.
• Diuréticos de asa:
– Recomendado: insuficiencia cardiaca congestiva.
• Betabloqueantes:
– Recomendado: insuficiencia cardiaca congestiva, coartación de aorta y migraña.
– Contraindicados: asma bronquial, diabetes, deportes de competición y psoriasis.
• Antagonistas del calcio:
– Recomendado: post-trasplante, migraña y coartación de aorta.
– Contraindicados: insuficiencia cardiaca congestiva.
• Inhibidores de la enzima de conversión de la angiotensina (IECA):
– Recomendado: insuficiencia renal crónica, diabetes mellitus, microalbuminuria, insuficiencia cardiaca congestiva y obesidad.
– Contraindicados: estenosis arteria renal bilateral, estenosis arteria renal en paciente monorreno, hiperpotasemia y embarazo.
• Bloqueantes de los receptores de la angiotensina II (ARAII):
– Recomendado: insuficiencia renal crónica, diabetes mellitus, microalbuminuria, insuficiencia cardiaca congestiva y obesidad.
– Contraindicados: estenosis arteria renal bilateral, estenosis arteria renal en paciente monorreno, hiperpotasemia y embarazo.
• Vasodilatadores intravenosos:
– Recomendado: condiciones que amenazan la vida.
Tratamiento de la crisis hipertensiva en Atención Primaria
Las crisis HTA se definen cuando la TA tiene un nivel 30% superior al percentil 95 o, aunque el valor no sea >30%, su aparición haya sido de forma rápida y brusca, o si se acompaña de síntomas por una disfunción orgánica aguda (neurológico, renal o cardiaco).
Recordar:
• Urgencia hipertensiva es HTA estadio 2, sin objetivarse daño de órgano diana, requiere tratamiento oral/sublingual, debe ingresar en planta con monitorización estrecha.
• Emergencia hipertensiva es HTA estadio 2, si se objetiva daño de órgano diana, es un riesgo vital y requiere tratamiento intravenoso, sin disminuir la TA más de un 25% en las primeras 8 horas. Debe ingresar en una Unidad de Cuidados Intensivos.
La crisis HTA puede ser el debut de una HTA y se trata de una urgencia médica, y, en Atención Primaria, se debe iniciar el manejo y tratamiento(22):
• Coger una vía venosa periférica.
• Nifedipino oral/sublingual (presentación: 1 ml = 30 mg, 10 mg = 0,34 ml.): Dosis: 0,25-0,30 mg/kg (máximo 10 mg).
– Peso <10 kg: 0,08 ml (2,5 mg).
– Peso 10-20 kg: 0,17 ml (5 mg).
– Peso >20 kg: 0,34 ml (10 mg).
– Adulto: 10 mg/dosis.
Vigilar efectos secundarios: caída brusca de la TA y taquicardia, rash cutáneo.
• Captopril: 0,2 mg/kg/dosis, oral/sublingual (adulto: 25 mg/dosis).
• La ansiedad se asocia con frecuencia a las crisis hipertensivas, la utilización de sedantes-ansiolíticos puede ser beneficiosa en el control de la TA: midazolam 0,2 mg/kg i.v., i.m., intranasal, oral.
Se debe realizar una derivación al Hospital en medios adecuados, con monitorización de la PA cada 5-10 minutos mediante manguito.
A nivel hospitalario, los fármacos más usados para la emergencia hipertensiva son:
• Nitroprusiato sódico: 0,5-8 mcg/kg/min en infusión intravenosa, se inactiva con la luz, vigilar hipotensión, toxicidad, metahemoglobinemia y acidosis metabólica.
• Labetalol: 0,25-3 mg/kg/hora en infusión intravenosa, vigilar bradicardia, broncoespasmo e hipoglucemia.
• Hidralacina: 0,2-0,6 mg/kg hasta 20 mg (dosis cada 4-6 h).
Bibliografía
1. Mancia G, Fagard R, Narkiewicz K, et al. 2013 ESH/ESC Guidelines for the management of arterial hypertension: the Task Force for the management of arterial hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). J Hypertens. 2013; 31: 1281-357.
2. Lurbe E, Agabiti-Rosei E, Cruickshank JK, et al. 2016 European Society of Hypertension guidelines for the management of high blood pressure in children and adolescents. J Hypertens. 2016; 34: 1887-920.
3. Battistoni A, Canichella F, Pignatelli G, et al. Hypertension in Young People: Epidemiology, Diagnostic Assessment and Therapeutic Approach. High Blood Press Cardiovasc Prev. 2015; 22: 381-8.
4. Sans S, Fitzgerald AP, Royo D, et al. Calibración de la tabla SCORE de riesgo cardiovascular para España. Rev Esp Cardiol. 2007; 60: 476-85.
5. Santi M, Simonetti BG, Leoni-Foglia CF, et al. Arterial hypertension in children. Curr Opin Cardiol. 2015; 30: 403-10.
6. National High Blood Pressure Education Program Working Group on High Blood Pressure in Children and Adolescents. Pediatrics. The Fourth Report on the Diagnosis, Evaluation, and Treatment of High Blood Pressure in Children and Adolescents. Pediatrics. 2004; 114: 555-76.
7. Sipola-Leppänen M, Vääräsmäki M, Tikanmäki M, et al. Cardiovascular risk factors in adolescents born preterm. Pediatrics. 2014; 134: e1072-81.
8. Gabriela R, Alonso M, Segura A, et al. Prevalencia, distribución y variabilidad geográfica de los principales factores de riesgo cardiovascular en España. Análisis agrupado de datos individuales de estudios epidemiológicos poblacionales: estudio ERICE. Rev Esp Cardiol. 2008; 61: 1030-40.
9. Kit BK, Kuklina E, Carroll MD, et al. Prevalence of and trends in dyslipidemia and blood pressure among US children and adolescents, 1999-2012. JAMA Pediatr. 2015; 169: 272-9.
10. Aguirre CJ, Sánchez JC, Hernández N, et al. Prevalencia de hipertensión arterial en la población infantil de una zona rural. Aten Primaria. 2012; 44: e16-17.
11. Yeste D, Carrascosa C. Complicaciones metabólicas de la obesidad infantil. An Pediatr. 2011; 75: 135.e1-135.e9.
12. Grupo cooperativo español para el estudio de factores de riesgo cardiovascular en la infancia y la adolescencia en España. Estudio RICARDIN II: valores de referencia. An Esp Pediatr. 1995; 43: 11-7.
13. Urbina E, Alpert B, Flynn J, et al. Ambulatory blood pressure monitoring in children and adolescents: Recommendations for standard assessment: a scientific statement from the American Heart Association Atherosclerosis, Hypertension, and Obesity in Youth Committee of the Council on Cardiovascular Disease in the Young and the Council for High Blood Pressure Research. Hypertension. 2008; 52: 433-51.
14. Sehgal A, Malikiwi A, Paul E, et al. Systemic arterial stiffness in infants with bronchopulmonary dysplasia: potential cause of systemic hypertension. J Perinatol. 2016; 36: 564-9.
15. Blechner M, Williamson AA. Consequences of Obstructive Sleep Apnea in Children. Curr Probl Pediatr Adolesc Health Care. 2016; 46: 19-26.
16. Endo A, Fuchigami T, Haseqawa M, et al. Posterior reversible encephalopathy syndrome in childhood: report of four cases and review of the literature. Pediatr Emerg Care. 2012; 28: 153-7.
17. Stein DR, Ferguson MA. Evaluation and treatment of hypertensive crises in children. Integr Blood Press Control. 2016; 9: 49-58.
18. Sabbadin C, Fallo F. Hyperaldosteronism: Screening and Diagnostic Tests. High Blood Press Cardiovasc Prev. 2016; 23: 69-72.
19. Farpour-Lambert NJ, Aggoun Y, Marchand LM, et al. Physical activity reduces systemic blood pressure and improves early markers of atherosclerosis in pre-pubertal obese children. J Am Coll Cardiol. 2009; 54: 2396-406.
20. He FJ, MacGregor GA. Importance of salt in determining blood pressure in children: meta-analysis of controlled trials. Hypertension. 2006; 48: 861-9.
21. Nguyen S, Choi HK, Lustig RH, et al. Sugar-sweetened beverages, serum uric acid, and blood pressure in adolescents. J Pediatr. 2009; 154: 807-13
22. Parra C, Quilis J. Hipertensión arterial en las urgencias pediátricas. En: Benito J, Luaces C, Mintegui S, et al, eds. Tratado de Urgencias Pediátricas. Madrid: Ergon; 2011. p. 433-48.
23. Ortigado Matamala A. Hipertensión arterial sistémica. Pediatr Integral. 2012; XVI(8): 636-46.
Bibliografía recomendada
– Mancia G, Fagard R, Narkiewicz K, et al. 2013 ESH/ESC Guidelines for the management of arterial hypertension: the Task Force for the management of arterial hypertension of the European Society of Hypertension (ESH) and of the European Society of Cardiology (ESC). J Hypertens. 2013; 31: 1281-357.
Artículo con las guías clínicas para el manejo de la HTA en población general, artículo muy completo.
– Lurbe E, Agabiti-Rosei E, Cruickshank JK, et al. 2016 European Society of Hypertension guidelines for the management of high blood pressure in children and adolescents. J Hypertens. 2016; 34: 1887-920.
Artículo que actualiza las guías clínicas de la HTA en Pediatría, documento imprescindible para consultar por el pediatra en el manejo de niños con HTA.
– National High Blood Pressure Education Program Working Group on High Blood Pressure in Children and Adolescents. Pediatrics. The Fourth Report on the Diagnosis, Evaluation, and Treatment of High Blood Pressure in Children and Adolescents. Pediatrics. 2004; 114: 555-76.
Artículo de obligada referencia, por aportar las bases del diagnóstico, evaluación y tratamiento de la HTA en Pediatría, aporta tablas de referencia.
– Battistoni A, Canichella F, Pignatelli G, et al. Hypertension in Young People: Epidemiology, Diagnostic Assessment and Therapeutic Approach. High Blood Press Cardiovasc Prev. 2015; 22: 381-8.
Artículo completo que trata todos los aspectos necesarios en la HTA en Pediatría de una forma práctica.
– Urbina E, Alpert B, Flynn, J et al. Ambulatory blood pressure monitoring in children and adolescents: Recommendations for standard assessment: a scientific statement from the American Heart Association Atherosclerosis, Hypertension, and Obesity in Youth Committee of the Council on Cardiovascular Disease in the Young and the Council for High Blood Pressure Research. Hypertension. 2008; 52: 433-51.
Artículo que valida la práctica de la monitorización ambulatoria de la presión arterial (MAPA) en Pediatría, la prueba con la que los pediatras se deben familiarizar para el correcto manejo de pacientes con HTA.
| Caso clínico |
|
Niño de 11 años que acude a la consulta de Niño Sano y en la medición de la presión arterial (PA) en brazo derecho se detecta 140/90 mmHg. Está tranquilo, es la primera vez que se toma la PA porque “nunca” ha estado enfermo. En los antecedentes personales, no hay ningún dato de interés. El niño está asintomático, aunque refiere cefaleas frecuentes en el último año (madre con cefalea tipo migraña) y epístaxis de repetición autolimitadas. No toma ninguna medicación y hace vida normal. Por vía paterna, existen varios miembros con HTA esencial.
Exploración física
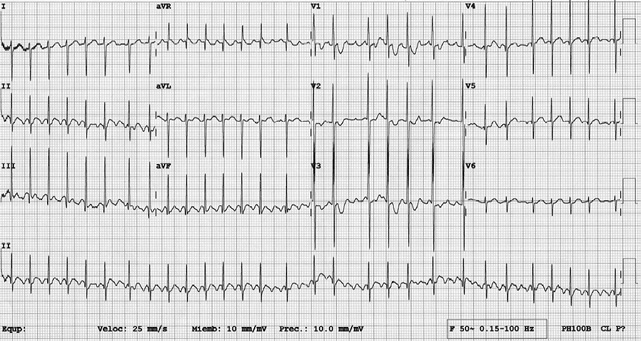
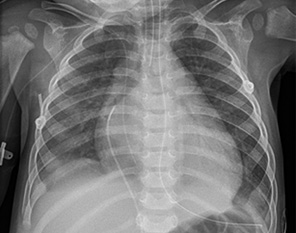
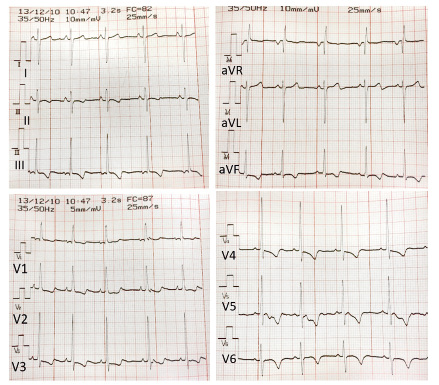
Peso: 36 kg (p50), talla 142 cm (p50). La exploración es aparentemente normal, sin discromías, auscultación cardiaca normal en mesocardio, abdomen normal, sin masas, exploración neurológica normal. El pediatra, en la consulta del centro de salud, le hace un análisis de orina con tira reactiva, que es normal, y un ECG (crecimiento ventricular izquierdo con alteración de la repolarización). Repite la medición tomada en miembro superior izquierda y se confirman los valores de PA.

|
|

















































 En Pediatría existe escasa evidencia científica acerca de los factores de riesgo cardiovascular (FRCV). Sin embargo, extrapolando los datos obtenidos de pacientes adultos, es razonable asumir que un correcto abordaje de los FRCV disminuirá la aparición de enfermedad cardiovascular(1).
En Pediatría existe escasa evidencia científica acerca de los factores de riesgo cardiovascular (FRCV). Sin embargo, extrapolando los datos obtenidos de pacientes adultos, es razonable asumir que un correcto abordaje de los FRCV disminuirá la aparición de enfermedad cardiovascular(1). El manejo de los FRCV en Pediatría, consiste en comprobar la adherencia a un estilo de vida saludable (prevención primordial) e identificar y tratar a los niños en riesgo de arterioesclerosis temprana (prevención primaria y secundaria)(2).
El manejo de los FRCV en Pediatría, consiste en comprobar la adherencia a un estilo de vida saludable (prevención primordial) e identificar y tratar a los niños en riesgo de arterioesclerosis temprana (prevención primaria y secundaria)(2).  En las revisiones de salud, se debe obtener información y dar pautas sobre: dieta, actividad física y exposición al tabaco. Se revisará el patrón de sueño y se identificarán los antecedentes familiares de enfermedad cardiovascular prematura(1,2).
En las revisiones de salud, se debe obtener información y dar pautas sobre: dieta, actividad física y exposición al tabaco. Se revisará el patrón de sueño y se identificarán los antecedentes familiares de enfermedad cardiovascular prematura(1,2).  Se recomienda el cribado universal de obesidad mediante la monitorización de la talla, el peso y el índice de masa corporal (IMC) en las revisiones de salud, a partir de los 6 años(3). USPSTF* 2017, grado de recomendación B.
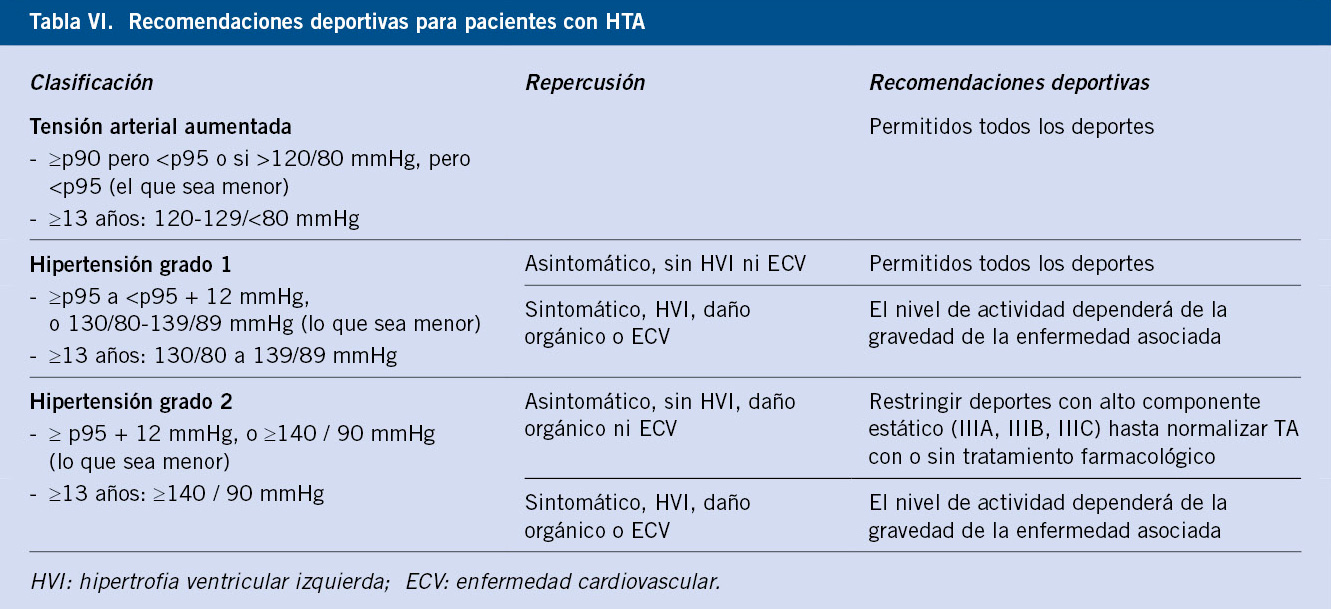
Se recomienda el cribado universal de obesidad mediante la monitorización de la talla, el peso y el índice de masa corporal (IMC) en las revisiones de salud, a partir de los 6 años(3). USPSTF* 2017, grado de recomendación B.  Se recomienda el cribado universal de hipertensión arterial (HTA), mediante la monitorización de la tensión arterial en las revisiones
Se recomienda el cribado universal de hipertensión arterial (HTA), mediante la monitorización de la tensión arterial en las revisiones No se recomienda un cribado universal de diabetes mellitus (DM)(5). ADA 2018, grado de recomendación A.
No se recomienda un cribado universal de diabetes mellitus (DM)(5). ADA 2018, grado de recomendación A.  Se realizará cribado de diabetes mellitus tipo 2 (DM2) mediante la determinación de glucemia en ayunas cada 2 años, en aquellos pacientes mayores de 10 años que presenten sobrepeso (IMC > percentil 85 para la edad y sexo) asociado a 2 o más de los siguientes factores de riesgo: DM2 en familiar de primer o segundo grado, grupo étnico de riesgo, signos de resistencia insulínica (acantosis, dislipemia, HTA o síndrome de ovario. poliquístico)(5). ADA 2018, grado de recomendación A
Se realizará cribado de diabetes mellitus tipo 2 (DM2) mediante la determinación de glucemia en ayunas cada 2 años, en aquellos pacientes mayores de 10 años que presenten sobrepeso (IMC > percentil 85 para la edad y sexo) asociado a 2 o más de los siguientes factores de riesgo: DM2 en familiar de primer o segundo grado, grupo étnico de riesgo, signos de resistencia insulínica (acantosis, dislipemia, HTA o síndrome de ovario. poliquístico)(5). ADA 2018, grado de recomendación A  La recomendación de un cribado universal de dislipemia (DL), mediante un perfil lipídico (colesterol total, triglicéridos y lipoproteínas) a los 9-11 años y a los 17-20 años es controvertida en el momento actual(1,6). USPSTF* 2016, grado recomendación I.
La recomendación de un cribado universal de dislipemia (DL), mediante un perfil lipídico (colesterol total, triglicéridos y lipoproteínas) a los 9-11 años y a los 17-20 años es controvertida en el momento actual(1,6). USPSTF* 2016, grado recomendación I.  Se recomienda el cribado de DL con perfil lipídico en mayores de 2 años, cada 3-5 años si existen los siguientes factores de riesgo: enfermedad cardiovascular prematura en la familia, hipercolesterolemia familiar, comorbilidades (HTA, DM, obesidad)(1,6). AHA 2019, grado de recomendación B.
Se recomienda el cribado de DL con perfil lipídico en mayores de 2 años, cada 3-5 años si existen los siguientes factores de riesgo: enfermedad cardiovascular prematura en la familia, hipercolesterolemia familiar, comorbilidades (HTA, DM, obesidad)(1,6). AHA 2019, grado de recomendación B. Se individualizará el seguimiento de los FRCV clásicos en presencia de otras patologías de alto riesgo (enfermedad renal crónica, enfermedades inflamatorias, cáncer y cardiopatías congénitas)(1).
Se individualizará el seguimiento de los FRCV clásicos en presencia de otras patologías de alto riesgo (enfermedad renal crónica, enfermedades inflamatorias, cáncer y cardiopatías congénitas)(1).