| Editorial |
S. Bonet Monné
Servicio de Atención Primaria Baix Llobregat Centre. Dirección de Atención Primaria Costa de Ponent. Cornellà de Llobregat. Barcelona
Importancia de los programas de optimización de antibióticos (PROA) en la Atención Primaria
Los antibióticos (AB) son medicamentos que han mostrado una elevada reducción de la morbimortalidad en el tratamiento de infecciones bacterianas en humanos, siendo su eficacia superior a la descrita para la mayoría de otros grupos terapéuticos utilizados en otras patologías(1,2).
Los AB actúan reduciendo el crecimiento, impidiendo la multiplicación o causando la muerte de las bacterias, y se utilizan en la prevención y el tratamiento de las infecciones bacterianas. El acceso a estos medicamentos se considera uno de los pilares básicos de la cobertura sanitaria universal(3), sin embargo, el uso inadecuado de los mismos, preocupa a nivel mundial, por ser uno de los principales factores de riesgo asociado al desarrollo de resistencias por parte de las bacterias, pudiendo contribuir al: incremento de gérmenes multirresistentes, incremento de la mortalidad asociada y aparición de epidemias. La resistencia a los antimicrobianos (RAM) se considera, por tanto, un problema de salud individual y de salud pública(4,5).
La RAM es un fenómeno de etiología múltiple. Los microorganismos, con el tiempo, pierden la sensibilidad a los antimicrobianos a través de la selección y transmisión de diversos mecanismos: los microrganismos presentan capacidad de adaptación, lo que se llamaría resistencia natural o intrínseca, por otro lado, estaría la resistencia adquirida debida a la modificación de la carga genética de los microorganismos, que aparece, sobre todo, por mutación cromosómica o por mecanismos de transferencia genética de bacteria a bacteria a través de plásmidos, transposones o integrones. El consumo de antibióticos influye no solo en las resistencias de bacterias patógenas, sino también de las saprofitas y oportunistas, produciéndose una presión selectiva sobre las bacterias sensibles y perpetuándose las cepas resistentes. Esta capacidad de generar resistencias de los microrganismos, por el uso excesivo e inadecuado de los mismos, es lo que se ha llamado “efecto ecológico de los AB”(6-8).
La sobreexposición a AB, no es solo en el uso humano, sino que es especialmente elevada en la industria ganadera, las piscifactorías y la agricultura. En este sentido, cada vez más, se utiliza el concepto de visión global de “One Health”, que reconoce que la salud humana, la sanidad animal y el medioambiente están entrelazados(4,5,9).
En Europa, se calcula que en el 2008, fallecieron aproximadamente 25.000 personas por infecciones producidas por microorganismos resistentes y, si no cambia el escenario, se estima que en el 2050 el número de muertes atribuibles a infecciones multirresistentes podría alcanzar los 10 millones al año (390.000/año en Europa y 40.000/año en España), y sería la primera causa de muerte, superior a las producidas por otras enfermedades como el cáncer(10). A esta situación, especialmente preocupante, hay que añadir las escasas perspectivas de desarrollo en los últimos años de nuevos antibacterianos(11,12).
España es uno de los países de la Comunidad Europea con un mayor consumo de AB por habitante (entre los 6 primeros en el 2021)(4), hecho que ha condicionado peores datos de sensibilidad de ciertas bacterias a determinados AB en relación a otros países, como por ejemplo de: Escherichia Coli a quinolonas(5,10). En los últimos años, se ha observado cierta tendencia a la reducción en el uso de AB(4), efecto más pronunciado durante la pandemia, registrándose una reducción, por ejemplo, en la comunidad de Asturias del 23,64 % del 2019 al 2020 (recetas oficiales)(13). Esta reducción durante la pandemia se produjo, en parte, por el impacto de las medidas aplicadas durante la pandemia (confinamiento, uso de mascarillas, menor socialización), que propició una reducción de la incidencia de determinados procesos infecciosos, sobre todo respiratorios(14) . Con la vuelta a la “normalidad” preocupa especialmente, que vuelva a incrementarse el uso inadecuado de los AB.
En este contexto de sobreutilización de AB y la aparición de gérmenes multirresistentes, hace años se empiezan a desarrollar a nivel mundial los llamados “antimicrobial stewardship programs”(15,16) que, por no disponer de una traducción equivalente del inglés, se han traducido como: Programas de Optimización del uso de antimicrobianos (PROA).
Estos programas tienen como objetivos comunes: 1) mejorar los resultados clínicos de los pacientes con infecciones en el ámbito hospitalario y en la comunidad; 2) minimizar los efectos adversos asociados a la utilización de antimicrobianos (incluyendo aquí la aparición y diseminación de resistencias), preservando el ecosistema; y 3) garantizar la utilización de tratamientos coste-efectivos. Los PROA son, por tanto, programas de mejora de la calidad.
Existen un gran número de publicaciones científicas, programas y documentos relacionados con políticas de uso de AB (mostramos en la tabla I, un resumen de las políticas europeas más recientes).
En España, se empezaron a desarrollar e implementar los PROA en los hospitales, de manera más generalizada, a partir del 2012(6) y, posteriormente, se han ido extendiendo en el ámbito de la comunidad. Hay que tener en cuenta, que es justamente en la comunidad, donde se diagnostican y resuelven la mayor parte de los procesos infecciosos y donde hay la mayor utilización de AB (80 % aproximadamente del total) y es, por tanto, en la comunidad, donde los PROA pueden tener un mayor impacto y donde existe una gran oportunidad de mejora(4). En el 2014, se publica la primera edición de Plan estratégico y de acción para reducir el riesgo de selección y diseminación de la resistencia a los antibióticos (PRAN)(9).
Es importante que los programas PROA se articulen conjuntamente con los programas territoriales de prevención y control de infecciones y que tengan apoyo institucional, y que exista una estrecha colaboración con otras áreas, como pueden ser las relacionadas con veterinaria y agricultura, con el objetivo de lograr una salud óptima para las personas, los animales y el medioambiente.
Estos programas orientados a la utilización responsable de los AB, implican el uso de los mismos solo en casos necesarios, la selección óptima (utilizar siempre que sea pertinente el AB sensible de menor espectro bacteriano, para preservar los de mayor espectro para situaciones más graves o complicadas), la dosis, la vía de administración y la duración más adecuada.
En cada comunidad, antes de que aparecieran los PROA como tales, desde hace años se han ido desarrollados proyectos relacionados con el uso adecuado de AB; así, por ejemplo, en Cataluña, en la Atención Primaria del sistema de salud público, hace más de 25 años que existen políticas relacionadas con la hiperprescripción y la selección de AB. Desde 1998, se monitorizan estos datos de manera sistemática en todos los equipos de Atención Primaria (EAP), en los médicos de medicina de familia y en otros especialistas como: pediatras, ginecólogos, médicos de servicios de urgencias en Atención Primaria y odontólogos. En el 2003, estos indicadores en médicos de familia y pediatras del Institut Català de la Salut (ICS) se asocian a incentivos económicos y a partir del 2006, se amplían estos incentivos a los EAP. Actualmente, se mantienen estos indicadores a nivel de los EAP, y los incentivos individuales se pactan (o no) en función de cada territorio.
En el 2006 se crea el sistema de vigilancia unificado de las infecciones nosocomiales en los hospitales de Cataluña (VINCat), como programa adscrito al Servei Català de la Salut. Este programa se creó ante la necesidad de disponer de datos sistematizados de infecciones, con el fin de establecer protocolos comunes para intentar reducir las tasas de infecciones nosocomiales.
A partir del 2019, el programa del VINCat se amplia y se crea: el programa de VINCat PROA comunitario (2019), el programa VINCat-PROA-de Pediatría (2019) y el programa VINCat -PROA-Socio sanitario (2020).
En relación a los PROA comunitarios, se constituye un programa para cada Área de Gestión Asistencial (AGA), que corresponderían a los equipos de Atención Primaria que comparten un mismo hospital de referencia (43 AGAs en Cataluña).
Cada PROA Comunitario en Cataluña, está constituido por un equipo de profesionales multidisciplinar (Tabla II).
Desde el VINCat, se proporcionan a cada PROA de los diferentes territorios (AGAs), los datos de consumo local de AB y de adecuación de los mismos, asociados a las patologías más prevalentes (Fig. 1).
Figura 1. Evolución del consumo de antibióticos en DHD en la comunidad de Cataluña. Fuente: aplicación de Farmacia del Institut Català de la Salud v1.0.
*Dosis Diaria Definida (DDD), por cada mil habitantes y día (DHD). Los datos locales mostrados no se pueden comparar con datos de estudios europeos por estar ponderados por el grado de envejecimiento de la población y por utilizar DDD de amoxicilina y amoxicilina + ácido clavulánico a 1.500 mg de amoxicilina (en Europa, la DDD de amoxicilina utilizada es de 1.000 mg), pero los datos sí sirven para evaluar el uso de AB según los diferentes años.
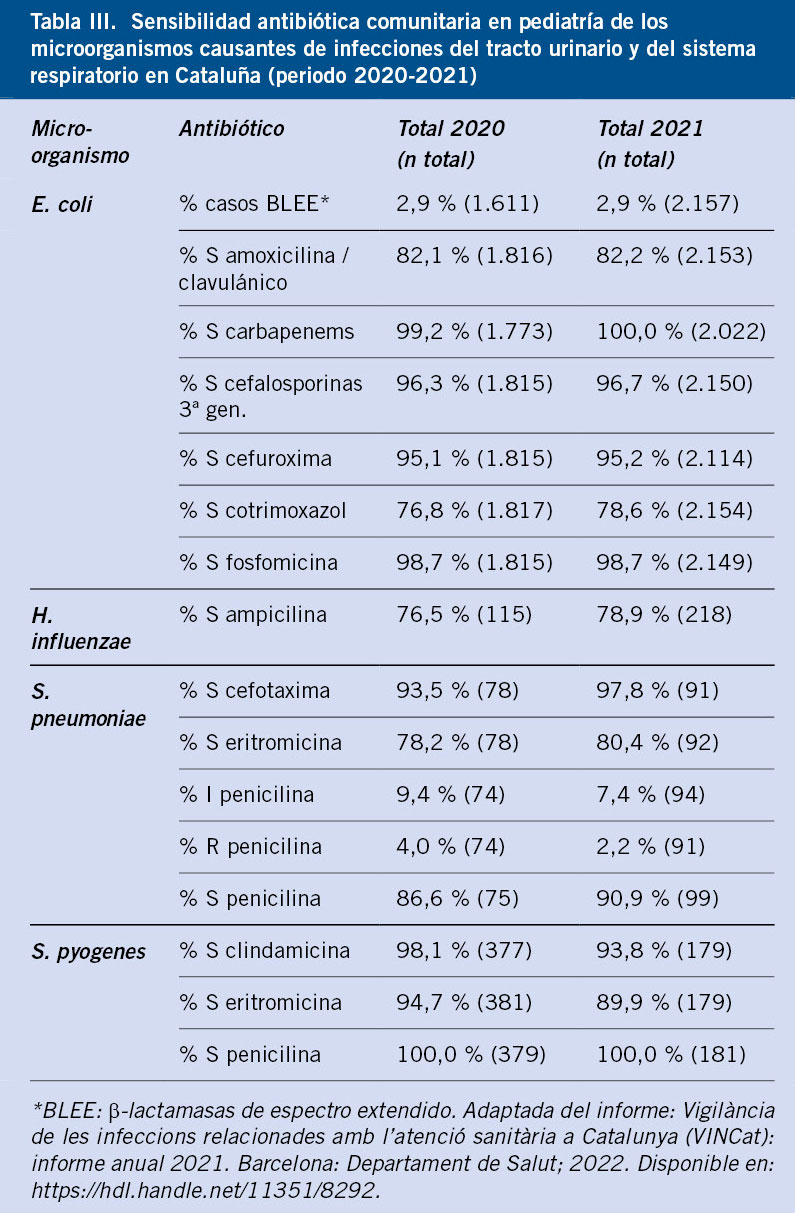
Es desde el VINCat también que, en colaboración estrecha con los diferentes servicios de microbiología del sistema sanitario público, se proporcionan anualmente los datos de sensibilidad microbiológica testados en muestras de la comunidad de los gérmenes más prevalentes del territorio, comparados con los de Cataluña (Tablas III y IV). Estos datos han permitido a los grupos PROA comunitarios en Cataluña:
• Disponer a nivel local por territorios, del perfil de sensibilidad a AB de muestras obtenidas en la comunidad de diferentes patógenos, diferenciadas según población pediátrica o adulta.
• Reducir el uso de AB del grupo de las fluoroquinolonas en las infecciones urinarias no complicadas de la mujer adulta.
• Reforzar el uso del test de diagnóstico rápido (TDR) para estreptococo beta hemolítico, como herramienta para la toma de decisión sobre el tratamiento antibiótico o no en la faringoamigdalitis.
• Establecer criterios de codificación diagnóstica para mejorar y simplificar la codificación de las principales patologías infecciosas.
• Detectar áreas de mejora en el uso de AB a nivel local y priorizar intervenciones.
Es por todo lo anteriormente mencionado, que consideramos necesario para seguir avanzando en el uso adecuado de los AB, implementar, desarrollar y ampliar las funciones de los programas PROA en la comunidad.
Frente a la política del uso adecuado de AB, hay que tener en cuenta que siempre pueden aparecer situaciones excepcionales, como la aparición de nuevas pandemias o el desabastecimiento de antibióticos en presentaciones pediátricas, como ha ocurrido durante el 2022, que dificultan la práctica asistencial, así como la implementación de estos programas.
Bibliografía
1. Armstrong GL, Conn LA, Pinner RW. Trends in infectious disease mortality in the United States during the 20th century. JAMA. 1999; 281: 61-6. Disponible en: https://jamanetwork.com/journals/jama/fullarticle/768249.
2. Paul M, Shani V, Muchtar E, Kariv G, Robenshtok E, Leibovici L. Systematic review and meta-analysis of the efficacy of appropriate empiric antibiotic therapy for sepsis. Antimicrob Agents Chemother. 2010; 54: 4851-63. Disponible en: https://doi.org/10.1128/AAC.00627-10.
3. Orientaciones normativas de la OMS sobre las actividades integrales para la optimización de los antimicrobianos. Organización Mundial de la Salud; 2021. Licencia: CC BY-NC-SA 3.0 IGO.S. Disponible en: https://apps.who.int/iris/bitstream/handle/10665/342644/9789240031203-spa.pdf?sequence=1&isAllowed=y.
4. Antimicrobial consumption in the EU/EEA (ESAC-Net) Annual Epidemiological Report for 2021. Disponible en: https://www.ecdc.europa.eu/sites/default/files/documents/ESAC-Net_AER_2021_final-rev.pdf.
5. Antimicrobial resistance surveillance in Europe 2020 data 2022. Disponible en: https://www.ecdc.europa.eu/sites/default/files/documents/Joint-WHO-ECDC-AMR-report-2022.pdf.
6. Oxford J, Kozlov R. Antibiotic resistance – a call to arms for primary healthcare providers. Int J Clin Pract Suppl. 2013; 180: 1-3. Disponible en: https://doi.org/10.1111/ijcp.12334.
7. Davies J, Davies D. Origins and evolution of antibiotic resistance. Microbiol Mol Biol Rev. 2010; 74: 417-33. Disponible en: https://doi.org/10.1128/MMBR.00016-10.
8. Celis Bustos YA, Rubio VV, Camacho Navarro MM. Perspectiva histórica del origen evolutivo de la resistencia a antibióticos. Rev. colomb. Biotecnol. 2017; 192: 105. Disponible en: https://doi.org/10.15446/rev.colomb.biote.v19n2.69501.
9. Plan estratégico y de acción para reducir el riesgo de selección y diseminación de la resistencia a los antibióticos. Agencia Española de Medicamentos y Productos Sanitarios (AEMPS). Madrid. 1ª ed.: 2014. Disponible en: https://www.aemps.gob.es/publicaciones/publica/plan-estrategico-antibioticos/v2/docs/plan-estrategico-antimicrobianos-AEMPS.pdf.
10. O’Neill J. Tackling drug-resistant infections globally: Final report and recommendations. Review on Antimicrobial Resistance. 2016. Disponible en: https://amr-review.org/sites/default/files/160518_Final%20paper_with%20cover.pdf.
11. Boucher HW, Talbot GH, Bradley JS, Edwards JE, Gilbert D, Rice LB, et al. Bad bugs, no drugs: no ESKAPE! An update from the Infectious Diseases Society of America. Clin Infect Dis. 2009; 48: 1-12. Disponible en: https://doi.org/10.1086/595011.
12. Vila J, Rodríguez-Baño J, Gargallo-Viola D. Prudent use of antibacterial agents: are we entering in an era of infections with no effective antibacterial agents? What can we do? Enferm Infecc Microbiol Clin. 2010; 28: 577-9. Disponible en: https://doi.org/10.1016/j.eimc.2010.09.002.
13. Nicieza García ML, Pérez Solís P, Gómez de Oña C, Suárez Gil P, Rolle Sóñora V, Suárez Mier B. Consumo de antibióticos en atención primaria en población adulta de Asturias durante el periodo 2014-2020. Aten Primaria. 2022; 54: 102261. Disponible en: https://doi.org/10.1016/j.aprim.2021.102261.
14. Kuitunen I, Artama M, Mäkelä L, Backman K, Heiskanen-Kosma T, Renko M. Effect of Social Distancing Due to the COVID-19 Pandemic on the Incidence of Viral Respiratory Tract Infections in Children in Finland During Early 2020. Pediatr Infect Dis J. 2020; 390: e423-7. Disponible en: https://journals.lww.com/pidj/Fulltext/2020/12000/Effect_of_Social_Distancing_Due_to_the_COVID_19.7.aspx.
15. Society for Healthcare Epidemiology of America; Infectious Diseases Society of America; Pediatric Infectious Diseases Society. Policy statement on antimicrobial stewardship by the Society for Healthcare Epidemiology of America (SHEA), the Infectious Diseases Society of America (IDSA), and the Pediatric Infectious Diseases Society (PIDS). Infect Control Hosp Epidemiol. 2012.
16. Barlam TF, Cosgrove SE, Abbo LM, MacDougall C, Schuetz AN, Septimus EJ, et al. Implementing an Antibiotic Stewardship Program: Guidelines by the Infectious Diseases Society of America and the Society for Healthcare Epidemiology of America. Clin Infect Dis. 2016; 62: e51-77. Disponible en: https://doi.org/10.1093/cid/ciw118.
17. Comunicación de la comisión al parlamento europeo del Plan de acción contra la amenaza creciente de las resistencias bacterianas. Comisión Europea Bruselas. 2011. Disponible en: https://eur-lex.europa.eu/LexUriServ/LexUriServ.do?uri=COM:2011:0748:FIN:ES:PDF.
18. Rodríguez-Baño J, Paño-Pardo JR, Álvarez-Rocha L, Asensio A, Calbo E, Cercenado E, et al. Programas de optimización de uso de antimicrobianos (PROA) en hospitales españoles: documento de consenso GEIH-SEIMC, SEFH y SEMPSPH. Enferm Infecc Microbiol Clin. 2012; 30: 22.e1-23. Disponible en: https://doi.org/10.1016/j.eimc.2011.09.018.
19. Plan nacional frente a la resistencia a los antibióticos (PRAN) 2019-2021. Agencia Española de Medicamentos y Productos Sanitarios (AEMPS.). Madrid. 2019. Disponible en: https://resistenciaantibioticos.es/sites/default/files/2022-04/pran_2019-2021_0.pdf.
20. Norma para la certificación de los equipos PROA Comunitarios. Agencia Española de Medicamentos y Productos Sanitarios (AEMPS). Madrid. 2023. Disponible en: https://resistenciaantibioticos.es/sites/default/files/2023-02/CertificaPROA%20Normativa%20COMUNITARIOS_VF.pdf.





 Fever of unknown origin
Fever of unknown origin