 |
| Temas de FC |
J.A. Alonso Cadenas, M. de la Torre Espí
Servicio de Urgencias. Hospital Infantil Universitario Niño Jesús. Madrid
| Resumen
La fiebre sin foco (FSF) es aquel proceso febril de menos de 48-72 horas de evolución en el que no se identifica la causa tras la anamnesis y la exploración física. El origen de la fiebre puede ser vírico o bacteriano. Entre otras causas, existen infecciones bacterianas no invasivas: infección del tracto urinario, neumonía, faringoamigdalitis aguda estreptocócica, gastroenteritis aguda bacteriana, o celulitis; e infecciones bacterianas invasivas: bacteriemia (bacteriemia oculta si el paciente tiene buen estado general), meningitis bacteriana, artritis séptica o neumonía complicada. Las pruebas complementarias en los niños con FSF se realizan en función del estado general, valorado a través del triángulo de evaluación pediátrica (TEP): edad, grado de temperatura y estado de inmunización. El tratamiento y los criterios de evolución clínica varían también según lo anterior; pero, sobre todo, atendiendo al estado general, que es el principal discriminador. El pediatra de Atención Primaria debe saber identificar y tratar al paciente con un TEP inestable hasta su traslado al hospital y, también, derivar a aquellos que se encuentran estables y necesitan pruebas complementarias y observación hospitalaria. |
| Abstract
Fever without source (FWS) is a febrile process with a course of less than 48-72 hours in which the cause is not identified after performing the history and physical examination. The origin of the fever can be viral or bacterial. Within the latter, there are non-invasive bacterial infections: urinary tract infection, pneumonia, acute streptococcal pharyngitis, acute bacterial gastroenteritis, or cellulitis; and invasive bacterial infections: bacteremia – occult bacteremia if the patient is in good general condition –, bacterial meningitis, septic arthritis, or complicated pneumonia. Complementary tests in children with FWS are conducted based on the following factors: general condition – assessed through the pediatric assessment triangle (PAT) –, age, temperature level, and immunization status. Treatment and criteria for clinical progress vary according to the aforementioned, however, the general condition is the main determinant of having a bacterial infection. The primary care pediatrician must know how to identify a patient with an unstable PAT and manage him during the initial minutes until transferred to the hospital, as well as to refer those who are stable and need additional tests and hospital observation. |
Palabras clave: Fiebre sin foco; Bacteriemia; Infección urinaria; Procalcitonina.
Key words: Fever without source; Bacteremia; Urinary tract infection; Procalcitonin.
Pediatr Integral 2023; XXVII (5): 240 – 248
OBJETIVOS
• Identificar a los lactantes menores de 3 meses de edad con criterios de bajo, intermedio o alto riesgo de infección bacteriana.
• Reconocer a los lactantes de entre 3 y 24 meses de edad que necesitan pruebas complementarias.
• Adecuar las indicaciones para realizar una punción lumbar.
• Tratar con un antibiótico solo a aquellos niños con riesgo de tener una infección bacteriana.
Fiebre sin foco
Introducción
Se define fiebre sin foco, como aquel proceso febril (Tª >38ºC), con menos de 48-72 horas de evolución, y en el que ni la historia clínica, ni la exploración identifican la causa.
La fiebre es un motivo de consulta muy frecuente en Pediatría, tanto en Atención Primaria (20 % de los episodios agudos) como en los servicios de urgencias infantiles (30 % de los episodios). Nuestros propios datos así lo corroboran: en el año 2022, de los 77.712 episodios atendidos en el servicio de urgencias del Hospital Infantil Universitario Niño Jesús de Madrid, 22.226 (28,6 %) tenían como principal motivo de consulta la fiebre. A pesar de ser tan frecuente, genera mucha ansiedad en los cuidadores, lo que provoca que consulten pronto con cuadros poco evolucionados, sobre todo si son lactantes. Por ejemplo, alrededor del 50 % de los niños menores de 3 meses con fiebre son evaluados en las primeras 6 horas(1).
La fiebre sin foco (FSF) es aquel proceso febril de menos de 48-72 horas de evolución, en el que no se identifica la causa tras la anamnesis y la exploración física. Habitualmente, se considera fiebre cuando la temperatura es mayor de 38ºC a nivel axilar o rectal (siendo la segunda 0,5 grados mayor que la primera), esta última tomada generalmente en los lactantes menores de 3 meses. No se recomienda la toma de temperatura: oral, en el oído o por infrarrojos con y sin contacto(2).
En los niños, el origen de la fiebre suele ser infeccioso. En la mayoría de las ocasiones, se trata de una infección benigna y autolimitada; sin embargo, algo menos del 10 % de los niños tiene una infección bacteriana grave.
Las infecciones bacterianas pueden ser no invasivas (IBNI): infección del tracto urinario (ITU), neumonía, faringoamigdalitis aguda estreptocócica, gastroenteritis aguda, celulitis; o invasivas (IBI): aislamiento de una bacteria patógena en un líquido estéril como: la sangre (bacteriemia), el líquido cefalorraquídeo (meningitis bacteriana), el líquido articular (artritis séptica) o la pleura (neumonía complicada)(3). Estas últimas asocian mayor morbilidad y mortalidad.
El principal objetivo cuando se atiende a un niño con fiebre sin foco es identificar a todos aquellos que tienen una infección bacteriana invasiva.
El cambio de la situación epidemiológica por las vacunas del Haemophilus influenzae, Neisseria meningitidis y del Streptococcus pneumoniae y meningo, junto con la aparición de nuevas pruebas diagnósticas de detección rápida de virus y bacterias, han provocado cambios en las estrategias diagnóstico-terapéuticas de los niños con FSF.
Etiología
La principal causa de la fiebre sin foco en los niños es vírica.
Los virus son la causa principal de FSF en los pacientes pediátricos, siendo los más frecuentes: adenovirus, virus de la gripe, virus herpes 6, enterovirus y parechovirus. La prevalencia de los dos últimos es mayor cuanto menor es la edad del niño y hay que tenerlos en cuenta, sobre todo en los menores de 3 meses de edad.
Lactantes menores de 3 meses
Es un grupo de especial atención, porque la incidencia de IBNI e IBI es mayor que en otras etapas de la vida, debido a que su sistema inmunológico está inmaduro y han recibido pocas dosis de vacunas. Además, las manifestaciones clínicas de las infecciones son menos evidentes. La prevalencia de infección bacteriana, IBNI e IBI, varía de un estudio a otro en función de los criterios de inclusión. En EE.UU. se suele incluir a todos los lactantes febriles, aunque tengan un foco (prevalencia ≈8 %), y en Europa solo aquellos con FSF (prevalencia ≈20 %). La infección bacteriana más frecuente en estos niños es la ITU. El riesgo de padecer una IBI es inversamente proporcional a la edad del paciente, con una prevalencia global del 2-4 %(4) (Fig. 1), llegando al máximo en el periodo neonatal. El 5-6 % de los neonatos atendidos en un servicio de urgencias pediátricas serán diagnosticados de una IBI. Las bacterias implicadas con más frecuencia son:
Figura 1. Riesgo de bacteriemia en función de las semanas de vida del lactante.
• Neonatos: Escherichia coli (principal microorganismo), Streptococcus agalactiae, Enterococcus faecalis, otras enterobacterias y Listeria monocytogenes(5).
• Lactantes de 1-3 meses de edad: E. coli, S. agalactiae, S. pneumoniae, Staphylococcus aureus y L. monocytogenes(5).
Lactantes de 3-24 meses de edad
Tienen una menor incidencia de IBNI e IBI que los lactantes menores de 3 meses pero es el grupo de edad con mayor incidencia de bacteriemia oculta (BO), aislamiento de una bacteria patógena en la sangre de un paciente con buen estado general. Se ha descrito en algún estudio(6) que, tras la introducción de la vacuna conjugada 13v, S. pneumoniae ha dejado de ser el germen más frecuente (en nuestro país probablemente ha sucedido lo mismo pero no se disponen de estudios actualizados)(7), al ser superado por E. coli, Salmonella spp y S. aureus. En la actualidad, la prevalencia de BO en lactantes con FSF y buen estado general es inferior al 1 %, incluso menor del 0,5 % en algunas series(7).
La ITU también es muy frecuente, siendo la prevalencia máxima en las niñas menores de 2 años y en los niños menores de 6 meses con temperaturas >39ºC.
Otras bacterias implicadas en las infecciones en este grupo de edad son: N. meningitidis, Streptococcus pyogenes y H. influenzae.
Niños mayores de 24 meses
La mayoría de las infecciones bacterianas son focales: neumonías, meningitis, o ITU, y en función de la localización predominará un microorganismo u otro.
Evaluación clínica
La edad del paciente, el estado general, el grado de la fiebre y el estado de inmunización, son los factores que determinan la atención inicial de los niños con fiebre sin foco.
Impresión inicial
Es muy importante evaluar el estado general con el triángulo de evaluación pediátrica (TEP), una herramienta desarrollada por la Academia Americana de Pediatría, que proporciona una primera impresión clínica del paciente de forma sencilla y rápida, con lo que se percibe con la vista y el oído(8), con independencia de la edad y del motivo de consulta. No se necesita ningún aparato, ni medir constantes vitales, ni siquiera tocar al paciente. La alteración del estado general es el factor de riesgo más importante de presentar una IBI. Los componentes del TEP son:
• Apariencia (lado más importante): refleja, en general, la función del sistema nervioso central. Hay que tener en cuenta: el tono, la interactividad, el llanto, si se consuela fácilmente, la mirada y la expresión verbal.
• Respiración: hay que evaluar los ruidos respiratorios, la postura (postura de olfateo y en trípode) y la presencia o no de retracciones costales, de cabeceo en los lactantes y de aleteo nasal. Refleja el estado de las funciones de oxigenación y ventilación.
• Circulación: determina si el gasto cardíaco y la perfusión de los órganos vitales son adecuados. La palidez, la piel marmórea y la cianosis son indicadores de una circulación reducida en la piel y las membranas mucosas.
Para clasificarlo como estable, los tres lados del TEP deben ser normales.
Anamnesis
Antecedentes personales
Hay que identificar los antecedentes que implican una mayor probabilidad de padecer una infección bacteriana.
• Periodo neonatal inmediato: fiebre durante el parto, bolsa rota más de 24 horas, líquido amniótico turbio o fétido, colonización vaginal por S. agalactiae, prematuridad, bajo peso, ingreso en una unidad de cuidados intensivos neonatales, realización de algunos procedimientos diagnósticos o terapéuticos (canalización de vía venosa umbilical, cateterismo central, nutrición parenteral, antibioterapia de amplio espectro o ingreso hospitalario prolongado).
• Lactante de 1-3 meses: prematuridad, antecedentes de hospitalización, tratamiento antibiótico previo o actual, tratamiento por hiperbilirrubinemia inexplicada, enfermedad de base (p. ej.: inmunodeficiencia, anemia drepanocítica, fibrosis quística, reflujo vesicoureteral y antecedentes de ITU) o tiempo de ingreso prolongado.
• Lactante de 3-24 meses: enfermedad de base y tratamiento con fármacos inmunosupresores.
Historia actual
• Lactantes menores de 3 meses: se averiguará la repercusión del proceso sobre el estado general: apetito, sueño y llanto. También es de interés el ambiente epidémico y, si es mayor de 2 meses, la fecha de la vacunación. Si la inmunización ha sido reciente, últimas 48 horas y, especialmente, últimas 24 horas, en estos lactantes el riesgo de tener una IBI es bajo y la fiebre suele estar relacionada con la vacuna(9).
• Lactantes de 3-24 meses: el estado general (TEP) y la temperatura son los elementos más importantes para evaluar el riesgo de tener una infección grave.
– Fiebre: se preguntará sobre la temperatura máxima y el tiempo de evolución. Lo más importante es el valor predictivo negativo (riesgo bajo de una infección grave) de una temperatura <39ºC en los lactantes con buen estado general.
– Estado general: se indagará sobre el grado de afectación (decaimiento, irritabilidad, actividad, comportamiento).
– Búsqueda de síntomas propios de las infecciones más frecuentes: mucosidad nasal, tos, diarrea, vómitos, etc.
– Estado vacunal: se registrará si está vacunado, principalmente contra S. pneumoniae, N. meningitidis y H. influenzae, y el número de dosis administradas.
– Fecha de la última inmunización: la DTP produce una reacción febril en las primeras 24-48 horas, que no suele prolongarse más de 2 días. La fiebre tras la vacuna de la triple vírica aparece 7-10 días después y se puede acompañar de un leve exantema.
– Otros: ambiente epidémico y si ha recibido tratamiento antibiótico previo.
Exploración física
Debe continuarse con una exploración física general, prestando especial atención a los signos que orienten a un foco de infección. La medición de constantes vitales se hará según los hallazgos del TEP, en primer lugar, y de la exploración posteriormente: temperatura siempre, frecuencia respiratoria (FR), cardiaca (FC) y saturación de oxígeno (SO2) si hay signos de dificultad respiratoria, FC y tensión arterial (TA) si hay signos de inestabilidad hemodinámica (palidez de piel, tiempo de relleno capilar prolongado, etc.).
Pruebas complementarias
Se solicitarán en función de la edad, el estado general, el grado de temperatura y de los hallazgos de la anamnesis y la exploración física.
Menores de 3 meses
En todos los lactantes menores de 3 meses de edad con fiebre sin foco, hay que realizar análisis de sangre y de orina y, en algunos pacientes seleccionados, una punción lumbar.
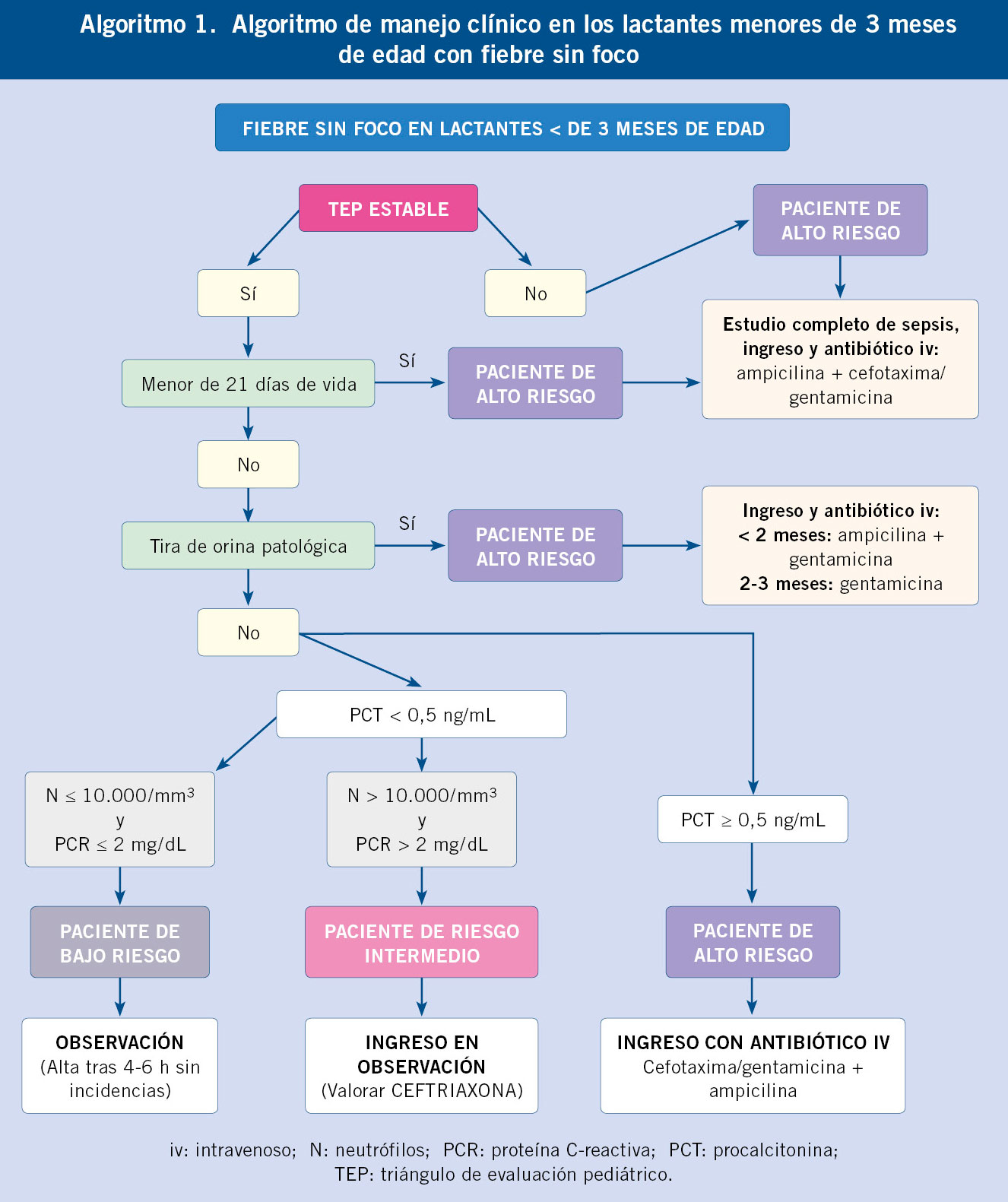
En época epidémica (bronquiolitis por virus respiratorio sincitial, gripe, SARS-CoV-2 +/- adenovirus), las pruebas de detección rápida de antígenos virales pueden ayudar en la toma de decisiones y evitar algunos análisis de sangre. La inclusión de nuevas pruebas, como las “Polymerase chain reaction” (PCR) para enterovirus o parechovirus, si son positivas, pueden identificar lactantes con menor riesgo de tener una IBI, acortando o evitando el tratamiento antibiótico y disminuyendo la estancia hospitalaria en estos pacientes(14). La tecnología de microarrays que permite secuenciar el ARN mensajero del microorganismo que causa la infección analizando su expresión génica, constituye un método rápido y eficaz de detección del patógeno, que será ampliamente usado en el futuro(10). La atención clínica de estos lactantes se muestra en el algoritmo 1(11).
• Análisis de orina: en los neonatos de 21 días o menos, se recomienda recoger directamente una muestra estéril (sondaje vesical, micción espontánea o punción suprapúbica) para realizar análisis de orina con tira reactiva (TRO) y urocultivo.
En los mayores de 21 días, se puede recoger una primera muestra con bolsa recolectora. Si es patológica (leucocituria ≥1+ y/o nitrituria), habría que obtener una nueva muestra estéril para repetir el análisis con TRO y cultivarla si se confirma el resultado patológico. El urocultivo solo se realizará en muestras estériles. La sensibilidad de la leucocituria es del 95 % (intervalo de confianza 95 %, 91-97 %)(12) e incluso es mayor si la ITU es bacteriémica. El diagnóstico de ITU se podrá establecer ante la presencia >10.000 unidades formadoras de colonias (ufc) de una bacteria patógena en una muestra obtenida por sondaje vesical y con un resultado patológico del análisis con TRO.
No está claro el diagnóstico, cuando el análisis de orina con TRO es normal y el urocultivo positivo, si se trata de una ITU, una bacteriuria asintomática o incluso una contaminación.
• Análisis de sangre: en los algoritmos de FSF (Step by Step) siempre se debe solicitar hemograma, procalcitonina (PCT), proteína C-reactiva (PCR) y hemocultivo. La PCT (>0,5 ng/ml) es el parámetro de laboratorio con mayor validez en el diagnóstico de una infección bacteriana, seguida de la PCR (>20 mg/L) y el valor absoluto de los neutrófilos (>10.000/mm3). Ni la leucocitosis ni la leucopenia son útiles como marcadores de IBI(13). En lactantes con una sospecha de infección por virus herpes simple (VHS) (antecedente de infección materna, vesículas en la exploración física, trombopenia, elevación de GPT), hay que solicitar PCR en plasma para VHS y en las lesiones. También se debe valorar la realización de pruebas microbiológicas virales en sangre (enterovirus, parechovirus) cuando la TRO sea normal. Un resultado positivo de la PCR para enterovirus disminuye de manera significativa el riesgo de IBI (2,6 % vs 0 %)(14). También hay que tener en cuenta la fecha de la inmunización, si fue en las últimas 24 horas y el lactante tiene buen estado general, puede obviarse el análisis de sangre(9).
• Punción lumbar: las indicaciones se muestran en la tabla I.
Se añadirá la PCR para VHS en los neonatos con pleocitosis y análisis con tinción de gram negativo (no se objetivan gérmenes). Tienen mayor riesgo de presentar una infección por VHS si: <15 días de vida, antecedente de convulsión, mal estado general, trombopenia, exantema vesicular o prematuridad. En los neonatos con buen estado general y una ITU, el riesgo de tener una meningitis bacteriana es muy bajo(17).
• Prueba de detección rápida de antígenos virales en nasofaringe (VRS, Influenza, SARS-CoV-2 +/- adenovirus): el rendimiento de estas pruebas depende de que se soliciten en el momento adecuado, durante la epidemia de bronquiolitis o de gripe en épocas de alta circulación de estos virus. Algunos trabajos han demostrado que el riesgo de IBI es menor en lactantes >28 días de vida con una prueba de detección vírica positiva, permitiendo en estos pacientes obviar el análisis de sangre, pero no el de orina, ya que la prevalencia de ITU continúa estando entre el 0,8 y el 4,2 %(18,19).
Estratificación del riesgo de padecer una IBI (bacteriemia/meningitis bacteriana) en los lactantes menores de 3 meses(10)
• Bajo riesgo (prevalencia de IBI: 0,7 %): lactantes >21 días de vida
con TEP estable, análisis de orina con TRO normal, PCT <0,5 ng/ml, PCR ≤20 mg/L y neutrófilos ≤10.000/mm3.
• Riesgo intermedio (prevalencia de IBI: 3,4 %): lactantes >21 días de vida con TEP estable, análisis de orina con TRO normal, PCT <0,5 ng/mL + PCR >20 mg/dL o neutrófilos >10.000/mm3.
• Alto riesgo (prevalencia de IBI: 7,2 %): TEP alterado, neonatos ≤21 días de vida, lactantes >21 días de vida con análisis de orina con TRO alterada y/o PCT ≥0,5 ng/mL.
Los lactantes de este grupo de edad consultan cada vez más pronto en los SU, lo que podría condicionar el rendimiento de las reglas de predicción clínica. Por el momento no se incluye el tiempo de evolución en las mismas aunque algunos autores aconsejan una actitud más cauta en aquellos que consultan con tiempos más recortados (<2 horas).
Lactantes de 3-24 meses
En función del TEP, la temperatura máxima y el número de dosis recibidas de la vacuna antineumocócica 13v, se estratifica a los lactantes en función del riesgo de presentar una infección bacteriana: IBI e IBNI (Algoritmo 2). No hay consenso en el punto de corte de la temperatura a partir del cual realizar un análisis de sangre, ni de los reactantes de fase aguda (RFA) –PCR, PCT–, en este grupo de edad los valores establecidos se han decidido de manera arbitraria.
• TEP estable (buen estado general):
– Análisis de orina: la ITU es la infección bacteriana más frecuente en los lactantes (prevalencia global aproximada del 5 %, aunque las niñas tienen el doble de riesgo que los niños). Las principales indicaciones para solicitar un análisis de orina con TRO (recogida con bolsa recolectora de orina) se muestran en la tabla II.
Un resultado patológico en la TRO (leucocituria ≥2+ y/o nitrituria) de una muestra recogida por bolsa, siempre debe ser confirmado en otra muestra estéril y obtener un urocultivo.
– Análisis de sangre (hemograma, PCR, PCT y hemocultivo): con la prevalencia actual de BO no está justificada la realización de un análisis de sangre a todos estos lactantes. Aunque no hay consenso, las indicaciones según algunos autores se muestran en la tabla III.
– Prueba de detección rápida de antígenos virales en nasofaringe (Influenza, adenovirus, SARS-CoV-2):
a. Virus gripe (Influenza) en muestra respiratoria en época epidémica con alta circulación del virus. La prevalencia de IBI es muy baja si el resultado es positivo, aunque siempre se deberá descartar una ITU en todas las niñas menores de 24 meses y en los niños menores de 12 meses, si la temperatura es >39ºC.
b. Adenovirus en muestra respiratoria (no presenta patrón estacional), se debe valorar en pacientes preferiblemente menores de 4 años con fiebre mayor de 39ºC, en ocasiones, se asocia hiperemia conjuntival. Si se realiza una analítica de sangre en estos lactantes, tendrán leucocitosis y neutrofilia con PCR y PCT generalmente negativas.
– Radiografía de tórax: valorar en lactantes, sobre todo, en mayores de 12 meses, con leucocitos ≥20.000/mm3 o neutrófilos ≥10.000/mm3 y una PCR >100 mg/L(21).
• TEP inestable (1 lado alterado: la apariencia o la circulación, excluyendo los pacientes con dificultad respiratoria): para evaluar a un lactante con FSF y alteración de la apariencia o de la circulación, es necesario realizar análisis de sangre (hemograma, PCR, PCT y hemocultivo) y de orina con TRO y urocultivo, independientemente del grado de la fiebre. Se considerará realizar una radiografía de tórax, si en la analítica de sangre tiene una leucocitosis >20.000/mm3 o neutrofilia >10.000/mm3 y RFA elevados, especialmente una PCR >100 mg/L(20). La realización de punción lumbar debe ser individualizada en función de la evolución del paciente.
• TEP inestable (2 o 3 lados alterados): se debe considerar que presenta una sepsis hasta que no se demuestre lo contrario y realizar un estudio completo de sepsis.
Niños mayores de 24 meses
El riesgo de presentar una IBI en niños previamente sanos con buen estado general es tan bajo, que no se recomienda la realización de pruebas complementarias de manera rutinaria. Si presentan regular/mal estado general se debe realizar estudio de sepsis.
Tratamiento
La estabilización del paciente con regular o mal estado general, es una prioridad en el manejo inicial. El tratamiento antimicrobiano debe individualizarse según la situación clínica.
A la llegada del lactante, se debe proceder con la evaluación y estabilización inicial mediante el TEP. Habitualmente, la inmensa mayoría de estos niños tienen un TEP estable y, tras su valoración, son dados de alta a domicilio con tratamiento sintomático con antitérmicos. El objetivo es aliviar el malestar que asocia la fiebre, no conseguir la normotermia. El paracetamol (7,5-15 mg/kg/dosis cada 6-8 h) o el ibuprofeno (5-10 mg/kg/dosis cada 6-8 h en niños mayores de 3 meses) son los fármacos más seguros. No hay evidencias concluyentes que apoyen la alternancia. Siempre se debe recomendar la ingesta frecuente y abundante de líquidos orales y, sobre todo, que se vigile el estado general, indicando que deben volver a consultar si aparecen los siguientes signos: decaimiento, somnolencia mayor de lo normal, irritabilidad, palidez o coloración azulada con frialdad de las extremidades cuando la fiebre baja o petequias fuera de la cara y tercio superior del tronco.
Los lactantes con TEP inestable y regular/mal estado general deben ser estabilizados (ABCDE), antes de realizar la historia y exploración física detalladas, proporcionando oxígeno en los casos necesarios, midiendo las constantes vitales (SO2, FR, TA y FC) y canalizando una vía venosa periférica para administrar líquidos intravenosos (10 mL/kg en 15-20 min) y antibioterapia de manera precoz con una revaluación clínica periódica.
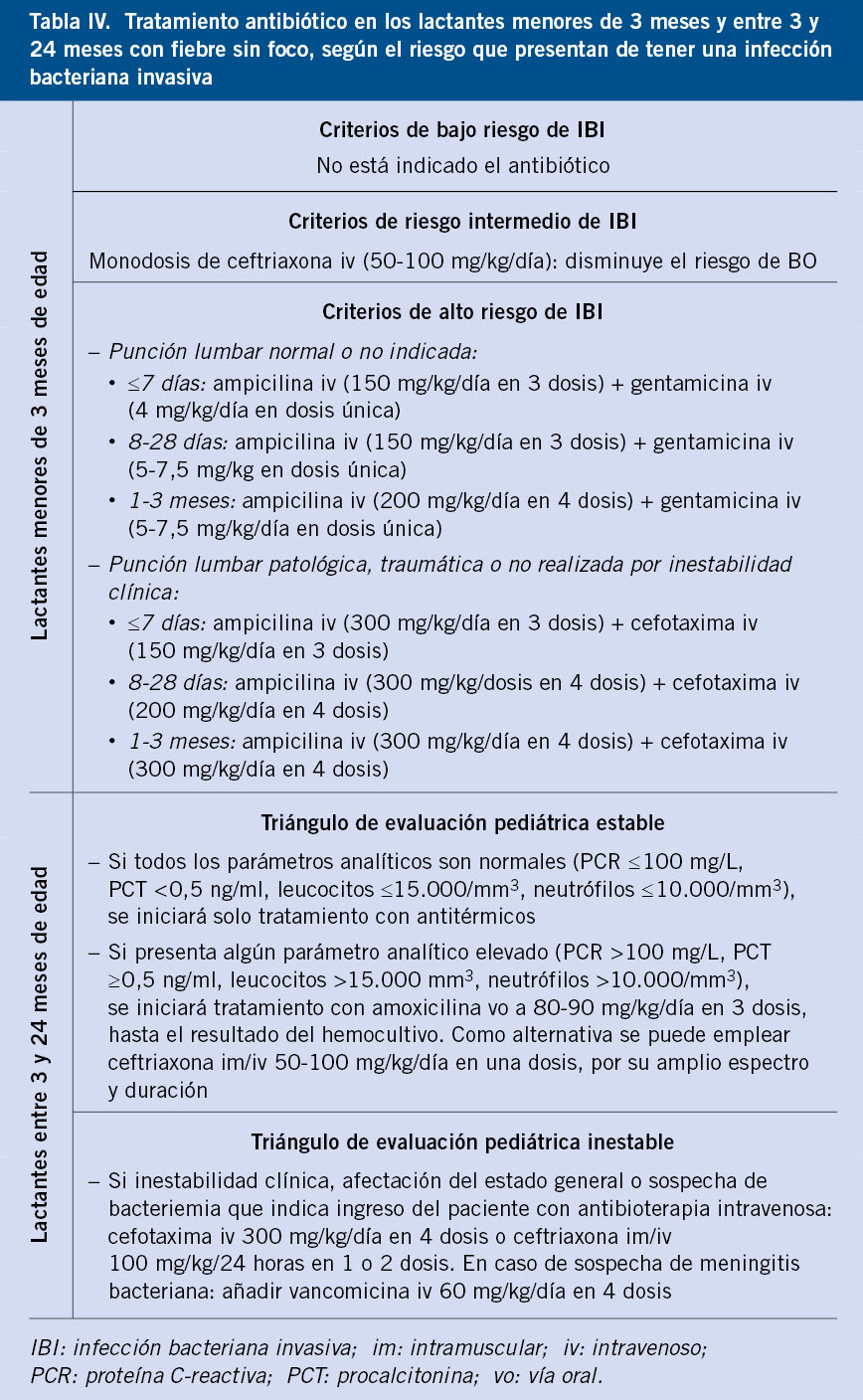
Si tras las pruebas diagnósticas se demuestra un foco de la infección, el tratamiento antimicrobiano será el específico para cada una de ellas (ITU, meningitis, neumonía, etc.). Si no se encuentra el foco, el tratamiento a pautar se muestra en la tabla IV pero deberá adaptarse a los patrones de sensibilidad del centro.
El tratamiento se mantendrá hasta obtener los resultados microbiológicos y, una vez conocidos, se adecuará al cuadro clínico y al antibiograma.
Criterios de evolución clínica
Domicilio
• Los lactantes menores de 3 meses de edad con criterios de bajo riesgo de IBI pueden ser controlados sin antibiótico de forma ambulatoria, si está garantizada la revisión por un pediatra en 24 horas (Tabla IV). Es conveniente dejarlos en observación 4-6 horas y consensuar con los padres el alta a domicilio. Se debe considerar una atención más cauta en aquellos lactantes que consulten con tiempos de evolución más recortados (<2 horas).
• Los lactantes mayores de 3 meses de edad con buen estado general, también pueden ser dados de alta a domicilio. En función de los resultados de los análisis de sangre, se pautará tratamiento sintomático +/- antibiótico oral (Tabla IV). Deben ser controlados por un pediatra en 48-72 horas, si persiste la fiebre.
Observación
• Lactantes menores de 3 meses de edad con criterios de riesgo intermedio de IBI. Se recomienda prolongar la observación, al menos, 12 horas desde el inicio de la fiebre y, si el paciente se mantiene estable, puede ser dado de alta a domicilio (Tabla IV).
• Lactantes entre 3 y 24 meses de edad con PCT ≥2 ng/mL, valorar prolongar la observación durante 10-12 horas y, si el paciente se mantiene estable, puede ser dado de alta a domicilio con antibiótico (Tabla IV).
Ingreso en planta de Pediatría
• Lactantes menores de 3 meses de edad con TEP estable y criterios de alto riesgo de IBI (Tabla IV).
• Lactantes menores de 3 meses de edad con criterios de riesgo intermedio de IBI que, tras una observación prolongada, no presentan buen estado general (Tabla IV).
• Lactantes mayores de 3 meses de edad con buen estado general, en los que se haya realizado una punción lumbar y el resultado del análisis del LCR no sea sugestivo de meningitis bacteriana (Tabla IV).
• Niños mayores de 24 meses que tengan sospecha de meningitis bacteriana.
Ingreso en cuidados intensivos
• Lactantes menores de 24 meses con TEP inestable que cumplan criterios de sepsis o tengan sospecha de meningitis bacteriana (Tabla IV).
Función del pediatra de Atención Primaria
• Identificar a los lactantes y preescolares con un TEP alterado, proceder a su estabilización (ABCDE) en los casos necesarios, con toma de constantes vitales (SO2, FR, TA y FC) y administración de antibioterapia precoz si cumple criterios de sepsis.
• Derivar a un centro hospitalario a los lactantes menores de 3 meses de edad con FSF, para realización de pruebas complementarias y observación hospitalaria.
• Derivar a un centro hospitalario a los lactantes entre los 3 y 24 meses de edad con un análisis de orina con tira reactiva normal, fiebre muy alta y/o vacunación incompleta, para realización de pruebas complementarias y observación hospitalaria.
• Informar a los cuidadores sobre lo que hay que vigilar en los lactantes febriles y cómo deben actuar.
Conflicto de intereses
No hay conflicto de interés en la elaboración del manuscrito. Declaración de intereses: ninguno.
Bibliografía
Los asteriscos muestran el interés del artículo a juicio de los autores.
1. Gómez B, Bressan S, Mintegi S, Da Dalt L, Blázquez D, Olaciregui I, et al. Diagnostic value of procalcitonin in well-appearing young febrile infants. Pediatrics. 2012; 130: 815-22.
2. Non-contact thermometers for detecting fever: A review of clinical effectiveness. Rapid Response Report: Summary with Critical Appraisal. Ottawa (ON): Canadian Agency for Drugs and Technologies in Health. 2014.
3. Byington CL, Rittichier KK, Bassett KE, Castillo H, Glasgow TS, Daly J, et al. Serious bacterial infections in febrile infants younger than 90 days of age: the importance of ampicillin-resistant pathogens. Pediatrics. 2003; 111: 964-8.
4. Powell EC, Mahajan PV, Roosevelt G,
Hoyle Jr JD, Gattu R, Cruz AT, et al. Febrile Infant Working Group of the Pediatric Emergency Care Applied Research Network (PECARN). Epidemiology of bacteremia in febrile infants aged 60 days and younger. Ann Emerg Med. 2018; 71: 211-6.
5. Greenhow TL, Hung YY, Herz AM, Losada E, Pantell RH. The changing epidemiology of serious bacterial infections in young infants. Pediatr Infect Dis J. 2014; 33: 595-9.
6. Greenhow TL, Hung Y-Y, Herz A. Bacteremia in Children 3 to 36 Months Old After Introduction of Conjugated Pneumococcal Vaccines. Pediatric. 2017; 139: e20162098.
7. Gómez B, Hernández-Bou S, García-García JJ. Bacteraemia Study Working Group from the Infectious Diseases Working Group, Spanish Society of Pediatric Emergencies (SEUP). Bacteremia in previously healthy children in emergency departments: clinical and microbiological characteristics and outcome. Eur J Clin Microbiol Infect Dis. 2015; 34: 453-60.
8.*** Dieckmann RA, Brownstein D, Gausche-Hill M. The pediatric assessment triangle: a novel approach for the rapid evaluation of children. Pediatr Emerg Care. 2010; 26: 312-5.
9. Barreiro-Parrado A, López E, Gómez B, Lejarzegui A, Fernández-Uria A, Benito J, et al. Rate of invasive bacterial infection in recently vaccinated young infants with fever without source. Arch Dis Child. 2022; archdischild-2022-324379.
10. Mahajan P, Kuppermann N, Mejías A, Suárez N, Chaussabel D, Casper TC, et al; Pediatric Emergency Care Applied Research Network (PECARN). Association of RNA Biosignatures With Bacterial Infections in Febrile Infants Aged 60 Days or Younger. JAMA. 2016; 316: 846-57.
11.*** Gómez B, Mintegi S, Bressan S, Da Dalt L, Gervaix A, Lacroix L; European Group for Validation of the Step-by-Step Approach. Validation of the “Step-by-Step” approach in the management of young febrile infants. Pediatrics. 2016; 138: e20154381.
12.** Tzimenatos L, Mahajan P, Dayan PS, Vitale M, Linakis JG, Blumberg S, et al. Pediatric Emergency Care Applied Research Network (PECARN). Accuracy of the urinalysis for urinary tract infections in febrile infants 60 days and younger. Pediatrics. 2018; 141: e20173068.
13. Gómez B, Mintegi S, Benito J. Group for the Study of Febrile Infant of the Ri-SeuP-SPERG Network. A Prospective Multicenter Study of Leukopenia in Infants Younger Than Ninety Days With Fever Without Source. Pediatr Infect Dis J. 2016; 35: 25-9.
14. Pintos C, Mintegi S, Benito J, Aranzamendi M, Bonilla L, Gómez B. Blood enterovirus polymerase chain reaction testing in young febrile infants. Arch Dis Child. 2021; 106: 1179-83.
15. Blaschke AJ, Korgnski EK, Byington CL. Meningitis in well-appearing febrile infants aged 1-90 days. Open Forum Infect Dis. 2018; 5: S133.
16. Martínez E, Mintegi S, Vilar B, Martinez MJ, López A, Catediano E, et al. Prevalence and predictors of bacterial meningitis in young infants with fever without a source. Pediatr Infect Dis J. 2015; 34: 494-8.
17. Wang ME, Biondi EA, McCulloh RJ, Garber MD, Natt BC, Lucas BP, et al. Testing for meningitis in febrile well-appearing young infants with a positive urinalysis. Pediatrics. 2019; 144: e20183979.
18. Ralston S, Hill V, Waters A. Occult Serious Bacterial Infection in Infants Younger Than 60 to 90 Days with Bronchiolitis. A Systematic Review. Arch Pediatr Adolesc Med. 2011; 165: 951-6.
19. Mintegi S, García-García JJ, Benito J, Carrasco-Colom J, Gómez B, Hernández-Bou S, et al. Rapid Influenza test in young febrile infants for the identification of low-risk patients. Pediatr Infect Dis J. 2009; 28: 1026-8.
20. Gangoiti I, Rodríguez E, Zubizarreta A, Benito J, Mintegi S. Prevalence of Occult Bacteremia in Infants With Very High Fever Without a Source. Pediatr Infect Dis J. 2018; 37: e271-3.
21. Mintegi S, Benito J, Pijoan JI, Marañón R, Peñalba A, González A, et al. Occult pneumonia in infants with high fever without source: a prospective multicenter study. Pediatr Emerg Care. 2010; 26: 470-4.
22. Gómez B, Mintegi S. Fiebre sin foco. Pediatr Integral. 2018; XXII: 211-8. Disponible en: https://www.pediatriaintegral.es/publicacion-2018-07/fiebre-sin-foco-2018/.
Bibliografía recomendada
– Dieckmann RA, Brownstein D, Gausche-Hill M. The pediatric assessment triangle: a novel approach for the rapid evaluation of children. Pediatr Emerg Care. 2010; 26: 312-5.
Artículo que describe el triángulo de evaluación pediátrica (TEP), que es una herramienta rápida y útil para la valoración inicial del paciente pediátrico. Se considera que es inestable si alguno de los 3 lados está alterado.
– Gómez B, Mintegi S, Bressan S, Da Dalt L, Gervaix A, Lacroix L; European Group for Validation of the Step-by-Step Approach. Validation of the “Step-by-Step” approach in the management of young febrile infants. Pediatrics. 2016; 138: e20154381.
Artículo prospectivo de ámbito europeo, que valida el algoritmo de actuación en los lactantes menores de 3 meses de edad con fiebre sin foco. Identifica a aquellos con bajo riesgo de tener una infección bacteriana invasiva de manera más precisa que los algoritmos propuestos previamente.
– Tzimenatos L, Mahajan P, Dayan PS, Vitale M, Linakis JG, Blumberg S, et al. Pediatric Emergency Care Applied Research Network (PECARN). Accuracy of the urinalysis for urinary tract infections in febrile infants 60 days and younger. Pediatrics. 2018; 141: e20173068.
Estudio multicéntrico desarrollado por la Red de Investigación de Urgencias Pediátricas de los EE.UU. (PECARN), que evalúa las características del análisis de orina para diagnosticar una infección del tracto urinario en los lactantes menores de 60 días de vida con fiebre.
| Caso clínico |
|
Un neonato de 26 días de vida consulta en su centro de salud por fiebre (temperatura axilar máxima de 38,5ºC) desde hace 2 horas, sin ningún síntoma asociado. No hay ambiente epidémico familiar. Antecedentes perinatales: embarazo controlado con ecografías normales, exudado vaginal Streptococcus agalactiae negativo, parto a término, vaginal eutócico, sin fiebre materna durante el parto. El peso al nacer fue 3,1 kg. Está con lactancia materna exclusiva a demanda y todavía no ha iniciado la vacunación. Triángulo de evaluación pediátrica estable. Exploración física sin alteraciones significativas. Debido a que es un lactante menor de 3 meses de edad, es derivado a un servicio de urgencias pediátrico para realizar pruebas complementarias.
|






 Fever of unknown origin
Fever of unknown origin