|
| Temas de FC |
J. Valdés Rodríguez*, N. Bolufer Vigrana**
*Pediatra extrahospitalario. Acreditado en Medicina del Adolescente. **Médico psicoterapeuta
| Resumen
Los problemas escolares incluyen tanto al alumno que suspende como al que ha tenido un descenso brusco y mantenido en su rendimiento. Pueden ocasionar por sí mismos una importante alteración en la vida y la salud del adolescente, y deben ser evaluados. El diagnóstico se basa en la anamnesis (con especial atención al medio familiar, escolar y social) y en la exploración. Una vez descartadas las enfermedades físicas propias de la edad, el pediatra derivará al paciente a los diferentes especialistas (psicopedagogía, psiquiatría infanto-juvenil), coordinando la relación entre la familia, los terapeutas y la escuela, vigilando la evolución y prestando apoyo continuo al adolescente. El principal papel de la Pediatría Extrahospitalaria es la prevención tanto primaria (educación para la salud) como secundaria (diagnóstico precoz). |
| Abstract
School problems include both the student who suspends and the student who has had a steep and sustained drop in performance. They can themselves cause an important alteration in the life and health of the adolescent, and they must be evaluated. |
Palabras clave: Adolescencia; Problemas escolares (PE); Pediatría de Atención Primaria
Key words: Adolescence; School problems (PE); Primary Care Pediatrics
Pediatr Integral 2017; XXI (4): 270-277
Problemas escolares en la adolescencia
Introducción
Los problemas escolares (PE) incluyen tanto al alumno que suspende, como al que ha tenido un descenso brusco en su rendimiento. Por su repercusión en la vida del adolescente, es obligado llegar a un diagnóstico.
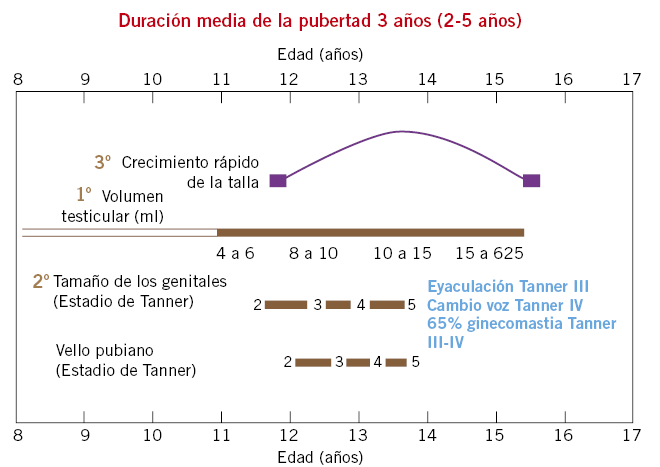
Por delimitar el concepto, y tomando como adolescentes (según la OMS) a aquellos individuos comprendidos entre los 10 y 19 años de edad, deberíamos hablar de aquellos alumnos que empiezan a plantear problemas escolares a partir de los dos últimos cursos de la Educación Primaria, o lo hacen hasta que termina el periodo que el Sistema Educativo les impone: la Educación Secundaria Obligatoria (ESO). Estas son las edades más conflictivas para las dificultades escolares, porque coinciden la metamorfosis puberal por un lado, con los cambios de sistema educativo por otro (el paso al Instituto), y todas las enormes adaptaciones psicosociales que el adolescente va a tener que ir haciendo. No obstante, teniendo en cuenta la gran variabilidad del desarrollo y la obligación que como médicos tenemos de respetar individualmente a cada paciente, es complicado hablar de límites de edad.
En la adolescencia, debemos considerar de forma general dos formas de presentación:
• “El que suspende”: alumno que sin limitaciones intelectuales conocidas, no alcanza los niveles de aprendizaje esperados para su edad, según un determinado plan de estudios y/o una institución escolar. En estos casos, todo el mundo reconoce que hay un problema, y salta la alarma.
• “El cambio a peor”: alumno que aun cumpliendo los objetivos establecidos, tiene un descenso brusco y mantenido en su rendimiento habitual. Aquí es posible que tardemos en reaccionar, porque los resultados se mantienen dentro de lo aceptable. Pero, también, hay (o habrá) un problema y así hay que enfocarlo.
Sabemos que de una forma u otra, los PE se presentan con una alta frecuencia a la edad que nos ocupa (para saber el alcance exacto, habría que ponerse de acuerdo primero en el concepto, y este es muy variable de unos investigadores a otros). Pero el hecho de que sea un fenómeno frecuente, no debe llevarnos a banalizar pensando que “… son cosas de la edad” o “…ya se le pasará”, que son frases que acompañan a menudo a la mala prensa que tienen los adolescentes. No debemos hacerlo, porque las dificultades escolares pueden ser producidas por algunas enfermedades que pueden aparecer a esta edad y deben ser descartadas, y porque con mayor frecuencia, los problemas en un entorno tan importante para el adolescente como es la escuela, son capaces por sí mismos de provocar comportamientos de alto riesgo para su salud.
Por tanto, cuando surjan los PE, debemos tratar de llegar a un diagnóstico, que como en cualquier otro tipo de enfermedad, es la base de un tratamiento adecuado.
Causas
Lo primero es conocer la historia escolar previa. Si los PE escolares aparecen de forma inesperada, una vez analizadas las posibles causas en el adolescente, habrá que valorar la influencia de los factores familiares, escolares y sociales.
Por su evolución en el tiempo, podemos dividir los PE en dos grupos:
1. Los que tienen dificultades desde los primeros cursos de escolarización. Puede suceder que, aunque hayan sido conocidas, se haya seguido una mala orientación en su tratamiento, o que a pesar de las limitaciones, estas hayan sido suplidas de alguna manera por el niño y pasen desapercibidas. Es evidente que este último supuesto es más improbable, porque la creación de gabinetes psicopedagógicos en guarderías y escuelas infantiles, hace que el diagnóstico sea precoz. Por otro lado, y aunque la decisión depende incluso de cada centro, los objetivos de lectura/escritura ya aparecen en el último curso de Educación Infantil. Por tanto, lo lógico es suponer que cualquier alumno que en 2º curso de Primaria no ha conseguido el nivel esperado de lectura, escritura, cálculo y/o capacidad de atención, va a ser considerado como un alumno que necesita un diagnóstico y también una atención especial y específica(1).
En cualquier caso, es complicado que conforme avanzan las necesidades de aprendizaje, niños con trastornos específicos (dislexia como problema más frecuente), coeficiente intelectual límite, y otros problemas mentales o del neurodesarrollo, lleguen a los últimos cursos de la Educación Primaria sin diagnosticar.
Un ejemplo de esta problemática que interesa comentar, por su frecuencia y porque es una enfermedad en constante revisión, es el trastorno de déficit de atención e hipercinesia (TDHA)(2). Si no es muy acusado, o si el niño es muy inteligente, puede haber compensado el problema con la ayuda de un maestro que lo conozca, y haya sabido conducirlo durante los primeros cursos, o con tratamientos temporales que han sido retirados por una evolución aceptable o por miedo a la medicación continuada. Mención especial hay que hacer al subtipo inatento, que suele ser más frecuente en chicas. En estos casos, la falta de atención es mayor que la impulsividad/hiperactividad, y al no originar los conflictos habituales, pasan más desapercibidos. De todas formas, a partir de 6º de Primaria, cuando cambia el sistema y pasa a tener un profesor para cada asignatura, se pone de manifiesto de forma evidente la dificultad de concentración (la hiperactividad suele disminuir a estas edades de forma general) y, especialmente, en determinadas materias o con profesores poco atractivos para ellos. Tan pronto pueden rendir mucho, como en determinados momentos, inexplicablemente, poco o nada. Tienen problemas para organizarse, necesitan de un esfuerzo mayor y mantenido para superar las dificultades y, a pesar de ello, acaba por afectarse el rendimiento global. La forma en que se produce, suele generar reproches por parte de padres y maestros, lo que aumenta la angustia que viven estos chicos y se favorece la aparición de otros síntomas psiquiátricos (depresión, comportamientos antisociales, abuso de alcohol y/o drogas) que son frecuentes en adolescentes con TDHA.
2. El alumno con rendimiento normal, y que empieza a fracasar en los estudios. Esta es la forma de presentación habitual en adolescentes. Las causas pueden variar según la edad y el momento del desarrollo puberal, pero lo que fundamentalmente hay que considerar es: el tiempo de evolución, la rapidez con que se instauran los problemas y su influencia, tanto sobre el rendimiento escolar como en la dinámica familiar y social del adolescente.
Cuanto más bruscos y mayor repercusión tengan los PE, más importante debe ser para el médico buscar las causas.
En cualquier etapa educativa, las dificultades escolares se producen por una conjunción de factores, que se interrelacionan entre sí y que afectan al INDIVIDUO, su FAMILIA, la ESCUELA y el ENTORNO SOCIAL. Es difícil que uno solo de ellos sea el responsable del problema, y desde luego, es imposible solucionarlo sin la participación de todos. En la adolescencia, todo ello es todavía más evidente.
Factores individuales
Enfermedades físicas propias de la edad
• Alteraciones de la audición o la visión.
• Enfermedades del sistema nervioso: tumores cerebrales, epilepsia.
• Patología de la glándula tiroidea.
• Trastornos nutricionales: carencia de hierro.
• Intoxicaciones (plomo) y consumo habitual de alcohol y/o drogas.
• Otras enfermedades (rinitis alérgica crónica, úlcera péptica, infecciones: tuberculosis, cáncer, síndrome de fatiga crónica…) que al principio pueden dar unos síntomas poco llamativos, y con la evolución van causando un cansancio progresivo y una dificultad para mantener la atención.
Todos estos procesos pueden manifestarse inicialmente como dificultades escolares y, por tanto, ante el problema que nos ocupa, lo primero será estar seguros de que el adolescente no tiene una enfermedad física.
Enfermedades psíquicas
En general, en cualquier cambio a peor en un adolescente, sea en el carácter, el comportamiento o el rendimiento escolar, una vez descartadas las enfermedades físicas debemos pensar en una depresión. Y esto es así, en primer lugar, por la frecuencia. En segundo, porque a diferencia de otros cuadros psiquiátricos con unos síntomas más evidentes, el fracaso súbito en los estudios puede ser el primer o el único síntoma de una depresión enmascarada. Y en tercer lugar, por la relación de las depresiones con la segunda causa de mortalidad en adolescentes: el suicidio (aunque aquí entren en consideración otro tipo de factores, como la personalidad del estudiante y su dinámica familiar).
Hace 20 años, hicimos una revisión del tema en esta misma revista(3). En este tiempo, el acceso de los niños a Internet es cada vez más precoz y el delito que más ha crecido entre los adolescentes (y en el que siempre debemos pensar) es el acoso escolar en sus distintas formas. Debemos tenerlo en cuenta, sobre todo, si no se ha producido el contacto con las drogas. Según la última encuesta ESTUDES(4), entre los escolares españoles, el inicio del consumo de drogas legales (alcohol, tabaco) se produce entre los 13,8/13,9 años, los hipnosedantes 13,9 y el cannabis a los 14,8 y, sin embargo, según la Guía de Ciberacoso para Profesionales(5), más del 41% de los niños españoles de 11 años de edad tiene un teléfono móvil.
Sabemos que las enfermedades psíquicas merman de forma importante la capacidad de aprendizaje, pero una cuestión que hay que considerar en casos con mala evolución sería: ¿es el problema emocional la causa o la consecuencia de los problemas escolares? Cuando estos aparecen, se genera una situación de ansiedad y comienzan a alterarse las relaciones con maestros y con los padres. La autoestima del adolescente desciende y, si la presión de los adultos centrada en el rendimiento escolar se mantiene, se le añaden sentimientos de culpabilidad. Todo ello puede provocar distintas formas de reaccionar: puede generar más ansiedad, irritabilidad y rechazo hacia el estudio o bien una actitud pasiva con sensación de impotencia y desmotivación. En cualquier caso, empieza a desconfiar que pueda superar nuevos obstáculos, no ve la salida, tiene una sensación de pérdida de control, y acaba por interiorizar el fracaso escolar como suyo, y asumirlo como algo peor: un fracaso existencial. En esas condiciones, es difícil que el adolescente sea capaz de dominar los impulsos (soledad-tristeza, rabia-agresividad…) y esto puede llevarle a diversas conductas de riesgo (borracheras, abuso de sustancias, huidas, accidentes, intentos de suicidio…) de consecuencias imprevisibles.
Está claro que acabamos de describir una situación límite, con la que desgraciadamente nos sorprenden las noticias de cuando en cuando, pero afortunadamente, poco frecuente. Lo importante es, que sin alarmismos, entendamos que las dificultades escolares, como cualquier otra enfermedad, puede llegar a convertirse en un problema grave, si no conseguimos modificar su evolución.
La familia
En ella, pueden originarse o no algunas causas de PE, pero donde adquiere una extraordinaria importancia es en la búsqueda de soluciones y, sobre todo en su papel preventivo. La familia actúa seleccionando y modificando los estímulos que le llegan del exterior: que unas malas notas constituyan o no una tragedia, depende de cómo se asimile en esa familia.
Dos son los conceptos en los que conviene profundizar: la relación existente entre los diversos miembros de una familia y la organización de los distintos aspectos de la vida cotidiana en ese núcleo familiar.
La dinámica familiar
El clima afectivo familiar influye decisivamente. Todo lo que suceda en casa, repercute en el adolescente y en su rendimiento escolar, independientemente de sus capacidades. De la actitud de sus padres hacia él, dependerá que pueda desarrollarlas. Todas las encuestas nos dicen que para el adolescente es su familia…, aunque no lo reconozca. Por tanto, si al valorar los PE descubrimos conflictividad en la familia, será la primera cuestión a resolver.
Por su frecuencia, una de las causas más importantes son las separaciones de los padres, cuando estas no se hacen pensando en los hijos. A la inseguridad y el sentimiento de enfado del adolescente, hay que añadir las actitudes de abandono, sobreprotección o permisividad, y otras formas de chantaje emocional a la que se ve sometido el hijo por las partes en conflicto y que, en la mayoría de casos, la Justicia es incapaz de resolver, porque tampoco tiene en cuenta, prioritariamente, las necesidades del menor, sino los derechos de los adultos. Es fácil comprender cómo, en estas situaciones, el adolescente corre un alto riesgo de tener PE.
Organización familiar
Existen otros factores dentro de la familia, que por secundarios que puedan parecer, también influyen en la motivación por el estudio y en la capacidad de concentración, y que deben haberse establecido con anterioridad, desde las primeras etapas de la escolarización, porque son importantes para la prevención de los PE. Esta es una función clave, que el pediatra debe desarrollar en los exámenes de salud previos a la adolescencia.
En el hogar, ha de existir un cierto orden establecido, con participación de los distintos miembros de la familia. Los adolescentes deben colaborar en las tareas de la casa. Es una forma de potenciar su autonomía, estimular la responsabilidad y favorecer una actitud positiva hacia las cosas bien hechas. En este ambiente, tiene importancia respetar unos horarios regulares que obliguen a unas horas mínimas de sueño(6) y permitan una adecuada distribución del tiempo para las comidas. Recordemos que no solo es necesaria una buena nutrición…, el momento de comer es, a veces, la única oportunidad para la convivencia y está completamente demostrado el efecto preventivo de, al menos, una comida en familia al día.
La habitación de un adolescente, suele ser un reducto inexpugnable de su identidad y conviene no crear conflictos al respecto. No obstante, el entorno físico puede jugar un papel nada despreciable en la predisposición para estudiar y habrá que intentar “negociar” algunos aspectos. El sitio de estudio debe ser: cómodo (cuidado con los vicios posturales), suficientemente espacioso y con luminosidad natural. La penumbra, el uso abusivo de luz artificial, múltiples obstáculos sobre la mesa o un exceso de estímulos visuales o auditivos, producen una fatiga fácil y rompen la armonía necesaria para la actividad intelectual.
Mención especial hay que hacer a la distribución del tiempo libre. Hay algunos estudiantes que desconocen su existencia (largos desplazamientos hacia “los mejores colegios”, casi todos en la periferia de las grandes ciudades, les suponen la estéril pérdida de 2 y 3 horas diarias; un apretado programa de actividades extraescolares, les obliga a sentarse a estudiar cuando llegan a casa, tras una jornada que empezó 12 horas antes…), y los adolescentes necesitan disponer de tiempo para relacionarse con sus amigos, hacer deporte o simplemente descansar.
La actividad física, tiene una importancia decisiva para mantener la salud, contribuir a la educación, mejorar el rendimiento intelectual y prevenir la adquisición de hábitos nocivos. Nunca debería pasarse a un segundo plano, ni siquiera en caso de dificultades académicas y, sobre todo, si al adolescente le gusta y destaca (se puede regular la actividad si hay que organizar mejor el tiempo, pero no quitar).
Un ambiente familiar amante de la cultura, contribuirá al interés por el conocimiento y la mejora personal de sus componentes. Desde las primeras etapas, debe fomentarse en los niños el hábito por la lectura, para posteriormente ir participando con ellos en aquellas expresiones culturales que prefieran (conciertos, exposiciones, teatro, cine…).
TV-videojuegos-ordenadores-teléfonos móviles. Como se ha comentado, la irrupción de las Tecnologías de la Información y la Comunicación (TIC) y, sobre todo, el acceso precoz a Internet (en España entre los 9 y los 11 años de edad), es lo que más está influyendo en las vidas de niños y adolescentes en la última década. La sociedad de consumo va a seguir induciendo y justificando su uso y corresponde a los padres poner los límites y las condiciones de utilización desde temprana edad. Es tan complicado, que parece una utopía no poner a los niños ante las pantallas antes de los dos años de edad como recomiendan las Sociedades Científicas, y debería ser una realidad.
Existen pruebas suficientes de los peligros de su abuso, sobre el comportamiento y el rendimiento escolar. La familia puede aprovechar sus indudables posibilidades didácticas, pero limitando el tiempo de utilización (nunca más de 1-2 horas de promedio día), evitando el acceso fácil (no deben estar en los dormitorios) y el uso indiscriminado. En líneas generales, podemos recomendar que cualquier momento no es válido (durante las comidas, antes de finalizar las tareas, al irse a dormir…), que los programas y la publicidad han de ser analizados conjuntamente y el zapping desterrado(7). De la misma forma, conviene tener unas normas claras para el uso de internet y el abuso de los teléfonos móviles(8).
El fin de semana y el consumo de drogas legales. No podemos aislar a los adolescentes para protegerlos, pero tampoco es lícito inhibirse ante costumbres que generan situaciones de alto riesgo e influyen negativamente, como ya se ha comentado, en el rendimiento escolar (alteración de los ritmos sueño-vigilia, alto consumo de alcohol, accidentes). Sin tratos autoritarios, debemos intentar conocer el grupo de amigos (sus hábitos, los medios de transporte que utilizan en los desplazamientos…), y saber llegar a un acuerdo sobre las condiciones del regreso a casa. Siempre debe existir una posibilidad para negociar.
La escuela
Debemos investigar los diferentes condicionantes que intervienen, para ayudar a los padres a tomar una decisión.
El sistema educativo
Cuando se ejecuta (en el sentido más literal del término) un determinado plan de estudios, nos podemos encontrar con un primer problema: la falta de respeto a la individualidad de los alumnos. Los pediatras conocemos bien lo distinta que es la maduración en todos los aspectos del desarrollo de unos pacientes a otros, y en el caso de los adolescentes, lo determinantes que pueden ser para su estabilidad psicoafectiva, la asincronía en los cambios puberales entre compañeros del mismo y de distinto sexo. Esta variabilidad física, emocional e intelectual, se tiene poco en cuenta a la hora de valorar el rendimiento académico. Un sistema educativo excesivamente regulado (con opciones y contenidos predeterminados), poco flexible (han de cumplirse “objetivos” independiente de los alumnos), con un nivel de exigencia que supera las capacidades del adolescente, va a condicionar la aparición de situaciones de inadaptación.
Otro problema dentro del sistema: sobredimensionar la importancia de la consecución de un título universitario, como única vía de éxito posible, infravalorando otras opciones perfectamente equiparables para la realización personal y más asequibles a las características individuales, como pueden ser los distintos grados de Formación Profesional.
El ambiente escolar
Haciendo un paralelismo con el factor familiar, haremos hincapié en dos conceptos: el ideario del colegio y la organización.
El alumno debe saber en qué tipo de colegio está, aceptarlo y recibir un trato coherente por parte de sus padres y los profesores (si existen diferencias, estas no deben airearse en presencia de los chicos). Sin criterios claros, será difícil que pueda mantenerse un mínimo de disciplina, orden y respeto mutuos, que son necesarios para favorecer la motivación hacia el estudio.
Es evidente, que una escuela con adecuadas infraestructuras (aulas luminosas, con buen aislamiento térmico y sonoro, instalaciones lúdicas o deportivas…), aumentan las posibilidades didácticas, pero no garantizan el buen funcionamiento. Hay dos condiciones que influyen negativamente que son: el cambio frecuente de profesores y el excesivo número de alumnos. Además, hay que indagar sobre la duración de las clases, los descansos y la programación de las asignaturas (las que exigen mayor atención deberían ser por la mañana). Un ejemplo claro de cómo puede influir la organización de los horarios, la tenemos en la aplicación de la “jornada intensiva”: no tiene en cuenta los ritmos de sueño de los adolescentes, ni los problemas nutricionales que implica (desayunos acelerados y escasos, recreos cortos donde consumen comida basura y la comida principal del día a una hora inadecuada).
El profesor
Todos tenemos experiencia de la influencia del buen maestro sobre el agrado hacia la materia que explicará y el interés que teníamos por corresponderle. La interacción profesor-alumno es decisiva, tanto en el origen como en el tratamiento de un PE.
En adolescentes, con varios profesores en las distintas asignaturas, esta coordinación se hará a través de la figura del tutor, que debe ser también la referencia para el intercambio de informaciones escolares y/o médicas con el pediatra o terapeuta, y es la pieza clave para la búsqueda y aplicación de las posibles soluciones. De todas formas, aunque la familia tiene que colaborar y respetar al maestro, hay que dejar claro que las tareas escolares son un asunto entre el adolescente y sus profesores, y cada uno debe cumplir con su función.
Los compañeros
Para un adolescente, no hay nada más importante que sentirse aceptado por su grupo de amigos. Se debe preguntar por la adaptación del muchacho al resto de la clase, cómo son sus compañeros como estudiantes (pueden preferir unas malas notas, antes que un fracaso relacional) y qué grado de concordancia sociocultural hay entre ellos.
No todos los adolescentes son igual de vulnerables a estas cuestiones, y los padres pueden sentirse atrapados por el sistema educativo o por un colegio cuyo funcionamiento no pueden modificar. Pero una vez analizadas, deben tomar la decisión que más convenga a su hijo en ese momento, porque en definitiva son los primeros responsables de su educación.
El entorno social
La relación entre la propia cultura del alumno y la del medio escolar puede no ser coincidente (emigrantes, bilingüismo…) y ocasionar problemas de adaptación.
Unas condiciones socioeconómicas adversas (paro o trabajo temporal, grupos marginales…) influyen negativamente sobre el factor familiar o pueden empujar al adolescente a integrarse en grupos o pandillas con diversas conductas de riesgo. En estas condiciones, lo habitual, es el abandono de las tareas escolares.
Diagnóstico
Se basa fundamentalmente en la anamnesis y la exploración, y debe completarse con un informe escolar
Ante una disminución inexplicable del rendimiento académico, lo primero es descartar una enfermedad física. Es fácil hacerlo si la consulta con el adolescente se consigue hacer correctamente. Con una detallada historia clínica y una exploración completa, en pocas ocasiones es necesario pedir pruebas analíticas o de otro tipo, pero deben fundamentarse en los hallazgos obtenidos durante la consulta y hacerse de forma escalonada según los resultados que vayamos obteniendo (Tabla I).
Lo siguiente es tener un informe escolar, para saber las capacidades del alumno desde los primeros cursos. Si esto no fuera posible, haremos una valoración psicopedagógica individual (puede tener otras hechas anteriormente junto a sus compañeros, pero es mejor repetirla) para conocer con exactitud si existe alguna limitación intelectual o de otro tipo para el aprendizaje. Cuando estamos ante un estudiante sin dificultades previas, hay que insistir en la necesidad de hacer constar en la historia clínica las impresiones de su tutor en cuanto a la génesis del problema, lo que nos orientará tanto para el diagnóstico como para las posibilidades de tratamiento.
En caso que todo lo anterior sea normal, es muy probable que estemos ante un problema emocional, y tendremos que remitir al paciente y su familia al psiquiatra infanto-juvenil. El pediatra debe insistir en la necesidad de esta evaluación conjunta (paciente-familia) indispensable, tanto para el diagnóstico como para la búsqueda de soluciones.
Tratamiento
Cuando se necesite un enfoque multidisciplinario, el pediatra coordinará la relación entre la familia, los terapeutas y la escuela, asegurándose que la evolución es favorable y prestando apoyo continuo al adolescente.
De la misma forma que es raro, que exista una sola causa desencadenante del problema, en el tratamiento, lo fundamental es coordinar a las distintas partes. Mientras se llevan a cabo las medidas terapéuticas oportunas (apoyo pedagógico, terapia individual y/o familiar, fármacos), la comunicación médico-familia- tutor es indispensable.
Los padres deben tener criterios uniformes sobre sus actitudes hacia el hijo y las medidas a tomar en la familia. En la tabla II, se incluyen una serie de consejos que pueden servir al pediatra para hablar con los padres, cuando aparecen los PE.
Un buen maestro preocupado por su alumno, que ensalce sus progresos y cualidades, y le corrija con cariño (y en privado), será determinante en el éxito del tratamiento. Un colegio “ejecutor” de sistemas y normas por encima de los individuos, un maestro desmotivado y poco participativo, nos deben hacer recapacitar sobre la conveniencia de darle al muchacho otra oportunidad en un ambiente distinto.
El pediatra, aunque derive el caso a otros especialistas, no debe delegar en ellos toda la responsabilidad. Sigue siendo el médico de confianza del adolescente y su familia, y tiene que ir interesándose por la evolución del problema.
Debemos tener en cuenta que, el fin prioritario no es mejorar los resultados académicos de ese curso, sino delimitar cuáles son las capacidades del adolescente para no pedirle objetivos imposibles (las expectativas deben ser reales: si no lo son, aumentaremos su frustración y el nivel de conflicto), estimular y potenciar sus destrezas para levantar su autoestima (siempre habrá algo que sepa hacer bien) y orientarle en el camino a seguir según sus posibilidades y sus preferencias.
En última instancia, lo importante es no abandonar. Seguir haciendo algo útil, buscar alternativas en los estudios o incluso, en caso de ser necesario, un descanso en los mismos, incorporar al mundo laboral. Los PE no deben convertirse en un fracaso existencial.
Función del pediatra de Atención Primaria
El papel primordial de la pediatría de AP está en la PREVENCIÓN:
• Prevención PRIMARIA, contribuyendo a la educación para la salud, que en el tema que nos ocupa, se centra en los hábitos de estudio y el resto de factores que los condicionan, y que hemos analizado al hablar de la importancia de una buena dinámica y organización familiar(9). En este sentido, hay que resaltar, la postura decidida que debe tomar el pediatra desde los primeros meses de vida, en cuanto al buen uso de las pantallas y el resto de las TIC. Por otro lado, sin una adecuada formación en estos temas, no es posible la prevención: para atender adolescentes, los pediatras deben ponerse al día sobre las distintas formas de comunicación de los jóvenes de hoy(10).
• Prevención SECUNDARIA, intentando hacer un diagnóstico lo más precoz posible de los PE desde el inicio de la escolarización del niño, para lo que es fundamental hacer constar en la historia, la adaptación y el rendimiento en la escuela en cada visita médica. En algunos programas de Salud Pública, se pasa de un examen a los 5-6 años a otro a los 11 años y se pierden muchas oportunidades de prevención. La revisión anual durante toda la época escolar debería ser una reivindicación de la Pediatría para mejorar la atención de nuestros pacientes.
Bibliografía
Los asteriscos reflejan el interés del artículo a juicio del autor.
1.** Sans A, Boix C, Colomé R, López-Sala A, Sanguinetti A. Trastornos del aprendizaje. Pediatr Integral. 2017; XXI(1): 23-31.
2.* Fernández-Jaén A, Martín Fernández-Mayoralas D, Fernández-Perrone AL, Calleja-Pérez B, Albert J, López-Martín S, et al. Disfunción en el trastorno por déficit de atención/hiperactividad: evaluación y respuesta al tratamiento. Rev Neurol. 2016; 62(Supl1): 579-84.
3.** Valdés Rodríguez J, Bolufer Vigrana N. Fracaso escolar en el adolescente. Pediatr Integral. 1997; 2(3): 272-84.
4.* Observatorio Español de la Droga y las Toxicomanías. Informe 2016. Disponible en: http://www.pnsd.msssi.gob.es/profesionales/sistemasInformacion/informesEstadisticas/pdf/2016_INFORME_OEDT.pdf.
5.** Grupo de trabajo de la Guía Clínica de ciberacoso para profesionales de la salud. Guía clínica de ciberacoso para profesionales de la salud. Plan de confianza del ámbito digital del Ministerio de Industria, Energía y Turismo. Hospital Universitario La Paz, Sociedad Española de Medicina del Adolescente, Red.es. Madrid. 2015. Disponible en: https://www.adolescenciasema.org/wp-content/uploads/2015/09/Gu%c3%ada-de-ciberacoso-para-profesionales-de-la-salud-castellano.pdf.
6.* Merino Andreu M, Pin Arboledas G. Trastornos del sueño durante la adolescencia. Adolescere. 2013; I: 29-66.
7.* AAP COUNCIL ON COMMUNICATIONS AND MEDIA. Media and Young Minds. Pediatrics. 2016; 138: e20162591. Disponible en:
http://pediatrics.aappublications.org/content/pediatrics/early/2016/10/19/peds.2016-2591.full.pdf.
8.* Cortejoso D, Arén E, Vázquez M. Decálogo para un Buen uso de las Tecnologías de la Información y la Comunicación. Disponible en: http://www.familiaysalud.es/vivimos-sanos/ocio-y-actividad-fisica/nuevas-tecnologias/decalogo-para-un-buen-uso-de-las.
9.** Ruiz Lázaro PJ. Los problemas escolares en la adolescencia. Pediatr Integral. 2013; XVII(2): 117-27.
10.* L’Ecuyer C. Educar en la realidad. Plataforma Editorial. 2015, ISBN 978-84-16256-56-3.
Bibliografía recomendada
Sobre los transtornos del aprendizaje
– Sans A, Boix C, Colomé R, López-Sala A, Sanguinetti A. Trastornos del aprendizaje. Pediatr Integral. 2017; XXI(1): 23-31.
Revisión actualizada de unos autores que son referencia en éstos temas
– Fernández-Jaén A, Martín Fernández-Mayoralas D, Fernández-Perrone AL, Calleja-Pérez B, Albert J, López-Martín S, et al. Disfunción en el trastorno por déficit de atención/hiperactividad: evaluación y respuesta al tratamiento. Rev Neurol. 2016; 62(Supl1): 579-84.
El TDAH genera abundante y continua bibliografía, porque es un tema en continua revisión en cuanto a su origen, sus formas clínicas y los distintos abordajes de tratamiento.
Sobre los problemas escolares de los adolescentes
– Valdés Rodríguez J, Bolufer Vigrana N. Fracaso escolar en el adolescente. Pediatr Integral. 1997; 2(3): 272-84.
Nos parece interesante comparar ambos trabajos, para resaltar que en el tiempo transcurrido el mayor cambio es la irrupción en el medio escolar de las nuevas tecnologías y el problema del ciberacoso. La bibliografía contiene algunas de las mejores referencias en psicopedagogía de nuestro país (Paulino Castells, MJ Comellas, MJ Mardomingo, Romeu i Bes…) y se puede comprobar que conceptualmente mantienen plena vigencia.
– Ruiz Lázaro PJ. Los problemas escolares en la adolescencia. Pediatr Integral. 2013; XVII(2):117-27.
Buena revisión sobre el tema, especialmente interesante en los aspectos preventivos. El autor demuestra su experiencia en el trabajo con los adolescentes dentro y fuera de las consultas.
Sobre los hábitos de los adolescentes
- Observatorio Español de la Droga y las Toxicomanías Informe 2016.Disponible en:
http://www.pnsd.msssi.gob.es/profesionales/sistemasInformacion/informesEstadisticas/pdf/2016_INFORME_OEDT.pdf
– Grupo de trabajo de la Guía Clínica de ciberacoso para profesionales de la salud. Guía clínica de ciberacoso para profesionales de la salud. Plan de confianza del ámbito digital del Ministerio de Industria, Energía y Turismo. Hospital Universitario La Paz, Sociedad Española de Medicina del Adolescente, Red.es. Madrid. 2015. Disponible en: https://www.adolescenciasema.org/wp-content/uploads/2015/09/Gu%c3%ada-de-ciberacoso-para-profesionales-de-la-salud-castellano.pdf.
La Dra. Mª Angustias Salmerón ha coordinado un documento de lectura imprescindible, sobre uno de los problemas más graves de los adolescentes en la actualidad.
- Merino Andreu M, Pin Arboledas G. Trastornos del sueño durante la adolescencia. Adolescere. 2013; I: 29-66.
A pesar de la abundante evidencia científica sobre los trastornos del sueño y los problemas escolares, esta es otra asignatura pendiente, en la que el pediatra de Atención Primaria debe incidir.
Sobre la importancia de las TIC en la educación
– AAP COUNCIL ON COMMUNICATIONS AND MEDIA. Media and Young Minds. Pediatrics. 2016; 138: e2016259. Disponible en:
http://pediatrics.aappublications.org/content/pediatrics/early/2016/10/19/peds.2016-2591.full.pdf.
Recomendaciones actuales de la Academia Americana de Pediatría.
– Cortejoso D, Arén E, Vazquez M. Decálogo para un Buen uso de las Tecnologías de la Información y la Comunicación. Disponible en: http://www.familiaysalud.es/vivimos-sanos/ocio-y-actividad-fisica/nuevas-tecnologias/decalogo-para-un-buen-uso-de-las.
Enero 2017. Nos parece un recurso sencillo y útil en la consulta del pediatra, para desempeñar la labor preventiva con las familias.
– L’Ecuyer C. Educar en la realidad. Plataforma Editorial. 2015, ISBN 978-84-16256-56-3.
Libro de divulgación, continuación de otro de la misma autora (Educar en el asombro), en los que con abundante bibliografía, se comentan los riesgos de la utilización de las TIC’s desde temprana edad.
| Caso clínico |
|
JJCA, Edad actual 16 años. Historia clínica JJCA, acude a esta consulta a los trece años, es hijo único, sus padres trabajan los dos, tienen una formación media, el padre es técnico de mantenimiento de ascensores y la madre auxiliar de clínica en un centro de paralíticos cerebrales. Fue un hijo deseado. Antecedentes médicos personales Nació a término, por cesárea, el embarazo fue de alto riesgo controlado en hospital. En las primeras revisiones por su pediatra, se aprecia rigidez de los miembros superiores y tendencia al opistótonos, es remitido a fisioterapia infantil y es tratado. De siempre mal comiente, vomitador, se le hace estudio de reflujo, y es negativo. Mal durmiente desde siempre, estudio ORL, y se le aprecia una hipertrofia de adenoides, se piensa en intervención, que al final no se hace, se le recomienda CPAP, pero no la tolera. Se le hace también un estudio alérgico, que resulta negativo. La madre siempre pendiente de su salud. Antecedentes médicos familiares Sin importancia. Antecedentes psiquiátricos personales No se observa patología psiquiátrica grave de base, aportan informes de gabinetes donde han llevado al niño, por bajo rendimiento escolar desde siempre. Sus conclusiones son, desmotivación, falta de rutina y de hábitos de estudio y baja tolerancia a la frustración. Dificultad en habilidades sociales y en hacer amigos. Se le recomienda apoyo escolar para superar dificultades. Hace dos años, es derivado hacia la USMI, por sospecha de TDAH, los resultados e informes que presentan no son concluyentes. Antecedentes psiquiátricos familiares La madre es muy controladora y sufridora. El padre, casi no participa en la dinámica familiar. No patologías relevantes. Psicobiografía Adecuado desarrollo psicofísico, con talla entre P10-P25 acorde con la talla media de los padres y peso actual normal para su talla (IMC: 19,5 kg/m2). Mal comedor y con dificultades en el sueño. Niño enfermizo, pero que nunca presentó una patología grave. La madre siempre estuvo muy pendiente de él, en la alimentación, en los estudios…, le estudia, le hace resúmenes, le repasa los temas. Constantemente llama al centro escolar para interesarse por la marcha de su hijo, los deberes, la agenda. Ejerce un seguimiento hacia las responsabilidades del hijo de forma exhaustiva. El padre, no interviene en nada. Informe escolar Toda la ESO, la ha sacado con dificultades, no presenta los trabajos, no lee los libros que le piden…, pero al final da un empujón y solo ha repetido el curso pasado, 4º de la ESO. Acude a una academia todas las tardes para hacer los deberes y “preguntar dudas”, pero luego no estudia nada en casa. JJ echa la culpa de su fracaso a los demás, y ha empezado a mentir para intentar lidiar con el control de la madre y de los profesores. A pesar de que se le ha explicado a la madre, que su actitud no es la correcta, la dinámica familiar no ha cambiado prácticamente nada. Él se deja caer, la madre lucha como puede y va sacando los cursos, de aquella manera. Este año, está en 1º de BAC y en el instituto ya le han dicho a la madre que no le van a dar tanta información y que lo deje “más suelto”. Exploraciones Su aspecto es adecuado, viene siempre limpio y con un peinado siempre a la moda, su lenguaje es correcto. Echa la culpa de sus problemas a los demás y, aunque está cansado de la vigilancia de la madre, cuando conseguimos que esta se distancie, le dice que “si es que ya no le importa que suspenda” y la madre vuelve a caer en la trampa. Presenta desorganizaciones a la hora de la alimentación, es muy selectivo, no toma fruta a no ser que se la pelen, no verduras, no es capaz de hacerse el bocadillo del almuerzo, rechaza probar alimentos nuevos. Se siguen apreciando en él, síntomas de falta de motivación, desapetencia por los estudios, no adquisición de hábitos de estudio. Está acudiendo a jugar al fútbol dos días por semana, tiene algunos amigos, no sale mucho con ellos. Está empezando a salir con chicas, no mantiene durante mucho tiempo la relación y va cambiando de una a otra. Desde hace un año, tiene móvil y acceso a Internet. A través de este y de las redes sociales es como se relaciona con sus amigos/as. Pruebas complementarias Hemograma, vitamina B12, ácido Fólico y TSH normales. No tóxicos en orina. WISC-lV: CI total de 120. CEDI y STAIC: dentro de la normalidad. Test de CONNERS: sin hallazgos significativos. Test SQD: normal. Diagnóstico Problema relacionado con el estilo de vida y educativo. No toma sus responsabilidades frente a la vida y los requerimientos de esta. La madre para evitar que fracase y con el excesivo proteccionismo está propiciando la falta de madurez del chico, que concibe la vida como algo que le cuesta enfrentar y prefiere que los demás lo hagan por él. Tratamiento • Psicoeducación al paciente y a la familia. • Trabajar la patológica relación madre-hijo. • Terapia cognitivo conductual, es la adecuada para el trabajo con él. • Habilidades sociales, ya que es una persona vulnerable, que prefiere el cierto anonimato de las redes sociales para relacionarse. • El trabajo con la familia debe consistir en dejarle crecer y caer, con una caída controlada y con la atenta mirada de sus terapeutas, sin ser demasiado intervencionistas, enfocar el tratamiento en ser él mismo, que él busque su camino. Debe aprender a tolerar la frustración para aprender a enfrentarla. • Reeducación alimentaria, probar alimentos nuevos, involucrarse en la cocina. • Ir aumentando sus responsabilidades en las tareas caseras.
|