 |
| Temas de FC |
M. Ridao Redondo
Pediatra de Atención Primaria. EAP Sant Vicenç dels Horts-Torrellas de Llobregat. Barcelona
| Resumen
La alergia alimentaria (AA) es un problema de salud pública importante y en evolución. En población pediátrica española, la prevalencia se sitúa entre un 6 % y un 8 % de los lactantes al año de vida y se estabiliza en torno al 4 % a los 4 años. Puede producir síntomas localizados leves o sistémicos como anafilaxia, que puede ser de riesgo vital. La AA es la causa del 50 % de las anafilaxia de la edad pediátrica. Cualquier alimento es potencialmente sensibilizante, los alimentos implicados varían geográficamente en función de la frecuencia de consumo en cada país. Las sensibilizaciones suelen aparecer en relación con la introducción de alimentos en la dieta del niño. En nuestro medio y durante la edad pediátrica, los implicados con mayor frecuencia en la AA IgE mediada son las proteínas de: huevo, leche, pescado, frutos secos y frutas. Se define como alergia a alimentos la reacción de hipersensibilidad mediada inmunológicamente y se clasifica en mediada por IgE o no mediada (mecanismo celular), en función del mecanismo que la produce. El pediatra de Atención Primaria debe estar familiarizado con su diagnóstico preciso y tratamiento dietético adecuado, evitando dietas de eliminación injustificadas que pueden suponer un riesgo nutricional y garantizar que los niños alcancen un normal crecimiento y desarrollo. |
| Abstract
Food allergy (FA) is an important and evolving public health problem. In the Spanish pediatric population, the prevalence ranges between 6 and 8 % of infants aged one year of life, and stabilizes at around 4 % by 4 years of life. It can produce mild localized or systemic symptoms such as anaphylaxis, which can be life-threatening. FA is the cause of 50 % of anaphylaxis in children. Any food is potentially sensitizing, the foods involved vary geographically depending on the frequency of consumption in each country. Sensitizations usually appear in relation to the introduction of food in the child’s diet. In our environment, and during the pediatric age, those most frequently involved in IgE-mediated FA are proteins contained in: egg, milk, fish, nuts and fruit. Food allergy is defined as an immunologically mediated hypersensitivity reaction and is classified as IgE-mediated or non-mediated (cellular mechanism), depending on the mechanism that produces it. The primary care pediatrician must be familiar with its precise diagnosis and adequate dietary treatment, avoiding unjustified elimination diets that can pose a nutritional risk, so as to ensure that children achieve normal growth and development. |
Palabras clave: Alergia alimentaria, Alergia IgE mediada proctocolitis alérgica; Enterocolitis inducida por proteínas.
Key words: Food allergy; Food protein-induced allergic proctocolitis (FPIAP); Food–protein induced enterocolitis syndrome (FPIES).
Pediatr Integral 2023; XXVII (2): 91 – 100
OBJETIVOS
• Conocer la clínica, diagnóstico y pronóstico de la hipersensibilidad mediada por IgE y de la hipersensibilidad no medida por IgE.
• Diferenciar entre sensibilización y alergia.
• Aprender los múltiples factores sobre el aumento de la prevalencia de la alergia alimentaria.
• Conocer el manejo y derivación desde la Atención Primaria, siguiendo el Consenso Pediátrico Español.
Alergias alimentarias mediadas y no mediadas por IgE
Introducción
La alergia alimentaria (AA) es un problema de salud pública importante y en evolución. Durante los últimos quince años, se ha incrementado como una “segunda ola” de la epidemia de alergia que comenzamos a ver en las consultas en las últimas décadas del siglo XX. No está claro por qué este nuevo fenómeno se ha retrasado con respecto a la “primera ola” de asma, rinitis alérgica y sensibilización a inhalantes.
En países como Australia, que lideran la epidemia respiratoria, la alergia alimentaria mediada por IgE afecta hasta el 10 % de los bebés. Sus padres se encontraban entre la primera generación en experimentar el aumento a gran escala de las enfermedades alérgicas, aunque en ese momento, los trastornos de tolerancia oral eran poco comunes. Otro motivo de preocupación es que esta nueva generación parece tener menos probabilidades de superar la alergia alimentaria que sus predecesores, lo que tiene implicaciones a largo plazo para la carga de la enfermedad. La enfermedad alérgica se ha relacionado con el estilo de vida moderna, incluido el cambio de los patrones dietéticos, el cambio de las bacterias comensales intestinales y la contaminación ambiental. Todavía no se sabe si el aumento de la alergia alimentaria es un presagio de efectos más tempranos y más graves de estos cambios ambientales progresivos o si están implicados factores de estilo de vida adicionales(1).
Actualmente, en la población pediátrica española, la prevalencia se sitúa entre un 6 % y un 8 % de los lactantes al año de vida y se estabiliza en torno al 4 % a los 4 años(2).
La confirmación del diagnóstico puede ser problemática, puesto que un tercio de los niños presentan reacciones adversas con más de un alimento. Puede producir síntomas localizados leves o sistémicos como anafilaxia, que puede ser de riesgo vital. La AA es la causa del 50 % de las anafilaxia de la edad pediátrica(3).
El pediatra de Atención Primaria debe estar familiarizado con su diagnóstico preciso y tratamiento dietético adecuado, evitando dietas de eliminación injustificadas, que pueden suponer un riesgo nutricional, y garantizar que los niños alcancen un normal crecimiento y desarrollo.
Cualquier alimento es potencialmente sensibilizante, los alimentos implicados varían geográficamente en función de la frecuencia de consumo en cada país. Las sensibilizaciones suelen aparecer en relación con la introducción de alimentos en la dieta del niño. En nuestro medio y durante la edad pediátrica, los implicados con mayor frecuencia en la AA IgE mediada son las proteínas de: huevo (39,1 %), leche (32,3 %), pescado (11,3 %), frutos secos (18,8 %) y frutas (12,4 %). Los patrones alimentarios justifican un mayor número de alergia a cacahuete en EE.UU. y en el Reino Unido, al sésamo en Israel o al trigo sarraceno en Japón o Corea. La aerobiología también puede condicionar las alergias alimentarias observadas en una determinada zona geográfica, por la aparición de síndromes de reacción cruzada; por ejemplo: los escolares y adolescentes alérgicos al polen de abedul, gramíneas o artemisia, presentan con frecuencia alergia a alimentos vegetales, asociada generalmente a frutas frescas y frutos secos(4,5).
Los pacientes con síntomas graves o complejos de AA necesitan derivación a un pediatra alergólogo. Una consulta de alergia es obligatoria para aquellos pacientes que presentan anafilaxia, dado que a menudo no se reconoce lo suficiente, lo que lleva a una prescripción inadecuada de adrenalina y/o capacitación insuficiente del paciente sobre cuándo y cómo usarla. Los esfuerzos educativos pueden reducir esta brecha en el conocimiento y mejorar la seguridad de los pacientes.
Además de eso, el diagnóstico adecuado y la evaluación del pronóstico de resolución de la alergia son componentes clave para el manejo de la AA. Cuando no se prevé una resolución espontánea, la inmunoterapia específica con alérgenos aparece como el único tratamiento prometedor.
La vigilancia constante y el miedo a las reacciones graves o anafilácticas pueden aumentar la ansiedad en los pacientes con AA y provocar una tendencia a restringir demasiado su dieta. Esto puede dar lugar a hábitos alimentarios deficientes o erráticos y al deterioro del estado nutricional, pero también a la reducción de su vida social y a un aumento de la angustia psicológica de los pacientes y, a menudo, de sus cuidadores. Los nutricionistas y los psicólogos pediátricos pueden ser de gran ayuda en pacientes complejos.
Definición
Las definiciones de reacción adversa a alimentos, intolerancia alimentaria y reacciones alérgicas a alimentos, se prestan a confusión y se utilizan de forma incorrecta en diversos ámbitos. Por ello, la Academia Europea de Alergología e Inmunología Clínica (EAACI) y la Organización Mundial de Alergia (WAO) llegaron a un consenso sobre las mismas. Cualquier reacción adversa a alimentos no tóxica (p. ej., una intoxicación con setas, sería una reacción tóxica), se denomina hipersensibilidad a alimentos. Se define como alergia a alimentos: la reacción de hipersensibilidad mediada inmunológicamente y se clasifica en mediada por IgE o no mediada (mecanismo celular), en función del mecanismo que la produce(6).
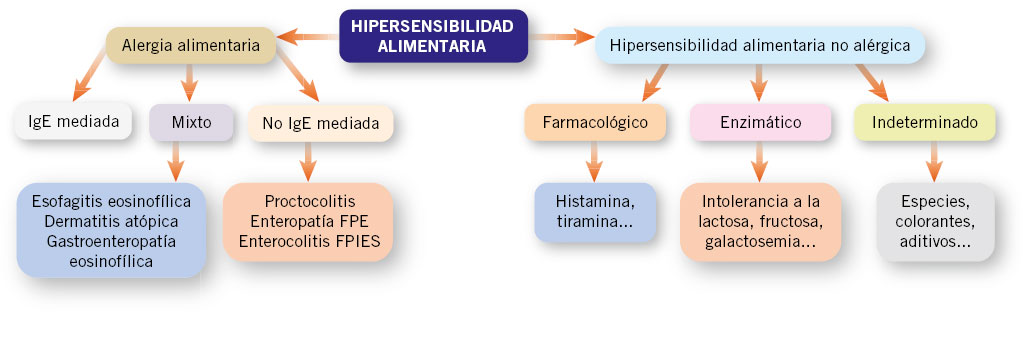
En este documento de posición, la EAACI define como “hipersensibilidad no alérgica a alimentos” al resto de reacciones adversas, referidas previamente como “intolerancias a alimentos”. Se distinguen tres tipos: enzimáticas, por ejemplo las producidas por déficit de lactasa, que se presentan con diarrea o flatulencia con la ingesta de leche; de tipo farmacológico, como las cefaleas producidas en algunas personas por alimentos ricos en tiramina (quesos muy curados); y en tercer lugar reacciones irritativas o indeterminadas, como por ejemplo al comer alimentos muy especiados (Fig. 1).
Figura 1. Clasificación de las reacciones adversas a alimentos (RAA) de la Academia Europea de Alergología e Inmunología Clínica (EAACI). Tomada de: clasificación de las RAA de la Comisión de Nomenclatura de la EAACI refrendada por la Organización Mundial de la Alergia (WAO). FPE: Enteropatía por proteínas. FPIES: Enterocolitis inducida por proteínas.
En la alergia a alimentos, hay que tener en cuenta que algunos pacientes precisan de la existencia de cofactores para que suceda la reacción alérgica. Es preciso que el individuo alérgico a un determinado alimento lo ingiera junto con la presencia de un cofactor para presentar clínica. Estos cofactores pueden ser: ejercicio físico, fiebre, infecciones víricas, estrés o la ingesta de antiinflamatorios o alcohol.
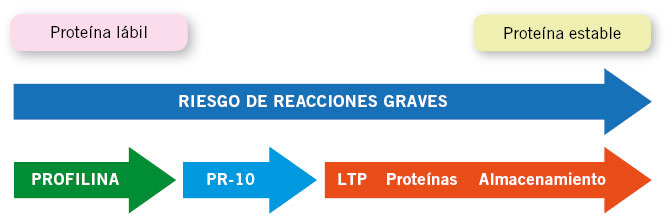
Los alimentos contienen múltiples proteínas y cada una de ellas puede actuar como alérgeno. Algunas proteínas son específicas de ese alimento y otras son compartidas por otros alimentos de la misma especie o incluso de familias muy alejadas. En cada alimento pueden identificarse alérgenos mayores y otros menores. Un alérgeno mayor es aquel con más del 50 % de frecuencia de reconocimiento por anticuerpos IgE, entre los pacientes positivos a la fuente alergénica de la cual proviene. Se conocen cerca de 400 alérgenos alimentarios, pertenecientes a 70 familias de proteínas, aunque la mayoría de los alérgenos están englobados en solo 10 familias. Algunas de estas proteínas se denominan panalérgenos, ya que son moléculas ubicuas en la naturaleza con una función esencial y cuya estructura se ha mantenido, compartiendo una elevada homología entre diferentes especies. Esto es lo que justifica la reactividad cruzada. Las distintas proteínas se agrupan en familias según su estructura y características fisicoquímicas lo que, a su vez, va a condicionar un diferente riesgo para originar reacciones más o menos graves. Aquellas familias que tienen alta labilidad frente al calor o la digestión, como son las profilinas, producirán habitualmente cuadros más leves, sobre todo locales, como el síndrome de alergia oral. Las proteínas resistentes al calor o a la degradación enzimática, como son las proteínas de almacenamiento de los frutos secos y las proteínas transportadoras de lípidos (LTP), llegarán intactas al torrente circulatorio y por ello ocasionarán potencialmente clínica más grave (Fig. 2).
Figura 2. Gravedad de las reacciones en función de la proteína implicada. LTP: proteínas transportadoras de lípidos.
Es muy importante diferenciar entre sensibilización y alergia. La sensibilización es una respuesta inmunitaria que sigue al contacto con un alérgeno y que se traduce por la presencia de IgE tisular, que nos positivizará las pruebas cutáneas (prick-test) y la IgE plasmática específica para ese alimento (CAP/RAST). Tras un nuevo contacto con el alérgeno, el niño puede no presentar síntomas clínicos, reflejando una sensibilización al alimento. En cambio, si presenta clínica, nos encontraremos ante una verdadera alergia alimentaria. La sensibilización a alimentos es más frecuente que la alergia. De hecho, hasta un 50-70 % de los pacientes que presentan sensibilización a un alimento toleran su ingestión(7).
Hipersensibilidad a alimentos mediada por IgE
Manifestaciones clínicas
Las reacciones alérgicas aparecen en las dos horas siguientes a la ingestión del alimento, normalmente en los primeros 30-60 minutos. Pueden afectar a uno o varios órganos que incluyen: la piel, el tracto digestivo, el respiratorio y el sistema cardiovascular(7).
La clínica más frecuente en la edad pediátrica es la afectación cutánea, con urticaria-angioedema, seguida de las reacciones localizadas en la mucosa oral y faríngea, que se manifiestan con prurito local (síndrome de alergia oral), especialmente frecuentes en adolescentes con alergia a alimentos vegetales asociada o no a alergia al polen. En tercer lugar en frecuencia, aparece la clínica digestiva con: vómitos, dolor abdominal y diarrea. La afectación respiratoria es en forma de rinitis y broncoespasmo. El broncoespasmo aislado es poco frecuente. Su presencia debe alertarnos de que estamos ante un cuadro de anafilaxia.
La anafilaxia se define como la afectación de dos o más órganos simultáneamente. Es una reacción de hipersensibilidad grave que pone en riesgo la vida. Los síntomas respiratorios graves aislados (afonía, tos repetitiva, dificultad para hablar, sibilantes) en relación a la ingesta de un alimento sospechoso, deben tratarse también como una anafilaxia. Esta suele ser la causa de la muerte en reacciones por alimentos de desenlace fatal. Los factores de riesgo para una anafilaxia de riesgo vital son: la presencia previa de asma, la ingestión inadvertida (alérgenos ocultos), la incapacidad para reconocer los síntomas y, sobre todo, el retraso en la administración de adrenalina. También puede aparecer anafilaxia por alimentos que no son ingeridos, solo por exposición por vía cutánea (un beso de alguien que ha comido huevo a un niño alérgico) o inhalatoria (vapores de cocción de pescado).
Diagnóstico
El diagnóstico de precisión en alergia alimentaria es importante, no solo para prevenir reacciones adversas, sino también para evitar dietas innecesarias que puedan alterar el desarrollo nutricional y el crecimiento del niño. Nunca podemos hablar de alergia alimentaria por tener un prick o una IgE específica positiva, pues la ingestión del alimento puede no tener ninguna repercusión clínica y esa sensibilización reflejar únicamente la predisposición a la atopia(8).
En primer lugar, mediante la anamnesis se debe conocer: qué alimentos están implicados, el tiempo de latencia entre la ingesta y el inicio de los síntomas, la cantidad de alimento ingerido, en qué forma estaba cocinado o si era crudo y si se ha tomado en ocasiones posteriores. Hay que investigar la presencia de cofactores, como la toma de fármacos o un proceso infeccioso intercurrente. Pueden ser útiles los diarios dietéticos. En la exploración física se buscarán marcadores de atopia, como presencia de rinoconjuntivitis, asma o dermatitis atópica. Se deben recoger informes de urgencias para valorar las reacciones acaecidas y tratamientos que el niño ha precisado. En muchos niños encontraremos antecedentes familiares de enfermedad atópica.
Estudio alergológico in vivo
Pruebas cutáneas (prick-test) con extractos estandarizados de la proteína y sus fracciones proteicas, con el alimento en fresco o cocinado (prick by prick). Actualmente, también pueden testarse componentes proteicos como LTP o profilinas.
Estudio alergológico in vitro
En el laboratorio se puede determinar IgE total e IgE específica al alimento y sus fracciones proteicas. El desarrollo de la biología molecular ha permitido la detección simultánea de IgE dirigidas a los diferentes componentes de más de 100 alérgenos procedentes de unas 50 fuentes alergénicas; por ejemplo, las proteínas del huevo son la suma de ovoalbúmina, ovomucoide, lisozima, etc. Algunos pacientes son alérgicos a unas proteínas y otros alérgicos a otras, pero en todos vamos a obtener el mismo resultado si se busca solo IgE a clara. Estos resultados tienen trascendencia en cuanto al pronóstico, la predicción de la gravedad de las reacciones en caso de una transgresión dietética y también nos explican los fenómenos de reactividad cruzada. El uso del diagnóstico por componentes está especialmente indicado en aquellos pacientes cuyo diagnóstico sea complejo, ya sea por la gravedad de las reacciones, la dificultad para identificar el alérgeno implicado o la presencia de múltiples alimentos sospechosos (Fig. 3).
Figura 3. Diagnóstico por componentes.
Prueba de provocación oral o de exposición controlada
Es el patrón oro para confirmar o descartar el diagnóstico de alergia a un alimento. Debe realizarse siempre en un centro hospitalario que disponga del personal entrenado y los recursos adecuados para poder realizar una reanimación cardiovascular. La provocación oral se puede realizar de forma abierta administrando el alimento, a ciego simple o a doble ciego controlado con placebo. La única contraindicación de la prueba de provocación oral es que la reacción con el alimento fuera de riesgo vital y todas las pruebas in vivo e in vitro aclaren la etiología de la reacción.
La provocación oral también se utiliza para valorar el riesgo de otros alimentos que puedan tener reactividad cruzada con el alimento identificado como responsable; por ejemplo, en el alérgico a las lentejas que presente IgE específicas a otras legumbres, se debe comprobar la tolerancia a garbanzo, soja, cacahuete, alubias o guisantes.
Pronóstico
Las alergias a la leche, el huevo, la soja y los cereales, que aparecen en los lactantes, suelen resolverse espontáneamente. A los 5 años de edad, cerca del 80 % de los niños alérgicos a la leche y más del 50 % de los alérgicos al huevo han superado su alergia. Las alergias a frutos secos, cacahuete, pescados y mariscos se consideran persistentes en la mayor parte de los pacientes.
Tratamiento
El tratamiento de la alergia a alimentos se ha basado hasta hace unos años en dos pilares: la dieta de evitación del alimento identificado y el tratamiento de las reacciones alérgicas en caso de ingesta accidental.
La dieta de evitación debe incluir la valoración, si es necesario por test de provocación de los alimentos del grupo alimentario implicado y conocer, en función de las proteínas implicadas, si el paciente es tolerante al alimento cocinado y horneado (Fig. 4).
Figura 4. Manejo de la alergia al huevo utilizando el diagnóstico por componentes. TPO: test de provocación oral. ITO: inmunoterapia oral con huevo.
La dieta de evitación es un reto para los alérgicos y sus familias, ya que supone la vigilancia continua, la revisión del etiquetado de cualquier alimento procesado y verificar la composición de las comidas que se realizan fuera de casa. La información sobre alérgenos presentes en los alimentos está regulada por la Unión Europea. Se exige, de forma obligatoria, que se identifiquen tanto en la industria como en la restauración 14 alérgenos que cubren una buena parte de los alérgenos alimentarios: cacahuete, moluscos, lácteos, mostaza, sésamo, altramuces, huevo, gluten, pescado, crustáceos, frutos de cascara, apio, dióxido de azufre, sulfitos y soja. Además, la industria utiliza el etiquetado precautorio de alimentos (EPA) para comunicar la posible presencia involuntaria de un alérgeno: “puede contener” “fabricado en una planta en la que”. El EPA reduce las posibilidades de compra de muchos pacientes alérgicos y se ha generalizado como un etiquetado defensivo. A pesar de toda esta regulación, entre el 30 % y el 50 % de los alérgicos a alimentos presentan reacciones accidentales(9,10).
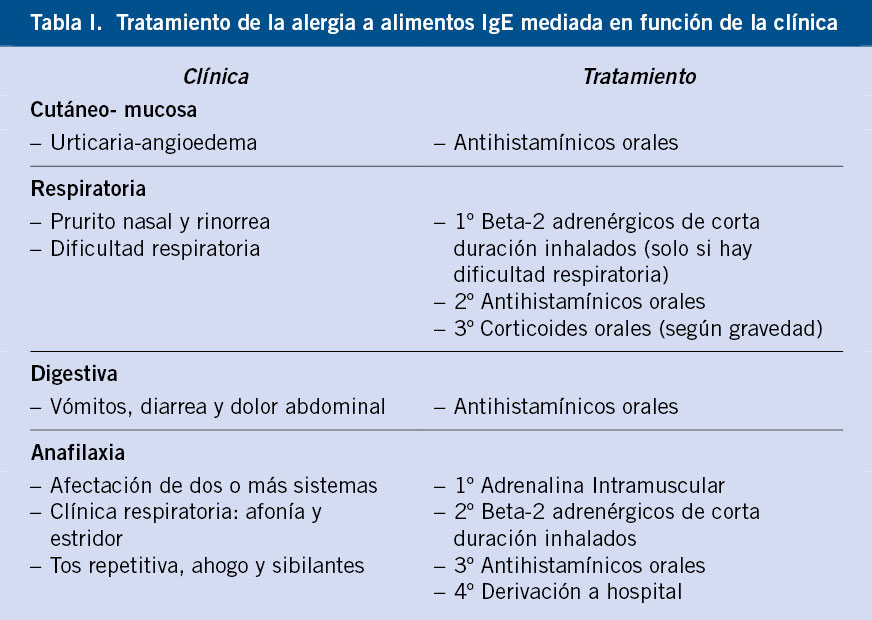
El tratamiento de las reacciones alérgicas es farmacológico. Las manifestaciones de urticaria-angioedema, digestivas o de rinoconjuntivitis se tratan con antihistamínicos orales. Si aparece broncoespasmo o están implicados dos o más órganos simultáneamente, hemos de pensar en una anafilaxia y la administración de adrenalina intramuscular es prioritaria, independientemente de que haya o no hipotensión arterial(11) (Tabla I).
Todo el personal sanitario debe estar entrenado en el reconocimiento de una reacción anafiláctica y en la administración de adrenalina. Todos los niños y sus cuidadores, incluidos maestros y monitores de comedor, deben recibir educación sanitaria y tener un plan de acción por escrito para saber cómo actuar (Fig. 5).
Figura 5. Plan de Acción para la escuela. Accesible e imprimible desde: https://www.fliedner.es/media/modules/news/121/protocolo-anafilaxia-15-16.pdf.
Se pueden consultar en la web de la Sociedad Española de Inmunología Clínica, Alergia y Asma Pediátrica (www.seicap.es), tanto el Manual de Anafilaxia Pediátrica como el Protocolo de acción para la escuela(12).
En caso de anafilaxia dependiente de los alimentos inducida por el ejercicio, se debe brindar asesoramiento dietético individualizado para evitar alérgenos alimentarios específicos 4 a 6 horas antes del ejercicio y 1 hora después.
En los últimos años, la inmunoterapia oral a alimentos (ITO) ha demostrado gran eficacia. Es potencialmente un tratamiento curativo que puede incrementar la cantidad de alimento tolerado por el paciente, previniendo los síntomas alérgicos y reduciendo el riesgo de una reacción anafiláctica potencialmente grave con riesgo vital. La ITO es un tratamiento activo que consiste en la administración de dosis progresivamente crecientes del alimento que produce la reacción alérgica, para reducir los síntomas frente a su exposición natural, es decir, conseguir la desensibilización y, si es posible, la tolerancia permanente del alimento. Actualmente, se realiza ITO a huevo y leche en la práctica habitual, y se está en fases menos avanzadas para avellana, cacahuete y melocotón. En los estudios controlados analizados en los metaanálisis, se observa que se puede alcanzar la desensibilización en el 87 % de los pacientes tratados con ITO con leche de vaca (62 % desensibilización completa y 25 % desensibilización parcial) y en el 79 % de los pacientes con ITO con huevo (39 % desensibilización completa y 40 % desensibilización parcial). La desensibilización puede ser más eficaz en niños pequeños, lo que sugiere que la inmunomodulación se podría conseguir más fácilmente cuando se inicia en edades más tempranas, como se especula con la inmunoterapia subcutánea con neumoalérgenos. En pacientes altamente sensibilizados se puede asociar omalizumab al tratamiento como adyuvante. El omalizumab es un anticuerpo monoclonal humanizado que se une a la IgE disminuyendo el riego de reacciones alérgicas durante la ITO, sin reducir la capacidad antigénica(13).
Actualmente, se están ensayando tratamientos con inmunoterapia a alimentos por vía subcutánea, sublingual y epicutánea.
Prevención
El aumento de la prevalencia de la AA se ha relacionado con múltiples factores como: el estilo de vida, el consumo de tabaco, los hábitos alimentarios actuales, la contaminación ambiental, el tipo de parto, el papel de la microbiota, etc. Estos factores, por mecanismos epigenéticos, pueden producir cambios en la expresión de determinados genes que pueden ser heredados y perpetuados en las siguientes generaciones. Además de un aumento en la incidencia, los estudios muestran más pacientes con multi-alergias y con menores probabilidades de conseguir la tolerancia al alimento al que son alérgicos.
Se estima que sin tener antecedentes de enfermedad alérgica, el riesgo de padecerla es del 5-15 %. Si un hermano es alérgico, el riesgo es de un 25-35 %, si el padre o la madre son alérgicos, el riesgo es de entre 20-40 %, siendo del 40-60 % si ambos padres son alérgicos y del 50-80 % si el padre o la madre tienen la misma enfermedad alérgica. De momento, estos factores genéticos no son modificables, aunque son los únicos para identificar a un niño de riesgo.
En los últimos años, múltiples trabajos y guías han intentado poner luz en las estrategias preventivas, tanto de cara a la madre embarazada y al lactante como en lo referente al niño. La Guía de la EAACI: Prevención del desarrollo de alergia alimentaria en lactantes y niños pequeños publicada en 2021, desaconseja las recomendaciones clásicas sobre restricciones dietéticas, evitando alérgenos alimentarios en la madre tanto embarazada como que amamanta o el uso de leches hidrolizadas en los lactantes o leches de soja en los primeros seis meses de vida. No hay recomendaciones, puesto que no hay evidencia sobre el uso de suplementos vitamínicos, aceites de pescado, prebióticos o probióticos durante el embarazo, la lactancia o la infancia. Los cambios clave se centran en las evidencias de que la introducción entre los 4-6 meses de huevo bien cocido como parte de la alimentación complementaria o cacahuete (según el consumo y, por tanto, la frecuencia de alergia alimentaria por zonas geográficas), aprovecharía una ventana de tolerancia y, por lo tanto, una oportunidad para intentar prevenir la alergia alimentaria. No se recomienda retrasar la introducción de alimentos clásicamente etiquetados de muy alergénicos. Por otro lado, se recomienda evitar la suplementación con fórmula de leche de vaca en la primera semana de vida (evidencia baja)(14).
Hipersensibilidad a alimentos no IgE mediada
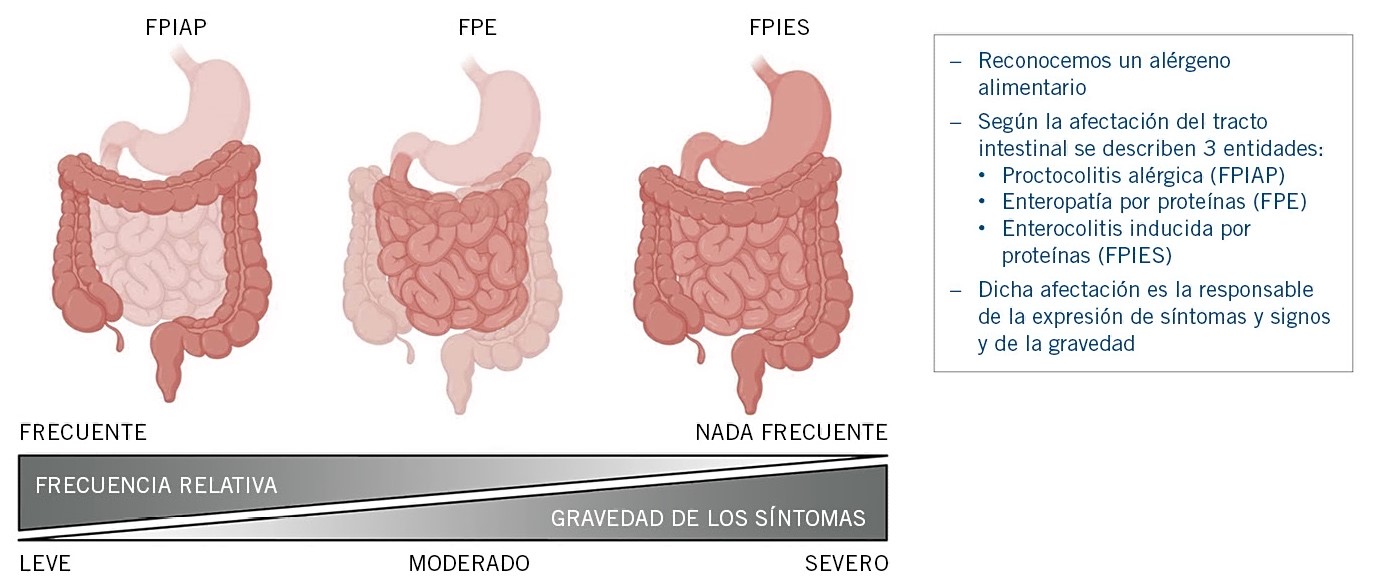
Se presentan de una forma más subaguda y/o con síntomas crónicos prácticamente siempre localizados en el tracto gastrointestinal. Estos procesos incluyen: síndrome de enterocolitis inducido por proteínas alimentarias (conocido por sus siglas en inglés FPIES), enteropatía inducida por proteínas y proctocolitis alérgica(15,16).
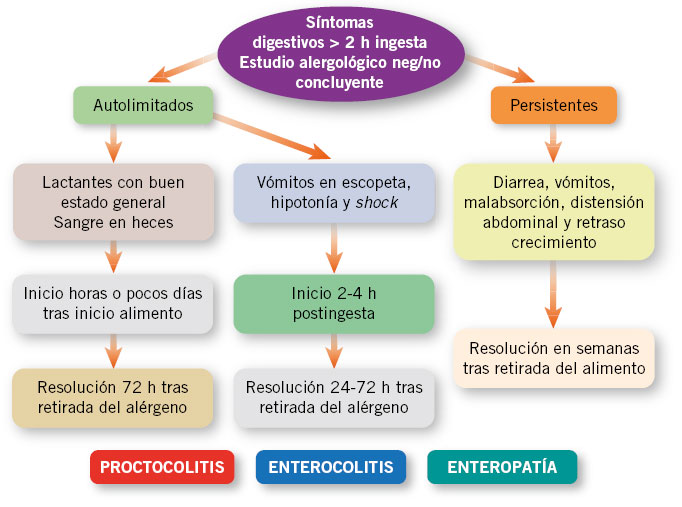
El periodo de latencia entre la ingestión del alimento y la aparición de síntomas es superior a las reacciones mediadas por IgE, estos trastornos aparecen en los primeros meses de vida, son de inicio insidioso, progresivo y tienden a desaparecer después de un periodo que varía entre uno y varios años (Figs. 6 y 7).
Figura 6. Clínica de la hipersensibilidad a alimentos no mediada por IgE.
Figura 7. Hipersensibilidad a alimentos no IgE mediada.Tomado de: Labrosse R, et al. Non-IgE-Mediated Gastrointestinal Food Allergies in Children: An Update. Nutrients. 2020; 12: 2086.
Manifestaciones clínicas
Proctocolitis alérgica
También recibe el nombre de colitis inducida por alimentos o colitis alérgica, se presenta antes de los seis meses de edad. Los síntomas clínicos son sangre roja en las heces en un lactante, con buen estado general y sin repercusión en su desarrollo pondoestatural.
La zona afectada del intestino se localiza en el colon y el recto. En caso de que se produzca una mayor afectación en el colón, podemos encontrar diarrea con moco. Está producida por proteínas de leche o por proteínas de soja. El 60 % de los casos se presentan en niños alimentados exclusivamente con lactancia materna.
Las mediciones de IgE específica son negativas, así como las pruebas cutáneas. Habitualmente, la exploración y la analítica son normales, aunque podemos encontrar anemia, hipoalbuminemia y eosinofilia periférica en algunos lactantes. Debe realizarse diagnóstico diferencial con: grietas anales, infecciones gastrointestinales, enterocolitis necrotizante o invaginación intestinal. El tratamiento consiste en eliminar la proteína responsable. La mejoría debe esperarse entre la primera y la segunda semana de la dieta de exclusión. En caso de que el lactante reciba alimentación materna, la madre deberá realizar una dieta exenta de proteínas (habitualmente, proteínas de leche de vaca). En el lactante alimentado con fórmula de leche entera, utilizaremos fórmulas extensamente hidrolizadas. No se debe utilizar leche de soja, ya que un 30 % de estos niños presentarán síntomas también con la soja.
Los síntomas clínicos son benignos y transitorios. Remiten mayoritariamente alrededor del año de vida. En caso de persistencia, se prolonga la dieta, realizando nuevos intentos de reintroducción cada 3-6 meses en el domicilio.
Enteropatía inducida por proteínas
La enteropatía asociada a proteínas de la dieta puede presentarse en los dos primeros años de vida, pero la mayoría de los niños la desarrollan antes de los doce meses. Normalmente, son niños más mayores que los que presentan enterocolitis y presentan una clínica más larvada.
Los alimentos implicados son la leche de vaca, que es la causa más frecuente, pero también se ha demostrado clínica con la participación de alimentos como: la soja, el gluten, el huevo, el pollo, el arroz y el pescado.
La clínica predominante es la diarrea crónica, distensión abdominal y estancamiento ponderal, pudiendo evolucionar a un síndrome de malabsorción.
Las pruebas cutáneas y las determinaciones séricas de IgE específicas frente a alimentos son negativas. No se detectan anticuerpos antigliadina, antiendomisio y antitransglutaminasa, y la retirada del gluten no produce una mejoría de los síntomas.
El diagnóstico se basa en la historia clínica detallada y la respuesta a la prueba de exclusión-provocación de las proteínas sospechosas. Puede tardar varias semanas en apreciar mejoría. En la biopsia se observan: grados variables de atrofia de vellosidades intestinales, hiperplasia de criptas, aumento de linfocitos interepiteliales y ligera infiltración eosinofílica. La biopsia no es imprescindible para el diagnóstico.
Se resuelve normalmente entre los doce y veinticuatro meses de vida y, raramente, persiste en edades superiores.
La retirada indiscriminada de alimentos no es correcta. El tratamiento consiste en identificar el antígeno y retirarlo de la dieta. La resolución de la enteropatía vendrá determinada por la realización de una prueba de provocación oral. Si el alimento implicado son las proteínas de la leche de vaca, se deben utilizar fórmulas de hidrolizados extensos de proteínas, la soja no es adecuada como sustitutivo, ya que puede estar implicada como desencadenante (Tabla II).
Síndrome de enterocolitis inducido por proteínas alimentarias (Food Protein-Induced Enterocolitis Syndrom [FPIES])
Conocido por sus siglas en inglés, en 2017 se publicó la primera guía de consenso para su diagnóstico y tratamiento. Representa la patología gastrointestinal alérgica más grave en el lactante. Se desencadena por la ingesta de leche de vaca, leche de soja, pescado, cereales (arroz y avena) o huevo. Existe un patrón geográfico, probablemente relacionado con los hábitos dietéticos. Así, en España, el pescado es el alimento sólido más frecuentemente implicado. La edad de inicio depende de la edad de introducción del alimento implicado. En adultos se ha descrito la ingesta de crustáceos como alimento desencadenante.
La sintomatología dependerá del tramo de intestino afectado. Si la afectación es de intestino delgado se presentará con la forma aguda, con vómitos intensos que se producen a las dos a cuatro horas de la ingesta de la proteína causante de la reacción. Puede producir deshidratación, o incluso shock hipovolémico, que ocasiona diagnósticos diferenciales no siempre fáciles de resolver. Si la afectación es en la parte distal del intestino delgado o en el colon, observaremos diarrea acuosa, ocasionalmente con moco y sangre macroscópica, de inicio en las 5-10 horas siguientes a la ingesta.
La forma crónica de FPIES no está tan bien definida. Se presenta en lactantes menores de cuatro meses, alimentados con fórmula de inicio, pero puede ser más tardía si el alimento implicado es arroz, huevo o pescado. Pueden presentar vómitos intermitentes, diarrea acuosa, irritabilidad y abdominalgias, que van aumentando en frecuencia con afectación del desarrollo pondoestatural. En el ámbito del laboratorio podemos encontrar hipoalbuminemia, anemia y leucocitosis con neutrofilia y trombocitosis. Es habitual la demora en el diagnóstico y hasta un 75 % de los niños presentan al diagnóstico una importante afectación del estado general.
FPIES es poco común en los bebés alimentados con leche materna exclusivamente, parece tener un papel protector. En caso de presentarse en niños alimentados con lactancia materna, debemos suprimir las proteínas de leche de vaca y soja de la dieta materna. En niños mayores y adultos es poco frecuente y, por lo general, presenta un síndrome leve de náuseas, vómitos prolongados y abdominalgias, varias horas después de la ingestión. Aproximadamente un 25 % de niños con FPIES desarrollarán anticuerpos específicos frente a alimentos (Tabla III).
La resolución de la reactividad clínica ocurre con la edad, típicamente antes de los tres años de edad para la leche, el huevo y el arroz, y suele prolongarse hasta los cinco años para el pescado.
La reintroducción del alimento debe realizarse siempre en medio hospitalario.
Función del Pediatra de Atención Primaria: criterios de derivación a Atención Especializada de Alergia Pediátrica (Algoritmo)
Es necesaria la derivación de todo niño con sospecha de alergia alimentaria para tener un diagnóstico adecuado, que evite tanto el infradiagnóstico como el sobrediagnóstico y, por tanto, que las medidas de evitación sean las adecuadas para afectar lo menos posible la calidad de vida del niño y su familia.
La derivación de la anafilaxia debe ser preferente. Los niños, su familia, su entorno escolar y lúdico/deportivo, deberán recibir toda la educación sanitaria que precisen para identificar los alérgenos responsables de su alergia, conocer la lectura de etiquetas, cómo gestionar el comedor escolar y los eventos extraescolares (fiestas de cumpleaños, celebraciones tradicionales con dulces típicos), donde aumenta la posibilidad de alérgenos ocultos y cómo tratar las posibles reacciones alérgicas. El pediatra de Atención Primaria debe implicarse en esta educación sanitaria y repasar con el paciente los tratamientos y, sobre todo, la autoadministración de adrenalina.
En caso de anafilaxia inducida por el ejercicio dependiente de los alimentos, se debe brindar asesoramiento dietético individualizado para evitar alérgenos alimentarios específicos 4 a 6 horas antes del ejercicio y 1 hora después.
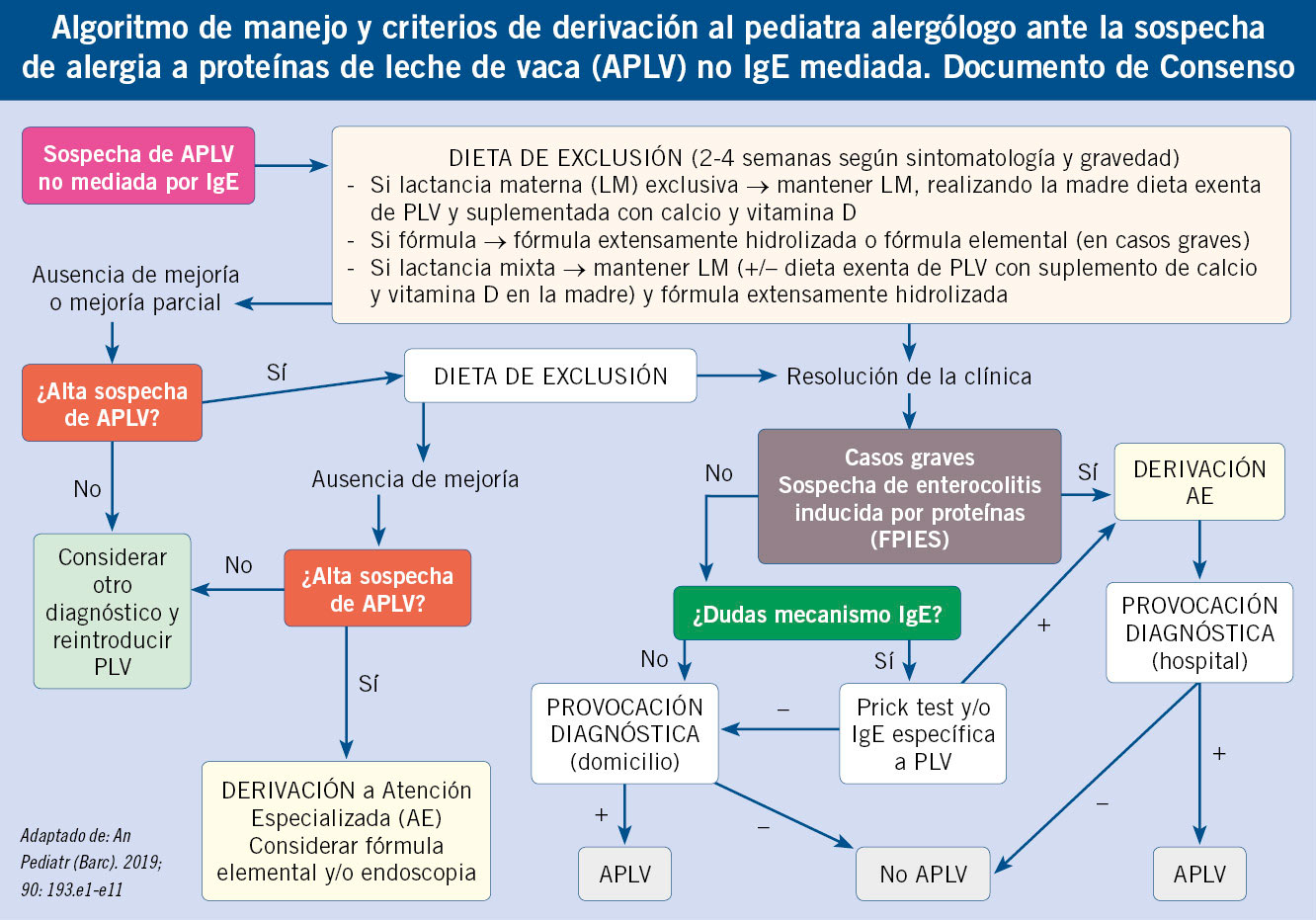
Debemos recordar que los cuadros de hipersensibilidad a alimentos no IgE mediada presentan un mecanismo inmunológico subyacente y, por tanto, una alergia no mediada por IgE. Se debe evitar el uso de terminología inapropiada como “intolerancia a las proteínas de leche de vaca”. Son patologías que hay que tener en mente, puesto que su diagnóstico es clínico y hay que sospecharlas en lactantes con sintomatología digestiva compatible. Son útiles las tablas con los criterios diagnósticos y el algoritmo de manejo y derivación del consenso pediátrico español publicado en Anales Españoles de Pediatría en 2019 (Algoritmo).
Las proctocolitis que responden bien a la exclusión de leche de vaca en dos semanas, se pueden manejar en primaria derivando las que tengan una evolución atípica, se debe valorar/observar la tolerancia a alimentos como soja y huevo.
Las enteropatías leves-moderadas, en las que las proteínas de leche de vaca son el agente causal y los síntomas revierten sin complicaciones tras la retirada de estas, pueden asumirse desde Atención Primaria. En los casos graves o en los que el alérgeno no es la leche de vaca, se recomienda la derivación.
Las FPIES deben remitirse siempre al especialista para la valoración inicial, seguimiento y la reintroducción de forma controlada siempre en ámbito hospitalario(17).
Actualmente, con mejores trabajos y estudios de calidad, se debe hacer un estudio riguroso de la alergia alimentaria. Las dietas de eliminación han de ser estrictas, pero muy precisas. Se debe tener un enfoque multidisciplinar, sobre todo en alergias complejas, para evitar la repercusión en el desarrollo físico y emocional del niño y su familia. La educación del paciente, la familia y todo el entorno escolar y lúdico deportivo han de ser una prioridad. Se debe seguir trabajando para tomar las medidas que, de una forma precoz, favorezcan la tolerancia, sobre todo en alergia IgE mediada(18).
Conflicto de intereses
No hay conflicto de interés en la elaboración del manuscrito. Declaración de intereses: ninguno.
Bibliografía
Los asteriscos reflejan el interés del artículo a juicio de la autora.
1. Prescott S, Allen KJ. Food allergy: Riding the second wave of the allergy epidemic. Pediatr Allergy Immunol. 2011; 22: 155-60.
2. Fundación de Seguridad Alimentaria y Prevención de Alergias. Incidencia de la alergia alimentaria. Acceso en octubre de 2022. Disponible en: https://funsapa.org/alergia-alimentaria/incidencia/.
3. Tanno LK, Clark E, Mamodaly M, Cardona V, Ebisawa M, Asontegui I, et al. Food-Induced Anaphylaxis Morbidity: Emergency Departmental Data and Hospitalization Preventive Support Strategies. Pediatrician Allergy Immunol. 2021; 32: 1730-42. Disponible en: https://doi.org/10.1111/pai.13578.
4. Escarrer-Jaume M, Juliá-Benito JC, Quevedo-Teruel S, Prieto del-Prado A, Sandoval-Ruballo M, Quesada-Sequeira F, et al. Cambios en la epidemiología y en la práctica clínica de la alergia mediada por IgE en Pediatría. An Pediatr. 2021; 95: 56e1-56e.8. Disponible en: https://doi.org/10.1016/j.anpedi.2021.04.014.
5.** Fernández-Rivas M, Vera Berrios RN. La alergia a los alimentos. ¿Cómo convivir con ella? En: El libro de las enfermedades alérgicas: Zubeldia JM, Baeza ML, Chivato T, eds. 2ª ed. Bilbao: Fundación BBVA; 2021. p. 223-9.
6.*** Valdesoiro Navarrete L, Vila Sexto L. Alergia a alimentos mediada por IgE. Protoc diagn ter Pediatr. 2019; 2: 185-94.
7. Artigas Magriña R. Alergia a alimentos. En: Bras J, De la Flor J. Pediatría en Atención Primaria, 4ª ed. Madrid: Ergon; 2018. p. 968-1001.
8.*** Echeverría Zudaire LA. Novedades en diagnóstico y prevención de la alergia alimentaria. En: AEPap (ed.). Congreso de Actualización Pediatría 2019. Madrid: Lúa Ediciones 3.0; 2019. p. 233-47. Disponible en: https://www.aepap.org/sites/default/files/pags._233-248_novedades_en_diagnostico_y_prevencion._.pdf.
9. Hicks A, Palmer C, Bauer M, Venter C. Accidental ingestions to known allergens by food allergic children and adolescents. Pediatric Allergy and Immunology. 2021; 32: 1718-29. Disponible en: https://doi.org/10.1111/pai.13573.
10. Sociedad Española de Inmunología Clínica A y AP. Legislación sobre declaración obligatoria de alérgenos alimentarios. 2019. Acceso en noviembre de 2022. Disponible en: https://seicap.es/wp-content/uploads/2022/05/Legislacion-Alergia-a-Alimentos.pdf.
11. Mayo Clinic. Alergia Alimentaria. Acceso en diciembre de 2022. Disponible en: https://www.mayoclinic.org/es-es/diseases-conditions/food-allergy/symptoms-causes/syc-20355095.
12. Julia Benito JC, Sánchez Salguero CA, Alvarado Izquierdo MI, Álvarez Caro F, Arroabarren Alemán E, Capataz Ledesma M, et al. Manual de Anafilaxia Pediátrica. Acceso en octubre de 2022. Disponible en: https://seicap.es/wp-content/uploads/2022/05/MAP2017-Version-2-1.pdf.
13. Martorell Aragonés A. Inmunoterapia específica con alérgenos alimentarios. Protoc diagn ter pediatr. 2019; 2: 271-84.
14.*** Halken S, Muraro A, de Silva D, Khaleva E, Angier E, Arasi S, et al; European Academy of Allergy and Clinical Immunology Food Allergy and Anaphylaxis Guidelines Group. EAACI guideline: Preventing the development of food allergy in infants and young children (2020 update). Pediatr Allergy Immunol. 2021; 32: 843-58. DOI: 10.1111/pai.13496.
15.*** Claver Monzón A, Pinto Fernández C. Alergia alimentaria no mediada por IgE. Protoc diagn ter pediatr. 2019; 2: 195-206.
16.*** Espín Jaime B, Díaz Martín JJ, Blesa Baviera LC, Claver Monzón A, Hernández Hernández A, García Burriel JI, et al. Alergia a las proteínas de leche de vaca no mediada por IgE: documento de consenso de la Sociedad Española de Gastroenterología, Hepatología y Nutrición Pediátrica (SEGHNP), la Asociación Española de Pediatría de Atención Primaria (AEPap), la Sociedad Española de Pediatría Extrahospitalaria y Atención Primaria (SEPEAP) y la Sociedad Española de Inmunología Clínica, Alergología y Asma Pediátrica (SEICAP). An Pediatr (Barc). 2019; 90: 193.e1-192.e11.
17. Labrosse R, Graham F, Caubet J-C. Non-IgE-Mediated Gastrointestinal Food Allergies in Children: An Update. Nutrients. 2020; 12: 2086.
18. Turner PJ, Arasi S, Ballmer-Weber B, Baseggio Conrado A, Deschildre A, Gerdts J, et al; the Global Allergy, Asthma European Network (GA2LEN) Food Allergy Guideline Group. Risk factors for severe reactions in food allergy: Rapid evidence review with meta-analysis. Allergy. 2022; 77: 2634-52.
19. Macías Iglesias EM. Alergia a los alimentos. Pediatr Integral. 2018; XXII: 87-93.
Bibliografía recomendada
– Echeverría Zudaire LA. Novedades en diagnóstico y prevención de la alergia alimentaria. En: AEPap (ed.). Congreso de Actualización Pediatría 2019. Madrid: Lúa Ediciones 3.0; 2019. p. 233-47. Disponible en: https://www.aepap.org/sites/default/files/pags._233-248_novedades_en_diagnostico_y_prevencion._.pdf.
Actualización dirigida al pediatra de Atención Primaria, de las novedades en el diagnóstico, manejo y prevención de la alergia alimentaria, desde la perspectiva de una pediatra alergólogo de gran experiencia.
– Halken S, Muraro A, de Silva D, Khaleva E, Angier E, Arasi S, et al; European Academy of Allergy and Clinical Immunology Food Allergy and Anaphylaxis Guidelines Group. EAACI guideline: Preventing the development of food allergy in infants and young children (2020 update). Pediatr Allergy Immunol. 2021; 32: 843-58. DOI: 10.1111/pai.13496.
Revisión de la evidencia publicada en un tema de gran importancia y trascendencia. ¿Podemos hacer alguna cosa los pediatras para evitar el incremento de la prevalencia de la alergia alimentaria y sus consecuencias? Desde la Academia Europea, nos proponen algunas líneas de actuación que se recogen en esta actualización.
– Valdesoiro Navarrete L, Vila Sexto L. Alergia a alimentos mediada por IgE. Protoc diagn ter pediatr. 2019; 2: 185-94.
Revisión de pediatras alergólogos dirigida a pediatras no especialistas sobre clínica, manejo y diagnóstico de la alergia alimentaria de tipo IgE. Publicación en el apartado de protocolos de la AEP.
– Espín Jaime B, Díaz Martín JJ, Blesa Baviera LC, Claver Monzón A, Hernández Hernández A, García Burriel JI, et al. Alergia a las proteínas de leche de vaca no mediada por IgE: documento de consenso de la Sociedad Española de Gastroenterología, Hepatología y Nutrición Pediátrica (SEGHNP), la Asociación Española de Pediatría de Atención Primaria (AEPap), la Sociedad Española de Pediatría Extrahospitalaria y Atención Primaria (SEPEAP) y la Sociedad Española de Inmunología Clínica, Alergología y Asma Pediátrica (SEICAP). An Pediatr (Barc). 2019; 90: 193.e1-192.e11.
Documento de consenso de todas las Sociedades científicas implicadas en un tema tan poco estructurado, hasta ese momento, sobre la alergia no IgE mediada a la leche de vaca. Imprescindible lectura.
| Caso clínico |
|
Lola es una lactante de 5 meses, toma lactancia materna exclusiva. Antecedentes familiares: padre rinitis alérgica. Antecedentes personales: dermatitis atópica leve. Inicia lactancia artificial por motivos laborales inexcusables de la madre. Tras la segunda toma presenta reacción cutánea consistente en eritema facial y sensación de picor ocular intenso, sin otros signos asociados.
|






 Eosinophilic disease of the esophago-gastro-intestinal tract
Eosinophilic disease of the esophago-gastro-intestinal tract