Profilaxis antimicrobiana
y postexposición
Introducción
La profilaxis antimicrobiana consiste en la administración preventiva de antibióticos con la finalidad de evitar el desarrollo de una enfermedad infecciosa. La profilaxis postexposición es una estrategia que pretende evitar el contagio de una infección cuando una persona se ha expuesto a ella.
Aunque la prescripción de antibióticos con el fin de evitar la aparición de una infección es una tentativa en la praxis clínica, son pocas y muy concretas las situaciones clínicas en las que esta estrategia se ha documentado como beneficiosa y recomendable.
La profilaxis antimicrobiana se basa en la utilización de antibióticos en ausencia de infección para prevenir el desarrollo de la misma. Existen unas premisas que deben tenerse muy en cuenta cuando se plantea esta estrategia preventiva y que permiten un adecuado balance entre el beneficio y los riesgos de la medida. Los fármacos utilizados deben: ofrecer una cobertura ajustada a los patógenos más prevalentes para cada indicación concreta, tener un espectro antimicrobiano lo más estrecho posible y utilizarse durante un periodo de tiempo breve(1). En cualquier contexto en que se plantee la profilaxis antibiótica, es obligado cuestionarse si los riesgos podrían minimizar significativamente el beneficio esperado: la aparición de resistencias bacterianas es un problema ya asociado al uso general de los antimicrobianos y, por tanto, muy a tener en cuenta cuando estos se utilizan profilácticamente, la presencia de efectos adversos relacionados con el fármaco utilizado y, finalmente, el impacto, reconocido pero no adecuadamente estudiado en cuanto a sus consecuencias para la salud, por la eliminación de la flora bacteriana comensal y muy concretamente por la modificación de la microflora intestinal(2). A pesar de estas consideraciones, existen situaciones en las que, para algunos microorganismos concretos, en situaciones clínicas bien definidas, o en huéspedes especialmente vulnerables, la profilaxis antibiótica es eficaz y puede ser recomendable.
La profilaxis postexposición es otra estrategia que pretende evitar el desarrollo de una enfermedad infecciosa en una persona susceptible a la misma, pero cuya indicación se sustenta por haber presentado un tipo de exposición que se considera de alto riesgo de contagio debido a un contacto con un paciente enfermo o con sus secreciones. En la profilaxis postexposición, y dependiente del microorganismo implicado, pueden utilizarse antibióticos (profilaxis antimicrobiana), inmunoglobulinas y/o vacunas (inmunoprofilaxis)(3).
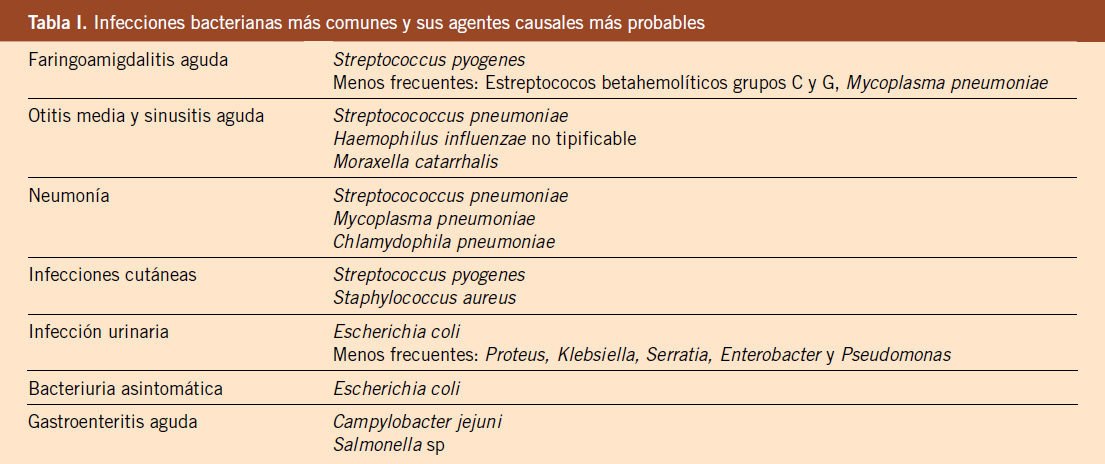
Por su mayor frecuencia y por requerir una implicación más específica del pediatra de Atención Primaria, se han seleccionado para este capítulo las situaciones clínicas y las enfermedades infecciosas tributarias de profilaxis antimicrobiana y postexposición que se incluyen en las tablas I y II. No se abordará la profilaxis antibiótica del paciente inmunodeprimido, oncológico, con enfermedad crónica, quemado o quirúrgico, y del viajero, ya que se escapa del objetivo de esta actualización.
Profilaxis antimicrobiana
En este apartado, se tratarán diversas situaciones clínicas de especial riesgo de infección, infecciones con tendencia a la recurrencia, procesos patológicos que hacen al huésped más vulnerable a determinadas infecciones y enfermedades prevenibles con profilaxis postexposición, todas ellas tributarias de profilaxis antimicrobiana (Tabla I).

Oftalmía neonatal
La profilaxis de la oftalmía neonatal es una estrategia recomendada para todos los neonatos.
Aunque se considera la oftalmía neonatal a toda conjuntivitis que se produce en las primeras 4 semanas de vida, la profilaxis de la misma va dirigida específicamente a la prevención de la infección ocular por Neisseria gonorrhoeae y Chlamydia trachomatis.De forma ideal, la profilaxis de estas infecciones debería ir dirigida a la detección y tratamiento antes del parto de las embarazadas afectadas y sus parejas sexuales, pero esta estrategia es compleja y, probablemente, insuficiente, debido a que la mayoría de estas infecciones pueden ser asintomáticas en las madres y suelen pasar desapercibidas(4). El neonato se contagia generalmente en el canal del parto, el riesgo de infección es elevado y causan conjuntivitis severas que pueden dejar graves secuelas, en algunos casos una ceguera. Se han descrito también infecciones por vía ascendente, por lo que también se considera a los nacidos por cesárea, neonatos con riesgo de infección(1). Otros patógenos implicados en la oftalmía neonatal son bacterias (estreptococos, estafilococos, Haemophilus influenzae no tipable) presentes en el canal del parto y que ocasionan conjuntivitis habitualmente leves, con excepción de las producidas por el virus del herpes simple de madres infectadas que puede generar una queratoconjuntivitis grave.
Se recomienda la profilaxis universal de la oftalmía neonatal a todos los neonatos (incluidos los nacidos por cesárea) mediante la aplicación tópica en ambos ojos de un antimicrobiano apropiado. Aunque la utilización de la solución de nitrato de plata al 1% es efectiva, su uso se ha abandonado por la gran incidencia de conjuntivitis química que provoca. Las dos preparaciones recomendadas son las pomadas oftálmicas de eritromicina al 0,5% o de aureomicina al 1%, ambas disponibles en nuestro medio y con una eficacia superponible. La profilaxis es muy efectiva frente a la conjuntivitis por gonococo y, aunque reduce también la conjuntivitis por C. trachomatis, no evita la colonización nasofaríngea y el riesgo de neumonía por clamidia. También, reduce la incidencia de oftalmía producida por otras bacterias presentes en el canal del parto(3,4).
Se administra una dosis única en el saco conjuntival inferior de ambos ojos, lo antes posible después del nacimiento, idealmente antes de 1 hora. El retraso en la aplicación puede reducir la eficacia de la medida. Tras la aplicación, deben frotarse suavemente los párpados para extender la pomada. No deben enjuagarse los ojos tras la aplicación.
Mordeduras humanas o por animales
Las mordeduras no requieren, de forma sistemática, profilaxis antibiótica.
Las mordeduras humanas o por animales son una consulta frecuente en Atención Primaria y plantea al pediatra la disyuntiva sobre la necesidad o no de indicación del tratamiento antibiótico para evitar la infección de la lesión. No hay datos fiables que cuantifiquen la frecuencia de las mordeduras humanas y, de hecho, muchas de ellas no llegan a ser atendidas en un centro sanitario. En lactantes y niños pequeños, suelen ser debidas a mordeduras directas entre ellos o por caídas con hincamiento de los dientes. En niños mayores, además de los mecanismos anteriores, se añaden las debidas a puñetazos en la cara, con lesiones incisas y punzantes en la mano del agresor provocadas por la dentición del agredido. Más del 80% de las mordeduras por animales en nuestro medio son producidas por perros, poco más del 10% por gatos y el resto por otros animales domésticos, como: conejos, hamsters u otras mascotas menos convencionales(2).
Aunque clásicamente se ha considerado que una mordedura es sinónimo de herida infectada, la realidad es que sólo entre un 10-15% de las mordeduras humanas se infectan, entre un 10-15% de las de perro y entre un 10 a 50% de las producidas por gatos. Cuando se produce la infección, suele ser polimicrobiana, con una media de hasta 5 gérmenes que, en más del 50% de los casos, corresponden a una mezcla de microorganismos aerobios y anaerobios. Son comunes las bacterias aerobias Gram + y Gram -, como: estafilococos, estreptococos, especies de Moraxella y de Neisseria, y anaerobias, como: Fusobacterium, Bacteroides, Porphyromonas, Prevotella, Propionibacterium, y especies de Peptostreptococcus.En las mordeduras infectadas por animales, las especies de Pasteurella son los microorganismos más frecuentemente aislados, predominantemente P. canis en caso de perros y P. multocida en caso de gatos; mientras que, en las humanas es muy frecuente Eikenella corrodens (anaerobio Gram -).
Una revisión de la Cochrane Libraryen 2001, concluía que existe evidencia que la administración de antibióticos reduce la probabilidad de infección después de las mordeduras humanas, pero no es concluyente cuando se aplica de forma sistemática en las de perros y gatos(6). Deben considerarse, además del origen, animal o humano, otros factores para recomendar la profilaxis de este tipo de lesiones, como son las características de la herida, el periodo transcurrido desde la mordedura, la localización y la presencia de patología en el huésped, que incrementen el riesgo de infección. No se requiere profilaxis antibiótica en todas las heridas por mordedura. Los pacientes con heridas leves en las que la piel está erosionada no necesitan ser tratados con agentes antimicrobianos. En el resto de mordeduras, debe limitarse la indicación de profilaxis a los casos con mayor riesgo de infección y que, en general, se concretan en(1,5):
• Heridas con lesiones moderadas y graves, especialmente si hay edema o lesión por compresión, o con dificultades para desbridar o limpiar.
• Heridas punzantes (especialmente, por gato) y siempre que exista penetración del hueso, la vaina del tendón o la articulación.
• Heridas en cara, manos, pies y zona genital.
• Heridas en personas inmunocomprometidas y asplénicas.
El primer paso para evitar la infección de una mordedura es la adecuada limpieza y desinfección de la herida. Si se considera tributaria de profilaxis, el antibiótico de elección, tanto para las mordeduras de origen humano como animal, es la asociación de amoxicilina-ácido clavulánico a la dosis de 40-50 mg/kg/día (en base a la amoxicilina), administrada cada 8 horas durante 3-5 días. La profilaxis debe iniciarse idealmente en las primera 8-12 horas tras sufrir la mordedura, y es recomendable revisar la herida a las 48 horas de iniciado el tratamiento para descartar la presencia de infección. En pacientes alérgicos a los betalactámicos, puede utilizarse cefadroxilo o cefuroxima asociados a clindamicina, o clotrimoxazol (trimetoprim-sulfametoxazol) también con clindamicina. La azitromicina presenta una adecuada cobertura para la mayoría de las bacterias implicadas, y es una alternativa en estos casos, aunque no hay datos clínicos que avalen su eficacia. En mayores de 8 años la doxiciclina es también una buena opción. Siempre debe comprobarse que el paciente está correctamente vacunado frente a tétanos, e iniciar o completar la vacunación si fuere necesario. En las mordeduras humanas, debe considerarse el riesgo potencial de transmisión de la hepatitis B, en función de la susceptibilidad y el estado serológico del agresor y del agredido. Aunque teóricamente también existe riesgo de transmisión del VIH y de hepatitis C, estas infecciones no se transmiten de una forma eficiente por las mordeduras y sólo debería considerarse el riesgo en situaciones muy concretas. En las mordeduras por animal, se debe tener en cuenta, según la zona geográfica, el animal y las circunstancias, la necesidad de observar el animal ante síntomas de rabia y/o la profilaxis postexposición antirrábica del paciente(1,5).
Otitis media aguda
Algunos de los pacientes con otitis media recurrente sin derrame crónico en oído medio pueden beneficiarse de una profilaxis antibiótica.
La otitis media aguda (OMA) es una de las enfermedades infecciosas en los niños que con mayor frecuencia es motivo de consulta médica y consumo de antibióticos. El problema adquiere aún más relevancia cuando hasta un 20-40% de los niños desarrollan episodios de otitis media aguda recurrente (OMAr), otitis media secretora o con exudado (OME) de larga evolución, o ambas. Es conveniente diferenciar estas dos situaciones, ya que su manejo es distinto. La OMAr hace referencia a los pacientes que presentan 3 episodios o más de OMA en los últimos 6 meses, o 4 episodios en los últimos 12 meses, habiendo presentado al menos el último episodio en los 6 meses precedentes a la consideración de este diagnóstico. La OME hace referencia a la persistencia del derrame del oído medio después de los episodios de OMA, situación que suele resolverse espontáneamente en la mayoría de los casos entre las 2 semanas y los 2 meses tras la OMA. La persistencia de la OME a partir de los 3 meses, indica cronicidad del derrame en el oído medio que puede tener repercusiones funcionales auditivas y, además, asociarse o no a recurrencias (OMAr)(7). Existen dificultades para el diagnóstico de la presencia de derrame en el oído medio; ya que, la otoscopia muchas veces no es concluyente y para ello debería realizarse una otoscopia neumática o, preferiblemente, una timpanometría.
Existen unos factores personales que incrementan el riesgo de padecer OMAr, como: ser varón, antecedentes de prematuridad, presentar un primer episodio de OMA en el primer año, especialmente en los primeros 6 meses, historia familiar de OMAr en padre o hermanos o historia personal de atopia. Pero también existen unos factores ambientales que incrementan el riesgo, que pueden ser modificables, y actuar sobre ellos es la primera estrategia a recomendar en caso de OMAr: tabaquismo pasivo, asistencia a la guardería o uso de chupete. La lactancia materna tiene un efecto protector sobre la incidencia de OMA y, por tanto, reduce el riesgo de OMAr. La vacunación antineumocócica y la vacunación antigripal también deben considerarse como herramientas preventivas para el desarrollo de OMA y OMAr(7).
En los niños con OMAr se han planteado diversas estrategias de manejo, desde la actitud expectante tratando los episodios agudos, la profilaxis antibiótica y la colocación de tubos de ventilación transtimpánica. Diversos estudios han corroborado que la profilaxis antibiótica (amoxicilina o sulfonamidas) reduce significativamente el número de episodios de OMA en estos niños, en una media de 1,5 a 3 episodios menos por año. Esta reducción es similar a la que se obtiene por la colocación de tubos de ventilación transtimpánicos, y en ambos casos superior al placebo. No obstante, la profilaxis antibiótica no debe recomendarse en los niños con derrame persistente en oído medio (OME), en los que la estrategia de elección, cuando está indicada la prevención, es el drenaje transtimpánico quirúrgico. La profilaxis antibiótica debe reservarse para los niños con criterios de OMAr que no presentan derrame persistente en oído medio (OME) entre los episodios de OMA. Además, por elevado riesgo de desarrollar recurrencias, deben considerarse como tributarios de profilaxis antibiótica los pacientes que han presentado un episodio de OMA en los primeros 6 meses de vida o dos en el primer año, si tienen historia familiar (padres o hermanos) de OMAr(2,7,8).
Los riesgos de la quimioprofilaxis están vinculados al desarrollo de resistencias bacterianas que compliquen el manejo posterior de nuevos episodios de OMA. Los antibióticos mejor estudiados y con los que se ha corroborado la eficacia de la estrategia preventiva son el clotrimoxazol (trimetoprim-sulfametoxazol) y la amoxicilina. Las dosis recomendadas son aproximadamente la mitad de la dosis terapéutica diaria (trimetoprim 3-4 mg/kg/día-sulfametoxazol 15-20 mg/kg/día, o amoxicilina a 20-25 mg/kg/día) administradas en una sola dosis, preferiblemente por la noche(7). En nuestro medio la mayoría de autores recomiendan amoxicilina dada la mayor tasa de resistencias in vitro al clotrimoxazol, aunque no hay estudios que evalúen las posibles diferencias de efectividad en nuestro entorno. La prevención debe realizarse durante los meses de mayor riesgo de infecciones respiratorias, otoño e invierno, con una duración de 3 a 6 meses, suspendiéndose en primavera y verano.
Aunque en la praxis clínica también se utiliza azitromicina en dosis única semanal o la asociación amoxicilina-ácido clavulánico en dosis única diaria, no hay estudios clínicos que avalen estas alternativas, y por su más amplio espectro antimicrobiano que, además, representa un mayor riesgo de desarrollo de cepas resistentes, no es recomendable su utilización, al menos como primera elección(2).
Las OMA que se produzcan durante el periodo de quimioprofilaxis, deben tratarse con un antibiótico distinto, siendo recomendable indicar amoxicilina-ácido clavulánico como tratamiento de elección y, en caso de fallo terapéutico, ceftriaxona intramuscular(7).
Infección del tracto urinario
No se recomienda de forma rutinaria la profilaxis antibiótica después de una primera infección urinaria no complicada en la infancia.
La profilaxis antibiótica en la prevención de las infecciones urinarias recurrentes ha sido una pauta establecida durante décadas, especialmente dirigida a los pacientes con reflujo vesicoureteral u otras anomalías urológicas. El objetivo de la profilaxis estuvo siempre planteado para evitar la aparición de cicatrices renales secundarias a pielonefritis y que conllevarán el desarrollo evolutivo de una nefropatía con proteinuria, hipertensión y, finalmente, con insuficiencia renal crónica (IRC). Con la aparición en los últimos años de diversos estudios que cuestionan el beneficio real de esta quimioprofilaxis, incluso en algunos casos de la corrección quirúrgica del reflujo, se han producido cambios muy relevantes en las recomendaciones del manejo de estas patologías y de la pauta de actuación ante un paciente con infección del tracto urinario (ITU).
La ITU es un proceso frecuente en la edad pediátrica, que afecta entre el 3 y el 7% de los niños, siendo frecuente la recurrencia, que se observa hasta en el 30% de los casos. Entre el 15 y 35% de los pacientes con ITU, presentan reflujo vesicoureteral (RVU) de grado variable y, alrededor de un 5-10%, otras malformaciones renales, como hidronefrosis o duplicación renal. El 60% de los niños con ITU febril presentan realmente una pielonefritis aguda y, de estos, el riesgo de daño renal con cicatrices permanentes oscila entre el 15 y el 60%. Cuanto mayor grado de RVU, mayor riesgo de cicatrices renales. También, la presencia de infecciones recurrentes, independientemente del grado de reflujo, se asocia a mayor riesgo de daño renal.
Hoy sabemos que el riesgo de que un niño con ITU desarrolle una IRC es de 1/10.000 y que, aunque la ITU es una patología frecuente que puede tener tendencia a la recurrencia, sólo de forma muy ocasional es un marcador de daño renal congénito o de obstrucción urinaria. Y, además, en ausencia de una de estas alteraciones estructurales, fácilmente demostrables con la ecografía, las infecciones urinarias recurrentes representan muy bajo riesgo de desarrollo de patología renal crónica. Por tanto, un niño con riñones normales no presenta un riesgo muy significativo de desarrollar una enfermedad renal crónica por el hecho de presentar una ITU incluso con recurrencias(9,10).
Paralelamente, en los últimos 10 años, diversos estudios han puesto en evidencia la ineficacia de la profilaxis en la prevención de infecciones urinarias recurrentes en pacientes con y sin RVE, incluso en la reducción del daño renal asociado o, en todo caso, con un beneficio discreto. Además, se corrobora un incremento de resistencias a los antibióticos en las infecciones en pacientes sometidos a profilaxis antimicrobiana. Sobre la base de todos estos datos, la American Academy of Pediatrics (AAP) actualiza en 2011 sus recomendaciones para el manejo de la ITU, enfatizando que lo más importante, cara a evitar un daño renal permanente, es el diagnóstico precoz y el tratamiento efectivo de la ITU y sus recurrencias, independientemente de la existencia de RVU o de que el paciente reciba profilaxis antibiótica(11).
En espera de nuevos datos de estudios prospectivos que clarifiquen el rol que juega la profilaxis en el manejo de estos pacientes, las recomendaciones actuales y definidas en la guía de práctica clínica del Sistema Nacional de Salud establecen, para la edad pediátrica, las siguientes consideraciones(12):
• No se aconseja la profilaxis antibiótica de forma rutinaria después de una primera ITU no complicada.
• No se recomienda la profilaxis en niños o niñas con bacteriuria asintomática.
• Se recomienda la profilaxis antibiótica en pacientes con RVU muy dilatado (grados IV-V) y de forma individualizada en pacientes con pielonefritis recurrentes.
• Se recomienda el uso de profilaxis antibiótica en los pacientes con dilatación de la vía urinaria con sospecha de obstrucción (ectasia piélica >10-15 mm en período postnatal), hasta que se confirme y se trate adecuadamente. No es necesaria la profilaxis en las dilataciones de la vía urinaria en las que se descarta la obstrucción.
Los fármacos de elección para la profilaxis son trimetoprim-sulfametozaxol y nitrofurantoína. En menores de 2 meses, y de forma transitoria hasta que superen esta edad, se recomienda la utilización de amoxicilina o una cefalosporina de primera generación, como cefalexina o cefadroxilo. En la tabla III, se incluye la pauta posológica de los fármacos utilizados. No se recomienda la utilización de otros antibióticos como amoxicilina-ácido clavulánico o cefalosporinas de espectro amplio, por su mayor impacto sobre la flora intestinal, y su mayor riesgo de generar resistencias, dificultando el manejo de nuevas ITU en caso de recurrencias.
Es aconsejable que la duración de la profilaxis se limite idealmente a un año, dependiendo de la recurrencia de infecciones, o hasta que se compruebe la reducción del grado de reflujo en los casos con reflujo de grado alto. En los pacientes con dilataciones obstructivas de la vía urinaria, debe mantenerse hasta la resolución de la obstrucción.

Endocarditis bacteriana
Las actuales recomendaciones reducen significativamente las condiciones cardiacas y los procedimientos en los que se aconseja la profilaxis.
Desde hace más de 50 años, la administración profiláctica de antibióticos ha sido una práctica médica habitual en la prevención de endocarditis bacteriana en pacientes con cardiopatías. Paralelamente, han ido apareciendo estudios que ponían en cuestión la validez de esta estrategia en algunas de las indicaciones universalmente aceptadas. En 2007, la Asociación Americana de Cardiología emitió unas nuevas recomendaciones que modificaban muy sensiblemente las establecidas previamente, y que en 2009 fueron también aceptadas y asumidas por la Sociedad Europea de Cardiología y la Sociedad Española de Cardiología. El cambio de recomendaciones se sustenta en la evidencia de que la endocarditis bacteriana es mucho más probable que se produzca como consecuencia de las bacteriemias espontáneas asociadas a las actividades diarias normales, que con las debidas a procedimientos odontológicos, gastrointestinales o genitourinarios. El mantenimiento de una óptima higiene y salud bucodental es más importante que la profilaxis antibiótica para reducir el riesgo de bacteriemias y de endocarditis bacteriana en pacientes con cardiopatías. Incluso considerando que la profilaxis antibiótica fuera altamente eficaz, sólo se conseguiría prevenir un número muy reducido de casos de endocarditis. Finalmente, los efectos adversos de la profilaxis antibiótica superan claramente los potenciales beneficios (si realmente estos existen)(13).
Con las actuales recomendaciones, se reducen significativamente las condiciones cardiacas en las que se aconseja la profilaxis. Se considera razonable indicar la profilaxis sólo en aquellas que tienen un mayor riesgo de mala evolución en caso de endocarditis, y se limitan a(1,4,13):
• Portadores de válvula cardiaca protésica o de material protésico para reparar una válvula.
• Antecedente de endocarditis bacteriana previa.
• Determinadas cardiopatías congénitas (CC):
– CC cianosantes no corregidas, incluyendo las que llevan conductos o shuntspaliativos.
– Defectos cardiacos congénitos reparados completamente con material protésico o dispositivos, colocados quirúrgicamente o mediante cateterismo, y sólo durante los primeros 6 meses siguientes al procedimiento.
– CC reparadas pero con defectos residuales en el lugar o en la zona adyacente de un parche o dispositivo protésico, que inhibe la endotelización.
• Receptores de trasplante cardiaco que desarrollan una valvulopatía.
En el momento actual, no se recomienda la profilaxis antibiótica en ninguna otra cardiopatía congénita o situación distinta a las enumeradas anteriormente(1,13).
También, se reducen las indicaciones en las que se considera razonable la práctica de profilaxis antibiótica, en los pacientes con las situaciones cardiacas citadas anteriormente, a los siguientes procedimientos(1,4,13):
• Procedimientos bucodentales que impliquen la manipulación de tejidos gingivales, la región periapical del diente o que perforen la mucosa oral. Si bien, debe considerarse cuando se realiza una biopsia o se retiran puntos de sutura, no se recomienda para la inyección de anestesia en mucosa no infectada, colocación o ajustes de ortodoncia extraíble o brackets, extracción de dientes deciduales, ni en los sangrados por traumatismos de los labios o de mucosa oral.
• Procedimientos invasivos de las vías respiratorias que conlleven la incisión de la mucosa del tracto respiratorio, como amigdalectomías, adenoidectomías o broncoscopia con biopsia. No se recomienda en la broncoscopia, laringoscopia o en la intubación endotraqueal.
• No se recomienda la profilaxis dirigida a endocarditis bacteriana en procedimientos sobre piel, estructuras cutáneas o tejido musculoesquelético. No se considera necesaria la profilaxis si estos pacientes se someten a tatuajes, pero se advierte del posible riesgo con la colocación de piercings.
• No se recomienda la profilaxis dirigida a endocarditis bacteriana en ningún procedimiento en el tracto genitourinario ni gastrointestinal. No se considera necesaria la profilaxis en el parto vaginal o por cesárea, ni en la práctica de histerectomías.
Un concepto distinto a la profilaxis de endocarditis en sentido estricto, pero que también pretende prevenirla. Hace referencia a la elección del antibiótico cuando se indica una pauta de tratamiento de un tejido infectado en el que se va a realizar un procedimiento invasivo. Así pues, cuando los pacientes con las condiciones cardiacas de riesgo citadas son sometidos a procedimientos invasivos de la vía respiratoria para tratar una infección establecida (absceso o empiema), en el régimen terapéutico debe incluirse un fármaco con actividad frente a estreptococos del grupo viridans y Staphylococcus aureus;en los que se realizan procedimientos frente a lesiones infectadas de la piel o sus estructuras, o en tejido musculoesquelético con infección, deben incluirse en la terapia antibióticos con cobertura para estafilococo y estreptococos beta-hemolíticos; y cuando se realizan en pacientes con infección establecida en el tracto gastroeintestinal o urogenital, o son intervenciones tributarias de profilaxis antibiótica prequirúrgica, deben utilizarse antibióticos con actividad frente a enterococos(13).
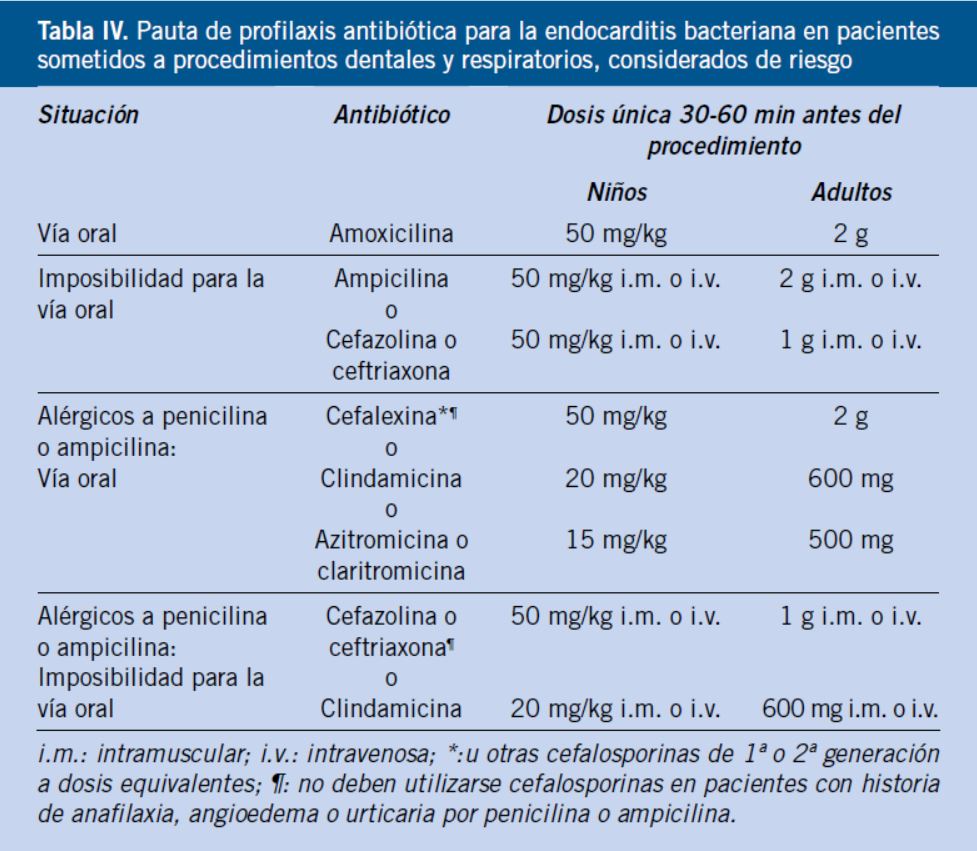
La profilaxis antibiótica en los procedimientos dentales y de la vía respiratoria, para los que se considera indicada, se realiza con una dosis única de antibiótico 30 a 60 minutos antes del procedimiento, siendo el fármaco de elección la amoxicilina. En la tabla IV, se esquematizan la pauta de elección, las alternativas y su posología.
Fiebre reumática
El adecuado tratamiento de la faringoamigdalitis por estreptococo beta-hemolítico del grupo A es realmente la principal estrategia de profilaxis primaria de la fiebre reumática.
El correcto diagnóstico de la etiología bacteriana de una faringitis, la elección del antibiótico adecuado y, muy especialmente, la duración del tratamiento tienen como objetivo principal, no ya la mejoría clínica y la curación del proceso, sino la prevención de la fiebre reumática(4). El inicio del tratamiento en los primeros 10 días desde el principio de los síntomas es eficaz para tal fin. La penicilina V por vía oral y la penicilina G benzatina por vía intramuscular siguen siendo los fármacos de elección. La amoxicilina por vía oral es una alternativa adecuada, especialmente en los niños pequeños, dado su mejor sabor y tolerancia, con eficacia parecida. Las cefalosporinas de primera o segunda generación deben reservarse para pacientes con alergia a la penicilina, y la clindamicina o los macrólidos para los que la alergia es de tipo anafiláctico. En la tabla V, se detalla la pauta posológica de todos estos fármacos(14).

La profilaxis secundaria va dirigida a prevenir las recurrencias de fiebre reumática debidas a nuevas infecciones por estreptococo beta-hemolítico del grupo A en pacientes ya diagnosticados de fiebre reumática, corea de Sydenham o con lesiones cardiacas de origen reumático. La prevención debe iniciarse inmediatamente en el momento en que se confirma el diagnóstico y deberá ser prolongada en función del mismo1,15):
• Fiebre reumática sin carditis: hasta 5 años después del último episodio o hasta cumplir 21 años (la opción más larga).
• Fiebre reumática con carditis pero sin lesión cardiaca residual (sin valvulopatía): hasta 10 años después del último episodio o hasta cumplir 21 años (la opción más larga).
• Pacientes con lesión cardiaca residual (valvulopatía persistente) de origen reumático: hasta 10 años después del último episodio o hasta cumplir 40 años (la opción más larga), aunque puede ser recomendable de por vida, incluso tras el recambio valvular protésico.
La profilaxis debe considerarse más allá de la edad recomendada para aquellas personas con riesgo alto de contacto con infectados por estreptococo beta-hemolítico del grupo A, como padres con hijos en edad escolar o maestros.
El fármaco de elección es la penicilina benzatina administrada por vía intramuscular cada 4 semanas. Aunque también puede utilizarse penicilina V por vía oral, la necesidad de su administración diaria durante periodos tan prolongados, hace que su cumplimento sea difícil de garantizar. En pacientes alérgicos a la penicilina, la profilaxis debe realizarse con eritromicina, siendo aceptables por su mejor tolerancia la claritromicina y la azitromicina, aunque su eficacia no ha sido evaluada para esta indicación (Tabla V).
Asplenia
Todos los pacientes sometidos a una esplenectomía deben recibir profilaxis antibiótica al menos durante 2 años.
Los pacientes con asplenia congénita o adquirida, o los que presentan una disfunción esplénica por presentar una hemoglobinopatía (drepanocitosis…), presentan mayor probabilidad de presentar una sepsis grave y con evolución fatal. Aunque los pacientes con drepanocitosis son los de mayor riesgo, en los niños sometidos a esplenectomía por trauma, el riesgo de sepsis es hasta 60 veces mayor en relación a los niños sanos. La mayor incidencia de sepsis en estos pacientes se observa en los primeros 5 años de vida y, especialmente, en los 2 años siguientes a sufrir la esplenectomía(3).
Aunque las infecciones pueden ser debidas a bacterias, virus, hongos o protozoos, los microorganismos causantes de las formas de sepsis grave son, por orden de frecuencia: Streptococcus pneumoniae, Haemophilus influenzae tipo b, Escherichia coliy Neisseria meningitidis(16).
La primera estrategia preventiva en los pacientes con asplenia es la vacunación frente a bacterias encapsuladas: neumococo, H. influenzae tipo b y meningococo. Una vez completada la vacunación antineumocócica con la vacuna conjugada 13-valente, debe administrase la vacuna polisacarídica 23-valente si el paciente tiene 2 o más años, o recibirla cuando alcance esa edad(4).
Es recomendable que todos los niños con asplenia, congénita o adquirida, reciban profilaxis antimicrobiana. Se ha comprobado una reducción >80% del riesgo de sepsis en niños con drepanocitosis menores de 3 años con la profilaxis. No obstante, ya no se observa beneficio por mantener la profilaxis más allá de los 5 años de edad. La profilaxis debe iniciarse a partir de los 2 meses de edad en los pacientes con asplenia congénita o disfunción esplénica, y mantenerse en todos los casos hasta cumplir los 5 años. En pacientes que se someten a una esplenectomía, la profilaxis debe realizarse al menos durante los 2 años siguientes, independiente de la edad. El antibiótico de elección es la penicilina V, a la dosis de 125 mg dos veces al día en menores de 5 años y de 250 mg dos veces al día en mayores de esta edad. Es aceptable utilizar amoxicilina, ya que es mejor tolerada en niños pequeños, a dosis de 20 mg/kg/día en dos tomas (dosis máxima: 250 mg por toma). Algunos autores recomiendan clotrimoxazol (4 mg/kg de TMP + 20 mg/kg de SMX) en lactantes de 2 a 6 meses por el mayor riesgo de sepsis por E. colien este rango de edad. En alérgicos a la penicilina, la alternativa son la eritromicina o el clotrimoxazol, aunque este último en nuestro medio, debido a la alta tasa de resistencia de neumococo, no es la mejor opción(3,4,16).
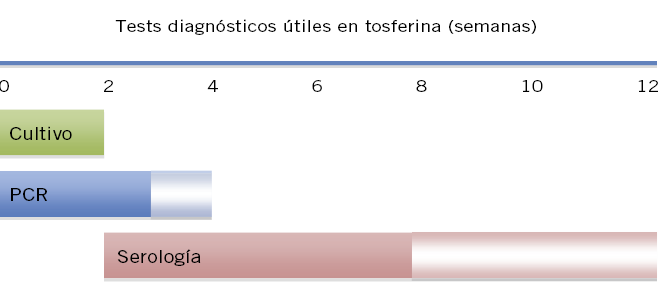
Tos ferina
La profilaxis de los contactos de un caso de tos ferina es prioritaria cuando estos son personas vulnerables con riesgo de enfermedad grave.
La profilaxis antimicrobiana postexposición frente a tos ferina tiene como objetivo interrumpir la transmisión y evitar la aparición de casos secundarios en la comunidad. Clásicamente, se ha dirigido a los contactos domésticos y otros contactos próximos de un caso con sospecha clínica fundada o confirmada de tos ferina. Aunque de forma genérica se han establecido recomendaciones de profilaxis para todos los contactos domésticos del caso índice, independientemente de su estado de vacunación(18), la quimioprofilaxis debería recomendarse siempre que existan convivientes no o incompletamente vacunados, y muy especialmente cuando existen contactos vulnerables: recién nacidos hijos de madres sintomáticas; neonatos, lactantes y niños vacunados parcialmente o no vacunados; personas con enfermedades crónicas (asma, cardiopatías, inmunodeprimidos…); y mujeres embarazadas(2).
No se recomienda la profilaxis de contactos en el entorno escolar dada su muy reducida eficacia. En cambio, debería considerarse en las guarderías, dirigida a todos los contactos de la misma aula (alumnos y educadores/as), independientemente de su estado de vacunación, especialmente si al aula acuden niños vacunados parcialmente o no vacunados.
Revisiones que han evaluado el impacto de la quimioprofilaxis en la reducción de casos secundarios obtienen una efectividad global baja. Sobre esta base, recomendaciones recientes proponen dirigir la quimioprofilaxis exclusivamente al entorno doméstico cuando en él existen contactos vulnerables y también a personas con contacto habitual con individuos de riesgo, con el único objetivo de evitar la aparición de casos graves.
La profilaxis debe iniciarse precozmente, siendo ineficaz si se instaura más allá de 21 días tras la aparición del caso índice. Los fármacos, la dosificación y la duración de la profilaxis son idénticos a las pautas de tratamiento. Los antibióticos de elección son los macrólidos: eritromicina, claritromicina y azitromicina. En menores de 1 mes, se recomienda utilizar azitromicina, por la asociación observada de la eritromicina con mayor riesgo de estenosis hipertrófica del píloro. En pacientes mayores de 2 meses de edad, con intolerancia a los macrólidos, puede utilizarse clotrimoxazol(1).
Finalmente, es recomendable actualizar o completar la vacunación frente a tos ferina de los contactos del caso índice tributarios de profilaxis antimicrobiana. En el capítulo sobre tos ferina en este mismo número de Pediatría Integral,se detallan las pautas posológicas de tratamiento y profilaxis, y se amplía la información de este apartado.
Infección meningocócica
Los contactos domésticos de un enfermo con enfermedad invasiva por meningococo son los que presentan mayor riesgo de contagio.
Los contactos, cercanos o íntimos, de niños o adultos con enfermedad meningocócica presentan un riesgo elevado de contraer la enfermedad invasiva y, por tanto, es aconsejable que reciban quimioprofilaxis. Los contactos en el entorno doméstico son los de mayor riesgo, con tasas de ataque de enfermedad muy superiores a las observadas en otros entornos o en la población general. Por esta razón, cualquier paciente con una enfermedad febril en el contexto de un paciente afecto de enfermedad meningocócica invasiva debe evaluarse sin demora.
Las situaciones consideradas de riesgo elevado en las que se recomienda la profilaxis antibiótica son(1,17):
• Convivientes: todas las personas que son contactos domésticos que mantienen una relación próxima, frecuente y duradera con el enfermo.
• Contactos esporádicos con exposición directa a secreciones del enfermo (besos), o han compartido cubiertos, vasos, cepillo de dientes, o han dormido en el mismo entorno en los 7 días previos.
• Personas que han practicado al paciente la respiración boca a boca o una intubación endotraqueal sin protección en los 7 días previos al inicio de la enfermedad o hasta 24 horas después de iniciar el tratamiento.
• Personas que, en los últimos 7 días, hayan viajado en avión sentados directamente al lado del caso índice, en vuelos de 8 o más horas de duración. Un contacto transitorio, como sentarse al lado del enfermo durante un viaje en coche, tren o autobús, no representa un riesgo especial.
• Contactos de guardería o parvulario: todos los compañeros y educadores/as del mismo grupo o clase del caso índice que han asistido a la guardería en los últimos 7 días. Sólo en los casos en que no sea factible delimitar el grupo o clase, podría considerarse la profilaxis en toda la guardería.
• En centros escolares de educación primaria, secundaria o bachillerato se debe valorar la administración de la quimioprofilaxis sólo a los compañeros que han tenido, en los últimos 7 días, un contacto más próximo y frecuente con el caso: compañeros más próximos en clase o de mesa en el comedor. Si no es posible delimitar el grupo de riesgo se puede considerar a toda la clase como máximo. Si aparecen más casos, al tratarse de un brote, deben seguirse las recomendaciones de las autoridades sanitarias.
No se considera necesaria la profilaxis a los contactos de bajo riesgo como:
• Contacto casual sin exposición directa a secreciones orales del caso índice (contacto laboral, escolar…).
• Contactos indirectos: son las personas que han estado en contacto con otro contacto de riesgo (incluso de alto riesgo) pero no con el caso índice.
• Profesionales sanitarios que han atendido al caso índice pero sin contacto directo con sus secreciones orales.
En situaciones de brote, puede ser recomendable la quimioprofilaxis incluso en los pacientes de bajo riesgo y, para ello, deben seguirse las indicaciones de las autoridades sanitarias competentes.
Los antimicrobianos adecuados para la quimioprofilaxis son: rifampicina, ceftriaxona, ciprofloxacino y azitromicina, todos con una eficacia similar, que oscila entre el 90-95%. El fármaco de elección, tanto en niños como en adultos, es la rifampicina. La dosis en lactantes mayores de 1 mes, niños y adultos, es de 10 mg/kg/dosis (máximo 600 mg), vía oral, cada 12 horas, durante 2 días. En menores de 1 mes de edad, la dosis se reduce a 5 mg/kg/dosis, también cada 12 horas y durante 2 días. La rifampicina interfiere con algunos antiepilépticos, anticoagulantes y con los anticonceptivos orales, y está contraindicada en embarazadas. La ceftriaxona se administra por vía intramuscular en dosis única de 125 mg en menores de 15 años y de 250 mg en mayores de esta edad y en adultos. Es el fármaco de elección en embarazadas y en todos los casos cuando no es factible la vía oral. El ciprofloxacino se administra en dosis única de 500 mg por vía oral, sólo indicado para mayores de 18 años. La azitromicina no se recomienda de forma rutinaria. En caso de que se utilice, la dosis de 10 mg/kg (dosis máxima 500 mg) en dosis única por vía oral, ha mostrado una eficacia similar a la rifampicina en la erradicación de la Neisseria meningitidis de la nasofaringe(1).
Infección por Haemophilus influenzae tipo b
La enfermedad invasiva por H. influenzae tipo b es actualmente excepcional en nuestra población gracias a la vacunación sistemática.
La vacunación, además de conseguir el descenso de la carga de la enfermedad invasiva, ha disminuido la colonización nasofaríngea por H. influenzaetipo b (Hib), reduciendo la capacidad de transmisión a personas no vacunadas, dando lugar a una inmunidad de grupo. El riesgo de enfermedad se circunscribe a niños menores de 4 años no vacunados, especialmente si son contactos domiciliarios y, en menor grado, a contactos de guardería.
La profilaxis se recomienda en todos los contactos domiciliarios, independientemente de la edad, si al menos uno de los contactos es menor de 4 años y no está correctamente inmunizado, o es menor de 12 meses y no ha completado la serie primaria de vacunación. También, en caso de que uno de los contactos sea un niño inmunodeprimido, independientemente de su estado de vacunación. La profilaxis de contactos en una guardería o parvulario se recomienda si se han producido 2 o más casos de enfermedad invasiva por Hib en un periodo de 60 días, pero sólo cuando asisten a ella niños menores de 4 años parcialmente inmunizados o no inmunizados. En tal situación, se recomienda quimioprofilaxis a todos los alumnos y cuidadores independientemente de su edad y estado vacunal. En todos los casos, debe procederse, además, a completar la vacunación frente a Hib con vacuna conjugada en los incompletamente vacunados o iniciarla en los no vacunados(1).
La quimioprofilaxis se realiza con rifampicina, a dosis de 20 mg/kg/dosis (máx. 600 mg), vía oral, cada 24 horas, durante 4 días. En menores de 1 mes de vida, la dosis se reduce a 10 mg/kg/dosis, cada 24 horas, durante 4 días. No se recomienda la profilaxis en las mujeres embarazadas.
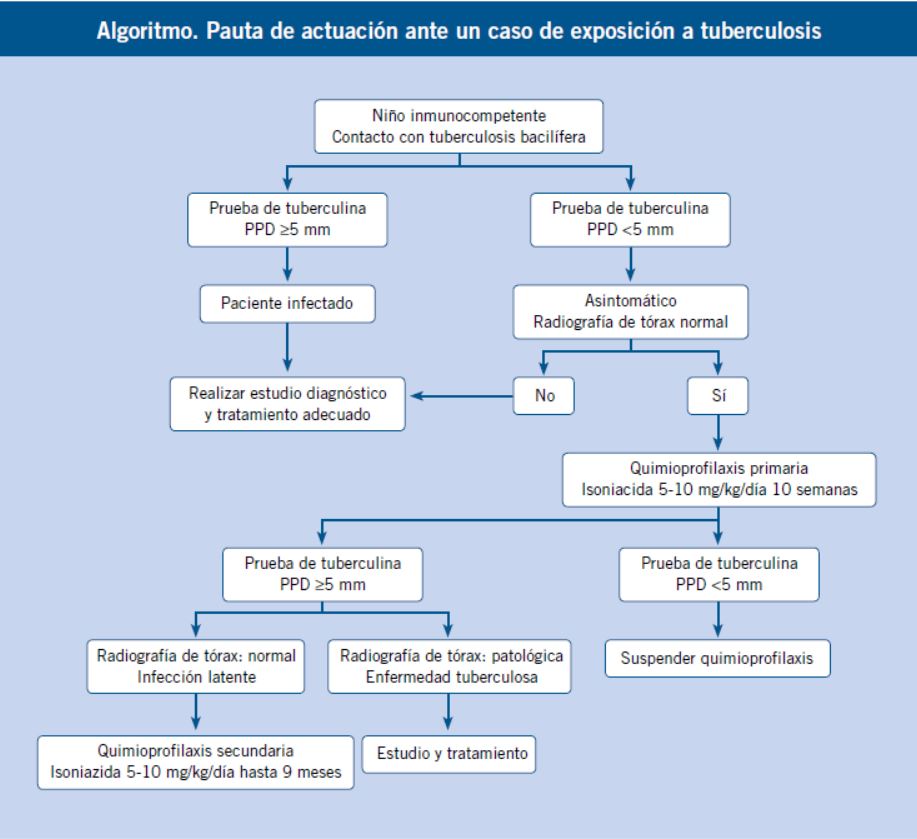
Tuberculosis
El objetivo de la quimioprofilaxis postexposición es evitar el desarrollo de formas graves de la enfermedad en los contactos.
La detección de un caso de tuberculosis bacilífera, habitualmente un adulto enfermo, implica siempre la evaluación de todas las personas que, por ser contactos de riesgo, puedan infectarse, tengan ya una infección tuberculosa latente o en algunos casos estén afectos de una enfermedad tuberculosa. La estrecha vigilancia del núcleo familiar, del entorno laboral y cuando proceda del entorno escolar, con un riguroso estudio de los contactos de riesgo y la instauración adecuada de pautas de quimioprofilaxis, permite evitar formas graves de tuberculosis, especialmente en los niños.
Se debe considerar a un niño como expuesto a tuberculosis cuando éste ha tenido un contacto reciente y sustancial (>4 horas diarias) con un adulto con sospecha fundada o confirmada de tuberculosis y, una vez evaluado, no presenta ni signos ni síntomas de la enfermedad, la radiografía de tórax es normal y la prueba de tuberculina es negativa. En esta situación está indicada la quimioprofilaxis primaria, especialmente en menores de 4 años e inmunodeprimidos, siendo el fármaco de elección la isoniazida a dosis de 5-10 mg/kg/día (dosis máxima 300 mg/día), administrada en una dosis diaria. En todos los contactos considerados como expuestos a tuberculosis, hayan iniciado o no la quimioprofilaxis primaria, debe repetirse una prueba de tuberculina a las 10-12 semanas de la exposición al caso fuente. Si persiste el resultado negativo el paciente puede considerarse como no infectado y suspender la quimioprofilaxis. Si la tuberculina resultara positiva (induración ≥5 mm), el paciente sigue asintomático y con radiografía de tórax normal se considerará afecto de infección tuberculosa latente y deberá continuar la terapia con isoniazida hasta completar 9 meses(1,18).
Se define como infección tuberculosa latente a los casos con prueba de tuberculina positiva, sin signos ni síntomas de enfermedad y con radiografía de tórax normal. En estos casos debe instaurarse una quimioprofilaxis secundaria, cuyo objetivo es evitar el desarrollo de la enfermedad en un paciente ya infectado. Aunque en adultos la eficacia de esta estrategia oscila entre el 60-80% por al menos 20 años, en niños se aproxima al 100%, especialmente cuando se realiza como continuación de la quimioprofilaxis primaria en pacientes que finalmente resultaron infectados. Todos los lactantes, niños y adolescentes con infección tuberculosa latente deben recibir isoniazida, a igual dosis que en la quimioprofilaxis primaria, durante un periodo de 9 meses. En los casos de tuberculosis resistente a la isoniazida, sospechada o confirmada en el caso fuente o por razones epidemiológicas (áreas geográficas de alta prevalencia de resistencia), o en caso de contraindicación, la terapia puede realizarse con rifampicina (10 mg/kg/día, dosis máxima 600 mg) durante 6 meses. Si en el caso fuente, la infección es debida a un bacilo multirresistente, la terapia deberá individualizarse con la utilización combinada de varios fármacos antituberculosos(1,18).
Inmunprofilaxis postexposición
La inmunoprofilaxis mediante inmunoglobulinas y vacunas permite reducir el riesgo de infección postexposición en determinadas infecciones víricas.
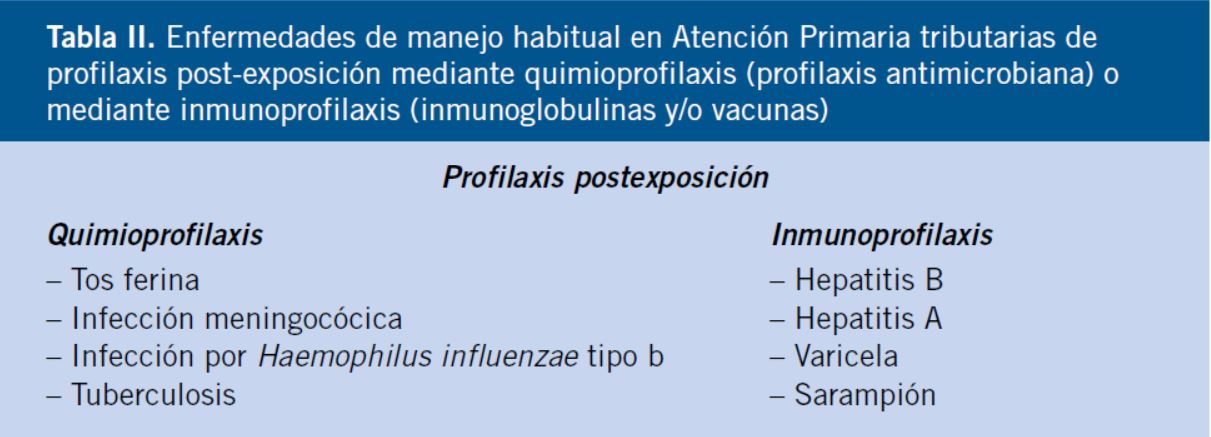
En este apartado se incluyen, de forma breve, enfermedades infecciosas que no son tributarias de profilaxis con antimicrobianos, pero en las que existen indicaciones precisas de profilaxis postexposición mediante la utilización de inmunoglobulinas o vacunas (Tabla II).
Hepatitis B
Los tipos de exposición con riesgo de contagio de hepatitis B en personas susceptibles en contacto con una persona HBsAg positivo, o con estado serológico desconocido y, por tanto, tributarias de profilaxis, son: la exposición perinatal por contagio a través del canal del parto, la exposición por contacto sexual, la percutánea por pinchazo accidental, la exposición cutáneo-mucosa por salpicaduras o contacto con sangre o secreciones, y el contacto familiar no sexual.
La profilaxis para el riesgo perinatal consiste en la administración en los recién nacidos de madre HBsAg positivo o desconocido, de una dosis de 0,5 ml (vía intramuscular) de inmunoglobulina hiperinmune frente a hepatitis B (IGHB), coadministrada con una dosis de vacuna antihepatitis B monovalente, en zonas anatómicas distintas y en las 12 primeras horas de vida. Posteriormente, debe completarse la vacunación con dos dosis adicionales a los 1-2 meses y 6 meses de edad. En los recién nacidos de peso inferior a 2.000 g, son necesarias 3 dosis adicionales, administradas a la edad de 1, 2 y 6 meses. La efectividad de la profilaxis es cercana al 95%(19).
Cuando se produce una exposición de riesgo a una persona HBsAg positivo o desconocido, la actitud a seguir dependerá del estado vacunal de la persona expuesta y del nivel de seroprotección adquirido (cuando es conocido) que determinarán su susceptibilidad a la infección. En la tabla VI, se describe el protocolo de actuación ante una exposición de riesgo a hepatitis B.

Las personas vacunadas en las que se haya comprobado la respuesta seroprotectora y presenten una concentración de anticuerpos frente al antígeno de superficie de hepatitis B (Ac-HBs) igual o mayor a 10 UI/ml tras la vacunación, deben considerarse seroprotegidas, sin necesidad de nuevas comprobaciones y a pesar de que, en un control posterior, la concentración de Ac-HBs fuera inferior a este nivel. Pero, si una persona vacunada, de la que se desconoce el estado de seroprotección, sufre una exposición de riesgo a sangre o secreciones de un individuo HBsAg + o desconocido, debe determinarse el nivel de Ac-HBs. Si el resultado es <10 UI/ml, se considera no seroprotegido y debe recibir 1 dosis de IGHB (0,06 ml/kg, dosis mínima 0,5 ml, dosis máxima 5 ml) por vía intramuscular y, simultáneamente, una dosis de vacuna frente a hepatitis B. Debe controlarse la tasa de Ac-HBs a los 1-3 meses y proseguir la vacunación con 2 dosis más si la concentración es menor a 10 UI/ml(19). Debe considerarse también en estos casos realizar una serología basal frente a VIH y hepatitis C, siendo necesario un nuevo control a los 3 y 6 meses tras la exposición para poder descartar con certeza un posible contagio(1).
En cuanto al riesgo de contagio por contacto familiar no sexual, debe recomendarse la vacunación de todos los contactos familiares de un portador crónico del virus de la hepatitis B. Será necesaria, además, la administración de inmunoglobulina hiperinmune si el familiar padece una hepatitis B aguda y los contactos son menores de 12 meses, o a cualquier edad si han compartido objetos que pudieran estar contaminados con sangre, como cepillo de dientes, etc.(19).
Hepatitis A
Actualmente, en España, las personas no vacunadas frente a hepatitis A y que tampoco la han padecido, deben considerarse susceptibles a esta infección independientemente de su edad. En nuestro país, la hepatitis A presenta una endemicidad baja o muy baja, lo que ocasiona que ya no sea una enfermedad de mayor incidencia en la infancia, donde generalmente es anictérica o asintomática, desplazándose a edades superiores y adultos con mayor expresividad clínica y gravedad. Esta situación también justifica el mayor riesgo de aparición de brotes en la comunidad cuando se produce un caso, debido a la facilidad de transmisión fecal-oral que presenta este virus. Ante un caso de hepatitis A, debe realizarse profilaxis post-exposición a todos los contactos susceptibles considerados de riesgo(1):
• Entorno doméstico: familiares y cuidadores convivientes, y contactos sexuales.
• Guarderías: profilaxis a todos los asistentes al centro, niños y cuidadores, siempre que se produzca:
– Uno o más casos de hepatitis A en el personal o en los niños de la guardería.
– Dos o más casos en contactos domiciliarios de niños que acuden a una misma guardería.
Si en la guardería no hay niños incontinentes, puede restringirse la profilaxis sólo a los que asisten a la misma clase del caso índice.
• Exposición a una fuente común (manipulador de alimentos):
– Se realizará a los que hayan consumido alimentos manipulados por el caso índice, cuando se haya corroborado el riesgo de transmisión en un entorno cerrado: comedores escolares, campamentos, casas de colonias, hospitales…
– A todos los manipuladores de alimentos que trabajan con el caso índice.
No se recomienda la profilaxis en los contactos escolares o laborales de un solo caso, aunque puede ser recomendable en los compañeros con contacto más estrecho o personal. El adecuado aislamiento y la correcta higiene de manos son las medidas más importantes en estas situaciones.
La inmunoglobulina polivalente (0,02 ml/kg, vía intramuscular), administrada en los primeros 14 días tras la exposición, es eficaz para la profilaxis post-exposición a todas las edades(1,20). No obstante, es más recomendable realizar la profilaxis con la administración de una dosis de vacuna frente a hepatitis A en todas las personas de edad comprendida entre 12 meses y 40 años, y reservar la inmunoglobulina polivalente para los menores de 12 meses y mayores de 40 años. Si el paciente es inmunodeprimido o sufre una hepatopatía crónica, se recomienda administrar simultáneamente la vacuna y la inmunoglobulina polivalente en lugares anatómicos distintos. La utilización de la vacuna, además de ofrecer una eficacia post-exposición superponible a la inmunoglobulina en el rango de edad comentado, confiere protección a largo plazo y, por ello, es preferible. Precisamente para garantizar esta protección a largo plazo, los vacunados deberán recibir una segunda dosis de vacuna pasados 6-12 meses(19).
Varicela
La vacunación universal frente a varicela a partir de los 12 meses de edad es la estrategia preventiva preferible para hacer frente a esta enfermedad, con un impacto beneficioso y claramente significativo en la comunidad, con reducción del número de casos, complicaciones, hospitalizaciones y mortalidad debidas a esta infección. En los niños mayores de 9 meses, adolescentes y adultos inmunocompetentes, no vacunados y susceptibles por no haber sufrido la enfermedad, la vacuna puede indicarse también como profilaxis post-exposición. La vacuna es eficaz si se administra en los 5 primeros días post-exposición, idealmente en los primeros 3 días, evitando el desarrollo de la enfermedad en el 70-80% de los casos(19).
Existen además situaciones de especial riesgo de varicela complicada o grave, en las que está indicada de forma específica la profilaxis postexposición a un caso de varicela, y en las que no es posible la administración de la vacuna. En estas situaciones, debe administrarse inmunoglobulina hiperinmune antivaricela (endovenosa o intramuscular) pero, al no estar disponible en nuestro país, puede realizarse con inmunoglobulina polivalente endovenosa (200-400 mg/kg) o intramuscular (0,6-1,2 ml/kg, dosis máxima: 20 ml)(20). Es efectiva si se administra, lo antes posible, en las primeras 96 horas tras la exposición, aunque se considera útil para evitar o atenuar la enfermedad si ha sido administrada hasta los 10 días posteriores al contacto. Son indicaciones de inmunoglobulina polivalente, como profilaxis postexposición a varicela(1):
• Personas con inmunodeficiencias o inmunodepresión. Los enfermos con VIH pueden recibir la vacuna si en el recuento de linfocitos el porcentaje de CD4 es ≥25%.
• Recién nacidos de madre que ha presentado la varicela 5 días antes o 2 días después del parto.
• Prematuros hospitalizados de edad gestacional menor de 28 semanas o peso inferior
a 1.000 g.
• Prematuros hospitalizados de madre susceptible.
• Embarazadas susceptibles.
También puede considerarse la utilización de aciclovir (20 mg/kg/dosis, 4 veces/día, 7 días) iniciando la administración a partir del 7º día postexposición como alternativa a la inmunoglobulina (sin disponibilidad) en sujetos de alto riesgo como inmunodeprimidos o enfermos con patologías cutáneas graves que no han podido ser vacunados. Aunque puede prevenir o atenuar la enfermedad, el aciclovir no evita la infección, y no se recomienda en inmunocompetentes(1).
Sarampión
La profilaxis post-exposición frente al sarampión en individuos susceptibles puede realizarse mediante vacunación, si no existe contraindicación para la misma, o con inmunoglobulinas, indicadas en personas que, por su edad, (menores de 6 meses) o por su estado (embarazo, inmunodepresión, etc.) no pueden vacunarse. La vacuna frente al sarampión, administrada en las primeras 72 horas de la exposición, proporciona una protección en la mayoría de los casos y es la estrategia de elección en el control de brotes en el entorno escolar. La inmunoglobulina puede prevenir o modificar el sarampión cuando se administra hasta 6 días después de la exposición. En la tabla VII, se detallan las indicaciones y la posología de ambas estrategias preventivas(1,19,20).

A los niños menores de 1 año que reciban una dosis de vacuna como profilaxis postexposición, se les deberán administrar dos dosis adicionales de vacuna a partir de la edad de 12 meses para considerarlos adecuadamente inmunizados. En los mayores de 1 año, ya vacunados con una sola dosis, es recomendable administrales la segunda dosis si se exponen a sarampión, no estando indicada la inmunoglobulina en esta situación. En cambio, en los pacientes inmunodeprimidos ya vacunados previamente con una o dos dosis, deberían recibir una dosis de inmunoglobulina polivalente en caso de exposición con riesgo de contagio de sarampión.
Bibliografía
Los asteriscos reflejan el interés del artículo a juicio del autor.
1.*** American Academy of Pediatrics. Red Book: 2012 Report of the Committee on Infectious Diseases. En: Pickering LK, ed. 29th ed. Elk Grove Village, IL: American Academy of Pediatrics; 2012.
2. Van Esso D, Rodrigo C. Profilaxis antibiótica y postexposición. Pediatr Integral. 2010; XIV: 66-74.
3.*** Bradley JS. Chemoprophylaxis. En: Long SS, Pickering LK, Prober CG, eds. Principles and practice of pediatric infectious diseases. 4th ed. Philadelphia: Elsevier Inc; 2012. p. 68-76.
4.*** Overturf GD. Antimicrobial prophylaxis. En: Feigin RD, Cherry J, Demmler GJ, Kaplan SL, eds. Feigin and Cherry’s textbook of pediatric infectious diseases. 6th ed. Philadelphia: Saunders Elsevier; 2009. p. 3220-38.
5. Harper MB. Infection following bites. En: Long SS, Pickering LK, Prober CG, eds. Principles and practice of pediatric infectious diseases. 4th ed. Philadelphia: Elsevier Inc; 2012. p. 521-6.
6. Medeiros I, Saconato H. Antibiotic prophylaxis for mammalian bites. Cochrane Database Syst Rev. 2001(2): CD001738.
7. Klein JO, Bluestone CD. Otitis Media. En: Feigin RD, Cherry J, Demmler GJ, Kaplan SL, eds. Feigin and Cherry’s textbook of pediatric infectious diseases. 6th ed. Philadelphia: Saunders Elsevier; 2009. p. 216-37.
8. Leach AJ, Morris PS. Antibiotics for the prevention of acute and chronic suppurative otitis media in children. Cochrane Database Syst Rev. 2006; 4: CD004401.
9. Craig JC, Williams GJ. Denominators do matter: it’s a myth-urinary tract infection does not cause chronic kidney disease. Pediatrics. 2011; 128: 984-5.
10. Salo J, Ikäheimo R, Tapiainem T, Uhari M. Childhood urinary tract infection as a cause of chronic kidney disease. Pediatrics. 2011; 128: 840-7.
11. Roberts KB, Subcommittee on urinary tract infection, Steering committee on quality improvement and management. Urinary tract infection: clinical practice guideline for the diagnosis and management of the initial UTI in febrile infants and children 2 to 24 months. Pediatrics. 2011; 128: 595-610.
12.** Grupo de trabajo de la Guía de Práctica Clínica sobre Infección del Tracto Urinario en la Población Pediátrica. Guía de práctica clínica sobre infección del tracto urinario en la población pediátrica. Plan de calidad para el Sistema Nacional de Salud del Ministerio de Sanidad, Política Social e Igualdad. Instituto Aragonés de Ciencias de la Salud; Guías de Práctica Clínica en el SNS: I+CS nº 2009/01; 2011.
13. Wilson W, Taubert KA, Gewitz M, Lockhart PB, Baddour LM, Levison M, et al. Prevention of infective endocarditis: guidelines from the American Heart Association: a guideline from the American Heart Association Rheumatic Fever, Endocarditis, and Kawasaki Disease Committee, Council on Cardiovascular Disease in the Young, and the Council on Clinical Cardiology, Council on Cardiovascular Surgery and Anesthesia, and the Quality of Care and Outcomes Research Interdisciplinary Working Group. Circulation. 2007; 116: 1736-54.
14. De la Flor JE. Patología otorrinlaringológica 1: Resfriado común. Faringitis. Laringitis. Gripe. En: Bras J, de la Flor JE, Martín I, Torregrosa MJ, eds. Pediatría en atención primaria. 3ª edición. Barcelona: Elsevier España, SL; 2013. p. 514-30.
15. Gerber MA, Baltimore RS, Eaton CB, Gewitz M, Rowley AH, Shulman ST, et al. Prevention of rheumatic fever and diagnosis and treatment of acute Streptococcal pharyngitis: a scientific statement from the American Heart Association Rheumatic Fever, Endocarditis, and Kawasaki Disease Committee of the Council on Cardiovascular Disease in the Young, the Interdisciplinary Council on Functional Genomics and Translational Biology, and the Interdisciplinary Council on Quality of Care and Outcomes Research: endorsed by the American Academy of Pediatrics. Circulation. 2009; 119: 1541-51.
16. Price VE, Blanchette VS, Ford-Jones EL. The prevention and management of infections in children with asplenia or hyposplenia. Infect Dis Clin N Am. 2007; 21: 697-710.
17. Arrazola P, de Juanes JR. Quimioprofilaxis y otras medidas de control de la transmisión de la infección meningocócica. En: Moraga Llop FA, ed. La enfermedad meningocócica: pasado, presente y futuro. Sant Hilari Sacalm (Girona): Grafiques Montseny; 2013. p. 367-81.
18.** Sociedad Española de Infectología Pediátrica. Documento de consenso sobre el tratamiento de la exposición a tuberculosis y de la infección tuberculosa latente en niños. An Pediatr (Barc). 2006; 64: 59-65.
19. Moraga FA, Campins M. Vacunación profiláctica post-exposición. En: Álvarez F, Arístegui J, Moreno D, eds. Vacunas en Pediatria. Manual de la AEP 2012. Madrid: Exlibris Ediciones SL; 2012. p. 147-57.
20. Moreno D, Moraga F. Inmunoglobulinas: indicaciones, dosificación y seguridad. En: Álvarez F, Arístegui J, Moreno D, eds. Vacunas en Pediatria. Manual de la AEP 2012. Madrid: Exlibris Ediciones SL; 2012. p. 547-61.
Bibliografía recomendada
– American Academy of Pediatrics. Red Book: 2012 Report of the Committee on Infectious Diseases. Pickering LK, ed. 29th ed. Elk Grove Village, IL: American Academy of Pediatrics; 2012.
Libro de consulta imprescindible. Revisión actualizada por los expertos de la American Academy of Pediatrics de gran utilidad para el manejo práctico de las enfermedades infecciosas en la edad pediátrica.
– Bradley JS. Chemoprophylaxis. En: Long SS, Pickering LK, Prober CG, eds. Principles and practice of pediatric infectious diseases. 4th ed. Philadelphia: Elsevier Inc; 2012. p. 68-76.
Tratado recientemente actualizado sobre enfermedades infecciosas en pediatría, cuyo capítulo sobre quimioprofilaxis ofrece una visión amplia y clara sobre los beneficios y las indicaciones de la misma. Lectura muy recomendable.
– Overturf GD. Antimicrobial prophylaxis. En: Feigin RD, Cherry J, Demmler GJ, Kaplan SL, eds. Feigin and Cherry’s textbook of pediatric infectious diseases. 6th ed. Philadelphia: Saunders Elsevier; 2009. p. 3220-38.
Tratado clásico sobre enfermedades infecciosas en pediatría, muy recomendable para profundizar en el conocimiento de la patología infecciosa, las estrategias terapéuticas y preventivas. Capítulo de profilaxis antimicrobiana excelente.
– Grupo de trabajo de la Guía de Práctica Clínica sobre Infección del Tracto Urinario en la Población Pediátrica. Guía de práctica clínica sobre infección del tracto urinario en la población pediátrica. Plan de calidad para el Sistema Nacional de Salud del Ministerio de Sanidad, Política Social e Igualdad. Instituto Aragonés de Ciencias de la Salud; Guías de Práctica Clínica en el SNS: I+CS nº 2009/01; 2011.
Guía de Práctica Clínica del SNS recientemente actualizada con las nuevas recomendaciones para el manejo de la infección urinaria en pediatría. Disponible en http://www.guiasalud.es/egpc/ITU/completa/index.html
– Sociedad Española de Infectología Pediátrica. Documento de consenso sobre el tratamiento de la exposición a tuberculosis y de la infección tuberculosa latente en niños. An Pediatr (Barc). 2006; 64: 59-65.
Actualización sobre el manejo de los contactos expuestos a tuberculosis y las pautas de tratamiento y profilaxis recomendadas en nuestro medio. Lectura recomendable.
| Caso clínico |
|
Juan es un varón de 8 años afecto de estenosis aórtica por malformación valvular congénita, con gradiente de 25 mmHg, sin repercusión hemodinámica, sin necesidad de tratamiento farmacológico y sin indicación quirúrgica actualmente. Sigue control semestral en consultas de cardiología. Está programado para practicar endodoncia y obturación de caries profunda en molar definitivo (pieza dental nº 46). Los padres nos consultan a petición del odontopediatra para valorar la necesidad de prevención antibiótica dada su cardiopatía.
|