|
| Temas de FC |
A. Méndez Echevarría
Servicio de Pediatría, Enfermedades Infecciosas y Tropicales. Hospital Universitario La Paz. Madrid
| Resumen
Las infecciones recurrentes son causa frecuente de consulta en Pediatría, pero la mayor parte de los niños que las presentan son inmunocompetentes. Además, patologías crónicas, como: el asma, el reflujo vesicoureteral, esofágico o las enfermedades neurológicas favorecen la aparición de infecciones recurrentes. Otras enfermedades precisan tratamientos inmunosupresores que favorecen la infección. Por otra parte, la presencia de un defecto inmunológico congénito, como causa de infecciones recurrentes, es un fenómeno muy infrecuente, pero su diagnóstico precoz resulta fundamental por condicionar el pronóstico de la enfermedad y evitar complicaciones. |
| Abstract
Recurrent infections are one of the most common cause of consultation of children in hospitals and health care centers. However, most of these infections occur in immunocompent children. In addition, some medical conditions such as asthma, vesicoureteral or esophageal reflux, or neurological diseases predispose to recurrent infections. Other chronic diseases require immunosuppressive treatments that also favor infections. The presence of a primary immunodeficiency causing recurrent infections is very infrequent, but a prompt diagnosis of the immunological defect could improve the prognosis of the disease, avoiding complications. |
Palabras clave: Síndromes de deficiencia inmunológica; Niño; Infección; Recurrencia
Key words: Immunologic Deficiency Syndromes; Child; Infection; Recurrence
Pediatr Integral 2018; XXII (5): 219 – 228
El niño con infecciones de repetición
Introducción
Las infecciones recurrentes son uno de los motivos más frecuentes de consulta en niños sanos. Por ello, la sospecha diagnóstica de inmunodeficiencia primaria es complicada y difícil de establecer, especialmente en niños menores de 2 años con infecciones recurrentes que acuden a guardería. Sin embargo, resulta fundamental su diagnóstico precoz para evitar su morbimortalidad.
El término “infecciones frecuentes” es impreciso. Los niños sanos, sin patología de base, durante su primera infancia, tienen una media de 6-8 infecciones de vías respiratorias altas al año(1-3). Además, si el niño asiste a guardería, tiene hermanos pequeños o presenta algún factor predisponente, como: asma, reflujo esofágico o vesicoureteral, puede llegar hasta 10-12 infecciones anuales(1,2,4).
La mayoría de estas infecciones en niños inmunocompetentes suelen ser virales, banales y transitorias, no aislándose ninguna bacteria, y curándose sin tratamiento antibiótico(2), estando el niño asintomático entre cada una de ellas, sin afectarse el desarrollo póndero-estatural(1,5). Sin embargo, la presencia de determinados factores de riesgo, la existencia de antecedentes familiares relevantes y/o consanguinidad, la afectación de múltiples órganos, la repercusión en la curva ponderal o la ausencia de mejoría clara entre episodios, deben hacernos sospechar la presencia de un defecto inmunológico de base predisponente(2,4-7).
En niños procedentes de países de alta endemia, siempre debemos descartar la presencia de infección por el virus de la inmunodeficiencia humana (VIH) ante infecciones recurrentes, especialmente si se aíslan microrganismos oportunistas(6,8,9). Aunque muy infrecuente, en niños nacidos en nuestro país, debemos descartar infección VIH si el embarazo no fue controlado o en adolescentes con hábitos sexuales de riesgo. Una vez descartada la infección VIH o la presencia de enfermedades crónicas predisponentes, en niños con clínica relevante, deberemos descartar la presencia de inmunodeficiencia primaria (IDP).
Sin embargo, la orientación diagnóstica de niños con infecciones recurrentes es difícil, debido a la diversidad de infecciones y manifestaciones que pueden presentar niños con IDPs, por su baja prevalencia y la gran heterogeneidad de estas enfermedades.
A lo largo del capítulo, se expondrán los principales signos de alarma que deben hacernos sospechar alguna patología de base o factor predisponente de infección en niños con infecciones recurrentes, así como el manejo básico de estos pacientes.
Epidemiología
Las infecciones recurrentes son uno de los principales motivos de consulta en Pediatría. Aunque las IDPs son enfermedades raras, su incidencia global no es despreciable. Las inmunodeficiencias secundarias en Pediatría son mucho menos relevantes. En las últimas décadas, ha aumentado la supervivencia de niños con patologías crónicas, muchos de los cuales asocian mayor riesgo de infecciones.
Como se ha comentado, las infecciones recurrentes son uno de los problemas de consulta más frecuente en Pediatría, en especial, las infecciones respiratorias, estimándose que un 23% de los niños presenta infecciones respiratorias recurrentes(10).
Sin embargo, no existen datos fiables de la incidencia real de IDPs en niños españoles. Obtener datos reales sobre la incidencia de inmunodeficiencias es difícil, dado que estas enfermedades permanecen muchas veces infra diagnosticadas(3).
A pesar de que cada una de las IDPs constituyen enfermedades raras, globalmente constituyen una patología cada vez más frecuente, con prevalencias de hasta 1/1.200 excluyendo el déficit de IgA(1,3), siendo, por tanto, al menos, tan frecuente como la fibrosis quística o la diabetes tipo 1.
La International Union of Immunological Societies se reúne periódicamente para actualizar su clasificación, incluyendo en cada nueva actualización, nuevas entidades descritas. En el año 2000, conocíamos aproximadamente unos 100 defectos que se asociaban a inmunodeficiencia, pero en la última clasificación ya son 354 las entidades descritas, lo que demuestra que son enfermedades poco conocidas y mucho más frecuentes de lo que se estimaba(11).
Las IDPs predominantes son los defectos de anticuerpos, siendo el déficit de Ig A la más común (1:500), aunque esta entidad no asocia infecciones recurrentes significativas. Algunas IDPs se heredan ligadas al X (enfermedad granulomatosa crónica, enfermedad de Bruton, síndrome linfoproliferativo ligado al X o imunodeficiencia combinada grave por déficit de cadena gamma), por lo que su incidencia es mayor en varones(1-4).
Igualmente, su incidencia aumenta en niños hijos de padres consanguíneos y, por ello, ante la presencia de antecedentes familiares y/o consanguinidad, se debe siempre descartar estas enfermedades en niños que consultan por infecciones recurrentes(7-12).
Por último, en los últimos años, ha aumentado la prevalencia de manera significativa de niños con patologías crónicas, así como la supervivencia de niños grandes prematuros(13-14), siendo éstas, poblaciones de riesgo de padecer infecciones recurrentes. Muchas de estas enfermedades favorecen la infección por predisposición anatómica, otras son causa de inmunodeficiencia secundaria y/o precisan tratamientos inmunosupresores. Las enfermedades que producen inmunodeficiencia secundaria deben ser valoradas y descartadas antes de establecer la sospecha de IDP(4). Son numerosísimas las enfermedades crónicas que asocian riesgo de infección y por ello no serán objeto de tratamiento detallado en este capítulo.
Orientación diagnóstica de los niños con infecciones recurrentes
La orientación diagnóstica de niños con infecciones recurrentes se debe basar siempre en una historia clínica y exploración física exhaustiva. Se sospecha un defecto inmunológico en: niños con infecciones en diversos órganos, retraso de medro, ausencia de respuesta al tratamiento, consanguinidad o infecciones por organismos oportunistas. Una cifra persistente de linfocitos < de 3.000 μL en sangre periférica puede ser la primera manifestación de una inmunodeficiencia combinada en lactantes. Algunas inmunodeficiencias pueden debutar con alteraciones autoinmunes o inflamatorias. No debemos olvidar en el estudio, el despistaje de infección por VIH o la presencia de inmunodeficiencias secundarias.
En niños con infecciones recurrentes, resulta fundamental la historia clínica y la exploración física para poder realizar la orientación diagnóstica. Son importantes los siguientes datos(2-4):
• Control del embarazo y despistaje VIH.
• Sexo del paciente y edad de presentación de los síntomas.
• Retraso de caída del cordón y onfalitis.
• Infecciones previas (número, localización, gravedad, microorganismos implicados, tratamiento realizado) y complicaciones.
• Afectación del estado general, nutricional y del desarrollo.
• Vacunaciones recibidas y complicaciones (especialmente, si administración de vacunas de virus vivos, como rotavirus y BCG).
• Antecedente de transfusiones.
• Patología de base y uso de medicaciones que puedan condicionar citopenias y/o inmunodeficiencia secundaria (cotrimoxazol, anticomiciales, corticoides, etc.).
• Antecedentes familiares (consanguinidad, lactantes fallecidos por infección, historia familiar de autoinmunidad, cáncer o IDPs).
• Patología autoinmune e inflamatoria asociada: artritis, enfermedad inflamatoria intestinal, citopenias autoinmunes o hipertiroidismo autoinmune. La incidencia de patología autoinmune e inflamatoria asociada es muchísimo mayor en niños con IDP en comparación con la población general. Por ejemplo, la incidencia de anemia hemolítica es 830 mayor en niños con IDP que en población infantil(15).
Aunque las infecciones recurrentes, en los primeros años de vida, son un motivo de consulta muy frecuente, en los pacientes con IDP es más probable que aparezcan infecciones graves, persistentes, recurrentes o causadas por microorganismos poco habituales(1-4). En niños que no tienen patologías crónicas ni reciben tratamientos inmunosupresores, la afectación de múltiples órganos y sistemas debe hacernos sospechar la presencia de una IDP.
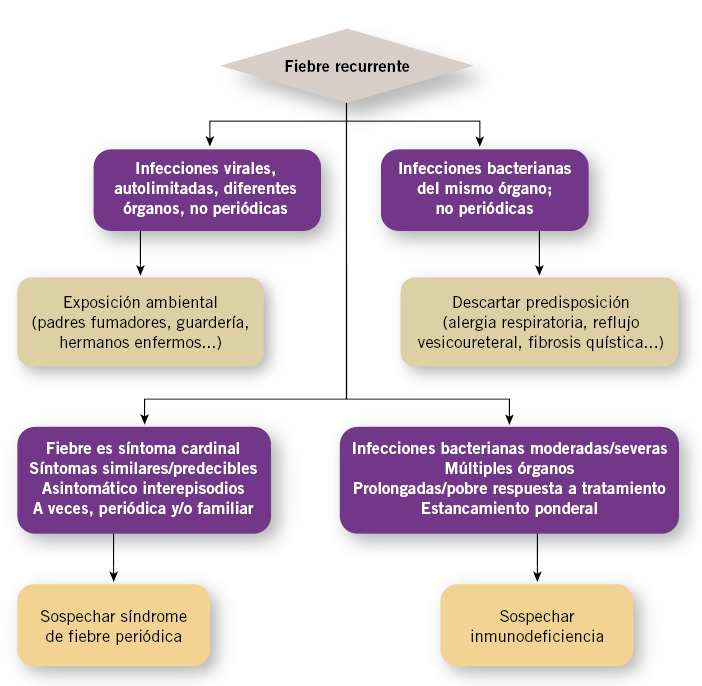
Sin embargo, cuando las infecciones recurren siempre en el mismo órgano (p. ej.: infecciones urinarias recurrentes, otitis o amigdalitis), quizá pueda existir un defecto anatómico o funcional que las favorezca, como: el reflujo vesicoureteral, la hipertrofia adenoidea o la colonización persistente faríngea por S. pyogenes(8,16) (Fig. 1).
Figura 1. Diagnóstico diferencial en niños con fiebre/infecciones recurrentes (modificado de Long SS. Pediatr Clin North Am. 2005; 52: 811-35)(16).
Las neumonías recurrentes merecen una mención especial, dado que las infecciones respiratorias de repetición pueden ser muy frecuentes en la población general(10), aunque igualmente el pulmón es el órgano que con más frecuencia se ve afectado en las IDPs4,5,8). Cuando las neumonías recurren siempre en el mismo lóbulo, debemos descartar defectos anatómicos o aspiración de cuerpo extraño. Sin embargo, infecciones respiratorias recurrentes de mala evolución iniciadas en edades tempranas, deben hacernos descartar IDP(6,7), al igual que neumonías bacterianas que afecten a diversos lóbulos en cada nueva infección5). En determinadas enfermedades crónicas, es mayor la frecuencia de infecciones, especialmente respiratorias: fibrosis quística, asma, reflujo gastroesofágico, cardiopatías, hipertrofia adenoidea, malformaciones congénitas, encefalopatías, etc.(4,8).
Existen, además, enfermedades que pueden causar pérdida de inmunoglobulinas (enteropatía pierde-proteínas y síndrome nefrótico), cursando con infecciones recurrentes e hipogammaglobulinemia, y confundirse con una IDP, por lo que deben descartarse las inmunodeficiencias secundarias antes de hacer el diagnóstico de IDP(4,8).
En caso de presentarse ≥2 signos de alarma, podría estar indicado un estudio de IDP, aunque estos signos clásicos son poco sensibles y específicos, especialmente con la descripción de nuevas entidades clínicas, muchas de las cuales no asocian tantas infecciones, pero presentan otras manifestaciones autoinmunes e inflamatorias(2,4,8) (Tabla I).
Dentro de las IDPs, el diagnóstico de inmunodeficiencia combinada grave (IDCG) constituye una urgencia pediátrica(4,6,7), ya que su diagnóstico tardío aumenta su morbimortalidad. Por ello, debemos derivar pronto a un centro de referencia a cualquier lactante que presente: infecciones recurrentes, graves, diarrea crónica, dermatitis moderada-grave y/o candidiasis mucocutánea, especialmente si presenta: linfocitos totales menores de 3.000, ausencia de sombra tímica en la radiografía de tórax (Fig. 2), de tejido linfático con ausencia de ganglios palpables o de amígdalas en pilares faríngeos (Fig. 3) y/o antecedentes familiares de lactantes fallecidos precozmente o consanguinidad(4,6,7).
Figura 2. Ausencia de sombra tímica en dos lactantes con inmunodeficiencia combinada grave (IDCG) e infección respiratoria viral (CMV y parainfluenza).
Figura 3. En los niños con inmunodeficiencia combinada grave (IDCG), hay una depleción de linfocitos, con ausencia de ganglios y de amígdalas en pilares faríngeos. En la imagen (A), vemos la anatomía patológica de un timo de un niño sano, con la corteza llena de linfocitos. En la imagen (B), vemos la histología del timo de un niño con IDCG, con una completa depleción de linfocitos en su corteza tímica.
Principales manifestaciones clínicas en niños con inmunodeficiencia primaria
En niños con IDP, el tipo de infección, así como otras manifestaciones asociadas, dependen del tipo de IDP que presenten. Conocer las manifestaciones más frecuentes permite establecer la sospecha diagnóstica.
Existen más de 300 tipos de IDPs, que se clasifican en grupos, según el defecto fundamental encontrado(4) (Tabla II).
En los déficits de anticuerpo (inmunidad humoral), las infecciones aparecen a partir de los 6 meses, suelen ser respiratorias y digestivas, fundamentalmente por bacterias y diarreas por Giardia. Las inmunodeficiencias combinadas (IDC) manifiestan infecciones desde el nacimiento por todos los tipos de microorganismo y constituyen una auténtica urgencia pediátrica. En los defectos del fagocito, las infecciones cutáneas con abscesos de partes blandas, hepáticos y neumonías bacterianas y fúngicas son las principales formas de presentación. En los déficits de anticuerpo, existe predilección por infecciones por bacterias encapsuladas, bien sean infecciones respiratorias por neumococo o H. influenzae, o sepsis graves y meningitis por N. meningitidis(1-4,8).
Las características clínicas, según el defecto inmunitario, se recogen en la tabla III(1-4,8).
En la exploración de niños con infecciones recurrentes en los que sospechamos una IDP, debemos fijarnos en los siguientes datos(1,2,4):
• Estado nutricional: muchas IDPs conllevan aumento de gasto calórico por infecciones recurrentes y, como consecuencia, fallo de medro.
• Auscultación pulmonar: muchas IDPs tienen el pulmón como órgano diana de sus infecciones. Por ello, es importante realizar una exploración pulmonar rigurosa.
• ORL: explorar presencia o ausencia de amígdalas (tejido linfático). En la otoscopia, comprobar si existe perforación timpánica, otorrea o tímpanos deslustrados.
• Exploración de la piel:
- Telangiectasias conjuntivales (ataxia-telangiectasia).
- Dermatitis atópica, facies tosca, alteración dentaria (síndrome de HiperIgE).
- Eritrodermia, dermatitis grave (IDCG, síndrome de Omenn) (Fig. 4).
Figura 4. Los niños con inmunodeficiencia combinada grave (IDCG) suelen presentar, con frecuencia, afectación cutánea. En la imagen vemos la dermatitis de niño con IDCG y enfermedad injerto contra huésped materno-fetal.
- Albinismo con nistagmo (Chediak-Higashi).
- Muguet, dermatitis del pañal, candidiasis (IDCG).
- Onicomicosis (candidasis mucocutánea crónica).
• Hepatoesplenomegalia y adenomegalias: inmunodeficiencia variable común (IDVC), enfermedad granulomatosa crónica (EGC), síndrome linfoproliferativo autoinmune).
• Afectación neurológica con ataxia (ataxia-telangiectasia).
• Cardiopatía, tetania, facies peculiar, retraso psicomotor (síndrome de DiGeorge).
• Sangrados, petequias, hematomas (Wiskott-Aldrich, trombopenias en IDVC).
• Pelo fino, talla baja (síndrome cartílago-pelo).
Orientación diagnóstica inicial en casos con sospecha de inmunodeficiencia primaria
Debemos mantener un alto índice de sospecha de IDPs en niños que presenten en las pruebas complementarias citopenias, especialmente linfopenias en lactantes, ausencia de sombra tímica en radiografía de tórax, hipogammaglobulinemia o ausencia de seroconversión tras vacunación. Una vez que se sospecha una IP, deben establecerse todas las medidas necesarias para prevenir las infecciones y contactar con un pediatra especialista en inmunodeficiencias.
En general, los estudios básicos para sospecha de IDPs en niños que presenten infecciones recurrentes, se llevan a cabo en la mayor parte de los hospitales de tercer nivel.
Sin embargo, podemos iniciar la sospecha diagnóstica desde Atención Primaria, manteniendo alto índice de sospecha, ante hallazgos concretos, en algunas pruebas complementarias. Debemos remarcar que, al tratarse de patologías raras con diagnóstico complejo, ante una sospecha diagnóstica, el paciente se debe remitir siempre a un Centro de Referencia para completar su estudio.
• Hemograma(1,6-8): muchos niños inmunocompetentes presentan con frecuencia leucopenias, linfopenias o trombopenias en el contexto de infecciones banales. Sin embargo, es labor del pediatra confirmar la normalización del hemograma una vez resuelto el proceso agudo infeccioso. En caso de mantenerse la presencia de citopenias, el paciente debe ser derivado para descartar IDP. De especial importancia resulta la presencia de linfopenias en lactantes menores de 1 año; ya que, como se ha comentado, la IDCG es una auténtica urgencia pediátrica. Además, muchos niños con IDP pueden asociar citopenias diversas (neutropenias, anemias o trombopenias) de origen autoinmune, que pueden ser la manifestación de debut de su IDP. Por ello, niños con citopenias persistentes y/o autoinmunes requieren también cribado de IDP15). A continuación, citamos los hallazgos en hemograma más frecuentes según tipo de IDP(4):
- Linfopenias/Leucopenia: IDC; IDVC.
- Neutropenia: neutropenia congénita; IDVC.
- Eosinofilia: algunas inmunodeficiencias combinadas; síndrome de HiperIgE.
- Trombopenia: Wiskott-Aldrich; IDVC.
- Leucocitosis/Neutrofilia extrema: déficit de adhesión leucocitaria.
- Anemia: por enfermedad crónica, de origen autoinmune, ferropénica en casos de infecciones gastrointestinales con malabsorción.
• Radiografía de tórax: en un lactante con infecciones en el que realicemos una radiografía de tórax, debemos fijarnos siempre en la presencia de sombra tímica(6,7). La ausencia de la misma, especialmente en lactantes con linfopenias, debe hacernos sospechar IDCG (Fig. 2).
• Niveles de inmunoglobulinas(1-4,8): deben valorarse en relación a la edad del paciente. En niños con hipogammaglobulinemia, debe descartarse la posibilidad de pérdida proteica. Las cifras de inmunoglobulinas no son valorables si el paciente ha recibido recientemente infusión de gammaglobulina. Durante los primeros años, algunos niños presentan hipogammaglobulinemia transitoria de la infancia, pero este no debe conllevar mayor susceptibilidad a infecciones.
• Otros estudios más específicos(1-4,8): una vez sospechada una IDP, el paciente debe ser remitido a un Centro de referencia, donde se estudiarán detenidamente porcentajes de subpoblaciones linfocitarias, respuesta a vacunas y presencia de linfocitos B memoria, valoración cualitativa de función de linfocitos T (respuesta a mitógenos o proliferación linfocitaria), la capacidad oxidativa de los neutrófilos o la vía del complemento. En muchas ocasiones, se precisa realizar estudios genéticos para identificar el gen responsable del defecto inmunológico.
En niños con sospecha de IDP en estudio o con IDP ya diagnosticada, resulta fundamental optimizar todas las pruebas microbiológicas para el diagnóstico de infecciones. La mayor parte de estas infecciones requieren de la evaluación de un especialista en infectología(4,7). Sin embargo, los pediatras de Urgencias y de Atención Primaria deben atender en primera instancia a estos niños. En inmunodeficiencias humorales resulta fundamental recoger cultivo de esputo y/o coprocultivo ante infecciones respiratorias y digestivas, así como test de gripe en época epidémica4). No debemos solicitar estudios serológicos en niños con inmunodeficiencias que no producen anticuerpos y/o que estén en tratamiento sustitutivo con gammaglobulina. En niños con IDC, pruebas como el test de tuberculina, pueden dar falsos negativos por defecto de la función T. Todos estos niños deben siempre ser remitidos a su pediatra especialista de referencia ante la presencia de una infección(4).
Prevención de infecciones en niños de riesgo
En poblaciones de riesgo (IDPs o niños con enfermedades que condicionen riesgo de infección o inmunodeficiencia secundaria), es fundamental establecer medidas profilácticas en función de la patología, para evitar infecciones recurrentes. La vacunación en estos pacientes es un pilar fundamental y debe individualizarse.
Los pacientes con infecciones de repetición que presentan una IDP o una enfermedad crónica/inmunodeficiencia secundaria tienen un elevado riesgo de adquirir infecciones, que pueden ser más graves, más frecuentes y recurrentes que en la población general(17,18). Por ello, en el tratamiento de estos pacientes, es fundamental la prevención de infecciones.
Vacunación
Las IDP son un grupo muy heterogéneo de enfermedades y, por ello, las recomendaciones vacunales han de ser individualizadas y orientadas por su pediatra especialista de referencia(19,20). Existen una serie de recomendaciones generales(6,18-20):
• Las vacunas atenuadas no deben nunca administrarse sin consultar previamente a su especialista de referencia, por riesgo grave de producir infección asociada a la vacunación. En las IDCG están contraindicadas todas las vacunas atenuadas (rotavirus, triple vírica, varicela) y la BCG y fiebre amarilla. Las vacunas inactivadas no plantean problemas de seguridad, pero pueden ser menos eficaces.
• Cuando el déficit de formación de anticuerpos es grave, no se recomiendan las vacunas atenuadas y, en pocos casos, estarían indicadas las inactivadas (pueden no dar respuesta, especialmente si hay un tratamiento con inmunoglobulinas instaurado).
• En los defectos de la fagocitosis, las únicas contraindicaciones son la vacuna frente a la fiebre tifoidea oral y la BCG.
• Los niños con déficit de complemento y con asplenia anatómica o funcional tienen especialmente indicadas las vacunas meningocócicas (ACYW y B), neumocócica, H. influenzae tipo b, varicela y gripe.
• Todos los convivientes deben tener actualizado el calendario vacunal, con especial énfasis en la vacunación antigripal anual, la varicela y la triple vírica. Están contraindicadas las vacunas orales atenuadas frente a la Salmonella typhi y rotavirus en el entorno de los convivientes.
En niños con enfermedades crónicas que predispongan a infección y/o que reciben tratamientos inmunosupresores, es igualmente importante tenerles protegidos mediante vacunación, requiriendo vacunaciones adicionales a las incluidas en el calendario financiado para cada CC.AA., como: vacunación antigripal, vacuna antineumocócica no conjugada 23valente o vacunación frente a VHA, según recomendación del CAV-AEP para cada patología en concreto(17). Sin embargo, muchos estudios demuestran que estos niños crónicos están peor vacunados que la población general y que, además, no cumplen con las recomendaciones adicionales de inmunización según patología de base(17). Es labor del pediatra asegurar el correcto cumplimiento del calendario vacunal, según cada tipo de patología.
Profilaxis antibiótica(1-4,6,18)
La profilaxis antibiótica está especialmente indicada en niños con IDCG y con EGC con cotrimoxazol a dosis 5 mg/kg/día cada 12 horas, al menos, 3 veces por semana, por el riesgo de infecciones bacterianas y P. jirovecii en las IDCG, y de infecciones bacterianas en la EGC.
En niños con otras IDPs o inmunodeficiencias secundarias que presenten linfopenia CD4, se asocia igualmente profilaxis con cotrimoxazol. En ocasiones, en niños con déficit de anticuerpos e infecciones respiratorias recurrentes, se asocia profilaxis con cotrimoxazol o con azitromicina, aunque esta pauta no está bien protocolizada y existe variabilidad en su prescripción entre distintos especialistas. La profilaxis antifúngica está especialmente indicada en niños con ECG y se individualiza en niños con IDCG(6,7).
Detección precoz de focos infecciosos(4,8)
La detección de focos infecciosos (odontológicos, senos paranasales y ORL…) es fundamental para su tratamiento temprano. Medidas simples, tales como lavarse las manos son muy importantes. Es necesaria una adecuada indicación de antibióticos cuando surjan infecciones.
Otras medidas preventivas(1-4,8)
Los niños con patologías respiratorias crónicas o IDPs que asocian patología respiratoria crónica, precisan la realización de fisioterapia respiratoria, especialmente si asocian bronquiectasias, para evitar las infecciones respiratorias recurrentes. En niños con IDP grave, resulta fundamental las medidas de aislamiento, restringiendo su acceso a guardería y el contacto con enfermos, para evitar la adquisición de infecciones6,8). La higiene dental y el control odontológico son importantes. Igualmente, es fundamental mantener un adecuado estado nutricional(1) y pueden ser necesarios soportes nutricionales en pacientes que asocien síndrome de malabsorción, ya que la malnutrición condiciona inmunodeficiencia secundaria, que aumenta el riesgo de infecciones. Respecto a la planificación de viajes, resulta fundamental en niños de riesgo con IDPs o enfermedades crónicas, que sean valorados en unidades de vacunación internacional, previamente a un viaje al extranjero, para adecuar vacunas y profilaxis. Por último, debemos recomendar la inmunización pasiva con palivizumab en lactantes que han sido prematuros, cardiópatas, con patologías respiratorias crónicas, con IDC o patología neuromuscular grave.
Función del pediatra de Atención Primaria
El papel del pediatra de Atención Primaria es fundamental para establecer la sospecha diagnóstica de IDP, así como para colaborar en los cuidados del paciente con patologías que aumenten su riesgo de infección.
El pediatra de Atención Primaria tiene dos papeles fundamentales en la atención de niños con inmunodeficiencias primarias y/o secundarias:
1. Iniciar la sospecha diagnóstica: como hemos visto a lo largo del capítulo, muchos niños se diagnostican tardíamente y, sin embargo, el diagnóstico precoz de los mismos puede marcar pronóstico. Por ello, es fundamental mantener un alto índice de sospecha en niños con infecciones recurrentes, sobre todo, cuando: se afecte la curva de peso, no respondan al tratamiento, existan antecedentes familiares de consanguinidad o de enfermedades autoinmunes o se asocien citopenias en las analíticas. Estos pacientes deben ser remitidos precozmente a centros de referencia para descartar la presencia de una inmunodeficiencia. El pediatra de Atención Primaria no debe olvidar que muchas inmunodeficiencias no debutan con infecciones, sino con autoinmunidad o manifestaciones inflamatorias.
2. Colaborar en el manejo y cuidado de pacientes con enfermedades que predisponen a infecciones recurrentes: estos niños acuden, con frecuencia, a consulta en Servicios de Urgencias o en Atención Primaria, por fiebre o infecciones intercurrentes. Resulta fundamental una adecuada comunicación entre el pediatra hospitalario de referencia para estas patologías y el pediatra de Atención Primaria que atiende a los pacientes. El pediatra de Atención Primaria debe:
• Conocer: el tipo de enfermedad, los tratamientos, profilaxis y vacunaciones recibidas. Igualmente, conocer infecciones previas y resultados de cultivos anteriores.
• Cuando el niño consulte, se debe realizar una exploración exhaustiva, deteniéndose en la patología más habitual, según el tipo de enfermedad (p. ej.: infección respiratoria en déficits de anticuerpos o abscesos en niños con EGC).
• En niños con inmunodeficiencias humorales, resulta fundamental recoger precozmente cultivo de esputo o coprocultivos si consultan en su Centro de Salud por clínica respiratoria o digestiva. En estos niños, especialmente con clínica respiratoria y aumento de secreciones de aspecto purulento, es fundamental iniciar tratamiento antibiótico precoz, para evitar el desarrollo de bronquiectasias en la edad adulta. Los niños con inmunodeficiencias más graves deben ser remitidos siempre a un Centro Hospitalario.
• El pediatra de primaria debe recordar que algunas inmunodeficiencias como la IDVC asocian complicaciones no infecciosas, como: citopenias autoinmunes, neumonitis linfoide o hepatoesplenomegalia. Todas sus manifestaciones no son siempre infecciosas y debemos tenerlo en cuenta cuando consulten.
Bibliografía
Los asteriscos reflejan el interés del artículo a juicio del autor.
1.** Ruiz-Contreras J. Inmunología básica. Aproximación a las inmunodeficiencias primarias. Pediatr Integral. 2014; XVIII(3): 183-92.
2.*** Jyothi S, Lissauer S, Welch S, Hackett S. Immune deficiencies in children: an overview. Arch Dis Child Educ Pract Ed. 2013; 98: 186-6.
3. García Martínez JM, Santos-Díez L, Dopazo L. Diagnóstico de las inmunodeficiencias primarias. Protoc diagn ter pediatr. 2013; 1: 81-92.
4. Méndez Echevarría A, Del Rosal R. Sospecha de Inmunodeficiencia Primaria. Orientación diagnóstica y manejo básico. Manual de diagnóstico y terapéutica en Pediatría. 6º Edición. Editorial Panamericana; p. 161-8.
5. Montella S, Corcione A, Santamaría F. Recurrent Pneumonia in Children: A Reasoned Diagnostic Approach and a Single Centre Experience. Int J Mol Sci. 2017; 18: pii: E296. doi: 10.3390/ijms18020296.
6. Rivers L, Gaspar HB. Severe combined immunodeficiency: recent developments and guidance on clinical management. Arch Dis Child. 2015; doi: 10.1136/archdischild-2014-306425.
7. Méndez-Echevarría A, Del Rosal T, Pérez-Costa E, Rodríguez-Pena R, Zarauza A, Ferreira-Cerdán A, et al. Clinical Features Before Hematopoietic Stem Cell Transplantation or Enzyme Replacement Therapy of Children With Combined Immunodeficiency. Pediatr Infect Dis J. 2016; 35: 794-8.
8.*** Hernández-Trujillo VP. Approach to Children with Recurrent Infections. Immunol Allergy Clin North Am. 2015; 35: 625-36.
9. Nguyen TK, Tran TH, Roberts CL, Fox GJ, Graham SM, Marais BJ. Risk factors for child pneumonia – focus on the Western Pacific Region. Paediatr Respir Rev. 2017; 21: 95-101.
10. Chicoulaa B, Haas H, Viala J, Salvetat M, Olives JP. How French general practitioners manage and prevent recurrent respiratory tract infections in children: the SOURIRRE survey. Int J Gen Med. 2017; 10: 61-8.
11. Picard C, Bobby Gaspar H, Al-Herz W, Bousfiha A, Casanova JL, Chatila T, et al. International Union of Immunological Societies: 2017 Primary ImmunodeficiencyDiseases Committee Report on Inborn Errors of Immunity. J Clin Immunol. 2018; 38: 96-128.
12. Al-Herz W, Aldhekri H, Barbouche MR, Rezaei N. Consanguinity and primary immunodeficiencies. Hum Hered. 2014; 77: 138-43.
13. Climent Alcalá FJ, García Fernández de Villalta M, Escosa García L, Rodríguez Alonso A, Albajara Velasco LA. Children’s medically complex diseases unit. A model required in all our hospitals. An Pediatr (Barc). 2018; 88: 12-8.
14. Burns KH, Casey PH, Lyle RE, Bird TM, Fussell JJ, Robbins JM. Increasing prevalence of medically complex children in US hospitals. Pediatrics. 2010; 126: 638-46.
15. Fischer A, Provot J, Jais JP, Alcais A, Mahlaoui N; members of the CEREDIH French PID study group. Autoimmune and inflammatory manifestations occur frequently in patients with primary immunodeficiencies. J Allergy Clin Immunol. 2017; 140: 1388-93.e8.
16. Long SS. Distinguishing among prolonged, recurrent, and periodic fever syndromes: approach of a pediatric infectious diseases subspecialist. Pediatr Clin North Am. 2005; 52: 811-35.
17. Pandolfi E, Carloni E, Marino MG, Ciofi degli Atti ML, Gesualdo F, Romano M, et al. Immunization coverage and timeliness of vaccination in Italian children with chronic diseases. Vaccine. 2012; 30: 5172-8.
18.** Aguilar C, Malphettes M, Donadieu J, Chandesris O, Coignard-Biehler H, Catherinot E, et al. Prevention of infections during primary immunodeficiency. Clin Infect Dis. 2014; 59: 1462-70.
19.** Mellado Peña M, Ruiz Contreras J, Moreno Pérez D, Navarro Gómez ML. Documento de consenso de la Sociedad Española de Infectología Pediátrica y el Comité Asesor de Vacunas de la Asociación Española de Pediatría para la vacunación en inmunodeprimidos. Respuesta de los autores. An Pediatr [Internet]. 2012; 77: 220-1. Disponible en: https://goo.gl/7dm2i5.
20.** Rubin LG, Levin MJ, Ljugman P, Daviers EG, Avery R, Tomblyn M, et al. 2013 IDSA Clinical Practice Guideline for Vaccination of the immunocompromised host. Clin Infect Dis. 2013; 58: e44-e100.
Bibliografía recomendada
– Jyothi S, Lissauer S, Welch S, Hackett S. Immune deficiencies in children: an overview. Arch Dis Child Educ Pract Ed. 2013; 98: 186-96.
Este artículo explica de manera clara y muy docente, dirigida a pediatras no especialistas, el enfoque de niños con sospecha de inmunodeficiencia primaria, comenzando con una breve explicación del funcionamiento y maduración del sistema inmune, y terminando el tema con la exposición de algunos casos clínicos, ilustrando la teoría expuesta. Muy recomendable lectura para la iniciación en el estudio de las inmunodeficiencias primarias.
– Hernández-Trujillo VP. Approach to Children with Recurrent Infections. Immunol Allergy Clin North Am. 2015; 35: 625-36.
En este artículo de revisión, se facilita la orientación diagnóstica de niños con infecciones recurrentes, explicando signos de alarma y orientando el diagnóstico de las posibles inmunodeficiencias, según el tipo de infección que los niños presenten.
– Mellado Peña M, Ruiz Contreras J, Moreno Pérez D, Navarro Gómez ML. Documento de consenso de la Sociedad Española de Infectología Pediátrica y el Comité Asesor de Vacunas de la Asociación Española de Pediatría para la vacunación en inmunodeprimidos. Respuesta de los autores. An Pediatr [Internet]. 2012; 77: 220-1. Disponible en: https://goo.gl/7dm2i5.
– Rubin LG, Levin MJ, Ljugman P, Daviers EG, Avery R, Tomblyn M, et al. 2013 IDSA Clinical Practice Guideline for Vaccination of the immunocompromised host. Clin Infect Dis. 2013; 58: e44-e100. doi: 10.1093/cid/cit684.
Estos dos artículos son las guías para la vacunación de los pacientes inmunodeprimidos de la Sociedad Americana de Enfermedades Infecciosas (IDSA) y de la Asociación Española de Pediatría/Sociedad Española de Pediatría (CAV-AEP y SEIP). Incluye los calendarios para todos los pacientes inmunodeprimidos y bibliografía actualizada.
| Caso clínico |
|
Niño de 4 años, marroquí, remitido por tos y fiebre que no responde tras 4 días de amoxicilina-clavulánico. Lleva 7 meses en España y ha presentado 3 bronconeumonías tratadas ambulatoriamente, sin realizarse radiografía, pero con auscultación focal que mejoró con tratamiento antibiótico. También, ha tenido una gastroenteritis por Campylobacter. Nacido en una zona rural de Marruecos, de padres consanguíneos, con antecedente neonatal de aspiración meconial y secuela de hemiparesia. Los padres refieren que tiene tendencia a broncoaspiración en las comidas. Presenta fallo de medro. A la auscultación, subcrepitantes bilaterales, sin hipoxemia. Talla baja (p<1, -2,84 DE), bajo peso (p<1; -3,76 DE), IMC: p2 (-2,12 DE), hemiparesia leve, referida como habitual desde nacimiento. En la radiografía torácica, infiltrado en lóbulo inferior derecho sin condensación. En la analítica: 3.220 leucocitos (linfocitos: 1.320; neutrófilos: 1.450), plaquetas: 156.000. PCR: 40 mg/L. En el aspirado nasofaríngeo resultó positivo para Adenovirus y en sangre detectamos carga viral positiva para citomegalovirus.
|