 |
| Temas de FC |
A. Bermejo Gómez, M. García-López Hortelano
Servicio de Pediatría. Enfermedades Infecciosas y Tropicales. Unidad de Adopción Internacional y Niño Viajero. Hospital Universitario Infantil La Paz – Hospital Carlos III. Madrid
| Resumen
Las zoonosis son enfermedades infecciosas que se transmiten desde los animales a los humanos. Pueden transmitirse a través de vectores, como garrapatas o mosquitos, o por contacto directo con el animal infectado. En este capítulo describimos las zoonosis más frecuentes en nuestro medio. Tanto la leishmaniasis visceral como la enfermedad de Lyme, tienen mal pronóstico sin tratamiento, por lo que es necesaria una alta sospecha diagnóstica para asegurar un tratamiento precoz. El diagnóstico se puede realizar por métodos serológicos (posibilidad de falsos negativos o reacciones cruzadas) o por métodos moleculares (de elección). La mayoría de las zoonosis virales no tienen tratamiento específico, mientras que las zoonosis bacterianas se tratan con antibióticos. |
| Abstract
Zoonoses are infectious diseases that are transmitted from animals to humans. They can be transmitted by vectors such as ticks or insects, or by direct contact with the infected animal. In this chapter we describe the most frequent zoonoses in our environment. Visceral leishmaniasis and Lyme disease have a poor prognosis without treatment, so a high diagnostic suspicion is necessary to ensure early treatment. Diagnosis can be made by serological methods (with the possibility of false negatives or cross-reactions) or by molecular methods (of choice). Most viral zoonoses have no specific treatment, while bacterial zoonoses are treated with antibiotics. |
Palabras clave: Zoonosis; Leishmaniasis; Borreliosis; Garrapata.
Key words: Zoonosis; Leishmaniasis; Borreliosis; Tick.
Pediatr Integral 2023; XXVII (7): 381 – 388
OBJETIVOS
• Conocer las zoonosis más frecuentes de nuestro medio, profundizando en los aspectos epidemiológicos de estas enfermedades.
• Recordar la importancia de una buena anamnesis e historia clínica, para asegurar un enfoque para el diagnóstico precoz.
• Conocer las principales etiologías, métodos diagnósticos y opciones terapéuticas adecuadas, según la edad y síntomas del niño.
• Aprender cuáles son las medidas de prevención pre-exposición y post-exposición de estas enfermedades.
Zoonosis
Introducción
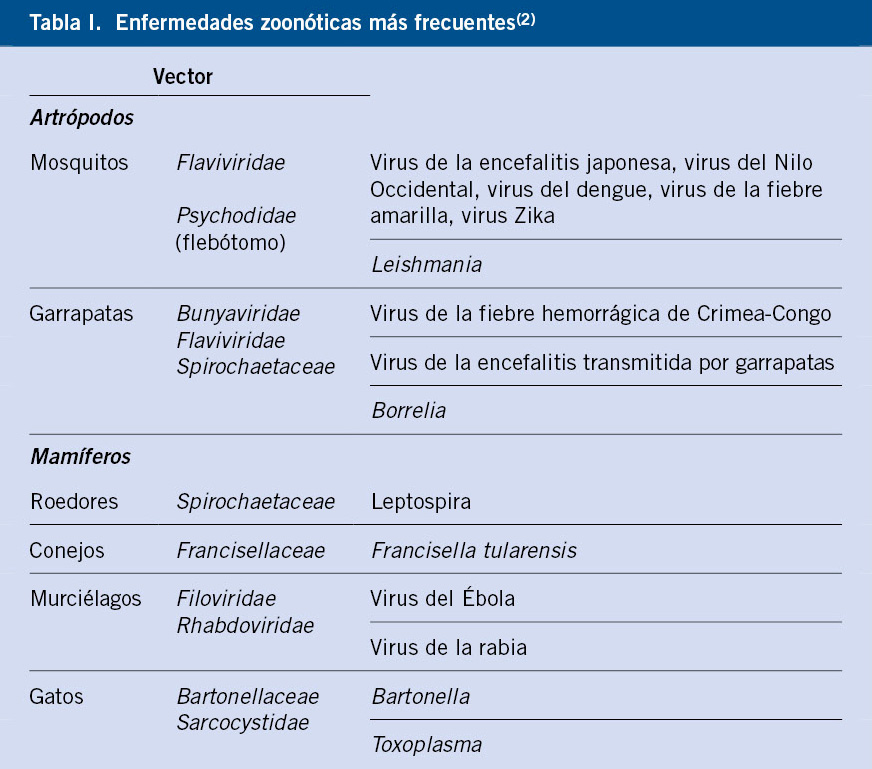
La Organización Mundial de la Salud (OMS) define las zoonosis como: las enfermedades infecciosas que se transmiten desde los animales a los humanos(1). Representan un importante problema de salud pública, debido a la estrecha relación con los animales en el medio agrícola, la vida cotidiana (animales de compañía) y el entorno natural(2). El ser humano suele ser un hospedador accidental que adquiere la enfermedad por contacto directo o indirecto con un animal infectado. Los mecanismos de transmisión son muy diversos: alimentos, vectores o contacto directo con fluidos o animales infectados(2) (Tabla I).
En toda historia clínica es importante incluir una anamnesis detallada, incluyendo los antecedentes de viajes, actividades rurales y contacto con animales; ya que esta información nos ayudará en el enfoque diagnóstico del paciente.
En este capítulo nos centramos en las principales zoonosis transmitidas en nuestro medio; aunque es importante recordar que, con los viajes internacionales, podemos atender en la consulta zoonosis adquiridas en otros países. Además, el calentamiento global está aumentando el intervalo geográfico de los mosquitos y las garrapatas que albergan y transmiten plasmodios y arbovirus, lo que condiciona la aparición de brotes en nuevas localizaciones (como ocurre con el dengue en Europa)(2,3).
Enfermedades transmitidas por mosquitos
Leishmaniasis
Enfermedad potencialmente mortal, endémica en regiones tropicales y subtropicales. La forma clínica más frecuente en España es la leishmaniasis visceral.
Introducción
La leishmaniasis es endémica en regiones tropicales y subtropicales, se encuentra en América del Norte y del Sur, sur de Europa, África y Asia(4) . Es una enfermedad de declaración obligatoria (EDO) y forma parte del grupo de Enfermedades Desatendidas de la OMS.
Se considera una zoonosis, ya que su reservorio principal es el perro (también se ha descrito en: gatos, roedores y liebres); sin embargo, puede transmitirse de persona a persona mediante un vector (en estos casos, se denomina antropozoonosis)(5). El vector principal es un flebótomo.
La leishmaniasis cutánea es el tipo de leishmaniasis más común en todo el mundo (0,6-1 millón de casos nuevos anuales), es más frecuente que la leishmaniasis visceral (50.000-90.000 casos nuevos al año)(4) (Figs. 1 y 2).
Figura 1. Epidemiología de leishmaniasis visceral. Fuente: OMS. 2021.
Figura 2. Epidemiología de leishmaniasis cutánea. Fuente: OMS. 2021.
Manifestaciones clínicas
Puede producir distintos síndromes clínicos(4), los tres principales son los siguientes:
1. Leishmaniasis cutánea (LC) o botón de Oriente: causada habitualmente por las especies del subgénero: Leishmania (L. tropica, L. major, L. aethiopica y por las especies L. mexicana, L. amazonensis) y Viannia (V. braziliensis, V. panamensis, V. guyanensis y V. peruviana). Tras la picadura del mosquito, se produce una pápula eritematosa que, en los casos típicos, aumenta, convirtiéndose en un nódulo. Posteriormente, se genera una lesión ulcerada con bordes indurados y elevados, que puede asociar una costra o exudado. Las lesiones cutáneas son generalmente indoloras y crónicas. A veces, pueden asociar adenopatías periféricas o lesiones satélites(4).
2. Leishmaniasis visceral (LV) o kala-azar: afecta principalmente a los niños menores de 5 años en América y en la región mediterránea (L. infantum), y a los niños mayores y adultos jóvenes en África y Asia (L. donovani)(5). Tras la inoculación cutánea por un mosquito infectado (flebotominos hembras), el parásito se disemina por todo el sistema reticuloendotelial (macrófagos, bazo, hígado y médula ósea). Las manifestaciones típicas son: fiebre, pérdida de peso, hepatoesplenomegalia, pancitopenia (anemia, leucopenia y trombocitopenia), hipoalbuminemia e hipergammaglobulinemia. La piel de algunos pacientes adquiere una coloración grisácea, que da origen al término kala-azar (“fiebre negra” en hindi). Algunos pacientes pueden permanecer asintomáticos(4).
3. Leishmaniasis mucosa (LM) o espundia: producida habitualmente por especies del subgénero Viannia. Las áreas de mayor riesgo de LM se encuentran al sur del Amazonas (Bolivia, Perú y Brasil)(6). Se refiere a una secuela metastásica de la infección cutánea, que afecta a la mucosa nasofaríngea o laríngea. Clínicamente, es visible meses o años después de que hayan cicatrizado las lesiones cutáneas originales(4).
Diagnóstico
El diagnóstico de certeza de la leishmaniasis se realiza por la observación directa de los amastigotes en tejidos, el diagnóstico indirecto se realiza detectando la respuesta humoral o celular frente al parásito(7).
• Técnicas microscópicas: visualización directa de amastigotes de Leishmania spp. en extensiones de material aspirado (médula ósea, sangre, biopsia cutánea o linfática)(7). La sensibilidad de esta técnica depende de muchos factores (calidad de la muestra, carga parasitaria y experiencia del observador)(7). En el caso de la LC, es importante retirar los restos de exudados o escaras, para que sea más sencillo visualizar el parásito(6).
• Cultivo: mayor sensibilidad que la microscopía directa, pero es más laborioso y requiere mayor tiempo para obtener los resultados (hasta 4 semanas)(7). El medio idóneo es el Novi-McNeal-Nicolle (NNN).
• Detección de antígenos en orina: suele utilizarse en los casos de LV(7).
• Detección de ácidos nucleicos (diagnóstico molecular): detección de ADN del parásito mediante reacción en cadena de polimerasa (PCR), evalúa la carga parasitaria y puede ser útil para monitorizar la respuesta al tratamiento(4). Permite el uso de procedimientos menos invasivos para el diagnóstico de LV, ya que se puede detectar en sangre periférica(7); aunque las guías americanas siguen recomendando el aspirado de médula ósea como la muestra más fiable para el diagnóstico(6).
• Técnicas serológicas: no se recomienda su uso en LC o LM, por escasa producción de anticuerpos(6). La sensibilidad y la especificidad de las pruebas serológicas dependen del ensayo y los antígenos utilizados. Si existe una sospecha clínica elevada, un resultado negativo no descarta la enfermedad(4,6,7), por este motivo, no se recomienda realizar la serología como única prueba en el diagnóstico de la leishmaniasis.
Tratamiento
El tratamiento sistémico está indicado en todos los niños con LV (por su elevada mortalidad) o LM (por la probabilidad de destrucción de la mucosa); sin embargo, no todos los menores con LC precisan tratamiento sistémico, ya que tienden a la curación espontánea (en años)(6). El tratamiento en esta forma acelera la cicatrización, disminuyendo la afectación de la mucosa y el riesgo de mortalidad en lesiones de gran tamaño (≥5 cm) o persistentes. En la tabla II se resumen las recomendaciones terapéuticas(4).
Enfermedades transmitidas por garrapatas
Enfermedad de Lyme
Existe un aumento de casos de borreliosis en nuestro país, sobre todo en el norte de España. Las manifestaciones clínicas van a depender del tiempo de evolución desde la mordedura de garrapata, teniendo en cuanta que, a veces, puede pasar desapercibida.
Introducción, etiología y epidemiología
La enfermedad de Lyme es una zoonosis producida por la bacteria Borrelia burgdorferi, transmitida por garrapatas duras (Ixodes ricinus). Es una patología emergente en Europa (Alemania, Austria, Eslovenia, Suecia) y en España (La Rioja, Navarra, Norte de Castilla y León, Asturias, Cantabria y País Vasco). En 2022 se publicó el último boletín de la Red Nacional de Vigilancia Epidemiológica (Instituto de Salud Carlos III), en el que se alerta del aumento de casos en nuestro país(8).
Manifestaciones clínicas
Las manifestaciones clínicas de la enfermedad de Lyme se dividen en tres fases, según el tiempo de evolución desde la mordedura de garrapata(9):
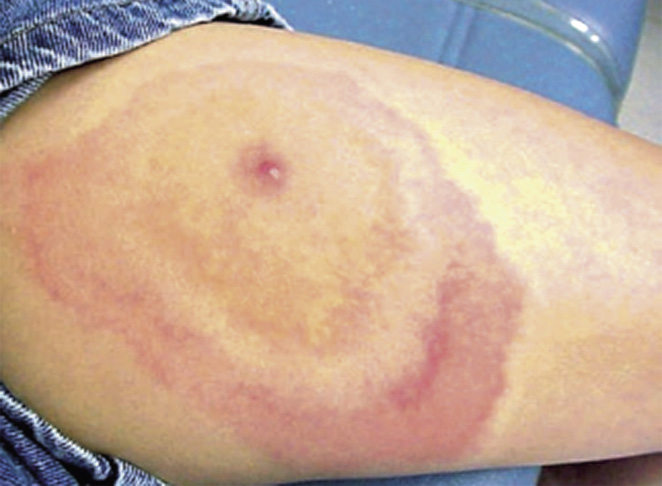
1. Manifestaciones tempranas localizadas: la manifestación temprana más característica es el eritema migrans (Fig. 3).
Figura 3. Eritema migrans o migratorio. Imagen en “ojo de buey” con anillos concéntricos (en una minoría de los casos). Puede asociar vesículas centrales o áreas necróticas Fuente: Long S. Principles and Practice of Pediatric Infectious Diseases. 2018; 185: 997-1001.e1.
Tras la mordedura de la garrapata, suele aparecer una mácula o pápula roja, que se extiende progresivamente hasta formar una lesión eritematosa anular grande (>5 cm de diámetro) en días o semanas. Puede asociar síntomas constitucionales como: malestar general, cefalea, fiebre, artralgias y rigidez cervical leve.
2. Manifestaciones tempranas diseminadas: lesiones diseminadas similares al eritema migrans, de tamaño más pequeño. Puede asociar: parálisis del VII par, meningitis linfocitaria y radiculitis. En varones adolescentes puede aparecer bloqueo auriculoventricular, lo que condiciona un mal pronóstico. También pueden estar presentes los síntomas constitucionales.
3. Manifestaciones tardías: suele darse en forma de monoartritis de grandes articulaciones (rodilla); en algunas ocasiones, puede ser poliarticular. Ocurre en aquellos niños que no han recibido tratamiento. Con menor frecuencia puede aparecer: polineuropatía, encefalopatía o afectación ocular (neuritis óptica, conjuntivitis, queratitis y uveítis).
Diagnóstico
El diagnóstico se basa en la historia epidemiológica, las manifestaciones clínicas y los hallazgos microbiológicos(10). Es frecuente que los menores no recuerden la mordedura de garrapata, pudiendo pasar desapercibida.
• Diagnóstico directo:
- Cultivo: es más sensible en la fase temprana de la enfermedad. Presenta un alto rendimiento en muestras cutáneas, disminuyendo la sensibilidad en fluidos estériles (LCR o líquido sinovial).
- Técnicas de diagnóstico molecular (PCR): método diagnóstico principal; sin embargo, estas técnicas no están estandarizadas. La sensibilidad depende del origen de la muestra, siendo mayor en las biopsias cutáneas (cercana al 70 %) y muestras de líquido sinovial (77,5 %), descendiendo considerablemente en muestras de LCR (22,5 %)(10). No está validada en sangre ni orina.
• Diagnóstico indirecto mediante técnicas serológicas. En fases precoces, la serología puede ser negativa (solo se detecta IgM en un 60 % de los pacientes en las 4 primeras semanas)(10); es importante confirmar la seroconversión a las 4-6 semanas (mediante detección de IgG). En casos de diagnóstico clínico claro (eritema migrans), no es necesario realizar serología de confirmación. En los que se ha realizado un tratamiento precoz, puede no haber seroconversión(10). Ocasionalmente, aparecen reacciones cruzadas con otras bacterias.
Tratamiento
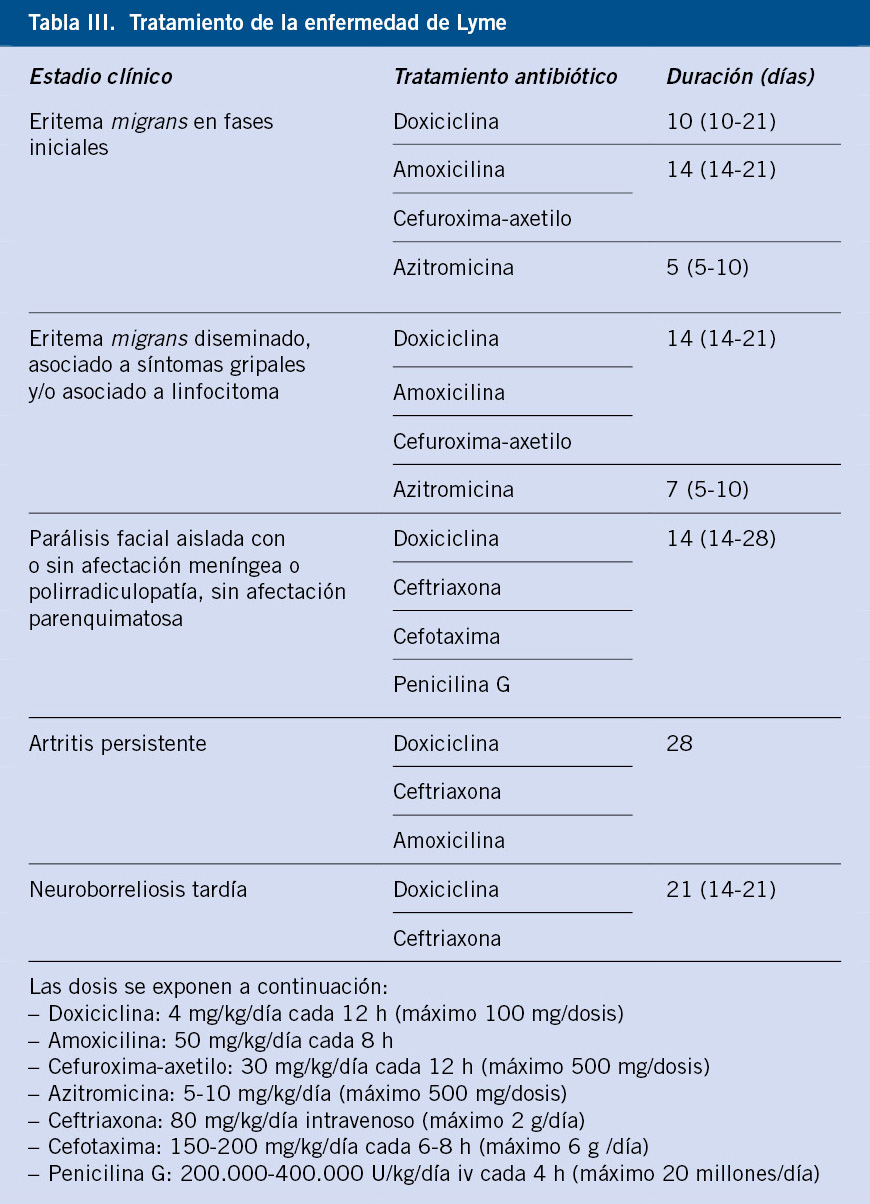
El tratamiento de elección será doxiciclina, siempre que no exista afectación del parénquima cerebral; en este caso, se recomienda un beta-lactámico(10). La doxiciclina en pauta corta (≤21 días) se puede utilizar independientemente de la edad del paciente(10,11). En la tabla III se detalla el tratamiento de la enfermedad de Lyme, según las últimas recomendaciones.
Fiebre botonosa mediterránea
Introducción, epidemiología y etiología
La fiebre botonosa mediterránea o fiebre exantemática mediterránea (FEM) es una zoonosis emergente y endémica en la cuenca del Mediterráneo. La sintomatología, a veces, es muy inespecífica, por lo que hay que sospecharla en pacientes con fiebre que hayan estado en áreas geográficas de riesgo. La incidencia es variable, se ha objetivado un aumento de esta en los últimos años, sobre todo en verano(12).
El agente causal de esta zoonosis es la Rickettsia conorii conorii (bacilo gram negativo, intracelular). Se ha descrito que el vector responsable de la infección es la garrapata marrón del perro (Rhipicephalus sanguineus). No está claro cuál es el reservorio principal de R. conorii, muchos autores postulan que se encuentra en perros y otros mamíferos (erizos, conejos y pequeños roedores), aunque también se ha descrito que la misma garrapata actúa como reservorio potencial de esta bacteria(12).
Manifestaciones clínicas
Las manifestaciones clínicas clásicas son: fiebre, exantema maculopapular y escara necrótica conocida como “mancha negra”.
Se caracteriza por la tríada clásica: fiebre, exantema maculopapular y una escara de inoculación en el sitio de la mordedura. La presencia de la escara característica, también conocida como mancha negra, es muy variable (29-60 % de los casos)(12). El exantema, generalmente, afecta a palmas y plantas, evitando zonas como la cara. Puede acompañarse de síntomas gastrointestinales, adenopatías (cervicales) y hepatoesplenomegalia, de forma más frecuente en la edad pediátrica, mientras que los adultos presentan cefalea, artralgias y mialgias. La duración de los síntomas suele ser de 12 a 20 días. No existe una forma crónica de la enfermedad, aunque hasta un 20 % de los pacientes pueden presentar complicaciones, sobre todo, enfermedades cardiacas(12).
Diagnóstico
La sensibilidad de las técnicas de diagnóstico directo es baja, siendo más elevada en el caso de biopsias.
• Diagnóstico directo. El cultivo no es rentable, debido a la naturaleza intracelular de la bacteria. Las técnicas de diagnóstico molecular (PCR) se pueden utilizar para muestras de sangre o tejido. La sensibilidad es muy baja y aumenta cuando se realiza en raspado o biopsia de la escara.
• Diagnóstico indirecto o serológico (IFI). Indican infección los títulos de IgM ≥64 e IgG ≥128, en zonas endémicas, o IgM ≥32 y títulos de IgG ≥64, en zonas no endémicas. Es necesario demostrar la seroconversión o aumento de títulos (x4) para poder confirmar la infección. Puede presentar reacciones cruzadas con otras Rickettsias.
Tratamiento
El tratamiento de elección es la doxiciclina a dosis de 2,2 mg/kg/12 horas para <45 kg y de 100 mg/12 horas en >45 kg, durante un mínimo de 5-7 días, siempre que se haya resuelto la fiebre en los tres días previos al fin del tratamiento. La azitromicina sería una alternativa al tratamiento con doxiciclina(12).
Enfermedades transmitidas por mamíferos
Enfermedad por arañazo de gato
La incidencia de la enfermedad por arañazo de gato es desconocida. Suele presentarse como linfadenopatía regional (axilar, cervical, epitroclear o inguinal) que puede resolverse de forma espontánea en meses. El diagnóstico principal es mediante técnicas moleculares.
Introducción, epidemiología y etiología
La enfermedad por arañazo de gato (EAG) está producida por Bartonella henselae. Los gatos, tanto domésticos como callejeros, son el reservorio natural de esta bacteria(13). La bacteriemia puede ocurrir en gatos aparentemente sanos y puede ser prolongada (semanas o meses). La infección se transmite a los humanos por mordeduras o arañazos, aunque también se ha descrito el contagio tras el contacto ocular o con heridas(14).
Se desconoce la incidencia real de la EAG, aunque se estima que se diagnostican 22.000 pacientes/año (EE.UU.), sobre todo en otoño e invierno(13). La edad de máxima incidencia es la comprendida entre los 5 y los 9 años(13,14).
Manifestaciones clínicas
La infección por B. henselae puede cursar de forma asintomática. Es característica la linfoadenopatía regional (suele ser: axilar, cervical, epitroclear o inguinal). Inicialmente, suele aparecer una pápula o pústula en la zona de inoculación y, a los 5-50 días, la linfoadenopatía, acompañada de eritema, tumefacción, calor y dolor de la piel circundante. En general, se resuelven de forma espontánea en 2-4 meses(13-15).
La EAG puede causar fiebre de origen desconocido (1-3 semanas), asociando síntomas inespecíficos, el más frecuente el dolor abdominal (>50 %)(13). Otras manifestaciones por diseminación hematógena son: endocarditis (cultivos negativos), lesiones osteolíticas, microabscesos en hígado o bazo, encefalopatía, glomerulonefritis, eritema nodoso, neurorretinitis y purpura trombocitopénica. La inoculación de la bacteria en el tejido ocular puede provocar el síndrome oculoglandular de Parinaud (conjuntivitis folicular y linfadenopatía preauricular homolateral).
Diagnóstico
• Diagnóstico directo: el cultivo es poco rentable, debido a las características de la bacteria(14). Por este motivo, se prefiere la detección mediante técnicas de diagnóstico molecular (PCR) de tejido o líquidos corporales.
• Diagnóstico indirecto, basado en técnicas serológicas: es la técnica más usada (IFI, ELISA). Puede ser negativa en pacientes con EAG y, además, tiene reactividad cruzada con B. quintana y otros microorganismos, por lo que hay que interpretarla con cautela.
Tratamiento
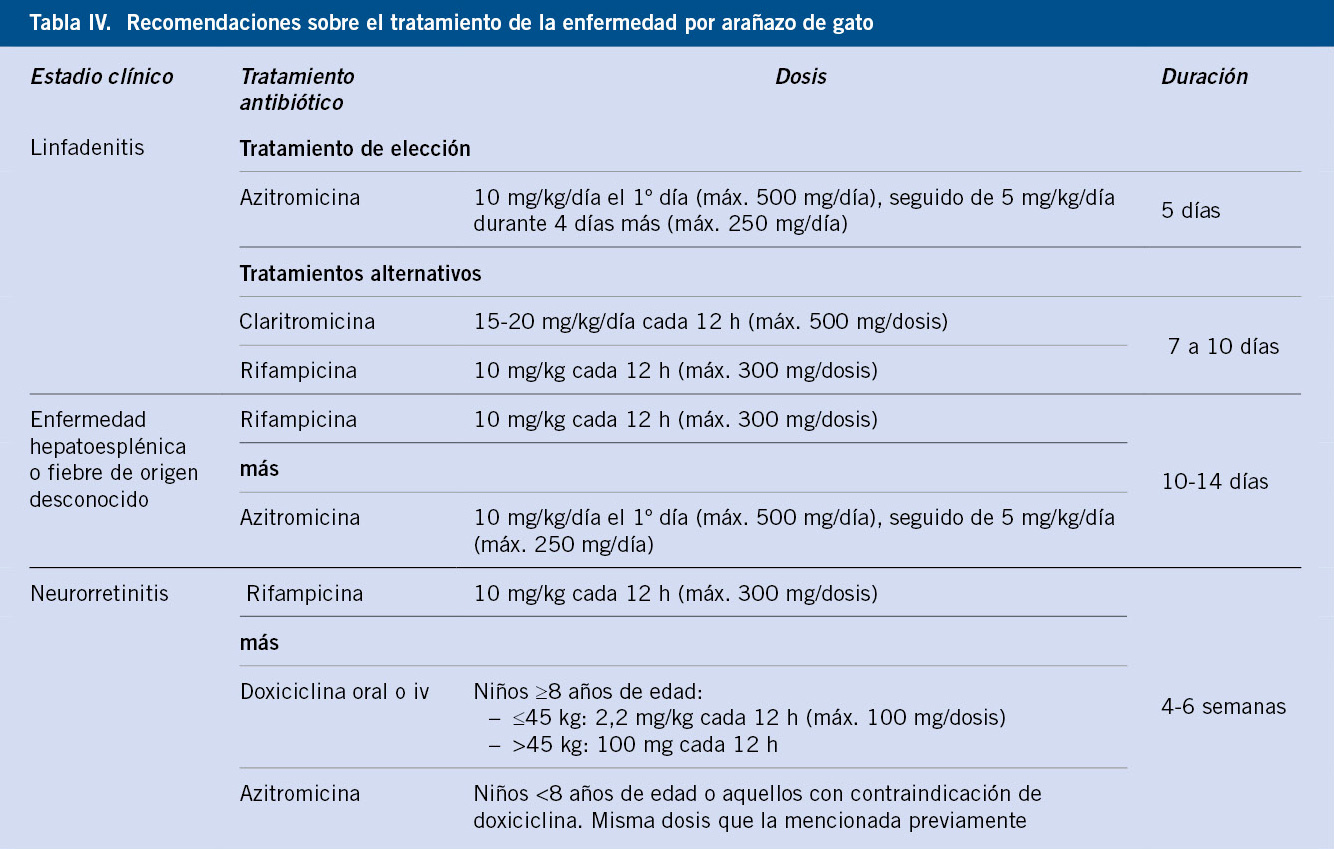
El valor del tratamiento antibiótico en pacientes con EAG típica (adenopatía regional) sigue siendo incierto, pero las últimas guías de la IDSA (Infectious Diseases Society of America) recomiendan utilizar antibiótico(15). No existen guías de tratamiento sobre la enfermedad sistémica, pero adjuntamos las recomendaciones expuestas en UpToDate(16) en inmunocompetentes (Tabla IV).
Para terminar, se incluyen otras enfermedades transmitidas por mamíferos que se exponen en la tabla V y transmitidos por vectores en la tabla VI.
Función del pediatra de Atención Primaria
Aunque la mayoría de los tratamientos de estas enfermedades se llevarán a cabo en el ámbito hospitalario, el pediatra de Atención Primaria es un pilar fundamental en la sospecha diagnóstica de las zoonosis. Los pacientes acuden a la consulta de Atención Primaria, en la mayoría de ocasiones, con síntomas inespecíficos y el pediatra tendrá que realizar una anamnesis detallada sobre exposiciones de riesgo: estancia en medios rurales, contacto con animales, viajes internacionales o viajes nacionales a áreas de riesgo, vacunación y/o tratamientos previos… Además, es necesario que el pediatra de Atención Primaria conozca cómo prevenir las mordeduras por garrapatas y sepa cómo retirarlas.
Conflicto de intereses
No hay conflicto de interés en la elaboración del manuscrito. Declaración de intereses: ninguno.
Bibliografía
Los asteriscos muestran el interés del artículo a juicio de las autoras.
1. Organización mundial de la Salud (OMS). Zoonosis. 2020. Disponible en: https://www.who.int/es/news-room/fact-sheets/detail/zoonoses.
2. Lipkin W. Zoonosis. En: Mandell, Douglas, Bennett. Enfermedades infecciosas. Principios y práctica. 9ª ed.: Elsevier; 2021. p. 3813-7.
3. Caminade C, McIntyre KM, Jones AE. Impact of recent and future climate change on vector-borne diseases. Ann N Y Acad Sci. 2019; 1436: 157-73.
4. Kimberlin DW, Brady MT, Jackson MA, Long SS. Red Book. Enfermedades Infecciosas en Pediatría. Informe 2021-2024 del Comité de Enfermedades Infecciosas. 32ª ed. EE.UU. Editorial Médica Panamericana; 2021. p. 468-72.
5. Melby PC. Nelson. Tratado de Pediatría. España: Elsevier. 2020; 311: 1839-44.
6. * Aronson N, Herwaldt BL, Libman M, Pearson R, López-Velez R, Weina P, et al. Diagnosis and Treatment of Leishmaniasis: Clinical Practice Guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH). Clin Infect Dis. 2016; 63: 1539-57.
7. Álvarez-Martínez MJ, Belhassen-García M, Flores-Chávez MD, Pérez de Ayala A, Sulleiro E. Diagnóstico de parasitosis importadas en España. Procedimientos en Microbiología Clínica. Sociedad Española de Enfermedades Infecciosas y Microbiología Clínica (SEIMC). 2020; 69: 12-8.
8. Amores Alguacil M, Estévez Reboredo R, Martínez de Aragón M, Carmona R, Cano Portero R. Carga hospitalaria de enfermedad de Lyme en España (2005-2019). Boletín Epidemiológico Semanal. Instituto de Salud Carlos III. 2022; 30: 01-10. Disponible en: https://revista.isciii.es/index.php/bes/article/view/1214.
9. Kimberlin DW, Brady MT, Jackson MA, Long SS. Red Book. Enfermedades Infecciosas en Pediatría. Informe 2021-2024 del Comité de Enfermedades Infecciosas. 32ª ed. EE.UU. Editorial Médica Panamericana; 2021. p. 482-9.
10.* Oteo JA, Corominas H, Escudero R, Fariñas-Guerrero F, García-Moncó JC, Goenaga MA, et al. Executive summary of the consensus statement of the Spanish Society of Infectious Diseases and Clinical Microbiology (SEIMC), Spanish Society of Neurology (SEN), Spanish Society of Immunology (SEI), Spanish Society of Pediatric Infectology (SEIP), Spanish Society of Rheumatology (SER), and Spanish Academy of Dermatology and Venereology (AEDV), on the diagnosis, treatment and prevention of Lyme borreliosis. Enferm Infecc Microbiol Clin (Engl Ed). 2023; 41: 40-5.
11.* Lantos PM, Rumbaugh J, Bockenstedt LK, Falck-Ytter YT, Aguero-Rosenfeld ME, Auwaerter PG, et al: Clinical practice guidelines by the Infectious Diseases Society of America (IDSA), American Academy of Neurology (AAN), and American College of Rheumatology (ACR): 2020 guidelines for the prevention, diagnosis, and treatment of Lyme disease. Arthritis Care Res (Hoboken). 2021; 73: 1-9.
12.* Spernovasilis N, Markaki I, Papadakis M, Mazonakis N, Ierodiakonou D. Mediterranean Spotted Fever: Current Knowledge and Recent Advances. Trop Med Infect Dis. 2021; 6: 172.
13. Han JY, Vijayan V, Long S. Pediatric Infectious Diseases. Sixth Edition. Elsevier; 2023. p. 901-5.
14. Kimberlin DW, Brady MT, Jackson MA, Long SS. Red Book. Enfermedades Infecciosas en Pediatría. Informe 2021-2024 del Comité de Enfermedades Infecciosas. 32ª ed. EE.UU. Editorial Médica Panamericana; 2021. p. 226-9.
15. Stevens DL, Bisno AL, Chambers HF, Dellinger EP, Goldstein EJ, Gorbach SL, et al. Practice guidelines for the diagnosis and management of skin and soft tissue infections: 2014 update by the infectious diseases society of America. Clin Infect Dis. 2014; 59: 147-59.
16. Spach DH, Kaplan SL, Treatment of cat scratch disease. Updated. 2021. Disponible en: https://www.uptodate.com/contents/treatment-of-cat-scratch-disease.
Bibliografía recomendada
– Guía de actuación ante picadura de garrapata. Ministerio de Sanidad y Servicios Sociales e Igualdad. 2016. Disponible en: https://www.sanidad.gob.es/profesionales/saludPublica/enfermedadesEmergentes/Crimea_Congo/docs/Guia_actuacion_picadura_garrapata_20161014.pdf.
Guía práctica sobre el abordaje de mordedura de garrapata. Incluye un algoritmo en el que se sintetiza los pasos a llevar a cabo. Además, una tabla que recoge de forma abreviada algunas de las enfermedades infecciosas transmitidas por las garrapatas, destacando los aspectos principales de cada una de ellas.
– Comité Asesor de Vacunas (CAV). Manual de inmunizaciones en línea de la Asociación Española de Pediatría. Encefalitis Japonesa. Cap. 23. 2020. Disponible en: https://vacunasaep.org/documentos/manual/cap-23#2.
La encefalitis japonesa es una enfermedad transmitida por garrapatas que afecta principalmente al continente de Asia. En este documento se resumen las indicaciones y pautas de vacunación frente a esta enfermedad. Además, de los aspectos principales sobre su clínica y epidemiología.
– Hills SL, Lindsey N, Fischer M. Japanese encephalitis. Centers for Disease Control and Prevention (CDC). En: CDC Yellow Book 2024. Disponible en: https://wwwnc.cdc.gov/travel/yellowbook/2024/infections-diseases/japanese-encephalitis.
En esta publicación del Instituto de Salud Pública de EE.UU. se recoge de forma más detallada las recomendaciones sanitarias sobre vacunación de la encefalitis japonesa, en función del destino y las circunstancias del viaje.
– Hills SL, Gould C, Cossaboom C. Tick-borne encephalitis (TBE) virus. Centers for Disease Control and Prevention (CDC). En: CDC Yellow Book 2024. Disponible en: https://wwwnc.cdc.gov/travel/yellowbook/2024/infections-diseases/tick-borne-encephalitis.
Publicación del Instituto de Salud Pública de EE.UU. que recoge de forma completa, la epidemiología de la encefalitis centroeuropea o “encefalitis transmitida por garrapatas” y las recomendaciones sobre su prevención en el viajero en función del destino y las circunstancias del viaje.
| Caso clínico |
|
Niño de 10 años que acude en verano a su pediatra de Atención Primaria por “bulto” doloroso en región axilar derecha. En los últimos 2 días, ha presentado fiebre asociada. No otra sintomatología. Antecedentes personales: calendario de inmunizaciones adecuado a la edad. Sin enfermedades ni ingresos previos. Exploración física: buen estado general. Bien hidratado y perfundido. Sin exantemas ni petequias. Adenopatía axilar derecha de 2 cm de diámetro, dolorosa a la palpación, asocia eritema circundante. Sin adenopatías en otras localizaciones. Resto de la exploración física normal.
|






 Rapid microbiological diagnostic test in the Primary Care Pediatric consultation
Rapid microbiological diagnostic test in the Primary Care Pediatric consultation