 |
| Regreso a las bases |
A. González Brabin, M.A. García Teresa, A. García-Salido
Unidad de Cuidados Intensivos. Hospital Infantil Universitario Niño Jesús. Madrid
| Resumen
La oxigenoterapia se define como el aporte de oxígeno a un paciente a una concentración mayor del aire ambiente. Se puede administrar en pacientes con ventilación mecánica o ventilación espontánea. El principal objetivo de la administración de oxígeno suplementario es tratar o prevenir la hipoxemia (PaO2 menor de 60 mmHg o saturación arterial de oxígeno menor al 90%). Tiene como objetivo evitar sus consecuencias (hipertensión arterial pulmonar, acidosis metabólica, poliglobulia e hipoxia tisular) y controlar la sintomatología, mediante la reducción del trabajo respiratorio y el trabajo miocárdico generados por la puesta en marcha de mecanismos compensatorios. |
| Abstract
Oxygen therapy is defined as the supply of oxygen to a patient at a concentration greater than 21%. It can be administered in patients with mechanical ventilation or spontaneous ventilation. The main objective of supplemental oxygen administration is to treat or prevent hypoxemia (PaO2 less than 60 mmHg or arterial oxygen saturation less than 90%). Its objective is to avoid its consequences (pulmonary arterial hypertension, metabolic acidosis, polyglobulia, and tissue hypoxia), and to control the symptoms, by reducing respiratory work and myocardial work generated by the start-up of compensatory mechanisms. |
Palabras clave: Hipoxemia; Oxígeno; Terapia.
Key words: Hypoxemia; Oxygen; Therapy.
Pediatr Integral 2021; XXV (1): 38 – 44
Oxigenoterapia
Introducción
La oxigenoterapia es el tratamiento fundamental de la hipoxemia e insuficiencia respiratoria. Su objetivo es lograr que la PaO2 sea superior a 60 mmHg y la SatO2 superior al 90-92%. Su eficacia se traducirá en una mejoría de los signos y síntomas asociados. También se observarán cambios gasométricos y en el valor continuo de la SatO2. Existen, en la actualidad, multitud de sistemas para su administración y diferentes parámetros empleados para la monitorización de la oxigenación. Se resumen y describen a continuación.
Historia de la oxigenoterapia
El origen de la oxigenoterapia, tal y como la conocemos hoy en día, surge en 1783, año en que se aplica por primera vez el oxígeno como fármaco. El responsable de tal avance fue el médico francés Caillens, empleándolo para uno de sus pacientes enfermo de tuberculosis.
Posteriormente, durante el siglo XIX y primera parte del XX, surgen numerosos avances e investigaciones. Destaca John Scott Haldane, considerado el padre de la fisiología respiratoria. Describió cómo el impulso respiratorio parecía estar regulado por la concentración de CO2 en sangre, y se centró en desarrollar métodos para el análisis de gases en sangre. Este autor define el llamado “efecto Haldane”. Mediante este efecto se describe la propiedad de la hemoglobina para modificarse estructuralmente en función del grado de oxigenación. La hipoxemia induce una mayor capacidad de la hemoglobina(1) para portar dióxido de carbono y, a la inversa, la hemoglobina oxigenada tiene una capacidad reducida para transportar CO2.
Posteriormente, en los años sesenta, surge la figura de Earl Campbell que se centró en desarrollar nuevos dispositivos de administración. Así, aplica el efecto Venturi sobre el diseño de sus dispositivos. Esto permitió mezclar oxígeno puro con el aire ambiente dentro de una máscara, permitiendo ajustar distintas concentraciones de oxígeno. Las primeras máscaras desarrolladas por Campbell permitían concentraciones desde el 24 hasta el 35% de oxígeno. Estas mascarillas de oxígeno se conocen en la actualidad como mascarillas Venturi.
Conceptos de interés
• FiO2: fracción inspiratoria de oxígeno. Hace referencia a la concentración de oxígeno del gas administrado al paciente. Se expresa en fracción de 1.
• Hipoxemia: bajo contenido de oxígeno en sangre arterial.
• Hipoxia: baja oxigenación tisular, las demandas de oxígeno no pueden ser satisfechas por los aportes.
• Anoxia: ausencia de oxigenación tisular.
• Ventilación: se determina a través de la PaCO2 (mmHg), cantidad de CO2 presente en sangre arterial. Aporta información sobre el intercambio gaseoso. El aumento de la PaCO2 se conoce como hipercapnia.
• Complianza: es la distensibilidad (propiedad que permite el alargamiento o distensión de una estructura) pulmonar determinada por su cambio de volumen con la presión del gas.
Parámetros respiratorios.
Monitorización y valores de normalidad
• Frecuencia respiratoria: número de respiraciones que se realizan por minuto. Los valores de normalidad varían en función de la edad, tal y como se muestra en la tabla I.
• Saturación de oxígeno: se puede medir gasométricamente o bien con ayuda de métodos fotoeléctricos (pulsioximetría). Los valores normales medidos mediante pulsioximetría varían entre el 95 y 99%.
• PaO2: presión parcial arterial de oxígeno. Para su medición, se requiere acceso a sangre arterial. Valores de normalidad: 80-100 mmHg en sangre arterial y 40 mmHg en sangre venosa (FiO2 0,21).
• Cociente PaO2/FiO2: proporciona un mayor grado de información respecto al parámetro previo. Relaciona la FiO2 necesaria para mantener una determinada presión arterial de oxígeno. A mayor PaO2 y menor el aporte de FiO2, más positiva será la relación, y refleja una menor gravedad del paciente. Clasificación del grado de hipoxemia según los siguientes valores: normal > 300; leve 300-200; moderado 100-200; y grave < 100 (pacientes con presión al final de la expiración –PEEP– >5 cm H2O).
• Índice de oxigenación (IO): valora la oxigenación en relación a la FiO2 y grado de asistencia respiratoria en ventilación mecánica invasiva. Para su cálculo, se requiere conocer la FiO2 y la presión media en la vía área o PMVA (ventilación mecánica invasiva). Clasificación del daño pulmonar según los siguientes valores: leve = 4 a 7,9; moderado = 8 a 15,9; y grave >= 16. Fórmula: IO = (FiO2 x PMVA en cm H2O) / PaO2.
• PaCO2: presión parcial arterial de CO2. Para su medición, se requiere acceso a sangre arterial. Valores de normalidad: 35-45 mmHg en sangre arterial y 45-50 mmHg en sangre venosa.
Valoración del estado de oxigenación
Existen diferentes parámetros usados para valorar los distintos componentes de la oxigenación, distinguiéndose el transporte y capacidad de cesión, y consumo de oxígeno.
Transporte de oxígeno
El oxígeno no se disuelve fácilmente en el agua, y dado que el plasma es un 93% agua, para facilitar la oxigenación se requiere de una molécula que lo transporte: la hemoglobina.
• PaO2: permite medir de forma indirecta la cantidad de oxígeno disuelto en el plasma.
• Saturación arterial de oxígeno (SatO2): refleja la proporción de hemoglobina oxigenada respecto a la hemoglobina total en sangre.
• Contenido arterial de oxígeno: resulta de la suma del oxígeno disuelto en plasma y del unido a hemoglobina, en sangre arterial.
• Contenido venoso de oxígeno: resulta de la suma del oxígeno disuelto en plasma y del unido a hemoglobina, en sangre venosa.
Aporte o distribución de oxígeno (AO2)
El oxígeno pasa a la sangre en el circuito pulmonar, y es transportado a los órganos a través del flujo de sangre, es decir, el gasto cardiaco (Q). El ritmo con el que esto ocurre se denomina aporte de oxígeno(2), y describe el volumen de oxígeno que alcanza los capilares sistémicos cada minuto.
Captación de oxígeno (VO2)
Cuando la sangre alcanza los capilares sistémicos, el oxígeno se disocia de la hemoglobina y es cedido a los tejidos. El ritmo con el que esto sucede se denomina captación y describe el volumen de oxígeno (ml) que abandona el lecho capilar y se desplaza a los tejidos cada minuto.
• Proporción de extracción de oxígeno: fracción de oxígeno proporcionado a los capilares que es captada por los tejidos.
• Saturación venosa mixta (SvO2): refleja la extracción tisular de oxígeno por parte de los tejidos. Para su correcta medición, se debe disponer de un catéter venoso central cuyo extremo distal se encuentre en aurícula derechapara que la muestra sea representativa (punto donde se mezcla el flujo de sangre que proviene de la vena cava inferior y superior).
En la tabla II, se describe la forma de calcular los distintos parámetros comentados, así como los valores de normalidad.
Indicaciones de oxigenoterapia
El principal objetivo de la administración de oxígeno suplementario es tratar o prevenir la hipoxemia (PaO2 menor de 60 mmHg o saturación arterial de oxígeno menor al 90%).
Tiene como objetivo evitar sus consecuencias (hipertensión arterial pulmonar, acidosis metabólica, poliglobulia e hipoxia tisular) y controlar la sintomatología, mediante la reducción del trabajo respiratorio y el trabajo miocárdico generados por la puesta en marcha de mecanismos compensatorios.
Patología aguda
• Enfermedades pulmonares: provocan una situación de hipoxemia-hipoventilación debido a la alteración en la relación ventilación-perfusión (neumonía, bronquiolitis…), hipoventilación alveolar.
• Enfermedades cardíacas: patologías que condicionan cortocircuito derecha-izquierda (cardiopatías cianosantes).
• Enfermedades infecciosas: situaciones de bajo gasto cardíaco o alta demanda de oxígeno (shock, sepsis…), condicionando una situación de hipoxia tisular sin hipoxemia.
Patología crónica
• Enfermedades pulmonares: hipertensión pulmonar, enfermedades parenquimatosas, fibrosis pulmonar y displasia broncopulmonar.
• Enfermedades cardíacas con hipertensión pulmonar.
• Enfermedades neuromusculares, de la pared torácica, obstrucción de la vía aérea superior.
Complicaciones de la oxigenoterapia
• Retinopatía proliferativa en pacientes neonatos prematuros.
• Toxicidad pulmonar: secundaria a la disminución de la síntesis de surfactante, alteraciones en la relación ventilación-perfusión y disminución de la actividad mucociliar, favoreciendo la formación de atelectasias.
• Depresión del centro respiratorio.
Sistemas de aporte de oxígeno
La oxigenoterapia se puede administrar tanto en pacientes con ventilación mecánica (invasiva o no invasiva) como en ventilación espontánea. En ventilación espontánea, los diferentes tipos de soporte respiratorio se clasifican de acuerdo al flujo administrado, diferenciando dos grupos: sistemas de bajo y alto flujo(7).
Sistemas de bajo flujo
Suministran O2 puro (100%) a un flujo menor que el pico de flujo inspiratorio del paciente. El O2 administrado se mezcla con el aire inspirado y, se obtiene una FiO2 variable, dependiente del flujo administrado y del volumen inspiratorio.
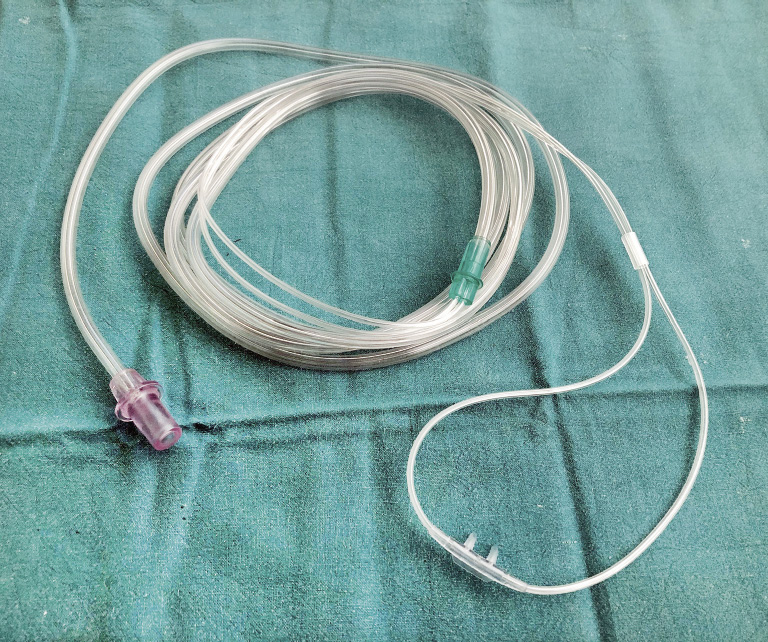
Oxigenoterapia en cánula o gafas nasales
Es la modalidad más empleada. Son ligeras y cómodas (Fig. 1).
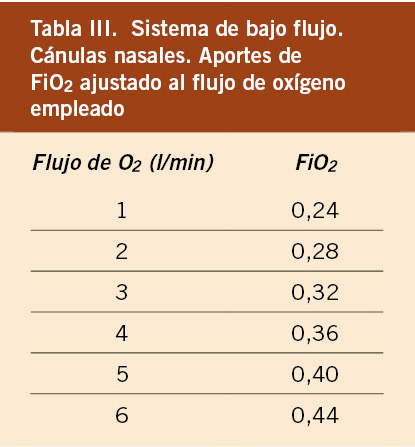
Suministra una FiO2 variable (desde 0,24 a 0,44) en función del flujo utilizado (Tabla III).
Su eficacia disminuye en respiradores bucales o durante el sueño. En recién nacidos, el flujo a través de este dispositivo se debe restringir a 2 l/min, y en pediátricos hasta 4 l/min.
No se aconseja la utilización de este tipo de cánulas cuando son necesarios flujos superiores a 6 l/min, debido a que flujos mayores a través de este dispositivo ocasionan irritación de la mucosa nasal y no aumentan la FiO2.
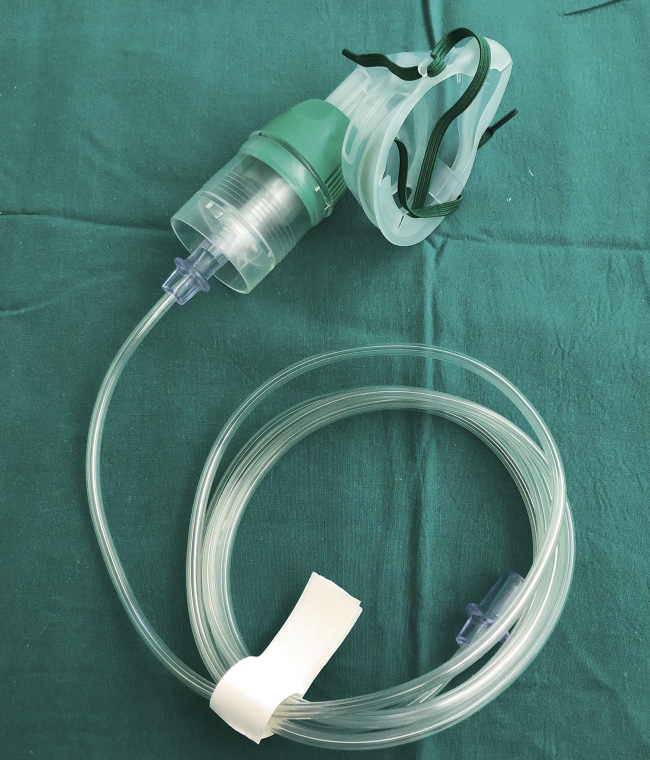
Mascarilla simple de oxígeno
Se trata de una mascarilla que cubre boca y nariz. Dispone de 2 orificios laterales por donde entra el aire ambiente y sale el aire espirado (Fig. 2).
Requiere de un flujo de O2 entre 4-10 l/min. No dispone de bolsa reservorio. Aporta una FiO2 variable entre 0,3 y 0,5.
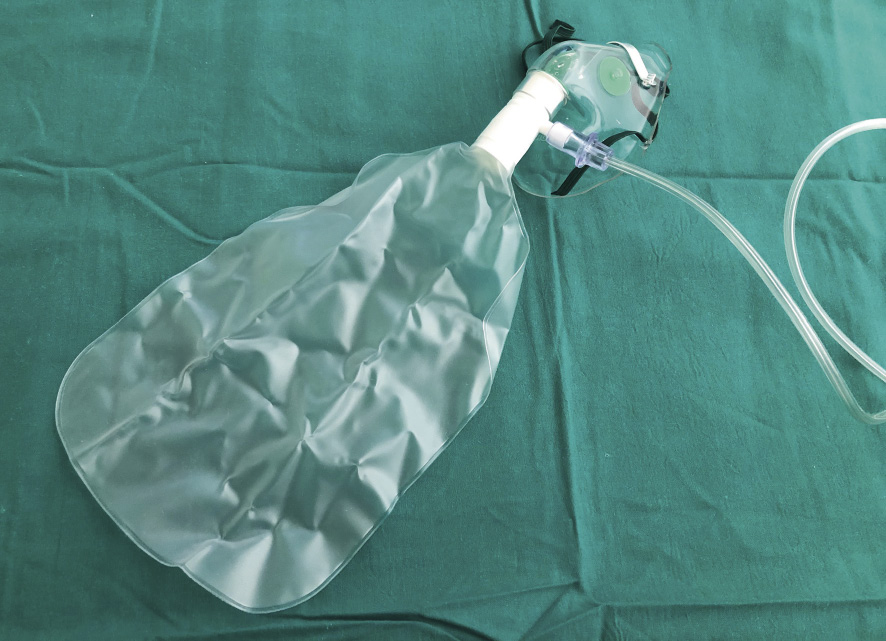
Mascarilla con reservorio
Se trata de una mascarilla que cubre boca y nariz, que lleva asociada una bolsa reservorio en la parte frontal de la misma (Fig. 3).
Se debe asegurar un flujo suficiente (entre 10 y 15 l/min) para llenar el reservorio y evitar su colapso durante la inspiración.
Dispone de orificios laterales en la mascarilla, que permite la salida de aire durante la espiración, evitando así su reinhalación. Estos orificios permanecen cerrados durante la inspiración para evitar la entrada de aire ambiente. Este dispositivo permite administrar FiO2 más elevadas, entre 0,6-0,9.
Sistemas de alto flujo(3,8,9)
El flujo administrado al paciente es suficiente para proporcionar la totalidad del gas inspirado, independientemente del patrón respiratorio del paciente, permitiendo con ello regular de forma más exacta la FiO2 administrada.
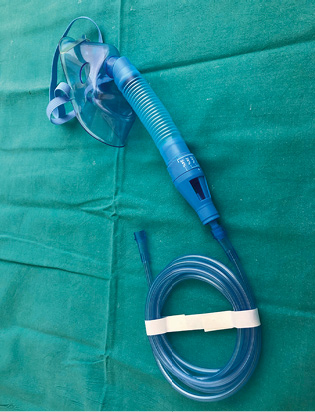
Mascarilla Venturi
Se trata de una mascarilla que cubre boca y nariz, que lleva asociado un mecanismo regulador de FiO2. El oxígeno y el aire se mezclan en este mecanismo que se ajusta en función de la concentración de oxígeno deseada (Figs. 4 y 5).
El flujo de oxígeno a alta velocidad arrastra aire del exterior hacia el interior del regulador (efecto Venturi). Cada dispositivo, en función del modelo comercializado, dispone de una tabla orientativa para ajustar el flujo de oxígeno.
Oxigenoterapia de alto flujo con cánulas nasales(4)
Administración de un flujo elevado de aire mezclado con oxígeno, u oxígeno puro a través de un dispositivo de cánulas nasales específicas (Fig. 6).
La FiO2 a administrar se ajustará mediante el dispositivo mezclador (Fig. 7).
Si no se dispone de un mezclador, se puede administrar mezclando dos caudalímetros, uno de aire y otro de O2, calculando la concentración de O2 con la siguiente fórmula: FiO2 = O2 (l/min) + aire (l/min) x 0,21) / O2 (l/min) + aire (l/min).
Dada la facilidad de uso y la buena adaptación que suele acompañar a este tipo de oxigenoterapia, su uso se ha visto extendido en los últimos años. Su indicación debe acompañarse de un seguimiento estrecho que confirme la buena respuesta e impida el retraso de otros tipos de asistencia.
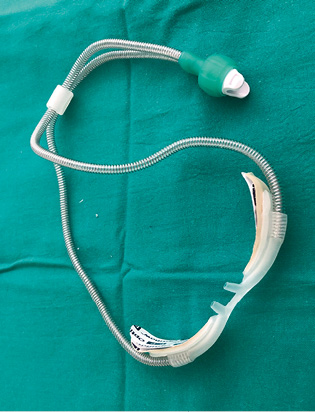
Para el uso de alto flujo en cánulas nasales, es indispensable humidificar y calentar el aire (Fig. 8).
Se debe comenzar con flujos bajos, en torno a 0,5-1 l/kg/min. Posteriormente, ir aumentando en función de las necesidades del paciente, y también de la tolerancia, hasta un máximo en torno a 1,5-2 l/kg/min. En la tabla IV aparece el flujo máximo por rango de edad.
Este sistema mejora la oxigenación del paciente, dado que el flujo de aire administrado es superior al pico de flujo inspiratorio del paciente, evitando teóricamente la inhalación de aire ambiente. Permite, además, renovar el gas del espacio muerto en nasofaringe.
Destaca en su uso que, a mayor flujo pautado peor tolerancia por parte del paciente. Esto suele limitar la eficacia del dispositivo. Otro limitador importante es el tamaño de la cánula nasal seleccionado, que puede restringir al flujo administrado (se debe elegir la cánula nasal adecuada en función de la edad y del flujo que se desee pautar).
Ventilación mecánica no invasiva(6-9)
Se trata de un nivel de asistencia mayor que lo previamente descrito. Se considera ventilación no invasiva (VNI) al tratamiento que no invade la vía aérea del paciente; por tanto, no supone la intubación endotraqueal o la traqueotomía. Existen diferentes modalidades, pero la más empleada es aquella que hace uso de presión positiva (modalidades de presión). Los dispositivos empleados para la ventilación hacen uso del gradiente de presión entre el dispositivo y las unidades alveolares del paciente, y es a través de este gradiente que consigue movilizar un determinado volumen de gas.
Este sistema de ventilación permite regular la FiO2 administrada para optimizar el estado de oxigenación del paciente. Se debe asegurar que el volumen corriente en cada respiración es suficiente para llevar a cabo un adecuado intercambio gaseoso, permitiendo con ello la oxigenación y el intercambio de PCO2.
Habitualmente, se buscan volúmenes en torno a 4-6 ml/kg en lactantes y volúmenes en torno a 6-8 ml/kg en edad pediátrica. Se debe tener en cuenta que la ventilación no invasiva tiene como principal inconveniente la no tolerancia del paciente y las fugas, que pueden llegar a condicionar su eficacia (no es un circuito hermético).
Cuando se emplea la ventilación no invasiva, es fundamental humidificar y calentar el aire que se administra. La ausencia de humedad puede hacer más secas las secreciones, dificultando la movilización de las mismas con el consecuente agravio para el paciente.
Indicaciones de ventilación no invasiva
• Insuficiencia respiratoria aguda(5): se distingue la forma hipoxémica, en la que se produce un fracaso en el intercambio de gases por afectación parenquimatosa pulmonar (p. ej.: neumonía, edema pulmonar cardiogénico, distrés respiratorio), y la forma hipercápnica, causada por el fracaso de la bomba respiratoria. Se iniciará soporte respiratorio con VNI en aquellos pacientes con deterioro respiratorio pese al tratamiento con las modalidades previamente descritas. Debe considerarse como primer nivel de asistencia en situaciones de debilidad neuromuscular o situación de dificultad respiratoria grave, en las que se requiera participación activa en la inspiración y espiración. El uso de este soporte permite asistir al paciente, disminuyendo el trabajo respiratorio y mejorar los parámetros de oxigenación.
• Insuficiencia respiratoria crónica: enfermos con patología respiratoria de larga evolución, enfermedades neuromusculares, anomalías en el sistema nervioso central. En este grupo de pacientes, el uso de la VNI es una medida de soporte a largo plazo.
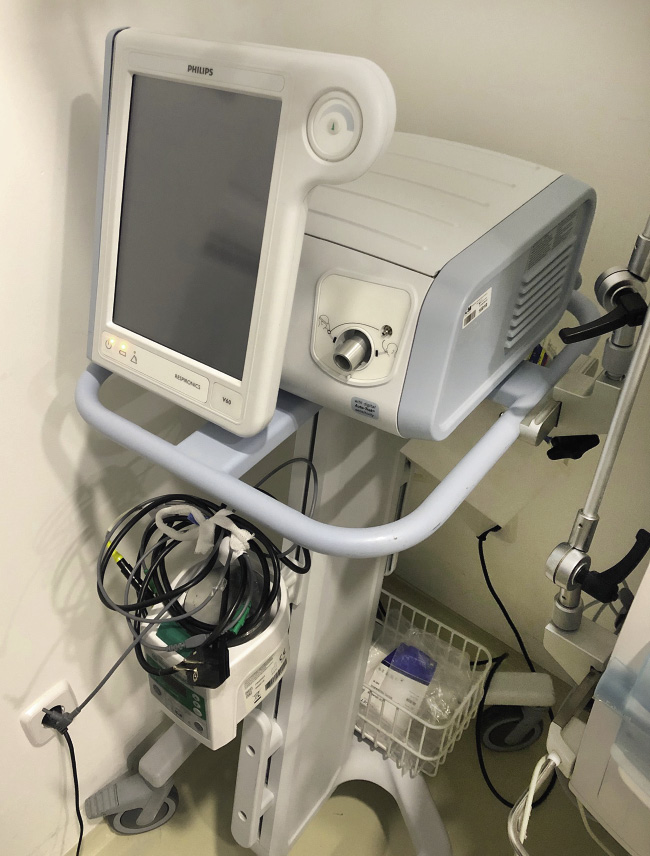
Dispositivos de administración de ventilación no invasiva
• Hospitalario: es recomendable el uso de dispositivos específicos con sistemas de flujo continuo de turbina, que permiten compensar las fugas (Fig. 9).
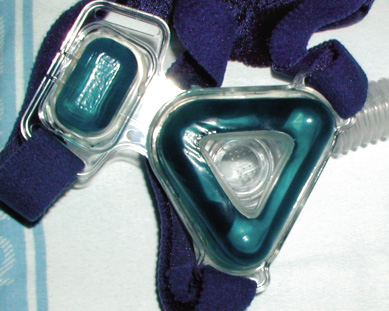
En ambos, se requiere de una interfase, que puede ser: facial (ocupando boca y nariz), nasal o bucal que se debe ajustar al paciente (Figs. 10 y 11).
Se pueden emplear respiradores de ventilación invasiva que dispongan de módulo de ventilación no invasiva. Sin embargo, este tipo de dispositivos no suelen realizar una compensación adecuada de las fugas del circuito.
• Domiciliario: como los comentados previamente, son respiradores específicos con funcionamiento mediante turbina, pero de pequeño tamaño (Fig. 12).
Disponen de modalidades de presión soporte, gran sensibilidad en el trigger inspiratorio/espiratorio (capacidad de detectar el flujo respiratorio del paciente) y capacidad de compensar las fugas del circuito. No disponen de mezclador de gases, por lo que si el paciente precisa oxígeno suplementario, se debe conectar una fuente externa mediante un sistema con alargadera.
Ventilación mecánica invasiva(6)
La ventilación mecánica invasiva (VMI) requiere de la intubación orotraqueal, nasotraqueal o traqueotomía/traqueostomía, que permite aislar la vía aérea (circuito cerrado).
Requiere de respiradores específicos designados para ello. Cuando se emplea este soporte, también es fundamental humidificar y calentar el aire que se administra al paciente.
Indicaciones
• Insuficiencia respiratoria grave por aumento de las resistencias de la vía área o por patología en el parénquima pulmonar, cuando la VNI ha fracasado. La decisión de iniciar depende de la situación clínica del paciente (trabajo respiratorio, nivel de conciencia) y de las alteraciones gasométricas (hipoxemia, saturación de O2 < 90% a pesar de FiO2 > 0,6; o hipercarpnia, PCO2 > 70 mmHg y pH < 7,20).
• Shock de cualquier etiología, en el que la demanda de oxígeno no se suple con los aportes.
• Disfunción del SNC, ocasionando: pausas centrales y/o el cese de la respiración. Disminución del nivel de conciencia, secundario a intoxicaciones, infecciones del sistema nervioso central o traumatismo craneoencefálico.
Los objetivos son conseguir una adecuada oxigenación y ventilación del paciente, disminuir el trabajo respiratorio y el consumo de oxígeno (sistémico y miocárdico).
Tipos de asistencia y modalidades de ventilación invasiva
El inicio de la ventilación invasiva requiere elegir el tipo de asistencia que el paciente precisa. Se puede optar por una ventilación controlada, en la que el paciente no interviene, siendo todos los ciclos respiratorios iguales, o bien por una ventilación asistida, donde se soporta la respiración iniciada por el paciente, siendo los ciclos respiratorios diferentes entre sí. Existen modalidades intermedias que no son objeto de este capítulo.
Elegir una modalidad u otra dependerá del contexto y la gravedad del paciente. La ventilación controlada permite un alivio en la bomba respiratoria para los pacientes más graves y requiere de un óptimo estado de sedación-analgesia (asociado o no a relajante muscular).
Decidido el tipo de asistencia, se debe elegir el modo de ventilación, diferenciando modalidades de: volumen, presión y mixtas.
• Ventilación por volumen: se pauta volumen, frecuencia respiratoria y un tiempo inspiratorio con pausa inspiratoria. Esta última permite que el volumen se distribuya de la forma más homogénea posible en las unidades alveolares, con distinta distensibilidad. La presión requerida para administrar el volumen es variable, dependiente de la resistencia y de la distensibilidad del circuito, y parénquima pulmonar. Durante la inspiración se administra el gas con un flujo constante. Esta modalidad disminuye el riesgo de hiperventilación/hipoventilación.
• Ventilación por presión: en esta modalidad se programa la presión deseada en inspiración y espiración. El volumen administrado depende de la presión, del tiempo inspiratorio, y de la distensibilidad (complianza) del parénquima pulmonar. Emplea un flujo decelerado, porque disminuye a medida que lo hace el gradiente de presión. Genera, por tanto, menor riesgo de barotrauma, una mejor distribución del aire dentro y facilita un adecuado reclutamiento alveolar. Sin embargo, tiene riesgo de hiperventilación/hipoventilación al no asegurar el volumen.
• Ventilación en modalidades mixtas, como volumen control regulado por presión. Es una modalidad de ventilación por presión con volumen garantizado, en la que se pauta un volumen y el respirador calcula en cada respiración la mínima presión necesaria para meter ese aire en el circuito respiratorio.
Bibliografía
1. Needleman JP, Setty BN, Varlotta L, Dampier C, Allen JL. Measurement of hemoglobin saturation by oxygen in children and adolescents with sickle cell disease. Pediatr Pulmonol. 1999; 28: 423.
2. Myers TR, American Association for Respiratory Care (AARC). AARC Clinical Practice Guideline: selection of an oxygen delivery device for neonatal and pediatric patients-2002 revision & update. Respir Care. 2002; 47: 707.
3. Pilar Orive FJ, López Fernández YM. Oxigenoterapia de alto flujo. An Pediatr Contin. 2014; 12: 25-9.
4. Spentzas T, Minarik M, Patters AB, Vinson B, Stidham G. Children with respiratory distress treated with high-flow nasal cánula. J Intensive Care Med. 2009; 24: 323-328.
5. Najaf-Zadeh A, Leclerc F. Noninvasive positive pressure ventilation for acute respiratory failure in children: a concise review. Ann Intensive Care. 2011; 1: 15.
6. Popat B, Jones A. Invasive and noninvasive mechanical ventilation. Medicine (Baltimore). 2012; 40: 298.
7. Amaddeo A, Khirani S, Griffon L, Teng T, Lanzeray A, Fauroux B. Non-invasive Ventilation and CPAP Failure in Children and Indications for Invasive Ventilation. Front Pediatr. 2020; 8: 544921. doi: 10.3389/fped.2020.544921.
8. Cataño-Jaramillo ML, Jaramillo-Bustamante JC, Florez ID. Continuous Positive Airway Pressure vs. High Flow Nasal Cannula in children with acute severe or moderate bronchiolitis. A systematic review and Meta-analysis. Med Intensiva.2020; S0210-5691: 30324-7. doi: 10.1016/j.medin.2020.09.008.
9. Slubowski D, Ruttan T. High-flow nasal cannula and noninvasive ventilation in pediatric emergency medicine. Review Pediatr Emerg Med Pract. 2020; 17: 1-24.









 Persistent cough
Persistent cough