|
| Temas de FC |
D. Infante Pina
Unidad de Gastroenterología y Nutrición Infantil. Hospital Universitario General de Catalunya. Grupo Quirónsalud. Barcelona
| Resumen
Estudios longitudinales prospectivos revelan que hasta un 24% de preescolares y adolescentes presentan dolor abdominal crónico y recidivante (DAR). A la hora de enfocar el diagnóstico se debe de huir de esas listas interminables, de algunos tratados, en los cuales se juntan, dentro del diagnóstico diferencial, causas muy habituales de morbilidad mínima, junto a patologías graves o complejas de escasa incidencia. Una revisión personal de 800 casos que consultaron por DAR, mostró que un 98% se localizaban en el tubo digestivo y de los mismos un 70% fueron catalogadas como orgánicas y un 30% de origen funcional. Solo un 5% de las orgánicas fueron causas graves. Un enfoque racional del abordaje debe efectuarse partiendo de una historia clínica detallada que, en la mayoría de los casos, nos orientará sin necesidad de efectuar estudios amplios y costosos. En el presente artículo, se abordan las causas más frecuentes del DAR, mecanismo fisiopatológico, sintomatología, pruebas para el diagnóstico y enfoque terapéutico.
|
| Abstract
Prospective longitudinal studies reveal that up to 24% of preschoolers and adolescents have chronic and relapsing abdominal pain (ARD). At the time of approaching the diagnosis, one must flee from those endless lists, from some treaties, in which very common causes of minimal morbidity are combined within the differential diagnosis, together with serious or complex pathologies of scarce incidence. A personal review of 8oo cases that consulted with ARD showed that 98% were located in the digestive tract and 70% of those were labeled as organic and 30% of functional origin. Only 5% of the organic ones were serious causes. A rational approach should be made based on a detailed clinical history that in most cases will guide us without the need for extensive and costly studies. In the present article the most frequent causes of the ARD, physiopathological mechanisms, symptomatology, tests for the diagnosis and therapeutic approach are discussed. |
Palabras clave: Infancia y adolescencia; Dolor abdominal crónico; Dolor abdominal recurrente; Dolor abdominal funcional.
Key words: Childhood and adolescence; Chronic abdominal pain; Recurrent abdominal pain; Functional abdominal pain.
Pediatr Integral 2019; XXIII (7): 339–347
Dolor abdominal crónico y recurrente
Introducción
Estudios longitudinales prospectivos revelan que hasta un 30% de los niños y adolescentes presentan episodios de dolor abdominal. No todos son organicidades, y un nuevo concepto dentro de las etiologías ha hecho su aparición: dolor abdominal de origen funcional.
Han pasado 40 años desde que John Apley nos dio su versión del dolor abdominal crónico y recurrente en la infancia (DAR)(1), definiéndolo como: “Aquel dolor que se presenta de una manera repetida durante semanas o meses, interfiriendo en el comportamiento del niño, pudiendo estar en plena normalidad entre los episodios. El tipo de dolor varía de unos niños a otros, puede ser de tipo vago o localización variable y descripción compleja”. Dicha definición, aunque con algunos matices, sigue siendo referenciada, pero en la actualidad, el DAR no se considera un diagnóstico, sino la descripción de un síntoma. Estudios longitudinales prospectivos revelan que hasta un 30% de los niños y adolescentes presentan, al menos, un episodio de dolor abdominal semanal (datos muy variables según estudios) y hasta en el 24% de los niños, este dolor se prolonga más de 8 semanas. Un hecho destacable es el aumento de la incidencia, lo cual no puede ser debido a un aumento de organicidades, sino al cambio de los estilos de vida de nuestros escolares y adolescentes en cuanto a las dietas, y al aumento del estrés y conflictividad de la vida moderna. Un nuevo concepto dentro de la categorización del DAR ha hecho su aparición dentro de las posibles etiologías y muy unido al comentario anterior, el dolor abdominal recidivante de origen funcional (DARF)(2,3) que se define como: “una combinación variable de síntomas gastrointestinales crónicos o recurrentes, no explicados por alteraciones bioquímicas o estructurales, siendo todos los exámenes que se efectúan negativos”. Paralelamente a la angustia familiar, alteración del ritmo escolar o vida cotidiana, está la preocupación del médico ante la etiología del DAR, las pruebas diagnósticas que debe solicitar y el pronóstico del proceso, ya que con frecuencia se busca una etiología orgánica.
Enfoque racional del DAR
Para un enfoque racional, es necesario basarnos en la “medicina basada en la evidencia”; es decir, ser buenos clínicos valorando atentamente los datos de la historia clínica antes que pensar en amplitud de exploraciones.
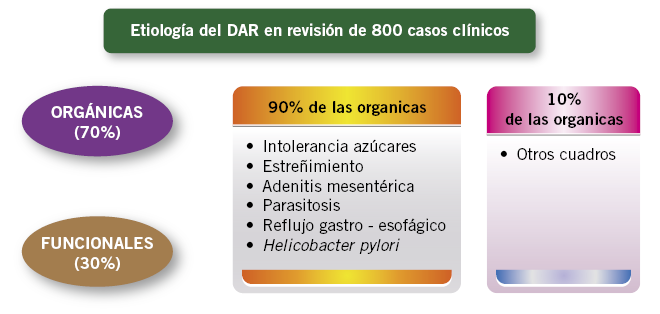
A la hora de enfocar el diagnóstico, se debe de huir de esas listas interminables, de algunos tratados, en los cuales se juntan, dentro del diagnóstico diferencial, causas muy habituales de morbilidad mínima, junto a patologías graves o complejas de escasa incidencia. Casi todas las causas orgánicas graves “suelen dar la cara”, se acompañan de síntomas relevantes y no suelen consultar como un cuadro crónico, en ocasiones de 1-2 años de duración. En la figura 1, podemos ver la clasificación etiológica de una revisión personal de 800 casos que consultaron por DAR(4).
Figura 1. Etiología del dolor abdominal crónico y recurrente (DAR) en revisión de 800 casos clínicos.
De ellos un 98% se localizaban en el tubo digestivo, aunque hablemos de dolor abdominal y no de dolor intestinal. Para un enfoque racional es necesario basarnos en la “medicina basada en la evidencia”; es decir, ser buenos clínicos valorando atentamente los datos de la historia clínica (Tabla I) en su más amplio contexto, antes que pensar en pedir un sinfín de exploraciones(5,6).
La exploración física será el siguiente escalón en el cual deberemos apoyarnos, si bien, por lo general, suele dar poco de sí. Las pruebas diagnósticas deberán orientarse, en primer lugar, en confirmar un diagnóstico concreto “si hay síntomas de sospecha o certeza”. Si en la historia clínica no hay ningún síntoma orientativo específico (DAR “sin materia”), sí que será obligado hacer un estudio general para encontrar posible organicidad o en su defecto catalogarlo de funcional (Tabla II).
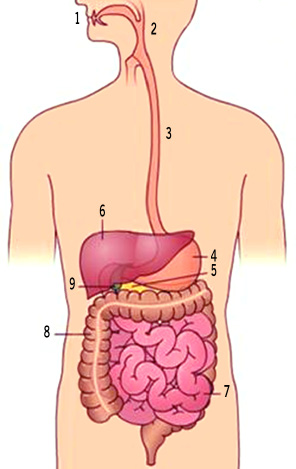
En este trabajo, nos centraremos en la descripción y manejo terapéutico de las causas más frecuentes del DAR, escalonado a la localización del mismo (Fig. 2) para facilitar el enfoque diagnóstico. Los niños y adolescentes colaboran perfectamente en referir la zona afecta, así como en la descripción de síntomas acompañantes.
Figura 2.
Localización abdominal según aparatos del dolor abdominal crónico y recurrente (DAR).
Aparato digestivo:
1. Boca – 2. Faringe – 3. Esófago
4. Estómago – 5. Páncreas
6. Hígado – 7. Intestino delgado
8. Intestino grueso – 9. Vesícula biliar
DAR zona epigastrio
Esofagitis por reflujo gastroesofágico
Suelen existir antecedentes de reflujo en época neonatal. El diagnóstico se efectúa mediante tránsito y el tratamiento con dieta sin irritantes e inhibidores bomba protones.
La esofagitis es debida a la incontinencia del cardias y producida por el contacto del ácido clorhídrico gástrico con la mucosa esofágica. Suelen aquejar un dolor en zona epigástrica, puntualmente cardial, acompañado de: pirosis, disfagia, náuseas o sensación de regurgitación. Con frecuencia, dicho dolor se presenta matutino y acompañado de anorexia. Entre los antecedentes existe casi siempre, el dato de regurgitaciones y vómitos en la época del lactante. Se trata de pacientes en los cuales desapareció la clínica alrededor de los 18-24 meses de vida, lo cual no presupone el cerrado adecuado del cardias. El desencadenante de la clínica puede ser una situación de estrés, que aumenta la secreción ácida o bien dietas que favorezcan un aumento de dicha secreción o relajación del cardias, como son: exceso de cacao, rico en xantinas; menta; bebidas gaseosas; alimentos muy ácidos, como cítricos y tomate, o muy grasos; café; alcohol; y mostaza o salsas picantes en caso de adolescentes. Un tránsito esofágico puede ser suficiente para confirmar nuestra sospecha diagnóstica. La fibroendoscopia está indicada cuando queramos visualizar el grado de esofagitis en aquellos casos de evolución tórpida. El tratamiento deberá hacerse con dieta de protección de secreción acida, evitando los alimentos mencionados. También se recomienda el tratamiento posicional, elevando la cama unos 30-40 cm. En la actualidad, es una práctica ya consensuada el uso de inhibidores de bomba de protones a dosis de 1 mg/kg/24 h (máximo 40 mg/día) mínimo 14 días. En función de la gravedad o evolución, puede asociarse un procinético como la Domperidona (Motiliun®) a dosis de 1 mg/kg/día repartido en tres dosis, que favorece el aclaramiento esofágico, haciendo que el contenido gástrico acorte su permanencia en el esófago. En casos de esofagitis importantes (fibroendoscopia), estaría indicado el Ziverel®, una asociación de ácido hialurónico y sulfato de condroitina, capaz de ejercer un mecanismo de protección de la mucosa esofágica.
Infección por Helicobacter Pylori
La prevalencia es cercana al 30%, pero es importante constatar que solo deben ser tratados aquellos pacientes con lesiones de la mucosa gástrica.
La infección por Helicobacter Pylori (HP) es muy frecuente, estimándose la prevalencia en edad pediátrica, según los estudios, en un 20% en nuestro medio, llegando al 60% en países subdesarrollados. Es frecuente que todos los miembros de una familia estén infectados por el mismo serotipo. El nicho natural de HP es la mucosa gástrica, si bien, se describe su presencia en otras zonas del tracto digestivo, como esófago y duodeno. No todos los infectados por este germen desarrollan cambios histológicos sugestivos de gastritis crónica o úlcera, y a menudo están asintomáticos. La infección sintomática puede manifestarse por dolor de localización claramente epigástrica, ocasionalmente tan intenso como para provocar despertar nocturno. En otros casos, la sintomatología es más vaga con: sensación de plenitud postpandrial, hinchazón, náuseas, eructos o vómitos(6,7). Puede constatarse, en casos graves, anemia ferropenia refractaria al tratamiento, con pérdidas ocultas de sangre en heces. La halitosis es un dato patognomónico de su presencia, dada la producción de amoniaco por el germen al descomponer la urea proteica de los alimentos. Los últimos datos aportados por el Registro Pediátrico Europeo (Grupo de trabajo de Sociedad Europea de Gastroenterología, Hepatología y Nutrición Infantil [ESPGHAN] del 2018) según hallazgos fibroendoscópicos en 934 pacientes con HP, revelaron que la úlcera péptica gástrica o duodenal es rara en pacientes pediátricos sintomáticos (5,7%), mientras que las gastritis sin úlcera se encuentran con mayor frecuencia (14,6%). El consenso internacional refiere que solo los pacientes “con lesión demostrada” deben ser tratados. Esto nos obligaría en caso de diagnosticar un paciente con síntomas “suficientes” de infección sintomática, indicar una fibroendoscopia. En la actualidad, no se utiliza ya la prueba serológica, basaba en la detección de anticuerpos Ig G frente a H. pylori en suero que podían indicar infección pasada, pero no activa. La prueba más aceptada, por su sencillez, inocuidad y fiabilidad es el test respiratorio de urea marcada con el isótopo estable C13. También es útil, la detección antigénica de HP en heces por técnicas de inmunocromatografía que ofrecen gran comodidad, sensibilidad (94%) y especificidad (99%), comparables al cultivo y al test del aliento con urea marcada. Este test no se debe utilizar como despistaje general en niños asintomáticos o ante todo DAR inespecífico, sino reservarlo para aquellos casos con clínica sugestiva. La determinación indiscriminada implicaría un sobrediagnóstico de pacientes asintomáticos que probablemente no requieren ningún tratamiento(7). Los datos del grupo de trabajo ESPGHAN acerca de las tasas de resistencia del microorganismo, obtenido por biopsia, a los antibióticos fueron: a claritromicina un 19,5%, a metronidazol un 16%, a amoxicilina un 1,4%, a levofloxacina un 4,87% y a rifampicina un 12,9%. Los datos obtenidos en pacientes que habían fracasado a una primera tanda de tratamiento de erradicación fueron: resistencia a claritromicina un 28,6% y a metronidazol un 29,4%. A la luz de estos resultados, la recomendación de la ESPGHAN es que la antibioterapia en pacientes pediátricos, debería adaptarse a la susceptibilidad a los mismos para alcanzar el objetivo de una tasa de erradicación primaria de, al menos, 90%. Las pautas recomendadas en estos momentos, si no se efectúa fibroendoscopia y antibiograma tras la biopsia, se exponen en la tabla III.
Dispepsia funcional
El cuadro simula una gastritis o dispepsia ulcerosa. Los exámenes diagnósticos de enfermedades orgánicas que puedan explicar los síntomas son negativos.
En ocasiones, se presenta asemejando un cuadro ulceroso o de gastritis, en el cual el dolor es el único síntoma, siendo persistente y localizado en zona epigástrica. En otras ocasiones, se presenta como un cuadro de dismotilidad dispéptica caracterizado por: malestar, disconfort, sin llegar a referir dolor, abarcando toda la parte superior del abdomen, a menudo acompañado de sensación de plenitud postpandrial rápida, hinchazón, náuseas y eructos. Los exámenes diagnósticos de enfermedades orgánicas (Tabla II) que puedan explicar los síntomas son negativos(3). El tratamiento se iniciará con inhibidores de bomba de protones a dosis de 1 mg/kg/24 h mínimo 14 días y dieta de protección gástrica como en el caso de esofagitis. En caso de no obtener mejoría, se debe valorar añadir a la terapia ansiolíticos o inhibidores selectivos de la serotonina.
Dolor epigástrico matutino por acetonemia
Algunos pacientes consultan por dolor epigástrico “al despertar”, acompañado en ocasiones, de sensación nauseosa o ganas de vomitar. Las molestias curiosamente calman con la ingesta del desayuno. En la investigación clínica constan: cenas tempranas, frugales y con pocos hidratos de carbono. El aliento suele tener el típico olor a acetona y los cuerpos cetónicos están presentes en orina. La comprobación del diagnóstico y la solución del problema radican en cambiar los hábitos dietéticos y hacer cenas más ricas en hidratos de carbono. La toma en los casos que sea necesario, unido a los anteriores cambios dietéticos comentados, de una cuchara de 5 ml de Emenea® (glucosa + fructosa + ácido fosfórico) al despertar y quedando unos minutos en cama en reposo, suele solucionar el cuadro clínico.
DAR zona mesogastrio
Parasitosis
Dos parásitos pueden dar origen al dolor recidivante: la Giardia lamblia y el Blastocystis Hominis. El dolor producido suele ser referido a zona duodenal-periumbilical en forma de crisis, más frecuentemente después de las comidas. Es debida a la irritación duodenal que produce el parásito. En caso de Giardia Lamblia, puede ir acompañado de crisis diarreicas e intolerancia secundaria y transitoria a la lactosa. El Blastocystis Hominis no produce diarrea, y puede ir acompañado de una eosinofilia, no así la Lamblia. El diagnóstico se efectuará mediante examen parasitológico de las heces y el tratamiento con Metronidazol, a razón de 20 mg/kg/día en dos tandas de 7 días. En caso de resistencia al Metronidazol, podemos emplear el Tinidazol, a dosis de 50 mg/dosis única, o la Espiromicina 50-100 mg/kg/24 horas, ambos en dos tandas de 7 días. Recordar que otro tipo de parasitosis frecuente en nuestro entorno, como los oxiuros, no se acompañan de DAR, por lo cual no deben de entrar en nuestra sospecha diagnóstica.
Enfermedad celíaca, intolerancia al gluten e intolerancia a los almidones
Muchos pacientes acuden relacionando su dolencia digestiva con la ingesta de gluten o prolaminas de otros cereales. Sin embargo, estamos ante tres entidades distintas.
La enfermedad celíaca es una enfermedad bien conocida por los pediatras y de diagnóstico creciente(8,9). En esta edad, suele presentar: dolorimiento abdominal difuso, pérdida de apetito y de peso, heces irregulares o completamente normales y cansancio. Pueden existir antecedentes familiares. El descubrimiento del anticuerpo anti-transglutaminasa tisular humana ha supuesto un gran avance en el diagnóstico y es el método serológico de elección para el despistaje, diagnóstico y seguimiento de la enfermedad celíaca, puesto que tiene un elevado valor predictivo, alta sensibilidad y especificidad. Posteriormente, deben ser remitidos al gastroenterólogo infantil para la confirmación diagnóstica. El tratamiento, es la exclusión del gluten de la dieta de manera estricta y de por vida.
Cada vez es más frecuente la consulta de pacientes que manifiestan síntomas varios de “disconfort” intestinal referido como: aerofagia, flatulencia, hinchazón abdominal, dolorimiento o crisis de diarreas, y que relacionan con la ingesta del gluten del trigo. Las pruebas bioquímicas excluyen la enfermedad celíaca, la alergia o sensibilidad a las proteínas del gluten o a las prolaminas de los diferentes cereales. La biopsia intestinal demuestra que no hay enteropatía de ninguna clase; sin embargo, constatan que los síntomas son dosis dependiente y que mejoran al suprimir los cereales de la dieta. En estos momentos, los mecanismos de dicha intolerancia al gluten no son conocidos y los pacientes deben ser tratados como celíacos. Sin embargo, la mayoría de casos que consultan no presentan dicha intolerancia “real al gluten” y el diagnóstico diferencial debe ser hecho con la intolerancia a los almidones de los cereales, en general. La sintomatología, en estos otros casos, es debida a la presencia de almidones y productos de la digestión de los mismos, no absorbidos por el intestino de individuos sanos, al ser resistentes a la digestión de los enzimas pancreáticos. Los modernos procesos de fabricación de los productos a base de cereales con variantes de temperatura de gelatinización y calor excesivo, conllevan inversión de las cadenas de amilosa o las secciones lineales de amilopectina que retrogradan y forman zonas con una organización cristalina muy rígida resistentes a las amilasas digestivas. El diagnóstico se efectuará mediante la prueba del hidrógeno espirado (test del aliento) que demuestra dicha fermentación y dietas de exclusión. La introducción de gluten purificado que no causa problemas confirma el diagnóstico diferencial con respecto a los pacientes con intolerancia “real al gluten” que sí los presentan. Posteriormente, una dieta de exclusión de cereales “pre-congelados” y, en general, un descenso en el consumo de cereales, mejora espectacularmente los síntomas de estos pacientes.
Intolerancia a azúcares
Determinados hidratos de carbono no son absorbidos por el intestino, conllevando: diarrea, meteorismo y dolorimiento intestinal. El diagnóstico se efectúa mediante la prueba del hidrógeno espirado (test del aliento) específicamente para cada azúcar y con la dosis adecuada.
Intolerancia a la lactosa
Los pacientes manifiestan dolor tras la ingesta de leche o molestias vagas, peri umbilicales a lo largo del día. En ocasiones, dichas molestias van acompañadas de heces más deshechas y meteorismo. La fisiopatología de los síntomas que se producen en la intolerancia reside en la presencia de lactosa no hidrolizada en la luz intestinal, que ocasiona la secreción de líquidos y electrólitos hasta que se alcanza el equilibrio osmótico. La mayor parte de la lactosa no absorbida es hidrolizada por determinadas bacterias intestinales del colon a moléculas de hidratos de carbono más pequeños y otros productos fermentativos, entre los cuales se incluyen: los ácidos orgánicos de cadena corta, los ácidos butírico, propiónico y acético, el ácido láctico y grandes cantidades de H2 que, a su vez, difundirá a través de la mucosa del colon y se eliminará por la respiración (Fig. 3).
Figura 3. Mecanismos de la fisiopatología de la intolerancia lactosa.
Se trata, por lo general, de sujetos con intolerancia inducidas genéticamente: “lactasopenia” (déficit inducido genéticamente de lactasa)(10). Estudios in vitro han demostrado que la cantidad de 10,5 g de lactosa (un vaso de leche) puede llegar a producir 120 mmol de ácidos orgánicos, lo cual permitiría producir 2.600 ml de CO2 y casi 4 litros de H2. La historia clínica es clara y la comprobación puede hacerse bien con la supresión de la leche de la dieta o con la prueba del hidrógeno espirado (test del aliento). En ocasiones, dicho diagnóstico esta supravalorado, ya que el resultado del test de aliento estará en función de la cantidad de sustrato empleado. La cantidad empleada de 2 g de lactosa/kg en solución acuosa al 20% (máximo, 50 g), que se practica por parte de algunos laboratorios o clínicos es excesiva, pues equivaldría a la ingesta aproximadamente de la lactosa contenida en un 1 litro de leche, y además en condiciones no fisiológicas, dado que no está en unión con los otros nutrientes de la leche. Por ello creemos, al igual que otros autores, que es más razonable hacer lo que hemos llamado “sobrecarga fisiológica de lactosa” con un vaso de leche de 250 ml (10,5 g de lactosa), que es la cantidad que habitualmente se ingiere y se debe tolerar. Nuestros datos refieren una frecuencia de malabsorción de lactosa en niños con sospecha de intolerancia del 32,5% tras la prueba con 2 g/kg de lactosa, disminuyendo al 13,7% tras la sobrecarga fisiológica, con 250 ml de leche(11). Datos similares han sido referidos por otros autores. Una vez efectuada la prueba diagnóstica “fisiológicamente”, debemos encontrar “el umbral de tolerancia” clínica para cada individuo con el fin de aportar aquellos alimentos lácteos ricos en calcio y con poca cantidad de lactosa. Debemos evitar el desarrollo de una osteopenia en estos sujetos, realizando dietas drásticas con supresión absoluta de lácteos, como bien es sabido el nutriente fundamental para el aporte de calcio(12). Actualmente, se dispone de leches de vaca sin lactosa o con baja concentración (> 0,7 g lactosa/100 ml) que suelen tolerarse perfectamente, así como de yogur sin lactosa y recordar que el queso solo contiene trazas de lactosa, siendo habitualmente perfectamente tolerado.
Intolerancia a la fructosa y sorbitol
El consumo de zumos y néctares de frutas industriales, con adición de jarabes de azúcares en sus diferentes presentaciones, por parte de escolares y adolescentes, ha aumentado drásticamente a lo largo de los últimos años debido a su disponibilidad y diversificación. Dichos jarabes se obtienen a partir del almidón de maíz por un proceso enzimático y suelen consistir en una mezcla de fructosa y glucosa en proporciones muy superiores a como se presentan en las frutas naturales o en los zumos frescos, y pueden contener también sorbitol. En la Tabla IV, se expone la composición en hidratos de carbono y el aporte calórico de algunos de los refrescos y tipos de zumos de frutas de mayor consumo en el mercado nacional.
Los mecanismos fisiopatológicos y clínica son extrapolables a los expuestos en el apartado de intolerancia a la lactosa (Fig. 3). La clínica dependerá del tipo de zumo/néctar consumido, de la cantidad y de su periodicidad. En nuestro estudio(13), pudimos observar como la sobrecarga fisiológica con 250 ml de néctar de melocotón, con un contenido en fructosa de 5%, que representa la ingesta de 15 g de fructosa, lo que conllevaría una dosis de 0,45 g a 1 g/kg, según los pesos de los niños estudiados, es suficiente para poder dar signos de malabsorción en el 50% de los niños. Sin embargo, a pesar de la constatación de fenómenos de malabsorción, solo 5 (25%) presentaron un cuadro clínico de intolerancia(13). Al igual que hemos referido con respecto a la lactosa, una dosis excesiva de 2 g/kg de fructosa, al efectuar la prueba del hidrógeno espirado (test del aliento) hará que sea patológica en prácticamente todos los sujetos estudiados. No existe la intolerancia “secundaria a la fructosa” (como en el caso de la lactosa) y la intolerancia a la fructosa congénita es una causa rarísima y de presencia neonatal. La intolerancia a la fructosa, por tanto, no podemos considerarla “una enfermedad” sino una incapacidad natural de absorción de la cantidad excesiva del substrato por parte de nuestro organismo(13). El tratamiento consiste en retirar de la dieta dichos zumos en exceso, pero no la retirada, como vemos habitualmente de los alimentos naturales que contienen fructosa y que son perfectamente tolerados, ya que contienen una cantidad perfectamente absorbible por el intestino.
Asimismo, un grupo de los alcoholes del azúcar, los hexasoles (sorbitol) empleados como edulcorantes artificiales no absorbibles para las dietas hipocalóricas o zumos son causa de malabsorción. Cantidades de 0,5 g/kg o más pequeñas como 0,3 g/kg de sorbitol, pueden condicionar episodios de diarrea y dolor abdominal. Dicha malabsorción aumenta cuando se asocia en los zumos a la fructosa. Este nutriente no está presente habitualmente en la dieta ni es absorbido por el intestino humano de los sujetos sanos, por tanto, la sobrecarga con cantidad excesiva será siempre patológica, por eso se describen tantos intolerantes en las sobrecargas practicadas. El tratamiento consiste en evitar los alimentos que lo contienen en cantidades excesivas.
Síndrome de hiperproliferación bacteriana
La microbiota intestinal es un complejo ecosistema compuesto por multitud de bacterias con capacidad metabólica extremadamente variada que puede producir efectos beneficiosos o perjudiciales. Un nivel anormalmente alto de población microbiana, unido a un cambio de la ecología habitual se conoce como sobrecrecimiento bacteriano del intestino delgado. Estudios recientes han señalado el aumento de los niveles microbianos en el intestino delgado como un mecanismo para generar síntomas en los niños con DARF(14,15). Se ha referido un aumento significativo en el riesgo de desarrollar DARF por sobrecrecimiento en niños: después de una infección gastrointestinal bacteriana, toma de antibióticos o dietas muy ricas en hidratos de carbono no digeridos (fructosa, sorbitol, almidones cristalizados). Por lo general, produce: hinchazón, diarrea, malestar o dolor abdominal y puede ir acompañado de despeños diarreicos. La sospecha clínica se confirmará con el test del aliento, empleando lactulosa o glucosa como sustrato(14,15). El tratamiento consistirá en una descontaminación bacteriana, con Metronidazol u otro tipo de antibiótico, asociado a una dieta exenta de oligosacáridos, disacáridos, monosacáridos y polioles fermentables (dieta FODMAP)(16,17).
Dolor abdominal funcional
Puede llegar a presentarse aproximadamente en un 20% de los niños y adolescentes. Son tres las formas de presentación que han sido referidas para el DARF y cabe recordar que los exámenes diagnósticos de enfermedades orgánicas que puedan explicar los síntomas son totalmente negativos.
El DARF definido como “puro” en zona meso gástrica se ha comunicado que puede llegar a presentarse aproximadamente en un 20% de los niños que asisten a la escuela en los Estados Unidos y Europa(15). Son tres las formas de presentación que han sido referidas para el DARF en esta zona y recordar que los exámenes diagnósticos de enfermedades orgánicas (Tabla II) que puedan explicar los síntomas son totalmente negativos(3).
Síndrome de intestino irritable
Los síntomas están referidos exclusivamente en relación con el cambio de hábito de la defecación. El dolor de tipo cólico se asocia con un cambio de la frecuencia de las deposiciones y de la consistencia de las mismas. Se asocia su desencadenamiento con situaciones de estrés. Se han ensayado en adultos diferentes pautas de tratamiento con medicamentos diversos sin éxito terapéutico real y prolongado. Lo más preconizado actualmente es un tratamiento dietético con dieta FODMAP(17).
Dolor abdominal funcional “puro”
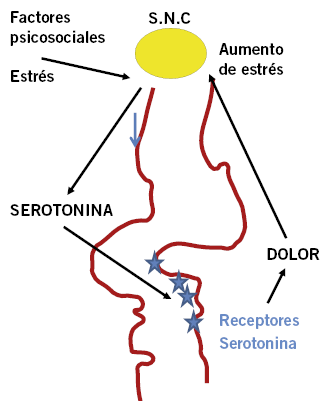
Es el más frecuente de los tres tipos. Ha sido definido como un dolor de abdomen con mayor o menor continuidad, sin localización precisa, en pacientes de edad escolar o adolescente, sin ninguna relación del dolor con alteraciones de eventos fisiológicos, como: comida, tipo de alimento ingerido, defecación u otra molestia orgánica. No se aprecia ningún tipo de desorden gastrointestinal o enfermedad que pueda justificarlo. Dicho dolor suele provocar perdida de días de escolaridad y altera el ritmo de actividad habitual del sujeto. Suele ser más bien intermitente, con periodos, a veces, prolongados de normalidad. En ocasiones, existen conflictos escolares o familiares y la personalidad del paciente puede ser lábil o se encuentra en proceso de maduración. Es importante destacar que el dolor no es simulado y el paciente se encuentra realmente quejoso, los niños no son unos simuladores o falsificadores, y la familia suele constatar con empeño este hecho. La fisiopatología precisa causante de estos trastornos no está en la actualidad totalmente dilucidada. La teoría más aceptada es que los síntomas pueden ser debidos a cambios del eje cerebro-intestino y sus relaciones con el sistema nervioso central y sistema nervioso autónomo intestinal (SIAN). El SIAN controla todas las funciones motoras y secretoras del sistema gastrointestinal, pudiendo modificar las acciones del sistema nervioso simpático y parasimpático. Los neurotransmisores controlados por el SIAN incluyen: serotonina (5-HT), acetilcolina, el péptido P, el péptido intestinal vasoactivo (VIP) y el péptido de relación con la calcitonina. Se sabe que los receptores de la 5-HT participan activamente en los procesos de sensibilidad de la mucosa del intestino. La hiperalgesia o hipersensibilidad visceral puede estar ligada: a alteraciones de los receptores de sensibilidad (nocirreceptores), a una anormal modulación, a una alteración en la trasmisión sensorial del sistema nervioso central o periférico, o bien a cambios en las percepciones corticales de las señales aferentes. La hiperalgesia se desencadena una vez que los nocirreceptores se vuelven hipersensibles, después de repetidos estímulos negativos o nocivos (p. ej., inflamaciones por infecciones, sustancias irritantes, alergias); entonces, envían señales de dolor después del estímulo que normalmente no causaría dolor o lo envían de una manera exagerada (hiperalgesia) (Fig. 4).
Figura 4. Hipótesis fisiopatológica del dolor abdominal recidivante funcional.
Está demostrado que la 5-HT está implicada en la generación de dichos impulsos de los nocirreceptores. Para el tratamiento han sido ensayados anticolinérgicos y antidepresivos tricíclicos, En estos momentos, el tratamiento más preconizado es la Ciproheptadina, potente antagonista de los receptores de serotonina(18). La hipótesis de su eficacia está basada en que bloquea los nocirreceptores del músculo liso intestinal(18). El manejo de la mediación debe efectuarse por especialistas con experiencia.
Migraña abdominal
Episodios paroxísticos de dolor abdominal intenso, agudo peri umbilical, en la línea media o difusa, durante 1 hora o más, debería ser el síntoma más severo y angustioso. Los episodios están separados por semanas o meses. El dolor es incapacitante e interfiere con la actividad normal. El patrón estereotípico y los síntomas son individuales para cada paciente, y puede ir asociado a: anorexia, náuseas, vómitos cefalea, fotofobia, palidez y mareos. El tratamiento puntual se efectúa con analgésicos convencionales (ibuprofeno, paracetamol). Si los cuadros son repetitivos, se debe emplear el tratamiento especificado en el apartado anterior con Ciproheptadina(18).
Enfermedad inflamatoria intestinal
Deberemos estar atentos a niños con: dolor abdominal, febrícula, pérdida de peso, anorexia y deposiciones anormales, líquidas, o bien, con moco o sangre. Debe, en estos pacientes, efectuarse un primer screening de sangre investigando marcadores de inflamación (VSG, PCR, ferritina y hemograma) y calprotectina; proteína que se libera por activación de los leucocitos en un proceso inflamatorio. Estará presente en las heces en concentración muy elevada en caso de enfermedad de Crohn o colitis ulcerosa. El DAR en estos pacientes puede derivarse igualmente a zona de hipogastrio. Ante la sospecha, estos pacientes deben ser urgentemente remitidos al especialista para completar urgentemente el estudio.
DAR en zona hipogastrio
Estreñimiento
El interrogatorio nos da fácilmente el diagnóstico, que puede confirmarse con Rx simple de abdomen o ecografía. El tratamiento debe efectuarse con polietilenglicol.
El estreñimiento es un trastorno frecuente en la infancia, responsable de aproximadamente el 5% de las consultas pediátricas ambulatorias y de un 18-25% de las consultas en las unidades de gastroenterología pediátrica. En el interrogatorio para la evaluación del DAR, se manifiesta claramente dicha sintomatología. Los dolores suelen ser frecuentes a lo largo del día, en forma de molestia vaga o “dolor punzante” y dificultad para la evacuación. Las heces duras, voluminosas, con escibalos en su progreso intestinal son la causa del dolor por contacto directo y, en ocasiones, desencadenando el mecanismo fisiopatológico descrito en el DARF puro. El interrogatorio, la palpación abdominal de fecalomas y una Rx simple o una ecografía de abdomen serán suficientes para llegar al diagnóstico. La resolución del estreñimiento y la consecuente desaparición de las molestias confirmarán definitivamente el diagnóstico. La aplicación de medidas dietéticas con alimentos ricos en fibra pueden ser un coadyuvante, pero rara vez, solucionan por sí solas el problema. Numerosos estudios avalan la eficacia del polietilenglicol (PEG) 3350, con electrolitos y sin electrolitos, (Movicol® y Casenlax®) en el tratamiento del estreñimiento crónico y la impactación fecal en niños(19). No existe una dosis establecida para el PEG y las dosis efectivas de mantenimiento empleadas por los diferentes autores oscilan entre 0,4-0,8 g/kg/día; si bien, las dosis de ataque, hasta el inicio de respuesta, sobre todo cuando se ha empleado para la desimpactación fecal, son más elevadas (alrededor de 1 g/kg/día). En nuestra experiencia, la eficacia inicial se consiguió en el plazo máximo de una semana (media de 5 días), con una dosis media de 1,7 ± 0,45 sobres/día de Movicol (rango 1-3 sobres). La dosis eficaz de PEG en el mantenimiento arrojó una mediana de 1 sobre/día (rango 0,5-2,5) equivalente a 6,5 g de PEG. Diferentes factores, como: grado de estreñimiento, tipo de dieta e ingesta de líquidos, se implican en la dosis terapéutica de efectividad. El peso de nuestros pacientes referenció una media de 21,5 kg (rango 12,5-50), equivaliendo a una dosis de PEG + E de 0,37 g/kg/día (rango 0,18-0,8). Dado que no se absorbe y que el mecanismo de acción es local, la dosis debe ser pautada por sobres/día más que por peso, buscando la dosis terapéutica eficaz(19).
Adenitis mesentérica
La linfadenitis es una afección en la que los ganglios linfáticos se inflaman. Cuando la linfadenitis afecta a los ganglios linfáticos de la membrana que conecta el intestino con el mesenterio, se produce la adenitis mesentérica. Principalmente afecta a niños y adolescentes. Suele presentarse tras una infección intestinal con o sin síntomas acompañantes, como vómitos y diarrea, o bien otro tipo de infecciones víricas generales, a veces, de vías respiratorias. Una vez pasado dicho cuadro, persiste un dolorimiento abdominal, a menudo, referido a toda la zona del hipogastrio. Esta afección dolorosa puede presentar signos y síntomas de advertencia similares a los de la apendicitis. El diagnóstico es ecográfico y su tratamiento con antiinflamatorios/analgésicos tipo AINE, mientras dure la sintomatología y la ecografía nos confirme la desaparición.
Otros procesos en general
Etiologías de presentación mucho más infrecuente, que pueden presentar dolor en cualquiera de las zonas referidas, como: tumores, quistes, pancreatitis, litiasis, malformaciones, patología urinaria y otros, raramente se encuentran en la práctica diaria (Fig. 1). Ya hemos referido en la tabla II, el estudio a efectuar en el caso de que el DAR no oriente inicialmente a enfocar nuestro estudio hacia una sospecha de los cuadros habituales a los que nos hemos referido. Con dicha evaluación, es improbable que se nos escape algún proceso orgánico.
Bibliografía
Los asteriscos muestran el interés del artículo a juicio del autor.
1. Apley J, Naish N. Recurrent abdominal pains: a field survey of 1000 school children. Arch Dis Child. 1958; 33: 165-70.
2. *Benninga MA, Nurco S, Faure Ch, Hyman P, Ian R, Schechter N. Childhood Functional Gastrointestinal Disorders: Neonate/ Toddler. Gastroenterology. 2016; 150: 1443-55.
3.*** Hyams J, Di Lorenzo C, Saps M, Shulman R, Staiano A, Filburg M. Childhood Functional Gastrointestinal Disorders: Child/ Adolescent. Gastroenterology. 2016; 150: 1456-68.
4. Infante Pina D. Dolor abdominal recurrente: Enfoque racional del problema. Distinciones Sandoz Nutrición. 1994. Sandoz Nutrición (eds).
5. Aparicio Hernán A. Dolor abdominal crónico y recurrente. Pediatría Integral. 2011; XV(1): 50-53.
6.** Hernández Hernández A, Monge Zamorano M, Quintana Herrera C. Dolor abdominal crónico y recurrente. Infección por Helicobacter pylori. Pediatría Integral. 2015:XIX(1): 33-50.
7. Ruggiero P. Helicobacter pylori infection: what’s new. Curr Opin Infect Dis. 2012: 25: 337- 44.
8. Infante Pina D. Manejo de la enfermedad celíaca en Atención Primaria. Pediatr Integral. 2007; XI(2): 1-10.
9. Coronel Rodríguez C, Espin Jaime B, Guisado Rasco MC. Enfermedad celíaca. Pediatr Integral. 2015; XIX(2): 102-18.
10.*** Infante D. Intolerancia a la lactosa: en quién y por qué, An Pediatr. 2008; 69: 103-5.
11.*** Tormo R. Infante D. Malabsorción de hidratos de carbono en la infancia. Aplicación de la prueba de dosificación del hidrógeno en el aire espirado. En: Premios Nutrición Infantil 1987. Barcelona: En Ed. Nestlé S.A.
12. Infante D, Tormo R. Risk of inadecuate bone mineralization in diseases involving long term supression of dairy products. J Pediatr Gastroenterol Nutr. 2000; 3: 10-3.
13.** Infante D, Martin B, Pich M, Tormo R. ¿Ha paso de moda el agua? Los hábitos de bebida en la edad pediátrica, su repercusión nutricional. Premio Nutrición 2001. En Ed. Nestlé S.A.
14.*** Korterink JJ, Benninga MA, van Wering IM, Deckers-Kocken JM. Glucose hydrogen breath test for small intestinal bacterial overgrowth in children with abdominal pain-related functional gastrointestinal disorders. J Pediatr Gastroenterol Nutr. 2015; 60: 498-502.
15.** Jones HF, Davidson GP, Brooks DA, Butler RN. Is small-bowel bacterial overgrowth an underdiagnosed disorder in children with gastrointestinal symptoms? J Pediatr Gastroenterol Nutr. 2011; 52: 632-33.
16.** Barrett JS, Gibson PR. Fermentable oligosaccharides, disaccharides, monosaccharides and polyols (FODMAPs) and nonallergic food intolerance: FODMAPs or food chemicals? Ther Adv Gastroenterol. 2012; 5: 261-268.
17. Halmos EP, Power VA, Shepherd SJ, Gibson PR, Muir JG. A diet low in FODMAPs reduces symptoms of irritable bowel syndrome. Gastroenterology 2014; 146: 67-75.
18.** Madani S, Cortes O, Thomas R. Cyproheptadine use in children with functional gastrointestinal disorders. J Pediatr Gastroenterol Nutr. 2016; 62: 409-13.
19. Pina DI, Cantón OS, Casas RV, de la Pardina JC, López Liñán MJ, Busoms CM. Eficacia, tolerancia y seguridad a largo plazo del polietilenglicol 3350 con electrolitos en el tratamiento del estreñimiento funcional en niños. An Pediatr. 2014; 80: 278-84.
Bibliografía recomendada
– Hyams J, Di Lorenzo C, Saps M, Shulman R, Staiano A, Filburg M. Childhood Functional Gastrointestinal Disorders: Child/ Adolescent. Gastroenterology. 2016; 150: 1456-68
Los autores efectúan una revisión y clasificación de un nuevo concepto dentro de la categorización del DAR, que ha hecho su aparición dentro de las posibles etiologías del dolor abdominal recidivante y que se ha denominado “de origen funcional”.
– Infante D. Intolerancia a la lactosa: en quién y por qué. An Pediatr. 2008; 69: 103-5.
El autor en el artículo expone con claridad que es la intolerancia a la lactosa inducida genéticamente, en quién se presenta y el porqué. Explica la fisiopatología de los síntomas, el enfoque diagnóstico y terapéutico.
– Tormo R. Infante D. Malabsorción de hidratos de carbono en la infancia. Aplicación de la prueba de dosificación del hidrógeno en el aire espirado. En: Premios Nutrición Infantil 1987. Barcelona: En Ed. Nestlé S.A.
Los autores revisan a qué hidratos de carbono suelen los niños y adolescentes presentar intolerancia con más frecuencia. Mecanismo fisiopatológico. Su prevalencia. Los métodos correctos de diagnóstico mediante la prueba de hidrógeno espirado (test del aliento). Consejos dietéticos.
– Korterink JJ, Benninga MA, van Wering IM, Deckers-Kocken JM. Glucose hydrogen breath test for small intestinal bacterial overgrowth in children with abdominal pain-related functional gastrointestinal disorders. J Pediatr Gastroenterol Nutr. 2015; 60: 498-502.
Actualmente, la flora intestinal ha tomado un gran protagonismo tanto en función de la salud como de la enfermedad. Los autores revisan los mecanismos fisiopatológicos por los cuales una alteración de la flora normal intestinal (Bacterial Overgrowth)puede producir DAR. Revisan la metodología diagnóstica para dicho proceso.
| Caso clínico |
|
Adolescente de 16 años de edad sin antecedentes personales de interés. Temperamento tranquilo y ambiente escolar y familiar sin problemática. Como antecedentes familiares, relatan una abuela y tía materna afectas de enfermedad celíaca. Sin antecedentes alérgicos. Desde hace un año aproximadamente refiere crisis esporádicas de dolor abdominal peri umbilical, no invalidante, de horas de duración. En ocasiones, está acompañado de deposiciones diarreicas de uno o dos días de duración. Entre las crisis está sin molestias. Refiere que muchos días coincide con la práctica de deporte (juega al baloncesto). También, no obstante, lo presenta en ocasiones en la época estival. No lo relaciona con la menstruación. Dicho cuadro no va acompañado de ningún otro tipo de síntomas. Entre la crisis se encuentra perfectamente y el ritmo deposicional y su consistencia es normal. Exploración: dentro de la normalidad. Exámenes solicitados: • Bioquímica: hemograma, sideremia, reactantes fase aguda, perfil hepático-renal- pancreático, glicemia, colesterol y marcadores de celiaquía: todo normal. • Heces: parásitos, sangre oculta y calprotectina: normal. • Ecografía abdominal: normal. • Mezcla de alérgenos alimenticios (frutos secos, pescado, frutas): negativo.
|