
Enseñanza no reglada y sin carácter oficial. Los créditos de formación continuada, no son aplicables
a los profesionales que estén formándose como especialistas en Ciencias de la Salud.

 |
| Editorial |
J. Pellegrini Belinchóna-b (Coordinador),
C. Ortega Casanuevac-b,
S. de Arriba Méndezd-b, S. García de la Rubiae-b, J. Martín Ruanof-b,
T. Sánchez Vélezd-b, F. Álvarez Carog-b
aCentro de Salud de Pizarrales. Salamanca, bGrupo de Trabajo de Asma y Alergia de la SEPEAP, cHospital Quirón San José. Madrid. dHospital Clínico Universitario. Salamanca. eCentro de Salud Infante. Murcia. fCentro de Salud Santa Marta. Salamanca, gHospital de Cabueñes. Gijón
| «La nueva Guía Española para el Manejo del Asma, GEMA4.0, actualiza la información existente y establece unos protocolos de actuación, con el objetivo de mejorar la calidad de vida de las personas con asma, mediante un mejor control de la enfermedad por parte de los pacientes y sus familias, y atendiendo a una mejor formación de los profesionales sanitarios en todos los ámbitos de actuación, en lo que se refiere a esta enfermedad crónica que, en el caso de la infancia, es la más prevalente" |
El pasado mes de mayo, se presentó en Madrid la última versión de la Guía Española para el Manejo del Asma(1), GEMA4.0. En un reciente editorial en esta misma revista, el grupo de Asma y Alergia de la SEPEAP abogábamos porque: “las Sociedades Científicas de Pediatría de Atención Primaria estuvieran representadas en los nuevos consensos de la GEMA, tal como lo están las Sociedades Científicas de primaria de adultos”, y esto ahora, es una realidad de la que como Sociedad Científica estamos satisfechos(2).
El desarrollo que ha presentado la GEMA desde su primera publicación en el año 2006, en la que participaron cinco Sociedades Científicas, hasta el momento actual, con la reciente publicación de la GEMA4.0, ha sido verdaderamente notable. Ya en su comienzo, fue un verdadero hito para la comprensión y desarrollo del diagnóstico y tratamiento de esta enfermedad. Posteriormente, la versión de 2009, con la mayor participación de especialistas pediátricos, alergólogos y neumólogos, hizo que los pediatras consideraran la GEMA 2009(3) como una guía fundamental para el tratamiento del asma en la infancia.
El International Study of Asthma and Allergies in Childhood (ISAAC)(4,5) ha permitido en los últimos años, disponer de datos epidemiológicos sobre el asma en la infancia y adolescencia temprana, tanto en nuestro país(6) como en amplias zonas del mundo.
En cuanto a los niños más pequeños, el Estudio Internacional de Sibilancias en Lactantes (EISL)(7), diseñado con el fin de estudiar otros factores distintos a los virus que puedan influir en la génesis de sibilancias durante el primer año de vida del niño, indica que la prevalencia de asma o sibilancias recurrentes, durante el primer año de vida, varían en nuestro país entre el 18,6% de Bilbao al 11,6% de Salamanca(8,9). El asma es la enfermedad crónica más prevalente en la edad pediátrica.
Con respecto a la población general española, los datos son escasos y muy variables, algunos trabajos parten de diferencias importantes como la definición del caso y no son comparables; si bien, el Estudio Europeo de Salud Respiratoria constató una gran variabilidad geográfica entre ciudades y regiones españolas, con aumento de la prevalencia en los últimos años(10,11).
La necesidad de aglutinar los esfuerzos realizados por los diversos comités y grupos de trabajo de sociedades científicas y grupos de apoyo, para enfocar de una forma coherente esta patología, ha conducido a que desde diversos ámbitos de actuación se provean la creación de guías de apoyo para profesionales, algunas regionales que inciden más en los recursos locales, y otras más ambiciosas, de ámbito nacional o internacional(12-14).
La actual versión de la GEMA4.0 ha supuesto una aspiración importante que teníamos los pediatras de Atención Primaria de participar en el desarrollo de esta guía, donde hay un apartado específico para niños, que al igual que la versión anterior, permite diferenciar el asma en los primeros meses y años de la vida con respecto a etapas posteriores de la vida. Pero, por primera vez, los pediatras que trabajamos en el ámbito de la Atención Primaria hemos tenido participación aportando nuestro punto de vista sobre esta enfermedad que vemos, diagnosticamos y tratamos en nuestras consultas(1).
Las anteriores ediciones de la GEMA han sido referencia para el tratamiento del asma, no solamente en España, también en Latinoamérica, donde varios países han demostrado su interés y hay constancia de su utilización. Probablemente, esto se ha debido a la estructura de la propia guía y es por lo que esta versión que presentamos, la GEMA4.0, mantiene el mismo formato que la versión anterior. Se trata de una guía basada en la evidencia disponible en cada momento, soportada en artículos y publicaciones de impacto y prestigio, con una redacción clara y conceptual, con tablas y algoritmos intuitivos que proporcionan un manejo rápido y útil.
El cambio de nombre a GEMA4.0 plantea una idea de continuidad en su desarrollo y vigencia. Si bien, el número 4 sobrevolado indica que es la 4ª edición de la guía, el .0 que le sigue en el superíndice hace referencia a las necesarias actualizaciones que se irán realizando, fundamentalmente por vía telemática, es decir según se vayan publicando nuevas evidencias, tendremos en nuestra mano la GEMA4.1, o la GEMA4.2, hasta que nuevas investigaciones y publicaciones aconsejen actualizarla de forma más completa con una nueva versión.
La GEMA4.0 incorpora nuevos capítulos, asma y EPOC, asma grave no controlada, este último apartado de más importancia para los pediatras, también aporta un plan de implementación para mejorar su difusión y aplicabilidad. Así, en los próximos meses verán la luz otros documentos, como: “GEMA para pacientes”, “GEMA de bolsillo”, “GEMA Educadores” y otros más que pensamos que pueden ser importantes para mejorar la comprensión y tratamiento por parte del personal sanitario, pacientes y familias y otros profesionales implicados en el control del asma.
En el prólogo de presentación, el Dr. Vicente Plaza, coordinador general de la obra, explica que la intención ha sido: “elaborar una guía de práctica clínica en asma, dirigida a profesionales sanitarios eminentemente asistenciales, muy práctica, independiente y consensuada entre el mayor número posible de expertos provenientes de las diversas sociedades científicas españolas implicadas en la asistencia de la enfermedad”(1). La participación de 14 sociedades científicas y grupos científicos, la incorporación a la nueva versión de sociedades de Farmacia, de Pediatría de Atención Primaria, de Urgencias y Emergencias, así como de asociaciones de pacientes con su visión propia de la enfermedad, hace que el consenso multidisciplinar alcanzado obtenga las mejores expectativas, en cuanto puede suponer una mejoría del abordaje y tratamiento del asma en nuestro ámbito en todas las edades de la población.
La guía está dirigida a todos aquellos profesionales que diagnostican y tratan el asma: médicos de Atención Primaria, pediatras tanto Hospitalarios como de Atención Primaria, neumólogos, alergólogos, pediatras alergólogos y pediatras neumólogos, otorrinolaringólogos, farmacólogos, farmacéuticos, enfermería general y especializada en patología respiratoria, pero también debe ser útil, tanto la guía en sí, como los documentos derivados de ella, a los educadores, profesores, pacientes y familiares de pacientes. La participación en la GEMA4.0 de la Federación Nacional de Asociaciones de Enfermedades Respiratorias hace que la potencialidad de la guía en cuanto a su capacidad resolutiva se implemente, ya que el asma como patología crónica, precisa de la “complicidad” de sanitarios y pacientes para mejorar el manejo de la enfermedad y, por lo tanto, la calidad de vida de los pacientes.
El asma infantil, precisa de una constante colaboración entre los diversos niveles asistenciales. La importancia de la coordinación entre la Atención Especializada con alergólogos y neumólogos infantiles, así como pediatras Hospitalarios y de Atención Primaria, mejora de forma fehaciente el manejo de esta enfermedad crónica. Además, como pediatras de Atención Primaria, somos conscientes de que nuestro ámbito de actuación es el más cercano al niño y a su familia, procurando un acceso fácil y rápido al sistema sanitario no urgente. La necesaria colaboración entre Pediatría Hospitalaria y de Atención Primaria se incluye en la GEMA4.0 como integración de todos los puntos de vista.
La actualización de la guía se ha realizado partiendo de las evidencias disponibles en la anterior edición de 2009, siguiendo las recomendaciones para la actualización de las Guías de Práctica Clínica del Sistema Nacional de Salud.
Los miembros del Comité Ejecutivo y redactores realizaron una búsqueda sistemática, con evaluación y selección de publicaciones sobre asma entre 2009 y 2014. Posteriormente, con los resultados obtenidos, se clasificó la evidencia partiendo del tipo de estudios publicados para cada uno de los aspectos tratados, según fueran estudios clínicos aleatorizados y controlados o la existencia de revisiones sistemáticas o metaanálisis, además de otros estudios observacionales, no controlados o no aleatorizados. Cuando no se disponía de otros artículos, se ha recurrido a la experiencia clínica de expertos.
Una vez establecidas las evidencias, la categorización del nivel de las recomendaciones de la guía se estableció mediante consenso, primero entre los redactores y posteriormente con los revisores. Fueron categorizadas en 2 niveles: recomendaciones robustas (R1), que indican aquellas actuaciones, a juicio de los autores y revisores, cuya aplicación implica más beneficios que riesgos; y recomendaciones débiles (R2), para aquellas en las que hay incertidumbre sobre el riesgo/beneficio de su aplicación.
Una vez consensuado el texto y las recomendaciones por los autores y un grupo de coordinadores con varios sistemas de control y modificaciones por capítulos asignados, los textos se enviaron a los coordinadores de cada capítulo, grupo formado por miembros del comité ejecutivo de la GEMA. Tras la unificación de cada capítulo, este volvía a los autores para realizar el primer consenso parcial. Posteriormente, se fusionaron todos los capítulos en un solo documento y el texto resultante se sometió a expertos en metodología de guías de práctica clínica del Instituto para la Excelencia Clínica y Sanitaria (INPECS), que efectuaron una revisión crítica de la metodología y redacción(1).
Las recomendaciones resultantes fueron revisadas y consensuadas, mediante método Delphi, por un grupo de 101 expertos en asma de todas las Sociedades Científicas participantes. Hay que señalar con cierto orgullo, que fueron consensuadas todas las conclusiones y recomendaciones realizadas por los autores, aunque con distinto grado de apoyo, y solamente una fue eliminada del documento final.
Los miembros del Grupo de Asma y Alergia de la SEPEAP, animamos a todos nuestros compañeros a acceder a la GEMA4.0. Pensamos que es una guía perfectamente adaptada a nuestro entorno y que puede ser una herramienta muy útil para el manejo de la enfermedad crónica más prevalente en la infancia y mejorar así la calidad de vida de nuestros pacientes y sus familias.
Bibliografía
1. GEMA 4.0. Guía Española para el Manejo del Asma. Consultada el 30 de junio de 2015. Disponible en: http://www.gemasma.com/.
2. Grupo de Trabajo de Asma y Alergia de la SEPEAP. Editorial. Pellegrini Belinchón J, de Arriba Méndez S, García de la Rubia S, Martín Ruano J, Ortega Casanueva C, Sánchez Vélez T, Álvarez Caro F. Pediatr. Integral. 2014; XVIII(5): 277-79. Consultado el 30 de junio de 2015. Disponible en: https://www.pediatriaintegral.es//wp-content/uploads/2014/10/Pediatria_Integral-XVIII-5.pdf.
3. GEMA 2009. Guía Española para el Manejo del Asma. 2009. Consultado el 16 de marzo de 2014. Disponible en: www.gemasma.com.
4. Worldwide variations in the prevalence of asthma symptoms: the International Study of Asthma and Allergies in Childhood (ISAAC). Eur Respir J. 1998; 12(2): 315-35.
5. Worldwide variation in prevalence of symptoms of asthma, allergic rhinoconjunctivitis, and atopic eczema: ISAAC. The International Study of Asthma and Allergies in Childhood (ISAAC) Steering Committee. Lancet. 1998; 351(9111):1225-32.
6. Carvajal-Urueña I, García-Marcos L, Busquets-Monge R, Morales Suárez-Varela M, García de Andoin N, Batlles-Garrido J, et al. Geographic variation in the prevalence of asthma symptoms in Spanish children and adolescents. International Study of Asthma and Allergies in Childhood (ISAAC) Phase 3, Spain. Arch Bronconeumol. 2005; 41(12): 659-66.
7. Mallol J, García-Marcos L. Observatorio del Estudio Internacional de Sibilancias en Lactantes (EISL). 2007. Consultado el 30 de junio de 2015. Disponible en: www.respirar.org/.
8. Mallol J, García-Marcos L. Solé D, Brand P; EISL Study Group. International prevalence of recurrent wheezing during the first year of life: variability, treatment patterns and use of health resources. Thorax, 2010. 65(11): p. 1004-9.
9. Pellegrini J, Miguel G, Dios de B, Vicente E, Lorente F, García-Marcos L. Study of wheezing and its risk factors in the first year of life in the Province of Salamanca, Spain. The EISL Study. Allergol Immunopathol (Madr). 2012. 40 (3): p. 164-171.
10. Grupo Español del Estudio Europeo en Asma. Estudio europeo del asma. Prevalencia de hiperreactividad bronquial y asma en jóvenes en 5 regiones de España. Med Clin (Barc). 1996; 106: 761-7.
11. Urrutia I, Aguirre U, Sunyer J, Plana E, Muniozgurren M, Martínez J, et al. Cambios en la prevalencia del asma en la población española del Estudio de Salud Respiratoria de la Comunidad Europea (ECRHS-II). Arch Bronconeumol. 2007; 43: 425-30.
12. From the Global Strategy for Asthma Management and Prevention, Global Initiative for Asthma (GINA) 2015. Consultado el 23 de junio de 2015. Disponible en: http://www.ginasthma.org/.
13. Castillo Laita JA, De Benito Fernández J, Escribano Montaner A, Fernández Benítez M, García de la Rubia S, Garde Garde J, et al. Consensus statement on the management of paediatric asthma. Update 2007. First Spanish Consensus for the Management of Asthma in Paediatrics. Allergologia et immunopathologia. 2008; 36(1): 31-52.
14. British guideline on the management of asthma. Consultada el 30 de junio 2015. Disponible en: https://www.brit-thoracic.org.uk/document-library/clinical-information/asthma/btssign-asthma-guideline-2014/.
 |
| 20 Aniversario |
F. López Sánchez
Catedrático de Psicología de la Sexualidad. Universidad de Salamanca

¿Por qué los adolescentes tienden a asumir riesgos en la actividad sexual?
El rol de los pediatras en la prevención
Lo que ha cambiado
Aproximadamente la mitad de los adolescentes, chicos y chicas, tienen relaciones sexuales, incluidas las coitales, siendo menores de edad. Antes de los 14 años en torno al 10%, y antes de los 17 en torno al 50%. Los profesionales no podemos ni debemos señalar la edad a la que supuestamente es más adecuado iniciarse en estas conductas, pero sí ayudar a los propios adolescentes a cometer menos errores. La mejor prevención es educar en la ética de las relaciones sexuales y amorosas; y en relación a los riesgos, un aspecto concreto llamado “ética de la salud” (López, 2015, en prensa). Ayudar también a los padres y educadores a cumplir con la obligación de ofrecer una buena educación sexual en la familia y la escuela, porque con frecuencia numerosos adolescentes (aunque es justo decir que también los jóvenes y adultos) asumen riesgos en las conductas sexuales.
Para ello es fundamental, en primer lugar, comprender las causas por las que cometen estos errores, justo porque algunas de ellas no se tienen en cuenta o no son fáciles de remover.
Lo primero que hay que comprender es que lo que piensan (contenidos mentales de la actitud) y sienten (contenidos emocionales de la actitud) los adolescentes, en relación con la sexualidad, ha cambiado de manera sustancial en las últimas décadas.
Los adolescentes, en efecto, tienen actitudes más liberales y se atribuyen, con convicción, el derecho a tener relaciones sexuales, sin estar casados, estar enamorados, tener una relación afectiva o incluso sin conocerse previamente. Basta que ambos lo decidan, la ética del consentimiento, es la única pieza del pasado que queda en pie. Y esto es así, tanto en el caso de la mayoría de chicos como de las chicas, aunque haya algunas diferencias. Porque hay que señalar que el cambio más significativo lo han hecho las mujeres, al reclamar, con razón, una igualdad de derechos y dejar de ser las que controlaban la sexualidad de los hombres hasta el noviazgo o el matrimonio. De esta forma, numerosos adolescentes se inician en la actividad sexual, tienen varias parejas durante esta etapa, esperan menos tiempo entre la seducción y las relaciones sexuales y, por último, los que tienen relaciones lo hacen con más frecuencia que en el pasado.
Este cambio en la manera de pensar, sentir y actuar es seguro que merece valoraciones muy distintas según nuestros valores y creencias, pero el problema es que sean cuales sean estos, van acompañados de hechos que un profesional no puede obviar: frecuentes relaciones sexuales con riesgos bien conocidos: embarazos, infecciones, SIDA, abusos sexuales, insatisfacción y disfunciones sexuales.
¿Por qué asumen riesgos?
¿Por qué asumen con demasiada frecuencia riesgos, si tienen informaciones suficientes sobre cómo evitarlos? La explicación no creemos que sea porque persisten algunas imprecisiones en la información o mitos del pasado, sino entre otras, las siguientes:
• La información procede de los amigos, los medios de comunicación, revistas e Internet. La obtienen y la usan en secreto. No está legitimada por los padres, los educadores y los profesionales de la salud. En una sociedad de mercado que excita e incita a tener actividad sexual, convirtiendo a esta en un producto más de mercado, todos hablan de sexualidad, menos los que deberían hablar. En efecto, salvo una minoría, la familia, la escuela y los profesionales de la salud guardan silencio. Sin información legitimada y acceso no secreto a ella, no es posible un buen uso de esta, por lo que no es coherente esperar que planifiquen bien su actividad sexual, especialmente los que la inician por debajo de 14-18 años.
• La actividad sexual de los adolescentes en la mayoría de los casos es furtiva, teniendo que ocultarla a los padres: educadores y los profesionales de la salud se sienten confusos y, con frecuencia, son permisivos, unos, o se resignan, otros. En régimen de furtividad, se puede comprender que la planificación y la responsabilidad se vean muy amenazadas.
En efecto, y este es el fondo del problema, los adolescentes no son considerados sexualmente activos, aunque lo sean, por los padres, los educadores y los profesionales de la salud, salvo excepciones, claro está.
Ambos hechos, la información no legitimada y la actividad sexual furtiva están en grave contradicción con una sociedad que usa la sexualidad como mediador de la publicidad, la cultura que se vende (cine, vídeos, revistas, etc.) y como producto en sí mismo: productos eróticos, pornografía, etc.
Los riesgos de esta sexualidad mercantilizada, puesta continuamente de manifiesto por el mercado y silenciada por los agentes educativos, pueden ser dramáticos. De hecho ya lo son, si tenemos en cuenta los datos. Y no me refiero solo a los embarazos. Por ejemplo, una chica de 17 años que me preguntó, “¿por qué duele tanto? Unas preguntas bastaron para saber lo que estaba pasando: “tenemos las relaciones, coitales, por la noche, al volver del botellón, en el portal de casa, yo vigilo mientras él lo hace, en unos minutos, los menos posibles”.
• Los viejos mitos sobre sexualidad (es peligrosa, solo legitimada en el matrimonio heterosexual, desgasta, etc.) están siendo sustituidos por nuevos mitos, más que por una formación sólida y bien fundada. No podemos comentar todos los nuevos mitos, pero sí señalar algunos, fomentados por la sociedad de mercado y algunos profesionales muy despistados, por no decir otra cosa:
– De la represión a la obligación de tener actividad sexual, confundiendo el hecho de que la actividad sexual es saludable, si se practica de forma segura, a decir de forma más o menos explícita que es necesaria, una condición sine qua non para la salud. Por ello, se supone que todos los adolescentes tienen o deberían tener actividad sexual. Incluso, a veces, se hace educación sexual con este presupuesto.
– De la fidelidad en la pareja a la defensa del “poliamor”; con un nuevo vocabulario porque, en este caso con razón, el de promiscuidad suena muy mal. Tener varias parejas a la vez no solo es un derecho, sino un supuesto consejo profesional.
– Del valor de la virginidad, al valor de la experiencia en la actividad sexual, con presiones comerciales y de grupo para iniciarlas.
– De la represión a la experimentación. Todo debe ser experimentado, probado por el hecho de que otros lo hacen o porque lo ven en los modelos de la televisión e Internet. Esta tendencia a la experimentación les lleva a probar diferentes conductas y favorece la asunción de riesgos.
– De la obligación de hacer las cosas “por el otro o con el otro”, a la idea de que hay que ser egoísta buscando el propio placer. Si el otro no queda satisfecho es “su problema”. Desde este punto de vista, si ella queda embarazada, también es su problema.
Profesionales sin formación e intereses comerciales se dan la mano, cantando estos mitos como nuevos “mantras”, en lugar de ofrecer conocimientos y educar en la libertad para que cada uno se sienta dueño de su vida sexual y amorosa, con o sin actividad sexual, con una pareja o con varias, tomando decisiones responsables con la salud y la ética del consentimiento, el placer compartido, la igualdad entre sexos y la honestidad.
• La asociación del tiempo ocio al consumo del alcohol y otras drogas. Esta sociedad escinde la vida del adolescente en dos: el tiempo que dependen de los demás (vivido por no pocos como tiempo de sufrimiento en la escuela, la familia, etc.) y tiempo propio, sobre el que ellos deciden (el de ocio, entendido muchas veces como tiempo de locura). Es así, como se asocia el ocio al consumo de sustancias que excitan, colocan, ayudan a perder el control y a relacionarse sin miedo. La hora de la noche, el tiempo sin frontera, con música y luces que excitan (impidiendo la comunicación verbal). Tiempo para beber juntos, justo para colocarse, no para disfrutar de la bebida, tiempo, en definitiva, para la locura. Todo propicia una disminución de la conciencia de riesgo y favorece las conductas sexuales que entrañan riesgo para la salud física y las relaciones amorosas (abusos, acoso, violación, etc.).
• Se trata de la conducta sexual. La pulsión sexual supone una alta motivación para tener conductas sexuales, premiadas con un intenso placer inmediato (hoy, aquí y ahora), mientras que los riesgos, si llegan a percibirse en ese momento de excitación, solo son probables y aparecerían en el futuro. Entre un placer seguro en el presente y un riesgo solo probable en el futuro, la posibilidad de asumir riesgos es elevada, sobre todo si no se ha planificado previamente la conducta sexual.
Además, con frecuencia, la relación sexual se da en un contexto en el que las palabras románticas sinceras o engañosas hacen que pueda parecerles inadecuado condicionar la relación al uso de métodos de control como el preservativo, por suponer que se valora al otro como una persona de riesgo. Por otra parte, si las relaciones ocasionales fuera de la pareja se tienen en condiciones de riesgo es frecuente ocultárselas a la pareja, extendiendo posibles contagios.
• Y todo ello sucede en la adolescencia, un periodo en el que la presión de los compañeros (hoy a favor de la actividad sexual), la tendencia a no postergar el placer, la minusvaloración de los consejos adultos, la escasa conciencia de riesgo, la tendencia a explorar y experimentar cosas nuevas, etc., favorece el que los adolescentes asuman conductas sexuales de riesgo.
En efecto, es propio de esta edad sentirse más invulnerables y muy dependientes de los valores dominantes en el grupo, con una posible pérdida de peso de los consejos familiares o, al menos, una ambivalencia hacia lo que los adultos les dicen.
• El precio de los preservativos, el acceso no siempre fácil a ellos, el tenerlos que ocultar a los padres, la falta de lugares adecuados para tener relaciones, el momento en que con frecuencia se tienen (por la noche, después de haber bebido, etc.), son dificultades añadidas para no pocos adolescentes.
Unidas todas estas posibles causas, se comprende que aun hoy, a pesar de la información que tienen, asuman con frecuencia riesgos en la conducta sexual. Y no solo se trata del embarazo no deseado, el Sida y las enfermedades de transmisión sexual, sino de otros muchos que están menos presentes en la mente de los profesionales: los abusos sexuales a menores, el acoso sexual, la violación, la coerción sexual, la frustración sexual y las disfunciones sexuales.
Por todo ello, según el punto de vista que adoptemos, nos balancearemos entre la sensación de caos social en las relaciones sexuales y amorosas (por los tipos de riesgo, su gravedad y frecuencia) y la esperanza (porque aun en estas condiciones y con todos estos factores de riesgo, la mayoría de los adolescentes no tiene conductas de riesgo o son afortunados pasando esta etapa evolutiva sin grandes sobresaltos). Este segundo grupo de adolescentes más saludables, el mayoritario, suele tener factores familiares (una buena historia de apego), grupales (un grupo de amigos y amigas que les apoyan y favorecen las conductas saludables o con menos excesos en los riesgos) y personales (mejor valoración de la vida, más conciencia de riesgo y de que estos pueden y deben ser evitados, mayor asertividad para decir sí o no a las relaciones sexuales, información más legitimada, etc.).
La intervención
La intervención debe ser familiar, escolar y también de los profesionales de la salud. Entre estos últimos, los pediatras tienen un rol fundamental. ¿Qué deberíamos hacer?
• Reconocimiento social de que numerosos adolescentes son, de hecho, sexualmente activos. La furtividad y el silencio de la familia, la escuela y los profesionales es lo primero que deberíamos romper, para que los que de hecho, tienen conductas sexuales las puedan planificas abiertamente.
Romper el silencio familiar, de forma que los padres hablen abiertamente con los hijos. Los padres pueden y deben darles sus criterios sobre estas relaciones, incluso si son contrarios a ellas, pero, sean cuales sean los valores y consejos de los padres, deben contribuir a aumentar la conciencia de riesgo, si se tienen conductas sexuales sin prácticas seguras, informales de cuáles son las prácticas seguras, legitimando la información. Pueden aconsejarles, si así lo creen, que retrasen las conductas sexuales, pero deben tener en cuenta que la información es un derecho de los hijos y no pueden negársela en un mundo de riesgos.
Por otra parte, la familia es el lugar de los valores particulares, religiosos o no, siempre que no contradigan los derechos humanos; pero no puede ser un núcleo educativo fundamentalista que limite el derecho de los hijos a la educación sexual.
• Generalizar la educación sexual en las escuelas. Es una obligación legal que debería llevar a generalizar la educación sexual, en el contexto de la educación para la salud. Los educadores deben ofrecer conocimientos profesionales y valores universales (López, 2005, 2006, 2015) en relación con la vida sexual y amorosa. Algunos contenidos centrales son:
– Una visión positiva de la sexualidad.
– El reconocimiento de las diferentes biografías sexuales (unos sin relaciones y otros con ellas).
– Conocer los riesgos reales de embarazo, SIDA, ETS y aumentar la conciencia de riesgo.
– Entrenarles, en situaciones simuladas a decir sí o no (ética del consentimiento) en las prácticas de sexo seguro.
– Poner a su disposición informaciones sobre los recursos materiales, como el preservativo, y asistenciales, como los centros de asesoramiento a jóvenes, consultas sanitarias, etc.
• Conseguir de la comunidad que ponga al servicio de los adolescentes medios, como el preservativo, y centros de asesoramiento en planificación sexual y oportunidades para formas de ocio no mediatizadas por el alcohol.
Los adolescentes deben aprender que tienen derecho a tener biografías sexuales diferentes, sin relaciones sexuales o con ellas, que la familia, la escuela y la sociedad están dispuestas a ayudarles a vivir su biografía sexual sin riesgos, que estos riesgos son difíciles de evitar si no se reconocen como sexualmente activos y lo son. Para evitarlos, deben aumentar su conciencia de riesgo, aprender a decir “no”, cuando esto es lo que quieren (reconociendo el derecho a ser diferente, distinto de los demás, si es el caso), ser asertivos con sus posibles parejas (no dejándose presionar y exigiendo condiciones de sexo seguro), y dejar de usar el alcohol como mediador de ocio.
• Todos los profesionales de la salud que tienen relación con los adolescentes deberían contribuir a prevenir los riesgos asociados a la actividad. Los pediatras tienen un rol especial por su relación continuada con los menores y sus familias, ¿qué podrían hacer?
– Concienciar a las familias para que rompan el silencio sobre la sexualidad, desde la primera infancia y muy especialmente en torno a la pubertad. Aconsejar a la familia que debe colaborar con la escuela, porque la educación sexual es un derecho de los menores.
– Colaborar con las escuelas en la transmisión de conocimientos profesionales sobre sexualidad y, más en concreto, de los riesgos y la forma de evitarlos. Así como a que aprendan, especialmente a partir de la pubertad, a pedir ayuda a los profesionales. La colaboración entre las escuelas y los centros de salud es, en este y otros muchos temas, fundamental.
Ambos, educadores y pediatras podrían establecer una alianza de colaboración para formar a los padres y a los menores.
– Tener, a partir de la pubertad, entrevistas personales (sin la presencia de la familia) con los menores, a petición propia o de los propios menores. Debería ser fácil obtener el apoyo familiar a estas entrevistas, si se les explica a los padres adecuadamente su sentido: crear un espacio de confianza para que puedan hablar de lo que quieran, especialmente de los malos secretos, si los hubiera. Un “mal secreto” es cuando les pasa algo que puede poner en riesgo su vida, su salud o su bienestar psicológico y social, y no tienen capacidad para afrontarlo bien por sí solos (por ejemplo: estar sufriendo acoso escolar, abuso sexual o cualquier forma de maltrato). En otras muchas ocasiones, se trata de pedir informaciones o ayudas concretas sobre su vida sexual o amorosa.
– Incluir en estas entrevistas, con carácter general, varias preguntas, en relación con este tema. Deben plantearse avanzada la entrevista, una vez establecida una relación de confianza. Las preguntas se podrían introducir así, o como el profesional considere más adecuado: “Te voy a hacer unas preguntas sobre tu vida personal, no necesitas contarme lo que no sea necesario, pero lo hago solo para ayudarte y ya sabes que son confidenciales, ¿sabes lo que quiere decir confidencial?
Preguntas sobre sexualidad:
a. Eres adolescente (o puber) y es posible que te intereses ya más por los chicos o las chicas que cuando eras pequeño, ¿te han hablado de estas cosas tus padres?, ¿y tus profesores? Ya sabes que debes tener buena información para si algún día (puede ser pronto o cuando seas mayor, no hay prisa) tienes relaciones. ¿Estás bien informado?
b. ¿Sabes lo que es el sexo seguro?
c. Ya sabes que puedes retrasar las relaciones sexuales, pero si las tienes, ¿sabrías tenerlas sin cometer errores?: embarazos no deseados, infecciones, insatisfacción sexual, etc.
d. ¿Tienes alguna duda o sabrías como resolverla? Puedes preguntarme lo que quieras.
Cada pregunta puede crear una comunicación abierta que incluya, por parte del pediatra, contenidos precisos sobre los riesgos y la forma de evitarlos.
Preguntas sobre diferentes formas de maltrato (López, 2014):
a. Y hablando de otros temas, algunos menores sufrís porque alguien os hace daño: ¿hay alguien que te haya hecho daño en el pasado o te lo esté haciendo ahora, que te haga sufrir injustamente, y que seguramente te dice que no lo digas nadie? Si fuera así, dímelo, te voy a creer y ayudar, es nuestro trabajo y nuestro deber. Nunca guardes un mal secreto, si alguna vez lo tienes, debes buscar ayuda en quien más confíes. Ya sabes que puedes recurrir a mí u a otra persona de tu confianza, pero defiende tus derechos, no dejes que nadie te maltrate.
b. Indicarle que siempre pueden pedir ayuda a través de los padres o por sí mismos directamente, así como darles referencias de los centros asistenciales (con teléfono y dirección precisa) a los que podrían recurrir en caso de tener algún problema por haber asumido riesgos o haber sufrido maltrato.
Se trata con estas preguntas de abrir la puerta a todo tipo de sufrimientos causados por otras personas o los compañeros del colegio o de la calle: el acoso escolar, los abusos sexuales, las diferentes formas de maltrato en la familia, la escuela o en otros lugares. Como es sabido, todos los profesionales estamos obligados a denunciar cualquier forma de maltrato, para lo cual, además de cumplir con el protocolo legal, aconsejamos conocer bien la red social de respuesta a estos problemas, en la comunidad donde trabaje el pediatra.
Si no necesita ayuda se le despide, alegrándose por ello, pero dejándole claro que puede recurrir al pediatra también para este tipo de problemas.
Bibliografía
Bullough V. Children and adolescents as sexual beings: a historical overview. Child and Adolescent Psychiatric Clinics of North America. 2004; 13: 447-59.
Kaeser F, DiSalvo C, Moglia R. Sexual behaviors of young children that occur in schools. Journal of Sex Education and Therapy. 2000; 25: 277-85.
Larsson I, Svedin C. Teachers’ and parents’ report on 3 to 6 year old children’s sexual behaviour: a comparison. Child Abuse and Neglect. 2002; 26: 247-66.
López F. La prevención de los abusos sexuales y la educación sexual. Salamanca: Amaru; 1995.
López F, Del Campo A. Programas de prevención de los abusos sexuales: padres, educadores, infantil, primaria y secundaria. Salamanca: Amaru; 1997.
López F, Del Campo A, Guijo V. Prepuberal sexuality. European Journal of Medical Sexology. 2003; 12: 49-65.
López F. Educación sexual. Madrid: Biblioteca Nueva; 2005.
López F. Educación sexual de los hijos. Madrid: Pirámide; 2006.
López F. Familia y Homosexualidad. Barcelona: Grao; 2007.
López F. Amores y Desamores: Vinculación y Desvinculación sexuales y afectivas. Madrid: Biblioteca Nueva; 2009.
López, F. Separarse sin grietas. Como sufrir menos y no hacer daño a los hijos. Barcelona: Grao; 2010.
López, F. Los abusos sexuales y otras formas de maltrato sexual. Madrid: Síntesis; 2014.
López, F. Ética de las relaciones sexuales y amorosas. Madrid: Pirámide; 2015.
Topolski T, Patrick D, Edwards T, Huebner C, Connell F, Mount K. Quality of life and health risk behaviors among adolescents. Journal of Adolescent Health. 2001; 29: 426-35.
 |
| Temas de FC |
J. Pozo Román*, M.T. Muñoz Calvo**
*Médico adjunto del Servicio de Endocrinología. Hospital Infantil Universitario Niño Jesús. Profesor asociado del Departamento de Pediatría de la UAM. CIBER Fisiopatología y Nutrición. Instituto de Salud Carlos III. Madrid. **Médico adjunto del Servicio de Endocrinología. Hospital Infantil Universitario Niño Jesús. Profesor asociado del Departamento de Pediatría de la UAM. CIBER Fisiopatología y Nutrición. Instituto de Salud Carlos III. Madrid
| Resumen
La edad en que la pubertad se inicia es muy variable y, en condiciones normales, está influenciada, además de por el sexo, por factores genéticos y ambientales. Su presentación precoz o tardía puede ser una simple variación extrema de la normalidad o el reflejo de alguna de las múltiples patologías que pueden influir o condicionar el momento de su aparición. En cualquier caso, aun en ausencia de patología, el desarrollo de los caracteres sexuales secundarios a una edad “inadecuada” es motivo de preocupación para los padres y los pacientes y puede tener repercusiones negativas en la vida adulta. El pediatra de Atención Primaria es el profesional que se enfrenta inicialmente a este tipo de situaciones y debe ser capaz de realizar un enfoque diagnóstico adecuado, diferenciar aquellas variantes normales del desarrollo de las que no lo son, orientar a los padres y al paciente y, en aquellos casos que considere necesario, derivar al paciente a un servicio de Endocrinología Pediátrica. |
| Abstract
The age in which puberty initiates varies greatly and, under normal conditions, is also influenced by gender, genetic and environmental factors. Its early or late presentation may be a simple extreme variation of normality or the reflex of any of the multiple conditions that may affect or condition the moment of its appearance. In any case, even in the absence of disease, the development of sexual characters secondary to an “inadequate” age is a reason for concern for the parents and the patients and may have negative repercussions in the adult age. In primary care in pediatrics, it is the professional who initially faces this type of situation and should be capable of performing an adequate diagnostic approach, of differentiating those normal variants from development which are not, of orienting the parents and patient, and in those cases were considered necessary, of referring the patient to a Pediatric Endocrinology service. |
Palabras clave: Pubertad normal; Pubertad precoz; Pubertad adelantada; Retraso puberal
Key words: Normal puberty; Precocious puberty; Early puberty; Pubertal delay
Pediatr Integral 2015; XIX (6): 389-410
Introducción
Las alteraciones en la cronología de la pubertad pueden determinar trastornos no solo del desarrollo gonadal y genital, sino también, del crecimiento, de la composición y proporciones corporales, así como de los aspectos psicológicos y emocionales propios de la adolescencia.
La pubertad es el periodo del desarrollo humano en el que tienen lugar los cambios biológicos y somáticos que marcan la diferencia entre la infancia y la edad adulta. Un proceso madurativo de límites muy imprecisos que, en condiciones normales, se inicia con la aparición de los caracteres sexuales secundarios y finaliza cuando se ha alcanzado la talla adulta, la maduración sexual completa y la capacidad reproductora. Este proceso conlleva no solo el desarrollo gonadal y genital, sino también, la aceleración del crecimiento, la modificación de la composición corporal y de las proporciones corporales, así como, cambios psicológicos y emocionales propios de la adolescencia. Por consiguiente, las alteraciones en la cronología de la pubertad pueden determinar trastornos en todos estos aspectos, cuya magnitud dependerá de la causa que las origine, del grado de adelanto o de retraso en su inicio y de la rapidez de su progresión.
Aspectos fisiopatológicos de la cronología puberal
La variabilidad en la edad de inicio puberal, entre individuos de condiciones de vida similares, es de unos 4-5 años. Esta variabilidad parece estar determinada por factores genéticos (˜50-80% de la variabilidad) y ambientales.
El eje hipotálamo-hipófiso-gonadal (HHG) se activa en la vida fetal, hacia la mitad de la gestación, y es posteriormente inhibido por el retrocontrol negativo de las hormonas placentarias, principalmente por el estradiol; por lo que, al nacimiento, el nivel sérico fetal de gonadotropinas es bajo. La desaparición de los esteroides placentarios después del nacimiento permite la reactivación del eje HHG, a partir aproximadamente de la 1ª semana de vida postnatal, y se mantiene activo durante los primeros meses de vida, lo que se conoce como mini-pubertad(1). La duración de esta actividad es variable, habitualmente hasta los 6-12 meses de vida, con un predominio de LH (hormona luteinizante) en los varones y de FSH (hormona folículo-estimulante) en las niñas; si bien, en ellas, la elevación de FSH suele persistir más tiempo, hasta los 2-3 años, a veces más. La secreción de gonadotropinas en la minipubertad provoca un cierto grado de estimulación gonadal. En los varones, la testosterona alcanza su pico de secreción alrededor de los 1-3 meses de vida, incrementando solo ligeramente el tamaño testicular y del pene; ya que, el aumento concomitante de los niveles de SHBG [proteína trasportadora de los esteroides sexuales (ES)] limita su actividad biológica. En las niñas, el incremento de gonadotropinas favorece el desarrollo folicular ovárico y la producción fluctuante de estradiol que puede traducirse en una telarquia del lactante que, con frecuencia, tiene también un carácter fluctuante. Después de la minipubertad, el eje HHG permanece quiescente, como consecuencia de una supresión activa de la secreción de GnRH (hormona hipotalámica liberadora de gonadotropinas), hasta que se aproxima el tiempo de la pubertad, momento en que se reactiva la secreción pulsátil de GnRH y, con ella, la de LH y FSH.
En la pubertad, LH y FSH son liberadas de forma pulsátil, inicialmente durante la noche y, posteriormente, a medida que la pubertad progresa, durante el resto del día, y actúan coordinadamente en la gónada para inducir la maduración de las células germinales (óvulos o espermatozoides) y la producción de ES, así como de otros péptidos gonadales, como es el caso, entre otros, de las inhibinas. La testosterona en el varón y el estradiol en la mujer son los principales responsables del desarrollo de los caracteres sexuales secundarios y ejercen un retrocontrol negativo en hipotálamo e hipófisis (Fig. 1), reduciendo la secreción de GnRH y LH; mientras que, las inhibinas controlan, en la hipófisis, la secreción de FSH a través de un asa de retrocontrol diferente.
Figura. 1. Eje hipotálamo-hipófiso-gonadal (HHG). La hormona hipotalámica liberadora de gonadotropinas (GnRH) induce, en las células gonadotropas hipofisarias, la síntesis y liberación pulsátil de las gonadotropinas hipofisarias, LH (hormona luteinizante) y FSH (hormona folículo-estimulante), que actúan coordinadamente en la gónada para inducir la maduración de las células germinales (óvulos o espermatozoides) y la producción de esteroides sexuales (ES), así como de otros péptidos gonadales (inhibinas, activinas, folistatina…). ES y péptidos gonadales, así como otras hormonas circulantes (leptina…), ejercen a través de mecanismos de retrocontrol, acciones estimulantes e inhibidoras, a diferentes niveles del eje HHG, modulando su complejo funcionamiento; así, por ejemplo, los ES, principalmente la testosterona en el varón y estradiol en la mujer, además de ser los responsables finales del desarrollo de los caracteres sexuales secundarios, ejercen un retrocontrol negativo en hipotálamo e hipófisis, reduciendo la secreción de GnRH y LH.
Desde el punto de vista endocrinológico(2), el primer signo del inicio de la pubertad y, por tanto, de la reactivación del eje HHG es el incremento de la secreción pulsátil de GnRH. Las neuronas productoras de GnRH tienen su origen embriológico en el ectodermo oral y a partir de la sexta semana de vida intrauterina migran desde la placoda olfatoria a su localización normal en el hipotálamo, desde donde proyectan sus axones liberadores de GnRH hacia la eminencia media. Se ha demostrado que estas neuronas, independientemente de estímulos externos, poseen la capacidad de secretar GnRH en forma pulsátil, con autorritmicidad sincronizada y espontánea; sin embargo, la amplitud de los pulsos secretorios de GnRH, cuyo incremento es característico del inicio de la pubertad, está regulada por la acción de señales estimulantes (sistema glutaminérgico, noradrenérgico, dopaminérgico, kisspeptinas…) e inhibidoras (sistema gabaérgico, opiáceos endógenos…) que, en forma de neuropéptidos y neurotransmisores, actúan en el hipotálamo. La secreción de GnRH está, además, modulada por la interacción entre las neuronas que la producen y las células gliales circundantes, así como por el sistema nervioso central (SNC) que, a su vez, integra los efectos de muchos factores externos, que influirían en el momento de inicio puberal, como serían: nutrición, ejercicio, estrés o factores sociales y psicológicos, entre otros.
Desde el punto de vista clínico, el inicio de la pubertad lo marca la aparición y el desarrollo de los caracteres sexuales secundarios, que siguen una secuencia relativamente predecible y que fue categorizada en cinco fases o estadios por James Tanner a principios de la década de los sesenta (estadios de Tanner). En las niñas, la telarquia o aparición del botón mamario suele ser el primer signo de desarrollo puberal (estadio II, a una edad media de 10,5-11 años; intervalo de 8 a 13 años) y coincide, habitualmente, con el inicio del “estirón puberal”. En los varones, el inicio de la pubertad lo marca el incremento del volumen testicular, que alcanza o supera los 4 mL o, si no se dispone de un orquidómetro, una longitud mayor o igual a 25 mm (estadio II, a una edad media de 11,5-12 años; intervalo de 9 a 14 años). En los varones, a diferencia de las niñas, el estirón puberal no coincide con el inicio de la pubertad, sino que se inicia más tardíamente, aproximadamente un año después (12,5-13 años), en el estadio III, y cuando el volumen testicular ha alcanzado los 8-12 mL de volumen.
Los datos descritos corresponden a estudios longitudinales europeos llevados a cabo en la década de los sesenta del siglo pasado. Desde mediados del siglo XIX a mediados del siglo XX, en los países occidentales desarrollados, se ha observado una mejoría en el crecimiento, con mayores tallas adultas en ambos sexos, y una tendencia a una maduración más rápida, especialmente en mujeres, donde la edad de la menarquia se ha adelantado desde los 15-17 años a menos de 14 años(3). Ambos fenómenos, conocidos como: “tendencia secular del crecimiento y desarrollo”, muestran variaciones de magnitud entre diferentes países y se han atribuido, especialmente, a la mejoría en la nutrición, salud y condiciones generales de vida; no obstante, es objeto de debate si esta tendencia secular continúa o se ha estabilizado. En cualquier caso, la edad de inicio puberal muestra una variabilidad de unos 4-5 años entre individuos con condiciones de vida similares(4). Esta variabilidad parece estar determinada por factores genéticos (˜50-80% de la variabilidad) y ambientales(5,6):
• Factores familiares y étnicos. La influencia genética en la edad de inicio puberal ha sido plenamente demostrada mediante estudios familiares y de concordancia entre gemelos monocigóticos; no obstante, sus bases genéticas no han sido claramente establecidas. Se han identificado polimorfismos en determinados genes que parecen estar relacionados con el momento de la menarquia [receptor de andrógenos, receptor alfa de estrógenos, CYP17 o proteína transportadora de esteroides sexuales (SHBG), entre otros]. Más recientemente, mediante estudios de asociación del genoma completo (GWAS), se han identificado más de 100 loci relacionados con el momento de la menarquia(4); entre los más importantes, uno en 6q21 (región próxima a LIN28B) y otro en 9q31.2 (región intergénica). También, recientemente, se ha demostrado que mecanismos epigenéticos modulan la interrelación entre genética y ambiente para poner en marcha la pubertad(5). Las diferencias en la edad de inicio puberal entre razas y etnias, al igual que ocurre entre diferentes áreas geográficas, es, probablemente, un reflejo de la combinación de factores genéticos, socioeconómicos y ambientales, cuya influencia individual es difícil de establecer; no obstante, determinadas razas, como la negra, en condiciones de vida similares, parecen mostrar una tendencia a una maduración más temprana.
• Factores nutricionales y socioeconómicos. Una adecuada nutrición y un ambiente socioeconómico favorable se asocian a un desarrollo puberal más temprano; por el contrario, condiciones nutricionales o socioeconómicas desfavorables condicionan un desarrollo puberal más tardío. En este sentido, la nutrición parece ser uno de los principales factores determinantes del momento de inicio puberal, una interrelación probablemente mediada por la leptina liberada por los adipocitos; aunque, otras sustancias, como glucosa, insulina o ghrelina podrían también actuar como fuentes de información para el hipotálamo del estado nutricional. En los países en vías de desarrollo, la malnutrición calórico-proteica (marasmo) temprana, pero no la proteica (kwashiorkor) condicionan un retraso puberal. Fuera de estas situaciones extremas, la malnutrición crónica, en general, induce un retraso puberal en ambos sexos y es, probablemente, uno de los factores responsables del retraso puberal asociado a las patologías crónicas o a la amenorrea atlética. En el otro extremo, el exceso de grasa subcutánea y el aumento del índice de masa corporal (IMC) durante el periodo prepuberal se asocian con un incremento en el riesgo de presentar una pubertad temprana, especialmente en niñas, y podrían ser uno de los factores implicados en la aceleración puberal observada en algunos países occidentales con tasas crecientes de obesidad infantil en las últimas décadas.
• Ciclo luz-oscuridad y condiciones climáticas. Aunque algunos estudios sugieren un gradiente norte-sur en la edad de la menarquia (más tardía en las latitudes norte) y la posibilidad de un efecto inhibitorio de la luz mediado por la melatonina sobre el desarrollo puberal, los efectos de la luz, el clima y la latitud en humanos son inciertos.
• Estrés crónico. El estrés crónico parece ser capaz de inhibir el eje HHG y sería uno de los factores implicados en el retraso puberal asociado a: enfermedades crónicas, ejercicio físico intenso-competición o conflictos bélicos, entre otras potenciales situaciones de estrés; no obstante, en muchas de ellas, es difícil separar el componente de estrés de otros componentes, habitualmente presentes en estas situaciones, como sería el caso de la malnutrición.
• Condiciones de vida intrauterina. Algunos estudios indican, que los recién nacidos, especialmente las niñas, con bajo peso al nacimiento (PRN < 2.500 g) o pequeños para su edad gestacional (RNPEG), muestran una mayor incidencia de pubertad adelantada o precoz, sobre todo, si experimentan un rápido crecimiento de recuperación.
• Disruptores endocrinos. En las últimas décadas, la industrialización ha producido un incremento gradual, pero significativo, en el número y cantidad de contaminantes ambientales. Algunos de ellos son sustancias, naturales o de síntesis, que debido a su similitud estructural con determinadas hormonas, pueden tener efectos negativos sobre el sistema endocrino (disruptores endocrinos)(5,6). En algunos de ellos: fitoestrógenos, estrógenos naturales (tópicos o sistémicos), pesticidas, fungicidas, sustancias químicas industriales o ftalatos, entre otros, se ha demostrado que son agentes capaces de producir en humanos: pubertad adelantada/precoz, pubertad retrasada o, incluso, trastornos de la diferenciación sexual, dependiendo de su mecanismo de acción (estrogénico, androgénico, antiandrogénico o antiestrogénico) y momento de actuación.
• Adopción. Los últimos 30 años han puesto de manifiesto la importancia, como causa de adelanto puberal, de la adopción internacional. Entre un 15-30% de los casos de pubertad precoz central (PPC) idiopática corresponden a niños adoptados de otros países, habitualmente en vías de desarrollo(3). En todos los estudios, existe un claro predominio de niñas, lo que podría estar en relación con la clásica e inexplicada preponderancia femenina en lo que a la PPC idiopática se refiere. En el año 2010, se publicaron los primeros resultados del Registro Español de Pubertad Precoz(7), donde se observó un riesgo 25 veces mayor de desarrollar PPC idiopática entre niñas adoptadas de otros países respecto a la población nacida en España. Las causas que motivan el adelanto puberal en estas niñas son desconocidas, aunque se han sugerido distintos factores, entre ellos: traslado a un ambiente socioeconómico más favorable, mejoría nutricional, reducción de la situación de estrés crónico o reducción de la exposición a disruptores endocrinos que pudieran estar inhibiendo y madurando el eje HHG. Se ha postulado, también, que el adelanto puberal podría ser el resultado de la combinación de unas condiciones vitales adversas en la infancia temprana, asociadas a condiciones de opulencia en el periodo prepuberal tardío, dos condiciones opuestas que favorecerían el desarrollo puberal temprano(8).
La duración de la pubertad es, al igual que el momento de su inicio, muy variable. En las niñas, suele utilizarse como marcador de finalización puberal el inicio de las menstruaciones, aunque, en la mayoría de los casos, en el momento de la menarquia, ni se ha completado el desarrollo puberal (estadio IV de Tanner), ni se ha finalizado el crecimiento (crecimiento postmenarquia medio de 4-6 cm, rango entre 2-12 cm), ni se ha alcanzado plenamente la fertilidad (frecuentes ciclos anovulatorios). El intervalo desde el inicio de la pubertad a la menarquia es de 2,4 años ± 1,1 año (media ± 1 SDS). Se ha observado una correlación negativa entre el inicio de la pubertad y la aparición de la menarquia; de forma que, las niñas que inician la pubertad más temprano tardan algo más en tener la menarquia que las niñas que maduran más tardíamente.
En los varones, la finalización de la pubertad es aún más difusa que en las niñas. Suele considerarse que la pubertad se ha completado cuando se alcanza un volumen testicular de adulto (media de unos 20 mL), lo que se produce habitualmente, unos 3,2 ± 1,8 años (media ± 1 SDS) después del inicio de la pubertad(2). No obstante, el criterio es poco claro, dada la variabilidad normal del volumen testicular de un adulto. De hecho, algunos varones normales no superan los 12-15 mL de volumen testicular; mientras que, otros superan los 25-30 mL. Por otro lado, como en el caso de las mujeres, en ese momento, habitualmente, tampoco se ha finalizado el crecimiento ni se han desarrollado completamente los caracteres sexuales secundarios.
Pubertad precoz (PP)
Concepto
El concepto de pubertad precoz es arbitrario, pero suele definirse como: la aparición de los caracteres sexuales secundarios antes de los 8 años en las niñas y de los 9 años en los niños (˜2,5-3 SDS por debajo de la edad media para el sexo y población estudiada; Fig. 2)(9).
Figura 2. Concepto estadístico de pubertad precoz (inicio puberal alrededor de 2,5-3 SDS por debajo de la edad media para el sexo y población estudiada), retrasada(inicio puberal alrededor de 2-2,5 SDS por encima de la edad media para el sexo y población estudiada) y normal para ambos sexos, basado en los rangos normales de inicio de la pubertad (Marshall, WA, Tanner, JM. Arch Dis Child. 1969; 44: 291).
En los últimos años, los límites de edad que delimitan el inicio normal de la pubertad y, en consecuencia, el concepto de PP han sido objeto de debate, especialmente tras la publicación en 1997 del estudio PROS (Pediatric Research in Office Setting) sobre la edad de desarrollo puberal en EE.UU. Los resultados de este estudio sugerían un inicio puberal más precoz, especialmente en las niñas afroamericanas, e hicieron plantear la conveniencia de cambiar los límites de edad para la PP a antes de los 7 años en niñas caucásicas y a antes de los 6 años en afroamericanas(10). No obstante, los potenciales errores de la metodología empleada en este estudio, así como el hecho de que estudios similares en Europa no pusieran de manifiesto la misma tendencia, han hecho que, en la mayor parte de la comunidad científica internacional, los límites de edad para considerar una pubertad como precoz no se hayan modificado.
Unido al concepto de PP, estaría el de “pubertad adelantada” (PA), como: aquella que se inicia próxima a los límites inferiores de la normalidad. Tampoco existe un consenso internacional que establezca con claridad sus límites, pero podríamos situarlos entre los 8-9 años en las niñas y entre los 9-10 años en los niños. Al igual que la PP, la PA es mucho más frecuente en niñas y se considera habitualmente la expresión de uno de los extremos del rango normal de edad de desarrollo puberal; es decir, una variante de la normalidad, que puede ser familiar (“aceleración constitucional del crecimiento y de la pubertad”; ACCP) o esporádica, pero que no precisaría, en general, tratamiento. Los niños con esta variante normal de pubertad se caracterizan, clínicamente, por un patrón de crecimiento y desarrollo característico, que conlleva un crecimiento acelerado a partir de los 1-2 años de vida, con talla prepuberal por encima del carril correspondiente a su talla diana, aceleración de la edad ósea (1-3 SDS por encima de su edad cronológica), inicio puberal a una edad en los límites inferiores del rango normal y finalización temprana del desarrollo puberal y del crecimiento, alcanzando, habitualmente, una talla acorde con su contexto familiar.
Morbilidad asociada al adelanto puberal
Las consecuencias de una PP dependen en gran medida de su etiopatogenia, pero, incluso cuando no se encuentra una base orgánica, el desarrollo precoz de la pubertad conlleva una serie de riesgos potenciales (auxológicos y psicosociales). La PA, aunque en principio no se considera patológica y, por consiguiente, no requeriría tratamiento, conlleva un riesgo intermedio entre una PP y una pubertad normal. Este riesgo es mayor cuando la pubertad es rápidamente progresiva o afecta a poblaciones con mayor riesgo de afectación de la talla adulta o a pacientes con alteraciones cognitivas. Por ello, aunque no existen criterios que permitan establecer qué pacientes podrían beneficiarse, en algunos casos muy individualizados, la PA podría ser también susceptible de tratamiento.
Riesgos auxológicos
El desarrollo puberal precoz acelera el ritmo de crecimiento, pero más aún la maduración ósea; de forma que, aunque estos niños parezcan inicialmente altos, el cierre de los cartílagos de crecimiento y la finalización del crecimiento a una edad temprana conlleva un riesgo de modificación de las proporciones corporales (acortamiento de extremidades) y, especialmente, de pérdida de talla final(11). Esta pérdida puede ser muy variable, pero suele ser tanto mayor cuanto más precoz es el inicio puberal, mayor la edad ósea (EO), mayor el tiempo de evolución y mayor la rapidez de progresión de la EO y del desarrollo puberal. Además, existirían determinadas poblaciones de riesgo para una mayor afectación de la talla, como serían aquellos pacientes con:
• Talla baja en el momento del diagnóstico.
• Cuadro sindrómico asociado a talla baja.
• Antecedentes de RNPEG.
• Deficiencia asociada de hormona de crecimiento (GH).
• Patología oncológica con radioterapia craneal y, especialmente, cráneo-espinal.
• Antecedentes de adopción internacional.
En cualquier caso, la repercusión auxológica es muy difícil de predecir en un sujeto concreto; ya que, los métodos de predicción de talla adulta de que disponemos son inadecuados para este tipo de pacientes y existen mecanismos normales de compensación responsables de que no en todas las PP la talla final sea baja.
Riesgo psicosocial
Las consecuencias psicosociales y conductuales de presentar una PP han sido poco estudiadas y, además, pocas veces son tenidas en consideración a la hora de valorar a estos pacientes. En las niñas, donde mayoritariamente se han llevado a cabo estos estudios, se han descrito situaciones de estrés y de dificultad de adaptación ante los rápidos cambios físicos y psicológicos que se producen, rechazo por parte de sus compañeros y tendencia al aislamiento y a la depresión. Ambos sexos, pero sobre todo los varones, pueden mostrar un aumento de la líbido, con desarrollo de conductas masturbatorias o sexuales inadecuadas, especialmente si existe un cierto grado de retraso mental que limite su capacidad de control. En las niñas, se ha descrito también un inicio más precoz de las relaciones sexuales e, incluso, un mayor riesgo de abuso sexual. Las pacientes que han tenido una PP muestran en la adolescencia más problemas de conducta, incluso delictiva, menor competencia social y suelen alcanzar niveles educativos más bajos(12). Esta desadaptación social parece limitarse a la adolescencia y desaparece en la edad adulta. En cualquier caso, al igual que ocurre con los riesgos auxológicos, los riesgos psicosociales en un paciente concreto son difíciles de predecir.
Otros riesgos potenciales
Aunque los datos disponibles son todavía insuficientes para poder establecer conclusiones definitivas, las mujeres adultas con antecedentes de menarquia temprana parecen presentar un mayor índice de masa corporal (IMC), con incremento de grasa abdominal, mayores cifras de tensión arterial y de hemoglobina glicada, así como un peor perfil lipídico. Todos estos factores sugieren que estas mujeres tendrían un mayor riesgo cardiovascular y de diabetes y, por tanto, de morbimortalidad. También, se ha sugerido en los pacientes con PP un posible incremento en el riesgo de cáncer de mama y de testículo.
Clasificación y epidemiología
El incremento de ES, que es lo que determina la aparición y desarrollo de los caracteres sexuales secundarios, puede tener distinto origen (Tabla I), lo que permite clasificar la PP en:
• PP central (PPC). Conocida, también, como: PP verdadera o PP dependiente de gonadotropinas; ya que, el incremento de ES es el resultado de una reactivación normal, pero precoz, del eje HHG y, por ello, siempre es isosexual.
• PP periférica (PPP).Conocida, también, como: pseudopubertad precoz o PP independiente de gonadotropinas. La fuente de ES puede ser exógena o endógena, gonadal o extragonadal, pero, en cualquier caso, el desarrollo de los caracteres sexuales secundarios no es la consecuencia de la activación del eje HHG. Dependiendo del ES aumentado (andrógeno o estrógeno) y del sexo del niño, las manifestaciones clínicas puede ser isosexuales (apropiadas al sexo del niño) o contrasexuales (contrarias al sexo del niño).
• PP mixta (PPM). Se la conoce, también, como: PP combinada o PPC secundaria; ya que, resulta de una mezcla o combinación de una PPP y una PPC. La exposición prolongada a ES, provocada por una PPP, aceleraría el crecimiento, la EO y la maduración de los centros hipotalámicos implicados en el inicio del desarrollo puberal, causando la reactivación precoz del eje HHG y el desarrollo secundario de una PPC.
La PP es una patología infrecuente, con una incidencia difícil de establecer (1:5.000-10.000 niños)(2) y, al contrario de lo que ocurre con la pubertad retrasada, con un claro predominio en niñas (relación que oscila entre 3:1 y 23:1 según las series; 10:1 en el estudio español de 2010(7)). Más del 90% de los casos corresponden a formas de PPC y la gran mayoría son de etiología idiopática. En el caso de pacientes con trastornos o lesiones del sistema nervioso central (neurofibromatosis, hidrocefalia, mielomeningocele…), determinados síndromes (Beuren-Williams…) o, como ya ha sido comentado, procedentes de adopción internacional, la frecuencia de PPC es claramente superior a la del resto de la población.
Etiopatogenia y manifestaciones clínicas
Pubertad precoz central (PPC)
La PPC se debe a una reactivación precoz del eje HHG y se caracteriza clínicamente por un desarrollo precoz de los caracteres sexuales secundarios, que siempre son isosexuales y que siguen la secuencia normal de aparición, con aumento del tamaño y de la actividad de las gónadas.
La PPC se caracteriza clínicamente, en las niñas, por la aparición (telarquia) y desarrollo progresivo de la mama antes de los 8 años, que puede ser, inicialmente y durante unos meses, unilateral, y por el incremento del volumen testicular (=4 mL) en los varones antes de los 9 años, que es seguido, habitualmente y en ambos casos, por el desarrollo de la pubarquia y axilarquia. La EO se adelanta, habitualmente más de 2 SDS por encima de la edad cronológica y, en las niñas, la VC experimenta una rápida aceleración (estirón puberal) que coincide o incluso puede preceder a la aparición del botón mamario. En los varones, el estirón puberal es un fenómeno más tardío en el desarrollo puberal (estadio III-IV de Tanner) y no suele coincidir con el incremento inicial del volumen testicular; no obstante, en los casos de PPC, también tiende a adelantarse (finales del estadio II o principio del III)(13).
Es una patología con un claro predominio en niñas, en las que la etiología es habitualmente idiopática (Fig. 3); mientras que, en los niños son más frecuentes que en las niñas las causas orgánicas (40-90% en varones frente a un 8-33% en niñas)(9). El motivo de estas diferencias entre sexos es desconocida. Otro factor relacionado con la organicidad es la edad; de forma que, a menor edad de inicio puberal, mayor riesgo de organicidad.
Figura. 3. Distribución por categorías diagnósticas en varones y mujeres con pubertad precoz (PP). La figura muestra los resultados, en porcentajes, de una serie de 93 pacientes recogidos entre 1971 y 1977 en Francia (JC Job y M Pierson. Endocrinología Pediátrica y Crecimiento. Barcelona: Editorial Científico-Médica 1983). PP: pubertad precoz; PPCI: pubertad precoz central idiopática; PPCO: pubertad precoz central de etiología orgánica; PPP: pubertad precoz periférica.
Dentro de las formas de PPC idiopática, alrededor de un 30% son familiares(2). Es probable que la mayoría correspondan a formas más o menos extremas de ACCP; no obstante, se han descrito situaciones de PPC familiares de base monogénica(14). Las primeras que se describieron fueron mutaciones activadoras en el sistema de las kisspeptinas, un grupo de péptidos que resultan del proceso proteolítico del producto del gen KiSS1 (1q32), secretados por neuronas de los núcleos arcuato y anteroventral del hipotálamo, y que se consideran como unos de los principales mediadores del inicio de la pubertad. Estos péptidos, en condiciones normales, incrementan su secreción antes del inicio de la pubertad y se unen a un receptor ligado a las proteínas G de la membrana de las neuronas productoras de GnRH, denominado GPR54 (GPR54 o KiSS1R, en 19p13.3), incrementando considerablemente la amplitud de los picos secretorios de GnRH. Se han descrito dos mutaciones activadoras en KiSS1, una en homocigosis y otra en heterocigosis, y una mutación activadora en el gen que codifica para su receptor (KiSS1R), todas ellas asociadas a una PPC hereditaria, aunque con expresividad familiar variable. Más recientemente, se han descrito, en varias familias con PPC familiar, mutaciones en heterocigosis, con pérdida de función en el alelo paterno, en el gen MKRN3 (15q11.2). El gen MKRN3 está localizado en la región crítica del síndrome de Prader-Willi y sometido a impronta genética (en condiciones normales, solo se expresa el gen de origen paterno) y codifica para una proteína relacionada con la ubiquitinación de proteínas, pero de funcionalidad incierta.
Dentro de las causas orgánicas de PPC, la más frecuente es el hamartoma hipotalámico(15), que puede encontrarse en un 2-28% de los casos de PPC (Fig. 4).
Figura. 4. Pubertad precoz central orgánica por hamartoma hipotalámico. Varón de 18 meses de edad con talla alta (+2 SDS), incremento de la velocidad de crecimiento, aumento del volumen testicular (6 mL de volumen) y del tamaño del pene, hábito atlético y aceleración de la edad ósea (4 años). Testosterona elevada (1,8 ng/mL; VN para la edad < 0,24) con test de LHRH de características puberales (cociente LH/FSH > 1 y pico de LH de 25 mUI/mL). En la RM craneal, se observa una masa retroquiasmática que cuelga del hipotálamo (flecha) y que corresponde al hamartoma hipotalámico. El paciente recibió tratamiento con triptorelina i.m. mensual con frenación completa del eje hipotálamo-hipófiso-gonadal y regresión parcial de los caracteres sexuales secundarios.
Estos tumores son malformaciones congénitas benignas formadas por tejido nervioso desorganizado en el que se incluyen neuronas productoras de GnRH. Aunque se ha especulado que estas neuronas podrían actuar como un generador ectópico de GnRH, el mecanismo responsable de la PPC no está plenamente aclarado. Típicamente, en la RM craneal, los hamartomas aparecen como una masa pedunculada que cuelga del hipotálamo, entre el tuber cinereum y los cuerpos mamilares, justo detrás del quiasma óptico. Pueden ser asintomáticos o asociarse a: PPC, crisis gelásticas (crisis comiciales de risa inmotivada), epilepsia secundariamente generalizada y alteraciones cognitivas y conductuales. La mayoría de estos tumores no crecen o lo hacen muy lentamente y responden al tratamiento habitual con análogos de GnRH; por lo que, la cirugía no suele estar indicada, salvo que condicionen una epilepsia intratable.
Otras múltiples alteraciones del sistema nervioso central (SNC), como: malformaciones, tumores, gliomas hipotalámicos o del quiasma en la neurofibromatosis tipo I, displasia septo-óptica, mielomeningocele e hidrocefalia, entre otras, pueden provocar una pubertad precoz (Tabla I). Se cree que estas lesiones alterarían las señales de inhibición tónica que recibe el hipotálamo, favoreciendo la reactivación del eje HHG.
La irradiación craneal, utilizada en el tratamiento de tumores del SNC o como tratamiento coadyuvante en otras patologías oncológicas, como la leucemia linfoblástica aguda, sobre todo cuando se administra a edades muy precoces, puede predisponer al desarrollo de una PA o PPC. Dosis bajas de radioterapia (18-24 Gy) a menudo se asocian a PPC en niñas; mientras que, dosis por encima de 25 Gy incrementan el riesgo de PPC en ambos sexos, con frecuente asociación a deficiencia de GH, combinación que puede ser especialmente negativa para la talla adulta del paciente. Por encima de los 30 Gy, es frecuente que tras una pubertad temprana/precoz desarrollen una deficiencia de gonadotropinas (hipogonadismo hipogonadotropo). Cuando se administran 50 o más Gy, no suele haber PP, sino una falta de desarrollo puberal secundaria a hipogonadismo hipogonadotropo(15). El diagnóstico de la PPC secundaria a irradiación craneal puede retrasarse o dificultarse debido a sus peculiaridades clínicas: la ausencia/disminución del estirón puberal, por la frecuente deficiencia asociada de GH, y, en el caso de los varones, el escaso o nulo incremento del volumen testicular por efecto de la quimioterapia recibida (hipogonadismo hipergonadotropo).
La neurofibromatosis, al igual que otros síndromes (Tabla I), en ausencia de gliomas del quiasma o hipotalámicos, presenta, también, con mayor frecuencia que la población normal PPC o PA.
Pubertad precoz periférica (PPP)
Es aquella PP en la que el incremento de ES responsable del desarrollo de los caracteres sexuales secundarios no es debido a una activación prematura del eje HHG. Por tanto, no es una verdadera pubertad, sino una pseudopubertad precoz, y los caracteres sexuales secundarios pueden, no solo perder su secuencia de aparición habitual, sino, en algunos casos, ser contrarios al sexo del paciente (contrasexuales).
Los ES implicados en el desarrollo de una PPP pueden ser andrógenos, estrógenos o una mezcla de ambos(2,13), y su origen exógeno (fuentes externas alimenticias, tópicas, orales o parenterales) o endógeno (suprarrenal o gonadal). El eje HHG no solo no está activado, sino que suele estar completamente inhibido por el exceso de ES circulantes, a través de los mecanismos normales de retrocontrol negativo. Las manifestaciones clínicas de la PPP dependen, fundamentalmente, del tipo de ES responsable:
• En las niñas, la pérdida de la secuencia normal en la aparición de los caracteres sexuales secundarios supone que, por ejemplo, el primer signo de desarrollo puberal pueda ser una menstruación, sin un claro desarrollo mamario previo ni aceleración del crecimiento. El hallazgo de hiperpigmentación areolar precoz con desarrollo mamario todavía incompleto es sugerente de rápida y marcada elevación de los niveles séricos de estrógenos (Fig. 5).
Figura. 5. Pubertad precoz periférica secundaria a tumor ovárico secretor de estrógenos. Niña de 14 meses que consultó por telarquia bilateral de, aparentemente, solo 15 días de evolución, con aceleración de la velocidad de crecimiento (talla en +5 SDS) y sangrado vaginal dos días antes de la consulta. En la exploración, se observó una telarquia bilateral (T3 de Tanner) con hiperpigmentación areolar (dato clínico sugerente de alta concentración de estrógenos), sin pubarquia ni axilarquia. Los niveles de estradiol se encontraron muy elevados (230 pg/mL; VN prepuberales < 10). En la ecografía, masa ovárica izquierda de 30 x 20 mm, que se confirmó en la RM pélvica (flecha en la figura). El estudio anatomopatológico estableció el diagnóstico de quiste luteínico. Regresión posterior de los caracteres sexuales secundarios tras la cirugía.
La presencia de un sangrado vaginal en ausencia completa de telarquia es más sugerente de una causa local (agresión sexual, cuerpo extraño o tumor vaginal) que de una verdadera PP. Un acné severo, de rápida progresión y, especialmente, el agrandamiento del clítoris (virilización) debe hacernos sospechar la presencia de un tumor productor de andrógenos. El vello pubiano que aparece precozmente y progresa lentamente, en ausencia de telarquia ni de otros signos de virilización, no sugiere PP central ni periférica, sino un incremento leve de la producción suprarrenal de andrógenos, habitualmente una adrenarquia prematura aislada (hiperplasia suprarrenal congénita de presentación tardía o una variante de la normalidad).
• En el caso de los varones, es muy característico de la PPP, el desarrollo progresivo de signos de virilización, como sería el incremento del tamaño del pene, sin un aumento significativo del tamaño testicular. En algunos casos (testotoxicosis, restos adrenales testiculares, tumores productores de gonadotropina coriónica –HCG–, etc.) el volumen testicular puede incrementarse ligeramente (4-8 mL), pero, en cualquier caso, es un volumen inadecuado para el grado de desarrollo de los caracteres sexuales secundarios. Al igual que en las niñas, el vello pubiano moderado que aparece precozmente y progresa lentamente, en ausencia de agrandamiento testicular o del pene, no sugiere PP central ni periférica, sino adrenarquia prematura aislada. El desarrollo de signos feminizantes (ginecomastia marcada) es excepcional, pero puede producirse en el contexto de exposición a una fuente externa de estrógenos o en raros casos de tumores testiculares (tumor de células de Sertoli asociado al síndrome de Peutz-Jegher) o adrenales productores de estrógenos.
Las causas que pueden determinar una PPP quedan reflejadas en la tabla I. Las dos entidades nosológicas más características responsables de PPP son: el síndrome de McCune-Albright y la testotoxicosis.
El síndrome de McCune-Albright (SMA) es una enfermedad rara, con una prevalencia estimada de 1:100.000-1.000.000, más frecuente en niñas, aunque puede darse en ambos sexos(16). Originalmente, fue definido clínicamente por la tríada de: displasia fibrosa poliostótica, manchas de color “café con leche” de bordes irregulares (“en costa de Maine”) y PPP, debida al desarrollo de quistes ováricos autónomos secretores de estrógenos. Posteriormente, se ha visto que otras endocrinopatías hiperfuncionantes pueden estar presentes, como: hipertiroidismo, gigantismo hipofisario, hipercortisolismo o raquitismo hipofosfatémico, entre otras. Se debe a una mutación activadora postcigótica en el gen de la subunidad alfa de la proteínas G de la membrana (GNAS1; 20q13.32), que se produce temprano en la embriogénesis y determina un mosaicismo que puede afectar, de forma variable, a tejidos endocrinos (gónadas, tiroides, adrenales, hipófisis y paratiroides) y no endocrinos (timo, bazo, páncreas, riñón, corazón, etc.). Debido a ello, la expresividad clínica puede ser, también, muy variable y el diagnóstico, en algunos casos, difícil.
La testotoxicosis o PP familiar del varón es una forma de PPP limitada a los varones, debida a una mutación activadora, de herencia autosómica dominante (esporádica o familiar) en el receptor de LH (LHCGR; 2p16.3), que ocasiona una activación autónoma de las células de Leydig. Suele ponerse de manifiesto a los 2-4 años de edad con la aparición de: signos puberales, virilización y aceleración del crecimiento que conduce a una talla final baja por cierre precoz de los cartílagos de crecimiento. En niñas, estas mutaciones no producen PPP; ya que, es necesaria la presencia de LH y FSH para la producción de estrógenos.
Los quistes foliculares ováricos secretan estrógenos de forma transitoria, lo que puede ocasionar desarrollo mamario y, en ocasiones, cuando la producción estrogénica cae, sangrado vaginal esporádico. Los quistes que producen esta sintomatología suelen ser relativamente grandes y pueden ser recurrentes, lo que puede acelerar la maduración ósea y favorecer el desarrollo de una PA o una PPC secundaria. Además, en los que alcanzan un mayor tamaño, puede favorecerse la torsión ovárica y la necesidad de tratamiento quirúrgico.
La exposición a ES exógenos (disruptores endocrinos) puede determinar una PPP iso o contrasexual, dependiendo de su acción hormonal y del sexo del paciente. Una de las hipótesis propuestas para explicar la alta incidencia de PA/PPC en niñas adoptadas de países en vías de desarrollo sería la de los disruptores endocrinos. En estas niñas se han encontrado frecuentemente niveles elevados de pesticidas derivados del DDT (diclorodifenildicloroetano), productos que siguen utilizándose en estos países como insecticidas en el ámbito rural. Según esta hipótesis, la exposición crónica a la actividad estrogénica de estos productos podría madurar el hipotálamo al tiempo que suprimiría su actividad. La eliminación de la exposición al migrar a países desarrollados, donde estos pesticidas están prohibidos, supondría el incremento de la liberación de GnRH y el inicio de la pubertad.
El hipotiroidismo primario severo y de larga duración puede, aunque raramente, presentarse como una PP (síndrome de Van Wyk-Grumbach) a través de mecanismos no completamente aclarados, pero que podrían afectar tanto a la hipófisis como a la gónada. Clínicamente, las niñas suelen presentar telarquia con galactorrea, por aumento concomitante de prolactina por acción de TRH (hormona hipotalámica estimulante de la secreción de TSH), y sangrados vaginales recurrentes; por su parte, los niños suelen mostrar incremento prematuro del volumen testicular. Estos signos puberales desaparecen con el tratamiento con L-tiroxina. La peculiaridad clínica de esta rara forma de PP es que, a diferencia de las demás, cursa con enlentecimiento del crecimiento y retraso de la EO.
La hiperplasia suprarrenal congénita, especialmente en su forma clásica, si está insuficientemente tratada, puede producir un PPP isosexual en el varón y contrasexual en la niña. De forma característica, en el varón, el tamaño testicular permanece prepuberal; no obstante, en algunos casos, pueden existir restos (habitualmente bilaterales) de tejido adrenal en los testículos y crecer por el efecto de la ACTH aumentada, requiriendo diagnóstico diferencial con una PPC o con tumores testiculares de otra extirpe anatomopatológica.
Tumores ováricos, testiculares o adrenales productores de ES, son causas raras de PPP iso o contrasexual. Los tumores ováricos (sobre todo los de células de la granulosa/teca) frecuentemente causan síntomas locales (dolor, distensión, ascitis, efecto masa, etc.) y suelen secretar estrógenos, aunque en ocasiones producen andrógenos y virilización. El diagnóstico en las formas típicas se basa en el hallazgo ecográfico de una masa sólida o sólido-quística en el ovario, con niveles séricos elevados de estradiol y suprimidos de LH/FSH (Fig. 5). Los tumores testiculares más frecuentemente asociados a PPP son los derivados de las células de Leydig, que suelen ser benignos en la infancia y presentarse con signos de virilización, incremento del tamaño de uno de los testículos (nódulo, frecuentemente palpable) y niveles séricos elevados de testosterona. Los tumores adrenales (adenomas y adenocarcinomas) suelen producir andrógenos (virilización) y cortisol (síndrome de Cushing); si bien, excepcionalmente pueden producir también estrógenos y feminización.
La resistencia generalizada a glucocorticoides es una rara enfermedad autosómica dominante, debida a mutaciones en el gen del receptor de los glucocorticoides (GCCR; en 5q31.3), que conlleva el aumento compensador de las concentraciones circulantes de la hormona adrenocorticotrópica (ACTH), lo que incrementa la producción de esteroides adrenales con actividad mineralocorticoide y/o androgénica, e incrementa la excreción urinaria de cortisol libre sin ninguna evidencia clínica de hipercortisolismo.
Tumores productores de gonadotropina coriónica (HCG), de efecto biológico similar a la LH, inducen en los niños la producción por las células de Leydig de testosterona y un incremento moderado del volumen testicular(15). En las niñas, estos tumores no producen PP; ya que, que es necesaria la presencia de ambas gonadotropinas, LH y FSH, para el desarrollo de los folículos ováricos. Los hepatoblastomas son los tumores más frecuentes productores de HCG, pero esta puede también ser producida, entre otros, por: pinealomas, germinomas intracraneales, coriocarcinomas o tumores de células germinales (testiculares o extratesticulares). El hallazgo de un tumor extratesticular de células germinales, especialmente mediastínico, obliga a descartar un síndrome de Klinefelter, donde la frecuencia de este tipo de tumores es 50 veces mayor que en el resto de la población. La presencia de marcadores tumorales alfa-fetoproteína y b-HCG) puede ser útil en el diagnóstico de este tipo de tumores.
Pubertad precoz mixta o combinada
Se habla de PP mixta o combinada, cuando una PPP desencadena secundariamente una PPC.
Niños expuestos a altos niveles séricos de ES como consecuencia de una PPP (hiperplasia suprarrenal congénita pobremente controlada, SMA…) pueden desarrollar una posterior PPC. Se ha especulado que los ES podrían “impregnar” el hipotálamo, causando la maduración del eje HHG y la puesta en marcha de la PPC; o bien que, el hipotálamo, acostumbrado a una inhibición por niveles muy elevados de ES, al disminuir estos como resultado de un tratamiento efectivo de la PPP, se reactivara, poniendo en marcha la PPC. En la mayoría de los casos, la PPC solo se inicia si la EO es superior a los 10 años.
Evaluación diagnóstica
La aparición antes de los 8 años en las niñas y de los 9 años en los niños de los caracteres sexuales secundarios, puede ser la manifestación de una PP (central o periférica y de causa orgánica o idiopática), pero con más frecuencia se tratará de una variante normal, benigna y no progresiva, de pubertad, que no requerirá habitualmente tratamiento (Algoritmo 1). Por ello, un diagnóstico correcto puede evitar costosos y prolongados tratamientos no exentos de potenciales efectos secundarios. La evaluación diagnóstica de estos pacientes conlleva una anamnesis y exploración completas, con énfasis en determinados aspectos, y un número limitado de pruebas complementarias básicas(9).
Anamnesis detallada
Debe interrogarse sobre la edad y orden de aparición de los caracteres sexuales secundarios, así como sobre las características de su progresión (rápida, lenta, cíclica). En las niñas, la evolución cíclica de la telarquia es muy sugerente de quistes foliculares recurrentes. La aparición precoz de vello pubiano y/o axilar sin otros signos de virilización (clitoromegalia o aumento del tamaño del pene, hirsutismo, marcada aceleración de la EO, aumento de la masa muscular…) sugiere adrenarquia prematura (variante de la normalidad) y no PP, y puede acompañarse de otros signos de androgenización leve-moderada, como: aceleración de la EO de 1-2 años, olor corporal de características puberales, presencia de comedones o acné leve y aumento de grasa en el pelo. Deben recogerse y llevarse a la gráfica de crecimiento los datos de la evolución de la talla, el peso y, sobre todo, de la VC. Debe interrogarse, también, sobre posibles signos de hipertensión intracraneal (cefalea, vómitos o trastornos visuales) sugerentes de patología orgánica intracraneal. Los antecedentes familiares (padres, hermanos y familiares próximos) de PA o PP, así como de patologías hereditarias que puedan modificar el tempo normal de la pubertad deben ser recogidas (hiperplasia suprarrenal congénita, testotoxicosis, resistencia a glucocorticoides…).
Exploración física
Se deben recoger cuidadosamente los parámetros antropométricos (talla, peso y proporciones corporales), el estadio puberal de Tanner, así como otros datos sugerentes de desarrollo puberal, virilización o feminización: olor corporal, acné, ginecomastia, galactorrea, pigmentación areolar, estrogenización de la mucosa vaginal, leucorrea, volumen y simetría testicular, tamaño del clítoris, etc. Debe recogerse, también, la presencia, localización y características de manchas cutáneas sugerentes de neurofibromatosis o SMA.
Edad ósea (EO)
Suele ser la primera prueba complementaria a realizar ante la sospecha de una PP; ya que, en condiciones normales, el grado de desarrollo puberal se correlaciona mejor con la EO (r = 0,82) que con la edad cronológica (r = 0,72). Así, por ejemplo, en las niñas, el desarrollo mamario se inicia a una EO media de 10,75 años y la menarquia se produce a una EO media de 13 años, con una varianza para la EO que es la mitad de la correspondiente a la EC. Además, trastornos que aceleran la EO (hiperplasia suprarrenal congénita…) se asocian a PA y los que la retrasan (deficiencia de GH, hipotiroidismo, patología crónica…) a pubertad retrasada. En las PPC idiopáticas, la EO está típicamente acelerada al menos un 20% por encima de la edad cronológica (˜2 SDS) y, en el caso de las niñas, próxima, habitualmente, a los 10-11 años. Por el contrario, en las PP de causa orgánica, la aceleración de la EO es más variable y depende de la duración y grado de exposición previa a los ES. También, la EO es útil para realizar predicciones de talla adulta y valorar la posible repercusión de la PP sobre la talla final, tanto en el momento del diagnóstico como a lo largo del seguimiento del paciente; no obstante, hay que tener en consideración que la fiabilidad de estas predicciones, en condiciones normales es escasa y, en los pacientes con PP, cuando la EO está muy acelerada, todavía menor y con tendencia a sobrevalorar las expectativas de talla adulta.
Determinaciones hormonales
La presencia de niveles séricos elevados de estradiol o testosterona sería, lógicamente, lo primero a demostrar ante una sospecha de PP; sin embargo, su determinación puede no ser de mucha utilidad en las fases iniciales de la pubertad, ya que, se sitúan con frecuencia por debajo del límite de detección de los inmunoanálisis convencionales, especialmente en el caso del estradiol.
La determinación en suero de andrógenos suprarrenales o de sus precursores, especialmente: sulfato de dehidroepiandrosterona (SDHEA), ∆4-androstendiona y 17-OH-progesterona, puede ser de utilidad en aquellas situaciones clínicas sugerentes de incremento de andrógenos de posible origen adrenal, como sería el caso de tumores suprarrenales o de la hiperplasia suprarrenal congénita; en este último caso, puede ser necesaria la estimulación previa con ACTH (test de ACTH) para descartar formas de presentación tardía.
La prueba hormonal más importante en el diagnóstico de PP es la determinación de los niveles séricos de gonadotropinas (LH y FSH) tras estímulo con 100 µg/m2 de LHRH (test de LHRH) o con un análogo de GnRH (test de GnRHa)(17). Esta prueba nos permitiría distinguir, al menos teóricamente, una PPC (patrón de respuesta puberal: claro incremento de LH y FSH, con predominio de LH: cociente LH/FSH > 1) de una variante de la pubertad no progresiva (patrón de respuesta prepuberal: escaso o nulo incremento de LH y FSH con predominio de FSH: LH/FSH <1) y de una PPP (secreción de LH/FSH inhibida). No obstante, su interpretación no siempre es sencilla; ya que, los puntos de corte diagnósticos (pico de LH) no son claros y dependen en gran medida de la sensibilidad y fiabilidad del inmunoanálisis empleado. Con los inmunoanálisis más modernos, el punto de corte para una respuesta prepuberal de LH sería de alrededor de 5 mUI/mL. Por otra parte, en la situación más frecuente en la práctica clínica, como es el caso de las niñas con inicio de desarrollo mamario entre los 7 y 8 años (70% de las telarquias prematuras), la diferenciación entre una PPC idiopática (susceptible de tratamiento) y una telarquia prematura aislada (variante de la normalidad que no precisa tratamiento) puede ser muy difícil y, a veces, solo un seguimiento estrecho puede diferenciarlas (Tabla II). En estos casos, es frecuente el hallazgo de un patrón de respuesta de LH y FSH a LHRH intermedio entre lo que hemos denominado puberal y prepuberal (incremento moderado en los picos de secreción de LH y FSH con predominio de FSH o solo un claro incremento de FSH); de hecho, algunos autores consideran que estas formas de telarquia prematura de evolución variable (pueden regresar, mantenerse sin progresar o progresar lentamente) serían parte de un continuum en la activación del eje HHG y que entre un 15-20% de ellas terminan evolucionando hacia una PP.
En los últimos años, la disponibilidad de inmunoensayos más sensibles y fiables para la determinación de gonadotropinas ha hecho que se plantee la posibilidad de determinar solo los niveles basales de gonadotropinas, en concreto de LH, para el diagnóstico o, al menos, el cribado de una PPC. Niveles basales de LH = 5 mUI/mL serían sugerentes de PPC, gonadotropín-dependiente; no obstante, el solapamiento en los resultados entre los pacientes prepuberales y aquellos que se sitúan en fases iniciales de la pubertad y la multiplicidad de inmunoanálisis utilizados, desaconsejan, al menos de momento, semejante práctica.
Pruebas de imagen
Una RM craneal, para evaluar la anatomía de la región hipotálamo-hipofisaria y descartar patología orgánica, debería realizarse si se demuestra una activación precoz del eje HHG, especialmente en varones, donde el riesgo de patología orgánica es claramente superior (40-90% en varones frente a un 8-33% en niñas)(9). En las niñas, cuando la pubertad se inicia entre los 6 y los 8 años y sin sintomatología neurológica, el riesgo de patología orgánica es muy escaso (2-7%) y se discute la conveniencia de realizar una RM craneal; no obstante, la mayoría de los centros continúa realizándola.
La ecografía abdómino-pélvica puede, además de descartar la presencia de tumoraciones (suprarrenales, ovario, hígado, etc.) responsables de una PPP, permitirnos, en el caso de las niñas, valorar el tamaño ovárico y uterino. Un volumen ovárico (longitud x anchura x altura x 0,5233) de <1 mL es claramente prepuberal, pero los límites para considerarlo puberal, varían entre 1 y 3 mL, según los autores. La presencia de pequeños quistes (<9 mm), en ocasiones múltiples (2 a 4), es un hallazgo frecuente y normal en niñas prepuberales (50-80%). Típicamente, no suelen producir cantidades significativas de estrógenos, aunque en ocasiones pueden elevar transitoriamente sus niveles séricos, determinando un desarrollo mamario transitorio. Un incremento del volumen (>2 mL), una relación cuerpo/cuello mayor de 1 o la presencia de línea endometrial, son signos sugerentes de niveles elevados de estrógenos circulantes y, por tanto, de inicio puberal.
La ecografía testicular puede ser de utilidad en varones con pubertad precoz periférica, especialmente si existe asimetría testicular, para detectar tumores o restos adrenales, en ocasiones no palpables.
Otros estudios
Dependiendo del caso y de los resultados previos, otros estudios pueden estar indicados: función tiroidea (hipotiroidismo en el síndrome de Van-Wyk-Grumbach o posible hipertiroidismo en el SMA), mapa óseo (lesiones de displasia fibrosa en SMA), marcadores tumorales (b-HCG, alfa-fetoproteína), estudios moleculares (detección de mutaciones conocidas), etc.
Tratamiento
El tratamiento de la PP central lo que pretende es, según los casos: revertir, detener o, al menos, enlentecer el desarrollo de los caracteres sexuales secundarios, conservar el potencial de crecimiento y evitar las consecuencias psicosociales y conductuales de una pubertad temprana.
Pubertad precoz central
En este caso, el tratamiento busca frenar o suprimir la activación del eje HHG. El tratamiento de elección son los análogos de GnRH (GnRHa) de liberación sostenida (depot). En los casos en los que exista una causa orgánica, deberá hacerse tratamiento etiológico si es posible, aunque este, rara vez tiene efecto sobre la evolución de la pubertad.
La administración de GnRHa de liberación sostenida produce, tras una breve estimulación de la liberación de gonadotropinas, una prolongada desensibilización de los receptores hipofisarios de GnRH, con inhibición de la secreción de LH/FSH y, como consecuencia, de la producción y liberación de ES. Los más utilizados son: la triptorelina depot, a la dosis de 80-100 µg/kg, y el acetato de leuprolerina, a la dosis de 150-200 µg/kg, que se administran, ambos, por vía intramuscular cada 25-28 días. Más recientemente, se han introducido preparados depot de una duración de 3 meses, pero la experiencia en su utilización en la PPC es menor y no se han aprobado en nuestro país para esa indicación(9). Tampoco han sido aprobados en Europa, los implantes subcutáneos de histrelina, un análogo de GnRH con efecto inhibidor de la secreción de LH y FSH superior a un año(9,18).
La utilización de los GnRHa en los casos de PPC idiopática con inicio a una edad próxima a los límites considerados normales es controvertida; ya que, los efectos beneficiosos del tratamiento sobre la talla final son, en la mayoría de los pacientes, escasos o nulos. Por ello, no existe un consenso internacional(19) y la indicación de tratamiento se establece de forma individualizada, teniendo en consideración factores psicosociales (repercusión psicológica, familiar, social y conductual) y auxológicos (expectativas de crecimiento, edad ósea, rapidez de progresión de la EO y de los caracteres sexuales secundarios). Tras el inicio de la terapia, la VC puede disminuir considerablemente; en estos casos, algunos estudios han sugerido que la adición de GH al tratamiento con GnRHa podría mejorar la VC y las expectativas de talla final; no obstante, no existen suficientes estudios controlados que demuestren la seguridad y eficacia de esta asociación, para poder establecer una clara indicación.
Otro aspecto controvertido sería el momento más adecuado para suspender el tratamiento con GnRHa. Aunque no existe consenso, en el caso de las niñas, se recomienda que se haga a una edad cronológica de ˜11 años y EO de ˜12-12,5 años; ya que, por encima de estas edades podría no solo no mejorar, sino incluso empeorar las expectativas de talla adulta. En los varones, la experiencia es muy escasa y suele recomendarse, sin mucha base científica, la suspensión del tratamiento alrededor de los 12 años de edad cronológica y de los 13-13,5 años de EO(17). Pocas semanas o meses después de la suspensión, la pubertad progresa y se recupera la respuesta puberal al estímulo con GnRH. En las niñas, la menarquia se produce, habitualmente, entre 6 y 18 meses después.
Los resultados del tratamiento con GnRHa sobre la talla final varían de unos pacientes a otros; aunque, en general, la mayoría de ellos alcanzan una talla final en el rango bajo de su talla diana y con escasos efectos secundarios locales (abscesos estériles, infecciones…) y generales (cefalea, sofocos…).
Pubertad precoz periférica
Los objetivos del tratamiento de la PPP son similares a los de la PPC; si bien, en este caso, los GnRHa son ineficaces y lo que se utilizan son fármacos que inhiben directamente la producción de ES o su acción sobre los órganos diana.
El tratamiento de la PPP será etiológico, en aquellos casos en los que sea posible: quirúrgico (extirpación del tumor ovárico, testicular, suprarrenal o productor de HCG), o médico (tratamiento con hidrocortisona en la hiperplasia suprarrenal congénita, quimioterapia en los suprarrenalomas malignos metastásicos, etc.). En el resto de los casos, el tratamiento será sintomático, con fármacos que, como: ketoconazol, acetato de ciproterona, espironolactona, flutamida, testolactona, letrozole y anastrozole, entre otros, son capaces, por diferentes mecanismos, de reducir o inhibir la producción de ES o de bloquear su acción en los órganos diana(18). En general, estos tratamientos no son demasiado eficaces, rara vez se alcanza con ellos una detención completa en el desarrollo de los caracteres sexuales secundarios y una adecuada talla final y, en algunos casos, sus efectos secundarios son importantes.
Pubertad retrasada (PR)
Concepto y morbilidad
No existe un consenso internacional que establezca con claridad el concepto de pubertad retrasada; de hecho, el término engloba varios conceptos: pubertad retrasada propiamente dicha, pubertad detenida y ausencia de pubertad o infantilismo sexual(20).
Se considera la “pubertad retrasada”, cuando no se ha iniciado el desarrollo puberal a una edad 2-2,5 SDS por encima de la edad media de su aparición en la población de referencia(21,22). A efectos prácticos, la ausencia de telarquia en las niñas a una edad de 13 años y la ausencia de incremento del volumen testicular (=4 mL) a los 14 años (Fig. 2). Se habla de “pubertad detenida”, cuando la pubertad, iniciada tardíamente o no, no llega a completarse y transcurren más de 4-5 años entre su inicio y el desarrollo gonadal completo en los varones o la menarquia en las mujeres. Por último, se habla de “ausencia de pubertad” o “infantilismo sexual”, cuando la pubertad no llega a iniciarse.
La PR, especialmente en los varones, puede conllevar importantes repercusiones psicosociales que son, con frecuencia, el motivo por el que el paciente acude a la consulta. En una época de extremada sensibilidad y labilidad psicológica, donde la imagen corporal es muy importante para la autoestima del sujeto, la falta de desarrollo puberal y la talla baja, que frecuentemente acompaña al retraso puberal, les hace con frecuencia objeto de burlas y vejaciones por parte de sus compañeros de edad, al tiempo que son relegados de las actividades deportivas y sociales, especialmente de aquellas que conllevan una interrelación con el otro sexo. Como consecuencia, es frecuente que los pacientes desarrollen una mala imagen de sí mismos, baja autoestima, conductas depresivas y tendencia al aislamiento y a una cierta agresividad, alteraciones que, en ocasiones, pueden desembocar en fracaso escolar y en problemas familiares y sociales graves. Por otra parte, la PR puede tener, también, repercusiones físicas, sobre la masa ósea (masa ósea disminuida por el retraso en la aparición de los ES) y auxológicas: alteración de las proporciones corporales (extremidades más largas con relativo acortamiento del segmento superior) y pérdida de talla final. Por motivos desconocidos, un pequeño porcentaje de los pacientes con PR pueden no alcanzar una talla adulta adecuada a su contexto familiar(23).
Etiopatogenia y clínica
Las causas que pueden provocar una PR son múltiples; no obstante, pueden ser fácilmente divididas en cuatro categorías (Tabla III):
• Retraso puberal simple. Englobaría aquellos retrasos temporales en el inicio puberal de causa desconocida (idiopáticos) o debidos a factores constitucionales o genéticos (“retraso constitucional del crecimiento y de la pubertad” –RCCP–).
• Retraso puberal secundario a enfermedades crónicas. Serían el resultado de trastornos funcionales en el eje HHG secundarios a múltiples patologías crónicas o endocrinopatías (hipogonadismo hipogonadotropo funcional o transitorio).
• Hipogonadismos hipogonadotropos (HHipo). Serían aquellos pacientes que fracasan en su desarrollo puberal por anomalías en los mecanismos de control hipotálamo-hipofisarios de la pubertad.
• Hipogonadismos hipergonadotropos (HHiper). Serían aquellos pacientes que fracasan en su desarrollo puberal por fallo gonadal primario.
La PR es una situación frecuente, aunque su incidencia real es difícil de establecer. Estadísticamente, debería afectar, al menos, a un 2-3% de la población. También, debería tener una incidencia similar en ambos sexos, pero, y al contrario de lo que ocurre con la PP, se presenta especialmente en varones (˜70%). En ambos sexos, la causa más frecuente es el simple retraso en su inicio, de etiología familiar o idiopática, que representaría alrededor del 60% de los casos de PR en varones y del 30% en mujeres (Fig. 6).
Figura. 6. Distribución por categorías diagnósticas en varones y mujeres con pubertad retrasada. La figura muestra los resultados, en porcentajes, de una serie de 232 casos, recogidos en Boston, EE.UU. (IL Sedlmeyer y MR Palmert. J Clin Endocrinol Metab 2002; 87: 1613-1620). RCCP: retraso constitucional del crecimiento y de la pubertad; RP2rio: retraso puberal secundario a patología crónica (hipogonadismo hipogonadotropo transitorio); HHipo: hipogonadismo hipogonadotropo permanente; HHiper: hipogonadismo hipergonadotropo permanente; Otros: etiología no clasificada claramente.
Es importante destacar, en las niñas, la gran importancia porcentual de los HHiper, ligada a la elevada incidencia del síndrome de Turner (45,X0 y sus variantes), que probablemente ha descendido en los últimos años como consecuencia de que muchas de estas anomalías cromosómicas terminan en interrupción voluntaria del embarazo, y, en ambos sexos, el incremento, en las últimas décadas, de los retrasos puberales secundarios a patología crónica, resultado de que los avances diagnóstico-terapéuticos han permitido que un mayor número de pacientes con patologías crónicas alcancen la edad puberal. Los hipogonadismos, dependiendo de la causa, de que sean parciales o totales, y del momento de su aparición, pueden determinar manifestaciones clínicas variables: retraso puberal, detención del desarrollo puberal, infantilismo sexual, ambigüedad genital, infertilidad, amenorrea secundaria, etc.
Retraso constitucional del crecimiento y de la pubertad
El retraso puberal simple de etiología idiopática o familiar (RCCP) es la causa más frecuente de PR y asociado o no a un componente de talla baja familiar, la causa más frecuente de talla baja en la infancia.
El RCCP es más frecuente en varones (Fig. 6), que llegan a consultar por este problema en proporciones de 9:1. Se considera una variante cronológica de la normalidad y, aunque puede presentarse de forma esporádica o idiopática, lo hace habitualmente en un contexto familiar de maduración tardía (60-90% de los casos). El patrón de herencia es sugerente de una herencia autosómica dominante. Serían niños normales con un patrón madurativo familiar más lento que la media de la población. El cuadro clínico se caracteriza por un hipocrecimiento de inicio postnatal, con un patrón de crecimiento característico, que se acompaña de un retraso en la maduración ósea y en el inicio de la pubertad de 2 a 4 años. Son niños que hasta los 12-18 meses de edad crecen normalmente. A partir de ese momento y hasta los 3-4 años (fenómeno de canalización del crecimiento), experimentan una caída en el ritmo de crecimiento que les lleva a situarse en un carril de crecimiento inferior al que les correspondería para su contexto familiar, con frecuencia próximo o por debajo del percentil 3. Cuando existe un componente familiar importante de talla baja, el hipocrecimiento puede ser muy severo, con tallas por debajo de –3 SDS. A partir de los 3-4 años, los niños crecen a un ritmo normal, aunque habitualmente por debajo del percentil 50 de VC, y tienden a mantener el percentil de talla. Cuando alcanzan la edad en la que habitualmente se produce la pubertad, se observa un nuevo periodo de desaceleración del ritmo de crecimiento, lo que se conoce como “depresión prepuberal de la VC”, que los aleja nuevamente de los percentiles normales hasta que se inicia el estirón puberal. Este se produce de forma normal, aunque tardíamente, y el pico de VC suele ser menor; de forma que, es un estirón menos aparente y se ganan menos centímetros que cuando este se produce a una edad media o temprana, compensándose así el mayor número de años de crecimiento. La talla final se alcanza también tardíamente y suele ser acorde con el contexto familiar, aunque, en alrededor del 15% de estos pacientes, por causas desconocidas, la talla final se sitúa por debajo de lo esperable para su contexto familiar.
Retraso puberal secundario a patología crónica
Prácticamente todas las enfermedades crónicas, si son lo suficientemente importantes en gravedad y duración, repercuten de un modo negativo sobre el crecimiento y la maduración (Tabla IV).
Los mecanismos fisiopatológicos que median el retraso puberal en las patologías crónicas son múltiples y varían dependiendo de la enfermedad y de la terapia empleada(24). En la mayoría de los casos, un cierto componente de malnutrición (exceso de pérdidas, disminución de ingesta o aumento de necesidades) suele estar presente, lo que condiciona unas modificaciones hormonales de adaptación que afectan, sobre todo, al eje GH-IGF-1 (resistencia parcial a la acción de la GH, retraso de crecimiento y de la maduración ósea) y al eje HHG (retraso puberal secundario a hipogonadismo hipogonadotropo funcional transitorio). Ambos fenómenos, el hipocrecimiento y la PR se consideran como mecanismos de adaptación a la escasez, absoluta o relativa, de nutrientes. Otros mecanismos fisiopatológicos implicados en la PR dependen de la enfermedad responsable, como son, entre otros: trastornos hidroelectrolíticos, hipoxia crónica, citoquinas inflamatorias, disfunciones hormonales, problemas psicopatológicos y tratamientos crónicos (corticoterapia, transfusiones repetidas, quimioterapia…).
En la mayoría de los casos, el cuadro clínico remeda clínica y hormonalmente al RCCP (hipocrecimiento con retraso de la maduración ósea y del inicio puberal con niveles bajos de gonadotropinas y ES). En otras ocasiones, cuando la enfermedad se manifiesta una vez iniciada la pubertad, puede condicionar una “pubertad detenida” (p. ej., anorexia nerviosa), con posterior progresión de los caracteres sexuales secundarios si la enfermedad mejora. Más raramente, algunas patologías crónicas, por la propia enfermedad (hemocromatosis, galactosemia) o por la terapia empleada (quimioterapia, radioterapia, cirugía), pueden a la larga determinar hipogonadismos hipo o hipergonadotropos definitivos con ausencia de desarrollo puberal.
Hipogonadismos hipogonadotropos (HHipo)
Los HHipo son responsables de alrededor del 10% de los retrasos puberales. Se caracterizan por niveles muy disminuidos o ausentes de las gonadotropinas circulantes, LH y FSH. Pueden ser debidos a defectos congénitos o adquiridos y presentarse aislados o asociados a otras deficiencias hormonales (Tabla III).
Los HHipo adquiridos son los más frecuentes y, en su mayoría, debidos a procesos tumorales o infiltrativos que afectan a la región hipotálamo-hipofisaria y que originan deficiencias hipofisarias múltiples(2). La causa más frecuente son los tumores, bien por invasión tumoral directa del área hipotálamo-hipofisaria, o bien como consecuencia de su extirpación quirúrgica o de la radioterapia aplicada para su tratamiento. El más frecuente de estos tumores en la infancia es el craneofaringioma, pero otros tumores, como: germinomas, gliomas o prolactinomas, pueden determinar manifestaciones clínicas similares. La dosis de radioterapia recibida por el hipotálamo o la hipófisis necesaria para producir un HHipo no está claramente establecida, aunque suele ser mayor de 40 Gy. Dosis de 30-55 Gy pueden determinar, inicialmente, una pubertad precoz o adelantada y, más adelante, por el efecto progresivo de la radiación, conducir a un HHipo. Procesos infiltrativos (histiocitosis, sarcoidosis, hemocromatosis), traumatismos craneales, procesos infecciosos o inflamatorios (hipofisitis autoinmune) que afecten al área hipotálamo-hipofisaria son otras posibles causas de HHipo. La hemocromatosis, por acúmulo de hierro en hipotálamo-hipófisis puede provocar un HHipo y por acúmulo gonadal un HHiper.
La prevalencia de HHipo congénitos se estima en alrededor de 1:10.000 personas y la mayoría son casos esporádicos, con un predominio en varones 3-5:1(25). Las formas familiares pueden heredarse con carácter autosómico dominante, recesivo o recesivo ligado al X. Los HHipo congénitos pueden presentarse aisladamente, asociados a otras deficiencias hipofisarias o en el contexto de otros cuadros sindrómicos complejos (Tabla III).
• HHipo congénitos aislados. Clásicamente y desde una visión clínica, estas formas de hipogonadismo se han clasificado como “HHipo congénitos con y sin alteraciones del olfato”; no obstante, esta diferenciación puede ser algo artificial, dado que el avance en los estudios genéticos ha puesto de manifiesto como, mutaciones en un mismo gen e incluso en una misma familia puede dar lugar a HHipo con y sin alteraciones del olfato.
La asociación de HHipo congénitos y alteración del olfato (anosmia o hipoosmia) secundaria a aplasia/hipoplasia de los bulbos olfatorios es lo que se conoce como síndrome de Maestre de San Juan-Kallmann o, simplemente, síndrome de Kallmann (SK). Este síndrome supone alrededor de un 15% de los HHipo y es cinco veces más frecuente en varones que en mujeres. La asociación de HHipo, por deficiencia de GnRH, y anosmia tiene su explicación en el origen embriológico común de las neuronas productoras de GnRH y de las neuronas olfatorias (Fig. 1). Los pacientes con SK pueden mostrar además de los trastornos del olfato, de los que frecuentemente no son conscientes, alteraciones muy variadas, entre ellas: agenesia renal unilateral, defectos atriales septales, ceguera para los colores, hipoacusia neurosensorial, sincinesias de los dedos, lesiones de línea media (labio-paladar hendido, agenesia de uno o más dientes y agenesia del cuerpo calloso), etc. Los casos esporádicos son los más frecuentes, más de dos terceras partes. En los casos familiares, las manifestaciones pueden ser muy variables entre los distintos familiares afectos: anosmia aislada, pubertad tardía, infertilidad, HHipo o pérdida temprana de la menstruación, entre otras. El primer gen responsable del SK, el gen KAL1 (Xp22.31), se descubrió en 1992 y codifica para una proteína, la anosmina, que facilita el crecimiento y la migración neuronal. Desde entonces, se han descrito, al menos, 16 genes diferentes asociados al síndrome (Tabla III) que serían responsables en conjunto de menos del 50% de los SK y con patrones hereditarios diferentes (autosómicos dominante, recesivo y ligado al X).
Las bases genéticas de los HHipo congénitos aislados sin anosmia (HHipo normoósmicos), al igual que ocurre con los SK, son solo parcialmente conocidas. Algunos de los genes que se han asociado a cuadros de HHipo sin anosmia son: GnRH1(GnRH), GnRHR (receptor de GnRH), KISS1 (kisspeptina) KISS1R (receptor de las kisspeptinas), LEP(leptina), LEPR (receptor de leptina), PC1 (prohormona convertasa-1), TAC3 (neurokinina B), TAC3R (receptor de TAC3), DAX1(miembro de la superfamilia de receptores nucleares huérfanos), LHβ (subunidad β de la LH) y FSHβ (subunidad β de la FSH). Las mutaciones en LEP, LEPR y PC1 cursan con obesidad de inicio temprano y las mutaciones en DAX1 se asocian a hipoplasia suprarrenal congénita. Sorprendentemente, alrededor del 10-20% de estas formas de HHipo aislado congénito, tanto con, como sin anosmia, pueden experimentar cierto grado de reversibilidad espontánea(25).
• HHipo asociados a otras deficiencias hipofisarias. Son debidas a anomalías congénitas en el desarrollo del SNC (displasia septo-óptica, holoprosencefalia, etc.) de base genética conocida o no, como sería el caso de algunas formas de displasia septo-óptica asociadas a mutaciones en HEX1, o a mutaciones en factores de transcripción implicados en el desarrollo de las diferentes líneas células hipofisarias: LHX3, LHX4, PROP1 y POU1F1 (Pit1). El gen más frecuentemente afectado es PROP1, cuyas mutaciones determinan una deficiencia combinada de: GH, Prl, LH, FSH, TSH y, frecuentemente, pero de forma más tardía, también de ACTH.
• HHipo asociados a cuadros sindrómicos. Determinados síndromes pueden asociar cuadros clínicos de HHipo, como es el caso de los síndromes de: Prader-Willi, CHARGE (cuando es por mutaciones en CDH7, se puede asociar anosmia), Laurence-Moon, Bardet-Biedl y 4H, entre otros.
Las manifestaciones clínicas de los HHipo son variables dependiendo de su etiopatogenia y momento de aparición (congénitos, infancia, pubertad o edad adulta), como sería el caso de: trastornos del olfato, rasgos sindrómicos, anomalías congénitas asociadas, síntomas debidos a otras deficiencias hipofisarias (GH, ADH, ACTH…), etc. En general, las formas congénitas, dado que la diferenciación sexual está controlada por la gonadotropina coriónica placentaria (HCG) y no por las gonadotropinas fetales, no presentan ambigüedad genital, aunque sí condicionan con frecuencia criptorquidia bilateral con micropene o una hipoplasia de labios menores, debido a su acción en la fase final de la gestación. Durante el periodo prepuberal, el crecimiento y la maduración ósea suelen ser normales, pero al llegar a la edad puberal, la ausencia de ES determina que no se desarrollen los caracteres sexuales secundarios (puede aparecer vello pubiano escaso por acción de los andrógenos suprarrenales) y se retrase el cierre de los cartílagos de crecimiento, lo que favorece el desarrollo de proporciones corporales eunucoides (aumento de las extremidades con incremento de la braza, >5 cm que la talla, y disminución del cociente segmento superior/segmento inferior). Algunos pacientes pueden iniciar la pubertad y no completarla (pubertad detenida) o completarla y desarrollar el hipogonadismo, posteriormente, en la edad adulta, manifestándose en forma de infertilidad y disfunción sexual.
Hipogonadismos hipergonadotropos (HHiper)
Este tipo de hipogonadismos son debidos a fallo gonadal primario y se caracterizan por niveles séricos elevados de gonadotropinas y disminuidos de ES. Pueden ser congénitos o adquiridos (Tabla III). La incapacidad de la gónada para producir adecuadas cantidades de ES e inhibina determina la falta de retroinhibición de estos sobre el hipotálamo y la hipófisis, incrementándose la secreción pulsátil de GnRH y, por tanto, de LH y FSH.
Las dos causas más frecuentes de HHiper congénito son dos cromosomopatías congénitas: el síndrome de Klinefelter y el síndrome de Turner.
• El síndrome de Klinefelter o síndrome de disgenesia de los túbulos seminíferos (47, XXY y sus variantes) es la causa más frecuente de hipogonadismo en el varón (1:500-1.000 niños nacidos vivos). La función de los túbulos seminíferos y de las células de Leydig está alterada y la espermatogénesis ausente. Dependiendo de los niveles de testosterona, la pubertad puede desarrollarse normalmente, retrasarse o empezar a una edad normal, aunque sin una adecuada progresión. Las manifestaciones clínicas son variables, pero la talla suele ser alta y en la pubertad y edad adulta los testes son pequeños y duros y la ginecomastia es frecuente. Otras anomalías asociadas incluirían: retraso mental variable, dificultades en el lenguaje, problemas de conducta, incremento en la incidencia de determinados tumores (cáncer de mama y tumores de células germinales de localización mediastínica, retroperitoneal y pineal) y alteraciones tiroideas, entre otras.
• El síndrome de Turner (45, X0 y sus variantes) es la causa más frecuente de HHiper en la mujer (1:2.500-3.000 niñas nacidas vivas). Sus manifestaciones clínicas resultan de la ausencia de genes que escapan a la inactivación del X. Estas niñas pueden presentar diferentes alteraciones y anomalías, incluyendo: hipocrecimiento, fallo gonadal, rasgos sindrómicos (pterigium colli, linfedema, tórax en coraza, hipoplasia areolar, cubitus valgo, alteraciones ungueales, acortamiento de metacarpianos, implantación baja del cabello y de las orejas, boca de pez, nevus múltiples, etc.), cardiopatía, malformaciones del sistema urinario, etc. Los síntomas más constantes son el hipocrecimiento (95%) y el fallo gonadal (90%). Pese a ello, un 30% son capaces de iniciar espontáneamente la pubertad, aunque solo un 2-5% llegan a completarla y a tener reglas espontáneas (menopausia precoz con amenorrea secundaria).
• Las causas adquiridas de HHiper son relativamente infrecuentes: torsión gonadal bilateral (testicular u ovárica), castración quirúrgica (tumores), traumatismos severos en el escroto y testículos, orquitis bilaterales (p. ej., parotiditis) y, en el caso de las mujeres, galactosemia o fracaso ovárico precoz de etiología idiopática o autoinmune. El tratamiento del cáncer, debido a la quimioterapia y radioterapia, con frecuencia aplicadas conjuntamente, es una causa creciente de HHiper adquirido.
Evaluación diagnóstica
Las causas que pueden provocar un retraso puberal son múltiples. Una valoración básica inicial incluiría: una cuidadosa historia médica, personal y familiar, una exploración física completa y una serie de pruebas complementarias (Algoritmo 2) que pueden variar en función de los hallazgos de la historia y exploración(20).
Anamnesis detallada
Una historia familiar de PR está presente en la gran mayoría de los casos de RCCP, pero también puede formar parte de la historia familiar en pacientes con HHipo. Un interrogatorio cuidadoso puede poner de manifiesto la presencia de síntomas sugerentes de patologías concretas (anosmia, infertilidad, galactorrea, hipotiroidismo, etc.) o de patologías crónicas inadvertidas, así como un exceso de ejercicio o un trastorno de la conducta alimentaria. Los antecedentes de criptorquidia, quimioterapia, radioterapia gonadal o craneal y la administración crónica o prolongada de medicamentos que puedan interferir en la función gonadal debe ser, también, recogida. La reconstrucción de la gráfica de crecimiento y peso puede ser de utilidad, junto con la los datos auxológicos parentales. El hipocrecimiento es un hallazgo habitual en: RCCP, malnutrición, patología crónica o Turner; mientras que, en la mayoría de las formas de HHipo la talla suele ser normal o incluso alta. Un bajo peso para la talla puede indicar trastornos nutricionales o enfermedad crónica inadvertida; mientras que: hipotiroidismo, exceso de glucocorticoides, deficiencia de GH o determinados síndromes (Prader Willi, Turner, etc.) suelen tener un claro o moderado incremento del peso para la talla.
Exploración física
Debe ser completa, analizando especialmente: talla, peso, signos de malnutrición o patología crónica, estigmas sindrómicos (Turner, Klinefelter…) y signos neurológicos sugerentes de patología intracraneal (fondo de ojo, campimetría y estudio del olfato pueden ser necesarios). Debe realizarse una cuidadosa valoración del estadio de desarrollo puberal; ya que, signos incipientes de desarrollo puberal pueden pasar inadvertidos para los pacientes o alteraciones en la secuencia normal de la pubertad pueden sugerir patología. En las niñas con desarrollo puberal normal, pero sin menarquia, deben descartarse causas anatómicas de amenorrea (himen imperforado, septum transverso vaginal o disgenesia mülleriana –síndrome de Rokitansky–), mediante una adecuada exploración ginecológica y ecográfica.
Edad ósea (EO)
El RCCP, la patología crónica, las endocrinopatías y los hipogonadismos presentan, habitualmente, un retraso de EO de 1 a 4 años. Una talla normal-baja, con ralentización reciente y EO inferior a 11 años en una niña y a 13 años en un varón es muy sugerente de retraso puberal simple; por el contrario, la ausencia de signos puberales a una EO de más de 11 años en las niñas y de más de 13 años en los niños es muy sugerente de hipogonadismo.
Otras pruebas complementarias
Su realización dependerá de la historia, exploración y EO.
• Analítica general. En pacientes en los que la historia clínica o la exploración física sugieran la presencia de patología crónica subyacente, debe realizarse una evaluación individual orientada a la sospecha clínica. Esta puede incluir: hemograma y bioquímica básica, marcadores de enfermedad celíaca, anticuerpos antitiroideos, TSH, T4 libre, prolactina y marcadores de deficiencia de GH (IGF-I, IGFBP-3). La sospecha de una deficiencia de GH puede obligar a realizar test de GH precedidos de la administración de ES (primación) para diferenciar una deficiencia real de GH de una deficiencia transitoria asociada a RCCP.
• Cariotipo. Su realización estaría indicada ante la presencia de estigmas sindrómicos o en el caso de: gonadotropinas elevadas, niñas con talla baja de etiología incierta o varones con testes pequeños e inadecuados para el grado de desarrollo puberal.
• RM craneal. Podría poner de manifiesto patología orgánica intracraneal, en área hipotálamo-hipofisaria, o anomalías de la vía olfatoria (agenesia de bulbos o nervios olfatorios).
• Ecografías pélvico-abdominales. Podrían poner de manifiesto malformaciones congénitas asociadas (renales en el SK) o anomalías vaginouterinas (agenesia o malformaciones uterinas, septum vaginal…), tamaño y morfología del útero y ovarios, localización de testes criptorquídicos, etc.
• Estudios hormonales. Un aspecto fundamental de la evaluación del retraso puberal, pero especialmente compleja, es la valoración del eje HHG. Los niveles séricos de testosterona y estradiol son de escasa utilidad en las fases iniciales de la pubertad; ya que, sus niveles séricos se sitúan, con frecuencia, por debajo del límite de detección de la mayoría de los inmunoanálisis. A partir de los 10-11 años de EO, a veces incluso antes, es frecuente observar en los HHiper niveles séricos elevados de LH y FSH basales o tras estímulo con GnRH. El diagnóstico de los HHipo completos también es sencillo cuando la EO supera, al menos en un año, la EO en la que habitualmente la pubertad se inicia. Se observan en este caso, niveles séricos disminuidos de LH y FSH tras estímulo con GnRH. El principal problema de diagnóstico diferencial se plantea entre el RCCP y el HHipo (sobre todo si es parcial, aislado e idiopático) cuando la EO del paciente está retrasada por debajo de las edades en que normalmente se inicia la pubertad. En estos casos, existe un considerable solapamiento entre la pobre respuesta de los pacientes con RCCP y la observada en pacientes con HHipo. Inhibina B y hormona antimülleriana, marcadores de la célula de Sertoli, pueden ser en ocasiones de utilidad para diferenciar HHipo y RCCP; ya que, la presencia de niveles séricos de inhibina B y hormona antimülleriana muy disminuidos o ausentes es más característico de los HHipo que de los RCCP. No obstante, en muchos casos, solo el tiempo y la evolución espontánea de la pubertad permitirán excluir o confirmar, definitivamente, el hipogonadismo(26).
• Estudios moleculares. Los pacientes con hipogonadismo y cariotipo normal, así como los hipogonadismos sindrómicos son candidatos para estudios moleculares más amplios. Estos deberían estar orientados, en función del diagnóstico y los hallazgos clínicos y hormonales, hacia genes concretos. En el caso de que las características clínicas del paciente no orienten hacia un diagnóstico concreto, se puede considerar, en colaboración con el genetista clínico, la posibilidad de realizar otros estudios genéticos más amplios: estudios de MLPA (Multiplex Ligation-dependent Probe Amplification), GWAS (Genoma-Wide Association Studies) o estudios de secuenciación de alto rendimiento (NGS: Next-Generation Sequencing). Este último tipo de estudios permite la secuenciación del genoma completo, de capturas selectivas (paneles de genes implicados en determinadas patologías), de regiones concretas o de todas las regiones codificantes y reguladoras conocidas de todo el genoma (exoma).
Tratamiento
Retraso constitucional del crecimiento y de la pubertad
El RCCP se considera una variante de la normalidad; por consiguiente, en la gran mayoría de los casos, una clara explicación al paciente y a los padres, junto con un adecuado control y apoyo psicológico, son suficientes. Solo aquellos casos en los que el retraso sea más severo y existan graves repercusiones psicológicas y sociales (depresión, baja autoestima, fracaso escolar, etc.) serán susceptibles de tratamiento.
En los varones, suele administrarse testosterona, a dosis baja, en forma de preparados depot de ésteres de testosterona (enantato o cipionato), en una inyección intramuscular mensual de 50-100 mg, y a partir de los 12-12,5 años de EO o de los 14 de edad cronológica(20). Por debajo de esa edad, rara vez es necesario desde el punto de vista psicológico y el riesgo de acelerar la EO y comprometer la talla definitiva es mayor. La testosterona acelera la VC, el desarrollo de los caracteres sexuales secundarios y favorece el desarrollo espontáneo de la pubertad. Se recomienda realizar ciclos de tratamiento de 3-6 meses, alternando con periodos similares de observación durante los cuales se vigila la progresión espontánea de la pubertad. Si tras 2-3 ciclos, la pubertad no se ha iniciado (aumento del volumen testicular), lo más probable es que nos encontremos ante un hipogonadismo hipogonadotropo.
En las niñas, la incidencia de RCCP es muy inferior a la de los varones y la experiencia menor. Se recomienda que el tratamiento no se inicie antes de los 13 años de edad cronológica y de los 11-12 años de EO y que se utilicen estrógenos (estradiol o etinil-estradiol) a dosis muy bajas, al objeto de no acelerar en exceso la maduración ósea y comprometer la talla final.
En pacientes con RCCP con malas expectativas de talla adulta, se ha sugerido la posibilidad de emplear otro tipo de tratamientos, como sería el caso de la GH; sin embargo, al menos con las pautas utilizadas, la GH no parece ser capaz de mejorar significativamente la talla final en estos pacientes. Otros estudios más recientes, sugerían que los inhibidores de la aromatasa de 3ª generación (letrozol y anastrozol) asociados a andrógenos podrían acelerar la VC, enlentecer la progresión de la maduración ósea y mejorar las expectativas de talla final y, todo ello, sin efectos secundarios reseñables; no obstante, los resultados disponibles a talla final, aunque todavía insuficientes para poder establecer conclusiones definitivas, no sostienen estos potenciales beneficios y sí posibles efectos secundarios, entre ellos: marcada elevación de los niveles séricos de testosterona, de repercusión incierta, desarrollo de anomalías vertebrales, disminución del colesterol HDL y aumento del hematocrito(27).
Retraso puberal secundario a patología crónica
El tratamiento y la prevención del retraso puberal en pacientes con patologías crónicas se basa en el tratamiento óptimo y precoz de la enfermedad de base, junto con una adecuada nutrición (aporte suficiente de macro y micronutrientes).
Las pautas para inducir y mantener el desarrollo puberal no difieren, en general, de las empleadas en el RCCP o en el hipogonadismo.
Hipogonadismos
En los hipogonadismos es necesario inducir o completar el desarrollo de los caracteres sexuales secundarios y posteriormente, establecer una pauta crónica de reemplazamiento de ES.
Disponemos de tres opciones terapéuticas para inducir la pubertad: administración pulsátil de GnRH, administración de gonadotropinas y administración de ES. La elección dependerá del diagnóstico (en los HHiper, la única opción son los ES), de los objetivos terapéuticos (incremento de volumen testicular, fertilidad…), de la disponibilidad (la terapia con GnRH está limitada a muy pocos centros en Europa) y de las preferencias del paciente.
Durante la infancia, en los varones con HHipo puede ser necesario tratamiento para resolver la criptorquidia y mejorar el micropene. La criptorquidia, sobre todo cuando es bilateral, puede tener consecuencias negativas para la fertilidad futura, por ello se recomienda su corrección quirúrgica temprana, preferiblemente entre los 6-12 meses de vida(25). En cuanto al micropene, puede ser tratado con pequeñas dosis de testosterona depot (25 mg/mes), 1-3 dosis, preferiblemente durante los primeros 6-12 meses de vida o con gonadotropinas (HCG y FSH). Estudios recientes sugieren que el tratamiento con gonadotropinas en este periodo de la vida podría tener, además, efectos beneficiosos sobre el desarrollo testicular y la futura fertilidad del paciente, aunque estos resultados son todavía muy preliminares para establecer conclusiones definitivas.
En la adolescencia y edad adulta, los objetivos del tratamiento son: conseguir un desarrollo puberal completo, con una secuencia y ritmo normal de aparición de los caracteres sexuales secundarios, lograr la mejor talla adulta posible, evitar la osteoporosis y las complicaciones cardiovasculares y psicosociales, y, en aquellos casos en que sea factible, adquirir y optimizar la capacidad reproductiva(28,29). Una propuesta aceptable sería, remedando el desarrollo puberal normal, inducirlo alrededor de los 11 años de EO en las niñas y de los 12 años en los varones e incrementar lentamente los niveles séricos de ES para conseguir el desarrollo puberal completo en un periodo de 3-4 años. Cuando la talla final está comprometida (deficiencia de GH, Turner), puede ser necesario retrasar la inducción de la pubertad, al objeto de lograr unas mejores expectativas de talla adulta.
En varones, la forma más sencilla de inducir el desarrollo puberal es la administración de testosterona, que puede ser por vía oral (no disponible en España), parenteral o transdérmica. En la práctica, suelen utilizarse preparados depot de testosterona de acción prolongada (enantato o cipionato) por vía intramuscular. La dosis inicial será de 25-50 mg cada 4 semanas y se incrementará en 50 mg, cada 6-12 meses, para, a lo largo de un periodo de 3-4 años, alcanzar la dosis de sustitución de un adulto, que oscilaría entre 200-250 mg cada 10-14 días. Un inconveniente de esta terapia es que el volumen testicular no aumenta ni se induce la fertilidad. En los niños con HHipo en los que se desee incrementar el volumen testicular, la terapia intramuscular o subcutánea con gonadotropinas o la administración pulsátil, mediante bomba, de bolos de GnRH, por vía subcutánea, puede ser una alternativa. Una vez completado el desarrollo puberal, la terapia de mantenimiento en los varones se realiza, habitualmente, con testosterona. Aunque en este caso, también puede administrarse por diferentes vías, las más utilizadas son: la intramuscular (200-250 mg de enantato de testosterona cada 10-14 días o 1.000 mg de undecanoato detestosterona c/2-3 meses) y la transdérmica (parches de testosterona); ya que, los preparados orales de testosterona (undecanoato de testosterona) no están comercializados en nuestro país. La fertilidad, en el adulto, requiere de la administración de gonadotropinas o de bolos de GnRH, por vía subcutánea, durante periodos prolongados para inducir la espermiogénesis.
En las niñas, la inducción de la pubertad se realizará con estrógenos y con dosis iniciales muy bajas; ya que, los estrógenos son un potente inductor de la fusión epifisaria. Los regímenes más habitualmente empleados incluyen la administración oral o transdérmica de estradiol. La vía transdérmica, con parches de composición matricial es la más recomendada, ya que tiene la ventaja sobre la vía oral, de una mayor biodisponibilidad, mejor tolerancia gastrointestinal y menor toxicidad hepato-biliar al evitar el paso inicial por el hígado. Estos parches matriciales, dependiendo del preparado, liberan 25, 50, 75 o 100 µg/día de estradiol, pero permiten su fragmentación y la administración de dosis más bajas y progresivamente crecientes de estradiol. La dosis inicial sería de 0,05-0,1 µg/kg, habitualmente 1/8 de parche de 25 µg que, de forma ideal, se aplicaría durante los primeros 3-4 meses solo por la noche (se pondría al acostarse y se retiraría por la mañana); posteriormente, el 1/8 de parche se mantendría durante todo el día (se cambian 2 veces/ semana) y las dosis se irían incrementando cada aproximadamente 6-12 meses, durante un periodo no inferior a 2-3 años, hasta alcanzar la dosis diaria de sustitución estrogénica de una mujer adulta, que correspondería habitualmente a unos 50 µg/día de estradiol. Una vez alcanzado un adecuado desarrollo mamario (T4-5) y uterino (útero en la ecografía de >35-40 mm, con línea endometrial visible), o bien, si produce un sangrado menstrual o pequeños manchados, debe añadirse un progestágeno cíclico, preferentemente micronizado para favorecer su absorción (200 mg/día, antes de acostarse, del 10 al 21 día de ciclo, en forma de cápsulas orales u óvulos vaginales) para la protección uterina y establecer ciclos menstruales regulares mensuales. Una vez completado el desarrollo puberal, es necesario establecer una terapia sustitutiva a largo plazo. Se podría seguir con la asociación de estrógeno transdérmico y progestágeno oral-vaginal, pero, en la mayoría de los casos, suele administrase una combinación continua o cíclica de estrógenos-progestágenos, habitualmente por vía oral o transdérmica. Una gran variedad de preparados combinados de estrógenos-progestágenos están disponibles en el mercado en forma de píldoras orales anticonceptivas y pueden ser empleados. Deben elegirse, si están disponibles, aquellos que contengan estrógenos naturales y, si no es posible, los de menor contenido estrogénico (15-20 µg de etinil estradiol). La opción a la vía oral es la administración transdérmica continua de estrógenos-progestágenos que, habitualmente, aportan una dosis diaria de 50 µg/día de estradiol. Los parches se cambian cada 3,5 días (dos por semana), durante 3 semanas, transcurridas las cuales se suspende una semana el tratamiento, durante la cual se produce la regla. La inducción de fertilidad, requiere, como en el caso de los varones, de la administración prolongada de gonadotropinas o GnRH.
Funciones del pediatra de Atención Primaria (AP)
El pediatra de Atención Primaria es el profesional que se enfrenta inicialmente a este tipo de situaciones y debe ser capaz de realizar un enfoque diagnóstico adecuado, diferenciar aquellas variantes normales del desarrollo de las que no lo son, orientar a los padres y al paciente y, en aquellos casos que considere necesario, derivar al paciente a un servicio de Endocrinología Pediátrica. Trasmitir a los padres una información veraz sobre la amplia variabilidad normal en el tempo de la pubertad, las escasas o nulas repercusiones que estas variaciones normales tienen sobre la talla adulta y la inconveniencia de llevar a cabo tratamientos, por innecesarios, contraindicados, es muchas veces suficiente para tranquilizar a los padres y a los pacientes. Por el contrario, derivar precozmente aquellos pacientes sospechosos de patología puede permitir el diagnóstico precoz de patologías orgánicas, potencialmente graves y que el tratamiento evite, o al menos minimice las repercusiones auxológicas y psicosociales de estas patologías.
Bibliografía
Los asteriscos reflejan el interés del artículo a juicio del autor.
1.** Kuiri-Hänninen T, Sankilampi U, Dunkel L. Activation of the hypothalamic-pituitary-gonadal axis in infancy: minipuberty. Horm Res Paediatr. 2014; 82: 73-80.
2. Nakamoto JM, Franklin SL, Geffner ME. Puberty. En: Kappy MS, Allen DB, Geffner ME, ed. Pediatric Practice Endocrinology. New York: Mc Graw Hill Medical; 2010. p. 257-98.
3.** Parent AS, Teilman G, Juul A, Skakkebaek NE, Toppari J, Bourguignon JP. The timing of normal puberty and the age limits of sexual precocity: variations around the world, secular trends and changes after migration. Endocr Rev. 2003; 24: 668-93.
4.** Day FR, Perry JR, Ong KK. Genetic Regulation of Puberty Timing in Humans. Neuroendocrinology. 2015 May 7 (artículo publicado electrónicamente previo a su publicación en papel). DOI: 10.1159/000431023.
5.** Parent AS, Franssen D, Fudvoye J, Gérard A, Bourguignon JP. Developmental variations in environmental influences including endocrine disruptors on pubertal timing and neuroendocrine control: Revision of human observations and mechanistic insight from rodents. Front Neuroendocrinol. 2015; 38: 12-36.
6. Özen S, Darcan S. Effects of Environmental Endocrine Disruptors on Pubertal Development. J Clin Res Ped Endo. 2011; 3: 1-6.
7.** Soriano-Guillén L, Corripio R, Labarta JI, et al. Central precocious puberty in children living in Spain: incidence, prevalence, and influence of adoption and immigration. J Clin Endocrinol Metab. 2010; 95: 4305-13.
8. Sloboda DM1, Hickey M, Hart R. Reproduction in females: the role of the early life environment. Hum Reprod Update. 2011; 17: 210-27.
9.** Carel JC, Léger J. Precocious puberty. N Engl J Med. 2008; 358: 2366-77.
10. Kaplowitz PB, Oberfield SE. Reexamination of the age limit for defining when puberty is precocious in girls in the United States: implications for evaluation and treatment. Drug and Therapeutics and Executive Committees of the Lawson Wilkins Pediatric Endocrine Society. Pediatrics. 1999; 104: 936-41.
11.** Carel JC, Lahlou N, Roger M, Chaussain JL. Precocious puberty and statural growth. Human Reprod Update. 2004; 10: 135-47.
12. Johansson T, Ritzzen EM. Very long-term follow-up of girls with early and late menarche. Endocr Dev 2005; 8: 126-36.
13. Barrio R, Carcavilla A, Martín M. Pubertad Precoz y Retrasada. Inf Ter Sist Nac Salud. 2006; 30: 95-107.
14. Bulcao Macedo D, Nahime Brito V, Latronico AC. New causes of central precocious puberty: the role of genetic factors. Neuroendocrinology. 2014; 100: 1-8.
15. Stephen MD, Zage PE, Waguespack SG. Gonadotropin-dependent precocious puberty: neoplastic causes and endocrine considerations. Int J Pediat Endocrinol. 2011; 2011: 184502. doi: 10.1155/2011/184502.
16.** Dumitrescu CE, Collins MT. McCune-Albright syndrome. Orphanet J Rare Dis. 2008; 3: 12.
17.** Soriano-Guillén L, Argente J. Pubertad precoz central: aspectos epidemiológicos, etiológicos y diagnóstico-terapéuticos. An Pediatr (Barc.). 2011; 74: 336-43.
18.** Fuqua JS. Treatment and outcomes of precocious puberty: An update. J Clin Endocrinol Metab. 2013; 98: 2198-207.
19.** Carel JC, Eugster EA, Rogol A, Ghizzoni L, Palmert MR, on behalf of the members of the ESPE-LWPES GnRH Analogs Consensus Conference Group. Consensus statement on the use of gonadotropin-releasing hormone analogs in children. Pediatrics. 2009; 123: e752-62.
20. Pozo J, Argente J. Ascertainment and treatment of delayed puberty. Horm Res. 2003; 60 (suppl 3): 35-48.
21.** Palmert MR, Dunkel L. Delayed puberty. N Engl J Med. 2012; 366: 443-53.
22. Villanueva C, Argente J. Pathology or normal variant: what constitutes a delay in puberty? Horm Res Paediatr. 2014; 82(4): 213-21.
23. Moreno L, Ibañez L. Pubertad retrasada. En: Cruz-Hernández, ed. Tratado de Pediatría (10ª edición). Madrid: Ergon S.A. 2011; p. 1.094-1.100.
24. Pozo J, Argente J. Delayed puberty in chronic illnes. Baillieres Best Pract Res Clin Endocrinol Metab. 2002; 16: 73-90.
25.*** Boehm U, Bouloux PM, Dattani MT, de Roux N, Dodé C, Dunkel L, et al. Expert consensus document: European Consensus Statement on congenital hypogonadotropic hypogonadism-pathogenesis, diagnosis and treatment. Nat Rev Endocrinol. 2015 (artículo publicado electrónicamente previo a su publicación en papel). doi: 10.1038/nrendo.2015.112.
26. Harrington J, Palmert MR. Clinical review: Distinguishing constitutional delay of growth and puberty from isolated hypogonadotropic hypogonadism: critical appraisal of available diagnostic tests. J Clin Endocrinol Metab. 2012; 97: 3056-67.
27. Shams K, Cameo T, Fennoy I, et al. Outcome analysis of aromatase inhibitor therapy to increase adult height in males with predicted short adult stature and/or rapid pubertal progress: a retrospective chart review. J Pediatr Endocrinol Metab. 2014; 27: 725-30.
28. Bouvattier C, Maione L, Bouligand J, Dodé C, Guiochon-Mantel A, Young J. Neonatal gonadotropin therapy in male congenital hypogonadotropic hypogonadism. Nat Rev Endocrinol. 2011; 8: 172-82.
29.** Barrio R, Roldán B, Martín Frías M. Inducción de la pubertad. Rev Esp Endocrinol Pediatr. 2015; 6 (Suppl): 39-44.
Bibliografía recomendada
- Parent AS, Franssen D, Fudvoye J, Gérard A, Bourguignon JP. Developmental variations in environmental influences including endocrine disruptors on pubertal timing and neuroendocrine control: Revision of human observations and mechanistic insight from rodents. Front Neuroendocrinol. 2015; 38: 12-36.
Una excelente y amplia revisión sobre los mecanismos genéticos y ambientales implicados en el inicio puberal y su interrelación. Amplia bibliografía que permite profundizar aún más en estos aspectos. Muy recomendable.
- Carel JC, Eugster EA, Rogol A, Ghizzoni L, Palmert MR, on behalf of the members of the ESPE-LWPES GnRH Analogs Consensus Conference Group. Consensus statement on the use of gonadotropin-releasing hormone analogs in children. Pediatrics. 2009; 123: e752-e762.
Este trabajo es el fruto de un reciente consenso de las principales sociedades internacionales de Endocrinología Pediátrica sobre un tema tan controvertido como es la utilización de los análogos de GnRH en niños. Además de su empleo en la pubertad precoz central (principal indicación de estos fármacos), se revisa su empleo en otras situaciones (talla baja, hiperplasia adrenal congénita…). El trabajo reúne las conclusiones de estos expertos a la luz de los datos disponibles en la literatura. La revisión corta, pero muy esclarecedora, es muy recomendable no solo para endocrinólogos infantiles, sino también, para todos los pediatras interesados en temas de pubertad y crecimiento.
- Boehm U, Bouloux PM, Dattani MT, de Roux N, Dodé C, Dunkel L, et al. Expert consensus document: European Consensus Statement on congenital hypogonadotropic hypogonadism-pathogenesis, diagnosis and treatment. Nat Rev Endocrinol. 2015 (artículo publicado electrónicamente previo a su publicación en papel). doi: 10.1038/nrendo.2015.112.
Una reciente publicación que recoge el consenso de un grupo de expertos europeos sobre diferentes aspectos de los hipogonadismos hipogonadotropos congénitos, con los más recientes conocimientos sobre sus bases genéticas y los aspectos diagnósticos y terapéuticos. Además, es posible descargársela libremente en la dirección http://www.nature.com/nrendo/journal/vaop/ncurrent/pdf/nrendo.2015.112.pdf.
| Caso clínico |
|
Motivo de consulta Varón de 13 años y 6 meses de edad, que consulta por ausencia de desarrollo puberal. Antecedentes familiares Madre: 39 años, sana. Talla: 165,6 cm. Menarquia a los 13 años. G.A.V. 2.0.2. Padre: 41 años, sano. Talla: 185 cm. Desarrollo puberal normal. Una hermana de 4 años: sana. Resto de antecedentes familiares sin interés. Antecedentes personales Embarazo y parto normales (cariotipo intraútero: 46,XY). Periodo neonatal: normal. PRN: 2.720 g. LRN: 50 cm. Alimentación: sin intolerancias ni alergias alimentarias. Desarrollo psicomotor: normal. Enfermedades anteriores: diagnosticado a los 4 años de edad, de sarcoma cerebeloso (meduloblastoma atípico) y tratado con: cirugía (resección completa y válvula de derivación ventrículo-peritoneal), altas dosis de quimioterapia y, para consolidación del tratamiento, trasplante autólogo de progenitores hematopoyéticos. Resto de antecedentes personales: sin interés. Exploración Edad cronológica: 13 años y 6 meses. Talla: 153 cm (P25-50). Peso: 55 kg (P50-75). Exploración normal con genitales externos masculinos normales en estadio puberal I de Tanner (G1, P1, Aa) con testes en bolsas de 3 mL de volumen. Pruebas complementarias • Edad ósea: 13 años. • Hemograma y bioquímica básica: normales. • Función tiroidea (T4L y TSH): normal. • Testosterona: 0,45 ng/mL (VN: 0,3-4). • Test de LHRH para LH y FSH: niveles basales y tras estímulo de LH y FSH elevados. - FSH basal: 78 UI/mL, pico de FSH: 134 mUI/mL. - LH basal: 39 mUI/mL, pico de LH: 164 mUI/mL.
|
 |
| Temas de FC |
J. Pozo Román
Médico adjunto del Servicio de Endocrinología Pediátrica del Hospital Infantil Universitario Niño Jesús de Madrid y Profesor asociado de Pediatría de la Universidad Autónoma de Madrid
| Resumen
El crecimiento es el proceso fisiológico más característico de la edad pediátrica. Aunque la talla adulta y la edad a la que esta se alcanza están, en cada sujeto, determinadas genéticamente, el resultado final puede variar dependiendo de la compleja interacción a lo largo de todo el período de crecimiento de factores genéticos y ambientales. La talla baja supone un motivo de preocupación para los padres y es una causa muy frecuente de consulta en Pediatría y en Endocrinología Pediátrica; si bien, en la gran mayoría de los casos, se tratará de variantes normales de talla baja que, salvo una adecuada información, no requerirán tratamiento. El conocimiento de las características normales del crecimiento y de los factores implicados en su regulación en los distintos períodos de la vida es una condición imprescindible para poder valorar la normalidad o anormalidad en el crecimiento de un niño. En esta revisión, se intenta resumir de forma sencilla, los aspectos básicos que, desde el ámbito de la Atención Primaria, permitan al pediatra: 1) valorar si el crecimiento de un niño es normal o no; 2) conocer las causas que con más frecuencia pueden provocar su alteración; 3) saber cómo orientar el diagnóstico y cuándo remitir al especialista (a partir de la historia clínica, de la edad ósea y, en algunos casos, de un reducido número de pruebas complementarias fácilmente disponibles); y 4) conocer las opciones terapéuticas disponibles. |
| Abstract
Growth is the most characteristic physiological process of the pediatric age. Although adult stature and age at which this is reached are genetically determined in each subject, the final result may vary according to the complex interaction of genetic and environmental factors over the growth period. Short stature causes concern for the parents and is a very frequent cause for consultation in Pediatrics and Pediatric Endocrinology. However, in most of the cases, this is due to normal variants of short stature which, except for adequate information, do not require treatment. Knowledge of the normal characteristics of the growth and of the factors involved in its regulation in the different periods of life is an essential condition to be able to evaluate the normality or abnormality in the growth of a child. In this review, an attempt is made to give a simple summary of the basic features which, from a community setting, allow the pediatrician to: 1) evaluate if the growth of a child is normal or not; 2) know the causes that most often may cause its alteration; 3) know how to orient the diagnosis and when to send the patient to the specialist (based on the clinical history, bone age and, in some cases, on a reduced number of easily available complementary tests); and 4) know the available therapeutic options./em> |
Palabras clave: Talla baja; Crecimiento; Hipocrecimiento; Fracaso de crecimiento
Key words: Short stature; Growth; Deficient growth; Growth failure
Pediatr Integral 2015; XIX (6): 411.e1-411.e23
Introducción
La talla baja es un motivo habitual de preocupación para los padres, de consulta al pediatra de Atención Primaria y de derivación a consultas de Endocrinología Infantil; sin embargo, la mayoría de los niños que consultan por este motivo son niños sanos cuyo hipocrecimiento resultaría de la variabilidad normal de la talla y del ritmo madurativo.
El crecimiento es el proceso biológico más característico de la edad pediátrica y se extiende desde la concepción hasta la finalización de la maduración esquelética y sexual. Conlleva un incremento de masa, pero también una progresiva maduración que lleva al sujeto a adquirir la plena capacidad funcional. Talla y ritmo madurativo están determinados por multitud de mecanismos genéticos y epigenéticos que interaccionan a lo largo de todo el proceso de crecimiento con factores ambientales intrínsecos y extrínsecos(1); de forma que, para que el potencial genético de crecimiento de un determinado individuo no se vea limitado, es imprescindible que “todo funcione bien”: nutrición, entorno psicosocial, medio interno, estructuras físicas, mecanismos biológicos de regulación, etc. Por ello, la valoración del crecimiento de un niño constituye un indicador sensible de su estado de salud y bienestar y forma parte de todos los programas de prevención de la salud en los niños (“control del niño sano”).
Desde el punto de vista médico, la talla baja puede ser un síntoma de múltiples patologías; sin embargo, en la mayoría de los casos, es simplemente la expresión de uno de los extremos de la distribución normal de la talla y del ritmo madurativo del ser humano. Pese a ello, socialmente, la talla baja es considerada frecuentemente como una causa de estrés psicosocial para el niño y un factor limitante de su futuro éxito social y profesional, especialmente en los varones. Por otra parte, los medios de comunicación y, en ocasiones, los propios médicos, hemos transmitido a la sociedad el concepto erróneo de que toda talla baja puede y debe ser tratada. La consecuencia es que, la mayoría de los niños que consultan por este motivo son niños normales que no requieren tratamiento y en los que la utilización de tratamientos intempestivos no conlleva claros beneficios y sí potenciales efectos secundarios. De ahí, la importancia de establecer un diagnóstico correcto y de transmitir a los padres una información adecuada y veraz.
Bases fisiopatológicas del crecimiento normal
El conocimiento del patrón normal de crecimiento de un niño y de sus factores reguladores es la base para poder detectar situaciones patológicas. No es posible valorar si el crecimiento de un niño es normal o no, si no se conocen las características normales del proceso, los principales factores que lo regulan y cómo la variabilidad normal o determinadas patologías pueden modificarlo.
Patrón de crecimiento
La curva que representa el crecimiento humano normal muestra una morfología sigmoide. A finales de los años ochenta, Kalberg(2) propuso un modelo matemático de la curva conocido como “modelo ICP” (Fetal-Infancy, Childhood, Puberty), según el cual, la curva de crecimiento normal estaría formada por la suma y solapamiento de tres componentes: 1) fetal-primera infancia; 2) prepuberal o de la segunda infancia; y 3) puberal, (Figs. 1 y 2). El objetivo de este modelo es relacionar sus distintos componentes con los factores biológicos de los que dependen; de forma que, la alteración o el retraso en la aparición de uno de estos componentes permitiera una orientación diagnóstica más rápida de las distintas patologías.
Figura 1. Gráfica de Kalberg (talla/longitud), donde se ponen de manifiesto los tres componentes de la curva normal de crecimiento humano: 1) fetal-primera infancia; 2) prepuberal o segunda infancia; y 3) puberal, así como los principales factores de los que dependen y los mecanismos hormonales que regulan el crecimiento en estas tres etapas de la vida: factores de crecimiento semejantes a la insulina (IGFs), hormona de crecimiento (GH) y hormonas sexuales (HS).
Componente fetal-primera infancia
La deceleración normal en la velocidad de crecimiento que experimentan los niños con talla baja familiar y/o maduración tardía, habitualmente, entre los 1-3 años de vida, es responsable de que numerosos niños sean erróneamente catalogados como “fracasos de crecimiento”.
El componente fetal-1ª infancia se extendería desde la media gestación hasta aproximadamente los 2-3 años. La velocidad de crecimiento (VC: ? talla/año) durante el periodo fetal es muy rápida y continúa siéndolo durante los tres primeros años de vida; si bien, la caída postnatal de la VC es clara y progresiva respecto a la vida intrauterina (Fig. 2).
Figura 2. Gráfica de Kalberg (velocidad de crecimiento), donde se ponen de manifiesto los tres componentes de la curva normal de crecimiento humano: 1) fetal-primera infancia; 2) prepuberal o segunda infancia; y 3) puberal.
El crecimiento fetal, en ausencia de anomalías genéticas, no depende prácticamente del genotipo, sino del espacio disponible para crecer (tamaño uterino y materno) y de la nutrición, que depende, a su vez, de la función placentaria (aporte de oxígeno y nutrientes). Después del nacimiento y durante los primeros meses de vida, la nutrición continúa siendo el principal factor determinante del crecimiento, pero la influencia del genotipo se va poniendo progresivamente de manifiesto y, como consecuencia, se producen aceleraciones o deceleraciones en el ritmo de crecimiento de los niños en función de su potencial de crecimiento (talla familiar alta, media o baja) y/o de su ritmo de maduración (rápido, normal o lento), rasgos ambos determinados genéticamente, que les llevarán a establecer su propio canal de crecimiento (fenómeno de “canalización”), habitualmente, entre el 2º y el 3er año de vida. Pasado este periodo de ajuste, la correlación (r) entre la talla del niño y la talla media parental (TMP) o la talla adulta se incrementa; de forma que, que pasa de 0,2-0,3 en el recién nacido (RN) a 0,7-0,8 a los 3 años de edad.
Los mecanismos hormonales que regulan el crecimiento fetal son, en gran medida, desconocidos; no obstante, la insulina y el sistema de los factores de crecimiento semejantes a la insulina (IGFs –insulin-like growth factors–), especialmente los IGFs números 1 y 2 (IGF-1 e IGF-2), parecen tener un papel relevante(3). Al contrario de lo que ocurre en la vida postnatal, la producción fetal de IGFs no es dependiente de hormona de crecimiento (GH); de hecho, la GH no es determinante en el crecimiento fetal. Esta situación se mantiene durante los primeros meses de vida extrauterina, aunque la influencia de la GH en el control del crecimiento se va poniendo de manifiesto de forma gradual y progresiva y está claramente presente, tan pronto como, a los 6 meses de vida.
Componente prepuberal o de la segunda infancia
La deceleración postnatal de la VC continúa durante todo el periodo prepuberal, pero de forma más lenta, debido a la adición del componente prepuberal (Figs. 1 y 2). Este se pone de manifiesto, habitualmente, entre los 6 y 12 meses de edad postnatal y se extiende hasta la finalización del crecimiento. La reducción progresiva del ritmo de crecimiento durante el periodo prepuberal mantiene las VC entre 5-7 cm/año durante la mayor parte del tiempo (Fig. 2) y persiste hasta el inicio del estirón puberal, momento en que se alcanza el nadir (4,5 y 5 cm/año). Este fenómeno, conocido como “depresión prepuberal de la VC”, es especialmente manifiesto en los maduradores tardíos, que llegan a alcanzar VC de solo 2-3 cm/año.
Durante el período prepuberal, el principal regulador del crecimiento es el genotipo. Los niños con talla familiar baja o maduración lenta tienden a crecer con una VC media inferior al percentil 50; mientras que, los niños con talla familiar alta o maduradores rápidos tienden a hacerlo con una VC media por encima del percentil 50. Esta diferencia en la VC, a lo largo de todo el periodo prepuberal, es la principal responsable de la diferencia de talla adulta entre sujetos con talla familiar alta o baja. Por el contrario, las diferencias de VC entre maduradores rápidos y lentos no suelen afectar significativamente la talla adulta; ya que, se compensan, al menos parcialmente, gracias a un mayor o menor número de años de crecimiento prepuberal.
El principal regulador de la VC durante el periodo prepuberal y, en general, en el periodo postnatal, es el eje GH-IGFs (Fig. 3); no obstante, otras muchas hormonas (insulina, hormonas tiroideas, andrógenos suprarrenales, glucocorticoides, leptina, paratohormona, vitamina D…) y factores de crecimiento locales contribuyen también a la regulación del crecimiento, aunque con frecuencia, a través de interacciones con el eje GH-IGFs.
Figura 3. Representación esquemática del sistema GH-IGFs. Se representan las acciones endocrinas, paracrinas y autocrinas de IGF-I, así como la formación del compejo trimolecular de alto peso molecular, formado por IGF-I, IGFBP-3 y ALS.
GHRH: hormona hipotalámica liberadora de hormona de crecimiento (GH); SRIH: hormona inhibidora de la liberación de GH, somatostatina; GHBP: proteína trasportadora de GH; GHR: receptor de GH; IGF-I: factor de crecimiento semejante a la insulina número 1; IGFBP-3: proteína trasportadora de IGFs número 3; ALS: subunidad ácido lábil; IGFIR: receptor de IGF-I.
La GH es sintetizada y secretada de forma pulsátil (4-6 pulsos secretorios/día) y con un predominio nocturno por las células somatotropas de la adenohipófisis(4). Posee acciones directas estimulantes del crecimiento, pero la mayoría de ellas son mediadas por los IGFs y especialmente por el IGF-1. Alrededor del 50% de la GH circula en la sangre unida a una proteína de transporte específica, la GHBP (growth hormone binding protein), que es idéntica a la porción extracelular del receptor de GH (GHR), del que deriva por rotura proteolítica. Cuando la GH se une al RGH, este debe dimerizar para poder transmitir el mensaje al interior de la célula, que no es otro que inducir la expresión de determinados genes, como es el caso del IGF-1, a través de diferentes vías intracelulares, de las cuales, la vía MAPK (mitogen-activated protein kinase), la STAT (signal transducers and activators of transcription) y la PI3-K (phosphatidylinositol 3-OH kinase) son las mejor caracterizadas.
Los IGFs (IGF-1 e IGF-2), previamente conocidos como somatomedinas, son péptidos de estructura similar a la insulina producidos en el hígado y en los tejidos periféricos, especialmente en hueso y músculo, que, de forma endocrina (IGFs circulantes) o paracrina-autocrina (IGFs sintetizados en los tejidos), ejercen acciones mitogénicas y anabolizantes sobre la mayoría de las células(4,5). Aproximadamente, el 99% de los IGFs que circulan en la sangre lo hacen unidos a proteínas de transporte específicas, las IGFBPs (IGFs binding proteins). La más importante desde el punto de vista clínico es la IGFBP-3, que transporta un 75-90% de los IGFs circulantes. El complejo IGF-IGFBP-3 se une en la sangre con otra proteína, la ALS (subunidad ácido-lábil), formando un complejo trimolecular (IGF-IGFB-3-ALS) de alto peso molecular, lo que limita la salida de los IGFs a los tejidos, aumentando su vida media y su concentración sérica, al tiempo que evita sus efectos hipoglucemiantes derivados de su similitud molecular con la insulina. Proteasas circulantes rompen lentamente estos complejos y permiten la liberación de los IGFs y su salida a los tejidos. Tanto la IGF-1 como la IGFBP-3 y la ALS son proteínas producidas en el hígado por estímulo directo de la GH y mantienen niveles séricos más o menos estables a lo largo del día; de forma que, su determinación puede utilizarse como un reflejo indirecto de la secreción de GH. Por el contrario, las características pulsátiles de la secreción normal de GH hacen que su determinación basal carezca de utilidad en el diagnóstico de los hipocrecimientos. De estas tres proteínas dependientes de GH, la más utilizada clínicamente ha sido la determinación de IGF-1. La IGFBP-3 presenta, sobre todo en menores de 3 años, algunas ventajas sobre la IGF-1 como marcador de deficiencia de GH: concentraciones séricas más elevadas (menor solapamiento entre sujetos normales y deficitarios), menor variación con la edad y el desarrollo puberal y menor influencia del estado nutricional sobre sus niveles séricos (IGF-1 e IGFBP-3 disminuyen en situaciones de malnutrición); en general, IGFBP3 es más específico pero menos sensible que IGF-1 para el diagnóstico de deficiencia de GH.
Componente puberal
Cuando la pubertad se inicia a una edad normal, aunque esta sea adelantada o retrasada respecto a la media, la talla final no se modifica, aunque sí el momento en que esta se alcanza.
El componente puberal se suma al prepuberal a una edad variable, que es determinada por el genotipo, responsable del ritmo de maduración individual y del momento en que se inicia la pubertad. Su aparición se manifiesta por una clara inflexión en la curva de crecimiento, el llamado “estirón puberal”. En las niñas, la aparición del botón mamario (estadio II de Tanner) marca el inicio puberal, a una edad media de 10,5-11 años, y suele coincidir con el inicio del “estirón puberal”. La menarquia, por el contrario, es un fenómeno tardío, que se produce alrededor de 2 años después del inicio puberal (estadio IV de Tanner), cuando el estirón está prácticamente finalizado. El crecimiento postmenarquia es muy variable, entre 4 y 11 cm (media de 6-7 cm). En los varones, el inicio de la pubertad lo marca el incremento del volumen testicular (=4 ml), que se produce a una edad media de 11,5-12 años. A diferencia de las niñas, el estirón puberal no coincide con el inicio de la pubertad, sino que se inicia, aproximadamente, un año después (12,5-13 años), en un estadio III de Tanner y unos 2 años más tarde que en las niñas.
El crecimiento cesa en los varones y mujeres a una edad media de 21 y 17 años, respectivamente. La ganancia de talla, desde el inicio del estirón hasta la finalización del crecimiento, supone unos 25-30 cm en los varones y unos 23-27 en las mujeres (15-20% de la talla adulta) y predomina proporcionalmente el aumento de tronco sobre el de extremidades. La magnitud del estirón es similar en sujetos con talla familiar alta o baja. En lo que al ritmo de maduración se refiere, los maduradores rápidos no solo crecen a un mayor ritmo durante el periodo prepuberal, sino que tienen un estirón puberal más potente que los maduradores normales y estos, a su vez, mayor que el de los maduradores tardíos, compensándose así el mayor o menor número de años de crecimiento prepuberal. Por ello, una maduración normal, pero adelantada o retrasada respecto a la media, modifica la edad a la que se alcanza la talla final, pero no la magnitud de esta. Los dos años más de crecimiento prepuberal que tienen los niños (8-10 cm) y la mayor amplitud de su estirón puberal (3-5 cm) determinan los 12,5-13 cm de diferencia entre la talla adulta de ambos sexos, así como la mayor longitud proporcional en los varones de las extremidades respecto al tronco (mayor periodo de crecimiento prepuberal).
La responsabilidad de la aparición del componente puberal de la curva de crecimiento corresponde a los esteroides sexuales, no solo porque poseen acciones anabolizantes directas sobre el cartílago de crecimiento, sino, también, porque incrementan la secreción de GH; de forma que, la actuación sinérgica de esteroides sexuales (especialmente estradiol) y GH sería la responsable del estirón puberal, pero también del cierre de los cartílagos de crecimiento y de la finalización de este.
Fenómenos de “crecimiento de recuperación”, “canalización” y “programación”
La capacidad de recuperación de la talla perdida tras la curación o mejoría de una enfermedad crónica es lo que se denomina “crecimiento de recuperación”(6). Puede definirse como: el incremento en el ritmo de crecimiento por encima de los límites normales, que se produce durante un tiempo limitado después de un periodo de detención del crecimiento y que permite recuperar total o parcialmente el crecimiento perdido. Su existencia presupone que cada niño, en condiciones normales, tendería a mantenerse dentro de un estrecho carril de crecimiento, un fenómeno que se conoce como “canalización del crecimiento”. Según esta hipótesis, cuando un sujeto, por la acción de una determinada noxa, se desvía de su canal de crecimiento, el organismo no solo es capaz de percibirlo, sino que, cuando la noxa desaparece, tiende a recuperarlo. Los mecanismos fisiológicos que median el fenómeno de la “canalización” no son bien conocidos y la recuperación del canal de crecimiento, dependiendo del momento de actuación de la noxa, así como de su gravedad y duración, puede no ser completo; de hecho, se ha postulado la existencia de “periodos críticos” o “de ventana”, durante los cuales, la actuación de una noxa podría alterar definitivamente la talla adulta. Estos periodos de alta vulnerabilidad, corresponderían a los momentos de máximo crecimiento, como es la pubertad y, especialmente, el periodo fetal y primer año de vida, cuando los fenómenos de proliferación celular son más intensos. Según la hipótesis de la “programación”, la repercusión de estas agresiones en periodos críticos sería mucho más amplia que la afectación aislada del crecimiento, ya que podrían inducir cambios permanentes, morfológicos y funcionales (expresión génica, replicación celular, estructura y función de órganos, composición corporal, secreción/acción de hormonas y factores del crecimiento…), que modificarían la susceptibilidad al desarrollo en la vida adulta de determinadas enfermedades degenerativas (hipótesis de Barker o del origen fetal de las enfermedades del adulto(7)), como sería el caso de: obesidad, síndrome metabólico o enfermedades cardiovasculares.
Concepto y epidemiología del hipocrecimiento
Establecer la normalidad en el crecimiento de un niño puede, en algunos casos, ser un problema complejo; ya que, no existe un punto de corte que discrimine de forma nítida entre tallas y VC “normales” y “patológicas”.
La “normalidad” de una talla no puede establecerse solo en relación con la edad, el sexo y la etnia del sujeto (normalidad estadística), sino que, al ser un rasgo genético e influenciado por el ritmo madurativo, debe analizarse también en su contexto familiar y en función del ritmo madurativo individual de cada sujeto(8,9).
La correlación de la talla de un niño con su contexto familiar suele hacerse comparando su “talla diana” (TD) con su expectativa de talla adulta (predicción de talla). La TD, también denominada talla genética, es, simplemente, la talla esperable para los hijos de una pareja determinada, asumiendo un proceso normal de herencia y unos efectos ambientales sobre el crecimiento, similares en ambas generaciones(9). La fórmula más comúnmente empleada para calcularla es la desarrollada por Tanner a partir de la talla media parental (TMP) ajustada al sexo del niño (Tabla I). En cuanto a la predicción de talla adulta (PTA), esta puede hacerse de diferentes maneras e incluir o no en los cálculos la TMP(9); pero todas ellas tienen en cuenta el ritmo madurativo individual, que se valora en la práctica clínica mediante la “edad ósea” (EO). La fiabilidad de los métodos de PTA es relativamente escasa y tanto menor cuanto menor es la edad del niño. En cualquier caso, la PTA no debería hacerse antes de que los ajustes en función del contexto familiar y del ritmo madurativo (canalización) se hayan realizado y el crecimiento sea más estable. El método más sencillo es utilizar la “talla proyectada”, que se calcula extrapolando la talla final que alcanzará el niño a partir del carril de crecimiento para la edad en el que se encuentra y siguiéndolo hasta los 18-20 años. Si la EO está retrasada o adelantada, es preferible extrapolar la talla final a partir de la talla para la EO. La talla final también puede predecirse mediante diferentes métodos matemáticos, todos los cuales tienen en consideración la EO como indicador del grado de maduración alcanzada. El más utilizado en la clínica, por su sencillez y fiabilidad, es el método de Bayley-Pinneau, que tiene en consideración, únicamente, la talla del niño y su EO determinada por el atlas de Greulich-Pyle(9).
Otro aspecto a la hora de valorar si el crecimiento de un niño es normal o no, es tener en consideración que el crecimiento es un proceso dinámico; mientras que, la talla es un parámetro estático y que, por ello, la observación en un momento dado de una talla “normal” no excluye la posibilidad de que se esté produciendo un fracaso de crecimiento. Es necesario analizar, también, si la VC a lo largo del tiempo es normal. La menor fiabilidad en el cálculo de la VC y las múltiples variaciones que, en condiciones normales, esta experimenta hacen que, con frecuencia, sea también difícil determinar su normalidad o anormalidad(8). Los criterios que, en la práctica clínica, utilizamos habitualmente para establecer cuándo un niño debe ser estudiado por un problema de hipocrecimiento(1) quedan reflejados en la tabla I.
La prevalencia de hipocrecimiento en un momento dado es difícil de establecer, no solo por las dificultades metodológicas inherentes a su definición, sino por la aparición, a lo largo de la infancia, de nuevos casos (patología crónica, alteraciones hormonales…) y por la recuperación de otros (pequeños para su edad gestacional que se recuperan, patologías crónicas que se curan o tratan…). Si consideramos aisladamente el concepto estadístico de talla baja, como una talla por debajo de ?2 SDS para su edad, sexo y etnia, el 2,3% de la población entraría en el concepto de hipocrecimiento; no obstante, el número de sujetos que se miden en los estudios poblacionales es insuficiente para determinar con fiabilidad los extremos de la curva de Gauss que representa la distribución de la talla y, dado que, es más factible que el crecimiento se vea gravemente frenado que acelerado, es probable que el porcentaje de tallas bajas sea superior al 2,3%. Si consideramos, además, las otras posibles definiciones de hipocrecimiento (Tabla I), es muy probable que el número de niños con hipocrecimiento sea superior al 3-5%.
Etiopatogenia y clasificación de los hipocrecimientos
Dentro de los hipocrecimientos, clásicamente, se han diferenciado dos grandes grupos etiopatogénicos: los hipocrecimientos normales o variantes normales de talla baja (VNTB) y los hipocrecimientos patológicos. En la actualidad, tienden a clasificarse más como: hipocrecimientos de causa conocida e hipocrecimientos de causa desconocida o idiopáticos (TBI), entre los que se incluirían las VNTB.
Hipocrecimientos de causa conocida
Representan alrededor del 20% de los hipocrecimientos(1) y serían la consecuencia de trastornos patológicos que alterarían la capacidad de crecimiento intrínseca de los tejidos (osteocondrodisplasias, alteraciones del metabolismo óseo, retrasos de crecimiento intrauterino, cromosomopatías y síndromes dismórficos), sus mecanismos reguladores (hipocrecimientos de causa endocrinológica) o el ambiente interno (malnutrición y patología crónica en diferentes órganos y sistemas) y emocional del niño (hipocrecimiento psicosocial).
Desde un punto de vista etiopatogénico y diagnóstico (Tabla II) es útil, diferenciar, dentro de los hipocrecimientos, el momento de su inicio (pre o postnatal) y si se conservan o no las proporciones corporales normales (armónico o disarmónico). Los hipocrecimientos de inicio prenatal suelen ser el resultado de una agresión al ambiente fetal o de un defecto genético; por el contrario, los de inicio postnatal suelen responder, en general, a una agresión iniciada fuera del período de vida intrauterino. En lo que se refiere al mantenimiento o no de la armonía corporal, los hipocrecimientos disarmónicos son siempre patológicos y pueden ser congénitos (osteocondrodisplasias) o, menos frecuentemente, adquiridos (p. ej., los secundarios a radioterapia espinal); por el contrario, los armónicos pueden ser normales o patológicos.
Hipocrecimientos de inicio prenatal
Son conocidos como recién nacidos pequeños para su edad gestacional (RNPEG) y el 80-90% experimentarán un crecimiento de recuperación, parcial o total, durante el primer o segundo año de vida y alcanzarán una talla dentro del rango normal (entre ± 2 SDS), aunque con frecuencia por debajo de su contexto familiar.
Se considera a un RN como RNPEG cuando su peso (PRN) y/o su longitud al nacimiento (LRN) se encuentran, al menos, 2 SDS por debajo de la media para su edad gestacional. En España, las tablas y graficas recomendadas para la clasificación de los RN como RNPEG son las correspondientes al Estudio Español de Crecimiento de 2010, que abarcan desde la 26 a las 42 semanas de edad gestacional.
En los países desarrollados, solo el 4-7% de los RN son RNPEG; sin embargo, es una de las causas más importantes de talla baja, ya que, el antecedente de RNPEG se encuentra en el 20% de los adultos con talla baja(10). Los RNPEG presentan una elevada morbimortalidad perinatal, así como una mayor frecuencia de secuelas a largo plazo, como son, entre otras: hipocrecimiento postnatal, disminución del rendimiento intelectual y psicológico y desarrollo de anomalías hormonales y metabólicas en la infancia y edad adulta (adrenarquia prematura, resistencia a la insulina, hiperandrogenismo ovárico, obesidad, diabetes mellitus tipo 2, dislipemia, hipertensión arterial y enfermedad cardiovascular), que han sido atribuidas a la modificación del “programa” genéticamente establecido como consecuencia de la alteración intrauterina (hipótesis de Baker)(7).
El patrón de crecimiento de los RNPEG suele ser característico. El 80-90% experimentan un crecimiento de recuperación, parcial o total, durante el primer y segundo año de vida, que puede prolongarse algo más en los RNPEG prematuros, y alcanzan una talla dentro del rango normal, entre ± 2 SDS, aunque con frecuencia por debajo de su contexto familiar. El 10-20% restante mantendrán la talla baja (< 2 SDS) después de los 2 años y en, al menos, un 50% de estos, la talla final será baja. La EO suele estar retrasada, pese a lo cual la pubertad se inicia habitualmente a una edad normal o incluso ligeramente adelantada, corrigiéndose rápidamente el retraso en la maduración ósea y alcanzando una talla final baja que, en la mayoría de los casos, es similar, en SDS, a la talla prepuberal. También, los niños prematuros con muy bajo peso al nacimiento (PRN < 1.500 g), aunque este sea adecuado a su EG, pueden mostrar también un patrón de crecimiento similar al de los RNPEG, con ausencia de un crecimiento de recuperación adecuado y talla final baja.
Cuando el RN presenta una disminución combinada del PRN y de la LRN (RNPEG armónico) el riesgo de alcanzar una talla adulta baja es mayor que cuando solo se afecta el PRN (RNPEG disarmónico).
Desde el punto de vista etiopatogénico (Tabla II), una tercera parte de los RNPEG se deberían a factores fetales (cromosomopatías, anomalías congénitas y síndromes dismórficos) y las otras dos terceras partes a factores maternos (malnutrición, infecciones, tóxicos…) y uterino-placentarios (malformaciones uterinas, arteria umbilical única…); no obstante, hasta en un 40% de los casos no se identifica ninguna causa patológica.
Multitud de cuadros sindrómicos (Russell-Silver, Seckel, Cornelia de Lange, Noonan, Prader-Willi…), muchos de ellos de causa genética (mutaciones, deleciones, disomías uniparentales…), al igual que ocurre en la mayoría de las cromosomopatías, presentan, como una de sus principales manifestaciones clínicas, talla baja, con frecuencia, pero no siempre, de inicio prenatal. El hipocrecimiento se asocia frecuentemente, además de a rasgos dismórficos más o menos específicos y marcados, a malformaciones en diferentes órganos y a un grado variable de retraso mental; de ahí, la importancia de buscar sistemáticamente en la exploración de todo niño con talla baja, la presencia de rasgos sindrómicos que orienten hacia este tipo de diagnósticos (Tabla III).
Entre las cromosomopatías, merecen especial mención por su frecuencia: el síndrome de Down (trisomía 21; 1:600 RN vivos) y el síndrome de Turner (45, X0, y sus variantes; 1:2.500-3.000 RN vivas). Las características fenotípicas del síndrome de Down hacen que su diagnóstico se realice, habitualmente, en el periodo neonatal; por el contrario, el diagnóstico del síndrome de Turner suele hacerse más tardíamente. Sus rasgos sindrómicos característicos (implantación posterior del cabello baja y en forma de “M”, pterigium colli, acortamiento de metacarpianos, cúbito valgo, tórax en coraza…) pueden ser poco manifiestos o pasar desapercibidos, aunque el fracaso de crecimiento, sobre todo a partir de los 2-3 años (solo un 16% son RNPEG), es prácticamente constante.
En cualquier niña con talla baja de causa poco clara, aun en ausencia de cualquier rasgo sindrómico, es obligada la realización de un cariotipo.
Osteocondrodisplasias
La desproporción entre los distintos segmentos corporales (hipocrecimiento disarmónico) debe hacer pensar en la existencia de una displasia ósea u osteocondrodisplasia.
Las displasias óseas (DO) representan anomalías primarias del hueso y del cartílago, de base genética y herencia variable que, habitualmente, dan lugar a una talla baja disarmónica. Individualmente, son entidades raras, pero colectivamente integran un grupo numeroso (2-5:10.000 RN). El hipocrecimiento y la desproporción entre miembros y tronco puede ser debida a un acortamiento preferentemente de los miembros (acondroplasia, hipocondroplasia, pseudoacondroplasia, discondrosteosis de Léri-Weill, condrodisplasia metafisaria…), del tronco (mucopolisacaridosis, displasias espondiloepifisarias…) o de ambos (displasia metatrópica…), y puede o no estar presente en el momento del nacimiento.
En los últimos años, se ha producido un considerable avance en el conocimiento de las bases moleculares de las DO. Su última clasificación distingue, en función de sus características clínicas, bioquímicas, radiológicas y moleculares, 456 entidades diferentes, agrupadas en 40 familias, con 226 genes implicados(11). Pero, si dejamos aparte las mutaciones del gen SHOX (short stature homeobox-containing gen) que no siempre dan lugar a hipocrecimientos disarmónicos, mutaciones en solo dos loci son responsables de las formas más frecuentes y, por consiguiente, de la mayoría de las DO: COL2A1 (gen del colágeno tipo 2, en 12q13.1-q13.3), responsable de la mayoría de las displasias espondiloepifisarias; y FGFR3 (gen del receptor tipo 3 del factor de crecimiento de los fibroblastos, en 4p16.3), responsable, entre otras entidades clínicas, de: acondroplasia (la DO más frecuente y conocida; 1: 15.000-40.000 RN vivos), hipocondroplasia, displasia de SADDAN y displasia tanatofórica.
El diagnóstico genérico de DO puede ser relativamente sencillo ante un paciente con marcada disarmonía corporal; sin embargo, un diagnóstico más preciso puede ser difícil, debido a la multitud de cuadros clínicos y a su variable expresividad clínica. Por otra parte, en algunas DO, la disarmonía corporal puede ser poco manifiesta; de forma que, con facilidad, pueden ser incluidas entre los hipocrecimientos armónicos de etiología incierta o idiopática (TBI). Entre las DO que por su frecuencia, expresividad clínica, herencia dominante y patrón de crecimiento pueden confundirse con un hipocrecimiento armónico, y en especial con una VNTB, se encontrarían la hipocondroplasia y la haploinsuficiencia del gen SHOX.
Las DO no siempre presentan disarmonía corporal o esta es claramente evidente; por ello, algunas formas de DO pueden entrar a formar parte del diagnóstico diferencial de la TBI. La haploinsuficiencia del gen SHOX es la causa monogénica más frecuente de talla baja en la especie humana.
Hipocondroplasia. Ha sido descrita como una “forma leve” de acondroplasia; no obstante, aunque ambas enfermedades se heredan de forma autosómica dominante y se deben a mutaciones en el mismo gen (FGFR3), no se han descrito familias en las que coincidan ambas entidades. La mutación responsable más frecuente es Asn540Lys, pero sus bases moleculares son más heterogéneas que en el caso de la acondroplasia y otros genes podrían estar implicados; de hecho, se han descrito fenotipos compatibles con hipocondroplasia asociados a mutaciones en SHOX. Desde el punto de vista clínico, no presentan el aspecto facial característico de la acondroplasia, el hipocrecimiento y la rizomelia son menos marcados y el incurvamiento de las piernas y el genu varum son frecuentes. Como en la acondroplasia, es característica la reducción progresiva de la distancia interpeduncular lumbar, de L1 a L5, y las anomalías en la pelvis. La talla adulta se sitúa alrededor de 132-150 cm, pero el hipocrecimiento puede no ser manifiesto hasta los dos años y confundirse, dados los antecedentes familiares, con una forma extrema de talla baja familiar.
Síndromes por deficiencia del gen SHOX. Este gen se localiza en la región PAR1 (región pseudoautosómica 1), en el extremo distal de Xp e Yp. Las mutaciones o deleciones en homocigosis o heterocigosis compuesta son excepcionales y dan lugar a una forma severa de DO, la llamada displasia mesomélica de Langer, con talla media inferior a -6 SDS y aplasia de cúbito y peroné. Por el contrario, la haploinsuficiencia del gen SHOX, debida a mutaciones o deleciones en heterocigosis en SHOX/PAR1, con herencia pseudoautosómica dominante, representan la causa monogénica más frecuente de talla baja en la especie humana (1:1.000-2.000) y es responsable: 1) de la mayoría de los casos de discondrosteosis de Léri-Weill (60-80%); 2) del 2-5% de las tallas bajas aparentemente armónicas y consideradas a priori como TBI; y 3) de algunas de las manifestaciones clínicas del síndrome de Turner(12).
Las manifestaciones clínicas más características de la haploinsuficiencia del gen SHOX son: hipocrecimiento mesomélico (acortamiento de antebrazos y tibias), cubitus valgo, deformidad de Madelung (Fig. 4), acortamiento de metacarpianos y metatarsianos, paladar ojival, desarrollo anormal de las orejas, micrognatia y cuello corto. Estas manifestaciones clínicas definen la discondrosteosis o síndrome de Léri-Weill y son más marcadas en mujeres y especialmente después de la pubertad. No obstante, la variabilidad fenotípica es muy amplia, incluso entre los miembros de una misma familia (falta de correlación genotipo-fenotipo); de forma que, el fenotipo clínico en la haploinsuficiencia del gen SHOX se muestra como un continuum (Fig. 4), que abarca desde formas muy graves de talla baja desproporcionada a formas muy leves de talla baja o talla normal-baja, armónica o disarmónica, con o sin otras anomalías clínicas y radiológicas(12).
Figura 4. Esquema donde se representa la variable expresividad clínica y fenotípica de la insuficiencia del gen SHOX que viene a ser un continuum que abarca desde formas muy severas de talla baja desproporcionada a formas muy leves de talla baja o normal, armónica o disarmónica, con o sin otras anomalías clínicas y radiológicas. Deformidad de Madelung: acortamiento e incurvación del radio con subluxación dorsal del extremo distal del cúbito, triangularización de los huesos del carpo y fusión prematura de las epífisis.
Por ello, se ha desarrollado un sistema de puntuación, basado en los hallazgos clínicos y antropométricos (Fig. 5), que permitiría optimizar la selección de pacientes en los que debería excluirse una haploinsuficiencia del SHOX y que no presentan las manifestaciones clínicas características del síndrome de Léri-Weill, como la clásica deformidad de Madelung. En lo que se refiere a la talla adulta, la talla media de estos pacientes es de 145 cm en mujeres y de 155 en varones, pero alrededor del 50% de los pacientes muestran una talla normal. Al comparar con los hermanos no afectados, la pérdida de talla supone, de media, unos 14,4 cm (2,4 SDS) en mujeres y unos 5,3 cm (0,8 SDS) en varones.
Figura 5. Esquema donde se representan aquellas circunstancias clínicas y antropométricas que deben hacer sospechar una haploinsuficiencia del SHOX y solicitar estudio genético. LWD: discondrosteosis de Léri-Weill; TB: talla baja. *Sistema de puntuación tomado de: Rappold G, et al. Genotypes and phenotypes in children with short stature: clinical indicators of SHOX haploinsufficiency. J Med Genet. 2007; 44: 306-13.
Malnutrición
En los países en vías de desarrollo, la malnutrición junto con los procesos infecciosos y parasitarios, especialmente gastrointestinales, actúan de manera sinérgica (binomio infección-malnutrición) en la génesis del fracaso de crecimiento.
En los países subdesarrollados o en vías de desarrollo, el binomio infección-malnutrición (Fig. 6) es con mucho la causa más frecuente de hipocrecimiento. En los países desarrollados, la escasez de alimentos es una situación excepcional y los hipocrecimientos de causa nutricional suelen ser secundarios a: patologías crónicas, dietas inadecuadas en su cantidad (ejercicio excesivo) o composición (vegetarianas estrictas, macrobióticas…) o trastornos más o menos graves de la conducta alimentaria (anorexia nerviosa, síndrome del miedo a la obesidad, fallo de medro…). En cualquier caso, el resultado final de todas estas situaciones es un aporte insuficiente de macro (malnutrición calórico-proteica) o de micronutrientes (minerales y vitaminas).
Figura 6. Esquema donde se refleja la interacción entre malnutrición e infección-infestación recurrente en la génesis del hipocrecimiento. La malnutrición, asociada a la pobreza, a enfermedades crónicas y a dietas inadecuadas, determina alteraciones en la inmunidad humoral y celular favoreciendo los procesos infecciosos y parasitarios, especialmente gastrointestinales, lo que a su vez induce una mayor malnutrición (incremento de pérdidas y catabolismo con disminución de aportes), cerrando así el circulo vicioso del binomio malnutrición-infección.
En la malnutrición calórico-proteica, una pérdida o inadecuada ganancia ponderal suele acompañar o preceder a la alteración del crecimiento en uno o dos años; si bien, no siempre es así, y el fracaso de crecimiento, acompañado de retraso de la EO y de la pubertad, puede ser el mecanismo de adaptación a la disminución de nutrientes, sin que se altere la relación peso/talla u otros marcadores clínicos/bioquímicos de malnutrición(13). En este proceso adaptativo, todo el sistema hormonal está implicado, pero son de especial importancia, las alteraciones en el eje GH-IGFs (resistencia a la GH, con niveles séricos normales o elevados de GH y disminuidos de IGF-1 y de IGFBP-3).
En lo referente a los déficits aislados de micronutrientes, se ha demostrado que, además de las deficiencias de calcio y fósforo, algunos oligoelementos, como: iodo, hierro, cobre, cromo y zinc, son capaces de provocar cuadros de retraso de crecimiento en humanos. En los déficits vitamínicos aislados, la alteración del crecimiento no suele ser una manifestación clínica precoz, con excepción hecha de la vitamina D, que al igual que el calcio y el fósforo, está directamente implicada en la mineralización y crecimiento del hueso.
Infecciones e infestaciones recurrentes
Son características de los países subdesarrollados, donde los procesos infecciosos y parasitarios, especialmente gastrointestinales, actúan de manera sinérgica con la malnutrición en la génesis del fracaso de crecimiento. En los países desarrollados, las infecciones recurrentes son poco frecuentes, pero, cuando alteran el crecimiento, suelen reflejar la existencia de malformaciones anatómicas (renales, pulmonares…) o inmunodeficiencias subyacentes (SIDA…) y contribuir al fracaso de crecimiento asociado a otras patologías crónicas. La malnutrición parece ser el principal mecanismo fisiopatológico implicado en estas formas de hipocrecimiento; ya que, la alimentación suplementaria durante los períodos de infección parece evitar o, al menos, disminuir sus repercusiones negativas sobre el crecimiento.
Enfermedades crónicas
Cualquier patología crónica (gastrointestinal, renal, cardíaca, pulmonar, hematooncológica…), si es lo suficientemente grave y prolongada, puede provocar un hipocrecimiento. En general, cuanto más precoz, grave y prolongada sea la enfermedad, menos posibilidades hay de que pueda recuperarse completamente.
El fracaso en el crecimiento y la talla baja consiguiente son hallazgos habituales en los niños que padecen enfermedades crónicas (Tabla II). Se calcula que, alrededor del 10-15% de los hipocrecimientos serían secundarios a enfermedades crónicas; no obstante, es probable que este porcentaje no solo esté infravalorado, sino que se incremente como consecuencia de la mayor supervivencia en muchas enfermedades crónicas. Los factores etiopatogénicos implicados en el fracaso del crecimiento asociado a las enfermedades crónicas son múltiples y varían dependiendo de la enfermedad de base, pero suelen estar en relación con: malnutrición, alteraciones metabólicas, efectos secundarios de la terapia, infecciones sobreañadidas y, posiblemente también, con los trastornos psicológicos que acompañan al padecimiento de una enfermedad crónica. Dentro de ellos, la malnutrición, a la que se puede llegar por múltiples mecanismos (disminución de aportes o incremento de pérdidas o demandas), es uno de los factores más importantes y constantes.
En lo que se refiere a las manifestaciones clínicas, las específicas de la enfermedad de base serán, en la mayoría de los casos, las predominantes en el cuadro clínico y el fracaso del crecimiento será solo un síntoma más. No obstante, en determinadas patologías, como: malnutrición, celiaquía, enfermedad inflamatoria intestinal o acidosis tubular renal, entre otras, el hipocrecimiento puede ser, durante años, el único o el principal síntoma de la enfermedad subyacente.
El patrón de crecimiento suele ser similar en todas ellas. La aparición de la enfermedad va a determinar un enlentecimiento más o menos marcado del ritmo de crecimiento (fracaso de crecimiento) que suele acompañarse de un retraso simultáneo de la EO y del desarrollo puberal. En caso de curación o mejoría significativa, se producirá un “crecimiento de recuperación” que puede permitir recuperar, total o parcialmente, la talla perdida. La medida en que el hipocrecimiento puede ser compensado depende de diferentes factores: edad de inicio, gravedad y duración del fracaso en el crecimiento, etiología y patogénesis de la enfermedad y, también, de factores individuales propios de cada sujeto.
Enfermedades endocrinológicas
El porcentaje de retrasos de crecimiento de origen endocrinológico es muy escaso, alrededor del 5%, y, en concreto, las deficiencias de GH suponen menos de un 1-2% de los hipocrecimientos.
Deficiencia de GH. Su incidencia oscila entre 1:3.500-1:10.000 RN vivos. Puede presentarse de forma aislada o asociado a otras deficiencias hipofisarias (hipopituitarismos) y puede ser congénita (alteraciones genéticas, malformaciones de línea media…) o adquirida (tumores, traumatismos, histiocitosis, infecciones, radioterapia…). En la mayoría de los casos, el déficit es idiopático y solo en aproximadamente un 20% de los casos es posible identificar una causa orgánica responsable. Entre las formas idiopáticas, es frecuente el hallazgo en la RM craneal de determinadas anomalías morfológicas, como son: hipoplasia hipofisaria, tallo hipofisario ausente o muy afilado y neurohipófisis ectópica. Esta asociación, conocida como “síndrome de sección del tallo hipofisario”, aunque de etiopatogenia no aclarada, constituye un dato diagnóstico relevante y conlleva un mayor riesgo de desarrollar en el tiempo otras deficiencias hipofisarias.
Se estima que entre un 5 y un 30% de las formas idiopáticas tendrían una base genética, bien por mutaciones en el gen de GH (GH1; deficiencia o GH biológicamente inactiva) o del receptor de la hormona hipotalámica liberadora de GH (GHRHR), que condicionarían una deficiencia aislada de GH, o bien por mutaciones en genes que codifican para factores de transcripción implicados en el desarrollo de la hipófisis (HESX1, LHX3, LHX4, POUIFI, PROPI…) que condicionarían, habitualmente, deficiencias hipofisarias múltiples(4).
La manifestación clínica más característica de la deficiencia de GH es el fracaso de crecimiento, que se acompaña de una marcada disminución de la VC y de retraso de la EO. La secreción espontánea de GH y/o la respuesta de GH a los diferentes test de estimulación están disminuidas, al igual que los niveles séricos de IGF-1 e IGFBP-3. En las formas congénitas o en las adquiridas de inicio muy precoz, el hipocrecimiento suele acompañarse de un fenotipo característico: cara de “muñeca”, voz aguda, incremento periabdominal de la grasa, manos y pies pequeños y disminución de la masa muscular. El déficit congénito de GH se asocia, frecuentemente, a complicaciones perinatales (sufrimiento fetal, presentación podálica, fórceps, hipoglucemia e hiperbilirrubinemia conjugada), así como a un pene pequeño en los varones (frecuente deficiencia asociada de gonadotropinas). En las formas adquiridas de inicio tardío, el fracaso de crecimiento puede ser la única manifestación clínica.
Insensibilidad a la GH. Se definiría como la ausencia de una apropiada respuesta metabólica y de crecimiento a la GH endógena o a la GH administrada a dosis fisiológica de sustitución. La insensibilidad adquirida a la GH es una situación clínica frecuente; ya que, se asocia a patologías crónicas y especialmente a la malnutrición calórico-proteica. Por el contrario, la formas de insensibilidad congénita a la GH por anomalías en el receptor de GH (RGH), salvo en determinadas poblaciones con alto grado de consanguinidad, son extraordinariamente infrecuentes(4). En la mayoría de los casos, se trata de mutaciones en el gen del RGH (GHR), de herencia autosómica recesiva, que dan lugar a una insensibilidad total a la acción de la GH con hipocrecimiento grave y fenotipo característico (síndrome de Laron), que es similar en muchos aspectos al de la deficiencia completa de GH. Los niveles séricos de GH son normales o elevados y disminuidos los de IGF-1 e IGFBP-3.
Se han descrito, también, formas congénitas de insensibilidad parcial a la GH, debidas a mutaciones en heterocigosis en el GHR, que dan lugar a formas de hipocrecimiento menos graves. Así mismo, se han descrito también situaciones excepcionales de insensibilidad total o parcial a la GH por alteración en los mecanismos post-receptor encargados de la transmisión del mensaje de GH (mutaciones en STAT-5b), así como por deficiencia de ALS (mutaciones en el gen de ALS), deficiencia de IGF-I (mutaciones en el gen de IGF-I) o resistencia a IGF-I (mutaciones en el receptor de IGF-I). La afectación del crecimiento en estos casos puede ser variable, con hipocrecimientos, en ocasiones, dentro del rango bajo de la normalidad y que pueden ser confundidos con VNTB.
Hipotiroidismo. Representa menos de un 1% del total de hipocrecimientos, gracias a la aplicación generalizada del screening neonatal, al mejor control en las áreas de bocio endémico y a la mejoría, en general, en el diagnóstico y tratamiento de los hipotiroidismos adquiridos (tiroiditis linfocitaria crónica, lo más frecuente). El hipocrecimiento, el sobrepeso y el retraso en la EO y en el inicio de la pubertad son hallazgos habituales en las situaciones de hipotiroidismo prolongado.
Exceso de esteroides sexuales. El incremento de esteroides sexuales durante la infancia puede obedecer a numerosas causas y puede resultar de una activación precoz, idiopática u orgánica, del eje hipotálamo-hipófiso-gonadal (pubertad precoz verdadera) o puede producirse independientemente de la secreción de gonadotropinas hipofisarias (pseudopubertad precoz o pubertad precoz periférica). La pubertad y la pseudopubertad precoces son una forma especial de hipocrecimiento; ya que, el exceso de esteroides sexuales durante la fase prepuberal condiciona un hipercrecimiento transitorio, por aceleración anormal de la VC y de la EO, con cierre precoz de los cartílagos de crecimiento y talla final baja.
Hipercortisolismo. El hipocrecimiento en situaciones de hipercortisolismo crónico (síndrome de Cushing) es un fenómeno prácticamente constante y suele ser, junto con la obesidad, su manifestación clínica más precoz. El hipercortisolismo puede ser secundario a: 1) patología hipofisaria (adenoma secretor de ACTH; enfermedad de Cushing); 2) patología suprarrenal (hipercortisolismo ACTH independiente: tumor suprarrenal, hiperplasia suprarrenal macro o micronodular…); o 3) administración exógena y mantenida de glucocorticoides. Salvo en este último caso, el hipercortisolismo es una causa excepcional de hipocrecimiento en la infancia. Los tumores adrenales suelen producir, además de cortisol, cantidades excesivas de andrógenos, lo que puede enmascarar el hipocrecimiento asociado a la hipercortisolemia. Los mecanismos fisiopatológicos que median la alteración del crecimiento en el hipercortisolismo son múltiples, entre otros: la alteración de la secreción-acción de la GH y el trastorno de la osificación y síntesis de colágeno en la placa de crecimiento. La gravedad del hipocrecimiento depende, entre otros factores, de la dosis, duración, vía, tipo de glucocorticoide y sensibilidad individual del paciente; además, puede no recuperarse completamente al cesar su administración y comprometer definitivamente la talla adulta. El efecto negativo sobre el crecimiento es mayor con corticoides de acción prolongada, como la dexametasona, y con la administración diaria frente a la administración a días alternos. Los corticoides inhalados, utilizados con frecuencia en el tratamiento crónico del asma, salvo dosis elevadas y mantenidas o especial sensibilidad del sujeto, suelen tener poca o nula repercusión sobre el crecimiento.
Pseudohipoparatiroidismo (PHP). Representan un grupo heterogéneo de enfermedades, extremadamente infrecuentes caracterizadas por la resistencia a la acción de la paratohormona (PTH) en sus órganos diana (hueso y riñón). Desde el punto de vista bioquímico, se caracterizan por hipocalcemia, hiperfosfatemia y niveles supranormales de PTH, pero sin hiperfosfaturia ni aumento de 1-25 (OH)2 vitamina D. Muchos de estos pacientes presentan, además, un fenotipo peculiar, denominado osteodistrofia hereditaria de Albright (OHA), que se caracteriza por: talla baja, obesidad, cara redonda, calcificaciones en tejidos blandos, anomalías óseas (acortamiento de metacarpianos, metatarsianos y falanges…) y, con frecuencia variable, retraso mental leve-moderado.
El patrón hereditario y fenotípico de los PHP es complejo, ya que, el gen implicado (GNAS; 20q13.32), que codifica para la subunidad alfa estimuladora de la proteína G que interviene en la transmisión del mensaje del receptor de PTH y de otros receptores hormonales (TSH, LH, FSH, GHRH…), está sometido a imprinting paterno; es decir, el alelo procedente del padre no se expresa en condiciones normales en: hipófisis, tiroides, gónadas y túbulo renal. Esta es la causa de que, el fenotipo pueda variar dependiendo de si la causa de la enfermedad es una mutación o una alteración de la impronta genética y de si el gen mutado es de origen materno (OHA con resistencia hormonal) o paterno (OHA sin resistencia hormonal, pseudopseudohipoparatiroidismo). La mayoría de los pacientes presentan mutaciones inactivantes en heterocigosis (herencia autosómica dominante) y pueden presentar resistencia, además de a la PTH, a otras hormonas, especialmente a la TSH.
Hipocrecimiento psicosocial
Se define el hipocrecimiento de causa psicosocial como: “un síndrome de talla baja y/o retraso puberal que se produce en niños y adolescentes en situaciones de hostigamiento psicológico o deprivación afectiva y para el que no se encuentra otra explicación”. Los mecanismos fisiopatológicos que median esta forma de hipocrecimiento son desconocidos, aunque en algunos casos se han implicado alteraciones en el eje de la GH-IGFs. Su diagnóstico es difícil y requiere un alto índice de sospecha.
Hipocrecimientos de causa desconocida (talla baja idiopática)
El concepto de TBI agruparía situaciones normales y patológicas de hipocrecimiento armónico de inicio postnatal, cuyo único denominador común es nuestra incapacidad para alcanzar un diagnóstico etiopatogénico. Se estima que, aproximadamente, el 80% de los niños que consultan por talla baja podrían ser diagnosticados de TBI.
La definición de TBI es el resultado del consenso entre expertos de las sociedades Americana y Europea de Endocrinología Pediátrica, así como de la Growth Hormone Research Society, reunidos en Santa Mónica (California) en octubre de 2007(15). En esta reunión, se definió la TBI como: una condición en la que la talla de un individuo se encuentra más de 2 SDS por debajo de media para su edad, sexo y grupo de población, sin evidencia de anomalías sistémicas, endocrinas, nutricionales o cromosómicas. Esta definición, según establece el propio consenso, incluye a los niños con VNTB y excluye, específicamente, niños con: peso y/o talla baja para su EG (RNPEG), fenotipo dismórfico o disarmónico (DO, síndromes de Turner, de Noonan…), trastorno psiquiátrico o emocional grave u otras causas claramente identificables de talla baja (por ejemplo: enfermedad celíaca, enfermedad inflamatoria intestinal, malnutrición, deficiencia o insensibilidad a la GH, hipotiroidismo, síndrome de Cushing, etc.).
Las VNTB serían los hipocrecimientos armónicos de inicio postnatal que resultarían de la variabilidad normal tanto de la talla como del ritmo madurativo que existe en la especie humana(1). Nuestro desconocimiento de los mecanismos fisiológicos que subyacen al control genético del crecimiento y del ritmo madurativo, así como nuestra incapacidad para predecir con fiabilidad la talla adulta de un niño, han condicionado su inclusión en el grupo de TBI. Dentro de las VNTB se incluyen: la talla baja familiar (TBF), el retraso constitucional del crecimiento y de la pubertad (RCCP) y la frecuente asociación de ambos patrones de crecimiento (Tabla IV).
El término de TBF hace referencia a un grupo de individuos con talla baja, por otro lado sanos, que maduran a un ritmo normal y cuyos familiares más próximos son de talla baja. Por su parte, los pacientes con RCCP serían sujetos sanos que, como consecuencia de un ritmo de maduración más lento que la media de la población (alrededor del 60% tienen antecedentes familiares de maduración tardía), presentan durante la infancia: talla baja, inadecuada para su contexto familiar, retraso de la EO e inicio puberal tardío (2-3 años después que la media), alcanzando la talla adulta a una edad superior a la media de la población. En ambas situaciones, la talla final es acorde con el contexto familiar.
El concepto de TBI es controvertido, artificial y heterogéneo; ya que, incluye situaciones normales y patológicas, cuyo único denominador común es nuestra incapacidad para alcanzar un diagnóstico etiopatogénico. Se estima que, aproximadamente, el 80% de los niños que consultan por talla baja podrían ser diagnosticados de TBI. La inmensa mayoría de estos niños (80-85%) corresponderían a VNTB y un pequeño porcentaje (15-20%) a patologías en las que, por desconocimiento o dificultad diagnóstica, no se llega a alcanzar un diagnóstico, como sería el caso de: hipocrecimientos nutricionales, hipocrecimientos psicosociales, alteraciones infrecuentes o menores en el eje GH-IGFs, así como osteocondrodisplasias, cuadros sindrómicos o alteraciones genéticas (mutaciones, microdeleciones, duplicaciones, disomías uniparentales…) de escasa expresividad clínica, entre otras posibles causas. Por consiguiente, a medida que nuestros conocimientos y métodos de diagnóstico, sobre todo moleculares, mejoren y puedan aplicarse en estos pacientes, muchos de estos niños diagnosticados de TBI deberán ser reclasificados a grupos de patología conocida.
Orientación diagnóstica y pruebas complementarias
La evaluación inicial de todo paciente que consulta por hipocrecimiento incluirá una historia clínica exhaustiva y un examen clínico completo (Tabla V y Algoritmo diagnóstico)(16), al que debe añadirse una valoración auxológica básica(8,9), la determinación de la maduración ósea (EO)(9) y, si es posible, el análisis del patrón de crecimiento a partir de los datos aportados por los padres o acumulados en la historia del niño (Fig. 7). Los datos obtenidos de esta evaluación inicial nos permitirán, al menos, determinar si se trata de un hipocrecimiento armónico o disarmónico y si es de inicio prenatal o postnatal, y así orientar el diagnóstico y las pruebas complementarias.
Figura 7. Patrones clínicos básicos de hipocrecimiento. Patrón de hipocrecimiento intrínseco: se observa en aquellas situaciones en las que existe una limitación en el crecimiento inherente a los propios tejidos, especialmente el esquelético, en la mayoría de los casos de base genética o congénita, lo que va a condicionar una talla final baja. Patrón de crecimiento retrasado: se traduce en un retraso puberal con prolongación del periodo de crecimiento y talla final, en la mayoría de los casos, normal. Patrón de crecimiento atenuado: se caracteriza por una velocidad de crecimiento disminuida de forma mantenida en el tiempo, que condiciona un alejamiento progresivo de la talla de los percentiles normales y una talla final baja. EC: edad cronológica; EO: edad ósea; ET: edad talla (edad para la que la talla del sujeto estaría en el percentil 50 de la población para su edad y sexo).
La EO es uno de los parámetros más sencillos e importantes en la valoración del crecimiento de un niño. No solo se utiliza en el cálculo de la PTA, sino que puede orientar a determinadas patologías (Fig. 7). Está habitualmente retrasada en los trastornos de crecimiento secundarios (patologías crónicas, endocrinopatías…) y en muchos de los niños con TBI; más aún, la ausencia de retraso en la EO, prácticamente, excluye una situación de deficiencia de GH. Por el contrario, en la mayoría de los trastornos primarios o intrínsecos del crecimiento (síndromes dismórficos, osteocondrodisplasias…), el retraso de la EO es menor o inexistente. Un cuidadoso análisis de la radiografía de mano puede, además, sugerir la existencia de una DO no diagnósticada (braquidactilias, haploinsuficiencia del SHOX, pseudohipoparatiroidismo…), en cuyo caso, al igual que ocurre cuando el hipocrecimiento es disarmónico, debería realizarse un estudio radiológico del resto del esqueleto.
Si el hipocrecimiento es armónico y de inicio prenatal
Si el hipocrecimiento es armónico y de inicio prenatal, debe observarse la evolución del niño y, si este no recupera su carril de crecimiento en el primer o segundo año de vida, debería remitirse al especialista; habida cuenta de la escasa posibilidad de recuperación espontánea del crecimiento a partir de esa edad y de la posibilidad de tratamiento con GH(10). Si no existe constancia de patología materna o placentaria que justifique el inicio prenatal del hipocrecimiento y especialmente si el niño presenta retraso mental o psicomotor, malformaciones mayores o menores, fenotipo peculiar o algún rasgo sindrómico, debe considerarse la posibilidad de que se trate de una cromosomopatía o de un síndrome dismórfico; por lo que, estaría indicada la realización de un cariotipo y la remisión al especialista.
Existe una multitud de cuadros síndrómicos en los que el hipocrecimiento es una de sus principales características, algunos de los más frecuentes se recogen en la tabla III. Muchos de ellos tienen una base genética, pero la mayoría no muestran alteraciones en el cariotipo convencional y su reconocimiento requiere de una gran experiencia por parte del médico que lo observa. Si se sospecha un síndrome de base genética conocida y la metodología está accesible, es recomendable confirmar molecularmente el diagnóstico clínico, lo que permitirá: establecer un diagnóstico de certeza, orientar a los padres sobre la futura evolución del paciente y realizar un adecuado consejo genético.
En caso de que las características clínicas del paciente no orienten hacia un diagnóstico concreto, se puede considerar, en colaboración con el genetista clínico, la posibilidad de realizar otros estudios genéticos más amplios (revisión en Palacios-Verdú y Pérez-Jurado(17)): estudios de MLPA (Multiplex Ligation-dependent Probe Amplification), que permiten analizar variantes del número de copias (CNV) en 40-50 loci simultáneamente (los loci de los síndromes más frecuentes asociados a hipocrecimiento), o lo que se conoce como “estudios de asociación a lo ancho del genoma” o GWAS (genoma-wide association studies). Dentro de estos estudios, los más utilizados en la detección de estas patologías son: los arrays-SNP (SNP: single nucleotide polymorphism), que permiten detectar cientos o miles de SNPs (variaciones de una sola base en el ADN), que son el tipo de polimorfismo más frecuente; y los arrays-CGH (CGH: hibridación genómica comparada) que permiten detectar variaciones en la dosis o número de copias del genoma (microdeleciones, microduplicaciones o disomías uniparentales). Más recientemente, se están incorporando progresivamente a la práctica clínica los llamados estudios de secuenciación de alto rendimiento (NGS: Next-Generation Sequencing). Este tipo de estudios permite la secuenciación del genoma completo, de capturas selectivas (paneles de genes implicados en determinadas patologías), de regiones concretas o de todas las regiones codificantes y reguladoras conocidas de todo el genoma (exoma). La secuenciación del exoma parece la mejor estrategia inicial o, al menos la de mayor eficiencia, ya que, analizando solo un 1-1,5% del genoma, es posible detectar el 80-90% de las mutaciones causantes de enfermedad, con rendimientos diagnósticos que oscilan según los estudios entre un 10 y un 54%. En cualquier caso, la indicación y, más aún, la interpretación de este tipo de estudios no es fácil y debería hacerse en colaboración con el genetista clínico; ya que, cada tipo de estudio presenta sus propias limitaciones diagnósticas y aunque nos señalan genes que podrían estar implicados en una enfermedad, no establecen una relación causa-efecto, lo que debe comprobarse y no siempre es fácil.
Si el hipocrecimiento es armónico y de inicio postnatal
Si la talla no está gravemente afectada, entre -2 y -3 SDS, existen antecedentes familiares de TBF o de RCDP y no existen datos sugerentes de hipocrecimiento patológico (ver Algoritmo diagnóstico), en la mayoría de los casos se tratará de una VNTB. Estos hallazgos, junto con un patrón de crecimiento característico y una predicción de talla adulta acorde con la talla familiar, permitirán establecer un diagnóstico provisional de VNTB. La constatación, a los 6 y 12 meses, de la existencia de una VC normal, prácticamente confirmará el diagnóstico. Si, por el contrario, la VC es patológica, se deberá reconsiderar el diagnóstico y valorar la realización de estudios complementarios o la remisión del paciente al especialista.
Si la afectación de la talla es severa, por debajo de -3 SDS, o existen datos sugerentes de patología (ver Algoritmo diagnóstico), deberán realizarse pruebas complementarias. En muchos de los casos, la valoración inicial nos permitirá establecer un diagnóstico de sospecha y orientar estas pruebas hacia una patología específica (nutricional, gastrointestinal, respiratoria…). Si no existen datos sugerentes de patología específica, será necesario practicar, junto con un seguimiento estrecho de la evolución clínica y auxológica del paciente, una serie de pruebas complementarias que permitan descartar, aquellas enfermedades en las que el hipocrecimiento pueda ser la manifestación inicial o que, por su escasa expresividad clínica, puedan pasar desapercibidas (Tabla VI). Estas pruebas básicas son las propuestas en la mayoría de los protocolos nacionales e internacionales de talla baja idiopática(16), pero pueden ampliarse o completarse, en función de la historia clínica, de la evolución o de los resultados de las pruebas previas, con otros estudios (Tabla VI).
La deficiencia de GH es muy infrecuente y más aún los cuadros clínicos de resistencia congénita a la GH, por lo que los estudios de valoración del eje GH-IGFs, salvo la determinación basal de IGF-1, no estarían incluidos en la valoración inicial de un niño con talla baja. En cualquier caso, IGF-1 carece de la sensibilidad y especificidad suficientes para establecer o descartar una alteración en el eje de la GH; de hecho, alrededor del 25-50% de las TBI presentan niveles séricos de IGF-1 por debajo de -2 SDS y pacientes deficitarios de GH pueden presentar niveles séricos de IGF-1 dentro del rango bajo de la normalidad(18). Pese a ello, la mayoría de los autores está de acuerdo en que si los niveles séricos de IGF-1 son claramente normales (entre ± 1 SDS para la edad y sexo), la EO no está claramente retrasada y la VC es normal, la probabilidad de que exista un trastorno en el eje GH-IGF-1 es muy escasa y no sería necesario realizar más estudios de valoración. Si por el contrario, los niveles de IGF-1 están por debajo de -2 DE para la edad y sexo o por debajo de la media junto con datos clínicos sugerentes de deficiencia de GH, estos deberían llevarse a cabo(18). La realización e interpretación de los test que valoran el eje GH-IGFs es compleja y tampoco existe un acuerdo sobre qué, cuándo y cómo deberían realizarse estos estudios (test de estimulación farmacológica con/sin primación, qué fármacos o estímulos utilizar, estudios de secreción espontánea, test de generación de IGF-I, niveles séricos de ALS, GHBP…). Por ello, su indicación e interpretación solo deberían realizarse por personal experimentado y siempre en un contexto clínico compatible.
Lo mismo podría decirse de los estudios genéticos orientados al diagnóstico de los hipocrecimientos(19). Deberían estar orientados por el especialista y en colaboración con el genetista clínico hacia genes concretos, en función del diagnóstico y los hallazgos clínicos y hormonales: deficiencia aislada de GH con historia familiar positiva (GH1, GHRH…), deficiencia combinada de hormonas hipofisarias (LHX3, LHX4, PROP1, HESX1…), deficiencia primaria de IGF-1 (GHR, STAT5b, IGF-1, IGF1ALS…) o resistencia a IGF-1 (IGF1R…)… En el caso de pacientes con TBI sin otras alteraciones y no sugerentes de ser VNTB, podría estar indicado el estudio inicial de alguno de los genes más frecuentes asociados a TBI, como sería el caso de SHOX (responsable del 5% de las TBI), FGFR3 o NPR2 (gen del receptor del péptido natriurético de tipo C –CNP–), o la realización de estudios más amplios: GWAS (rendimiento diagnóstico del 5-10% en TBI) o NGS (rendimiento diagnóstico del 10-54%)(19-21).
Si el hipocrecimiento es disarmónico, prenatal o postnatal
Si la talla baja se asocia con unas proporciones corporales anormales, debe remitirse al especialista y considerarse como una DO. Un diagnóstico preciso va a depender en gran medida de la experiencia del especialista y del radiólogo; ya que, el estudio radiológico del esqueleto (mapa óseo) es la prueba diagnóstica más importante. A menudo, y dada la aparición tardía de las deformidades y de algunas de las anomalías radiológicas, es necesario repetir el examen a lo largo de la infancia y valorar cuidadosamente la armonía corporal y la presencia de deformidades en los progenitores. El estudio anatomopatológico del cartílago y hueso puede ser de utilidad en algunos casos, aunque rara vez se lleva a cabo. Cuando existe la sospecha clínica de una osteocondrodisplasia de base genética conocida y la metodología está disponible (acondroplasia, hipocondroplasia, mucopolisacaridosis, haploinsuficiencia de SHOX, entre otras), pueden realizarse estudios bioquímicos o moleculares que confirmen el diagnóstico, lo que permitirá un adecuado consejo genético y un diagnóstico prenatal precoz. Cuando no es así, pueden realizarse estudios genéticos más amplios que incluyan paneles con los genes asociados a las DO más frecuentes o estudios más amplios del genoma completo.
Opciones terapéuticas en la talla baja
Orientación general
La talla baja no es una enfermedad, sino un síntoma. El tratamiento, en la mayoría de los casos (VNTB), consistirá en aportar una adecuada información al niño y a sus padres de las causas y las expectativas de crecimiento y realizar un seguimiento clínico y auxológico. En otros casos, consistirá únicamente en el tratamiento de la enfermedad responsable. Por último, en un pequeño número de pacientes, puede ser necesaria la utilización de tratamientos específicos para estimular o mejorar el crecimiento.
En la práctica clínica, disponemos de un número limitado de terapias capaces de influir beneficiosamente sobre el crecimiento, como son: la GH y el IGF-1 recombinantes, los fármacos moduladores de la pubertad y el alargamiento óseo.
Tratamiento con GH
La GH estimula el crecimiento longitudinal de los huesos largos de manera prácticamente dosis-dependiente y es el tratamiento específico del déficit de GH. Además, desde que la ingeniería genética permitió la biosíntesis de GH en la década de los 80, con su consiguiente disponibilidad solo limitada por su precio y potenciales efectos secundarios, se ha utilizado experimentalmente en la mayoría de las formas de hipocrecimiento (TBI, displasias esqueléticas, síndromes dismórficos, hipercortisolismos, fibrosis quística, PHP…)(22), con resultados, en el mejor de los casos discretos (mejorías medias de 1-1,5 cm/año de tratamiento en la talla adulta). En la actualidad, las indicaciones aceptadas para el tratamiento con GH en España y en Europa, además de la deficiencia de GH en niños y adultos, son: el síndrome de Turner, el hipocrecimiento asociado a insuficiencia renal crónica, la falta de recuperación de la talla en los RNPEG, el síndrome de Prader Willi y la haploinsuficiencia del gen SHOX. La GH se administra por vía subcutánea, diaria, habitualmente antes de acostarse, en una dosis única de 0,025-0,035 mg/kg/día, en los pacientes deficitarios, y de 0,045-0,05 mg/kg/día, en el resto de situaciones no deficitarias. No obstante, las pautas idóneas de tratamiento, en función del diagnóstico, la respuesta terapéutica y el grado de desarrollo puberal, entre otras variables, no han sido plenamente establecidas.
Los riesgos conocidos del tratamiento con GH en los pacientes deficitarios son escasos, los más frecuentes: epifisiolisis de la cabeza femoral y pseudotumor cerebri (hipertensión intracraneal benigna), con una frecuencia aproximada, en ambos casos, de 1:1000 niños tratados. A dosis más altas y mantenidas, puede haber disminución de la sensibilidad a la insulina, desarrollo de rasgos acromegaloides y elevación suprafisiológica de los niveles séricos de IGF-1 de repercusión incierta. En cualquier caso, la experiencia a largo plazo en pacientes no deficitarios y tratados con dosis altas de GH es escasa y sus potenciales riesgos, en gran medida, desconocidos. Esta incertidumbre debería hacer extremar la prudencia sobre su uso indiscriminado en patologías en las que sus hipotéticos beneficios no hayan sido suficientemente probados.
Tratamiento con IGF-1
La utilización de IGF-1 recombinante fue aprobada por la Agencia Europea del Medicamento (AEM) en 2008 para su utilización en los hipocrecimientos por deficiencia primaria grave de IGF-I (anomalías en el receptor de GH, en sus vías de señalización intracelular o mutaciones en el gen de IGF-1, entre otras posibles causas). La dosis recomendada es de 0,04-0,08 mg/kg/día (máximo: 0,12 mg/kg/día), repartida en dos dosis y administrada, cada 12 horas, por vía subcutánea, preferentemente antes de una comida para prevenir sus efectos hipoglucemiantes.
La experiencia clínica en la utilización del IGF-1 recombinante es relativamente escasa y prácticamente limitada al tratamiento de pacientes con insensibilidad congénita a la GH (síndrome de Laron). Los estudios a corto y medio plazo demuestran en ellos la eficacia del tratamiento, aunque sus resultados son menores que los obtenidos con la GH en los pacientes deficitarios. Los efectos secundarios más frecuentes serían: hipoglucemias, aumento del tejido linfático (amígdalas, adenoides, bazo y timo), náuseas, vómitos, cefalea, papiledema (pseudotumor cerebri), prurito y aumento de transaminasas(23).
Recientemente, se ha publicado el primer estudio sobre eficacia y seguridad del tratamiento combinado con GH e IGF-1, llevado a cabo en pacientes con TBI y niveles séricos disminuidos de IGF-1(24). Los resultados del estudio indican una discreta mejoría en el crecimiento respecto a los pacientes tratados solo con GH, que no justificaría, al menos de forma generalizada, la utilización combinada de GH e IGF-1.
Tratamiento con moduladores de la pubertad
Los beneficios de la utilización de fármacos moduladores de la pubertad en el tratamiento de la talla baja no están claramente demostrados(25). Los fármacos más utilizados han sido los análogos de GnRH (aGnRH) y más recientemente los inhibidores de 3ª generación de la aromatasa (IA: anastrozole y letrozole), la enzima que cataliza, en condiciones normales, el paso de andrógenos a estrógenos. Los estudios disponibles indican que, los aGnRH administrados aisladamente en pacientes con talla baja y pubertad normal o adelantada, pese frenar el desarrollo puberal y prolongar el periodo de crecimiento, no son útiles para mejorar la talla adulta, y que asociados con GH conducirían, en el mejor de los casos, a un beneficio modesto en la talla adulta, cuando el tratamiento combinado se mantiene durante, al menos, 3 años. En el caso de los IA, su objetivo sería enlentecer el cierre de las placas de crecimiento (mediado principalmente por los estrógenos) y prolongar el crecimiento lineal. Aunque los estudios iniciales, en varones con RCCP y TBI, eran muy prometedores y sugerían beneficios en la talla adulta de alrededor de 5 cm tras 1-2 años de tratamiento, los resultados disponibles a talla final, aunque todavía insuficientes para poder establecer conclusiones definitivas, no sostienen estos potenciales beneficios y sí posibles efectos secundarios, entre ellos: marcada elevación de los niveles séricos de testosterona, de repercusión incierta, desarrollo de anomalías vertebrales, disminución del colesterol HDL y aumento del hematocrito(26).
Tratamiento quirúrgico de la talla baja
Se basa en la realización de alargamientos óseos, habitualmente en tibias, fémures y húmeros. Su objetivo no es solo obtener una talla más alta, sino también mantener o mejorar la proporcionalidad de los segmentos corporales y, en casos concretos, conseguir, mejorías funcionales. Su indicación más habitual, generalmente a partir de los 9-12 años, son las DO, especialmente aquellas con huesos sólidos y afectación preferente de extremidades, como la acondroplasia. En las tallas bajas no displásicas, la indicación de la elongación ósea es más controvertida y suele realizarse en hipocrecimientos severos (por debajo de -3 SDS), una vez finalizado el crecimiento, cuando otros tratamientos han fracasado en la consecución de una talla “aceptable”. Antes de aconsejar este tipo de terapia, es importante informar al paciente y a sus padres de que las grandes elongaciones (30-35 cm en extremidades inferiores, 10-12 cm en las superiores) conllevan procesos de larga duración, dolorosos, en los que las incidencias y complicaciones (infecciosas, cicatriciales, óseas, musculotendinosas, vasculares y nerviosas) son relativamente frecuentes y, en ocasiones, graves, con resultados no siempre satisfactorios. Por ello, el paciente debe estar muy motivado y solo deberían ser llevadas a cabo por unidades muy experimentadas.
Tratamiento específico de las distintas formas de talla baja
Retrasos de crecimiento intrauterino
El 80-90% de los hipocrecimientos prenatales alcanzan una talla en los 2-4 primeros años de vida dentro de la normalidad y no requieren tratamiento. En el 10-20% que no lo hace, estaría indicado el tratamiento con GH, en Europa, a partir de los 4 años de edad, ya que, no solo mejora la talla final de muchos de estos pacientes, sino que parece ejercer también efectos positivos sobre la composición corporal, la tensión arterial y el metabolismo lipídico(10).
Cuadros sindrómicos y cromosomopatías
El hipocrecimiento asociado a los cuadros sindrómicos y cromosomopatías carece en general de tratamiento específico. En Europa, solo el síndrome de Turner (1,4 mg/m2/día) y el síndrome de Prader-Willi (1 mg/m2/día, sin sobrepasar los 2,7 mg/día) son indicaciones aceptadas para el empleo de la GH. En EE.UU., en 2007, la FDA (Food and Drug Administration) aprobó, también, la utilización de la GH en el síndrome de Noonan. Los resultados disponibles en síndrome de Noonan(27), aunque todavía insuficientes, indican una respuesta positiva, pero variable, entre los diferentes pacientes, con mejorías en la talla final que oscilan entre 0,5-1,4 SDS, sin aparentes repercusiones cardiacas o metabólicas. Tampoco parece que el tratamiento con GH influya sobre el potencial riesgo tumoral que presentan estos pacientes (mayor incidencia de leucemias y de ciertos tumores sólidos), aunque el seguimiento es todavía insuficiente para poder establecer conclusiones definitivas.
Osteocondrodisplasias
El tratamiento de la mayoría de las osteocondrodisplasias es todavía sintomático y ortopédico. Si el hipocrecimiento se produce a expensas del acortamiento de las extremidades inferiores y la calidad del hueso lo permite, el alargamiento óseo puede ser una alternativa. Aunque se ha utilizado la GH de forma experimental en diferentes displasias óseas, con escasos resultados, en Europa, solo en los hipocrecimientos por haploinsuficiencia del SHOX está aceptada la utilización de la GH (0,045-0,050 mg/kg/día). La experiencia a talla final en estos pacientes es todavía escasa, aunque los resultados preliminares sugieren una eficacia a largo plazo similar a la obtenida en las niñas con síndrome de Turner(28). Un ensayo clínico de tratamiento con análogo subcutáneo de CNP (péptido natriurético de tipo C) en pacientes con acondroplasia está en marcha y parece abrir la posibilidad de nuevas vías para el tratamiento de las DO(21).
Hipocrecimientos secundarios a enfermedades crónicas
Cuando el hipocrecimiento es el resultado de una enfermedad crónica (insuficiencia renal, fibrosis quística, malabsorción…), los esfuerzos terapéuticos deben dirigirse a mejorar la nutrición y, si es posible, a curar la enfermedad de base. La sensibilidad creciente respecto a las secuelas que sobre el crecimiento tienen estas enfermedades ha conducido a la modificación de muchos de los protocolos de tratamiento, al objeto de minimizar dichas secuelas e, incluso, a que se instauren terapias específicas encaminadas a mejorar el pronóstico de talla de estos pacientes, como es el caso, en algunas de ellas, de la administración de GH: insuficiencia renal crónica (IRC), enfermedad inflamatoria intestinal, corticoterapia crónica, artritis reumatoide y trasplantes hepático y cardíaco, entre otros. Salvo en el caso de la IRC, donde la indicación de GH ha sido aceptada, la utilización de la GH en el resto de situaciones continúa siendo experimental.
Hipocrecimientos secundarios a patología endocrinológica
La mayoría de los hipocrecimientos secundarios a patología endocrinológica tienen un tratamiento específico: GH en la deficiencia de GH, IGF-1 en la de insensibilidad congénita a la GH, levotiroxina sódica en los hipotiroidismos, hidrocortisona en la hiperplasia suprarrenal congénita, aGnRH en la pubertad precoz central, etc. El tratamiento del hipercortisolismo crónico requiere la supresión de la fuente de cortisol, habitualmente mediante la extirpación del tumor productor de ACTH (adenoma hipofisario) o de la suprarrenal (suprarrenaloma) o suprarrenales responsables de la hipercortisolemia. En aquellos casos en que el hipercortisolismo es iatrogénico, se debe intentar administrar los corticoides a días alternos y reducir, en la medida de lo posible, tanto la duración como la dosis.
Hipocrecimiento psicosocial
El tratamiento del hipocrecimiento de causa psicosocial es, al igual que su diagnóstico, complejo y difícil. En algunos casos, será suficiente con mejorar el aporte nutricional y modificar las actitudes familiares para conseguir un adecuado crecimiento de recuperación, pero, en la mayoría de los casos, solo un adecuado tratamiento psicológico y la separación del niño del ambiente familiar, no siempre posible, permitirá una normalización del crecimiento(14).
Talla baja idiopática
Las VNTB englobadas dentro del concepto de TBI no suelen requerir ningún tipo de tratamiento, salvo el apoyo psicológico y el aporte de una adecuada información a los padres y al paciente sobre la normalidad del cuadro clínico, su previsible patrón de crecimiento y las expectativas de talla adulta. En algunos pacientes con RCCP, el retraso en el crecimiento y, sobre todo, la aparición tardía de los caracteres sexuales secundarios puede determinar una mala adaptación psicosocial y baja autoestima. En estos casos, puede estar indicada la utilización durante un corto periodo de tiempo de esteroides sexuales a dosis bajas.
En el año 2003, la FDA norteamericana y posteriormente otros países han aprobado el uso de la GH (0,035-0,050 mg/kg/día) en pacientes con TBI(15,29). Pocas veces, una indicación de tratamiento ha generado y sigue generando, tanta polémica y tanto papel gastado en consideraciones clínicas, éticas, económicas y de toda índole. En resumen, los dos principales argumentos para esta aprobación fueron: 1) que la talla baja sería responsable de problemas psicosociales tanto en la infancia como en la edad adulta que condicionarían un menor estatus social y una menor calidad de vida; y 2) que desde 1993, se han ido aprobando indicaciones para la GH en situaciones no deficitarias basándose solo en la talla baja y su repercusión psicológica. Por consiguiente, la etiología de la talla baja no debería ser moralmente relevante en la decisión de quién debe o no ser tratado con GH; ya que, el objetivo del tratamiento sería corregir las consecuencias psicosociales negativas de la talla baja.
En España y en el resto de Europa la situación es distinta, y aunque multitud de tratamientos en esta indicación se están realizando off-label, la indicación de GH en la TBI no ha sido todavía aceptada por la AEM. En primer lugar, porque los estudios más recientes indican que la talla baja, aunque puede conllevar alguna situación de estrés emocional, no se asocia a problemas psicopatológicos, ni a menor estatus social, ni a menor calidad de vida. En segundo lugar, porque la relación coste-beneficio es mala: elevado coste económico (6.000-12.000 €/año de tratamiento) con discretos efectos beneficiosos sobre la talla final (1-1,5 cm/año de tratamiento). Por último, porque aunque los efectos secundarios a corto-medio plazo son escasos, existe un cierto grado de incertidumbre sobre sus efectos a largo plazo.
Otras opciones terapéuticas, como los IA o la asociación de GH y aGnRH, son todavía objeto de discusión y deberían ser considerados solo en el marco de estudios controlados(25).
Funciones del pediatra de Atención Primaria (AP)
No existe un consenso establecido sobre cuándo el pediatra de Atención Primaria debe iniciar un estudio por talla baja, qué pruebas deber realizar o qué criterios debe emplear para remitir a un paciente a una consulta especializada. Un intento de aproximación a cuál podría ser su papel en esta patología queda reflejado en el algoritmo diagnóstico. En cualquier caso, sería labor del pediatra de Atención Primaria:
• Monitorizar el crecimiento y desarrollo de todos los niños a lo largo de la infancia y adolescencia.
• Realizar los pasos iniciales en la orientación diagnóstica de estos pacientes: historia clínica, exploración, valoración auxológica y pruebas complementarias básicas, estableciendo el diagnóstico, en muchos casos, y decidiendo, en otros, la necesidad de derivación al especialista.
• Realizar el seguimiento de la mayoría de los niños con VNTB, pero también de otras causas de talla baja que no requieran tratamientos especializados, contando siempre con la potencial colaboración del especialista, si lo considera necesario, en función de la evolución o de las circunstancias individuales de cada caso.
• Por último, y no por ello menos importante, tranquilizar e informar a los padres y al niño, transmitiéndoles una información veraz y realista de las expectativas de crecimiento de sus hijos y de las opciones terapéuticas disponibles en cada caso, evitando crear falsas expectativas respecto a la bondad de tratamientos cuyos efectos sobre la talla final son discretos o escasamente probados y cuyos efectos secundarios a largo plazo son inciertos y, en algunos casos, potencialmente graves.
Bibliografía
Los asteriscos reflejan el interés del artículo a juicio del autor.
1.*** Pozo J, Argente J. Hipocrecimiento armónico. En: Moro M, Málaga S, Madero L, ed. Cruz Tratado de Pediatría. (11ª edición). Madrid: Editorial Panamericana, S.A.; 2014. p. 1223-33.
2.** Karlberg J. A biologically-oriented mathematical model (ICP) for human growth. Acta Paediatr Scand. 1989; (Suppl 350): 70-94.
3.** Fowden AL, Forhead AJ. Endocrine regulation of feto-placental growth. Horm Res. 2009; 72: 257-65.
4.** Backeljauw PF, Dattani MT, Cohen P, Rosenfeld RG. Disorders of Growth Hormone/Insulin-Like Growth Factor Secretion and Action. En: Sperling MA, ed. Pediatric Endocrinology (fourth edition). Philadelphia: Elsevier Saunders; 2014. p. 292-404.
5.*** Juul A. Serum levels of insulin-like growth factor I and its binding proteins in health and disease. Growth Horm IGF Res. 2003; 13: 113-70.
6.** Boersma B, Wit JM. Catch up growth. Endo Rev. 1997; 18: 646-61.
7.** Barker DJP. Maternal nutrition, fetal nutrition, and disease in later life. Nutrition. 1997; 13: 807-13.
8.** Pozo J. Valoración auxológica del crecimiento I. Pediatr Integral. 2011; XV: 590-8.
9.** Pozo J. Valoración auxológica del crecimiento II. Pediatr Integral. 2011; XV: 691-701.
10.*** Clayton PE, Cianfarani S, Czernichow P, Johannsson G, Rapaport R, Rogol A. Consensus Statement: Management of the Child Born Small for Gestational Age through to Adulthood: A Consensus Statement of the International Societies of Pediatric Endocrinology and the Growth Hormone Research Society. J Clin Endocrinol Metab. 2007; 92: 804-10.
11.** Warman ML, Cormier-Daire V, Hall C, et al. Nosology and classification of genetic skeletal disorders: 2010 revision. Am J Med Genet Part A. 2011; 155: 943-68.
12.** Binder G. Short stature due to SHOX deficiency: genotype, phenotype, and therapy. Horm Res Paediatr. 2011; 75: 81-9.
13.** Lifshitz F. Nutrition and growth. J Clin Res Ped Endo. 2009; 1: 157-63.
14.** Pozo J, Argente J. Retraso de crecimiento de causa psicosocial En: Pombo M y cols., ed. Tratado de Endocrinología Pediátrica (4ª edición). Madrid: McGraw-Hill/Interamericana S.A.; 2009; p. 199-203.
15.*** Cohen P, Rogol AD, Deal CL, et al. Consensus statement on the diagnosis and treatment of children with idiopathic short stature: a summary of the Growth Hormone Research Society, the Lawson Wilkins Pediatric Endocrine Society, and the European Society for Paediatric Endocrinology Workshop. J Clin Endocrinol Metab. 2008; 93: 4210-17.
16.** Oostdijk W, Grote FK, de Muinck Keizer-Schrama SM, Wit JM. Diagnostic approach in children with short stature. Horm Res. 2009; 72: 206-17.
17.*** Palacios-Verdú MG, Pérez-Jurado LA. Nuevas metodologías en el estudio de enfermedades genéticas y sus indicaciones. Pediatr Integral. 2014; XVIII: 515-28.
18.*** Wit JM, Clayton PE, Rogol AD, Savage MO, Saenger PH, Cohen P. Idiopathic short stature: definition, epidemiology, and diagnostic evaluation. Growth Horm IGF Res. 2008; 18: 89-110.
19.** Dauber A, Rosenfeld RG, Hirschhorn JN. Genetic evaluation of short stature. J Clin Endocrinol Metab. 2014; 99: 3080-92.
20.** Guo MH, Shen Y, Walvoord EC, et al. Whole exome sequencing to identify genetic causes of short stature. Horm Res Paediatr. 2014; 82: 44-52.
21.** Vasques GA, Arnhold IJ, Jorge AA. Role of the natriuretic peptide system in normal growth and growth disorders. Horm Res Paediatr. 2014; 82: 222-9.
22.** Pozo J, Argente J. La hormona de crecimiento (GH) en Pediatría. Rev Horm Crecim. 2007; X: 108-32.
23.** Bang P, Polak M, Woelfle J, Houchard A. Effectiveness and Safety of rhIGF-1 Therapy in Children: The European Increlex® Growth Forum Database Experience. Horm Res Paediatr. 2015; 83: 345-57.
24.** Backeljauw PF, Miller BS, Dutailly P, et al. Recombinant human growth hormone plus recombinant human insulin-like growth factor-1 coadministration therapy in short children with low insulin-like growth factor-1 and growth hormone sufficiency: results from a randomized, multicenter, open-label, parallel-group, active treatment-controlled trial. Horm Res Paediatr. 2015; 83: 268-79.
25.** Dunkel L. Treatment of Idiopathic Short Stature: Effects of Gonadotropin-Releasing Hormone Analogs, Aromatase Inhibitors and Anabolic Steroids. Horm Res Paediatr. 2011; 76 (suppl 3): 27-9.
26.** Shams K, Cameo T, Fennoy I, et al. Outcome analysis of aromatase inhibitor therapy to increase adult height in males with predicted short adult stature and/or rapid pubertal progress: a retrospective chart review. J Pediatr Endocrinol Metab. 2014; 27: 725-30.
27.** Giacomozzi C, Deodati A, Shaikh MG, Ahmed SF, Cianfarani S. The impact of growth hormone therapy on adult height in Noonan syndrome: a systematic review. Horm Res Paediatr. 2015; 83: 167-76.
28.** Blum WF1, Ross JL, Zimmermann AG, et al. GH treatment to final height produces similar height gains in patients with SHOX deficiency and Turner syndrome: results of a multicenter trial. J Clin Endocrinol Metab. 2013; 98: E1383-92.
29.*** Wit JM, Reiter EO, Ross JL, et al. Idiopathic short stature: Management and growth hormone treatment. Growth Horm IGF Res. 2008; 18: 111-35.
Bibliografía recomendada
- Cruz Tratado de Pediatría. (11ª edición). Madrid: Editorial Panamericana, S.A.; 2014.
La nueva edición (11ª) del “Cruz Tratado de Pediatría”, libro de referencia de la Pediatría española revisa y actualiza, en diferentes capítulos a lo largo de la obra, el crecimiento normal, su valoración y, por supuesto, las alteraciones del crecimiento.
- Wit JM, Clayton PE, Rogol AD, Savage MO, Saenger PH, Cohen P. Idiopathic short stature: Definition, epidemiology, and diagnostic evaluation. Growth Horm IGF Res. 2008; 18: 89-110.
- Wit JM, Reiter EO, Ross JL, et al. Idiopathic short stature: Management and growth hormone treatment. Growth Horm IGF Res. 2008; 18: 111-35.
Estos dos trabajos recogen las reflexiones de expertos de reconocido prestigio internacional, norteamericanos y europeos, reunidos en el año 2007, en Santa Mónica (California), para analizar los diferentes aspectos (conceptuales, diagnósticos y terapéuticos) de la talla baja idiopática (TBI), o lo que es lo mismo, del 80% de los hipocrecimientos. Fueron la base del consenso internacional sobre el diagnóstico y tratamiento de la TBI publicado posteriormente, en el año 2008 (referencia 15 de la Bibliografía). Son dos amplias revisiones que analizan en profundidad todos los aspectos de la TBI y, por ende, de la talla baja en general. Su lectura detenida es muy recomendable para todos aquellos que quieran profundizar en este tema tan controvertido.
- Palacios-Verdú MG, Pérez-Jurado LA. Nuevas metodologías en el estudio de enfermedades genéticas y sus indicaciones. Pediatr Integral. 2014; XVIII: 515-28.
Si algo está cambiando y a pasos muy rápidos en el estudio de los hipocrecimientos, cuadros dismórficos y, en general, en toda la Pediatría, es el desarrollo de nuevas tecnologías capaces de estudiar casi toda la información genética de un individuo. Este trabajo, recientemente publicado en Pediatría Integral describe con sencillez, poco habitual, la batería de recursos tecnológicos disponibles, así como sus indicaciones, limitaciones y utilidad en el estudio de las enfermedades con base genética.
| Caso clínico |
|
Motivo de consulta Varón de 10 años y 2 meses que consulta por talla baja desde siempre. Refiere la madre que ya nació pequeño y que no se ha recuperado. Los datos de su pediatra muestran que ha mantenido un canal de crecimiento paralelo, pero por debajo del P3, alejado del canal de crecimiento que correspondería a su talla diana (170,5 ± 5 cm; P10-25). Antecedentes familiares Madre: hipertensión arterial. G.A.V.: 1/0/1. Menarquia: 13 años. Talla: 153,9 cm. Padre: estenosis mitral por fiebre reumática. Talla: 173 cm. Desconoce la edad de desarrollo puberal. No consanguinidad ni otros antecedentes familiares de interés. Antecedentes personales Embarazo con hipertensión arterial. Parto a las 37 + 3 semanas de gestación (EG), cesárea por fracaso de la inducción. Periodo neonatal: Apgar 7/8. PRN: 2.335 g (-1,59 SDS para EG). LRN: 43 cm (-3,3 SDS para EG). Estuvo en incubadora por hipoglucemia e irritabilidad neuromuscular con ictericia que precisó fototerapia. Pruebas metabólicas normales. Alimentación: sin alergias ni intolerancias alimenticias. Desarrollo psicomotor: normal, aunque refieren mal rendimiento escolar que ha requerido adaptación curricular y apoyos en el colegio. Ha tenido problemas psicológicos en relación, al parecer, con separación de los padres y fallecimiento de familiar próximo, por lo que se encuentra en seguimiento por un psicopedagogo. Enfermedades anteriores: estenosis pulmonar severa (valvuloplastia a los 5 años) y comunicación auricular de tipo ostium secundum (precisó también cierre quirúrgico). Criptorquidia bilateral con respuesta positiva a gonadotropina coriónica. Resto de antecedentes personales: sin interés. Exploración Edad: 10 años y 2 meses. Talla 122,7 (P < 3/-2,63 SDS). Peso 27,1 kg (P10-25). T/A: 112/66 mm Hg. FC: 78 lpm. Buen estado general. Hábito armónico con algún rasgo fenotípico peculiar con: implantación posterior del cabello baja, hendiduras palpebrales antimongoloides, mentón prominente y nevus múltiples. Sin adenias significativas. Cuello: normal, no se palpa bocio. Tórax normal con pectus excavatum leve. Auscultación cardiopulmonar: normal. Abdomen: normal. Genitales externos masculinos normales, en estadio puberal I de Tanner (G1, P1, Aa), con testes en bolsas de 2 mL de volumen. Resto de la exploración normal. Pruebas complementarias iniciales • Hemograma, ferritina, VSG, lipidograma y bioquímica básica: normales. • IgA y Ac antitransglutaminasa: negativos. • Función tiroidea (T4L y TSH): normal. • IGF-1: 162 ng/mL (VN: 81-430); IGFBP3: 3,67 mg/L (VN: 2,47-5,92). • Edad ósea: 10 años para una edad cronológica de 10 años y 10 meses con predicción de talla final de 160 ± 5 cm. • Cariotipo: normal (46, XY). |
 |
| Representación del niño en la pintura española |
J. Fleta Zaragozano
Sociedad Española de Pediatría Extrahospitalaria y Atención Primaria
Facultad de Ciencias de la Salud. Universidad de Zaragoza
Pediatr Integral 2015; XIX (6): 439.e1-439.e3
La obra de Alonso Cano ha sufrido, quizá más que ninguno de sus contemporáneos, pérdidas irreparables a lo largo del tiempo. Incendios, guerras, robos y saqueos, nos han privado de una parte importante de su legado. En la actualidad, su obra se halla dispersa y, en ocasiones, oculta o mal conservada; pocas de la obras se encuentran aún en su ubicación original. Sigue siendo, sin embargo, un legado inmenso que abarca, además de pintura y escultura, obras arquitectónicas de relevancia. Mención aparte merecen sus dibujos, de los que se conserva gran número y que permiten seguir el desarrollo de la carrera de este artista y su gran influencia en los ámbitos en los que ejerció su labor: Sevilla, Madrid y Granada.
Vida y obra
Alonso Cano Almansa (Granada, 1601-1667) fue pintor, escultor y arquitecto. Por su contribución en las tres disciplinas y la influencia de su obra en los lugares donde trabajó, se le considera uno de los más importantes artistas del barroco en España; fue además, el iniciador de la Escuela granadina de pintura y escultura. Su padre, Miguel Cano, era un prestigioso ensamblador de retablos de origen manchego y su madre, María Almansa, podría haber practicado el dibujo. Alonso aprendió sus primeras nociones de dibujo arquitectónico y de imaginería, llegando a colaborar tempranamente en los encargos granadinos de su padre, pues muy pronto sus progenitores comenzaron a descubrir su talento.
En 1614 o 1615, se traslada junto a su familia a la ciudad de Sevilla, donde al poco tiempo entra en el taller de pintura de Francisco Pacheco, el más prestigioso maestro de la ciudad, maestro de Velázquez, de quien fue compañero y mantuvo amistad durante toda su vida. Como escultor se considera tradicionalmente que se formó con Juan Martínez Montañés, aunque no hay constancia documental de ello. De 1624, dos años antes de obtener el título de Maestro Pintor, es su primer cuadro conocido y firmado, un San Francisco de Borja (Museo de Bellas Artes de Sevilla) con la inconfundible huella de Pacheco. En esta época seguiría colaborando con su padre en el diseño y ensamblado de retablos. En 1627 muere, al parecer de parto, su primera esposa, María de Figueroa. Vuelve a casarse en 1631, esta vez con Magdalena de Uceda, sobrina del pintor Juan de Uceda.
En 1638, Cano se trasladó a la capital, donde el valido de Felipe IV, el poderoso conde-duque de Olivares, lo nombró pintor de cámara. Fue también profesor de dibujo del Príncipe Baltasar Carlos. Por su proximidad a la Corte, Cano pudo conocer las colecciones reales, ricas en pintura veneciana del siglo XVI y en obras recientes de su colega Velázquez. Todo esto ayuda a explicar su evolución, del tenebrismo derivado de Caravaggio a un estilo más colorista y de figuras elegantes que, a veces, recuerdan a Van Dyck.
En 1652 marchó a Granada donde obtuvo el cargo de racionero de la catedral, gracias a la influencia de Felipe IV. Allí completó la decoración de la capilla mayor. Sin embargo, tuvo constantes enfrentamientos con los canónigos. Consiguió poco después ser maestro mayor de la catedral, aunque al poco tiempo de este nombramiento, murió. Fue enterrado en la cripta de la catedral de Granada. Tuvo un carácter pendenciero e intervino en duelos. Pese a ganar grandes cantidades de dinero, mantuvo muchas deudas a lo largo de su vida, llegando a pisar la cárcel, aunque su amigo Juan del Castillo pagó sus deudas.
Como pintor, podemos distinguir tres periodos estilísticos en su obra. De su primera etapa sevillana es poco lo que nos ha llegado, la aportación más temprana es el citado San Francisco de Borja y algunas obras menores. Hacia 1635, se observa un importante cambio con obras con un colorido más brillante y una interpretación más lírica de los modelos de Pacheco, como en La Visión de San Juan de 1637 (Londres, Wallace Collection) o la perdida Santa Inés, de la que se conserva sin embargo una buena copia descubierta recientemente. Este avance estilístico de mitad de la década de los 30 hace pensar en una posible visita a la Corte en esa época (no documentada) antes de su marcha definitiva a Madrid en 1638.
De su primera etapa madrileña, algunas pinturas destacadas son: El milagro del pozo, alusivo a San Isidro Labrador (Museo del Prado), y el Retablo del Niño Jesús de la Catedral de Getafe. También son suyas el Cristo atado a la columna y Cristo flagelado por dos verdugos, conservados en el Convento del Santísimo Cristo de la Victoria de Serradilla (Cáceres). Establecido ya de nuevo en Granada, recibe el encargo más importante de su vida, completar la decoración de la capilla mayor de la Catedral de su ciudad natal con siete enormes lienzos con episodios de la vida de la Virgen, que constituyen lo principal de su obra pictórica y uno de los conjuntos más impresionantes de la pintura barroca europea. El dibujo fue fundamental como parte del proceso creativo de Alonso Cano. Ya sus coetáneos destacan su gran habilidad, su extraordinaria inventiva y su exquisita técnica, a lo que se añade la cualidad de saber dibujar cualquier cosa, desde un motivo arquitectónico a una figura.
Los niños en su obra
El Príncipe Baltasar Carlos de caza. La primera llegada de Cano a Madrid se produce en 1634, a instancias de Velázquez, pero no para participar en la decoración del Buen Retiro, como fue el caso de Zurbarán, sino para constituirse como maestro de dibujo del Príncipe Baltasar Carlos, al que pintó en un retrato como cazador, anterior a otro del propio Velázquez, de similares características en la figura, en la pose y en los fondos de la obra, si bien, Velázquez incluyó en su cuadro a dos perros. Se cree que Cano también estaría presente con seguridad en la boda de la hija de Velázquez, ya que Alonso Cano estuvo bastante unido no solo al pintor, sino también a la familia Mazo-Velázquez, apadrinando a dos de sus hijos: Inés y José, este último junto con su segunda esposa, María Magdalena de Uceda. Este cuadro describe al Príncipe Baltasar Carlos de niño (1629-1646) de cuerpo entero, en una escena de caza con escopeta y ataviado a la moda infantil cortesana del siglo XVII y típica de la pintura barroca española. Data de 1635 y pertenece al Museo de Bellas Artes de Budapest, Hungría (Fig. 1).

Figura 1. El Príncipe Baltasar Carlos de caza.
El milagro del pozo. La influencia de los pintores venecianos y de Velázquez en la técnica de Cano se hace evidente en este lienzo. El pintor emplea una gama cromática muy rica y una pincelada suelta y vibrante con la luz difuminada, envolviendo a las figuras como en Tiziano y en Velázquez. Además, las figuras femeninas están dotadas de una sensualidad muy veneciana.
El cuadro fue pintado para el retablo del altar mayor de la desaparecida iglesia de Santa María de la Almudena de Madrid, donde se dice que fue visitado por el propio rey Felipe IV después de oír las múltiples alabanzas que recibía la obra. La pintura recoge un hecho de la vida de San Isidro Labrador, el patrón de Madrid, que aparece en pie con sus herramientas en el suelo. Un hijo del santo cae a un pozo y es salvado por un ángel. En la imagen aparece San Isidro, varios niños y tres mujeres, dispuestos todos ellos en torno al pozo seco, del que nuevamente brota agua. Cuando en 1941 el Museo del Prado adquirió el cuadro, este estaba roto y en mal estado. Había sido recortado por los bordes superior e inferior y repintado de forma poco hábil en muchos puntos (como la cabeza del niño del centro). Con las últimas restauraciones, el cuadro ha recuperado parte de su belleza primitiva. Es un óleo sobre lienzo de 216 por 149 cm. Pintado hacia 1638-1640 y pertenece al Museo del Prado (Fig. 2).

Figura 2.El milagro del pozo.
La Virgen de la leche. Se trata de una pintura de formato vertical que recoge en primer plano a la Virgen sentada en actitud de amamantar al Niño desnudo que sostiene en su regazo. Representa una mujer joven con la cabeza ligeramente inclinada a su derecha, mirando a este. Viste túnica roja sobre camisa blanca y manto azul que le cubre los hombros, las piernas y el brazo derecho sobre el que sostiene al Niño, al que ofrece el pecho derecho, que sujeta con su mano izquierda. En la cabeza, se aprecia un velo transparente que baja hacia su hombro derecho. El Niño aparece semitumbado, sentado sobre la pierna derecha de la Virgen con la espalda apoyada en el brazo del mismo lado, sobre un paño blanco que puede ser la prolongación del velo citado, con la cabeza vuelta mirando hacia el exterior del cuadro. La escena se desarrolla sobre un fondo neutro de colores pardos oscuros. A la altura del asiento, una línea horizontal en el fondo, al lado derecho de las figuras, marca la inflexión entre suelo y pared; delante de ellas, en la parte inferior del cuadro, dos líneas más marcan algo parecido al inicio de un escalón.
Esta obra refleja la atmósfera serena y luminosa de la madurez como artista de Alonso Cano, lejos de su tenebrismo inicial, gracias al equilibrio de las formas, la delicadísima belleza y el fresco colorido, azul luminoso el manto y roja la túnica, que acentúan las delicadas carnaciones en rosas con toques blancos del desnudo del Niño y la cara, manos y pecho de la Virgen. Data de 1659. Es un óleo sobre lienzo de 166 por 109 cm y pertenece al Museo de Guadalajara (Fig. 3).

Figura 3. La Virgen de la leche.
La Virgen con el Niño. En opinión de Urrea, esta deliciosa composición de la que no existen precedentes en la obra del artista granadino, aunque tratase en diversas ocasiones el tema de María sosteniendo en brazos a su Hijo niño, parece derivar de un esquema renacentista cuyo punto de partida podría haberlo tomado Cano de la famosísima pintura de Rafael La Virgen de la Silla, repetidamente divulgada por grabados, alguno de los cuales pudo utilizar el pintor para introducir las variaciones que aporta su propia personalidad.
Por lo que respecta a la figura materna, esta adopta una postura caprichosa, como sorprendida en un giro o media vuelta para mostrar el Niño al espectador, y su expresión se envuelve en la misma serenidad atemporal de otros modelos de Cano; su rostro ovalado concuerda también con esquemas femeninos repetidamente utilizados por Cano, tanto en pintura como en escultura. Además, la manera de mostrar el elegante y prolongado cuello de la Virgen coincide también con distintos ejemplos suyos de belleza femenina. Por lo que respecta a la figura del Niño, se trata de una de las más hermosas pintadas por este maestro, tiene su cálida entonación habitual y responde a su tipología más exquisita y apurada. Es un óleo sobre lienzo de 91 por 76 cm y pertenece a la Colegiata de San Antolín, de Medina del Campo (Fig. 4).

Figura 4. La Virgen con el Niño.
Bibliografía
– VV. AA. Alonso Cano. Arte e iconografía. Catálogo de exposición. Granada: Arzobispado de Granada, 2002.
– Gómez Moreno, ME. Alonso Cano. Granada, 1954.
– Martínez M. Alonso Cano. Pintor, escultor y arquitecto. Madrid, 1949.
– Pérez AE. Pintura Barroca en España, 1600-1750. Madrid. Cátedra, 1992.
– Sánchez-Mesa D. El arte del barroco: escultura-pintura y artes decorativas. En: Pareja, E. Historia del Arte en Andalucía. Tomo VII. Sevilla, 1991.
– Véliz Z, Cerón M. Alonso Cano (1601-1667), dibujos: catálogo razonado, Santander. Fundación Botín, 2011.
– Wethey HE. Alonso Cano: pintor, escultor y arquitecto, Madrid. Alianza Editorial, 1983.
 |
| Temas de FC |
L. Soriano Guillén
Servicio de Pediatría. Instituto de Investigación Sanitaria Fundación Jiménez Díaz.
Universidad Autónoma de Madrid.
Laboratorio de Lípidos. Instituto de Investigación Sanitaria Fundación Jiménez Díaz. Madrid
| Resumen
La pubertad es un periodo de transición entre la infancia y la vida adulta, regulada por complejos mecanismos biológicos que, a su vez, están controlados por la interacción entre redes nodales de genes y el ambiente. Aunque ha existido una notable tendencia secular en el inicio de la pubertad, desde el siglo XIX hasta mediados del siglo XX, esta se ha estabilizado en las últimas décadas. De esta forma, se define como pubertad normal aquella que acontece entre los ocho y los trece años en las niñas y entre los nueve y catorce en los niños. El principal signo físico a tener en cuenta para la valoración del desarrollo puberal, es la aparición de telarquia progresiva en las niñas y el incremento del tamaño testicular en los niños. Seguidamente, se desarrollarán otros caracteres sexuales secundarios y se objetivará un incremento de la velocidad del crecimiento. En el diagnóstico diferencial de trastornos de la pubertad, aparte de conocer los límites normales de la pubertad, deberemos tener en cuenta una serie de variantes de la normalidad, como son: la adrenarquia prematura idiopática, la telarquia prematura aislada, la pubertad adelantada y el retraso constitucional del crecimiento y pubertad. |
| Abstract
Puberty is a transition period between childhood and adulthood regulated by complex biological mechanisms, which in turn are controlled by the interaction between gene networks and environment. Although there has been a significant secular trend in onset of puberty from the XIX century to the mid XX century, it has been stabilized in recent decades. Thus, it is defined normal puberty as that occurs between eight and thirteen years old in girls and between nine and fourteen years old in boys. The main physical sign to be considered for assessment of pubertal development is the emergence of progressive thelarche in girls and increased testicular size in boys. Then, other secondary sexual characteristics will develop and increased growth velocity will be observed. In the differential diagnosis of puberty disorders, apart from knowing the normal limits of puberty, we must consider a number of variants of normality such as idiopathic premature adrenarche, premature thelarche, early puberty and constitutional delay of growth and puberty. |
Palabras clave: Pubertad normal; Pubertad adelantada; Telarquia prematura; Adrenarquia prematura idiopática; Retraso constitucional del crecimiento y desarrollo
Key words: Normal and early puberty; Idiopathic premature adrenarche; Premature thelarche; Constitutional delay of growth and puberty
Pediatr Integral 2015; XIX (6): 380-388
Pubertad normal y tendencia secular
La pubertad normal corresponde a un criterio estadístico, en la que como signo principal se tiene en cuenta la aparición de telarquia entre los 8 y 13 años en las niñas y el aumento de tamaño testicular entre los 9 y 14 años en los niños.
La pubertad es un fenómeno biológico complejo a través del cual se desarrollan los caracteres sexuales secundarios, se obtiene la maduración sexual completa y se alcanza la talla adulta. En los seres humanos, la pubertad se manifiesta no solamente en forma de cambios hormonales y físicos, sino también con cambios conductuales y psicológicos(1,2).
La definición de pubertad normal obedece a criterios puramente estadísticos; es decir, si la aparición de los caracteres sexuales secundarios se encuentran dentro del intervalo de +/–2,5 SDS (Z-score) para sexo y población de referencia. Así, se considera una pubertad normal la que acontece entre los 8 y 13 años en niñas y entre 9 y 14 años en niños(3,4).
El inicio de la pubertad en las niñas, lo marca la aparición de telarquia (aproximadamente entre los 10,5 y 11 años de media), frente al incremento del tamaño testicular (≥4 ml) observado en los niños (entre los 11,5 y 12 años de media). Seguidamente, de forma progresiva, se desarrollan el resto de caracteres sexuales secundarios en paralelo al incremento del ritmo de crecimiento (Tabla I).
A continuación, de forma resumida, se describen algunos hitos del periodo puberal(5,6):
• Duración global: el tiempo transcurrido entre el inicio del estadio puberal Tanner II hasta alcanzar el estadio puberal Tanner V es variable, pudiendo oscilar en la mayoría de ocasiones entre tres y cuatro años. Generalmente, este intervalo es menor en las niñas.
• Adrenarquia: la aparición de vello púbico y/o axilar es un fenómeno dependiente de la glándula suprarrenal y es independiente del eje hipotálamo-hipófisis-gónadas. En la mayoría de ocasiones, suele aparecer en los seis meses siguientes al inicio de la telarquia. No obstante, entre un 10-15% de las ocasiones, puede preceder a la telarquia.
• Menarquia: la primera menstruación suele presentarse unos dos años después de la aparición de la telarquia. Esta suele aparecer en el estadio puberal Tanner IV.
• El cambio de voz en el niño aparece en el estadio puberal Tanner IV. Con posterioridad, los niños se afeitan. Generalmente, el afeitado completo suele observarse en el estadio puberal Tanner V.
• Crecimiento: el pico máximo de crecimiento observado durante la pubertad es algo más temprano en las niñas, entre el estadio puberal Tanner II y III, precediendo a la menarquia. En los niños, esta aceleración de crecimiento se objetiva en el estadio puberal Tanner IV. Desde el comienzo de Tanner II hasta alcanzar la talla adulta, las niñas crecen entre unos 20 y 25 cm de media y los niños, aproximadamente, entre 28 y 30 cm. El remanente medio de crecimiento después de tener la menarquia oscila entre 6 y 8 cm, pudiéndose incrementar si la aparición de la primera menstruación ha sido más temprana.
Es preciso indicar, que ha existido una tendencia secular de disminución de la edad de inicio de la pubertad en niñas. Esta tendencia ha sido documentada a través de la recogida de información sobre la edad de la menarquia en el último siglo y medio. De esta forma, sabemos que la edad de la menarquia a mediados del siglo XIX se situaba entre los 16 y 17,5 años, para un siglo después, colocarse entre los 12,5 y 13,5 años. Este hallazgo ha sido relacionado con la mejoría en las condiciones de vida de niños y adolescentes, fundamentalmente en lo referente a aspectos nutricionales. No obstante, este adelanto de la edad de aparición de la pubertad parece haberse atenuado en las dos últimas décadas del siglo XX(2,7). Aun así, los límites de edad para definir los criterios de pubertad normal fueron cuestionados en la última década del siglo XX(8), tras la aparición de un estudio transversal americano que alarmó a la comunidad científica internacional(9), ya que consideraba como límite inferior del comienzo de la pubertad los 7 años. Es necesario reseñar, sin embargo, que este estudio presentaba importantes errores metodológicos. El principal de ellos fue que la estimación del estadio puberal a través de la evaluación del grado de telarquia se realizó por inspección y no por palpación. En consecuencia, los límites anteriormente citados para la definición de pubertad normal siguen vigentes para la comunidad científica internacional desde la primera década del siglo XXI.
Más recientemente, estudios epidemiológicos daneses han mostrado cierto adelanto en la aparición de telarquia que no se acompaña de incrementos de los niveles de estradiol ni de gonadotropinas ni de un anticipo en la edad de la menarquia, sugiriendo un mecanismo gonadotropín-independiente relacionado con el ambiente, la nutrición y con mayor biodisponibilidad y/o sensibilidad a los estrógenos circulantes(7). Aunque este hallazgo debe corroborarse con estudios multicéntricos, en el que participen distintos países, parece que el intervalo entre telarquia y menarquia se prolonga, y deberemos tenerlo presente a la hora de emitir predicciones sobre la evolución de la pubertad.
Fisiología de la pubertad
Neurorregulación de la pubertad
La pubertad es un fenómeno biológico muy complejo, controlado por redes nodales de genes, que comienza tras el incremento de la secreción de hormona liberadora de gonadotropinas (GnRH). En este incremento de secreción, están implicados cambios transinápticos y gliales.
El inicio de la pubertad es el resultado final de la interacción entre importantes determinantes genéticos y un gran número de factores reguladores que incluyen diferentes elementos endógenos y señales ambientales, como: la disponibilidad de nutrientes, disruptores endocrinos ambientales y los ciclos de luz/oscuridad. Estas interacciones se inician en etapas tempranas del desarrollo, por lo que la pubertad puede considerarse el punto final de un proceso madurativo constituido por las interacciones dinámicas de genes y ambiente. Así, se estima que entre el 70-80% de la variabilidad en la edad de la menarquia, elemento clave del desarrollo puberal de las niñas, dependería de factores genéticos, frente a un 20-30% de factores ambientales(1,2,10).
Desde una perspectiva neurobiológica, ya desde hace dos décadas, se ha propuesto que el fenómeno final que pone en marcha la pubertad es el aumento en el número y en la amplitud de los picos de secreción de hormona liberadora de gonadotropinas (GnRH), por parte de las neuronas hipotalámicas productoras de GnRH, que conlleva un aumento en la secreción de gonadotropinas y, consecuentemente, de esteroides sexuales, favoreciendo, entre otros cambios, el desarrollo de los caracteres sexuales secundarios. Ahora bien, ¿qué regula este aumento de la secreción y pulsatilidad de GnRH?(10).
Tradicionalmente, se hablaba de dos teorías sobre el inicio y mantenimiento de la pubertad, merced a un predominio de estímulos inhibitorios o excitatorios, que a su vez, estarían regulados por factores genéticos y ambientales (Fig. 1).
Figura. 1. A. La secreción de GnRH estaría tónicamente reprimida durante la niñez por estímulos trans-sinápticos inhibitorios. De acuerdo a esta hipótesis, la pubertad se iniciaría en paralelo a la pérdida del estímulo inhibitorio. B. La secreción de GnRH durante la niñez estaría disminuida, debido a la falta de impulsos excitatorios sobre las neuronas secretoras de GnRH y la pubertad se iniciaría por un incremento de estos pulsos excitatorios.
En los últimos años, Ojeda y colaboradores(10) postulan que la neurorregulación de la pubertad depende de redes nodales de genes que codifican proteínas cuyas acciones se solapan e interaccionan, tanto de una forma jerárquica como independiente. De esta manera, se piensa que hay unos centros de actividad (hubs), compuestos por varios genes que previamente se habían relacionado con formación/represión de tumores (red central TGR: CDP/CULT1/CUX1, MAF, p53, YY1, USF2). Estos genes del centro de la red interactuarían entre ellos y, a su vez, regularían la transcripción de genes subordinados localizados en la periferia: regularían una primera red periférica de genes, que a su vez, interaccionaría con una segunda y tercera red nodal de genes. Lógicamente, la interrelación entre el eje central y la primera red de genes vecinos es superior al resto de redes. En esta periferia de redes nodales de genes, por ejemplo, se encuentran más de 20 genes relacionados con la edad de la menarquia, descubiertos mediante la realización de estudios de asociación de genoma completo (GWAS).
Por otra parte, junto al sistema de regulación transcripcional antes descrito, recientemente se ha descubierto un sistema de control postranscripcional que contribuye a la regulación del inicio de la pubertad, merced a un efecto inhibitorio. La red central de este sistema la constituye el gen LIN28b, que previamente, en estudios GWAS, había sido relacionado con la edad de la menarquia. En definitiva, la pubertad no es un evento desencadenado por la acción de un único gen.
La puesta en marcha de la pubertad, regulada por la red nodal de genes antes descrita, conlleva cambios en circuitos neuronales del núcleo arcuato del hipotálamo(10):
• Cambios transinápticos:
– Incremento de estímulos excitatorios de las neuronas secretoras de GnRH: vía glutamato y, fundamentalmente, vía kisspeptina.
– Disminución de los estímulos inhibitorios: neuronas gabaérgicas, neuronas productoras de sustancias opioides y neuronas productoras de péptido relacionado con RFamide [ortólogo mamífero del péptido inhibidor de gonadotropinas (GnIH)].
• Cambios en células gliales: las células gliales contribuyen a la activación de la secreción de GnRH por dos mecanismos relacionados. Uno es a través de la liberación de factores de crecimiento que actúan sobre receptores de las neuronas GnRH [factor de crecimiento transformador tipo b (TGFb), factor de crecimiento epidérmico (EGF) y factor de crecimiento similar a la insulina tipo 1 (IGF-1)]. El segundo mecanismo implica cambios en la adhesividad de las células gliales sobre las neuronas GnRH, a través de la molécula de adhesión celular tipo 1 (SynCAM1) y del receptor tipo de la proteína tirosinfosfatasa b (RPTPb).
El descubrimiento del sistema kisspeptina/receptor de kisspeptina ha permitido un avance espectacular en el conocimiento de la regulación de la secreción de GnRH. Estudios recientes han mostrado que las kisspeptinas, familia de neuropéptidos secretados por neuronas hipotalámicas, son factores esenciales en la regulación de las neuronas productoras de GnRH, ya que estas últimas neuronas expresan receptores para kisspeptina. Además, las neuronas productoras de kisspeptinas presentan un mecanismo de retroalimentación negativo por parte de los estrógenos. Por todo ello, esta familia de péptidos ha emergido como un factor primordial en la regulación de la pubertad(11).
Finalmente, en el conocimiento más profundo de la neurorregulación de la pubertad, resulta de sumo interés el estudio de la interacción entre genes y ambiente(10). Así, en los próximos años, se avanzará notablemente en la comprensión de la influencia de mecanismos epigenéticos (cambios en la expresión de distintos genes, no debidos a cambios de la secuencia de nucleótidos de un gen) sobre el normal desarrollo puberal. De esta forma, a día de hoy, existen varias líneas de investigación, de las que cabría destacar:
• Cambios epigenéticos relacionados con alteración del estado nutricional desde etapas tempranas de la vida.
• Influencia del ritmo circadiano y horas de luz sobre mecanismos epigenéticos.
• Disruptores endocrinos ambientales, fundamentalmente pesticidas, que pudieran influir sobre distintas alteraciones epigenéticas.
Estado nutricional y pubertad
Existe una vinculación muy estrecha entre metabolismo y reproducción, merced a señales periféricas que informan del estado nutricional al cerebro. Así, la obesidad se relaciona con adelanto puberal y la desnutrición se vincula con retraso puberal.
Desde hace tiempo, se apunta al tejido adiposo y al estado nutricional como factores determinantes del inicio y mantenimiento de la pubertad, siendo más evidente en niñas que en niños(12,13). Entre otros factores, se conoció, en primer lugar, la necesidad de alcanzar un peso crítico para la aparición de la edad de la menarquia y, con posterioridad, se demostró la relevancia de un mínimo de masa grasa corporal. A continuación, paralelamente a la constatación de la existencia de un incremento del grado de adiposidad a lo largo de la infancia, se mostró una relación inversa entre el estado nutricional y el tiempo de desarrollo puberal. Más recientemente, se ha sugerido que péptidos sintetizados en el tejido adiposo pudieran desempeñar un importante papel como enlaces entre el estado nutricional y la reproducción. Así, es indiscutible el papel desempeñado por la leptina, a la que se ha señalado con un factor favorecedor del desarrollo puberal. Menos clara es la implicación atribuible a adiponectina en el desarrollo puberal, aunque se especula que su papel en la regulación de la sensibilidad a la insulina pudiera ser importante en la maduración del eje reproductor.
Por otra parte, el péptido ghrelina, sintetizado principalmente en las células oxínticas del estómago, factor orexígeno y relacionado con el estado metabólico, ha sido también, relacionado con la reproducción, ya que parece desempeñar un papel inhibitorio sobre la secreción de hormona liberadora de gonadotropinas, merced al estímulo que ejerce sobre neuronas hipotalámicas productoras de neuropéptido Y. Además, contrariamente a lo que ocurre con leptina, se ha observado una reducción progresiva de los niveles de ghrelina a lo largo de la pubertad, lo que sugiere un papel permisivo sobre el inicio de la pubertad.
Ahora bien, ¿cómo es posible explicar que sustancias sintetizadas en tejidos periféricos como el tejido adiposo o en el intestino puedan influir en la neurorregulación de la pubertad, máxime, si tenemos en cuenta que las neuronas productoras de GnRH no expresan receptores para leptina ni adiponectina ni ghrelina? Pues bien, es ahí donde surge el papel de kisspeptina, ya que el sistema kisspeptina-receptor de kisspeptina es el mayor estimulador del sistema GnRH/gonadotropinas conocido hasta el momento. Los descubrimientos relacionados con este sistema nos han mostrado que las neuronas productoras de kisspeptina se encuentran en el núcleo arcuato y anteroventral periventricular hipotalámicos y presentan receptores de leptina, sugiriendo un nexo entre metabolismo y reproducción. En esta línea, también se ha demostrado una disminución de la expresión hipotalámica de kisspeptina en modelos animales de desnutrición por insuficiente aporte calórico.
Desde el punto de vista clínico, en el ámbito de la Pediatría, hay dos entidades de elevada prevalencia, obesidad y anorexia nerviosa, que afectan al metabolismo y que tienen consecuencias sobre la pubertad. El exceso de peso tiene una elevada prevalencia en la población infanto-juvenil y entre los riesgos que conlleva en la infancia destaca el adelanto puberal entre las niñas obesas(12). Por otra parte, la anorexia nerviosa es una patología psiquiátrica crónica en la que existe una distorsión de la imagen corporal, que provoca una pauta alimentaria restrictiva/purgativa, disminuyendo notablemente la ingesta calórica, produciendo disminución del IMC y de la masa grasa corporal. Esta situación de malnutrición crónica favorece la aparición de hipogonadismo hipogonadotropo. Este hecho condiciona, en función de la edad de inicio del trastorno, las siguientes consecuencias: retraso puberal, pubertad enlentecida y amenorrea primara o secundaria(14).
Desde hace años, se ha investigado la influencia de la etapa fetal en la vida adulta, sobre todo, en lo referente al recién nacido pequeño para la edad gestacional (PEG), definido como: recién nacido cuyo peso y/o longitud se sitúa por debajo de 2 SDS (Z-score) para la edad gestacional y sexo, según tablas de referencia poblacionales. Una de las líneas surgida de la investigación sobre la repercusión en la vida adulta de los recién nacidos PEG, ha sido la relativa a la influencia sobre la pubertad. Así, parece ser que niñas con el antecedente de PEG y, especialmente aquellas que han experimentado un rápido crecimiento recuperador y ganancia ponderal, parecen más expuestas a presentar adrenarquia prematura, adelanto puberal y síndrome de ovario poliquístico. No obstante, no todos los estudios han demostrado la evolución anteriormente descrita, por lo que se antoja necesario plantear el diseño de estudios prospectivos que evalúen la evolución de los recién nacidos PEG hasta el final de la adolescencia(15).
Historia clínica de utilidad en la valoración del desarrollo puberal
Anamnesis
Historia reciente: describir detalladamente la secuencia de aparición de posibles caracteres sexuales secundarios.
• Niña: aparición de telarquia, si esta es fluctuante o progresiva, unilateral o bilateral. Si ha notado incremento de la sensibilidad en el área de la areola. ¿Ha aparecido pubarquia y/o axilarquia? ¿Ha precedido o ha sido posterior a la telarquia? Valorar la curva de crecimiento, ¿ha existido aceleración del mismo?
• Niño: precisar si han notado aumento del tamaño testicular (valorando incremento de la bolsa escrotal) y desde cuando. ¿Son los testículos simétricos? ¿Han notado incremento del tamaño del pene? ¿Ha aparecido pubarquia y/o axilarquia? Evaluar la curva de crecimiento.
Antecedentes familiares: en primer lugar, descartar consanguinidad. Seguidamente, solicitar datos sobre raza y país de origen de los padres. A continuación, demandar información sobre talla de los progenitores y cálculo de talla genética, para comparar con los percentiles de talla de su hijo. Recoger datos sobre el desarrollo puberal de los padres (menarquia de la madre, edad de afeitado del padre, entre otros). Asimismo, resulta de interés conocer antecedentes entre las mujeres de síndrome de ovario poliquístico (SOP) e hirsutismo.
Antecedentes personales: embarazo, parto y datos antropométricos perinatales. En el supuesto de antecedente de bajo peso para edad gestacional, es necesario conocer si ha tenido un adecuado crecimiento recuperador o, si por el contrario, no lo ha realizado y ha precisado tratamiento con hormona de crecimiento. También es importante conocer si es adoptado y el tiempo que lleva en España. Interrogar por la presencia de patología crónica. Recoger datos sobre estado nutricional y grado de actividad física, así como de distorsión de imagen corporal. Otro dato que resulta de interés para la valoración de la patología puberal por retraso, es la existencia de alteración del sentido del olfato.
Examen físico
Inspección: fenotipo, bocio, lesiones cutáneas (manchas café con leche, acné, estrías), incremento del vello corporal, telarquia/adipomastia, aumento del tamaño de la bolsa escrotal, aumento del tamaño del pene, presencia de pubarquia/axilarquia.
Palpación: distinguir entre posible telarquia versus adipomastia, tamaño y simetría testicular, posibilidad de bocio, visceromegalias.
Recogida de datos: peso (kg, percentil, SDS), talla (cm, percentil, SDS), índice de masa corporal (valor absoluto, percentil, SDS), velocidad de crecimiento (cm/año, percentil, SDS) y tensión arterial. Si es preciso, calcular otros índices nutricionales.
Describir estadio puberal de Tanner (Tabla I): de I a V con subapartados:
a. Niñas:
• S (seno) o T (telarquia) de 1 a 5. Su puntuación es la que va a indicar el estadio Tanner.
• P (pubarquia) de 1 a 5.
• A (axilarquia): a (sin vello), b, c.
b. Niños:
• P (pubarquia) de 1 a 5. Junto con la evolución del tamaño del pene, marcará el estadio puberal de Tanner.
• A (axilarquia): a, b, c.
• Tamaño testicular mediante orquidómetro de Prader:
– <4 ml: prepuberal (Tanner I).
– ≥4 ml: inicio de la pubertad (Tanner II).
– ≥8 ml: generalmente coincide con Tanner III, aunque lo marca el crecimiento del pene y la pubarquia.
– ≥12 ml: generalmente coincide con Tanner IV.
– ≥18-20 ml: la mayoría de ocasiones coincide con Tanner V.
Variantes de la normalidad (ver algoritmo al final del artículo)
En el diagnóstico diferencial de la patología puberal, deberemos tener en cuenta unas entidades que se consideran variantes del desarrollo puberal normal: adrenarquia prematura idiopática, telarquia prematura aislada, pubertad adelantada y retraso constitucional del crecimiento y desarrollo.
Adrenarquia prematura idiopática
Se define como la aparición de vello púbico y/o axilar y/o aumento del olor corporal (olor apocrino) antes de los 8 años en niñas y de los 9 años en niños, una vez excluidas otras patologías de semiología similar(15).
Presenta un claro predominio femenino (relación 9:1) y se caracteriza por ser un fenómeno independiente de la pubertad. Por tanto, no se acompaña de desarrollo mamario en las niñas, ni de aumento del volumen testicular o del pene en los niños. Asimismo, no suele observarse una aceleración brusca del crecimiento, aunque la talla suele estar por encima de la talla diana. Por otra parte, es frecuente que la edad ósea se encuentre ligeramente adelantada con respecto a la edad cronológica.
Aún se desconoce la causa exacta de esta activación temprana de la funcionalidad de la glándula suprarrenal, que conlleva un aumento de la síntesis de dehidroepiandrostendiona sulfato en la zona reticularis. Algunos estudios poblacionales han mostrado mayor prevalencia de adrenarquia prematura en niñas con antecedentes de bajo peso para la edad gestacional.
La adrenarquia prematura idiopática es un diagnóstico de exclusión, existiendo dos entidades con semiología clínica parecida que debemos descartar:
• Hiperplasia suprarrenal congénita (HSR) de presentación tardía.
• Patología tumoral productora de andrógenos (origen ovárico o suprarrenal).
Por tanto, siempre deben derivarse a estos niños/as de Atención Primaria a Especializada. Para facilitar la orientación diagnóstica, es de suma utilidad aportar gráficas de crecimiento, así como la realización de una edad ósea.
Estas niñas, no requieren tratamiento, aunque es recomendable realizar seguimientos periódicos hasta el final de la pubertad; ya que, los datos disponibles de distintas investigaciones sobre las consecuencias a largo plazo de la adrenarquia prematura idiopática no son unánimes. Por ello, se necesitan más estudios longitudinales multicéntricos (englobando distintas áreas geográficas) para evaluar la talla final de estas pacientes, así como el porcentaje de niñas que desarrolla síndrome de ovario poliquístico, obesidad y alteraciones metabólicas.
Telarquia prematura aislada
Se define como el desarrollo mamario uni o bilateral antes de los 8 años, sin evidencia de otros signos de pubertad precoz como aceleración del crecimiento, edad ósea incrementada y aparición de vello púbico y/o axilar(16,17).
Es una entidad relativamente frecuente, con una incidencia aproximada de hasta 21,2 casos por 100.000/año. En la mayoría de ocasiones, aparece antes de los 2 años y tiende a la regresión espontánea. El otro pico de presentación se sitúa entre los 5 y 7 años, y es en estas situaciones, donde se han descrito mayor probabilidad de evolucionar a un cuadro de pubertad precoz central. Algunas series cifran esta probabilidad hasta en un 14%.
La etiología es desconocida, considerándose diferentes teorías:
• Activación transitoria parcial del eje hipotálamo-hipofisario-gonadal con aumento de FSH.
• Fallo de la involución folicular con o sin formación ovárica quística.
• Sensibilidad excesiva del tejido mamario a la misma cantidad de estrógenos.
• Contaminantes ambientales (disruptores endocrinos) con actividad estrogénica.
• Formas incompletas de síndrome de McCune-Albright en telarquias prematuras exageradas.
La telarquia prematura aislada suele ser un proceso autolimitado que tiende a la regresión espontánea. Por tanto, en la mayoría de ocasiones, no precisa de estudios complementarios y puede controlarse en Atención Primaria, vigilando estrechamente si la telarquia es progresiva, si existe aceleración del crecimiento y si aparece pubarquia/axilarquia. Tendremos especial precaución en el seguimiento de niñas en las que aparece telarquia por encima de los 2 años, ya que es en este grupo donde se ha documentado mayor probabilidad de evolución hacia una activación central de la pubertad.
No es preciso tratar a estas pacientes, aunque es recomendable realizar seguimientos periódicos hasta la desaparición de la telarquia. En el caso de no regresar, se recomienda seguimiento hasta los 8-9 años, momento en el que el inicio de la pubertad es normal.
Pubertad adelantada
Variante de la normalidad, en la que el desarrollo puberal se inicia entre los ocho y los nueve años en las niñas y entre los nueve y diez años en los niños(17). La etiología puede ser muy diversa. En esta revisión, presentamos algunos de los ejemplos más representativos:
1. Aceleración constitucional del crecimiento y desarrollo: son niños/as con antecedentes familiares de pubertad temprana y que ya, desde la etapa preescolar, se sitúan en percentiles elevados de talla (>percentil 90-97), generalmente, por encima de la talla diana. Asimismo, hasta la aparición temprana de la pubertad, presentan adelanto de la maduración ósea, con una velocidad de crecimiento en percentiles elevados para edad y sexo de las tablas de referencia. Con el inicio de la pubertad, se objetiva un incremento de la velocidad de crecimiento, situándose muy por encima del percentil 97, puesto que el pico de velocidad de crecimiento se adelanta al compararlo con niños/as de la misma edad. Estos niños/as terminan su crecimiento antes que el resto y suelen alcanzar una talla acorde con la talla genética.
2. Obesidad: entre las niñas hay mayor riesgo de adelanto puberal, particularmente en aquellas niñas que incrementan notablemente su índice de masa corporal a partir de los seis años. Por tanto, en el seguimiento de las niñas obesas, deberemos vigilar la posibilidad de adelanto puberal teniendo en consideración que, en ocasiones, es muy difícil el diagnóstico diferencial entre verdadera telarquia y adipomastia.
3. Adopción: las niñas adoptadas presentan mayor riesgo de pubertad precoz y pubertad adelantada que las niñas autóctonas del país. Deberemos fijarnos con detalle en el desarrollo temprano de los caracteres sexuales secundarios, en las valoraciones periódicas de estas niñas.
4. Antecedente de PEG: en fase de investigación. No obstante, conviene revisar periódicamente en estos pacientes, la posible relación con adelanto puberal, tanto en los que tuvieron un rápido crecimiento recuperador, como aquellos que no lo realizaron y reciben terapia con hormona de crecimiento.
Debe plantearse el diagnóstico diferencial con una pubertad precoz. Aunque como hemos comentado anteriormente, existe un criterio estadístico claro que define pubertad precoz y pubertad adelantada.
Estos niños y niñas pueden manejarse en Atención Primaria, puesto que no es necesaria la realización de pruebas complementarias específicas, ni la instauración de un tratamiento frenador de la pubertad, debido a que no existe evidencia científica suficiente que avale su utilidad para mejorar el pronóstico de talla final. No obstante, valoraremos derivaciones a Atención Especializada ante:
• Importante ansiedad familiar.
• Situaciones de pubertad adelantada rápidamente progresiva, en el que pudiera verse afectada el pronóstico de talla final.
Retraso constitucional del crecimiento y pubertad (RCCP)
Variante de la normalidad que se manifiesta en las niñas por ausencia de telarquia, a partir de los 13 años y, en los niños, por no objetivarse incremento del tamaño testicular (≥4 ml), a partir de los 14 años. Constituye la causa más frecuente de retraso puberal, aproximadamente un 65% de los casos en niños y un 35% de las niñas(18-20).
Aunque se desconoce la etiología del RCCP, se concede un papel primordial al componente genético, puesto que hasta, en un 75% de las ocasiones, existen antecedentes familiares. El patrón de herencia suele ser dominante con un grado penetrancia variable. Pese a ello, hasta la fecha, no se ha documentado ninguna alteración genética causante de RCCP.
Estos niños/as se caracterizan por presentar unos datos antropométricos perinatales normales, con posterior desaceleración de la velocidad de crecimiento, generalmente, a partir de los 18 meses de vida, que les hace situar su talla por debajo del percentil tres, entre los dos y tres años de edad. A veces, la talla se encuentra entre percentil tres y diez o entre diez y veinticinco, pero marcadamente por debajo de su talla genética. A partir de ese momento, su velocidad de crecimiento adquiere un ritmo adecuado y la talla progresa paralelamente al percentil tres (Fig. 2).
Figura. 2. Curva de crecimiento de un niño con Retraso Constitucional del Crecimiento y Pubertad.
La realización de una edad ósea muestra un retardo de la misma con respecto a la edad cronológica, que con frecuencia es superior a dos años. A la edad correspondiente a un inicio normal de la pubertad, sufren una desaceleración del crecimiento, puesto que su ritmo de crecimiento es prepuberal; es decir, presentan mayor depresión prepuberal que los niños/as con un inicio normal de la pubertad. En ocasiones, este ritmo de crecimiento puede ser incluso inferior a 3 cm/año. Así pues, su curva de talla se aleja del percentil tres. Seguidamente, comienzan tardíamente la pubertad. Llegados a este punto, es preciso destacar que el pico de velocidad de crecimiento observado en estos niños/as, no es tan acentuado como en sujetos con pubertad normal. Finalmente, en la mayoría de casos, suelen alcanzar una talla normal acorde con su talla genética.
El RCCP entra en el diagnóstico diferencial con otras etiologías causantes de retraso puberal (ver capítulo correspondiente) y constituye un diagnóstico de exclusión. Por tanto, la anamnesis y el examen físico deben ser minuciosos y, en no pocas ocasiones, puede ser necesaria la realización de pruebas complementarias. Por ello, es aconsejable su derivación a Atención Especializada. A pesar de ello, con cierta frecuencia, solo el tiempo nos permitirá comprobar si se trata de un verdadero RCCD. Como datos sugestivos de esta variante de la normalidad, tomaremos en consideración:
• Existencia de antecedentes familiares.
• Ser niño.
• Curva de crecimiento antes descrita (Fig. 2).
• Retraso de edad ósea.
• Ausencia de adrenarquia.
• Sin antecedentes de criptorquidia ni micropene ni anosmia.
Normalmente, no requieren tratamiento médico, sin embargo, en aquellas situaciones en las que exista repercusión psicológica, puede ser aconsejable la administración de esteroides sexuales, ya sea testosterona, ya sea 17-β-estradiol, en ciclos de tres a seis meses con el propósito de favorecer el desarrollo de los caracteres sexuales secundarios y, de esta forma, mitigar, al menos en parte, las alteraciones psicológicas derivadas del retraso puberal.
Bibliografía
Los asteriscos reflejan el interés del artículo a juicio del autor.
1. Cartault A, Edouard T, Pienkowski C, Tauber M. Normal puberty. Rev Prat. 2008; 58: 1311-6.
2.*** Parent AS, Teilmann G, Juul A, Skakkebaek NE, Toppari J, Bourguignon JP. The timing of normal puberty and the age limits of sexual precocity: variations around the world, secular trends, and changes after migration. Endocr Rev. 2003; 668-93.
3.** Marshall WA, Tanner JM. Variations in the pattern of pubertal changes in girls. Arch Dis Child. 1969; 44: 291-303.
4.** Marshall WA, Tanner JM. Variations in the pattern of pubertal changes in boys. Arch Dis Child. 1970; 45: 13-24.
5.*** Rodríguez Hierro F. Pubertad normal. En: Argente Oliver J, Carrascosa Lezcano A, Gracia Bouthelier R, Rodríguez Hierro F, ed. Tratado de Endocrinología Pediátrica y de la Adolescencia (1ª edición). Madrid: Edimsa; 1995. p. 679-88.
6.** Basdemir D, Rogol AD. Maduración puberal. En: Argente Oliver J, Carrascosa Lezcano A, Gracia Bouthelier R, Rodríguez Hierro F, ed. Tratado de Endocrinología Pediátrica y de la Adolescencia (2ª edición). Madrid: Doyma; 2000. p. 843-66.
7.*** Sørensen K, Mouritsen A, Aksglaede L, Hagen CP, Mogensen SS, Juul A. Recent secular trends in pubertal timing: implications for evaluation and diagnosis of precocious puberty. Horm Res Paediatr. 2012; 77: 137-45.
8. Kaplowitz PB, Oberfield SE. Reexamination of the age limit for defining when puberty is precocious in girls in the United States: implications for evaluation and treatment. Pediatrics. 1999; 104: 936-41.
9. Herman-Giddens ME, Slora EJ, Wasserman RC, et al. Secondary sexual characteristics and menses in young girls seen in office practice: a study from the Pediatric Research in Office Settings Network. Pediatrics. 1997; 99: 505-12.
10.*** Lomniczi A, Wright H, Ojeda SR. Epigenetic regulation of female puberty. Front Neuroendocrinol. 2015; 36C: 90-107.
11.** Castellano JM, Tena-Sempere M. Metabolic regulation of Kisspeptin. Adv Exp Med Biol. 2013; 784: 363-83.
12.*** Kaplowitz PB. Link between body fat and the timing of puberty. Pediatrics. 2008; 121: S208-17.
13.** Sánchez-Garrido MA, Tena-Sempere M. Metabolic control of puberty: roles of leptin and kisspeptins. Horm Behav. 2013; 64: 187-94.
14.** Muñoz MT, Argente J. Anorexia nervosa in female adolescents: endocrine and bone mineral density disturbances. Eur J Endocrinol. 2002; 147: 275-86.
15.*** Williams RM, Ward CE, Hughes IA. Premature adrenarche. Arch Dis Child. 2012; 97: 250-4.
16.*** Codner E, Román R. Premature thelarche from phenotype to genotype. Pediatr Endocrinol Rev. 2008; 5: 760-5.
17. Cassorla F, Codner E. Pubertad precoz y adelantada. En: Argente Oliver J, Carrascosa Lezcano A, Gracia Bouthelier R, Rodríguez Hierro F, ed. Tratado de Endocrinología Pediátrica y de la Adolescencia (2ª edición). Madrid: Doyma; 2000. p. 867-81.
18. Rodríguez Hierro F. Pubertad retrasada e hipogonadismos. En: Argente Oliver J, Carrascosa Lezcano A, Gracia Bouthelier R, Rodríguez Hierro F, ed. Tratado de Endocrinología Pediátrica y de la Adolescencia (2ª edición). Madrid: Doyma; 2000. p. 883-911.
19.** Harrington J, Palmert MR. Distinguishing constitutional delay of growth and puberty from isolated hypogonadotropic hypogonadism: critical appraisal of available diagnostic tests. J Clin Endocrinol Metab. 2012; 97: 3056-67.
20.*** Palmert MR, Dunkel L. Delayed puberty. N Engl J Med. 2012; 366: 443-53.
Bibliografía recomendada
– Parent AS, Teilmann G, Juul A, Skakkebaek NE, Toppari J, Bourguignon JP. The timing of normal puberty and the age limits of sexual precocity: variations around the world, secular trends, and changes after migration. Endocr Rev. 2003; 668-93.
Excelente revisión sobre los límites normales de la pubertad, la evolución de la tendencia secular en distintos países del mundo y la influencia de factores ambientales sobre el normal desarrollo puberal.
– Rodríguez Hierro F. Pubertad normal. En: Argente Oliver J, Carrascosa Lezcano A, Gracia Bouthelier R, Rodríguez Hierro F, ed. Tratado de Endocrinología Pediátrica y de la Adolescencia (1ª edición). Madrid: Edimsa; 1995. p. 679-88.
Capítulo de la primera edición de un Tratado de Endocrinología Infantil de enorme prestigio y difusión, en el que se describe de forma muy minuciosa y didáctica todos los cambios físicos que acontecen a lo largo del desarrollo puberal.
– Lomniczi A, Wright H, Ojeda SR. Epigenetic regulation of female puberty. Front Neuroendocrinol. 2015; 36C: 90-107.
Puesta al día de los conocimientos adquiridos sobre el complejo mecanismo de regulación del inicio y mantenimiento de la pubertad. Este grupo de autores es pionero en la investigación de la neurorregulación de la pubertad, destacando sus aportaciones sobre los mecanismos genéticos y epigenéticos implicados en el inicio y mantenimiento de la pubertad.
– Williams RM, Ward CE, Hughes IA. Premature adrenarche. Arch Dis Child. 2012; 97: 250-4.
Magnífica revisión sobre la etiopatogenia, abordaje diagnóstico, evolución y seguimiento de la adrenarquia prematura idiopática. Analiza de forma concienzuda, estudios procedentes de distintos países sobre la etiología y evolución a largo plaza de niños/as con adrenarquia prematura.
– Palmert MR, Dunkel L. Delayed puberty. N Engl J Med. 2012; 366: 443-53.
Actualización muy didáctica sobre el retraso puberal, con un apartado especial dedicado al retraso constitucional del crecimiento y pubertad: epidemiología, carga familiar, diagnóstico diferencial y orientación terapéutica.
| Caso clínico |
|
Historia reciente: niña que, desde aproximadamente los dos años y cuatro meses, presentaba telarquia izquierda, sin molestias locales ni cambios de pigmentación de areola. Dicha telarquia era fluctuante, no progresiva. A los dos años y nueve meses aparece telarquia derecha. Por otra parte, no presentaba ni pubarquia ni axilarquia ni aceleración del crecimiento, así como tampoco ningún episodio de sangrado vaginal. Antecedentes: como antecedentes familiares, destaca que la madre tuvo la menarquia a la edad de 9 años y el desarrollo puberal del padre fue normal. La talla diana es de 168 cm (p90). Sobre los antecedentes personales, hay que indicar que el embarazo fue de curso normal y el parto ocurrió a las 39 semanas de edad gestacional, con un peso y longitud de recién nacido dentro de percentiles normales (PRN 3.200 gramos; LRN 50 cm). No presentó telarquia en el periodo neonatal. Examen físico A los dos años y diez meses, mostraba un peso de 15,2 kg (percentil 75-90) y una talla de 98 cm (percentil 90-97). No presentaba lesiones cutáneas reseñables y la exploración abdominal fue normal. Presentaba genitales externos femeninos normales y era reseñable la presencia de telarquia izquierda de 1 x 1 cm y derecha de 1,5 x 2 cm. Por otra parte, no se objetiva pubarquia ni axilarquia. Pruebas complementarias iniciales A los dos años y sietes meses, se solicitó una edad ósea que correspondía a tres años (Fig. 3). A los dos años y diez meses, se realizó una ecografía pélvica que mostraba los siguientes datos: a) tamaño uterino de 20 mm (rango prepuberal); b) relación cuello fundus de 1/1 (rango prepuberal); c) sin línea endometrial (hallazgo prepuberal); d) volumen de ovario izquierdo de 1,7 cc y derecho de 1,8 cc (rangos prepuberales). Evolución A los tres años y seis meses, mostraba una talla de 106,2 cm (percentil >97/ + 2,36 SDS), es decir, se había objetivado una aceleración franca de la velocidad de crecimiento (ocho centímetros en ocho meses) y, paralelamente, la telarquia había progresado notablemente (telarquia izquierda de unos 3 x 2 cm, telarquia derecha de unos 3 x 3 cm). En ese momento, la edad ósea era de 5 años, objetivando un avance notable respecto a la previa (Fig. 3). Figura. 3. Evolución de las edades óseas realizadas a la paciente y descrita en el caso clínico. |
 |
| Temas de FC |
M. Güemes-Hidalgo*, M.T. Muñoz-Calvo**
*Departamento de Endocrinología. Great Ormond Street Hospital for Children. Londres. Reino Unido. **Servicio de Endocrinología. Hospital Infantil Universitario Niño Jesús. Profesora Asociada de Pediatría. Universidad Autónoma. Madrid
| Resumen
En la actualidad, la obesidad se considera un problema de salud pública mundial dado el aumento de su prevalencia, su continuidad en la edad adulta, los cambios en los estilos de vida de la población, la comorbilidad que se asocia y la baja percepción del riesgo por parte de la población. La prevalencia actual de obesidad infantojuvenil en nuestro país se estima en un 12,6%. Determinados sujetos pueden tener una mayor predisposición genética a aumentar de peso, y los genes pueden no expresarse totalmente hasta la etapa adulta. A continuación, se aborda: la etiopatogenia multifactorial, la comorbilidad, así como el abordaje diagnóstico, terapéutico y la prevención que debe iniciarse en edades precoces, ya que los hábitos de salud se establecen en la infancia y posteriormente será difícil modificarlos. El diagnóstico es fundamentalmente clínico. El tratamiento es multidisciplinar, actuando sobre el paciente y su entorno. El pediatra tiene un papel importante detectando los factores y poblaciones de riesgo, colaborando en el tratamiento y ejerciendo una acción preventiva educadora en los diferentes niveles: familiar, escolar, social y político. |
| Abstract
Obesity is considered a worldwide public health problem given its increasing prevalence, its continuation into adulthood, society ́s lifestyle changes, the associated comorbidities and society ́s low perception of its risk. Spain ́s current estimated prevalence among children and adolescents is 12.6%. Certain individuals have a higher genetic predisposition to gain weight, although the genes involved may not be fully expressed until adult age. This review includes the multifactorial pathogenesis, comorbidities, diagnostic and therapeutic approaches, and prevention strategies. The latter ought to be commenced in early ages as health habits are established during infancy, hence the difficulty in modifying these at a later stage. The diagnosis remains mainly clinical. The management requires a multidisciplinary intervention over the patient and their environment. The pediatrician has a significant role in identifying risk factors and at-risk individuals, participating in treatment and conducting preventive educational actions at different levels such as family, school, social and political. |
Palabras clave: Sobrepeso; Obesidad; Alimentación saludable; Actividad física; Prevención; Estrategias comunitarias; Infancia
Key words: Overweight; Obesity; Healthy eating; Physical activity; Prevention; Community strategies; Childhood
Pediatr Integral 2015; XIX (6): 412-427
Introducción
En los últimos años, la obesidad ha ido aumentado de forma alarmante a nivel mundial, constituyendo un problema de salud pública.
Según la OMS (2015), la prevalencia de la obesidad (OB) en la población infantojuvenil va en aumento en todos los países, y los ascensos más rápidos se registran en los países de ingresos bajos y medianos. El número de lactantes y niños pequeños con sobrepeso (SP) u OB se incrementó en todo el mundo, de 31 millones en 1990 a 42 millones en 2013. Si la tendencia actual continúa y no se interviene, se llegará a los 70 millones en 2025. Ya en mayo de 2004, la 57ª Asamblea Mundial de Salud declaró a la OB como la epidemia del siglo XXI.
La OB infantojuvenil constituye un importante problema de salud debido no solo a su prevalencia ascendente, sino también a su persistencia en la edad adulta, su asociación con otras enfermedades, además del enorme impacto económico que supone(1). Cuando se inicia en la segunda década de la vida, es un factor predictivo de obesidad adulta y si continúa en el tiempo, se asocia con un mayor riesgo de enfermedad cardiovascular y de muerte(1,2).
En la figura 1, puede observarse que, independientemente de la adiposidad de los padres; la probabilidad de que la OB infantil persista en la edad adulta, aumenta simplemente con la edad, con un agudo incremento en el periodo peri puberal(3).
Figura 1. Riesgo relativo de ser un adulto obeso (21-29 años) sobre la base de si se es obeso de niño, según las diferentes edades. Fuente: M Rosenbaum. Special Considerations Relative to Pediatric Obesity. Endotext [Internet]. www.endotext.org
La OB es el trastorno nutricional más frecuente en la población infantojuvenil y tiene su origen en una interacción genética y ambiental-conductual, siendo esta última la más importante, ya que establece un desequilibrio entre la ingesta y el gasto energético. El desarrollo del SP y posteriormente la OB, gira en torno a vivir en “la sociedad de la abundancia” donde junto a una importante oferta de alimentos hipercalóricos, coexisten cambios en los estilos de vida, como el sedentarismo, e inadecuados hábitos alimentarios, con una ingesta basada en las características organolépticas de los alimentos desconociendo sus características nutricionales.
En los últimos años, se han adquirido conocimientos en los mecanismos reguladores del peso y de la composición corporal descubriéndose nuevas hormonas, genes y vías reguladoras, pero el tratamiento de la OB sigue siendo uno de los problemas más difíciles de resolver en la práctica clínica. Los pilares del tratamiento son modificar la conducta alimentaria, estimular la actividad física y motivar al paciente; en la infancia se añade, además, la influencia familiar, ya que los niños aprenden por imitación y los hábitos que se establecen en la infancia tienden a mantenerse en la edad adulta. Es preciso un tratamiento multidisciplinar que puede ser coordinado por el pediatra quien, además de identificar las poblaciones y factores de riesgo, debe educar e instaurar medidas preventivas, y saber cómo abordar a los pacientes y sus familias. Serán precisas además, intervenciones en el ámbito escolar, sanitario y comunitario(1).
Concepto de sobrepeso y obesidad
En la práctica clínica, la estimación del contenido graso corporal se realiza determinando el Índice de Masa Corporal (IMC), a pesar de que aporta escasa información sobre los diferentes depósitos grasos corporales. El IMC se calcula dividiendo el peso (kilogramos) por la talla (metros) al cuadrado.
La OB consiste en el acúmulo de tejido graso en el organismo en relación con otros componentes corporales y suele ser el resultado de un balance energético positivo. Se acepta, que un niño presenta OB cuando su IMC sobrepasa en dos o más desviaciones estándar (DE) el valor medio de este parámetro estimado en individuos de la misma población, edad y sexo. Por el contrario, el concepto de SP hace referencia a aquellos individuos que presentan un exceso de tejido graso, pese a lo cual su IMC no sobrepasa +2 DE en idénticas condiciones a las anteriormente mencionadas(4).
Para la edad pediátrica, la International Obesity Task Force (IOTF) propone utilizar las gráficas de Cole et al. para definir el SP y la OB(5). Tomaron muestras representativas de poblaciones de EE.UU., Brasil, Reino Unido, Hong Kong, Singapur y Holanda y combinaron los datos. Se definieron los valores de IMC para cada sexo entre 2 y 18 años que se corresponden con los valores de 25 y 30 kg/m2 del adulto, equivalente a puntos de corte de SP y OB. Los niños y adolescentes con SP se corresponden con un percentil 85 y la OB con el percentil 95.
La Guía de Práctica Clínica para la Prevención y Tratamiento de la Obesidad Infanto-Juvenil(6), considera los criterios para definir el SP y la OB, los percentiles 90 y 97, respectivamente, específicos para edad y sexo, referido a los datos y curvas de Hernández et al., del año 1988.
El término “obesidad mórbida” se emplea, en ocasiones, para definir aquellos individuos con comorbilidades asociadas a OB. A menudo se usa de forma errónea para definir OB grave, con connotación negativa para el sujeto, por lo que se desaconseja su empleo.
Epidemiología
La prevalencia de SP y OB infantojuvenil en España sigue siendo muy alta (cercana al 40%), pero no ha crecido en los últimos 12 años. Se estima, actualmente, una prevalencia de obesidad del 12,6%, y de sobrepeso del 26,0% con ligero predominio en los varones y se asocia con clase social y nivel de estudios inferiores.
En los países occidentales, se ha señalado un rápido aumento de la prevalencia de OB en los últimos años, afectando por igual a ambos sexos, a todos los grupos de edad, a distintos grupos raciales, a familias con alto y bajo nivel económico, tanto en el medio rural como en el urbano.
La prevalencia de la OB infantil en nuestro medio es difícil de precisar. En parte, debido a los distintos criterios empleados en los diferentes estudios efectuados. El estudio enKid (utilizando las gráficas de Hernández et al.), desarrollado de forma multicéntrica entre los años 1998 y 2000, arrojaba cifras de prevalencia de OB del 12% para las niñas y del 15,6% en el caso de los niños, así como del 13% respecto al SP, si bien la distribución de los pacientes incluidos no era uniforme, predominando la franja infantil(2).
A través de los estudios: Paidos’84 donde el 4,9% de los niños de 6-12 años eran obesos, Ricardin-1995 y EnKid-1998-2000(2), se observa que se triplicaron las cifras y que el IMC medio aumentó un 0,7 kg/m2 y 2,7 kg/m2 en niños de 10 y 13 años, respectivamente. Todo ello condiciona que las expectativas de futuro para la población adulta sean muy negativas. Durante el periodo 1979-2001, el estudio GALINUT también demostró un incremento significativo de la media del IMC. El estudio AVENA (Alimentación y Valoración del Estado Nutricional en Adolescentes) desarrollado en varias ciudades españolas en el período 2000-2002, demostraba una prevalencia de SP más OB en adolescentes de 13 a 19 años del 25,69% y 19,13% en varones y mujeres, respectivamente(7). Según el estudio transversal español de crecimiento, realizado en 32.064 sujetos (16.607 varones y 15.457 mujeres), desde el nacimiento hasta la talla adulta, en una población caucásica española procedente de Andalucía, Barcelona, Bilbao y Zaragoza, realizado entre los años 2000 y 2004, afirmaban que en nuestro país y en cualquier edad en la infancia y la adolescencia, valores superiores a los de los percentiles 80 y 85, podrían utilizarse respectivamente para definir el SP en varones y mujeres, y que valores superiores al percentil 97 definirían OB en ambos sexos(8).
El Ministerio de Sanidad en el año 2006 publicó los datos nacionales correspondientes a la última Encuesta Nacional de Salud de España, en población de 2 a 17 años, donde observaban una prevalencia de OB del 8,9% y de SP del 18,7%.
En un reciente estudio realizado en 2012 sobre la prevalencia de la OB en la población infantojuvenil española entre los 8-17 años(9), se observa que la prevalencia de sobrepeso es del 26% y la de OB del 12,6%; 4 de cada 10 jóvenes sufren exceso de peso. En el grupo comprendido entre los 8 y los 13 años, el exceso de peso supera el 45%, mientras que para el grupo de 14 a 17 años, el exceso de peso es del 25,5%. La OB se asocia con las clases sociales más desfavorecidas y con menos estudios. Aunque la prevalencia sigue siendo muy alta, parece que no ha crecido en los últimos 12 años(9).
En Europa, la tasa de OB en niños y jóvenes ha aumentado considerablemente en las dos últimas décadas y, en la actualidad, son los países del sur de Europa los que expresan las cifras más elevadas, con tasas de sobrecarga ponderal entre el 20% y el 35%, frente al 10%-20% en países nórdicos(1,2). Estudios realizados en Estados Unidos, estiman que la prevalencia de OB en algunos grupos de edad de este colectivo se ha duplicado en relación con las tasas de los años setenta. En la población adolescente americana, se estima un aumento de la tasa del 5%(2).
En la figura 2, se recoge la prevalencia de SP y OB en la población infanto-juvenil (5-17 años) en diferentes países.
Figura 2. Porcentaje de sobrepeso y obesidad en niños de 5-17 años de edad de diferentes países. Fuente: The Organisation for Economic Co-operation and Development (OECD) (2011), Health at a Glance 2011: OECD Indicators, OECD Publishing. doi: 10.1787/health_glance-2011-en.
Etiología. Factores de riesgo
La identificación de factores genéticos y ambientales causantes del disbalance energético servirá para plantear estrategias preventivas.
La etiología de la OB es compleja y multifactorial. Se tendrán en cuenta factores individuales y biológicos (metabólicos y genéticos), así como los conocimientos, actitudes y comportamientos. Las influencias biológicas contribuyen entre un 30-70% en la determinación de la obesidad y las ambientales modulan su manifestación y el grado de OB. También, se considerará el balance energético positivo por una mayor ingesta de alimentos ricos en grasas, pobres en agua y fibra y el incremento del tamaño de las raciones. Igualmente, las causas que originan una disminución del consumo de energía que favorecen la inactividad física y el ocio. El ambiente económico, político y sociocultural facilitará las causas anteriores.
Los factores de riesgo (FR) de obesidad se exponen a continuación:
• Factores genéticos. Diversos estudios han encontrado asociación entre el IMC de los padres y de los hijos a partir de los 3 años. Si uno de los padres es obeso, el riesgo se triplica, si son ambos se multiplica por 15. También se hereda el patrón de distribución de la grasa, de la masa magra y otros FR cardiovascular. Es difícil diferenciar el origen genético y ambiental por la gran influencia de los estilos de vida similares entre padres e hijos.
• Exposición durante el periodo fetal. La hipótesis de Barker establece: que una agresión in útero produce una programación anormal del desarrollo de órganos y aparatos que se manifestará en etapas tardías de la vida(12). Ejemplo: la exposición al tabaquismo durante el embarazo y el sobrepeso en la infancia, se explica por la pérdida de apetito materno por la nicotina y una vasoconstricción y compromiso en la circulación útero-placentaria, además de exposición a mayores niveles de CO2, de esta forma disminuye el aporte de O2 al feto, se produce una afectación de su crecimiento y desarrollo, con impronta metabólica y efectos sobre su salud a corto, medio y largo plazo(10).
• Peso al nacimiento. Se ha observado una asociación positiva entre macrosomia (peso superior a 4 kg al nacimiento) y padecer OB en la infancia y edad adulta(11). También se ha observado una relación entre el bajo peso al nacimiento y el síndrome metabólico, observándose un mayor riesgo para la OB central. Los recién nacidos pequeños para la edad gestacional que ganan rápidamente peso durante los primeros meses de vida, son los que presentan más riesgo de desarrollar OB en la adolescencia tardía(11).
• Alimentación en el primer año de vida. Protección de la Lactancia materna (LM). Los lactantes alimentados con LM tienen menor riesgo de desarrollar OB que los alimentados artificialmente(11) y podría incrementarse con la duración de la LM. Además, son más capaces de autorregular su alimentación que los lactados con fórmula. Los lactantes en los que se introduce alimentación complementaria antes de los 4-6 meses de vida presentan una mayor ganancia ponderal y se asocia con menor duración de LM(11).
• Precocidad del rebote adiposo. En las curvas del IMC se ha identificado un crecimiento en el primer año de vida que decrece posteriormente llegando a valores mínimos entre los 5-6 años, momento en que se produce un nuevo aumento hasta la edad adulta. Esto se ha llamado “rebote adiposo” y cuando se produce precozmente antes de los 5 años de edad, conduce a una elevación rápida del IMC y se asocia con mayor riesgo de OB en la edad adulta(11).
• Etapa de la adolescencia y maduración sexual precoz. La adolescencia es una etapa de riesgo, ya que la probabilidad de que un niño obeso se convierta en adulto obeso aumenta del 20% a los 4 años de edad a un 80% en la adolescencia. Diferentes estudios han observado que la aparición precoz de la menarquía (< o igual a 11 años) incrementa el riesgo de OB en la época adulta.
• Sexo y edad. Diversos estudios han observado una prevalencia de obesidad superior en los varones. En el estudio Enkid, en los varones era del 15,6% y en mujeres del 12,0%, y también para el SP (14,3% vs.10, 5%, respectivamente). Por edades, la OB fue superior de los 6 a los 13 años(2,9).
• Nivel socioeconómico (NSC). El NSC elevado es un FR de OB en los países pobres y en los de transición. En el estudio Enkid(2), la OB fue mayor en niveles socioeconómicos y de instrucción más bajos (15,1 y 15,2%, respectivamente).
• Distribución geográfica. El medio rural parece ser un factor de protección de la OB en los países pobres y de transición nutricional, sin embargo, en estudios en países desarrollados se ha identificado como de riesgo.
• Estilos de vida:
- Tipo de Alimentación: En el estudio Enkid(2), se evidenciaron como factores protectores para la OB, además de la LM durante tres o más meses, el consumo de 4 o más raciones de frutas y verduras al día, un consumo graso menor del 35% del aporte energético total, el fraccionamiento de la ingesta diaria en 3 o más comidas al día y un estilo de vida activo.
Por el contrario, el consumo elevado de productos de bollería, refrescos azucarados y embutidos, un perfil dietético con un 38% o superior de la ingesta energética a partir de las grasas, la ausencia de la ración del desayuno y una baja actividad física, dedicando 3 o más horas al día a ver TV, aumentaba la probabilidad de ser obeso.
- Actividad física. La actividad física moderada se identifica como un factor protector de OB(11). A partir de la Encuesta Nacional de Salud(9) se estimó que los niños pasan una media de 2 horas y media al día viendo la TV, a lo que hay que sumar media hora adicional jugando con el ordenador o videojuegos.
- Sueño. Varios estudios han encontrado relación entre la menor duración del sueño y la OB infantil. En el estudio Enkid(2), la prevalencia de OB fue inferior en el grupo que dormía una media de 10 horas en relación con los que dormían menos de 7 horas. Por otro lado, el 47% de los niños obesos tienen problemas respiratorios del sueño moderados-intensos.
• Sociedad. Influencia de los medios de comunicación, la escuela, el barrio y la ciudad en que se vive. Estos dependen de políticas que afectan a la ordenación del sistema educativo, del mercado de la alimentación y de las condiciones sociosanitarias locales(12).
• Otros. Se investiga el posible papel de la flora microbiana intestinal, toxinas ambientales (“disruptores endocrinos”) y virus.
Clasificación
Dentro de los tipos de obesidad, la más frecuente es la exógena o poligénica, cuya etiología es multifactorial.
1. Obesidad exógena: es la más frecuente de las causas de OB, siendo la etiología multifactorial. La acumulación del exceso de energía en forma de tejido adiposo es debida a la existencia de una inadecuada nutrición, así como una disminución de la actividad física. Estos factores ambientales actuarían sobre una base poligénica que determinarían el desarrollo de un fenotipo obeso.
Se han descubierto unos 52 polimorfismos (variantes alélicas) asociados a rasgos de obesidad. El primero en descubrirse fue el gen FTO, relacionado con patrones de alimentación que conducen a un mayor aporte energético, con un efecto pequeño, pero acumulativo, sobre el IMC(13).
2. Obesidad monogénica: el hipotálamo es un órgano clave en el control del metabolismo energético. Por una parte, es responsable de la sensación de hambre y saciedad y, por tanto, del ingreso energético; y por otra parte, mediante la modulación del sistema nervioso simpático, interviene en la termogénesis adaptativa y, por tanto, en el gasto energético, ambas funciones son controladas por diferentes neuropéptidos. En el núcleo arcuato existen dos estirpes neuronales funcionantes antagónicas; por un lado, el neuropéptido Y que genera estímulos orexígenicos, y por otro la proopiomelanocortina (POMC), encargada de señales anorexigénicas. La leptina es una hormona derivada de los adipocitos cuyos niveles circulantes se correlacionan estrechamente con la cantidad de tejido graso corporal. La leptina ejerce su efecto homeostático, en parte actuando sobre hipotálamo generando POMC.
En la actualidad, se conocen, al menos, 20 enfermedades monogénicas, cuya manifestación fenotípica más importante es la instauración de una OB de comienzo temprano, por mutaciones en los genes de: leptina, receptor de leptina, POMC, receptor 4 de la melanocortina (MC4R) y prohormona convertasa 1 (PCSK1).
La deficiencia congénita de leptina (OMIM: 164160) genera OB de inicio temprano (durante los tres primeros meses de vida) junto a un hipogonadismo hipogonadotropo(14).
Las mutaciones en el receptor de leptina (OMIM: 164160) y de POMC (OMIM:176830) presentan OB de inicio antes de los 6 meses de vida con un peso al nacer normal. Las primeras, asocian: deficiencia de TSH, hormona de crecimiento e hipogonadismo hipogonadotropo(14).
Las mutaciones en el MC4R (OMIM: 155541) suponen la causa más frecuente de OB monogénica (2,6%). La mayoría de las mutaciones son heterocigotas, heredadas de forma dominante. Clínicamente cursan con OB e hiperfagia(15).
Las mutaciones en PCSK1 asocian: OB de inicio temprano, diarrea, homeostasis glucídica anormal, hipogonadismo hipogonadotropo y niveles altos de proinsulina y POMC(15).
3. Obesidad asociada a síndromes polimalformativos:entre los múltiples síndromes dismorfológicos pediátricos en los que se puede observar el desarrollo de un mayor o menor grado de OB a lo largo de su curso evolutivo, cabe destacar:
- Síndrome de Prader-Willi (OMIM: 176270):
La secuencia clínica que presentan los pacientes afectos de este síndrome puede comenzar ya a lo largo del periodo fetal, con la presencia de polihidramnios y la escasez, en número e intensidad, de los movimientos fetales. Tras el parto, destaca la intensa hipotonía que presentan estos pacientes y que llega a causarles dificultades para la succión, comprometiendo su ganancia ponderal durante los primeros meses de vida; y desde los 12 a 18 meses, se desarrolla una hiperfagia incontrolable(16). Son típicos, determinados rasgos fenotípicos como: ojos de forma “almendrada”, hipogonadismo hipogonadotropo, retraso mental e hipotonía muscular.
Se desconoce el mecanismo por el que se ocasiona la OB en estos pacientes, debido a la falta de expresión de copias paternas de genes improntadores en la región 15q11.2q13, fundamentalmente del gen SNRPN (small nuclear ribonucleoproten polypeptide N) (OMIM:182279) y también del gen NDN (OMIM:602117). Puede estar causado por delecciones en el cromosoma paterno, disomía uniparental materna o mutaciones que afecten a la impronta de la región.
- Síndrome de Alstrom (OMIM: 203800):
Los pacientes encuadrados en esta entidad nosológica comparten con aquellos afectos del síndrome de Bardet-Biedl: la presencia de defectos neuroftalmológicos, la presencia de OB y la instauración frecuente de diabetes mellitus tipo 2 (en la 2ª o 3ª década de la vida). Sin embargo, se distinguen por la ausencia de retraso mental y de las alteraciones digitales; así como, por la existencia del rasgo más distintivo de este síndrome, como es la presencia de miocardiopatía de inicio a muy temprana edad(17). En estos pacientes, es frecuente la aparición, a largo plazo, de alteraciones metabólicas, tales como: la hiperuricemia y la hipertrigliceridemia.
El gen considerado responsable de esta entidad se denomina ALMS1(2p13.1). (OMIM: 203800).
- Síndrome de Bardet-Biedl (OMIM: 209900):
Las características cardinales de este síndrome son: la existencia, prácticamente constante de retraso mental (más acusado en aptitudes verbales que manipulativas), alteraciones digitales (sobre todo polidactilia postaxial), distrofia retiniana y alteraciones renales, tanto funcionales como anatómicas. En estos pacientes, la OB (más acusada en el subtipo 4 y mucho menos en el subtipo 2), comienza a instaurarse en torno a los 2 o 3 años de vida.
Hay que señalar, que el síndrome de Laurence-Moon (OMIM: 245800), con el que compartió denominación desde el año 1925, se diferencia de este por la ausencia de alteraciones digitales y la presencia, prácticamente constante de paraplejia espástica y, de la característicamente descrita, retinitis pigmentaria.
En la actualidad, se conocen varios subtipos diferentes de este síndrome (asociados a mutaciones en diferentes localizaciones genéticas), algunos de los cuales se presentan debido a la asociación de mutaciones en diferentes locus cromosómicos, por lo que se les ha definido como ejemplo de una posible herencia trialélica(18).
En la tabla I, pueden verse la semiología clínica que indica que la obesidad puede ser el resultado de un síndrome genético.
4. Obesidad secundaria: las lesiones del SNC que afectan a la región hipotalámica pueden cursar con OB, ya sean secundarias a traumatismos, a tumores o a su tratamiento (gliomas, hamartomas, disgerminomas), a secuelas de infecciones o a cierto grado de hipertensión endocraneal crónica compensada (portadores de válvulas de derivación en las hidrocefalias).
Menos del 1% de los casos de OB infantojuvenil se deberán a etiología endocrinológica. Estas endocrinopatías pueden ser: el hipercortisolismo primario (síndrome de Cushing) o secundario al uso terapéutico de glucocorticoides, el hipotiroidismo, el déficit de hormona de crecimiento, el pseudohipoparatiroidismo tipo 1a y el hiperinsulinismo.
Determinados fármacos (antipsicóticos, antiepilépticos y esteroides) pueden producir OB.
Diagnóstico
El diagnóstico de la OB se realiza mediante una historia clínica detallada, investigando los antecedentes personales y familiares, encuesta nutricional con hábitos dietéticos, además de la exploración física y determinadas pruebas complementarias según la situación del paciente.
Historia clínica
Ante un paciente con sospecha de OB, nos interesa realizar una historia clínica detallada y conocer los antecedentes personales, tales como: la edad gestacional, el peso y la longitud al nacimiento, el tipo de lactancia, o la edad de introducción de los alimentos sólidos, así como conocer la edad del inicio de la ganancia ponderal y el grado de actividad física. Es importante conocer la distribución de las comidas a lo largo del día, el número de comidas fuera de las comidas principales y la presencia o no de ingesta compulsiva. Asimismo, en las adolescentes, se debe investigar la presencia de oligomenorrea o alteraciones del ciclo menstrual. El estilo de vida sedentario puede valorarse por parámetros, como las horas de ver televisión o jugando con ordenadores, fácilmente registrados con cuestionarios sencillos.
Entre los antecedentes familiares, es importante conocer la etnia y país de origen, el peso y el IMC de los padres y hermanos y los hábitos dietéticos de la familia, utilizando principalmente encuestas nutricionales. Se debe valorar la historia familiar de hipertensión arterial, dislipemia, enfermedad cardiovascular, diabetes mellitus tipo 2 y OB de distribución central.
Examen físico
• Estudio auxológico: peso, talla, índice de masa corporal (IMC), perímetro de cintura (IDF 2004)
(Fig. 3).
Figura 3. Medida del perímetro de la cintura.
• Registro de la tensión arterial.
• Distribución de la grasa: obesidad abdominal.
• Rasgos dismórficos faciales: implantación del cabello y de los pabellones auriculares, paladar ojival o hendido, aplanamiento de la raíz nasal.
• Piel: acantosis nigricans, estrías, xantomas, hirsutismo.
• Desarrollo psicomotor.
• Presencia de alteraciones ortopédicas compensatorias (genu valgo), alteraciones de la marcha.
Pruebas complementarias
• Hemograma y bioquímica completa con transaminasas.
• Lipidograma: colesterol total, triglicéridos, C-HDL y C-LDL.
• Función tiroidea: T4 libre y TSH.
• Glucemia e insulina basal (cálculo de índice de sensibilidad para la insulina: HOMA: [glucosa (mmol) x insulina (microUI/ml)/22,5].
• Se debe realizar una sobrecarga oral de glucosa (SOG):
- Ante una obesidad moderada-grave.
- Si los niveles de glucemia son > 100 mg/dl.
- Si los niveles de insulina son > 15 microUI/ml.
- Antecedentes familiares de DM2 en 1º y 2º grado, etnia (hispana y afroamericana), hipertensión arterial, dislipemia y signos de resistencia a la insulina (acantosis nigricans, síndrome de ovario poliquístico).
Según la American Diabetes Association (ADA) 2015, se considera:
- Alteración de la glucemia en ayunas (AGA), cuando los niveles son > 100 mg/dl.
- Intolerancia a los hidratos de carbono: glucemia a las 2 horas de la SOG > 140 g/dl.
- Diabetes mellitus: glucemia en ayunas > 126 mg/dl o a las 2 horas de la SOG > 200 mg/dl, repetidas en dos ocasiones.
- Niveles de hemoglobina glicosilada como marcador de prediabetes: 5,7-6,4%, y diabetes > 6,5%.
• Rx de mano-muñeca izquierda: en general, los niños obesos presentan una edad ósea acelerada respecto a su edad cronológica, pero adecuada a la edad/talla del niño.
• El estudio de las concentraciones de adipoquinas y el estudio de las mutaciones monogénicas no están indicadas de forma sistemática
Comorbilidad asociada
Las consecuencias para la salud de la OB infantil incluyen numerosos problemas médicos que pueden verse en la tabla II. Además del riesgo de continuar padeciendo OB en la edad adulta (más riesgo a más edad y, especialmente, si se asocia con OB en los progenitores, el llamado fenómeno tracking), conviene tener presente que muchas de las complicaciones no se ponen en evidencia hasta pasadas algunas décadas.
Los factores nutricionales y los estilos de vida sedentarios, además de las enfermedades cardiovasculares, se relacionan con diabetes, tumores, osteoporosis y sus complicaciones.
Probablemente, los trastornos más frecuentes asociados a la OB infantil son los de tipo psicológico como: disminución de la autoestima, estigmatización y fracaso escolar. Ello les conduce a dificultades en: las relaciones amistosas entre pares, alteraciones del comportamiento, síntomas de depresión y ansiedad. Es difícil saber si estos trastornos psicológicos preceden a la OB o son consecuencia. Conocer esta diferencia es fundamental para planificar el tratamiento.
La OB y el SP pueden ser condiciones preexistentes, en algunos casos, de jóvenes que desarrollan trastornos del comportamiento alimentario, tales como: comer compulsivamente o hacer dieta de forma crónica. Aunque no se han encontrado evidencias que apoyen una relación estrecha entre bulimia o anorexia y OB, parece que hay riesgo de que una insistencia exclusiva en emplear la dieta como forma de mantener el peso y la imagen corporal, pueda contribuir al desarrollo de anorexia en niños con factores de riesgo psicológicos.
La OB se asocia con niveles de tensión arterial y triglicéridos elevados, niveles de C-HDL bajos, resistencia a la insulina y alteraciones vasculares e inflamatorias.
Hiperinsulinismo y resistencia a la insulina
En presencia de resistencia a la insulina, la célula beta pancreática incrementará la secreción de insulina y se producirá hiperinsulinismo. Si consigue compensar la resistencia insulínica, se alcanzará la normoglucemia, pero con los años este mecanismo compensador irá fallando y se producirá la intolerancia a los hidratos de carbono y la diabetes tipo 2. La hiperglucemia traerá como consecuencia glucotoxicidad con incremento del potencial aterogénico(19).
La determinación de la glucemia y la insulina en ayunas son necesarios para identificar las alteraciones de la homeostasis de la glucemia y reflejan fundamentalmente la secreción de insulina y la sensibilidad hepática y periférica. Además, tienen una alta especificidad y sensibilidad en identificar sujetos con resistencia a la insulina. La obesidad es el mayor factor de riesgo para el desarrollo de diabetes mellitus tipo 2 en los adolescentes(19).
Síndrome metabólico (SM)
Es el conjunto de alteraciones metabólicas y cardiovasculares que están relacionadas con la resistencia a la insulina y la OB abdominal, ejes centrales del síndrome que se desarrollaría en individuos metabólicamente susceptibles. Por ello y debido a que en las últimas décadas ha aumentado de forma importante su prevalencia, puede considerarse este síndrome un problema de salud pública de gran importancia, tanto en los países desarrollados como en algunos en transición económica y nutricional. Será abordado en el siguiente capítulo.
La OB infantojuvenil tiene asociados, además, unos costes económicos importantes. En España, representó el 7% del gasto sanitario en 2007. Padecer OB disminuye las expectativas de vida y aumenta el tiempo de estancia hospitalaria por cualquier proceso y en casi todas las edades.
Abordaje terapéutico
La base fundamental del tratamiento es la instauración de un programa multidisciplinar a largo plazo que asocie: educación nutricional, aumento de la actividad física y modificaciones de la conducta de la población.
En la actualidad, hay pocos ensayos aleatorios a largo plazo para poder determinar si las técnicas para prevenir y tratar la obesidad son eficaces. Las recomendaciones están basadas en consensos de expertos con experiencia clínica, observación de conductas que se asocian a la OB y evidencias científicas a corto plazo. Incluyen: medir el IMC y ver su evolución; evitar los factores de riesgo relacionados (intervenciones tempranas); utilizar intervenciones clínicas breves (mensajes educativos, centrados en el niño y la familia); establecer cambios a largo plazo centrados en la conducta que se asocia al riesgo de OB, en lugar de confiar exclusivamente en dietas y planes de ejercicio que tienden a establecer metas a corto plazo; e implementar un enfoque gradual en el control de peso para hacer frente a la OB en las diferentes edades y niveles de gravedad.
Dada la complejidad y variedad de los factores etiológicos involucrados en la génesis y mantenimiento de la OB y a las dificultades halladas hasta la fecha para lograr enfoques terapéuticos eficaces y resultados mantenidos, las recomendaciones propuestas se exponen a continuación.
En primer lugar, se debe realizar un correcto diagnóstico y asegurarse de que tanto el paciente como su familia desean iniciar el tratamiento, investigando la dinámica familiar. Se debe seguir el modelo de motivación al cambio de Prochaska y Diclemente(20). Según dicho modelo, las intervenciones se adaptarán en función del estadio en que se encuentre el paciente y la familia e incluyen 5 fases: Precontemplación: el individuo no considera la posibilidad del cambio. Contemplación: está considerando la posibilidad de cambiar, está planificando y comprometiéndose con el cambio. Acción: está realizando la conducta del cambio. Mantenimiento: sostener a largo plazo el cambio. El ciclo incluye la posibilidad de recaída, la que siempre debe ser anticipada para diseñar con el paciente como se enfrentará a ella.
La base del tratamiento de la OB es la instauración de un programa multidisciplinar a largo plazo que asocie: reorganización de los hábitos alimentarios, realización de actividad física y tratamiento conductual.
Reorganización de los hábitos alimentarios
Tiene como objetivo mejorar la sensibilidad a la insulina y prevenir o corregir las alteraciones metabólicas y cardiovasculares asociadas. Es importante corregir los errores como: la elevada ingesta de grasa a expensas de la disminución de los carbohidratos, la distribución de energía a lo largo del día, la selección de los menús y las técnicas culinarias. Si el paciente no responde a la corrección de los errores, se realizará una intervención nutricional.
En cuanto a la composición de la dieta, se aconseja una dieta equilibrada en la que el porcentaje de calorías aportadas por cada uno de los principios inmediatos sea: 50% en forma de hidratos de carbono, 30% de grasas y 20% de proteínas. Las proteínas deben ser de alto valor biológico. La grasa aportará ácidos grasos esenciales y vitaminas liposolubles, y favorecerá la sensación de saciedad. Asimismo, los alimentos con bajo índice glucémico ayudarán a controlar la sensibilidad a la insulina y las alteraciones lipídicas, así como asegurar un aporte extra de fibra que produce mayor sensación de saciedad y que disminuye la ingesta energética. Respecto a la ingesta de líquidos, la bebida habitual será la leche (requerimientos diarios) y el agua, evitando las bebidas azucaradas.
En los niños prepúberes, en general, se deben recomendar dietas normocalóricas, mientras se van desarrollando. No se recomiendan dietas hipocalóricas en menores de 2 años de edad. En OB moderada, será necesario una intervención nutricional con una dieta hipocalórica, calculada en función de la edad cronológica, no del peso. En obesidades graves, se utilizará dietas hipocalóricas llegando a restringir hasta un 20-25% de las calorías recomendadas al niño de la misma edad y sexo. Se distribuirá el total de las calorías en tres comidas principales y dos secundarias (media mañana y merienda), evitando periodos de ayuno prolongado, y evitando una ingesta rápida de comida, favoreciendo así la sensación de saciedad.
Existe otro grupo de dietas no aconsejable, tales como dietas muy restrictivas, sustitución por componentes líquidos o purificados de proteínas o dietas heterodoxas, donde no se aconseja su empleo en la edad pediátrica, debido a las posibles deficiencias nutricionales y complicaciones médicas asociadas.
Incremento de la actividad física
El ejercicio aumenta el gasto energético, mejora la sensibilidad a la insulina y disminuye la lipogénesis. Es útil para mantener la pérdida de peso y debe ser individualizado. Hay que estimular la realización de paseos diarios en niños que no tengan hábitos deportivos (ir al colegio andando o subir escaleras). Animarlos a que participen en deportes escolares y actividades deportivas durante el fin de semana. Es necesario que el ejercicio sea aceptado y forme parte de la vida diaria. Hay que evitar el sedentarismo, así como el uso de videojuegos y ver televisión demasiadas horas, en las que los niños tienen un consumo energético reducido y además, toman alimentos hipercalóricos. Asimismo, se aconseja la retirada de la TV y/o ordenador de las habitaciones de los niños y adolescentes, y limitar el tiempo dedicado a estos juegos.
Tratamiento conductual
Tanto el paciente como la familia deben tomar conciencia de las conductas que han conducido al exceso de peso, y deben ser capaces de introducir cambios en la alimentación y en los estilos de vida a medio y largo plazo. Se aconseja diseñar un plan de vida diario para toda la familia.
Los padres deberán aprender a controlar el entorno del hogar: tipos de alimentos que se compran, cómo se preparan, cómo se puede controlar el tiempo dedicado a la televisión, entre otros. El paciente irá aprendiendo a descubrir las situaciones, pensamientos o sensaciones que actúan de desencadenantes, incitándole a comer y también cómo se siente cuando cumple los objetivos. Se le darán pautas de comer sentado, masticar despacio, y no utilizar la comida para recompensas…
Se tendrán en cuenta los aspectos emocionales. Se evitaran las críticas o la estigmatización. Los profesionales deben utilizar la empatía y el estímulo. Con frecuencia son las sensaciones de tristeza o baja autoestima las que actúan como desencadenantes para ingerir alimentos. Se debe favorecer la imagen positiva de la alimentación, del ejercicio y del propio cuerpo ayudando a construir y reforzar la autoestima.
Es necesario proporcionar instrumentos para afrontar las situaciones estresantes o desencadenantes, mediante el entrenamiento en habilidades específicas para manejar el estrés, autoinstrucciones y formulación de objetivos. Se recomienda el apoyo psicológico con terapia conductual o cognitivo-conductual en menores y adolescentes (evidencia B). Hay que esperar recaídas, para las que se deben tener soluciones.
La entrevista motivacional, permite ayudar al paciente a descubrir sus deseos, emociones y motivaciones. Al centrarse en el paciente, permite que vaya descubriendo por sí mismo las barreras y dificultades, y lograr objetivos poco a poco, diseñando nuevas estrategias de superación adaptadas a cada situación.
Frente a la intervención paciente-profesional que con el tiempo aumenta el riesgo de fracaso terapéutico por desgaste de ambos, se perfila el tratamiento grupal que, aunque tienen algunas dificultades (perfiles de los profesionales a incluir, los contenidos adecuados a cada edad, el número de sesiones, el tiempo de seguimiento, etc.), parece que ofrece buenas expectativas.
Tratamiento farmacológico
La indicación del tratamiento farmacológico de la OB no debe utilizarse como terapia aislada, sino de forma complementaria a las terapias básicas de reeducación alimentaria, actividad física y tratamiento conductual.
El Comité de Expertos para la Prevención y Tratamiento de la Obesidad Infantil de la Academia Americana de Pediatría plantea su uso en la adolescencia, cuando no se hayan alcanzado los objetivos de pérdida de peso con los cambios en los estilos de vida y presenten comorbilidad severa.
Actualmente, solo está comercializado un fármaco con indicación aprobada para el tratamiento de la OB, el Orlistat(21). La sibutramina fue retirada del mercado en el 2010, por aumento del riesgo cardiovascular. La metformina no está indicada en la obesidad, pero sí en el tratamiento diabetes tipo 2 y en la alteración de la glucemia basal o la alteración de la tolerancia a la glucosa en pacientes con un IMC >35 kg/m2.
El Orlistat inhibe la acción de la lipasa pancreática y gástrica, lo que disminuye la absorción de grasa hasta en un 30%, con un perfil de seguridad favorable a pesar de efectos secundarios como: flatulencia, deposiciones grasas/oleosas y déficit de vitaminas liposolubles, en hasta un 50% de los pacientes(21). Es más eficaz cuando se asocia a control dietético y aumento de la actividad física. Su uso está permitido por la FDA a partir de los 12 años. El ensayo clínico con mayor número de sujetos y duración de seguimiento fue realizado en el año 2005 con Orlistat en una población de 539 adolescentes obesos durante 54 semanas, demostró una reducción significativa en el IMC y del perímetro de cintura(21). Es posible que mejore los FR cardiovasculares(22).
Tratamientos en fase de desarrollo
Actualmente, hay numerosos ensayos clínicos dirigidos a establecer la eficacia y la seguridad de diferentes sustancias, fármacos y hormonas neuroentéricas que participan de manera directa o indirecta en la regulación del peso corporal. La lorcaserina, fentermina, fentermina/topiramato y naltrexona/bupropion de liberación sostenida, son cuatro terapias adicionales para la pérdida de peso aprobadas para el manejo de OB en adultos, pero sin estudios en población adolescente(22).
La lorcaserina es un agonista del receptor de serotonina 5-HT2c que conduce a pérdida ponderal al aumentar la saciedad y disminuir el consumo de alimentos, posee beneficios sobre los FR cardiovasculares.
La fentermina es un simpatomimético que disminuye el apetito, estando aprobada por la FDA para duración breve en adultos, estando asociada a efectos adversos cardiovasculares. Su combinación con topiramato, también conduce a pérdida de peso significativa, así como la combinación del antagonista de opioides (Naltrexone) y el antidepresivo bupropion.
Otras medicaciones indicadas para otras condiciones médicas –distintas a la OB–, se ha visto que resultan efectivas para la pérdida de peso, como el bupropion, metformina, análogos de GLP-1 (glucagon-like-peptide-1), análogos de amilina y el topiramato.
Tratamiento quirúrgico
La Asociación Americana de Cirugía Pediátrica ha realizado unas recomendaciones para la práctica de Cirugía Bariátrica en adolescentes con OB mórbida (Tabla III). La sociedad Americana de Cirugía Bariátrica y Metabólica (ASMBS), recientemente, ha publicado la guía de práctica clínica para cirugía bariátrica pediátrica(23), recomendando un equipo multidisciplinar, incluyendo: cirujano bariátrico, pediatra especializado en obesidad, nutricionista, especialista en salud mental, especialista en la fisiología del ejercicio y un coordinador de salud, para evaluar el tratamiento óptimo para aquel niño candidato a cirugía bariátrica, basándose en la presencia de comorbilidades y fallo de otras intervenciones terapéuticas.
Las técnicas quirúrgicas más empleadas a nivel mundial en adolescentes y adultos son: el bypass gástrico mediante Y de Roux y la banda gástrica ajustable.
En un metaanálisis sobre adolescentes OB, la media de reducción de IMC fue de 17,8 a 22,3 kg/m2 con el bypass gástrico mediante Y de Roux, entre 1 a 6 años de seguimiento(24); mientras que fue de 10,6 to 13,7 kg/m2 en aquellos sometidos a banda gástrica, en estudios de 1-3 años de seguimiento. La banda gástrica mediante abordaje por laparoscopia, es una técnica restrictiva con colocación de una banda de silicona que circunda la parte proximal del estómago.
La gastrectomía en banda está en auge en adultos y adolescentes. Es una técnica menos compleja que la Y de Roux y con menor riesgo de déficit de micronutrientes y con disminución del IMC entre 32-37% en estudios en adolescentes(25).
La implantación endoscópica de un balón intragástrico por periodos máximos de 6 meses, produce una reducción ponderal leve y sus efectos secundarios más importantes son náuseas, vómitos, así como perforación o migración intestinal.
Recientemente, en 2015, la Canadian Task Force on Preventive Health Care (CTFPH)(26) ha dado una serie de recomendaciones con evidencia científica, para la vigilancia del crecimiento y la prevención y gestión del sobrepeso y la obesidad en los niños y adolescentes en AP. Recomienda intervenciones conductuales entre los 2 y 17 años y no recomienda ofrecer intervenciones farmacológicas o referir a los pacientes para intervenciones quirúrgicas, debido a la falta de datos que muestren efectividad y por los posibles daños potenciales. Aunque estadísticamente significativo, los beneficios clínicos de las intervenciones conductuales son pequeños y son necesarios datos a largo plazo para determinar si los beneficios se mantienen en el tiempo. En la tabla IV, pueden verse las recomendaciones sobre prevención y tratamiento del SP y OB según diferentes guías de práctica clínica.
Prevención
El mejor tratamiento de la obesidad infantil es la prevención, ya que es muy difícil tratar la obesidad una vez establecida.
Para luchar contra el SP y la OB infantil es fundamental la prevención primaria o universal, ya que es muy difícil tratar la enfermedad una vez establecida. Debe ser parte de una política nacional de salud pública para mejorar la alimentación y el ejercicio físico de la comunidad, disminuyendo el riesgo de enfermedades crónicas, mejorando la salud y la calidad de vida.
La intervención se basa en realizar consejos educativos a toda la población con especial enfoque hacia las familias, la población infantil y los distintos ámbitos sociales que les rodean: guardería, escuela, centros de salud, comunidad, ámbito legislativo y medios de comunicación(27) (Tabla V).
Los consejos forman parte del estilo de vida sana, que se adaptará a la edad del paciente, y las características socioculturales. El objetivo es promover y modelar actitudes positivas hacia la alimentación y la actividad física, sin centrarse en el peso corporal para evitar efectos adversos como los trastornos de la alimentación. Se realizará en los controles de salud programados y también de forma oportunista.
Se iniciará en la 1ª visita, con la promoción y apoyo a la lactancia materna. También se realizará intervención prenatal sobre factores relacionados con el peso elevado al nacimiento. El peso pregestacional y la ganancia de peso neta en el embarazo son las principales fuentes de información sobre las reservas nutricionales disponibles y el aporte nutritivo al feto(11). Se evitará culpabilizar y estigmatizar al paciente y las familias.
La prevención secundaria (cribado) se centrará en los niños con factores de riesgo para el SP y la OB. Aquí, es esencial la actuación médica identificando y dirigiendo a estos pacientes.
Aunque no existe suficiente evidencia para recomendar el cribado anual(6), dada la importancia del problema a prevenir, sí se recomienda monitorizar de forma periódica el peso, la talla y el IMC, que deben quedar reflejados no solo en la historia clínica, sino sobre las gráficas de crecimiento, para observar la tendencia. Además, hay suficiente evidencia que relaciona las técnicas de cribado con la detección de problemas de salud(6).
Una vez detectados los niños con FR, se debe evaluar: la alimentación, los conocimientos y actitudes hacia esta, la actividad física, así como los estilos de vida. El consejo se adaptará a la edad del paciente, aprovechando las actitudes y puntos fuertes(6).
La OMS y otros organismos, han llamado la atención sobre la necesidad urgente de poner en marcha planes de acción. En 2004, aprobó la Estrategia Global sobre Dieta y Actividad Física e instando a los estados miembros a la implantación de planes nacionales de actuación. Las estrategias de prevención frente a la OB infantil deben realizarse, como ya se ha comentado, a todos los niveles(27): familia, colegio, profesionales de la salud, industria, medios de comunicación y gobierno. En nuestro país, desde 2004, el Ministerio de Sanidad y Consumo lleva a cabo la estrategia NAOS (Nutrición, Actividad Física y Obesidad) con un programa específico dirigido de manera prioritaria a la intervención en el medio escolar, como es el Programa PERSEO (Programa Educativo de Referencia para la Salud, Ejercicio Físico y contra la Obesidad) realizado en diferentes provincias españolas entre los 6-10 años con resultados muy favorables.
Niño@s en movimiento es un programa multidisciplinario dirigido a niños de 7-12 años de edad con SP / OB y a su entorno familiar. Centra su atención en la salud general del niño, y no solo en el peso y la alimentación. También utiliza técnicas cognitivo-conductuales y afectivas. El estudio Evasyon es un programa educacional (nutricional y de actividad física) multidisciplinar, útil, dirigido específicamente a adolescentes con SP y OB, a partir de los resultados obtenidos del estudio AVENA. El programa Thao es un programa piloto nacional de prevención de la OB infantil que se realiza en el ámbito de los municipios, con acciones continuadas durante 4 años desde 2007. Dirigido a los niños escolarizados de 0 hasta 12 años, implicando a todos los actores en contacto con la población infantil.
Otras medidas adoptadas en nuestro país, incluyen el código de autorregulación de la publicidad de alimentos y bebidas (PAOS) y cambios en el etiquetado de los alimentos e información a los consumidores. El código PAOS pretendía proteger a los menores de 12 años de la presión excesiva de la publicidad de alimentos y bebidas, y ha sido muy positivo durante estos años también para garantizar el control y aplicación de las normas. Se revisó en 2013 para adaptar la publicidad en internet en menores de 15 años.
A nivel internacional, destacan: el proyecto HELENA (Healthy Lifestyle in Europe by Nutrition in Adolescence) y el proyecto HBSC (Health Behaviour in School-aged Children) o estudio sobre las conductas saludables de jóvenes escolarizados que se realiza cada 4 años; es un proyecto auspiciado por la OMS en el que participan más de 40 países occidentales.
Actividades del pediatra de Atención Primaria
El pediatra de AP tiene un papel esencial en la detección precoz, tanto del SP y OB como de los factores y poblaciones de riesgo, el tratamiento y la instauración de medidas de promoción y prevención en los diferentes ámbitos familiar, escolar y social.
La OB constituye un reto para los pediatras por: la alta prevalencia, la poca sensibilidad por parte de las familias hacia la enfermedad, la dificultad para conseguir cambiar los hábitos de forma permanente, la poca formación en técnicas de consejo y entrevista motivacional y la necesidad de controles y seguimiento a largo plazo, entre otras. Las actividades a realizar están basadas en las recomendaciones de las diferentes Guías de Práctica Clínica(6,26).
1. Detección precoz de poblaciones y factores de riesgo. Investigar factores personales: peso al nacer (elevado o bajo para la edad gestacional), ausencia de LM y rapidez en la ganancia de peso durante el primer año y el rebote adiposo precoz. Los periodos críticos para el desarrollo de OB en la edad pediátrica son: el primer año, antes de los 6 años y la adolescencia. Igualmente, los antecedentes familiares.
2. Promover y favorecer la LM. Se hará de forma general, con mensajes claros sobre su superioridad. Se propondrán alternativas al destete: en caso de enfermedad de la madre o el hijo, ingesta de fármacos, cirugía o el retorno de la madre al trabajo. La duración de la LM debe ser la que decida la familia. Se recomienda LM exclusiva los 6 primeros meses por sus grandes beneficios(6). Además de las curvas de crecimiento del estudio español, se dispone de las curvas de crecimiento de la OMS, basadas en lactantes amamantados. Se tendrá presente que la normalidad del peso es muy amplia y que los percentiles son descriptores estadísticos, y no indicadores de salud.
3. Favorecer una correcta alimentación en las diferentes edades. Respetando los mecanismos de saciedad del lactante, evitando pautas rígidas tanto en la LM como con fórmula artificial. La correcta introducción de la alimentación complementaria después de los 4 meses, adaptándola a la maduración psicomotriz del niño y favoreciendo las comidas tradicionales sobre las industriales. No se añadirá al biberón miel ni azúcar. La alimentación será equilibrada y variada, evitándose la sobrealimentación. El tamaño de las raciones se adaptará a la edad del niño. Se explicará a las familias que la velocidad de crecimiento y las necesidades nutricionales disminuyen a partir de los 18-24 meses. La alimentación del preescolar, escolar y adolescente puede verse en el nº 4 (mayo) de PI.
4. Evitar conductas que favorezcan una ganancia excesiva de peso. Como dedicar más de 2 horas/día a cualquier tipo de pantalla (con la TV se consume más cantidad y se asocia la influencia de los anuncios). Evitar comidas/bebidas con alto contenido en azúcares o grasas, picoteos, saltarse comidas o comidas rápidas, entre otras.
5. Recomendar conductas protectoras de una ganancia excesiva de peso. Alimentación saludable (pirámide nutricional) y comer en familia, incremento de la actividad diaria (juegos activos, usar escaleras, bici, tareas del hogar, caminar al colegio…) y una hora de actividad física vigorosa al día.
6. Diagnóstico de SP, OB, así como de las comorbilidades asociadas.
7. Comunicación al paciente y a la familia. Es importante, la forma de comunicar el diagnóstico al paciente y a la familia para el seguimiento y colaboración posterior. Expresiones negativas o estigmatizantes desencadenarán rechazo, mientras que una aproximación sensible con empatía, explorando conocimientos, actitudes y prácticas facilitará la colaboración.
Detectar los puntos fuertes o conductas saludables que servirán de apoyo para iniciar los cambios, así como las dinámicas familiares, estilos educativos y factores psicopatológicos que pueden ser el origen de la OB (ansiedad, depresión).
8. Tratamiento de la obesidad y seguimiento. La familia debe colaborar siempre, para no provocar rechazo. Esta llevará el peso del cumplimiento en los menores de 5 años. Entre los 5-10 años se le dará cierta responsabilidad vigilada y controlada al paciente. En la adolescencia, la familia tiene poca influencia y es el propio paciente el que debe controlarse.
9. Colaborar con otros profesionales, familias, escuelas y otros agentes sociales en actividades de promoción y prevención.
10. Derivar a la atención especializada. Si se asocian comorbilidades, sobre todo, si son del área de salud mental, obesidades extremas y por debajo de los 2 años, y si hay necesidad de intervención farmacológica o quirúrgica (Tabla VI).
Bibliografía
Los asteriscos reflejan el interés del artículo a juicio del autor.
1.** Speiser PW, Rudolf MC, Anhalt H, Camacho-Hubner C, Chiarelli F, Eliakim A, et al. Consensus statement: Childhood obesity. J Clin Endocrinol Metab. 2005; 90: 1871-87.
2.*** Serra Majem L, Ribas L, Aranceta J, Pérez C, Saavedra P. Epidemiología de la obesidad infantil y juvenil en España. Resultados del estudio enKid (1998-2000). En: Serra Majem L, Aranceta Bartrina J (eds.). Obesidad infantil y juvenil. Estudio enKid. Barcelona: Masson, S.A.; 2001. p. 81-108.
3.** Rosenbaum M. Special Considerations Relative to Pediatric Obesity. Endotext [Internet]. www.endotext.org. Última actualización: 8 Abril, 2013.
4.** Cali AM, Caprio S. Obesity in children and adolescents. J Clin Endocrinol Metab. 2008; 93(11 Suppl 1): S31-6.
5.*** Cole T, Bellizi M, Flegal K, Dietz WH. Establishing a standard definition for child overweight and obesity worldwide: international survey. BMJ 2000; 320: 1240-43.
6.*** Grupo de trabajo de la guía sobre la prevención y el tratamiento de la obesidad infantojuvenil. Centro Cochrane Iberoamericano, coordinador. Guía de práctica clínica sobre la prevención y el tratamiento de la obesidad infantojuvenil. Madrid: Plan de Calidad para el Sistema Nacional de Salud del Ministerio de Sanidad y Política Social. Agència d´Avaluació de Tecnología i Recerca Mèdiques; 2009. Guía de práctica clínica: AATRM N.º 2007/25.
7.** Moreno LA, Mesana MI, Fleta J, Ruiz JR, González-Cross M, Sarria A et al. Overweight, obesity and body fat composition in spanish adolescents. The AVENA Study. Ann Nutr Metab 2005; 49: 71-6.
8.** Carrascosa A, Fernández JM, Fernández C, Ferrández-Longás A, López-Siguero JP, Sánchez E, et al.; Grupo Colaborador Español. Spanish cross-sectional growth study 2008. Part II. Height, weight and body mass index values from birth to adulthood. An Pediatr (Barc). 2008; 68: 552-69.
9.* Sánchez-Cruz JJ, Jiménez-Moleo JJ, Fernández-Quesada F, Sánchez MJ. Prevalencia de obesidad infantil y juvenil en España en 2012. Rev Esp Cardiol. 2013; 66(5): 371-76.
10.** Rankinen T, Zuberi A, Chagnon YC, Weisnagel SJ, Argyropoulos G, Walls B, et al. The human obesity gene map: The 2005 update. Obesity. 2006; 14: 529-644.
11.** Lama More RA, Alonso Franch A, Gil-Campos M, Leis Trabazo R, Martínez Suárez V, et al., y Comité de Nutrición de la AEP Obesidad Infantil. Recomendaciones del Comité de Nutrición de la Asociación Española de Pediatría Parte I. Prevención. Detección precoz. Papel del pediatra. An Pediatr (Barc). 2006; 65: 607-15.
12.* Canadian Institute for Health Information. Obesity in Canada. Identifying Policy Priorities. 2003: 23-6. En: https://secure.cihi.ca/free…/CPHI_proceed_e.pdf.
13.** Kissileff H, Thornton M, Torres M, Pavlovich K, Leibel R, Rosenbaum M. Maintenance of reduced body weight in humans is associated with leptin-reversible declines in satiation. Amer J Clin Nutr. 2012; 95: 309-17.
14.** Farooqi IS, Wangensteen T, Collins S, Kimber W, Matarese G, Keogh JM, et al. Clinical and molecular genetic spectrum of congenital deficiency of the leptin receptor. N Engl J Med. 2007; 356: 237-47.
15.** Lubrano-Berthelier C, Dubern B, Lacorte JM, Picard F, Shapiro A, Zhang S, Bertrais S, Hercberg S, Basdevant A, Clement K, Vaisse C. Melanocortin 4 receptor mutations in a large cohort of severely obese adults: prevalence, functional classification, genotype phenotype relationship, and lack of association with binge eating. J Clin Endocrinol Metab. 2006; 91: 1811-18.
16.* Goldstone AP, Holland AJ, Hauffa BP, Hokken-Koelega AC, Tauber M; speakers contributors at the Second Expert Meeting of the Comprehensive Care of Patients with PWS. Recommendations for the diagnosis and management of Prader-Willi syndrome. J Clin Endocrinol Metab. 2008; 93: 4183-97.
17.* Li G, Vega R, Neims K, Gekakis N, Goodnow C, McNamara P, et al. A role for Alsmtröm syndrome protein, alms1, in kidney ciliogenesis and cellular quiescence. PLOs Genet. 2007; 3: 9-20.
18.* Abu Safieh L, Aldahmesh M, Shamseldin H, Hashem M, Shaheen R, Alkuraya H, et al. Clinical and molecular characterization of Bardet-Biedl syndrome in consanguineous populations: The power of homozygosity mapping. J Med Genet. 2010; 47: 236-41.
19.* Rosenbaum M, Fennoy I, Accacha S, Altshuler L, Carey D, Holleran S, Rapaport R, Shelov S, Speiser P, Ten S, The ROAD Project Study Group. Ethnic differences in clinical and biochemical type 2 diabetes mellitus risk factors in children. Obesity (Silver Spring). 2013; 21(10): 2081-90.
20.* Resnicow K, McMaster F, Bocian A, et al. Motivational interviewing and dietary counseling for obesity in primary care: an RCT. Pediatrics. 2015; 135: 649.
21.** Chanoine JP, Hampl S, Jensen C, Boldrin M, Hauptman J. Effect of orlistat on weight and body composition in obese adolescents: a randomized controlled trial. JAMA. 2005; 293: 2873-83.
22.*** Boland CL, Harris JB, Harris KB. Pharmacological Management of Obesity in Pediatric Patients. Annals of Pharmacotherapy. 2015, Vol. 49(2) 220-32.
23.*** Michalsky M, Reichard K, Inge T, Pratt J, Lenders C. ASMBS pediatric committee best practice guidelines. Surg Obes Relat Dis. 2012; 8: 1-7.
24.* Treadwell JR, Sun F, Schoelles K. Systematic review and meta-analysis of bariatric surgery for pediatric obesity. Ann Surg. 2008; 248(5): 763-76.
25.** Alqahtani AR, Antonisamy B, Alamri H, Elahmedi M, Zimmerman VA. Laparoscopic sleeve gastrectomy in 108 obese children and adolescents aged 5 to 21 years. Ann Surg. 2012; 256(2): 266.
26.*** Canadian Task Force on Preventive Health Care. Recommendations for growth monitoring, and prevention and management of overweight and obesity in children and youth in primary care. CMAJ, 2015: 187(6).
27.** Barlow SE, Expert Committee. Expert committee recommendations regarding the prevention, assessment, and treatment of child and adolescent overweight and obesity: summary report. Pediatrics. 2007; 120 Suppl 4: S164-S192.
Bibliografía recomendada
- Scottish Intercollegiate Guidelines Network (SIGN). Management of obesity. A national clinical guideline. 2010.
Guía de Práctica Clínica que provee evidencia para la prevención y el tratamiento de la obesidad en la consulta clínica dirigido a niños, jóvenes y adultos. Se focaliza en la prevención primaria para individuos con peso saludable y/o sobrepeso para evitar o retrasar el inicio de la obesidad.
- Canadian Task Force on Preventive Health Care. Recommendations for growth monitoring, and prevention and management of overweight and obesity in children and youth in primary care. CMAJ, 2015: 187(6).
Recoge la información de todas las guías previas y la evidencia científica actual.
- Grupo de trabajo de la guía sobre la prevención y el tratamiento de la obesidad infantojuvenil. Centro Cochrane Iberoamericano, coordinador. Guía de práctica clínica sobre la prevención y el tratamiento de la obesidad infantojuvenil. Madrid: Plan de Calidad para el Sistema Nacional de Salud del Ministerio de Sanidad y Política Social. Agència d´Avaluació de Tecnologia i Recerca Mèdiques; 2009. Guía de práctica clínica: AATRM N.º 2007/25.
Guía de Práctica Clínica de gran interés para la prevención y el tratamiento de la obesidad en España
- Martos-Moreno GA y Argente J. Obesidades pediátricas: de la lactancia a la adolescencia. An Pediatr (Barc). 2011; 75(1): 63.e1-63.e23.
Actualización de la obesidad desde la infancia a la adolescencia. Los autores resaltan la ausencia de una definición universalmente aceptada para la misma y señalan que es preciso un cambio de la mentalidad de los pediatras en el abordaje de estos pacientes, haciéndose necesaria la consideración de distintas «obesidades» o enfermedades diferentes que convergen en un mismo rasgo fenotípico, el aumento del peso corporal.
- Lama More RA, Alonso Franch A, Gil-Campos M, Leis Trabazo R, Martínez Suárez V, Moráis López A, Moreno Villares JM, Pedrón Giner MC y Comité de Nutrición de la AEP Obesidad Infantil. Recomendaciones del Comité de Nutrición de la Asociación Española de Pediatría Parte I. Prevención. Detección precoz. Papel del pediatra. An Pediatr (Barc). 2006; 65: 607-15.
Consenso nacional que revisa la epidemiología y los períodos de riesgo en la edad pediátrica. Reconoce el importante papel del pediatra de Atención Primaria y ofrecen pautas de estilo de vida saludable teniendo en cuenta la oferta dietética y la actividad física a lo largo de la infancia, con el objetivo de conseguir una prevención del sobrepeso y obesidad.
- Aranceta Bartrina J. Obesidad infantil: Nuevos hábitos alimentarios y nuevos riesgos para la salud. Análisis de sus causas. En: Díaz Méndez C, Gómez Benito C (coord.). Alimentación, consumo y salud. Colección Estudios Sociales, nº 24. Barcelona: Obra Social Fundación “La Caixa”, 2008: pp. 216-46.
Estudio de referencia sobre los nuevos hábitos alimentarios de la población española, las causas y los problemas que conlleva para la salud
- Carrascosa A, Fernández JM, Fernández C, Ferrández-Longás A, López-Siguero JP, Sánchez E, et al.; Grupo Colaborador Español. Spanish cross-sectional growth study 2008. Part II. Height, weight and body mass index values from birth to adulthood. An Pediatr (Barc). 2008; 68: 552-69.
Estudio transversal español de crecimiento, realizado en 32.064 sujetos (16.607 varones y 15.457 mujeres), desde el nacimiento hasta la talla adulta, en una población caucásica española procedente de Andalucía, Barcelona, Bilbao y Zaragoza, realizado entre los años 2000 y 2004.
| Caso clínico |
|
Motivo de consulta Niño de 9 años y 6 meses que consulta por exceso de peso desde siempre, más exacerbado en el último año. Anamnesis Dieta rica en grasas con escasas verduras y frutas. A menudo, realiza tentempiés de patatas fritas, golosinas, bollería industrial y refrescos azucarados en casa. La familia no realiza las comidas juntos, sino que realizan numerosos picoteos a lo largo del día, cada uno cuando quiere. Actividad física limitada exclusivamente a las 2 horas semanales de clase de educación física obligatoria en la escuela. En el último año, el paciente permanece la mayor parte del tiempo recluido en su cuarto jugando videojuegos al llegar de la escuela, y los padres creen que tiene bajo estado de ánimo. Antecedentes familiares Padre: talla 165 cm; peso: 112 kg; IMC: 41 kg/m2; desarrollo puberal normal; diabetes mellitus tipo 2 en tratamiento con antidiabéticos orales; hipercolesterolemia en tratamiento con estatinas. Madre: talla 150 cm; peso: 65 kg; IMC: 29 kg/m2; menarquía a los 12 años; hipertensión arterial en tratamiento médico; antecedente de diabetes gestacional en los 2 últimos embarazos. G-A-V: 3-0-3. Abuela materna diabetes tipo 2. Dos hermanos mayores con sobrepeso. Sin otros antecedentes de interés. Antecedentes personales Embarazo controlado, normal. Parto a las 40 semanas, cesárea por no progresión de parto debido a macrosomía. PRN: 4.500 g; LRN: 50 cm. Periodo neonatal normal. Pruebas metabólicas normales. Lactancia materna once meses, sin intolerancias alimentarias. Desarrollo psicomotor normal. Inmunizaciones correctas. Enfermedades anteriores: nada que reseñar. Medicaciones: ninguna en la actualidad. Exploración física Peso: 53 kg (+4,4 DE); talla: 130 cm (-0,77 DE); IMC: 31,3 kg/m2 (+5,6 DE). T.A.: 110/60 mmHg. Buen estado general. Coloración normal de piel y mucosas. Sin rasgos dismórficos. Obesidad generalizada, sin estrías ni acantosis. Sin bocio. ACP: normal. Abdomen: blando, depresible, sin visceromegalias. Genitales externos masculinos normales, pene embebido en grasa, 5 cm de longitud desde la sínfisis del pubis. Tanner I (genitales 1, pubarquia 1, axilarquia 1). Estudios complementarios Hemograma: fórmula y recuentos normales. Bioquímica general: normal. Hormonas tiroideas: normales. Glucemia en ayunas: 98 mg/dl. Insulina en ayunas: 9 mcU/l, HOMA-IR: 2.17. Lipidograma: CT: 210 mg/dl (vn: 120-200); Triglicéridos: 120 mg/dl (vn: < 100); C-HDL: 40 mg/dl (vn: 35-75); C-LDL: 140 mg/dl (vn: 60-130); C-VLDL: 30 mg/dl (vn: 5-23); C-LDL/C-HDL: 3,5 (vn: <2,2). Edad ósea: 8 años para una edad cronológica de 9 años y 6 meses. |
 |
| Temas de FC |
M. Güemes-Hidalgo*, M.T. Muñoz-Calvo**
*Departamento de Endocrinología. Great Ormond Street Hospital for Children. Londres. Reino Unido. **Servicio de Endocrinología. Hospital Infantil Universitario Niño Jesús. Profesora Asociada de Pediatría. Universidad Autónoma. Madrid
| Resumen
El síndrome metabólico es un conjunto de factores de riesgo, que requieren la presencia de obesidad de predominio central, dislipemia, hipertensión arterial y resistencia a la insulina, todos ellos, predictores de enfermedad cardiovascular y diabetes tipo 2 en el futuro. La mayoría de los estudios demuestran que la prevalencia de síndrome metabólico es dependiente de las definiciones utilizadas, observando una prevalencia mayor en la región mediterránea que en la zona central y norte de Europa. Dentro de los mecanismos fisiopatológicos, uno de los principales es la resistencia a la insulina. La determinación de la glucemia y la insulina en ayunas son necesarias para identificar las alteraciones de la homeostasis de la glucemia, y reflejan fundamentalmente la secreción de insulina y la sensibilidad hepática y periférica. El tratamiento del síndrome metabólico comprende, en primer lugar, la realización de una dieta adecuada que tiene como objetivo mejorar la sensibilidad a la insulina y prevenir o corregir las alteraciones metabólicas y cardiovasculares asociadas. Asimismo, se debe acompañar de la realización de ejercicio físico regular y un adecuado soporte psicológico. En las alteraciones de la tolerancia a la glucemia, la modificación de los estilos de vida mejora, tanto la glucemia como los factores de riesgo cardiovascular. A menudo, hay que recurrir al tratamiento farmacológico, ya que los cambios en el estilo de vida son, a veces, complicados en los adolescentes. Por último, las estrategias para la prevención de la obesidad y el síndrome metabólico deben iniciarse en Atención Primaria, con programas dirigidos al ambiente familiar del niño con riesgo de obesidad y con programas desarrollados en el medio escolar. |
| Abstract
Metabolic syndrome is a combination of risk factors, namely centrally distributed obesity, dyslipidemia, hypertension and insulin resistance, all of which are future predisposing factors for cardiovascular disease and type 2 diabetes. |
Palabras clave: Obesidad; Glucemia; Triglicéridos; Diabetes; Insulina
Key words: Obesity; Glycaemia; Triglycerides; Diabetes; Insulin
Pediatr Integral 2015; XIX (6): 428-435
Concepto
El síndrome metabólico (SM) es un conjunto de factores de riesgo, que requieren la presencia de obesidad de predominio central, dislipemia, hipertensión arterial y resistencia a la insulina, todos ellos, predictores de enfermedad cardiovascular y diabetes tipo 2 en el futuro.
Fue descrito por primera vez en 1988 y los criterios diagnósticos en adultos han sido revisados recientemente, aunque en relación con los pacientes pediátricos no hay un consenso reconocido internacionalmente. Existen diferentes definiciones de síndrome metabólico, entre las que cabe destacar la realizada por la Organización Mundial de la Salud(1) y la plasmada en el tercer informe de la National Cholesterol Education Program Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults(2). Estos criterios han sido modificados para la utilización en adolescentes por Cook et al.(3), y se han basado en los criterios del NCEP-ATPIII, los de la Asociación Americana de Diabetes y la Task Force para el diagnóstico de hipertensión arterial.
Los criterios establecidos por la Internacional Diabetes Federation en 2007(4) postulan una modificación sobre los criterios ATP-III, donde se especifican puntos de corte para el perímetro de la cintura propios de la población europea (y otras poblaciones) y, además, resulta ser también una clasificación de uso clínico fácil y asequible. La nueva definición ha sido dividida en los siguientes grupos de edades: de 6 a 10, de 10 a 16 y =16 años. Se sugiere que por debajo de los 10 años, no debería hablarse de síndrome metabólico, pero hay que tener en cuenta la existencia de comorbilidad y la historia familiar. De 10 a 16 años existirían criterios diagnósticos específicos, y por encima de los 16 años se utilizarían los criterios de la IDF para adultos. En la tabla I, se exponen estos criterios diagnósticos.
Prevalencia
La prevalencia en la infancia se incrementa en los niños y adolescentes obesos; tanto más, cuanto más obesos son.
Estudios recientes en nuestro país, en adolescentes entre 12 y 17 años, observan una prevalencia del 3,8% según los criterios IDF, no encontrando diferencias entre sexos ni en grupos de edad. Los factores asociados fueron la obesidad y la resistencia a la insulina(5). En adolescentes de 15 años, en un estudio conjunto de Dinamarca, Estonia y Portugal, la prevalencia fue de un 1,4%, según los criterios IDF(6). En adolescentes griegos, la prevalencia fue del 8%, con los criterios anteriores(7). Por tanto, en la región mediterránea, la prevalencia es mayor que en la zona central y norte de Europa.
Fisiopatología
Uno de los principales factores implicados es la resistencia a la insulina, junto a otros como: la diabetes tipo 2, la obesidad, la dislipemia y los estados inflamatorios, protrombóticos y aterogénicos.
Resistencia a la insulina (RI)
La RI se define como la disminución de la capacidad de la insulina plasmática para, en concentraciones habituales, promover la captación periférica de glucosa, suprimir la gluconeogénesis hepática e inhibir la producción de lipoproteínas de muy baja densidad (VLDL), lo que ocasiona un aumento compensador de la secreción de insulina que puede derivar en una intolerancia a los hidratos de carbono e incluso en una diabetes mellitus tipo 2 (DM2), cuando esta capacidad compensadora fracasa(8).
El trastorno inicial de la RI parece centrarse en el adipocito, y consiste en una incapacidad para continuar almacenando ácidos grasos. En condiciones normales, los triglicéridos circulantes se acumulan en el adipocito, una vez que han sido desdoblados a ácidos grasos por acción de la enzima lipoproteín-lipasa, que a su vez es estimulada por la insulina(8).
En personas obesas, se produce un aumento de la liberación de ácidos grasos al torrente circulatorio, que juegan un papel importante en el desarrollo de la RI, contribuyendo al estrés oxidativo, la inflamación y la reactividad vascular. Además, los niveles mantenidos de ácidos grasos a largo plazo pueden llegar a ser tóxicos para la célula beta pancreática, con lo que quedaría establecida la relación entre la obesidad, la resistencia a la insulina y la diabetes tipo 2(9) (Fig. 1).
Figura 1. Mecanismos de influencia de la obesidad sobre la enfermedad cardiovascular y la diabetes tipo 2.
En presencia de resistencia a la insulina, la célula beta pancreática incrementará la secreción de insulina y, para intentar compensar esta situación, se producirá hiperinsulinismo.
Si lo consigue, se alcanzará la normoglucemia, pero con los años este mecanismo compensador irá fallando (Fig. 2). La hiperglucemia traerá como consecuencia la glucotoxicidad, con incremento del potencial aterogénico. Progresivamente, se irán sumando otros cuadros como: la hipertrigliceridemia, la hipertensión arterial, entre otros, hasta el desarrollo del cuadro completo de SM(9).
Figura 2. Insulinorresistencia: factores y consecuencias.
Los niños nacidos pequeños para la edad gestacional, en particular si se ha seguido de un rápido incremento del peso en los primeros meses de vida, presentan un mayor riesgo de resistencia a la insulina (RI), diabetes mellitus tipo 2, hipertensión arterial y aterosclerosis en la vida adulta (Fig. 3). La reducción del aporte de oxígeno y nutrientes determina una respuesta adaptativa en el feto, que tiende a preservar la diferenciación y maduración de los órganos a expensas de un menor crecimiento y una menor acumulación de energía (glucógeno y grasa)(10). Es posible que estas alteraciones metabólicas adaptativas sean las responsables de una especie de “impronta metabólica” que condicionaría en la edad adulta, la mayor frecuencia observada de desarrollo del síndrome metabólico, con el consiguiente incremento de enfermedades cardiovasculares.
Figura 3. Causas potenciales que podrían relacionar el bajo peso al nacer con la adrenarquia prematura, síndrome de ovario poliquístico y el desarrollo de síndrome metabólico en la vida adulta.
El síndrome de ovario poliquístico (SOP) y la acantosis nigricans, se asocian a resistencia a la insulina. Diferentes estudios han demostrado que el 30% de las mujeres entre 14 y 19 años con SOP tienen alteraciones de la tolerancia a la glucosa, y el 55%-75% asocian sobrepeso/obesidad(11). La acantosis nigricans es una alteración relacionada con la activación de los receptores de insulina en la piel por el exceso de insulina, y se encuentra presente en el 90% de niños y adolescentes con DM2(12).
La determinación de la glucemia y la insulina en ayunas son necesarias para identificar las alteraciones de la homeostasis de la glucemia, y reflejan fundamentalmente la secreción de insulina y la sensibilidad hepática y periférica.
Los valores de los índices de RI cambian a lo largo de la infancia, sobre todo en los diferentes estadios de la pubertad, ya que esta contribuye a la insulinorresistencia. Diferentes estudios(13) han demostrado que el metabolismo de la glucosa estimulado por la insulina es un 30% más bajo en los niños en estadios de Tanner II al IV, comparado con el estadio I y el adulto. El pico de menor sensibilidad a la insulina está en el estadio III, y se recupera en el estadio V.
La cuantificación de la RI se puede realizar por métodos basados en la medida de los niveles de glucemia e insulina en ayunas o tras sobrecarga oral de glucosa. Asimismo, el índice HOMA (Homeostasis Model Assessment) estima la RI como el producto de la insulina en ayunas (en mcUI/ml) por la glucemia en ayunas (en mmol/l), dividido por 22,5. Estudios realizados en nuestro país en niños y adolescentes, establecen el punto de corte según los estadios de Tanner II, III y IV en 3,23, 4,27 y 4,87, respectivamente(14).
Diabetes mellitus tipo 2 (DM2)
La etiología de la DM2 es multifactorial en niños y adolescentes, destacando los factores genéticos y los ambientales. El aumento de la incidencia de DM2 se ha producido de forma paralela al aumento de la frecuencia de obesidad infantil, que puede considerarse el factor de riesgo principal para su desarrollo.
El estudio SEARCH observa una incidencia de DM2 en blancos no hispanos de 3/100.000 entre 10 y 19 años, y la edad más prevalente son jóvenes entre 15 y 19 años(15).
Los factores de riesgo para la DM2 incluyen: historia familiar de primer grado, tipo de etnia, obesidad y vida sedentaria. El riesgo de desarrollar DM2 es cinco veces más elevada si hay familiares de primer grado con esta patología(15).
El método de cribado recomendado es la determinación de la glucemia basal, aunque la mayoría de los centros prefieren utilizar la sobrecarga oral de glucosa para aumentar la sensibilidad, especialmente si la glucemia basal es superior a 100 mg/dl.
Los criterios diagnósticos de la DM (ADA, 2015) son los siguientes(16):
• HbA1c = 6,5% (método que debe estar estandarizado con el DCCT).
• Glucemia en ayunas = 126 mg/dl.
• Glucemia a las 2 horas de la sobrecarga oral de glucosa = 200 mg/dl.
• Síntomas de hiperglucemia o crisis hiperglucémicas con glucemia plasmática = 200 mg/dl.
El test de tolerancia oral a la glucosa (TTOG) se hará en aquellos casos en los que el paciente pertenezca a un grupo étnico de riesgo (hispano, afroamericano) y/o existan alteraciones de la glucemia (> 100 mg/dl) o insulinemia basales (> 15 µU/ml), dislipemia, hipertensión arterial, antecedentes familiares de DM2, o condiciones asociadas a la RI, tales como acantosis nigricans o síntomas del SOP. Por medio de estos estudios, se pueden definir las siguientes entidades diagnósticas: alteración de la glucemia en ayunas (AGA, > 100 mg/dl); intolerancia a los hidratos de carbono (IHC, glucemia tras 2 horas en el TTOG = 140-199 mg/dl); y DM2 (glucemia en ayunas > 126 mg/dl o tras 2 horas del TTOG > 200 mg/dl, repetidas en 2 ocasiones). En este último caso, es preciso registrar la cifra de hemoglobina glicosilada (HbA1c), que desde el año 2010, es también propuesta por la American Diabetes Association (ADA) como marcador diagnóstico de prediabetes (5,7-6,4%) o diabetes (si supera 6,5%)(16).
Obesidad
La obesidad en la infancia y la adolescencia ha experimentado un incremento progresivo en los últimos años en todos los países desarrollados.
En el capítulo correspondiente de esta revista, podemos revisar los aspectos más importantes de la obesidad, incluyendo el concepto, la fisiopatología y el diagnóstico.
Dislipemia
Se caracteriza por un aumento de los niveles de triglicéridos, disminución del C-HDL y aumento del C-LDL, que se asocian estrechamente con RI. La hipertrigliceridemia es la alteración más precoz en el SM, se debe al aumento de la síntesis hepática de partículas de lipoproteínas de muy baja densidad (C-VLDL) y a la alteración de su catabolismo por disminución de la actividad de la lipoproteinlipasa. Como consecuencia de estas alteraciones, se produce un aumento de las lipoproteínas ricas en triglicéridos y, por ello, de los triglicéridos plasmáticos(17).
Estado proinflamatorio y protrombótico
El tejido adiposo no es un reservorio pasivo de energía, al contrario, se trata de un auténtico órgano de gran actividad endocrina y metabólica, que segrega determinados péptidos y citoquinas a la circulación. Actualmente, se dispone de suficiente evidencia científica para afirmar la participación de la inflamación en el desarrollo de la aterosclerosis. El fenómeno inicial es la disfunción endotelial, que provoca una respuesta inflamatoria de linfocitos y monocitos que termina en la aterotrombosis(18).
Así, diferentes estudios poblacionales indican que los marcadores biológicos de la inflamación son predictores de enfermedad cardiovascular, siendo la elevación de los niveles séricos de la proteína C reactiva (PCR), la interleuquina 6 (IL-6) y el factor de necrosis tumoral alfa (TNF-a), los que presentan una mayor correlación con las alteraciones que constituyen el síndrome metabólico. Los niveles circulantes de adiponectina se correlacionan de forma negativa con el índice de masa corporal y con el contenido de masa grasa, en asociación con la grasa visceral. La correlación negativa entre la adiponectina circulante y la presencia de obesidad está bien establecida y la pérdida de peso determina un aumento en la concentración de adiponectina(18). Asimismo, el estado protrombótico observado en el SM produce cambios en la coagulación, en el sistema fibrinolítico, en los trombocitos y en la células endoteliales vasculares.
Otros componentes y SM
Disfunción endotelial
Más recientemente, métodos de imagen incruentos han permitido el estudio del desarrollo de la aterosclerosis. Por un lado, la medición del grosor del complejo íntima-media en localizaciones estandarizadas de las arterias carótidas, es indicador de afectación vascular arteriosclerótica. Este grosor aumenta a medida que aumentan los factores de riesgo cardiovascular, y algunos autores han observado que el incremento de los niveles de LDL-C puede predecir el grosor del complejo íntima-media en jóvenes adultos. Por otro, está la dilatación mediada por flujo, que permite establecer las propiedades funcionales de las arterias, incluyendo las propiedades mecánicas como la rigidez y la distensibilidad y las propiedades adaptativas como la vasodilatación en respuesta a un estímulo(19).
Estrés oxidativo
En adolescentes, se ha observado una asociación entre los niveles de hipertensión arterial y el estrés oxidativo, independiente del índice de masa corporal (IMC). En un estudio realizado en 295 adolescentes, se observó una relación entre el estrés oxidativo con la adiposidad y la resistencia a la insulina(20).
SOP
Es un trastorno de presentación heterogénea, cuyas manifestaciones pueden ser diferentes entre pacientes. Las manifestaciones clínicas son: hirsutismo, irregularidades menstruales (oligomenorrea que persiste más de dos años después de la menarquia, amenorrea o hemorragia uterina disfuncional), acné, alopecia y, durante la etapa reproductiva, infertilidad. Se asocia con hiperinsulinemia y resistencia a la insulina, y se acompaña con frecuencia de dislipemia, alteraciones de los marcadores de la inflamación, y aumento de la adiposidad central, siendo estos factores de riesgo para el desarrollo de DM2 y enfermedad cardiovascular(21).
Esteatosis hepática
Varios mecanismos fisiopatológicos parecen estar implicados en su patogénesis. Por un lado, la hiperinsulinemia asociada con la resistencia a la insulina, secundaria fundamentalmente a adiposidad central. Por otro, el estrés oxidativo, debido a la acumulación excesiva de grasa a nivel hepático, especialmente de triglicéridos, que produce la liberación de adipocitocinas proinflamatorias que, a nivel del hepatocito causan apoptosis y necrosis por activación de la cascada inflamatoria, fundamentalmente del factor de necrosis tumoral alfa(22).
Tratamiento
Nutricional
Se deben realizar medidas preventivas, como cambios a estilos de vida saludables, incluyendo las medidas nutricionales y la actividad física, con el objetivo de mejorar la sensibilidad a la insulina y prevenir o corregir las alteraciones metabólicas y cardiovasculares asociadas.
En cuanto a la composición de la dieta, se aconseja una dieta equilibrada, en la que el porcentaje de calorías aportadas por cada uno de los principios inmediatos sea: 50% en forma de hidratos de carbono, 30% de grasas y 20% de proteínas. Las proteínas deben ser de alto valor biológico. La grasa aportará ácidos grasos esenciales y vitaminas liposolubles, y favorecerá la sensación de saciedad. Asimismo, los alimentos con bajo índice glucémico ayudarán a controlar la sensibilidad a la insulina y las alteraciones lipídicas, así como asegurar un aporte extra de fibra que produce mayor sensación de saciedad y disminuye la ingesta energética.
Ejercicio físico
El ejercicio físico regular puede mejorar la sensibilidad a la insulina en un 40% y disminuir la lipogénesis. Además, mejora los niveles de C-HDL y la función endotelial. Es útil para mantener la pérdida de peso y debe ser individualizado, realizando 30-60 minutos de ejercicio aeróbico diario. Las actividades sedentarias deben realizarse durante menos de 2 horas al día.
Aspectos psicológicos
Se ha observado que los síntomas depresivos y el SM están unidos en ambas direcciones. Así, determinadas características psicológicas como la depresión y la hostilidad, pueden incrementar el riesgo para el desarrollo de SM.
Tratamiento farmacológico
Obesidad
Ver capítulo correspondiente en esta revista.
Alteraciones de la tolerancia a la glucemia-Diabetes tipo 2
La modificación de los estilos de vida: dieta, ejercicio físico regular y control del peso, mejoran tanto la glucemia como los factores de riesgo cardiovascular (hipertensión arterial y dislipemia). A menudo, hay que recurrir al tratamiento farmacológico, ya que los cambios en el estilo de vida son, a veces, complicados en los adolescentes. Los pacientes sintomáticos en el momento del diagnóstico, especialmente si tienen cetosis, deben recibir tratamiento con insulina. Una vez controlada la hiperglucemia, puede sustituirse progresivamente por Metformina, que es una biguanida cuya acción consiste en la disminución de la producción hepática de glucosa, incremento de la sensibilidad a la insulina y mayor captación periférica de glucosa mediada por la insulina(23). Asimismo, la esteatohepatitis no alcohólica asociada a obesidad presenta buena respuesta a metformina, al igual que en niñas y adolescentes con hirsutismo, obesidad e hiperandrogenismo. Como principal efecto secundario, está descrita la diarrea (30%) que es dosis dependiente, pero el efecto más grave es la acidosis láctica, así que en situaciones que predispongan a hipoxia celular deberá ser interrumpida (infecciones, cirugía, insuficiencia respiratoria). Está aprobado a partir de los 10 años por la FDA y la Agencia Europea del Medicamento.
En los pacientes asintomáticos, cuando no son suficientes las recomendaciones del cambio en los estilos de vida para conseguir los objetivos glucémicos, debe iniciarse tratamiento con Metformina. Su efecto a largo plazo sobre la HbA1c o el peso corporal es escaso en adolescentes con DM2 asintomática(24). Esto podría deberse, al mal cumplimiento terapéutico debido a las molestias gastrointestinales que provoca. Se recomienda comenzar con dosis bajas e ir incrementando progresivamente según tolerancia. En los casos en que la metformina no consiga un control metabólico adecuado, debe iniciarse tratamiento con análogos de insulina. En la figura 4, está representado el algoritmo de tratamiento de la DM2 en niños y adolescentes(15).
Figura 4. Algoritmo de tratamiento de la diabetes tipo 2 en niños y adolescentes (Onge ES et al., cita 15).
Dislipemias
La American Heart Association y la Academia Americana de Pediatría han ofrecido unas recomendaciones dietéticas basadas en las nuevas pautas para niños mayores de 2 años de edad y adolescentes. La ingesta calórica debe ser adecuada con la suficiente actividad física, para conseguir un peso adecuado. Se deben consumir más frutas, verduras, pescados, cereales integrales y productos lácteos desnatados. Se recomienda la disminución de zumos de frutas, bebidas y alimentos edulcorados con azúcar y sal. Además, recomiendan una ingesta de ácidos grasos trans(alimentos procesados y preparados) de <1% de las calorías totales.
Los estanoles y esteroles de plantas se añaden a las margarinas, zumos de naranja, yogur líquido, barras de cereales y suplementos dietéticos. Estos compuestos actúan disminuyendo la absorción intestinal de colesterol exógeno de origen alimentario, así como del colesterol endógeno de origen biliar, demostrándose en adultos una disminución del CT de un 10-15%, con mínimos efectos adversos. La seguridad de estos compuestos no está suficientemente establecida, ya que pueden disminuir la absorción de vitaminas y betacarotenos solubles(25).
Los diferentes consensos y guías clínicas recomiendan el inicio del tratamiento farmacológico a partir de los 10 años de edad o en varones al inicio de la pubertad (Tanner II) y en mujeres tras la primera menstruación, después de un tratamiento dietético adecuado de seis meses a un año, siempre que los niveles de C-LDL sean superiores a 190 mg/dl o a 160 mg/dl y existan antecedentes familiares de enfermedad cardiovascular o el niño tenga dos o más factores de riesgo asociados.
Entre los fármacos que podemos disponer en la infancia y la adolescencia están los siguientes(26):
• Resinas de intercambio iónico: los estudios en población infantil han demostrado una reducción en los niveles de C-LDL de un 16% a un 19%. El grado de cumplimiento es variable, oscilando alrededor de un 75%, y no se han observado cambios en el patrón de crecimiento, aunque sí se detecta una disminución de los niveles séricos de folatos, carotinoides y vitamina E. Estas sustancias no tienen toxicidad sistémica, ya que no se absorben, por lo cual son potencialmente seguras en niños(25).
• Ezetimibe: se localiza en las microvellosidades del intestino delgado e inhibe la absorción de colesterol, reduciendo su paso hacía el hígado. Posiblemente, por su mecanismo de acción y la casi ausencia de efectos adversos, va a ser el sustituto ideal de las resinas, mucho peor toleradas y menos eficaces. Sería el paso inicial junto a la dieta en el tratamiento de las hipercolesterolemias(25).
• Estatinas: disminuyen la síntesis endógena de colesterol mediante inhibición competitiva de la enzima HMG-CoA reductasa, enzima limitante en la biosíntesis del colesterol. Respecto a los efectos adversos, no se han publicado casos de miositis, miopatía o rabdomiolisis, y se han encontrado algunos casos de elevaciones asintomáticas de la CPK y enzimas hepáticas, que han revertido con un descenso de las dosis de la medicación sin necesidad de suspender el tratamiento. Tampoco se han detectado trastornos del crecimiento, ni del desarrollo puberal ni del metabolismo de las vitaminas. La reducción de los niveles de LDL-C oscila entre el 17-45% dependiendo de la estatina y la dosis utilizada(27).
• Fibratos: son sustancias químicas derivadas del ácido fíbrico (ácido clorofenoxiisobutírico). Actúan estimulando los receptores nucleares denominados “receptores activados de proliferación de los peroxisomas” (PPAR), en concreto los alfa. Dan lugar a un aumento del catabolismo de las partículas ricas en TG y a una disminución plasmática de las concentraciones de VLDL y triglicéridos. Producen un aumento de HDL-C y una disminución moderada del LDL-C. Los más utilizados son: bezafibrato, fenabibrato y gemfibrozil(25). Los principales efectos adversos encontrados en adultos han sido leves y pasajeros, siendo los más frecuentes: gastrointestinales (anorexia, sensación de opresión del estómago, náuseas, elevación de transaminasas), dermatológicos (erupción cutánea, prurito, urticaria), hematológicos (citopenias), musculares (mialgias, debilidad muscular, calambres musculares y aumentos considerables de la CPK) y neurológicos (cefalea). Hay aún escasos ensayos sobre su utilización en niños; si bien, muy recientemente, ha sido publicada una propuesta de manejo de la hipertrigliceridemia durante la infancia, en la que los fibratos juegan un papel primordial.
Hipertensión arterial
En la fase de pre-hipertensión (niveles de T.A. entre el percentil 90-95 o TA >120/80 mmHg en adolescentes), la recomendación es realizar cambios en los estilos de vida, principalmente si existe historia familiar de hipertensión arterial o enfermedad cardiovascular prematura, con pérdida de 1-2 kg de peso/mes. Si existieran niveles de tensión arterial superior al percentil 95, deberá iniciarse tratamiento farmacológico, aunque no hay consenso sobre qué fármacos utilizar en niños y adolescentes, siendo el objetivo reducir la morbi-mortalidad cardiovascular a largo plazo(28).
Prevención
Las estrategias para la prevención de la obesidad y el SM deben iniciarse en Atención Primaria, con programas dirigidos al ambiente familiar del niño con riesgo de obesidad y con programas desarrollados en el medio escolar.
La modificación de los estilos de vida se considera un elemento clave a la hora de mejorar los diferentes factores que definen el SM. Asimismo, la ingesta de fibra vegetal sería beneficiosa para disminuir la respuesta de la glucemia y la insulina postprandial, así como para disminuir los niveles de C-HDL y tener efectos positivos sobre la tensión arterial y los diferentes marcadores de la inflamación.
Se deben recomendar prácticas alimentarias saludables, entre las que destacan: crear costumbres culinarias sanas en el hogar (alimentos bajos en grasa y raciones de tamaño pequeño), evitando la ingesta de bebidas azucaradas (refrescos), reducir el número de comidas fuera del hogar (hipercalóricas y ricas en grasa) hasta un máximo de una vez a la semana, acostumbrar a los niños a que coman en lugares y horarios asignados para ello y esforzarse en ofrecer los alimentos recomendables de la forma más apetecible para cada niño en concreto(29).
La DM2, hasta hace algunos años excepcional en adolescentes y niños, ha incrementado su prevalencia, sobre todo durante la pubertad. Como puede permanecer asintomática durante años, la Asociación Americana de Diabetes ha publicado unas recomendaciones para la búsqueda selectiva de DM2 en pacientes pediátricos.
Es conveniente sensibilizar a la opinión pública y al personal sanitario de que la obesidad puede llegar a ser imposible de curar, y que la identificación precoz de los niños obesos y su correcto tratamiento puede, al menos en parte, reducir la intensidad de este trastorno y prevenir las complicaciones a largo plazo.
Bibliografía
1. WHO. Definition, diagnosis and classification of diabetes mellitus and its complications: Report of a WHO Consultation. Geneva: Department of Non-communicable Disease Surveillance, World Health Organization, 1999.
2. ATPIII. Executive Summary of The Third Report of The National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, And Treatment of High Blood Cholesterol In Adults (Adult Treatment Panel III). JAMA. 2001; 285: 2486-97.
3. Cook S, Weitzman M, Auinger P, Nguyen M, Dietz WH. Prevalence of a Metabolic Syndrome Phenotype in Adolescents Findings from the Third National Health And Nutrition Examination Survey, 1988-1994. Arch Pediatr Adolesc Med. 2003; 157: 821-7.
4. Zimmet P, Alberti KG, Kaufman F, Tajima N, Silink M, Arslanian S, et al. The metabolic syndrome in children and adolescents – an IDF consensus report. Ped Diabetes. 2007; 8: 299-306.
5. Galera-Martínez R, García-García E, Vázquez-López Mª, Ortíz-Pérez M, Ruiz-Sánchez M, Martín-González M, et al. Prevalence of metabolic syndrome among adolescents in a city in the Mediterranean area: comparison of two definitions. Nutr Hosp. 2015; 32: 627-33.
6. Ekelund U, Anderssen S, Andersen LB, Riddoch CJ, Sardinha LB, Luan J, Froberg K, Brage S. Prevalence and correlates of the metabolic syndrome in a population-based sample of European youth. Am J Clin Nutr. 2009; 89: 90-6.
7. Efstathiou SP, Skeva II, Zorbala E, Georgiou E, Mountokalakis TD. Metabolic syndrome in adolescence: can it be predicted from natal and parental profile? The Prediction of Metabolic Syndrome in Adolescence (PREMA) study. Circulation. 2012; 125: 902-10.
8. Ho M, Garnett SP, Baur LA. Childhood obesity and insulin resistance: how should it be managed? Curr Treat Options Cardiovasc Med. 2014; 16: 351.
9. Nelson RA, Bremer AA. Insulin resistance and metabolic syndrome in the pediatric population. Metab Syndr Relat Disord. 2010; 8: 1-14.
10. Lakshmy R. Metabolic syndrome: role of maternal undernutrition and fetal programming. Rev Endocr Metab Disord. 2013; 14: 229-40.
11. Witchel SF, Oberfield S, Rosenfield RL, Codner E, Bonny A, Ibáñez L, et al. The Diagnosis of Polycystic Ovary Syndrome during Adolescence. Horm Res Paediatr. 2015; 83: 376-89.
12. Yang M, Gong S, Ye SQ, Lyman B, Geng L, Chen P, et al. Non-alcoholic fatty liver disease in children: focus on nutritional interventions. Nutrients. 2014; 6: 4691-705.
13. Levy-Marchal C, Arslanian S, Cutfield W, Sinaiko A, Druet C, Marcovecchio ML, Chiarelli F; ESPE-LWPES-ISPAD-APPES-APEG-SLEP-JSPE; Insulin Resistance in Children Consensus Conference Group. Insulin resistance in children: consensus, perspective, and future directions. J Clin Endocrinol Metab. 2010; 95: 5189-98.
14. García Cuartero B, García Lacalle C, Jiménez Lobo C, González Vergaz A, Calvo Rey C, Alcázar Villar MJ, et al. The HOMA and QUICKI indexes, and insulin and C-peptide levels in healthy children. Cut off points to identify metabolic syndrome in healthy children. An Pediatr (Barc). 2007; 66: 481-90.
15. Onge ES, Miller SA, Motycka C, DeBerry A. A review of the treatment of type 2 diabetes in children. J Pediatr Pharmacol Ther. 2015; 20: 4-16.
16. American Diabetes Association. Classification and diagnosis of diabetes. Diabetes Care. 2015; 38, suppl S8-S16.
17. Mata P, Alonso R, Ruiz A, González-Juanatey JR, Badimón L, Díaz-Díaz JL, Muñoz MT, Muñiz O, Galve E, Irigoyen L, Fuentes-Jiménez F, Dalmau J, Pérez-Jiménez F y otros colaboradores. Diagnóstico y Tratamiento de la Hipercolesterolemia Familiar en España. Documento de Consenso. Semergen. 2015; 41: 24-33.
18. Piya MK, McTernan PG, Kumar S. Adipokine inflammation and insulin resistance: the role of glucose, lipids and endotoxin. J Endocrinol. 2013; 216: T1-T15.
19. Masquio DC, de Piano A, Sanches PL, Corgosinho FC, Campos RM, Carnier J, et al. The effect of weight loss magnitude on pro-/anti-inflammatory adipokines and carotid intima-media thickness in obese adolescents engaged in interdisciplinary weight loss therapy. Clin Endocrinol (Oxf). 2013; 79: 55-64.
20. Kelly AS, Steinberger J, Kaiser DR, Olson TP, Bank AJ, Dengel DR. Oxidative stress and adverse adipokine profile characterize the metabolic syndrome in children. J Cardiometab Syndr. 2006; 1: 248-52.
21. Michaliszyn SF, Lee S, Tfayli H, Arslanian S. Polycystic ovary syndrome and nonalcoholic fatty liver in obese adolescents: association with metabolic risk profile. Fertil Steril. 2013; 100: 1745-51.
22. Alterio A, Alisi A, Liccardo D, Nobili V. Non-alcoholic fatty liver and metabolic syndrome in children: a vicious circle. Horm Res Paediatr. 2014; 82: 283-9.
23. Brufani C, Crinò A, Fintini D, Patera PI, Cappa M, Manco M. Systematic review of metformin use in obese nondiabetic children and adolescents. Horm Res Paediatr. 2013; 80: 78-85.
24. TODAY Study Group. Effects of metformin, metformin plus rosiglitazone, and metformin plus lifestyle on insulin sensitivity and b-cell function in TODAY. Diabetes Care. 2013; 36(6): 1749-57.
25. Braamskamp MJ, Hutten BA, Wiegman A, Kastelein JJ. Management of hypercholesterolemia in children. Paediatr Drugs. 2014; 16(2): 105-14.
26. Steinberger J, Daniels SR, Eckel RH, Hayman L, Lustig RH, McCrindle B, Mietus-Snyder ML; American Heart Association Atherosclerosis, Hypertension, and Obesity in the Young Committee of the Council on Cardiovascular Disease in the Young; Council on Cardiovascular Nursing; and Council on Nutrition, Physical Activity, and Metabolism. Progress and challenges in metabolic syndrome in children and adolescents: a scientific statement from the American Heart Association Atherosclerosis, Hypertension, and Obesity in the Young Committee of the Council on Cardiovascular Disease in the Young; Council on Cardiovascular Nursing; and Council on Nutrition, Physical Activity, and Metabolism. Circulation. 2009; 119: 628-47.
27. Vuorio A, Kuoppala J, Kovanen PT, Humphries SE, Tonstad S, Wiegman A, Drogari E. Statins for children with familial hypercholesterolemia. Cochrane Database Syst Rev. 2014; 23; 7: CD006401.
28. Barlow SE, Expert Committee. Expert committee recommendations regarding the prevention, assessment, and treatment of child and adolescent overweight and obesity: summary report. Pediatrics. 2007; 120 Suppl 4: S164-S192.
29. Gurnani M, Birken C, Hamilton J. Childhood Obesity: Causes, Consequences, and Management. Pediatr Clin North Am. 2015; 62: 821-40
| Caso clínico |
|
Motivo de consulta Adolescente de 14 años y 6 meses, de raza caucásica, que consulta por incremento de peso desde los ocho años de edad. Antecedentes familiares Madre: diabetes tipo 2 (en tratamiento con dieta e hipoglucemiantes orales), talla: 160 cm, menarquia a los 12 años, G-A-V: 3-0-3. Padre: obesidad e hipercolesterolemia (en tratamiento con estatinas), talla: 170 cm, desarrollo puberal normal. Talla genética: 158 ± 5 cm. Tío materno y abuela materna diabetes tipo 2. Antecedentes personales Embarazo controlado, normal. Parto a las 39 semanas, eutócico, vaginal. PRN: 3.050 g, LRN: 49 cm. Periodo neonatal normal. Pruebas metabólicas normales. Lactancia materna cuatro meses, sin intolerancias alimentarias. Desarrollo psicomotor normal. Inmunizaciones correctas. Menarquia a los 12 años y 6 meses, ciclos irregulares. Exploración física Edad: 14 años y 6 meses; peso: 71 kg (+2,73 DE), talla: 159 cm (P 50-75); IMC: 28,08 (+ 2,57 DE). Perímetro de cintura 90 cm (P>90). T.A.: 100/60 mmHg. Buen estado general. Coloración normal de piel y mucosas. Obesidad central. Estrías de distensión en abdomen y cara interna de muslos. Acantosis en cuello. Cuello: no se palpa bocio. ACP: normal. Abdomen: blando, depresible, sin visceromegalias. Genitales femeninos normales. Tanner V (telarquia 5, pubarquia 5, axilarquia c). Resto de la exploración normal. Estudios complementarios Hemograma: fórmula y recuentos normales. Bioquímica general: normal. Lipidograma: CT: 280 mg/dl (vn: 120-200), Triglicéridos: 240 mg/dl (vn: < 150), C-HDL: 35 mg/dl (vn: 35-75), C-LDL: 210 mg/dl, C-VLDL: 34 mg/dl. Función tiroidea: TSH: 4,5 mUI/ml (vn: 0,5-6), T4 libre: 0,99 ng/dl (vn: 0,65-1,4). Glucemia: 110 mg/dl (vn: 70-100). Insulina basal: 25 µUI/ml. Sobrecarga oral de glucosa: Glucemia basal: 110 mg/dl, a los 120 minutos: 190 mg/dl. Insulina basal: 38 µUI/ml, pico: 250 µUI/ml, a los 120 minutos: 100 µUI/ml. HbA1c: 6,9%. Cortisol libre en orina de 24 horas: 35 µg/24 h (vn: 30-243). Ecografía hepática: signos de marcada esteatosis hepática.
|
 |
| Regreso a las bases |
D. Yeste, A. Carrascosa
Hospital Universitari Vall d’Hebron de Barcelona. Servicio de Endocrinología Pediátrica. Universidad Autónoma de Barcelona
Pediatr Integral 2015; XIX (6): 436.e1-436.e9
Introducción
El crecimiento y la mineralización del esqueleto óseo son procesos que se inician durante el desarrollo fetal y continúan a ritmos diferentes durante la infancia y adolescencia hasta la tercera década de la vida, momento en que se alcanza el pico máximo de masa ósea. A partir de entonces la masa ósea se mantiene constante hasta la quinta-sexta décadas, edad en la que comienza a declinar progresivamente. El capital óseo con el que se llega a la edad adulta es por tanto un factor condicionante del potencial desarrollo de osteoporosis que se acompaña con la edad. Factores genéticos, nutricionales, hormonales y estilos de vida desempeñan un papel determinante de la mineralización del esqueleto. En consecuencia, las patologías crónicas que afecten a estos factores durante la infancia y adolescencia pueden ser condicionantes de una deficiente o insuficiente mineralización ósea en estas edades de la vida y ser responsables de estados de osteopenia que incrementen el riesgo de desarrollar patología osteoporótica en edades tempranas o tardías de la vida. Por consiguiente, es del máximo interés que todas las poblaciones pediátricas, tanto normales como con patología, lleguen a la tercera década de la vida con un nivel óptimo de masa ósea para prevenir el ulterior desarrollo de la osteoporosis(1,2) (Fig. 1).
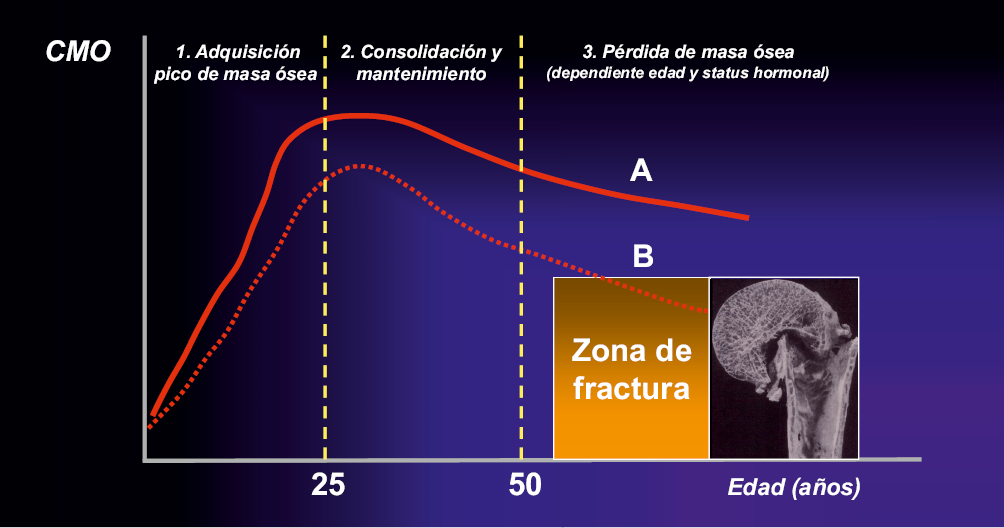
Figura 1. Evolución de la masa ósea desde el nacimiento a la edad adulta. A. Población normal. B. Población con osteopenia iniciada en la infancia y/o adolescencia.
Crecimiento y mineralización del tejido óseo
El hueso es un tejido conjuntivo que posee la característica de tener una matriz extracelular mineralizada, convirtiéndose en una estructura apta para el soporte del organismo. Es un tejido metabólicamente muy activo, sometido a un proceso constante de aposición y resorción. Alberga en su interior la médula ósea hematopoyética y es reservorio de importantes iones que pueden ser almacenados y liberados de forma controlada. Se desarrolla a partir de moldes cartilaginosos y su volumen aumenta progresivamente durante los periodos embrionario, fetal y postnatal, estando totalmente formado al finalizar la pubertad, coincidiendo con el momento en que se alcanza la talla adulta.
El proceso de osificación se desarrolla de dos modos diferentes: la osificación endocondral, a partir del cartílago de crecimiento (huesos largos) y la osificación intramembranosa a partir de estructuras mesenquimales (huesos planos). El crecimiento en grosor se realiza a partir de la capa de osteoblastos del periostio del hueso previamente formado. Macroscópicamente se distinguen dos formas de hueso: el hueso cortical, más compacto y resistente que se localiza en la periferia del hueso, y el hueso trabecular dispuesto en forma de láminas, menos compacto, pero metabólicamente más activo, localizándose en el interior del hueso en contacto con la médula ósea.
Las células óseas provienen de dos estirpes. Los preosteoblastos, los osteoblastos y los osteocitos son de origen mesenquimal y los osteoclastos de origen hematopoyético. Los osteocitos son las células maduras localizadas en el interior de la matriz ósea, están interconectadas a través de sus prolongaciones citoplasmáticas y desempeñan un importante papel en la regulación del intercambio de minerales, así como en la integración y respuesta a estímulos físicos y químicos procedentes de los tejidos adyacentes. Constituyen más del 90% del total de células del hueso. Los osteoblastos son responsables de la síntesis de la matriz ósea y regulan la actividad de los osteoclastos a través de la síntesis de citocinas y factores de crecimiento. Los osteoclastos son grandes células multinucleadas provenientes de los monocitos y encargadas de la resorción de la matriz ósea. Osteoblastos y osteoclastos se acoplan en unidades funcionales de resorción y neoformación ósea denominadas de remodelado óseo.
La matriz ósea está formada por un componente orgánico y otro inorgánico. El componente orgánico está constituido en un 90% por fibras de colágeno tipo I, y en el 10% restante, por proteoglucanos y otras proteínas no colágenas. El componente inorgánico está integrado por sales de hidroxiapatita depositadas entre las fibras de colágeno, carbonato cálcico, magnesio, sodio y potasio. El componente orgánico representa un 25% del peso óseo, el componente inorgánico un 70% y el restante 5% corresponde al agua. El depósito, en concentraciones adecuadas, de estas sales minerales en la matriz junto a la orientación anatómica de las fibras de colágeno mineralizadas, confiere al hueso las características de rigidez y elasticidad que le permiten ser soporte del organismo y resistir las cargas y fuerzas de tracción a las que constantemente están sometidas las estructuras óseas. Una mineralización insuficiente y la desestructuración de la arquitectura ósea pueden ser el origen de la aparición de fracturas osteoporóticas.
El hueso es un tejido metabólicamente muy activo, estando sometido a un proceso continuo de neoformación. Durante la infancia y la adolescencia hasta la adquisición de la talla adulta concurren dos fenómenos: formación de nuevo hueso a partir del cartílago de crecimiento (osificación endocondral) y resorción-neoformación de la matriz extracelular previamente sintetizada (acción de osteoblastos y osteoclastos). Ambos fenómenos se combinan y acoplan teniendo como resultado la adquisición la masa ósea (Fig. 2). Durante la edad adulta la masa ósea se mantiene y durante las últimas décadas de la vida disminuye la neoformación ósea, el balance se negativiza y conlleva una disminución progresiva de la masa ósea.

Figura 2. Actividad de remodelado óseo. Acoplamiento de la actividad de los osteoclastos y osteoblastos. Resorción y neoformación ósea.
La cantidad total de calcio depositada en el esqueleto de un recién nacido se incrementa desde unos 22 g (8 g/kg de peso) hasta unos 1.300 g (19 g/kg de peso) en el adulto. Las cifras correspondientes de fósforo pasan de 17 g en el recién nacido (5,8 g/kg de peso) a 700 g (10 g/kg de peso) en el adulto. Se estima aproximadamente que entre un 7,5% y un 10% del volumen óseo total del organismo adulto es renovado anualmente(3).
Masa ósea. Concepto de osteopenia y de osteoporosis
El término de masa ósea define la cantidad total de tejido óseo del organismo y depende del volumen del esqueleto y de la cantidad de células y matriz extracelular mineralizada, en él albergadas. En condiciones fisiológicas, la cantidad total de sales minerales depositadas en la matriz por unidad de volumen es relativamente constante; sin embargo, en situaciones patológicas la cantidad de sales minerales puede ser superior (osteopetrosis) o inferior (raquitismo/osteomalacia).
La osteoporosis se define como una situación en la que existe una pérdida global de masa ósea. La celularidad y los componentes orgánico e inorgánico de la matriz están disminuidos. La disminución de la matriz extracelular puede ser homogénea y afectar por igual al componente orgánico e inorgánico, o puede afectar más al componente mineral que al componente orgánico. La osteoporosis puede ser uniforme en todo el hueso o afectar más a unas partes que a otras del mismo hueso. El resultado final siempre es la pérdida de la arquitectura normal del hueso e implica una disminución de su resistencia y elasticidad, teniendo como consecuencia la posible aparición de fracturas patológicas.
Osteopenia y osteoporosis son dos términos que definen grados diferentes de pérdida de la masa ósea. El desarrollo de métodos no invasivos para cuantificar la masa ósea ha permitido valorar el contenido mineral óseo en diversas regiones anatómicas y definir los conceptos de osteopenia y de osteoporosis y su relación con la aparición de fracturas, en la edad adulta. Según los criterios de la Organización Mundial de la Salud, los valores de densidad mineral ósea (DMO) comprendidos entre -1 y -2,5 desviaciones estándar (DE) de los valores de la media correspondientes a una población adulta de similar edad y sexo definen el concepto de osteopenia. Cuando estos valores son inferiores a -2,5 DE definen el concepto de osteoporosis; con estos valores ya existe un riesgo franco para la aparición de fracturas óseas, pero no significa que todos los sujetos que los tengan las vayan a presentar necesariamente.
A diferencia de lo que ocurre en la población adulta, en la que ya se ha alcanzado el pico de masa ósea, y los criterios de osteopenia y osteoporosis reflejan el riesgo para la aparición de fracturas patológicas, ya que las posibilidades de recuperación son limitadas, en la infancia y la adolescencia, la masa ósea se está adquiriendo y valores bajos de masa ósea pueden recuperarse con la terapia adecuada en muchas ocasiones. Por esta razón, los conceptos de osteopenia y osteoporosis no pueden tener el mismo significado que en la edad adulta y, en general, se prefiere hablar de valores bajos de masa ósea en relación con los de una población de similar edad, sexo y estadio puberal, categorizando estos valores en forma de valor z-score. En Pediatría y por debajo de los 20 años de edad, se recomienda utilizar el concepto de “densidad mineral baja o disminuida para la edad cronológica” cuando los valores de z-score son inferiores a -2.
La osteopenia/osteoporosis se clasifica en dos tipos: primaria y secundaria. La primaria se refiere a aquellas situaciones en las que la pérdida de masa ósea está relacionada con procesos fisiológicos, como la menopausia y el envejecimiento. La secundaria se refiere a situaciones clínicas de etiología bien definida: trastornos nutricionales, hormonales y de la estructura de la matriz ósea. La osteopenia/osteoporosis primaria es propia del adulto y puede prevenirse durante la infancia y adolescencia logrando un pico óptimo de masa ósea. La osteopenia/osteoporosis secundaria puede presentarse en cualquier edad. Cuando ocurre durante la infancia y adolescencia (“densidad mineral baja para la edad cronológica”), la consecución de un pico de masa ósea adecuado puede verse seriamente afectada(4,5).
Factores reguladores de la masa ósea
Muchos son los factores que regulan la adquisición de la masa ósea: la carga genética, la nutrición, los estilos de vida, la actividad física, diferentes hormonas, múltiples factores locales de crecimiento y algunas citocinas (Fig. 3).

Figura 3. Factores reguladores de la masa ósea.
Durante la infancia y la adolescencia favorecen el anabolismo óseo y la adquisición del pico de masa ósea. Durante la edad adulta contribuyen al equilibrio entre resorción y neoformación óseas y favorecen el mantenimiento de la masa ósea(3,5).
Factores genéticos
Diversos estudios han evaluado que los factores genéticos pueden explicar entre un 60-80% de la variabilidad de la masa ósea en la población normal. Los hijos tienden a tener una masa ósea similar a la de sus padres. Esta aseveración ha sido comprobada en varios estudios realizados en gemelos y en parejas de madres e hijas y de padres e hijos. Los gemelos monocigóticos tienen una densidad mineral ósea más concordante que los gemelos dicigóticos. Así mismo, también se ha comprobado que los familiares de personas con osteoporosis tienen valores de densidad mineral ósea inferiores a los de la población normal. Aceptándose que la regulación de la masa ósea es un proceso poligénico, en el curso de estos últimos años una parte importante de la investigación sobre marcadores genéticos se ha centrado en el estudio de genes de receptores hormonales, genes de hormonas, genes de factores de crecimiento, genes de factores de transcripción y genes de proteínas de la matriz del hueso.
Actividad física
La actividad física es un determinante mayor de la masa ósea. Regula la síntesis del componente orgánico de la matriz ósea, el depósito de sales minerales, la orientación espacial de las fibrillas de colágeno mineralizadas y la orientación espacial de la arquitectura ósea. Sus efectos van en el sentido de optimizar la fuerza y la resistencia del hueso frente a los micro y macrotraumatismos a los que está continuamente sometido. Los niños y adolescentes con actividad física apreciable tienen valores mayores de densidad mineral ósea que aquellos que tienen una actividad sedentaria. Las atletas de élite, corredoras y gimnastas, incluso a pesar de presentar cierto grado de hipogonadismo, tienen valores de densidad mineral ósea superiores a los individuos sedentarios. Estudios controlados en adolescentes con diversos grados de actividad física, han mostrado que el ejercicio prolongado estimula la aposición de masa ósea.
Estilos de vida
El consumo excesivo de alcohol y el hábito de fumar también ha sido relacionado con valores de densidad mineral ósea bajos y con una mayor incidencia de fracturas óseas.
Factores hormonales y factores locales de crecimiento
La parathormona tiene un efecto dual sobre el metabolismo óseo. Concentraciones séricas fisiológicas estimulan el anabolismo óseo; por contra, concentraciones séricas elevadas favorecen el catabolismo óseo. A nivel renal estimula la actividad 1-a-hidroxilasa, y la síntesis del metabolito activo de la vitamina D, el calcitriol 1,25-(OH)2D, favoreciendo indirectamente la absorción intestinal de calcio. La calcitonina inhibe la acción de los osteoclastos y por este motivo ha sido utilizada para el tratamiento de la osteoporosis. La hormona de crecimiento regula junto con la nutrición la síntesis del factor de crecimiento IGF-I con importantes efectos anabólicos sobre el cartílago de crecimiento y el hueso. En este sentido, los niños y adolescentes afectos de deficiencia de hormona de crecimiento presentan una masa ósea disminuida. Los esteroides gonadales (estradiol y andrógenos) son agentes reguladores del crecimiento y de la mineralización ósea y a través de las influencias que la nutrición tiene sobre su secreción, esta última también regula estos procesos. Su presencia es necesaria para realizar el brote de crecimiento puberal y para la adecuada mineralización del cartílago de crecimiento y del hueso. Situaciones clínicas de hipogonadismo en ambos sexos condicionan una disminución de la masa ósea. Las hormonas tiroideas estimulan la mineralización del cartílago de crecimiento y regulan la actividad de remodelado óseo; en situación de hipertiroidismo se observa disminución de masa ósea. Los glucocorticoides a dosis suprafisiológicas inhiben tanto el crecimiento como la mineralización del hueso. Sin embargo, a dosis fisiológicas o dosis discretamente superiores, como las administradas en la hiperplasia suprarrenal congénita, no tienen repercusiones negativas importantes sobre la masa ósea, aunque sí sobre el crecimiento.
La leptina, hormona sintetizada por los adipocitos y que informa al hipotálamo de las reservas energéticas, ha sido considerada también como un posible mediador que estimularía el gonadostato. Más recientemente, un efecto de la leptina sobre el metabolismo óseo ha sido también sugerido. Finalmente, existen múltiples factores locales de crecimiento y citocinas que regulan también el metabolismo óseo.
Factores nutricionales
La nutrición regula el proceso de adquisición y mantenimiento de la masa ósea a través de diversos mecanismos:
• Aporta nutrientes energéticos y plásticos necesarios para la multiplicación celular y la síntesis de la matriz del cartílago y del hueso.
• Aporta vitaminas que regulan la formación de esta matriz.
• Aporta sales minerales de calcio, fósforo y magnesio que se depositan en la matriz.
• Condiciona la síntesis de hormonas y factores locales de crecimiento que regulan globalmente, tanto el proceso de crecimiento en longitud de los huesos como el de su mineralización: hormona de crecimiento, IGF-I y esteroides gonadales.
La malnutrición condiciona una situación de hipogonadismo hipogonadotropo. Cuando se produce antes de la pubertad, condiciona un retraso en la aparición del desarrollo puberal; cuando se produce durante el desarrollo puberal, condiciona un paro en el desarrollo de la pubertad, y cuando se produce en la adolescencia o en el adulto condiciona una abolición de la función gonadal normal, manifestándose mediante una amenorrea en las mujeres y un hipogonadismo en los varones. No son completamente conocidos los mecanismos a través de los cuales el estado nutricional puede regular la secreción de gonadotrofinas.
Calcio y mineralización ósea
El calcio es el quinto elemento del organismo en abundancia. Un 99,4% está depositado en el esqueleto óseo, un 0,5% en los tejidos blandos y el 0,4% restante en el líquido extracelular, fundamentalmente en el plasma. La cantidad total de calcio depositada en el esqueleto óseo pasa de 30 g en el recién nacido a 1.300 g en el adulto, manteniéndose estable desde entonces hasta las últimas décadas de la vida, momento en que existe una pérdida relacionada con la disminución fisiológica de la masa ósea. El balance cálcico es netamente positivo durante la infancia y adolescencia, es neutro durante la edad adulta y está relacionado con el proceso de adquisición y mantenimiento de la masa ósea.
El depósito de calcio en el hueso depende de la cantidad total de calcio presente en la alimentación, de su tasa de absorción intestinal y de su eliminación urinaria. La cantidad total de calcio en la dieta puede variar desde 300 a 2.000 mg/día según el tipo de dieta realizada. La absorción intestinal de calcio varía según la edad. Durante los dos primeros años de la vida, período de tiempo en el cual la aposición de calcio en el esqueleto es máxima, la capacidad intestinal de absorción de calcio se estima que puede llegar hasta un 40% del total ingerido. Esta cantidad puede aumentar hasta un 70% cuando la fuente de calcio es la leche materna. Durante la infancia y hasta el inicio del desarrollo puberal, esta puede ser hasta un 27%, para incrementarse durante el desarrollo puberal hasta un 30% y disminuir posteriormente en la edad adulta desde un 20% en los adultos jóvenes (hasta los 30 años de edad) hasta un 4-8% en edades posteriores. Un 90% de la absorción intestinal de calcio se realiza en el intestino delgado y solo un 10% en el intestino grueso. La absorción intestinal de calcio se realiza en el yeyuno y en el íleon y depende de la biodisponibilidad del calcio y de la vitamina D. La vitamina D regula la calbindina, proteína transportadora de calcio. La biodisponibilidad del calcio depende de los compuestos químicos de los que forma parte y de la presencia de otros factores presentes en la dieta (fibra, oxalatos, fitatos).
En situaciones clínicas de bajo aporte de calcio, su absorción intestinal puede incluso incrementarse por encima de los niveles antes comentados, siempre que los niveles plasmáticos de 1,25-(OH)2D sean adecuados, con objeto de permitir una aposición ósea correcta, aunque aportes inferiores a 450 mg/día han mostrado ser claramente insuficientes para mantener un adecuado ritmo de incremento de la masa ósea. Por contra, situaciones de aporte excesivo de calcio no comportan un incremento lineal de la absorción intestinal del mismo, existiendo incluso unos valores a partir de los que ya no se incrementa la absorción intestinal de calcio.
Una cuestión debatida durante estos últimos años es la relación existente entre aporte de calcio en la dieta y masa ósea. Se acepta que existe un umbral fisiológico para la absorción de calcio dependiente de la edad y en íntima relación con las necesidades de calcio para lograr un ritmo normal de adquisición de masa ósea. Aunque este umbral puede ser forzado con la suplementación de calcio, no se conocen los efectos a largo término de este hecho, siendo necesarios estudios prospectivos que indiquen:
• Qué épocas de la vida son más sensibles a esta suplementación: infancia, niñez, desarrollo puberal, adolescencia o adulto joven.
• Cuáles son las necesidades óptimas para cada época.
• Si los cambios inducidos en la masa ósea son permanentes o desaparecen al suprimir la suplementación.
• Si esta suplementación resulta en un pico de masa ósea superior.
• Si este pico de masa ósea es beneficioso o no para evitar la aparición de fracturas osteoporóticas.
Responder a todas estas cuestiones es difícil y requiere estudios a muy largo término. Mientras tanto, parece útil seguir las recomendaciones de aporte de calcio sugeridas en diversas reuniones de consenso y por diferentes sociedades médicas y lograr que todos los niños y adolescentes tengan niveles óptimos de vitamina D.
Las recomendaciones actuales de aporte de calcio en la dieta fueron revisadas a finales de 2010, por el Food and Nutrition Board del Instituto de Medicina de la Academia Americana de Ciencias y varían entre los 200 mg para los lactantes a 1.300 mg para los adolescentes. Las principales fuentes alimentarias de calcio las constituyen: los productos lácteos, el pan, los huevos y los cítricos.
En resumen, teniendo en cuenta la variabilidad en la absorción intestinal de calcio según las diferentes edades e incluso la capacidad de incrementarse en situaciones de aporte cálcico restringido, y que la vitamina D es el mayor agente responsable de la absorción intestinal de calcio, parece razonable recomendar que si el aporte de vitamina D es suficiente, no son necesarios aportes superiores de calcio a los recomendados, para adquirir y mantener la masa ósea. Aportes más elevados de calcio podrían condicionar una hipercalciuria y el riesgo relativo de nefrocalcinosis, particularmente si se asocian a dosis superiores a las recomendadas de vitamina D, tal como se ha observado en la intoxicación por vitamina D. La suplementación de calcio solo estaría indicada cuando las ingestas son inferiores a las recomendadas, particularmente durante los períodos de máxima acreción de masa ósea: los primeros años de vida y el desarrollo puberal. La suplementación de calcio en las poblaciones con trastornos de la absorción intestinal y con necesidades fisiológicas aumentadas (prematuridad, embarazo y lactancia durante la adolescencia), siempre tendrá como objeto no sobrepasar las recomendaciones anteriormente comentadas.
Fósforo y mineralización ósea
El fósforo es el sexto elemento del organismo en cantidad. Un 85% está unido al calcio en la matriz del esqueleto en forma de cristales de hidroxiapatita. Un 14% forma parte de los tejidos blandos y un 1% está en el espacio extracelular. Las concentraciones plasmáticas de fósforo inorgánico se mantienen entre 4 y 7 mg/dl y no tienen el papel trascendental de las de calcio iónico. El balance de fósforo durante la infancia y adolescencia es netamente positivo, estimándose en unos 90-100 mg/día, para permitir que los depósitos óseos pasen de 17 g en el recién nacido a 700 g en el adulto. Aproximadamente, la cantidad de fósforo depositada en el esqueleto óseo representa la mitad de la de calcio. La presencia de fósforo en los alimentos es universal y una dieta variada cubre las necesidades diarias, sin que se hayan descrito situaciones clínicas carenciales.
Vitamina D y mineralización ósea
Los precursores de vitamina D (colecalciferol, ergocalciferol) no poseen por sí mismas, a dosis fisiológicas, actividad biológica. De forma similar, a las formas principales circulantes de la hormona 25(OH)D, no se les conoce una actividad específica. Estas últimas moléculas y los metabolitos precursores de vitamina D son consideradas las principales formas de almacenamiento y depósito de vitamina D en el organismo y precisan su conversión a calcitriol 1,25-(OH)2D para ejercer sus efectos biológicos sobre sus tres órganos diana tradicionales: el intestino, el hueso y el riñón. A nivel intestinal, el calcitriol incrementa la absorción de calcio y fósforo procedentes de la dieta, adaptando este proceso a las fluctuaciones de su aporte alimentario. Incrementa los niveles intracelulares de las proteínas transportadoras de calcio (calbindina) y la expresión de canales selectivos para la absorción del calcio en el enterocito. En el tejido óseo, el 1,25-(OH)2D es un agente esencial del desarrollo, crecimiento y mineralización del tejido óseo y regula la actividad de remodelado óseo. Sus mecanismos reguladores no son completamente conocidos, aunque diversos estudios de base experimental ponen de manifiesto que posiblemente el papel principal de la vitamina D en el tejido óseo sea el de proveer los minerales necesarios para promover la mineralización del tejido osteoide. En el riñón, el 1,25-(OH)2D, además de regular su propia síntesis, incrementa la eficiencia de la reabsorción de calcio y fósforo en el túbulo distal a través de la expresión y regulación de transportadores de calcio (calbindina D28k, calbindina D9k) y de canales epiteliales de calcio (TRPV5 y TRPV6). Un interés particular durante los últimos años ha sido dado al receptor de la vitamina D, en relación con la adquisición de la masa ósea, y en este sentido, diversos trabajos han asociado la presencia de ciertos polimorfismos de este receptor con la masa ósea(5,6).
Métodos para valorar la masa ósea y el metabolismo del hueso
Métodos no invasivos
Las técnicas no invasivas han contribuido a conocer los patrones normales del proceso de adquisición de la masa ósea durante la infancia y adolescencia y a detectar poblaciones pediátricas de riesgo. La densitometría fotónica simple, la densitometría fotónica dual, la densitometría radiológica de doble energía, la tomografía axial computerizada, la medición del espesor de las corticales de las falanges de los huesos de la mano y los ultrasonidos son las más utilizadas. En todas, menos en los ultrasonidos, existe un grado mayor o menor de radiación del paciente. De entre todas, la densitometría radiológica de doble energía (DEXA) es la más adecuada para la cuantificación de la masa ósea en Pediatría, por su alto índice de reproductibilidad (99%), su escaso error de precisión (1%), el limitado tiempo que se precisa para su realización (3-5 minutos) y su mínima dosis de radiación (0,02% de límite anual establecido para la población).
La masa ósea evaluada mediante densitometría dual de rayos X y expresada como DMO (gramos de hidroxiapatita/cm2), se puede evaluar en la región lumbar, femoral y en todo el esqueleto. Se incrementa progresivamente desde el nacimiento hasta la edad de 20-25 años, siendo los primeros años de la vida y el desarrollo puberal los períodos de máximo crecimiento en longitud del esqueleto y de máximo incremento en la DMO.
Los ultrasonidos son una técnica no invasiva y exenta de radiaciones, que también se ha utilizado para cuantificar la masa ósea. Las falanges de extremidades superiores y el calcáneo son las dos regiones anatómicas valoradas. Los datos disponibles hoy día indican que mientras los datos obtenidos en el calcáneo pueden ser representativos de la masa ósea, del riesgo de osteoporosis y de las fracturas osteoporóticas, los datos obtenidos en las falanges de las extremidades superiores están en curso de validación.
Marcadores bioquímicos
Los marcadores bioquímicos del metabolismo óseo son moléculas sintetizadas por los osteoblastos y osteoclastos o moléculas procedentes de la reabsorción de la matriz ósea. Pueden cuantificarse en plasma y en orina y se clasifican en dos grupos: marcadores de neoformación ósea y marcadores de resorción ósea.
Los marcadores de neoformación ósea son moléculas sintetizadas por los osteoblastos, siendo la osteocalcina y la fosfatasa alcalina (FA) los mejor caracterizados, los más utilizados en clínica y los que mejor relación tienen con los valores de densidad mineral ósea. Los marcadores de resorción ósea son moléculas sintetizadas por los osteoclastos (fosfatasa ácida tartratorresistente) o moléculas que proceden de la degradación de la matriz ósea en el curso de su resorción (hidroxiprolina, piridinolinas, péptidos derivados de la degradación de moléculas precursoras del colágeno: telopéptido carboxiterminal y telopéptido aminoterminal). La deoxipiridinolina cuantificada en orina y el telopéptido carboxiterminal del colágeno tipo I (ICTP) son los marcadores más específicos, más utilizados en clínica y los que mejor relación guardan con los valores de densidad mineral ósea.
Patrones de mineralización ósea normal en la infancia y adolescencia evaluados mediante DEXA
La DEXA ha contribuido a conocer los patrones normales de adquisición de la masa ósea durante la infancia y la adolescencia y a detectar poblaciones pediátricas de riesgo. Nosotros hemos estudiado la evolución de la masa ósea durante la infancia y la adolescencia a nivel de la columna lumbar (L2-L4) en un estudio transversal realizado en 256 niños y 215 niñas de edades comprendidas entre los tres meses y los 21 años y hemos establecido el patrón de adquisición de masa ósea en nuestra población (Figs. 4 y 5). Mediante esta técnica, se cuantifica la cantidad total de mineral (CMO) depositado en tres cuerpos vertebrales (L2-L4) y se divide por el área proyectada de los tres cuerpos vertebrales. Los resultados se expresan como gramos de hidroxiapatita/cm2y representa la densidad mineral ósea (DMO).

Figura 4. Valores de densidad mineral ósea (gramos de hidroxiapatita/cm2) y (gramos de hidroxiapatita/cm3) a nivel de columna vertebral (L2-L4) en nuestra población en función de la edad y sexo.

Figura 5. Evolución de la densidad mineral ósea (gramos de hidroxiapatita/cm2) en la infancia y adolescencia (media ± 1 DE).
La masa ósea se incrementa progresivamente desde el nacimiento hasta la edad de 20-25 años, con ritmos diferentes según el período considerado. Desde el nacimiento hasta la edad de 3 años, el incremento representa aproximadamente un 30% del incremento total, desde los 3 años hasta el inicio del desarrollo puberal se incrementa un 20%, durante el desarrollo puberal se incrementa otro 30-40% y desde la finalización del crecimiento hasta la edad de 21 años se incrementa otro 15-20%. Estos datos indican que los primeros años de la vida y el desarrollo puberal son los períodos de máximo crecimiento en longitud del esqueleto y de máximo incremento en la DMO, que la mineralización del esqueleto se prolonga más allá de la finalización del crecimiento en longitud y se continúa durante la adolescencia tardía hasta los 25 años de edad, y que en estas épocas de la vida son las de mayor riesgo para no alcanzar una masa ósea adecuada, si en ellas inciden procesos patológicos que condicionen un menor ritmo de ganancia y/o pérdida de masa ósea(7-9)(Fig. 6).

Figura 6. Incrementos anuales de densidad mineral ósea (gramos de hidroxiapatita/cm2) en la infancia y adolescencia. Los tres primeros años de la vida y la adolescencia son las etapas de mayor depósito de sales minerales en el esqueleto en desarrollo.
Poblaciones pediátricas con riesgo de masa ósea disminuida
Cuatro grandes grupos de enfermedades pueden interferir con el proceso de adquisición de masa ósea en la infancia y adolescencia: enfermedades estructurales (osteogénesis imperfecta), nefropatías, trastornos nutricionales (síndromes de malabsorción intestinal, situaciones de malnutrición crónica y situaciones de carencia de vitamina D o anomalías en su mecanismo de acción) y endocrinopatías, siendo, con mucho, estos dos últimos los más frecuentes (Tabla I).
El pediatra de asistencia primaria tiene una gran responsabilidad en la identificación de estas poblaciones pediátricas con riesgo de adquisición de una masa ósea disminuida y también en la adopción de todas aquellas medidas tanto preventivas como terapéuticas dirigidas a promover una salud ósea óptima durante la infancia y adolescencia y que eviten la aparición de la osteoporosis en edades tempranas de la vida(10).
Bibliografía
1. Carrascosa A, Gussinyé M, Yeste D, Del Rio L, Audi L. Bone mass acquisition during infancy, childhood and adolescence. Acta Paediatr 1995; suppl. 411: 18-23.
2. Davies JH, Evans BA, Gregory JW. Bone mass acquisition in healthy children. Arch Dis Child. 2005; 90: 373-78.
3. Carrascosa A, Gussinyé M, Yeste D. En Tratado de endocrinología de la infancia y de la adolescencia. 2ª Edición. Argente J, Carrascosa A, Gracia R, Rodríguez F editores. Capítulo 54. “Masa ósea, osteopenia y osteoporosis”, págs. 1353-82. Ediciones Doyma S.L. Barcelona. 2000.
4. Van Kuijk C. Pediatric bone densitometry. Radiol Clin North Am. 2010; 48: 623-27.
5. Yeste D, Carrascosa A. Osteopenia/osteoporosis de origen nutricional. Rev Esp Ped. 2003; 59: 99-105.
6. Carrascosa A, Ballabriga A. Masa ósea y nutrición. En: Nutrición en la Infancia y Adolescencia; Ballabriga A, Carrascosa A (editores). Ergón, Madrid 2006, págs. 919-49.
7. Del Río L, Carrascosa A, Pons F, Gussinyé M, Yeste D, Domenec FM. Bone mineral density of the lumbar spine in caucasian mediterranean spanish children and adolescents. Changes related to age, sex and puberty. Pediatr Res. 1994; 35: 362-66.
8. Yeste D, Del Río L, Carrascosa A. En Tratado de endocrinología de la infancia y de la adolescencia. 2ª Edición. Argente J, Carrascosa A, Gracia R, Rodriguez F, editores. Capítulo 58. “Valores de contenido mineral óseo, densidad mineral ósea (DMO) y densidad mineral ósea volumétrica en niños y adolescentes en la columna lumbar y en el fémur”, págs. 1501-13. Ediciones Doyma S.L. Barcelona. 2000.
9. Shaw NJ. Osteoporosis in paediatrics. Arch Dis Child Educ Pract Ed. 2007; 92: 169-75.
10. Sopher AB, Fennoy I, Oberfield SE. An update on childhood bone health: mineral accrual, assessment and treatment. Curr Opin Endocrinol Diabetes Obes. 2015; 22: 35-40.
| 10 Cosas que deberías saber sobre…seguridad vial infantil |
E. Pérez Costa, D. Rodríguez Álvarez, E. Ballesteros Moya, F. Campillo i López
 Los accidentes de tráfico son la primera causa de muerte en el grupo de población de 1 a 14 años.
Los accidentes de tráfico son la primera causa de muerte en el grupo de población de 1 a 14 años.
 El 30% de los niños viaja incorrectamente protegido. Las excusas favoritas son la pereza y la brevedad del trayecto.
El 30% de los niños viaja incorrectamente protegido. Las excusas favoritas son la pereza y la brevedad del trayecto.
 El uso de los dispositivos de seguridad infantil evitaría el 75% de las muertes infantiles y el 90% de los daños graves ocasionados por accidentes de tráfico.
El uso de los dispositivos de seguridad infantil evitaría el 75% de las muertes infantiles y el 90% de los daños graves ocasionados por accidentes de tráfico.
 La mayoría de los recién nacidos pueden usar indistintamente tanto cucos o capazos como sillas portabebés. Durante el primer año de vida y hasta que el niño pese 9 kg los bebés tiene que viajar mirando siempre hacia atrás.
La mayoría de los recién nacidos pueden usar indistintamente tanto cucos o capazos como sillas portabebés. Durante el primer año de vida y hasta que el niño pese 9 kg los bebés tiene que viajar mirando siempre hacia atrás.
 Las personas cuya estatura no alcance los 135 cm deben utilizar sistemas de retención adaptados a su peso y talla. Las personas cuya estatura sea igual o superior a 135 centímetros y no supere los 150 centímetros, podrán utilizar indistintamente un dispositivo de retención homologado adaptado a su talla y a su peso o el cinturón de seguridad para adultos.
Las personas cuya estatura no alcance los 135 cm deben utilizar sistemas de retención adaptados a su peso y talla. Las personas cuya estatura sea igual o superior a 135 centímetros y no supere los 150 centímetros, podrán utilizar indistintamente un dispositivo de retención homologado adaptado a su talla y a su peso o el cinturón de seguridad para adultos.
 Los niños no podrán utilizar un dispositivo de retención orientado hacia atrás, instalado en un asiento del pasajero protegido con un airbag frontal, a menos que haya sido desactivado.
Los niños no podrán utilizar un dispositivo de retención orientado hacia atrás, instalado en un asiento del pasajero protegido con un airbag frontal, a menos que haya sido desactivado.
 Las sillas se dividen en los siguientes grupos: grupo 0 o 0+ hasta 13 kg, deben colocarse siempre mirando hacia atrás. Grupo I de 9 a 18 kg, se sujetan con el cinturón de seguridad mirando hacia delante de forma habitual. Grupo II desde los 15 a los 25 kg, este tipo de asientos eleva a su ocupante para que el cinturón de seguridad se le ajuste correctamente. Grupo III desde los 22 hasta los 36 kg, similares al anterior.
Las sillas se dividen en los siguientes grupos: grupo 0 o 0+ hasta 13 kg, deben colocarse siempre mirando hacia atrás. Grupo I de 9 a 18 kg, se sujetan con el cinturón de seguridad mirando hacia delante de forma habitual. Grupo II desde los 15 a los 25 kg, este tipo de asientos eleva a su ocupante para que el cinturón de seguridad se le ajuste correctamente. Grupo III desde los 22 hasta los 36 kg, similares al anterior.
.
 En un taxi, cuando circulen en tráfico urbano podrá transportar a personas cuya estatura no alcance los 135 centímetros sin utilizar un dispositivo de retención homologado adaptado a su talla y a su peso, siempre que ocupen un asiento trasero.
En un taxi, cuando circulen en tráfico urbano podrá transportar a personas cuya estatura no alcance los 135 centímetros sin utilizar un dispositivo de retención homologado adaptado a su talla y a su peso, siempre que ocupen un asiento trasero.
 El asiento del pasajero delantero es mucho menos seguro que el asiento trasero y, en particular, que el asiento trasero central (el más seguro de todos).
El asiento del pasajero delantero es mucho menos seguro que el asiento trasero y, en particular, que el asiento trasero central (el más seguro de todos).
 Los niños aprenden fundamentalmente por imitación de conductas, si los niños nos ven ponernos el cinturón, ellos se lo pondrán.
Los niños aprenden fundamentalmente por imitación de conductas, si los niños nos ven ponernos el cinturón, ellos se lo pondrán.
Para saber aún más…
1. Instituto de Seguridad Vial, Fundación MAPFRE. Niños y seguridad vial. Disponible en http://www.fundacionmapfre.org/fundacion/es_es/images/estudio-ninyos-y-seguridad-vial_tcm164-12413.pdf.
2. Gómez Luque, MJ. La seguridad vial en los niños: cuestión de familia. Rev Pediatr Aten Primaria. 2007; 9: 31-40.
3. Dirección General de Tráfico. Disponible en www.dgt.es
 |
C. García Mauriño, A. Molina García
Residentes hospital infantil universitario La Paz
3. Role Play: Abdominal pain. Outpatient appointment.
Doctor: Hello, I’m Doctor Simmons. You’ve been given an appointment because last week you presented to the emergency room with your son, with a history of abdominal pain is that right?
Mother: Yes, I’ve been visiting many hospitals, but no one seems to understand my son’s illness.
Doctor: Tell me, when did it all start?
Mother: Since two months ago he has had stomach pain, which usually lasts 3 hours and then goes away by itself. At first, I wasn’t sure if it was real, because he complained but kept doing his normal every day activities. The thing is, the boy kept complaining day after day, and so I decided I should take him to be examined, just in case it was something bad.
Doctor: Has this pain been persistent in time? Does it hurt every day? Can you describe a pattern?
Mother: Well; the first couple of weeks it was during the afternoons, when he came back from school, but it became gradually less regular appearing even during the night, waking him up from sleep.
Doctor: Did the pain associate vomiting, fever, diarrhea or any urinary tract symptoms?
Mother: No, he has never vomited, but its true that last week he had loose stools for a couple of days. What I do have noticed is that he has less appetite than before.
Doctor: Have you noticed any recent weight loss?
Mother: Not really.
Doctor: Have any test been performed by any other physicians, or pills prescribed?
Mother: Yes, one of the doctors we saw tested his blood and urine and said everything was normal. He prescribed some antibiotics, but I never gave them to him.
Doctor: Although the symptoms you described, and the history of the abdominal pain, didn’t seem to correlate with any severe disease, during the examination we have found some abnormal signs, and we would like to perform an abdominal ultrasound apart from repeating both the urine and blood tests, in order to be able to identify what is causing the pain.
PHYSICAL EXAMINATION:
Good general condition. Well hydrated. Slightly obese.
Cardiac auscultation: regular, no heart murmur.
Pulmonary auscultation: good bilateral ventilation, no wheezes, ronchi or rubs.
HEENT: normal tonsils. Normal tympanic membranes. No adenopathy.
Abdomen: soft. Bowel sounds present, no bruits. Flat, not distended. Liver edge, spleen and kidney not felt. No masses. Slightly painfull with focal tenderness in the left flank. No rebound tenderness.
Neurological: awake, alert, and fully orientated.
KEY WORDS:
Outpatient appointment: cita en consultas externas.
Presented to the emergency room: consultar en urgencias.
Stomach pain: dolor de tripa.
Normal every day activities: actividades de la vida diaria.
Loose stools: deposiciones líquidas.
Weight loss: pérdida de peso.
Physician: médico.
Pills: pastillas.
Rubs: roce pleural.
Bowel sounds present: ruidos hidroaéreos presentes.
No bruits: no soplos abdominal.
Liver edge: reborde hepático.
Focal tenderness: defensa abdominal localizada.
No rebound tenderness: Blumberg negativo.
Abdominal ultrasound: ecografía abdominal.
 |
| A Hombros de Gigantes |
D. Gómez Andrés
F.E. Pediatría. Hospital Universitario Infanta Sofía.
Médico Asistente en Neurología Pediátrica. Hospital Universitario La Paz.
Trastornos del Desarrollo y Maduración Neurológica. IdiPaz-UAM.
| Las revisiones de pediatría que te pueden interesar publicadas en las revistas internacionales más importantes. |
Pediatr Integral 2015; XIX (6): 438.e1-438.e2
Pediatría General y Extrahospitalaria
★★★★★ Being baby friendly: evidence-based breastfeeding support. Arch Dis Child Fetal Neonatal Ed. 2015; 100(2): F173–8. PMID: 25293712
Los autores relatan los cambios provocados por el programa de promoción a la lactancia en el Reino Unido. En un artículo que no sigue un claro objetivo, los autores repasan datos muy interesantes sobre la lactancia materna en el sistema británico, que son en parte extrapolables a nuestro medio.
★★★★✩ The management of acute testicular pain in children and adolescents. BMJ. 2015; 350: h1563. PMID: 25838433
Resumen muy claro sobre el manejo del dolor testicular agudo en el paciente pediátrico.
★★★★✩ Teenagers with back pain. BMJ. 2015; 350: h1275. PMID: 25838410
Buen artículo que repasa el manejo de un problema relativamente frecuente. Los autores proponen un esquema de interrogatorio y examen físico muy interesante para conseguir ser sistemático. Recalcan la importancia de la “cronificación” de este dolor que puede ser sospechado a través de una herramienta de cribado.
★★★★✩ Joint hypermobility syndrome: a review for clinicians. J Paediatr Child Health. 2015; 51(4): 373–80. PMID: 25290912
Aunque la hipermovilidad es muy común en los pacientes pediátricos, algunos de estos niños presentan problemas musculoesqueléticos y de otros órganos conformando un síndrome de hipermovilidad articular que precisan un manejo diagnóstico-terapéutico específico. El diagnóstico se orienta a descartar enfermedades que presentan hipermovilidad articular (X-frágil, Klinefelter, enfermedades del colágeno…). Los pacientes con síndrome de hipermovilidad articular precisan de un manejo integral destinado a controlar el dolor musculoesquelético, evitar la lesión articular y de tejidos blandos, adaptar y promover la actividad física, manejar la fatiga, apoyar psicológicamente a pacientes que presenten problemas asociados y mejorar la función manual (sobre todo, en la escritura manual).
Dermatología
★★★★✩ Pityriasis versicolor. BMJ. 2015; 350: h1394. PMID: 25852089
Resumen sobre esta infección fúngica superficial producida por las especies Malassezia. El diagnóstico es habitualmente clínico basado en un exantema papular hipopigmentado o eritematoso crónico, pero pitiriásico. En ocasiones, se requieren estudios de laboratorios. Especialmente interesante es el repaso del diagnóstico diferencial. El tratamiento es generalmente tópico con ketoconazol o champús con sulfuro de selenio o piritionato de zinc.
★★★✩✩ What’s new with common, uncommon and rare rashes in childhood. Curr Opin Pediatr. 2015; 27(2): 261–6. PMID: 25689452
El autor discute avances sobre el intertrigo, el síndrome de shock tóxico, los exantemas por enterovirus, las manifestaciones cutáneas del Mycoplasma y el eritema recurrente del periné.
Digestivo
★★★★✩ Crohn disease and ulcerative colitis in children: an update for 2014. J Paediatr Child Health. 2015; 51(3): 266–70. PMID: 25039307
Útil revisión sobre la enfermedad inflamatoria intestinal orientada para pediatras generales. Está muy orientada a las pistas diagnósticas y revisan de forma muy general las opciones terapéuticas existentes.
Endocrinología
★★★★✩ Diagnostic value of serum IGF-1 and IGFBP-3 in growth hormone deficiency: a systematic review with meta-analysis. Eur J Pediatr. 2015; 174(4): 419–27. PMID: 25213432
Los resultados de este meta-análisis son bastante importantes a la hora de interpretar los resultados ante sospecha de déficit de GH. La IGF-1 tiene una sensibilidad de 66% y una especificidad del 69% respecto a un 49% y 79% de la IGFBP-3. En el caso de la IGF-1, los resultados parecen orientar a la existencia de sesgos de publicación y a que la inmunoradiometría es superior al radioinmunoensayo. También es bastante interesante la discusión donde los autores comentan problemas adicionales de estos biomarcadores.
Genética y Dismorfología
★★★★★ Phenotyping: targeting genotype’s rich cousin for diagnosis. J Paediatr Child Health. 2015; 51(4): 381–6. PMID: 25109851
Aunque era esperable, sigue siendo paradójico que sean los avances genéticos los que hayan provocado que la información clínica tradicional consistente en síntomas, signos y resultados analíticos esté recuperando una importancia que parecía que iban a perder dentro del diagnóstico. Sin embargo, estos avances seguramente provoquen cambios en nuestra forma de trabajo tradicional. Para poder avanzar en el conocimiento del fenotipo de enfermedades necesitamos crear ontologías que permitan la clasificación organizada de términos más precisos para referirnos a síntomas o signos, desarrollar métodos no invasivos que consigan ser objetivos en la caracterización de medidas clásicas, incorporar esta metodología en el trabajo clínico sin alargar ni complicar la atención, añadir métodos de diagnóstico asistido por ordenador y conseguir métodos para compartir datos respetando la confidencialidad y el trabajo de cada investigador.
★★★★✩ Genetic investigations in childhood deafness. Arch Dis Child. 2015; 100(3): 271–8. PMID: 25324569
El diagnóstico genético de la pérdida de audición es un tema complejo, pero los autores son capaces de resumir y transmitirlo claramente. Dividen las pérdidas de audición en sindrómicas y no sindrómicas, dedicando un resumen corto a cada diagnóstico genético.
Infectología
★★★★★ Ebola in children: epidemiology, clinical features, diagnosis and outcomes. Pediatr Infect Dis J. 2015; 34(3): 314–6. PMID: 25522340
Excelente resumen sobre la epidemia de Ébola desde una perspectiva pediátrica. A pesar de que los niños están relativamente protegidos de esta enfermedad por las formas de transmisión de la enfermedad, estos también padecen esta infección con alta mortalidad. Tristemente, existen pocos datos específicos sobre la afectación en edad pediátrica.
Neonatología
★★★★★ Hypoxic-ischemic encephalopathy: a review for the clinician. JAMA Pediatr. 2015; 169(4): 397–403. PMID: 25685948
Excelente resumen sobre el manejo clínico del paciente con encefalopatía hipóxico-isquémica neonatal. Es claro, conciso y orientado a comprender el proceso diagnóstico y de soporte de estos pacientes. Discute algunas incertidumbres sobre la hipotermia (ventana terapéutico, papel en el prematuro…), y terapias emergentes como el xenón, la eritropoyetina, la melatonina y el trasplante de células autólogas de cordón umbilical.
★★★★✩ TORCH infections. Clinics in Perinatology. 2015; 42(1): 77–103. PMID: 25677998
★★★★✩ Perinatal cytomegalovirus and varicella zoster virus infections: epidemiology, prevention, and treatment. Clinics in Perinatology. 2015; 42(1): 61–75. PMID: 25677997
Dos buenos artículos que resumen las principales infecciones de transmisión vertical.
Neurología
★★★★★ Applications of optical coherence tomography in pediatric clinical neuroscience. Neuropediatrics. 2015; 46(2): 88–97. PMID: 25803824
La OCT es probablemente una tecnología emergente que ha llegado para quedarse en la Neuropediatría y en la Oftalmología pediátrica. La posibilidad de realizar una microscopía in vivo de la retina parece ciencia ficción, pero los resultados que ofrece la OCT son verdaderamente próximos. Aunque los autores revisan el papel de esta técnica en el papiledema, la neuritis óptica, los tumores de la vía ósea, la vigabatrina, el nistagmus y algunas patologías neurodegenerativas, los avances en el análisis de los datos que proporciona y el acúmulo de información en investigación probablemente conviertan a esta tecnología en un arma interesante para monitorizar o diagnosticar muchas patologías.
★★★★✩ Epilepsy: new advances. Lancet. 2015; 385(9971): 884–98. PMID: 25260236
Aunque no presenta una visión exclusivamente pediátrica, este artículo recorre los retos actuales del manejo de los pacientes con epilepsia. Discute los nuevos datos procedentes de estudios epidemiológicos, ensayos clínicos farmacológicos y estudios sobre la consolidada utilidad de la cirugía y sobre nuevos métodos de neuroestimulación.
★★★★✩ Current role of melatonin in pediatric neurology: clinical recommendations. Eur J Paediatr Neurol. 2015; 19(2): 122–33. PMID: 25553845
Buena revisión sobre las evidencias que sostienen (en parte) el uso actual de melatonina en el tratamiento de trastornos del sueño en pacientes con o sin comorbilidad neurológica asociada. Como crítica, cabe decir que es quizá demasiado teórica y que ofrece pocos consejos sobre el manejo diario de este interesante fármaco.
Psiquiatría infantil
★★★★★ Conduct disorder and callous-unemotional traits in youth. N Engl J Med. 2014; 371(23): 2207–16. PMID: 25470696
Buena revisión sobre el trastorno de conducta y los rasgos antisociales en la edad infantil. Aunque los autores plantean una revisión clásica donde hablar de los conceptos nosológicos relacionados con los problemas de conducta y también de las distintas opciones terapéuticas, hay que destacar su discusión sobre la fisiopatología de estos problemas y sobre las diferencias neurobiológicas entre los distintos patrones de enfermedad. Se plantea una brillante discusión sobre la necesidad de biomarcadores basados en los trastornos biológicos subyacentes como método para avanzar en el conocimiento de los mecanismos detrás de estos trastornos, para mejorar el diagnóstico diferencial, conseguir un tratamiento personalizado y afinar en el complejo, pero vital, pronóstico a largo plazo de estos pacientes.
 |
| El Rincón del Residente |
Coordinadores:
F. Campillo i López, E. Pérez Costa, D. Rodríguez Álvarez, E. Ballesteros Moya
Residentes de Pediatría del Hospital Universitario La Paz. Madrid
Autores:
R. Maseda Pedrero*, L. Turrión Merino**, M. Feito Rodríguez***
*Médico Interno Residente de Dermatología en Hospital Universitario La Paz. **Médico Interno Residente de Dermatología en Hospital Universitario Ramón y Cajal. ***Médico Adjunto del Servicio de Dermatología del Hospital Universitario La Paz.
| El Rincón del Residente es una apuesta arriesgada de Pediatría Integral. No hemos querido hacer una sección por residentes para residentes. Yendo más allá, hemos querido hacer una sección por residentes para todo aquel que pueda estar interesado. Tiene la intención de ser un espacio para publicaciones hechas por residentes sobre casos clínicos e imágenes entre otras. ¡Envíanos tu caso! Normas de publicación aquí |
Pediatr Integral 2015; XIX(6): 437.e1-437.e7
Recién nacida con hemangioma segmentario superficial
Historia clínica
Recién nacida a término, que presenta desde el nacimiento una lesión deprimida en región lumbar de 4 x 3 mm (Fig. 1), con aparición a los quince días de vida de un hemangioma segmentario superficial sobre la misma (Fig. 2). Se realizó una ecografía a las 24 horas de vida, en la que se observó una situación baja del cono medular, por lo que se solicitó una resonancia magnética nuclear (Fig. 3).
 |
| El Rincón del Residente |
Coordinadores:
F. Campillo i López, E. Pérez Costa, D. Rodríguez Álvarez, E. Ballesteros Moya
Residentes de Pediatría del Hospital Universitario La Paz. Madrid
Autores:
P. Sánchez Moreno*, I.O. Alonso Rueda**, P. Olbrich***, P.J. Terol Barrero****
*Médico Interno Residente de tercer año de Pediatría del Hospital Universitario Virgen del Rocío. **Médico adjunto del Servicio de Pediatría del Instituto Hispalense de Pediatría. ***Médico adjunto del Servicio de Pediatría del Hospital Universitario Virgen del Rocío. ****Médico adjunto del Servicio de Pediatría del Hospital Universitario Virgen Macarena.
| El Rincón del Residente es una apuesta arriesgada de Pediatría Integral. No hemos querido hacer una sección por residentes para residentes. Yendo más allá, hemos querido hacer una sección por residentes para todo aquel que pueda estar interesado. Tiene la intención de ser un espacio para publicaciones hechas por residentes sobre casos clínicos e imágenes entre otras. ¡Envíanos tu caso! Normas de publicación aquí |
Pediatr Integral 2015; XIX(6): 437.e1-437.e7
Niña de 16 meses con tumefacción en la cara
Historia clínica
Niña de 16 meses previamente sana, que consulta por tumefacción en cara de 12 días de evolución. Al comienzo, de coloración rojiza y dura y en unos días se torna violácea y fluctuante (Fig. 1), apareciendo una nueva tumefacción de menor tamaño a nivel retroauricular. No refiere dolor, fiebre, decaimiento u otro síntoma acompañante. Ha recibido tratamiento con ibuprofeno y amoxicilina-clavulánico a dosis habituales durante una semana, sin mejoría. Pruebas complementarias: hemograma normal, ligera linfocitosis relativa (62%), bioquímica, amilasa y transaminasas normales, PCR: 0,92 mg/L, LDH: 505 U/L. Prueba de tuberculina: 0 mm de induración. Ecografía parotídea: imagen intraparotídea de contornos lobulados hipoecoica bien definida de unos 12 x 18 mm.