|
| Regreso a las bases |
J.J. Menéndez Suso
Servicio de Cuidados Intensivos Pediátricos. Hospital Universitario La Paz. Madrid
Pediatr Integral 2014; XVIII(4): 252-260
Reanimación cardiopulmonar básica en pediatría
Introducción
Concepto de parada cardiorrespiratoria
Se entiende por parada cardiorrespiratoria, en adelante PCR, la interrupción, generalmente inesperada y potencialmente reversible, de la respiración y de la actividad mecánica del corazón.
Identificación de la PCR
El niño en situación de PCR, se identifica por la presencia de los siguientes tres signos clínicos fundamentales:
1. Inconsciencia.
2. Apnea o respiración agónica (gasping).
3. Ausencia de pulso o de signos vitales (no se mueve, no respira, no tose).
Incidencia de la PCR en la edad pediátrica
Afortunadamente, la PCR en el niño es un evento raro. La incidencia estimada de PCR extrahospitalaria en la edad pediátrica, es de 8 a 20 casos/100.000 niños/por año, y la de PCR hospitalaria, aproximadamente, cien veces mayor (2-6% de los niños ingresados en unidades de cuidados intensivos)(1,2).
A diferencia con el adulto, generalmente, no se presenta de manera inesperada, sino que se suele poder predecir. Esto es así, porque la causa que con más frecuencia conduce a la PCR en el niño, es la insuficiencia respiratoria, que suele instaurarse de manera gradual. Por el contrario, en el adulto, la PCR es, con más frecuencia, consecuencia de una insuficiencia cardiovascular, que suele precipitarse de manera brusca y, por tanto, es menos predecible.
Causas de PCR en la edad pediátrica
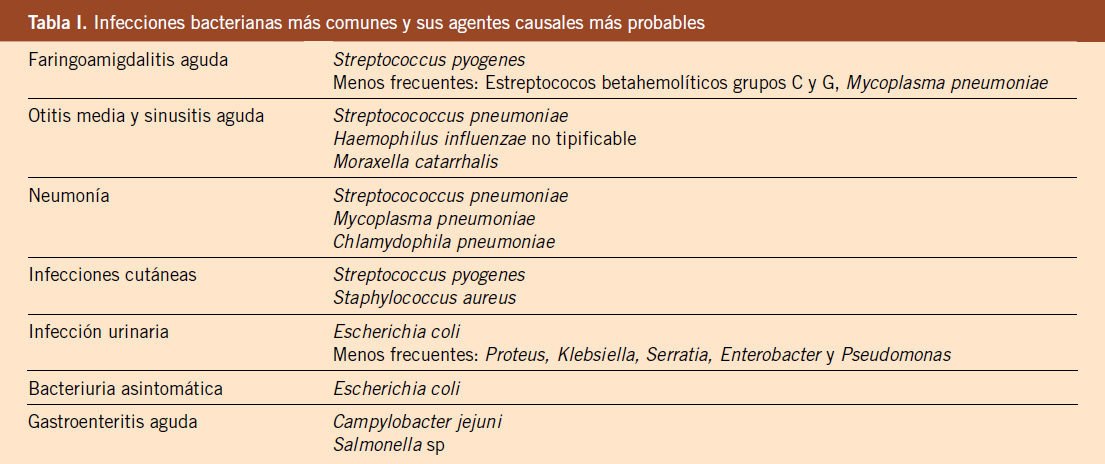
Las causas más frecuentes de PCR en el niño se resumen en la tabla 1. En general, la PCR en el niño suele ser de causa respiratoria y se presenta con más frecuencia en los lactantes, siendo las causas fundamentales en ellos: el síndrome de muerte súbita (SMSL), las malformaciones congénitas, las complicaciones de la prematuridad y la enfermedad respiratoria aguda. En el niño mayor de 1 año, la causa más frecuente de PCR es el traumatismo grave, generalmente, secundario a un accidente con vehículo a motor, seguido por las enfermedades cardiovasculares y el cáncer. La PCR de origen cardíaco se observa casi exclusivamente en niños con cardiopatías congénitas, especialmente en el postoperatorio de la cirugía cardiaca(2).
Identificación del niño con riesgo de presentar una PCR
La identificación de los signos clínicos propios de la insuficiencia respiratoria y/o cardiovascular permite, por un lado, detectar precozmente los pacientes con riesgo de presentar PCR y, por otro, instaurar medidas terapéuticas específicas que prevengan su presentación. En este sentido, la prevención de la PCR debe ser un objetivo prioritario, debiéndose implementar tanto planes de formación específicos para los profesionales sanitarios como medidas de educación sanitaria para la población general y, especialmente, para los padres/cuidadores de niños con enfermedades crónicas.
Conviene recordar que, cuando una enfermedad precipita una situación de insuficiencia respiratoria o cardiovascular, suele existir una respuesta fisiológica inicial de compensación, con la que el organismo pone en marcha una serie de mecanismos que pretenden preservar la distribución de oxígeno y nutrientes, especialmente a los órganos vitales. Es en esta fase de compensación, cuando más conviene detectar al niño en riesgo. En la tabla 2, se resumen los principales signos de alarma que caracterizan las situaciones de insuficiencia cardiorrespiratoria grave.
Pronóstico de la PCR
Estudios recientes demuestran que, aunque del 43% al 64% de los pacientes pediátricos que presentan una PCR recuperan la circulación espontánea con la aplicación de maniobras de RCP, la supervivencia global a la PCR sigue siendo baja, superior al 25% en los casos de PCR intrahospitalaria y cercana al 10% en las ocurridas fuera del hospital. La supervivencia en los niños con PCR hospitalaria es del 24% cuando el ritmo inicial es una fibrilación ventricular (FV)/taquicardia ventricular (TV) sin pulso, del 38% cuando es una actividad eléctrica sin pulso (AESP), y del 24% si es una asistolia, siendo, en general, algo mejor la supervivencia en lactantes, que en niños y adultos. Los niños con mala perfusión y bradicardia grave, pero con pulso, en los que se administra RCP, son los que tienen mayor supervivencia (64%)(3-7).
Aunque es un campo todavía en estudio, actualmente se han identificado algunos factores que influyen significativamente en la supervivencia y la calidad de vida tras una PCR: el estado clínico previo del paciente, la causa de la PCR (las de causa respiratoria tienen mejor pronóstico que las de causa cardiaca), la aplicación precoz de la RCP, la calidad de las maniobras de RCP administradas y la calidad de los cuidados post-resucitación.
El inicio de las maniobras de RCP por los testigos que presencian una PCR mejora significativamente el pronóstico del paciente. Dado que, con un correcto entrenamiento, las maniobras de RCP básica son fáciles de aprender y de administrar, en la actualidad existe cada vez más conciencia de la necesidad de trasladar su conocimiento a toda la población y no solo al personal sanitario. En este sentido, hay que recordar que la mayoría de las paradas pediátricas extrahospitalarias se producen en el domicilio, cuando los niños están solos o acompañados por sus familiares.
Con el objetivo de mejorar la supervivencia y la calidad de vida tras la PCR, todas las estrategias de educación para la salud de la población y de mejora en la provisión de los servicios sanitarios deberían contemplar los 5 aspectos fundamentales que componen la denominada “cadena de supervivencia” (Fig. 1), y que son: prevención de la PCR, administración precoz de las maniobras de RCP, acceso rápido a los servicios médicos de emergencias y aplicación óptima de las maniobras de RCP avanzada y de los cuidados post-resucitación.

Figura 1. Cadena de supervivencia pediátrica.
Reanimación cardiopulmonar básica
Generalidades
Las maniobras de reanimación cardiopulmonar (RCP) son un conjunto de medidas y actuaciones que, por un lado, permiten identificar la situación de PCR y, por otro, pretenden sustituir, primero, y tratar de recuperar, después, la respiración y la circulación espontáneas, constituyendo el tratamiento esencial de la PCR. Su objetivo fundamental es procurar una distribución suficiente de oxígeno al cerebro y a otros órganos vitales.
En la RCP básica, las maniobras de reanimación se realizan sin contar con ningún equipamiento específico, pudiendo ser realizadas por cualquier persona. En la RCP básica instrumentalizada, se contempla la incorporación de cierto material, con objeto de mejorar la ventilación (bolsas autoinflables, mascarillas faciales y cánulas orofaríngeas), el tratamiento de los ritmos desfibrilables (desfibrilador semiautomático) y la seguridad del reanimador (material de protección y bioseguridad). La RCP básica instrumentalizada la deberían poder administrar grupos específicos de la población (policías, bomberos, socorristas, protección civil, etc.), así como todo el personal sanitario, independientemente de su especialización. Por último, en la RCP avanzada, se cuenta con la ayuda de material específico, como, por ejemplo: oxígeno, material de instrumentalización de la vía aérea o fármacos, y se debe aplicar por personal sanitario especialmente entrenado y capacitado.
Guías para la realización de RCP en la edad pediátrica
En el año 2011, el Consejo Español de Resucitación, publica el Manual de Soporte Vital Pediátrico, basado en las guías del European Resuscitation Council (ERC) del 2010(8). Con fines didácticos y por evitar controversias innecesarias, el algoritmo de RCP básica (Fig. 2) es el recomendado por este manual.
Secuencia de RCP básica
A continuación, se detallan las maniobras que componen la RCP básica según las recomendaciones actuales. Con fines didácticos, se presentan como una secuencia escalonada de actuaciones. No obstante, cuando exista más de un reanimador, éstas podrán ser realizadas de forma simultánea (p. ej.: administrar ventilaciones de rescate y activar los servicios de emergencias).
Conviene también aclarar, que en lo que respecta a las guías de RCP, se consideran lactantes a los menores de un año (excluyendo al recién nacido) y niños, a los que tienen más de un año y hasta la pubertad, entendiéndose ésta como la presencia de desarrollo mamario en las niñas y de vello axilar en los niños. No obstante, si el reanimador considera que la víctima es un niño, deberá también seguir las recomendaciones pediátricas.
Por último, y aunque la American Heart Association (AHA), en sus guías del 2010, propone emplear la secuencia “CAB” y acceder rápidamente a un desfibrilador, comenzando la RCP por las compresiones y no por la ventilación(9-10), la ERC sigue recomendando mantener la secuencia clásica “ABC”, dado que, con mucha más frecuencia, la PCR en el niño es de causa respiratoria-hipóxica, siendo la bradicardia grave-asistolia el ritmo más habitual.
La secuencia de actuaciones que componen la RCP básica se describe a continuación, y se resume en la figura 2.

Figura 2. Algoritmo de la reanimación cardiopulmonar (RCP) básica pediátrica. SEM: Servicio de Emergencia Médica. DESA: desfibrilador semiautomático.
1. Garantizar la seguridad del niño y del reanimador:
• Antes de iniciar la RCP, se asegurará la integridad del niño y la del reanimador, movilizando, si es preciso, a la víctima a un lugar seguro.
• El reanimador se protegerá con todas las medidas que tenga disponibles (guantes, métodos barrera, dispositivos de señalización, etc.).
2. Comprobar la respuesta a la estimulación:
• Estimular al niño: primero verbalmente preguntando en voz alta “¿cómo estás?” o llamándole por su nombre, si se conoce. Si no hay respuesta, aplicar estimulación táctil intensa o dolorosa (p. ej., pellizcos), evitando sacudidas vigorosas.
• Se considerará que el niño responde si habla, llora, grita o se mueve.
• Si hay respuesta a estímulos: mantener la posición, investigar la presencia de lesiones y valorar si precisa atención médica.
• Si no hay respuesta a estímulos: el niño está inconsciente, y se debe continuar con la secuencia de RCP.
3. Solicitar ayuda y activar los servicios de emergencia médica (SEM):
• Solicitar inmediatamente ayuda: gritar “ayuda”.
• Activar los SEM y obtener un desfibrilador semiautomático (DESA): tras comprobar la inconsciencia y la apnea del paciente, mediante llamada telefónica al número de emergencias internacional (112) o local (061), o al equipo hospitalario especializado. En la tabla 3, se detalla la información mínima que se debe facilitar al activar los SEM.
- Dos o más reanimadores: uno permanece junto a la víctima y continua con la RCP, y otro llama al 112 y busca un DESA.
- Un reanimador: incluso aunque éste disponga de teléfono móvil, debe administrar 1 minuto de RCP básica antes de activar los SEM, salvo en el raro caso que presencie una parada súbita, especialmente si se conoce que el niño es cardiópata, que debe entonces activar primero los SEM y conseguir un DESA, para, después, iniciar la RCP.
4. Optimizar la posición del niño:
• Colocar al niño sobre una superficie dura y plana (fundamental para optimizar la calidad de las compresiones torácicas), en decúbito supino y con la cabeza, cuello, tronco y extremidades bien alineados.
• Si se sospecha la presencia de lesión espinal (accidentes de tráfico, caídas desde cierta altura, etc.), se movilizará al niño en bloque, al menos por 2 reanimadores, procurando proteger la columna cervical.
5. Abrir la vía aérea:
Ya que, en el niño inconsciente es frecuente la obstrucción parcial o completa de la vía aérea por la lengua o por secreciones/cuerpos extraños, es esencial aplicar correctamente las maniobras de apertura de la vía aérea, para permitir una correcta ventilación posteriormente.
• Maniobra frente mentón: es la maniobra de elección. Una mano del reanimador en la frente y la otra elevando el mentón, como se describe en la figura 3, extendiendo la cabeza hasta una posición neutra en el lactante, y algo más, hasta la posición de “olfateo”, en el niño. Es importante, no hacer presión sobre los tejidos blandos bajo la mandíbula, ya que esto puede obstruir la vía aérea.
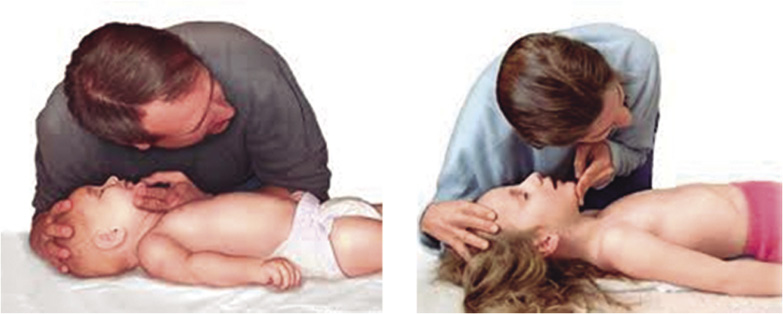
Figura 3. Maniobra de apertura de la vía aérea tipo frente-mentón y comprobación de la respiración espontánea (“ver-sentir-oír”).
• Maniobra de tracción mandibular: similar a la anterior pero, en este caso, no se produce extensión cervical con la mano de la frente, y con la otra mano se tracciona de la mandíbula hacia arriba y hacia adelante, colocando el pulgar tras los incisivos y el índice y el corazón bajo el mentón. Esta técnica se debe emplear cuando se sospeche lesión cervical.
• Tras abrir la vía aérea, inspeccionar la cavidad oral en busca de cuerpos extraños, procurando retirarlos mediante barrido lateral con el dedo, solo si están claramente accesibles.
6. Comprobar si existe respiración espontánea:
• Comprobar la presencia de respiración espontánea acercando la mejilla a la boca del niño, para “ver” si hay excursiones torácicas, “oír” si hay ruidos respiratorios y “sentir” en su mejilla el movimiento del aire (Fig. 3). En este proceso no se debe invertir más de 10 segundos.
• Si el niño está inconsciente pero respira, se colocará en posición de seguridad, como se detalla en la figura 4, siempre que no existan o se sospechen lesiones que lo impidan, buscando mantener la vía aérea permeable y reducir el riesgo de aspiración. Activar los servicios de emergencias y permanecer a su lado, reevaluando su situación periódicamente.
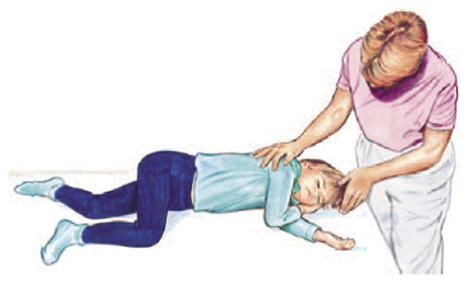
Figura 4. Posición de seguridad para el paciente inconsciente con respiración espontánea normal.
• Si el niño está inconsciente y no respira o presenta movimientos respiratorios ineficaces, en forma de bocanadas ocasionales (gasping), se deben administrar 5 ventilaciones de rescate, para demostrar la permeabilidad de la vía aérea.
7. Administrar 5 insuflaciones de rescate:
Con las ventilaciones de rescate se pretende fundamentalmente demostrar la permeabilidad de la vía aérea.
• Dar 5 insuflaciones, manteniendo la apertura de la vía aérea, con técnica de “boca a boca-nariz” en el lactante o “boca a boca” en el niño, como se describe en la figura 5, o con mascarilla facial y bolsa autoinflable (RCP básica instrumentalizada), como se describe en la figura 6, si se dispone de ellas en ese momento. También, se recomienda la ventilación con oxígeno siempre que esté disponible. Tras cada ventilación, el reanimador debe separar por completo su boca de la del niño, realizando una inspiración profunda antes de la siguiente, para así optimizar la cantidad de O2 y disminuir la cantidad de CO2 que se administra al niño. Las insuflaciones serán de aproximadamente 1 segundo, con la intensidad suficiente para producir una excursión evidente del tórax del niño.
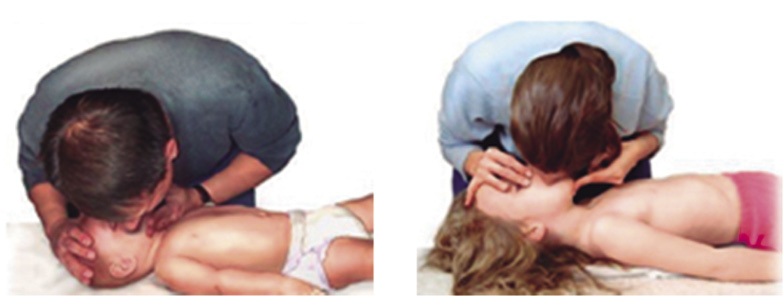
Figura 5. Ventilación boca a boca-nariz en el lactante y boca a boca en el niño.
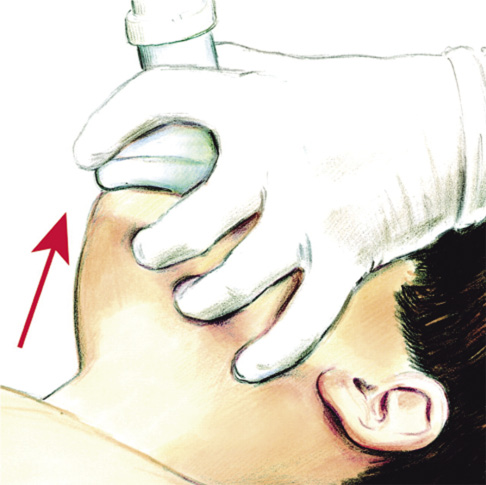
Figura 6. Técnica de sujeción de la mascarilla facial para ventilación con bolsa autoinflable.
• Si no se consigue movimiento torácico con las primeras insuflaciones de rescate: optimizar la posición de apertura de la vía aérea y asegurar el correcto sellado de la boca y la nariz del niño.
• Si aun así no se consigue expandir el tórax: considerar que existe una obstrucción completa de la vía aérea, e iniciar en ese momento las compresiones torácicas, sin necesidad de comprobar la circulación.
• Si se consigue expandir el tórax, al menos con 2 de las 5 insuflaciones: se descarta la obstrucción completa de la vía aérea, y se debe continuar con la evaluación de la situación circulatoria (signos de vida).
8. Comprobar si existe circulación espontánea:
• Comprobar el estado circulatorio mediante la búsqueda de “signos de vida” (movimientos, tos o respiraciones normales), sin emplear para ello más de 10 segundos. Habitualmente, esto se puede hacer mientras se administran las 5 insuflaciones de rescate.
• Solo el personal sanitario con experiencia puede investigar también la presencia de pulsos centrales (braquial o femoral en el lactante; carotídeo o femoral en el niño).
• Si se detectan signos de vida o si se palpa con seguridad un pulso central a una frecuencia mayor de 60 por minuto: continuar manteniendo la apertura de la vía aérea, administrando entre 12 y 20 ventilaciones por minuto, según la edad del niño. Reevaluar continuamente, la situación respiratoria y circulatoria hasta que llegue personal del SEM o más cualificado, o hasta que se recupere la respiración espontánea, debiéndose colocar al niño en posición de seguridad en ese momento.
• Si no hay signos de vida: administrar compresiones torácicas.
9. Administrar compresiones torácicas:
Las compresiones torácicas son la piedra angular de la RCP básica; por lo que, la administración precoz y con calidad de las mismas es un objetivo prioritario. Para conseguir compresiones de calidad, se deben cumplir las siguientes recomendaciones:
• Comprimir “rápido y con fuerza” (Push fast, Push hard): administrar “al menos” 100 compresiones/minuto, deprimiendo “al menos” un tercio del diámetro torácico anteroposterior (unos 4 cm en lactantes y 5 cm en niños).
• Permitir una expansión torácica completa tras cada compresión, buscando favorecer el máximo llenado del corazón. La expansión incompleta del tórax durante la RCP se asocia a mayor aumento de la presión intratorácica, lo que dificulta el retorno venoso y la perfusión coronaria y cerebral(11).
• El personal no sanitario: tras cada 30 compresiones administrar 2 ventilaciones (ratio 30:2), tanto en lactantes como en niños, procurando reducir al mínimo el tiempo que se interrumpen las compresiones torácicas.
• El personal sanitario: tras cada 15 compresiones administrar 2 ventilaciones (ratio 15:2), tanto en lactantes como en niños, pudiendo también aplicarlas con el ratio 30:2 en caso de fatiga o si hay un único reanimador.
• Con respecto a la técnica de las compresiones (Fig. 7):
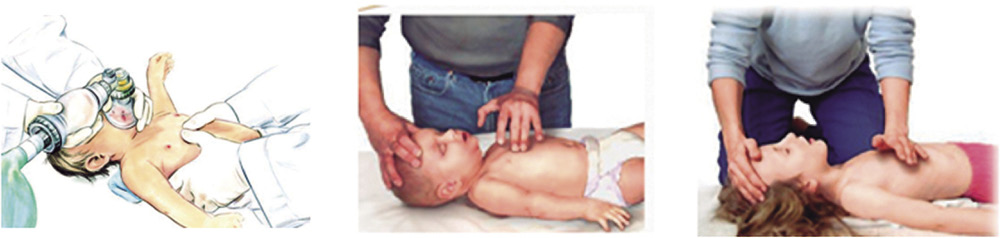
Figura 7. Técnicas para administrar las compresiones torácicas en el lactante y en el niño.
- En lactantes: si solo existe un reanimador, comprimir con dos dedos el tercio inferior del esternón, justo bajo la línea intermamilar, evitando realizar las compresiones sobre el xifoides, las costillas o en el abdomen. Si hay dos o más reanimadores, abrazar el tórax con las manos y comprimir el tórax con los dos pulgares, en el mismo punto que con la técnica anterior.
- En niños: emplear una mano o las dos superpuestas, según preferencia del reanimador, manteniendo los brazos estirados, sin flexionar los codos, y separando ligeramente los dedos del tórax, para administrar la compresión con el talón de la mano sobre el tercio inferior del esternón.
• Dado que en la edad pediátrica, la PCR suele ser de causa respiratoria, el éxito de la RCP es mayor cuando se combinan compresiones con ventilaciones, pero si el reanimador no tiene entrenamiento suficiente o no desea hacerlas, es preferible que administre solo compresiones torácicas (Hands-only) hasta la llegada de los SEM, en vez de que no realice nada.
• Para evitar la fatiga, si hay más de un reanimador, cada 2 minutos estos se irán sustituyendo en la tarea de administrar las compresiones.
10. Comprobación de la eficacia de las maniobras de RCP:
• Cada 2 minutos desde el inicio de la RCP, se detendrá brevemente la secuencia de compresiones-ventilaciones para reevaluar la presencia de respiración y circulación espontáneas, debiéndose emplear para ello el menor tiempo posible (no más de 10 segundos).
Duración de la RCP básica
Las maniobras de RCP se mantendrán hasta que:
• Se comprueba la recuperación de la respiración y circulación espontáneas (signos vitales o pulso central a más de 60 por minuto).
• Llega personal más cualificado que continua con la RCP.
• El reanimador está agotado.
Integración del desfibrilador semiautomático en la RCP básica pediátrica
El desfibrilador semiautomático (DESA), mediante unos electrodos adhesivos que se colocan en el tórax, analiza el electrocardiograma del paciente, determina si está indicado el tratamiento con desfibrilación y, si es el caso, posibilita al reanimador su administración. Suelen ser aparatos sencillos, con un pulsador para comenzar el análisis del ritmo y otro para administrar la descarga, generalmente con una energía fija de 150-200 julios. Algunos equipos permiten atenuar la dosis de energía, sobre 50-75 julios, para su aplicación en la edad pediátrica.
Las guías de RCP del 2010 recomiendan el uso sistemático del DEA durante la RCP de niños mayores de 1 año. En niños mayores de 8 años (25 Kg), se debe emplear un DESA de adultos, pero en niños de 1 a 8 años de edad, se recomienda emplear un DESA pediátrico, con atenuador de energía, aunque, si no se dispone de el, también se recomienda utilizar un DESA de adulto (es más adecuado administrar alta energía que no administrar ninguna descarga a un niño en situación de PCR y ritmo desfibrilable). En los lactantes, no se ha establecido la seguridad del empleo del DESA, aunque también se recomienda emplearlo si se detecta un ritmo desfibrilable, aunque, en este caso, se preferiría un desfibrilador manual con selector de energía (2-4 J/kg), sobre los semiautomáticos. Los electrodos se deben posicionar, uno en la región infraclavicular derecha y otro en la línea medio-axilar izquierda (Fig. 8), aunque en los niños pequeños (<8 años), se pueden colocar uno en la parte anterior y otro en la parte posterior del tórax, para evitar que contacten entre sí. Aunque los electrodos suelen estar identificados como “derecho” e “izquierdo”, no importa si se colocan en la posición opuesta.

Figura 8. Posicionamiento de los electrodos del desfibrilador semiautomático (DESA) en un niño mayor.
A continuación se refleja la manera de integrar el uso del DESA en la RCP básica de niños:
• Si no se dispone de él al iniciar la RCP:
- Un reanimador: administrar 1 minuto de RCP antes de ir a buscarlo (salvo parada súbita presenciada y sospecha de enfermedad cardiaca).
- Dos reanimadores: uno de los reanimadores inicia RCP y otro busca DESA.
• Si se dispone de él al iniciar la RCP: administrar siempre 1 minuto de RCP antes de monitorizar y analizar el ritmo con el DESA (salvo en parada súbita, que se debe usar inmediatamente).
Para evitar que la calidad de la RCP disminuya: mantener las compresiones mientras se colocan los electrodos en el niño, finalizando el ciclo de RCP por las compresiones antes de analizar el ritmo, y reiniciar inmediatamente la RCP con compresiones, tras administrar la descarga eléctrica.
Obstrucción de la vía aérea por cuerpo extraño (OVACE)
En la tabla 4, se resumen las características propias de un episodio de obstrucción de la vía aérea por un cuerpo extraño (CE) y, en la figura 9, el algoritmo para su tratamiento, propuesto por el ERC en las guías del 2010, que se describe a continuación:
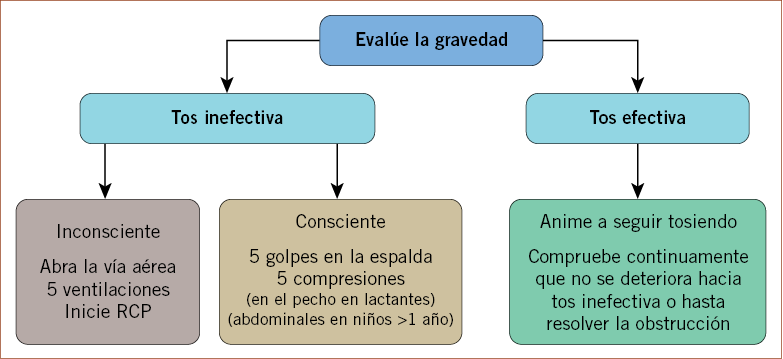
Figura 9. Algoritmo para el tratamiento de la obstrucción de la vía aérea por cuerpo extraño.
1. Si el niño respira eficazmente (habla o llora y tose con fuerza):
• Animar a que el niño siga tosiendo o a que el lactante llore, vigilando su condición respiratoria y si se produce o no la expulsión del CE.
2. Si el niño no respira eficazmente (habla o llora con debilidad, tos ineficaz):
• Revisar la cavidad oral y, solo si se identifica un CE accesible, intentar extraerlo realizando una maniobra de gancho con el dedo, haciendo un barrido de un lado a otro de la boca.
• Si no se identifica un cuerpo extraño o éste no es accesible, se aplican las siguientes maniobras de desobstrucción (Fig. 10):
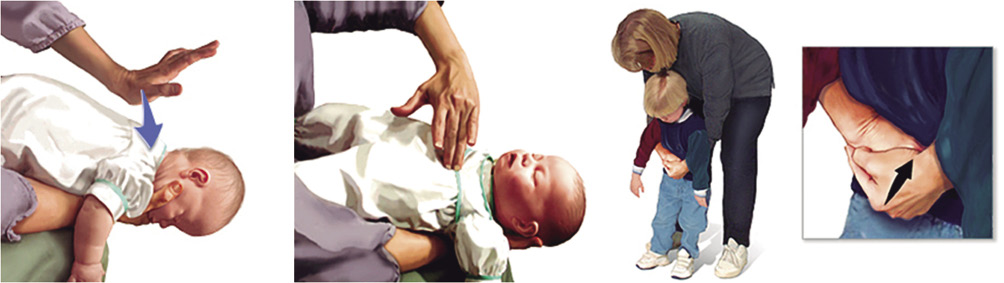
Figura 10. Maniobras de desobstrucción de la vía aérea en el lactante y en el niño.
- Lactantes: primero, colocar al lactante en decúbito prono, reposando sobre el antebrazo del reanimador, sujetándolo firmemente por la mandíbula y con la cabeza algo más baja que el tronco. En esta posición, administrar 5 compresiones, con el talón de la otra mano, en la zona interescapular. Posteriormente, cambiando al lactante de antebrazo, y en decúbito supino, se sujeta la cabeza con la mano algo más baja que el tronco. En esta posición, administrar 5 compresiones torácicas, en el mismo punto y con la misma intensidad que para realizar el masaje cardíaco, pero algo más lentas. Por último, examinar la cavidad oral en busca del CE, procurando extraerlo si está accesible, y comprobar la presencia y eficacia de la respiración. Si las maniobras no han sido eficaces, y el niño sigue consciente, repetir la secuencia.
- Niños: primero, administrar 5 compresiones interescapulares, para lo cual, el reanimador se colocará detrás del niño, haciendo pasar uno de sus brazos por debajo de la axila, para sujetarle a nivel de la región esternal, mientras se favorece la inclinación hacia delante de la cabeza. Posteriormente, administrar 5 compresiones abdominales (maniobra de Heimlich), abrazando al paciente por debajo de las axilas desde atrás, rodeando el tórax, y colocando los puños en la región epigástrica.
Se debe recordar que estas maniobras persiguen desobstruir la vía aérea, no expulsar el CE. Por tanto, si se recuperan la respiración y la tos eficaz, se deben suspender.
3. Si el niño está o se queda inconsciente (en apnea o con respiración ineficaz):
• Solicitar ayuda y activar los SEM.
• Tumbar al paciente en el suelo y colocarle en posición de RCP.
• Abrir la vía aérea y revisar la cavidad oral en busca del CE, procurando extraerlo, solo si está accesible.
• Administrar 5 ventilaciones de rescate para comprobar si existe o no, una obstrucción completa de la vía aérea:
- Si hay excursión torácica (ausencia de obstrucción completa): buscar signos de vida. Si están presentes, mantener las ventilaciones a la frecuencia apropiada para la edad del niño, hasta que lleguen los SEM. Si no lo están, iniciar compresiones torácicas, alternándolas con ventilaciones, con una relación 30:2 (personal no sanitario) o 15:2 (personal sanitario), revisando la cavidad oral periódicamente.
- Si no hay excursión torácica (obstrucción completa de la vía aérea): iniciar las compresiones torácicas, sin que sea necesario comprobar la presencia de signos de vida, alternándolas con ventilaciones con una relación 30:2 (personal no sanitario) o 15:2 (personal sanitario), revisando la cavidad oral periódicamente.
Bibliografía
1. Berg M, Nadkarni VM, Zuercher M, Berg RA. In-Hospital pediatric cardiac arrest. Pediatr Clin N Am. 2008; 55: 589-604.
2. Donoghue AJ, Nadkarni V, Berg RA, Osmond MH, Wells G, Nesbitt L, Stiell IG. Out-of-hospital pediatric cardiac arrest: an epidemiologic review and assessment of current knowledge. Ann Emerg Med. 2005; 46: 512-22.
3. López-Herce J, García C, Rodríguez-Núñez A, Domínguez P, Carrillo A, Calvo C, Delgado MA. Long-term outcome of paediatric cardiorespiratory arrest in Spain. Resuscitation. 2005; 64: 79-85.
4. Schindler MB, Bohn D, Cox PN, McCrindle BW, Jarvis A, Edmonds J, Barker G. Outcome of out-of-hospital cardiac or respiratory arrest in children. N Engl J Med. 1996; 335: 1473-79.
5. López-Herce J, García C, Domínguez P, Carrillo A, Rodríguez-Núnez A, Calvo C, Delgado MA. Characteristics and outcome of cardiorespiratory arrest in children. Resuscitation. 2004; 63: 311-20.
6. López-Herce J, Del Castillo J, Matamoros M, Cañadas S, Rodríguez-Calvo A, Cecchetti C, Rodríguez-Núñez A, Álvarez AC; Iberoamerican Pediatric Cardiac Arrest Study Network RIBEPCI. Factors associated with mortality in pediatric in-hospital cardiac arrest: a prospective multicenter multinational observational study. Intensive Care Med. 2013; 39: 309-18.
7. Atkins DL, Stewart SE, Sears GK, Daya M, Osmond MH, Warden CR, et al. Epidemiology and Outcomes From Out of-Hospital Cardiac Arrest in Children. The Resuscitation Outcomes Consortium Epistry–Cardiac Arrest. Circulation. 2009; 119: 1484-91.
8. Biarent D, Bingham R, Eich C, López-Herce J, Maconochie I, Rodríguez-Núñez A, Rajka T, Zideman D. European Resuscitation Council Guidelines for Resuscitation 2010 Section 6. Paediatric life support. Resuscitation. 2010; 81: 1364-88.
9. Berg MD, Schexnayder SM, Chameides L, Terry M, Donoghue A, Hickey RW, Berg RA, Sutton RM, Hazinski MF. Part 13: pediatric basic life support: 2010 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular Care. Circulation. 2010; 122: S862-S875.
10. Kleinman ME, de Caen AR, Chameides L, Atkins DL, Berg RA, Berg MD, Bhanji F, Biarent D, Bingham R, Coovadia AH, Hazinski MF, Hickey RW, Nadkarni VM, Reis AG, Rodríguez-Núnez A, Tibballs J, Zaritsky AL, Zideman D; on behalf of the Pediatric Basic and Advanced Life Support Chapter Collaborators. Special report-pediatric basic and advanced life support: 2010 International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science With Treatment Recommendations. Circulation. 2010; 122: S466-S515.