|
| Temas de FC |
V. Losa Frías*, M. Herrera López**, I. Cabello García**, P.I. Navas Alonso**
*Centro de Salud de Fuensalida, Toledo. **Servicio de Pediatría. Hospital Virgen de la Salud, Toledo
| Resumen
El cáncer en la infancia presenta baja incidencia, su presentación clínica con frecuencia es inespecífica y simula patologías comunes de curso benigno, lo que dificulta su diagnóstico en Atención Primaria. Los principales síntomas y signos de sospecha de cáncer en Pediatría son: palidez, masas (en cabeza, cuello y otras localizaciones), adenopatías, movimientos anormales, hematomas y signos de sangrado, fatiga, cefalea, anormalidades visuales, dolor y síntomas musculoesqueléticos. El pediatra de Atención Primaria ha de reconocer cuando una sintomatología aparentemente benigna puede ser el inicio de una patología grave, identificando aquellos signos de alarma que requieren estudio inmediato. Son necesarios una buena historia clínica, una exploración física completa y un seguimiento clínico evolutivo. El objetivo es disminuir el tiempo desde el inicio de los síntomas hasta el diagnóstico final; de tal forma que, permita un diagnóstico precoz de cáncer infantil. |
| Abstract
The incidence of childhood cancer is low, and often, many of the early symptoms are non-specific and similar to more common and benign illnesses, because of this, the diagnosis in primary care is so difficult. The main symptoms and signs of suspected childhood cancer are: pallor, masses (in head, neck and other body areas), lymphadenopathy, symptoms/sings of abnormal movement, bruising and bleeding signs, fatigue, headache, visual symptoms, pain and musculoskeletal symptoms. |
Palabras clave: Lactante; Niño; Neoplasias; Atención Primaria; Diagnóstico precoz de cáncer
Key words: Infant; Child; Neoplasms; Primary health care; Early detection of cancer
Pediatr Integral 2016; XX (6): 367-379
Diagnóstico precoz de cáncer en Atención Primaria
Introducción
El cáncer infantil presenta baja incidencia y se manifiesta, a menudo, de forma inespecífica simulando otros procesos frecuentes y benignos. Estas particularidades dificultan la sospecha y el diagnóstico de cáncer en Atención Primaria. Sin embargo, un diagnóstico precoz y una rápida derivación del paciente a un centro especializado pueden tener importantes implicaciones a nivel pronóstico y terapéutico.
Epidemiología
El cáncer infantil es la segunda causa de mortalidad a partir del primer año de vida, detrás de los accidentes.
La incidencia anual estandarizada de cáncer infantil en España es de 155,5 casos nuevos anuales por millón de niños de 0-14 años, lo que supone 1100 casos nuevos de cáncer infantil al año, incidencia similar a la del resto de Europa(1). Se estima que un pediatra de Atención Primaria con un cupo de 1.500 pacientes verá un caso nuevo de cáncer cada 5 años. La supervivencia global a los 5 años del diagnóstico, se sitúa en torno al 75%(1). A pesar de los últimos avances, el cáncer infantil es la segunda causa de muerte desde el primer año de vida hasta la adolescencia, por detrás de los accidentes. En el año 2013, murieron en España 209 menores de 14 años por cáncer, lo que supone 4 niños fallecidos a la semana por este motivo(2).
Las neoplasias más frecuentes en niños de 0-14 años son: leucemias (26,3%), tumores del sistema nervioso central (SNC) (20,7%) y linfomas (13,3%), con un patrón de distribución por sexo y edad superponible con el del resto de Europa; mientras que, entre los 15-19 años son: tumores óseos (26,9%), linfomas (20,3%) y tumores del SNC (15,3%). Los diagnósticos más frecuentes en función de la edad se exponen en la tabla I(1).
Pacientes de riesgo
La historia clínica es la herramienta más eficaz en la identificación de los síndromes de predisposición a cáncer.
En un 5-10% de todas las neoplasias subyace una base hereditaria. Dentro de este porcentaje, se engloban los síndromes de predisposición a cáncer (SPC), un grupo heterogéneo de condiciones genéticas e inmunodeficiencias que predisponen a un mayor riesgo de cáncer (Tabla II).
La mayoría de estos síndromes son poco frecuentes y presentan una expresividad variable dentro de la misma familia. Es importante identificar a estos pacientes, dado que pueden beneficiarse de medidas de prevención y detección precoz de cáncer, así como de la posibilidad de consejo genético.
La historia clínica es la herramienta más eficaz para la identificación de los SPC. Hemos de prestar especial atención a la incidencia de cáncer en la familia, la ocurrencia del mismo tipo de cáncer, la edad de presentación inusualmente temprana para el tipo de tumor, la bilateralidad en caso de afectación de órganos pares, la multifocalidad, (varios focos tumorales independientes en el órgano en donde asientan), la aparición de varios cánceres primarios en un mismo individuo o la asociación de cánceres con defectos del desarrollo (asociación de tumores con sobrecrecimiento corporal generalizado o asimétrico, dismorfias, malformaciones congénitas o retraso mental).
Signos y síntomas de alarma
Una sintomatología aparentemente benigna, pero de presentación atípica o curso tórpido puede ser el inicio de un proceso neoplásico.
El cáncer infantil puede manifestarse en sus etapas iniciales con clínica similar a procesos frecuentes y benignos. Nuestro objetivo es reconocer cuándo esta sintomatología aparentemente benigna puede ser el inicio de una patología grave, así como identificar aquellos hallazgos que nos han de poner en alerta ante la posibilidad de cáncer y que requieren estudio inmediato (Tabla III).
Para ello, se necesita escuchar a los padres(3), que, en general, son los mejores observadores de los síntomas de sus hijos/as, realizar una historia clínica completa incluyendo los antecedentes personales y familiares y una exploración física minuciosa. En el momento actual, no existen métodos de cribado bien establecidos para el diagnóstico precoz de cáncer infantil.
Los signos y síntomas identificados en Atención Primaria que con más frecuencia se asocian a cáncer son: palidez, masas, adenopatías, movimientos anormales, hematomas y signos de sangrado, fatiga, cefalea, anormalidades visuales, dolor y síntomas musculoesqueléticos. Dicha sintomatología, cuando se presenta sin un diagnóstico claro y da lugar a un aumento en el número de consultas (3 o más en un período de 3 meses), nos ha de poner en alerta ante la posibilidad de un proceso neoplásico(4).
Cefalea y otros signos y síntomas neurológicos
Los tumores primarios del SNC son los segundos más frecuentes en la infancia, tras las leucemias(1), siendo la segunda causa de muerte por cáncer infantil(2). Su sintomatología se debe a la invasión y compresión del tejido nervioso adyacente, así como al aumento de la presión intracraneal por efecto de masa o por hidrocefalia obstructiva (Fig. 1).
Figura 1. Resonancia magnética sagital que muestra masa en fosa posterior compatible con meduloblastoma. El paciente de 13 años presentaba cefalea y edema de papila.
La presentación clínica es muy heterogénea; Wilne y cols.(5) analizaron 74 artículos (n = 4.171), identificando hasta un total de 56 signos y síntomas al diagnóstico de tumor del SNC, los cuales dependían de la edad, la localización y del antecedente de neurofibromatosis (NF). En los tumores intracraneales, excluyendo NF, la clínica más frecuente fue: cefalea, náuseas y vómitos, anormalidad de la marcha y coordinación y papiledema; en los tumores intracraneales asociados a NF, fue: disminución de la agudeza visual, exoftalmos, atrofia óptica y estrabismo; en los tumores intracraneales en menores de 4 años, fue: macrocefalia, náuseas y vómitos, irritabilidad, letargia y ataxia; en los tumores de médula espinal, fue: dolor de espalda, anormalidad de la marcha y coordinación, deformidad de columna, debilidad focal y alteraciones esfinterianas. Ante esta variabilidad clínica, posteriormente, estudiaron en una cohorte retrospectiva (n = 139), la progresión de la sintomatología, describiendo un aumento progresivo en el número de los síntomas desde el inicio de la clínica hasta el diagnóstico, con una mediana (rango) de 1 (1-8) y 6 (1-16) síntomas, respectivamente(6). Desde Atención Primaria, hemos de estar alerta ante pacientes con síntomas de evolución progresiva, no resolutivos, así como en los que va apareciendo nueva sintomatología. En esta línea, Ansell y cols.(7) describieron los motivos de consulta en Atención Primaria, desde el nacimiento hasta el diagnóstico de tumor del SNC, en una serie de pacientes, comparándola con un grupo control. Observaron, cómo los casos consultaron 3 veces más por un signo o síntoma sugestivo de tumor del SNC (IC95% 2,82-3,83), llegando a consultar hasta 7 veces más (IC95% 5,38-9,13) cuando asociaban dos o más signos o síntomas.
Con el objetivo de ayudar a los profesionales sanitarios en la identificación de pacientes con sospecha de tumor del SNC, el grupo Children’s Brain Tumour Research Center ha desarrollado una guía clínica basada en la evidencia(8) (Tabla IV).
Ante la sospecha clínica de tumor del SNC, se ha de derivar al paciente a un centro especializado en un plazo de 48 horas(9). Cabe destacar, la estrategia “HeadSmart: be brain tumours aware” (http://www.headsmart.org.uk/) lanzada en el Reino Unido en el año 2011 y dirigida tanto a profesionales sanitarios como al público en general. Esta iniciativa se ha mostrado útil en la disminución del tiempo transcurrido desde el inicio de los síntomas hasta el diagnóstico, con una mediana de 6,7 (media 21,3) semanas, así como del tiempo desde la primera consulta hasta la realización de prueba de imagen, pasando de una mediana de 3,3 a 1,4 semanas (p = 0,009)(10).
Síntomas constitucionales
La fiebre, en la mayor parte de las ocasiones, es de etiología infecciosa. Tan solo entre el 2-9% de los casos de fiebre prolongada se asocia a neoplasias. Esta fiebre puede ser de origen tumoral, como ocurre en el linfoma de Hodgkin, o secundaria a una infección ante la alteración del sistema inmunológico debido al cáncer, como ocurre en la neutropenia febril del paciente con leucemia linfoblástica aguda (LLA). La combinación de fiebre persistente e inexplicada junto con: palidez, astenia, adenopatías generalizadas, dolor óseo/articular o hematomas no justificados, ha de ser evaluada con un hemograma completo, extensión de sangre periférica y radiografía de tórax en un plazo de 48 horas ante la sospecha de leucemia o linfoma. En el caso de asociarse petequias o hepatoesplenomegalia inexplicada, se ha de derivar al paciente a un centro especializado de forma inmediata (ha de ser valorado en las horas siguientes)(9).
Alteraciones hematológicas
La forma de presentación más frecuente de las leucemias es la alteración de una o varias series hematológicas. Tumores sólidos con metástasis en médula ósea, como: el neuroblastoma, el rabdomiosarcoma o el sarcoma de Ewing, también se pueden manifestar con citopenias. Las manifestaciones clínicas del fallo medular son: palidez y astenia secundarias a anemia, generalmente normocítica; diátesis hemorrágica con petequias, equimosis, epistaxis recurrente, sangrado de encías y/o hematomas secundarios a trombopenia o coagulación intravascular diseminada; y leucopenia, leucocitosis (20 x 109/L) o hiperleucocitosis (100 x 109/L) con blastos en sangre periférica. Estos hallazgos pueden ir acompañados de síntomas constitucionales o de infiltración blástica de órganos extramedulares con: hepatoesplenomegalia, adenopatías, masa mediastínica, afectación ósea, afectación del SNC o infiltración testicular. La anemia, la trombopenia o la leucopenia aisladas pueden deberse a procesos benignos (leucopenia tras infección viral o púrpura trombocitopénica idiopática). Ante el hallazgo de dos o más citopenias y/o blastos en sangre periférica, se ha de derivar al paciente de forma inmediata a un centro especializado(9).
Adenopatías
Los ganglios linfáticos son estructuras dinámicas que cambian de tamaño durante el crecimiento, generalmente, en respuesta a infecciones. La mayoría de los niños presentan pequeños ganglios palpables a nivel cervical, axilar o inguinal. Se considera significativo el aumento de tamaño por encima de 1 cm de diámetro en ganglios cervicales y axilares, 1,5 cm en los inguinales y 0,5 cm en los epitrocleares. Las adenopatías son generalizadas, cuando se extienden en más de 2 cadenas ganglionares no contiguas y localizadas, cuando aparecen en una única región, como el cuello o la axila. Según el tiempo de evolución, distinguimos entre: agudas (menos de 2 semanas), subagudas (entre 2-6 semanas) y crónicas (más de 6 semanas). Las neoplasias más frecuentes que se presentan como adenopatías en cabeza y cuello son: neuroblastoma, leucemia, rabdomiosarcoma y linfoma no Hodgkin (menores de 6 años), linfomas de Hodgkin y no Hodgkin (entre 7-13 años) y linfomas de Hodgkin (mayores de 13 años).
La anamnesis será dirigida en función de la sospecha clínica. Hemos de conocer: el diagnóstico diferencial, la evolución y los signos de alarma que nos ayudarán a distinguir a los pocos pacientes con procesos graves. Interrogaremos sobre: la duración de las adenopatías; la presencia de síntomas sugestivos de infección, problemas dentales (anaerobios) o aftas bucales (gingivoestomatitis herpética); síntomas constitucionales [fiebre, pérdida de peso, sudoración nocturna, prurito, rash o artralgias (tuberculosis, enfermedades reumatológicas, neoplasias)]; estado de inmunización (rubéola) y vacunas recientes; medicaciones (fenitoína, carbamacepina); contacto con animales [gatos (enfermedad del arañazo de gato, toxoplasmosis), cabras (brucelosis), conejos (turalemia)], picaduras de insectos (enfermedad de Lyme), ingesta de leche no pasteurizada (brucelosis, Mycobacterium bovis), carne poco cocinada (toxoplasmosis, turalemia); antecedentes de enfermedades autoinmunes (síndrome linfoproliferativo autoinmune); e infecciones recurrentes con adenitis supurativas de repetición (enfermedad granulomatosa crónica). La exploración física será completa, buscando: signos de enfermedad sistémica, lesiones cutáneas, palidez, hematomas, petequias, lesiones orofaríngeas, conjuntivales o auditivas, hepatoesplenomegalia y masas abdominales. Las adenopatías serán evaluadas en función de su localización, tamaño, dolor, consistencia y fijación a tejidos. Hemos de palpar, de forma sistemática, todas las cadenas ganglionares accesibles: occipital, retroauricular, preauricular, parotídea, tonsilar, submandibular, submental, caras anterior y posterior de cuello, supraclavicular, infraclavicular, axilar, epitroclear, inguinal y poplítea.
Los factores predictivos de malignidad de las adenopatías han sido objeto de estudio por varios autores. Soldes y cols.(11) en una serie (n = 60) de pacientes menores de 18 años, los describen como: mayor tamaño del ganglio, mayor número de lugares afectados, aumento de la edad, localización supraclavicular, radiografía de tórax patológica y fijación a los tejidos. A su vez, Yaris y cols.(12), en otra serie (n = 98) de pacientes con adenopatías, de las cuales 23 son de origen maligno, los describen como: aumento de la edad, localización generalizada o supraclavicular, tamaño mayor de 3 cm, presencia de hepatoesplenomegalia y aumento de lactato deshidrogenasa (LDH).
La actitud terapéutica se resume en el algoritmo 2, al final del artículo(13). Cabe destacar que, los corticoides deben ser evitados en el manejo inicial de las adenopatías, dado que pueden enmascarar y retrasar el diagnóstico de leucemias y linfomas (Fig. 2).
Figura 2. Ensanchamiento mediastínico en paciente de 12 años, diagnosticada de linfoma de Hodgkin. Clínicamente, presentaba múltiples adenopatías laterocervicales y supraclaviculares adheridas, no dolorosas y de tamaño mayor a 2 cm.
Además, los pacientes con neoplasias hematológicas que han recibido tratamientos previos con corticoides presentan peor pronóstico, con mayor riesgo de recaída y mortalidad.
Masa mediastínica
Entre el 55-80% de las masas mediastínicas en la infancia son de naturaleza maligna. Por ello, todo paciente con sospecha de masa mediastínica (con la excepción de la hiperplasia tímica del lactante) ha de ser referido a un centro hospitalario de forma inmediata para completar el estudio(9). Una valoración clínica minuciosa y un alto índice de sospecha, son importantes para un diagnóstico precoz.
Desde el punto de vista anatómico, el mediastino se divide en 3 compartimentos: anterior, medio y posterior. La localización de la masa orientará el diagnóstico, dado que el tipo de neoplasia dependerá de las estructuras contenidas en cada compartimento (Tabla V).
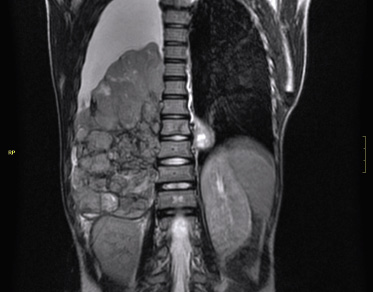
Las neoplasias más frecuentes según su localización son: LLA y linfoma de célula T (Fig. 3) en el mediastino anterior; linfoma de Hodgkin en el mediastino medio; y tumores neurogénicos (neuroblastoma y ganglioneuroma) en el mediastino posterior. Las masas mediastínicas posteriores (neuroblastoma) son más frecuentes en lactantes y niños pequeños, mientras que las anteriores (leucemias, linfomas) lo son más en el niño mayor y adolescente.
Figura 3. Masa mediastínica anterior en niño de 12 años con Leucemia T. Refiere astenia y edema palpebral bilateral de 3 días de evolución, así como hematomas, equimosis y petequias en esclavina desde hace 48 horas.
La sintomatología depende de la localización de la masa, de su tamaño, rapidez de crecimiento y de las estructuras que comprime. Aun así, hasta un cuarto de los pacientes pediátricos con masa mediastínica se encuentran asintomáticos al diagnóstico. La compresión de la vía aérea es la clínica más frecuente y da lugar a síntomas inespecíficos, como: estridor, tos no productiva, sibilancias, infecciones respiratorias de repetición, dolor torácico y dificultad respiratoria, que a menudo simulan enfermedades respiratorias frecuentes, como el asma o la laringitis. La compresión esofágica da lugar a disfagia. La compresión de la médula espinal (típica de los neuroblastomas) da lugar a dorsalgia en banda o radicular que aumenta con el Valsalva, debilidad de la marcha, paraplejía y alteraciones sensoriales y esfinterianas. La compresión de la vena cava superior (típica de leucemias y linfomas T) se manifiesta con: plétora facial, cefalea, visión borrosa, tos, dolor torácico, ortopnea que aumenta con el Valsalva, hipotensión y fallo cardiaco. La compresión del frénico da lugar a elevación hemidiafragmática. Por último, la lesión de la vía simpática (por neuroblastomas) puede provocar un síndrome de Horner con: ptosis, miosis y enoftalmos. A su vez, podemos encontrar síntomas sistémicos secundarios a metástasis o al propio proceso tumoral.
Como ya hemos visto, el tratamiento con corticoides sistémicos en el paciente con neoplasias hematológicas tiene implicaciones diagnósticas y pronósticas adversas. Además, en presencia de masa mediastínica, puede precipitar complicaciones graves, como el síndrome de lisis tumoral, con insuficiencia renal aguda y riesgo vital. En esta línea, Saraswatula y cols.(14) proponen la necesidad de realizar una radiografía de tórax en pacientes con sibilancias u otra clínica respiratoria de presentación atípica o evolución tórpida, así como en el niño mayor o adolescente con clínica de laringitis previo al inicio del tratamiento con corticoides orales.
Masa abdominal
El hallazgo de una masa abdominal es una de las formas de presentación de neoplasias en la infancia. Aunque algunas son de etiología benigna, todo paciente con masa abdominal ha de ser valorado bajo sospecha de malignidad.
La masa abdominal es con frecuencia detectada por los padres o cuidadores. En la anamnesis, tendremos en cuenta la edad del paciente por sus consideraciones diagnósticas (Tabla VI).
Las masas abdominales más frecuentes son: en los menores de 1 año, las malformaciones congénitas genitourinarias; entre 1-5 años, el neuroblastoma (Fig. 4)
Figura 4. Neuroblastoma en paciente de 7 años, que refiere dolor costal de semanas de evolución asociado a astenia y anorexia en los últimos días.
y el nefroblastoma o tumor de Wilms (Fig. 5);
Figura 5. Tumor de Wilms derecho. La paciente de 2 años consultó, porque los padres palparon la masa abdominal mientras la vestían.
y en niños mayores y adolescentes, el linfoma no Hodking, generalmente tipo Burkitt. Este último se presenta como masa abdominal de crecimiento rápido con: distensión, dolor, síntomas obstructivos intestinales, alteraciones metabólicas secundarias a la lisis tumoral y, en algunos casos, invaginación intestinal. De hecho, ante una invaginación intestinal en un niño mayor, hemos de sospechar la presencia de un linfoma como causa de la misma. En las niñas y adolescentes, tendremos en cuenta los tumores ováricos y el embarazo. Hemos de investigar, a su vez, los síntomas asociados, como: dolor; disfunción de órganos por efecto de la masa (obstrucción intestinal o urinaria); hematuria (nefroblastoma); síntomas sistémicos [sudoración nocturna, fiebre, astenia, pérdida de peso o dolor óseo (neuroblastoma metastásico)]; tiempo de evolución (las masas malignas son de crecimiento más rápido); y antecedentes personales, como prematuridad y bajo peso al nacimiento (hepatoblastoma).
La exploración física ha de ser meticulosa, con toma de constantes vitales y tensión arterial. Se ha de realizar con el paciente relajado y tranquilo, lo que suele ser más fácil en presencia y contacto físico con los padres. En la inspección, buscaremos irregularidades en la superficie abdominal. En la palpación, hemos de tener en cuenta que, en pacientes sanos, sobre todo en los lactantes, algunas estructuras son palpables, como: hígado, bazo, riñones, aorta abdominal, colon sigmoide, heces y/o columna vertebral. Se ha de valorar la realización de un tacto rectal, excepto en el paciente con neutropenia por el riesgo de infección. En la exploración pélvica de la niña pequeña, es preferible la palpación abdominal y/o rectal bimanual. Es importante establecer: la localización, el tamaño, la forma y el contorno de la masa, así como la presencia de dolor a la palpación. Las masas localizadas en el cuadrante superior derecho suelen tener un origen hepático, renal o adrenal. Las masas del cuadrante superior izquierdo con frecuencia dependen del bazo y pueden ser causadas por infiltración metastásica. Las masas abdominales bajas suelen ser secundarias a tumores ováricos o a linfoma intestinal. En el paciente con sospecha de neuroblastoma, es importante la exploración neurológica completa ante la posibilidad de invasión del canal medular. Otros signos de la exploración que pueden orientar el diagnóstico son: aniridia, hemihipertrofia y malformaciones genitourinarias (nefroblastoma); nódulos subcutáneos, equimosis periorbitarias, proptosis, diarrea acuosa intratable, síndrome de Horner o síndrome de opsoclono-mioclono (neuroblastoma); pubertad precoz, feminización o virilización (masas hepáticas, gonadales, suprarrenales o germinales) y fenotipo Cushing (neoplasias de la corteza suprarrenal).
Ante el hallazgo de una masa abdominal, hemos de derivar al paciente a un centro especializado en un plazo de 48 horas(9).
Masas de partes blandas y cutáneas
Los sarcomas de tejidos blandos (STB) presentan una incidencia en la edad pediátrica del 6,7%. Constituyen un grupo heterogéneo, siendo el más frecuente el rabdomiosarcoma (58,1%)(1), tumor originario de las células mesenquimales involucradas en el desarrollo del músculo estriado y con una edad media de máxima incidencia en torno a los 5 años. Los STB pueden aparecer en cualquier localización anatómica, siendo las más frecuentes: región genitourinaria, cabeza-cuello y extremidades. La clínica de presentación depende de la localización, el tamaño y las estructuras vecinas. Una tumoración no justificada en cualquier localización con alguna de las siguientes características es sospechosa de STB: diámetro mayor de 2 cm, afectación de planos profundos, consistencia aumentada, crecimiento progresivo y adenopatías regionales, así como las masas de aparición en un recién nacido y crecimiento posterior (excluyendo los hemangiomas). En cabeza y cuello, la presencia de una masa de partes blandas de localización inusual puede dar lugar a sintomatología local no justificada o que simula otras patologías: proptosis, obstrucción nasal unilateral persistente y no justificada con o sin rinorrea y/o sangrado, pólipo aural u otorrea persistente. En región genitourinaria, se puede presentar como: retención de orina, masa pélvica, tumefacción escrotal, sangrado vaginal o como masa mamelonada vaginal. Ante la sospecha de un tumor de partes blandas, hemos de derivar al paciente a un centro especializado en un plazo de 48 horas(9).
Síntomas y signos musculoesqueléticos
El dolor musculoesquelético es un motivo de consulta frecuente en Atención Primaria, con una frecuencia del 6,2% en mayores de 3 años. Sin embargo, el origen será tumoral en menos del 1% de los casos. La causas que lo producen pueden ser: traumáticas (las más frecuentes), síndromes por sobrecarga, osteocondrosis, inflamatorias, infecciosas y neoplásicas. Entre los cánceres más frecuentes, que se presentan como dolor óseo y/o articular, encontramos: tumores óseos primarios, neuroblastomas, linfomas no Hodgkin y leucemias.
El dolor óseo localizado de origen tumoral suele ser: persistente, asimétrico, progresivo, responde mal a los analgésicos habituales y puede despertar por la noche. En un 60-70% de los casos, se observa una masa palpable adherida a planos profundos, indurada y de crecimiento rápido y progresivo. Las neoplasias más frecuentes en estos casos son los tumores óseos primarios, como el osteosarcoma o el sarcoma de Ewing. El dolor musculoesquelético generalizado se manifiesta como: dolor de miembros inferiores, de espalda, artralgias o artritis. Los tumores que lo producen son: leucemias, sobre todo linfoblásticas, y metástasis óseas o medulares de tumores como el sarcoma de Ewing o el neuroblastoma.
Varios autores han resaltado la importancia de incorporar las leucemias y los tumores óseos en el diagnóstico diferencial de pacientes con sospecha de osteomielitis o enfermedades reumatológicas. De hecho, en la artritis idiopática juvenil (AIJ) y la artritis reactiva, la presencia de dolor muscular, sobre todo, en forma de dolor de miembros inferiores o de espalda, es poco frecuente, por lo que su presencia nos ha de alertar ante la posibilidad de cáncer. Por otra parte, las leucemias que se presentan con síntomas musculoesqueléticos y articulares (generalmente en forma de oligoartritis asimétrica) asocian con menos frecuencia la sintomatología típica de la leucemia (como síndrome constitucional, signos de sangrado…), lo que dificulta el diagnóstico(15). Los datos del hemograma pueden ser poco significativos, describiéndose hasta un 25% de pacientes con leucemia y clínica musculoesquelética, sin alteraciones iniciales en el mismo(15). Sin embargo, cuando sí aparecen, son una ayuda en el diagnóstico diferencial. Así, han sido descritos como factores predictivos diagnósticos de leucemia: leucopenia (<4 x 109/L), plaquetas en límite bajo de la normalidad (150 – 250 x 109/L) e historia de dolor nocturno. Cuando estos 3 factores se presentan de forma simultánea, la sensibilidad y la especificidad en el diagnóstico de leucemia son del 100% y del 85%, respectivamente(16). Cabe destacar, la importancia de un diagnóstico preciso previo al inicio del tratamiento con corticoides, ante la posibilidad de enmascarar una neoplasia hematológica e influir en su pronóstico a largo plazo. Por ello, algunos autores sugieren la realización de un estudio de médula ósea antes de comenzar el tratamiento con corticoides en aquellos pacientes con sospecha de enfermedad reumatológica y datos atípicos(17).
En el paciente con dolor óseo y/o articular, con sospecha de cáncer, realizaremos una radiografía simple, así como un hemograma completo con frotis de sangre periférica, reactantes de fase aguda, fosfatasa alcalina y LDH en un plazo de 48 horas. Si la radiografía es patológica, se derivará al paciente a un centro especializado en las siguientes 48 horas. Ante la sospecha de leucemia (dos o más citopenias y/o blastos) la derivación será inmediata(9).
Alteraciones oculares
El retinoblastoma es la neoplasia ocular más frecuente y representa un 3% de los tumores infantiles(1). Dos terceras partes de los casos son diagnosticados antes de los 2 años y un 95% antes de los 5 años de edad. Se manifiesta de forma bilateral/multifocal (25%) (siendo el 25% hereditarios y el 75% resultado de una nueva mutación en la línea germinal) o unilateral/unifocal (75%) (la mayor parte de los casos no hereditarios). En más de la mitad de los casos, el signo de presentación es la leucocoria, que aparece como consecuencia de la presencia de una masa situada detrás del cristalino. En el diagnóstico diferencial de la leucocoria, además del retinoblastoma, se incluyen las cataratas congénitas (preguntar antecedentes de infección en el embarazo, como la toxoplasmosis) y la enfermedad de Coats (una telangiectasia retiniana con deposición de exudados intrarretinianos o subrretinianos que afecta a niños pequeños). Otros síntomas y signos que nos han de alertar son: estrabismo, pérdida de agudeza visual, dolor ocular o proptosis. Los tumores que pueden manifestarse en forma de proptosis son: neuroblastoma, retinoblastoma, rabdomiosarcoma, linfoma e histiocitosis.
El manejo exitoso del retinoblastoma depende de la posibilidad de detectar la enfermedad mientras sea intraocular. Por esta razón, es muy importante explorar el reflejo rojo en todos los recién nacidos y en todas la visitas del programa de salud infantil. El resultado anormal de la exploración del reflejo rojo es indicación de derivación preferente (en menos de 2 semanas) al oftalmólogo(9). Los pacientes con antecedentes familiares de retinoblastoma han de ser derivados, a su vez, para seguimiento oftalmológico especializado.
Otra manifestación ocular de cáncer es el síndrome paraneoplásico opsoclono-mioclono, que se asocia a neuroblastoma en el 50% de los casos. Se caracteriza por movimientos oculares rápidos multidireccionales, involuntarios y caóticos persistentes durante el sueño, mioclonías, ataxia y alteraciones del comportamiento.
El tiempo hasta el diagnóstico en cáncer infantil
La disminución del tiempo hasta el diagnóstico tiene implicaciones pronósticas en algunos tumores infantiles.
El tiempo hasta el diagnóstico (TD), aquel transcurrido desde el inicio de los síntomas hasta el diagnóstico del cáncer, ha sido objeto de varias revisiones en los últimos años (Algoritmo 1). Dang-Tan y cols.(18) agruparon los factores que influyen en el TD como dependientes de los padres y/o del paciente, de la propia enfermedad y del tipo del sistema sanitario. Revisiones posteriores destacan la edad del paciente (a más edad, mayor TD), el tipo de tumor (tumores óseos, del SNC, germinales y el retinoblastoma tienen un TD más prolongado en comparación con leucemias y tumores renales)(19), así como la propia biología tumoral(20) como los factores más involucrados. La relación del TD con la supervivencia es variable. En algunos tumores como el retinoblastoma, un TD corto mejora la supervivencia. Sin embargo, para el meduloblastoma y el sarcoma de Ewing, un TD corto se asocia a menor supervivencia (tumores de alto grado) y un TD prolongado a mayor supervivencia a los 5 años(20).
Función del pediatra de Atención Primaria
El pediatra de Atención Primaria comparte la responsabilidad de disminuir el TD, identificando a aquellos pacientes sospechosos de cáncer y realizando una derivación precoz desde Atención Primaria a especializada. Esta disminución del TD puede tener un papel pronóstico para algunos tumores y, además, contribuye a la disminución de la ansiedad y el estrés vividos por los pacientes y sus familias durante el difícil período previo al diagnóstico de un cáncer infantil(3).
Bibliografía
Los asteriscos reflejan el interés del artículo a juicio del autor.
1. Peris Bonet R, et al. Cáncer infantil de España. Estadísticas 1980-2013. Registro Nacional de Tumores Infantiles (RNTI-SEHOP). Valencia: Universitat de València, 2014 (Edición preliminar, CD-Rom).
2. Ministerio de Sanidad, Servicios Sociales e Igualdad. Portal Estadístico. [sede Web] [acceso 26 de febrero de 2016.]. Disponible en:
http://pestadistico.inteligenciadegestion.msssi.es/publicoSNS/Comun/DefaultPublico.aspx.
3.** Dixon-Woods M, Findlay M, Young B, et al. Parents’ accounts of obtaining a diagnosis of childhood cancer. Lancet. 2001; 357: 670-4.
4. Dommett RM, Redaniel T, Stevens MCG, et al. Risk of childhood cancer with symptoms in primary care: a population-based case-control study. Br J Gen Pract. 2013; 63: e22-9.
5. Wilne S, Collier J, Kennedy C, et al. Presentation of childhood CNS tumours: a systematic review and meta-analysis. Lancet Oncol. 2007; 8: 685-95.
6. Wilne S, Collier J, Kennedy C, et al. Progression from first symptom to diagnosis in childhood brain tumours. Eur J Pediatr. 2012; 171: 87-93.
7. Ansell P, Johnston T, Simpson J, et al. Brain Tumor Signs and Symptoms: Analysis of primary health care records from the UKCCS. Pediatrics. 2010; 125: 112-9.
8.*** Wilne S, Koller K, Collier J, et al. The diagnosis of brain tumours in children: a guideline to assist healthcare professionals in the assessment of children who may have a brain tumour. Arch Dis Child. 2010; 95: 534-39.
9.** NICE. Suspected cancer: recognition and referral. Jun 2015. Disponible en:
www.nice.org.uk/guidance/ng12.
10.*** Walker D, Wilne S, Grundy R, et al. A new clinical guideline from the Royal College of Paediatrics and Child Health with a national awareness campaign accelerates brain tumor diagnosis in UK children “HeadSmart: Be Brain Tumour Aware”. Neuro Oncol. 2016; 18: 445-54.
11. Soldes OS, Younger JG, Hirschl RB. Predictors of malignancy in childhood peripheral lymphadenopathy. J Pediatr Surg. 1999; 34: 1447-52.
12. Yaris N, Cakir M, Sozen E, et al. Analysis of children with peripheral lymphadenopathy. Clin Pediatr (Phila). 2006; 45: 544-9.
13. Nield LS, Kamat D. Lympahdenopathy in children: when and how to evaluate? Clin Pediatr. 2004; 43: 25-33.
14.** Saraswatula A, McShane D, Tideswell D, et al. Mediastinal masses masquerading as common respiratory conditions of childhood: a case series. Eur J Pediatr. 2009; 168: 1395-9.
15.** Brix N, Rosthøj S, Herlin T, Hasle H. Arthritis as presenting manifestation of acute lymphoblastic leukaemia in children. Arch Dis Child. 2015; 100: 821-5.
16. Jones OY, Spencer CH, Bowyer SL, et al. A multicenter case-control study on predictive factors distinguishing childhood leukemia from juvenile rheumatoid arthritis. Pediatrics. 2006; 117: e840-4.
17. Sen ES, Moppett JP, Ramanan AV. Are you missing leukaemia? Arch Dis Child. 2015; 100: 811-2.
18. Dang-Tan T, Franco EL. Diagnosis delays in childhood cancer: a review. Cancer. 2007; 110: 701-13.
19.** Lethaby CD, Picton S, Kinsey SE, et al. A systematic review of time to diagnosis in children and young adults with cancer. Arch Dis Child. 2013; 98: 349-55.
20. Brasme JF, Morfouace M, Grill J, et al. Delays in diagnosis of paediatric cancers: a systematic review comparison with expert testimony in lawsuits. Lancet Oncol. 2012; 13: e445-59.
Bibliografía recomendada
- Alonso Sánchez MA, et al, ed. Cáncer Hereditario. Madrid: Dispublic S.L.; 2006.
Libro muy completo, publicado por la Sociedad Española de Oncología Médica para todo el que quiera saber más sobre el cáncer hereditario.
- Fragkandrea I, Nixon JA, Panagopoulou P. Signs and Symptoms of childhood cáncer: A guide for early recognition. Am Fam Physician. 2013; 88: 185-92.
Artículo enfocado al diagnóstico precoz de cáncer infantil en Atención Primaria; pone el enfoque en aquellos signos de alarma que nos han de poner en alerta ante la posibilidad de procesos neoplásicos.
- Saraswatula A, McShane D, Tideswell D, et al. Mediastinal masses masquerading as common respiratory conditions of childhood: a case series. Eur J Pediatr. 2009; 168: 1395-9.
Muy recomendable. Sugiere la necesidad de revisar el diagnóstico y plantear radiografía de tórax cuando los pacientes con clínica respiratoria no evolucionen de la forma esperada. Advierte, a su vez, de los peligros potenciales de los corticoides cuando se utilizan sin un diagnóstico definitivo.
- Wilne S, Koller K, Collier J, et al. The diagnosis of brain tumours in children: a guideline to assist healthcare professionals in the assessment of children who may have a brain tumour. Arch Dis Child. 2010; 95: 534-9.
Imprescindible. Guía clínica para la sospecha y diagnóstico precoz de tumores del sistema nervioso central.
- Walker D, Wilne S, Grundy R, et al. A new clinical guideline from the Royal College of Paediatrics and Child Health with a national awareness campaign accelerates brain tumor diagnosis in UK children “HeadSmart: Be Brain Tumour Aware”. Neuro Oncol. 2016; 18: 445-54.
Muy interesante. Estrategia lanzada en el año 2011 en el Reino Unido dirigida a profesionales sanitarios y al público en general, con el objetivo de disminuir el intervalo de tiempo desde el inicio de la sintomatología hasta el diagnóstico de tumor del SNC en pacientes pediátricos.
- Pizzo PA, Poplack DG. Principles and practice of pediatric oncology. 6th edition. Philadelphia: Wolters Kluwer/Lippincott Williams and Wikins Health; 2011.
Tratado de Oncología Pediátrica, donde se establecen las directrices para el diagnóstico y el tratamiento de enfermedades hemato-oncológicas infantiles.
| Caso clínico |
|
Paciente de 7 años que presenta cefalea frontal, vespertina de 3 días de evolución, así como pérdida progresiva de visión del ojo izquierdo desde hace 2 semanas. Antecedentes personales: embarazo de curso normal. Parto eutócico. Período neonatal normal. Desarrollo psicomotor normal. Vacunación adecuada para la edad. Antecedentes familiares: madre: 32 años, sana. GAV: 1/0/1. Padre: 38 años, sano. Exploración física: FC: 90 lpm, FR: 18 rpm, TA: 100/60 mmHg. Sat: 97%. Talla: 122 cm (p50). Peso: 24 kg (p50). Buen estado general. Bien hidratado y perfundido. No exantemas ni petequias. No adenopatías significativas. ACP: normal. Abdomen: blando y depresible, no doloroso, no masas ni megalias. Neurológico. Glasgow 15, pares craneales normales. Tono, fuerza y sensibilidad: normales. Reflejos osteotendinosos: normales. Marcha normal. No dismetrías ni disdiadococinesia. Exploración oftalmológica: ojo izquierdo con disminución de agudeza visual, signos de atrofia de papila, así como hemianopsia temporal izquierda. Pruebas complementarias: hemograma, bioquímica y coagulación normales. Se realiza resonancia magnética cerebral observando: masa heterogénea en línea media, supraselar, multiquística, de 40 x 36 x 39 mm (Fig. 6), con realce intenso y heterogéneo tras la administración de contraste (Fig. 7). Sistema ventricular normal sin signos de hidrocefalia. Juicio clínico: craneofaringioma (patrón adamantinomatoso).
Figura 6. Masa heterogénea en línea media, supraselar, multiquística, de 40 x 36 x 39 mm. Figura 7. Masa en línea media con realce intenso y heterogéneo tras la administración de contraste.
|