|
| Regreso a las bases |
J. Marès Bermúdez*, D. van Esso Arbolave**, A. Saiz de Marco***
*Institut Pediàtric Marès-Riera. Blanes. Girona. **EAPRASnet Steering Committee. European Academy of Pediatrics. Bruselas. ***CAP Federico del Castillo. Jaén
| Resumen
Los defectos de refracción afectan hasta el 10 % de niños preescolares. Las ametropías no detectadas precozmente, especialmente las anisometropías, pueden interferir con el proceso madurativo de la visión y generar una ambliopía. La determinación de la agudeza visual con optotipos es la técnica más utilizada para la detección de defectos visuales, pero su principal limitación es que no puede realizarse antes de los 3-4 años de forma fiable. Entre los 1 a 3 años es la “edad crítica” en la que se generan la mayoría de las ambliopías anisometrópicas y, en la que su detección y tratamiento, consiguen alcanzar los mejores resultados visuales. Los autorefractómetros permiten a los profesionales explorar la visión en este rango de edad, y detectar precozmente defectos potencialmente ambliogénicos, convirtiendo a esta técnica instrumental como la de elección para el cribado de los defectos de refracción entre 1 a 4 años de edad en Atención Primaria. |
| Abstract
Refractive errors affect up to 10 % of preschool children. Undetected ametropia, especially anisometropia, can interfere with the maturation process of vision and lead to amblyopia. |
Palabras clave: Defectos de refracción; Ametropías; Anisometropías; Ambliopía; Autorefractómetro.
Key words: Refractive errors; Ametropia; Anisometropia; Amblyopia; Autorefractometers.
Pediatr Integral 2023; XXVII (1): 57.e1 – 57.e8
OBJETIVOS
• Justificar la necesidad de una detección más precoz de los defectos de refracción en los primeros años de la vida.
• Conocer las herramientas disponibles para anticipar la detección precoz en Atención Primaria.
• Proponer la utilización de los autorefractómetros automáticos binoculares, como la técnica instrumental de elección para el cribado de los defectos de refracción en Atención Primaria en niñas y niños de 1 a 4 años de edad.
Detección precoz de los trastornos de refracción en Atención Primaria
Introducción
La detección precoz de los defectos de refracción, habitualmente asintomáticos, es esencial para el pronóstico visual del paciente, para el desarrollo de sus habilidades o capacidades, y para una óptima calidad de vida.
Las pruebas de screening visual están incluidas en los protocolos de actividades preventivas de la edad pediátrica y tienen la finalidad de detectar los defectos de la visión para poder tratarlos precozmente. La mayoría de estos defectos son asintomáticos y, por lo tanto, el cribado debe ser universal, sistemático y, a ser posible, con instrumentos que permitan la máxima objetividad en la evaluación, minimizando los errores de detección debidos a la subjetividad, tanto de los pacientes explorados como del explorador.
Los defectos de refracción (hipermetropía, miopía y astigmatismo), también denominados ametropías, son extremadamente frecuentes y afectan a un 10 % de los niños en edad preescolar y hasta el 20 % en edad escolar. A diferencia del ojo normal o emétrope, cuando existe un defecto de la refracción, la imagen del objeto no se proyecta correctamente sobre la retina, dando lugar a una visión poco nítida y, por tanto, una menor agudeza visual, haciendo necesario un esfuerzo acomodativo para intentar mejorar la nitidez de la imagen. Una de las potenciales consecuencias de los defectos de refracción, especialmente cuando son asimétricos (anisometropía), cuando cada ojo tiene una refracción diferente, es la ambliopía(1,2).
La ambliopía es la pérdida de visión, generalmente en un ojo (ojo vago), a consecuencia de la falta de estimulación adecuada durante el periodo de desarrollo de la visión. La maduración visual es un proceso continuo que comienza al nacimiento y finaliza, aproximadamente, a los 7 años. Durante este periodo, si existe una ausencia de estimulación visual adecuada, generalmente debida a un defecto de refracción unilateral o asimétrico, el cerebro elimina la imagen borrosa que proviene del ojo con mayor defecto dando lugar a una ambliopía. La ambliopía es la causa prevenible de pérdida permanente de la visión más importante en la edad pediátrica y ocurre en el 2-4 % de los niños(1,2).
El adecuado tratamiento de la ambliopía es edad dependiente, siendo más efectivo cuanto más precoz se inicie. El 90 % de las ambliopías estrábicas o anisometrópicas se resuelven completamente con un tratamiento correcto si el mismo se inicia antes de los 4 años, un 60 % cuando el tratamiento se inicia entre los 4-6 años, y los resultados son malos (<30 % de resolución) si el tratamiento se demora más allá de los 6 años(3)
Otros defectos de refracción no ambliogénicos, pero presentes en los primeros años de la vida, interfieren en la capacidad visual del pequeño pudiendo afectar, en mayor o menor grado, su aprendizaje, desarrollo, conducta o en la adquisición de habilidades.
Por estas razones, la detección precoz de los defectos de refracción es un reto para el pediatra, la ausencia de síntomas obliga a plantear estrategias específicas para descubrirlos, y el retraso en su diagnóstico y tratamiento puede tener consecuencias muy relevantes, en ocasiones, irreversibles, para el paciente.
Detección de las ametropías en la consulta de Atención Primaria
Las pruebas para la detección precoz de los defectos de refracción visual deben incorporarse de forma rutinaria en el programa de seguimiento del niño sano.
Si tenemos en cuenta que la mayoría de ametropías, la anisometropía y la ambliopía suelen ser asintomáticas, su detección precoz requiere una planificación, en función de las técnicas de cribado disponibles, que permita una evaluación sistemática y universal desde el primer año de vida, en la etapa preescolar y en la edad escolar.
Evaluación en el primer año de vida
En el recién nacido y en el lactante de pocos meses de vida, la detección de posibles defectos visuales y de refracción se basará en(1,2):
• Examen del tamaño y transparencia corneal.
• Presencia de reflejo fotomotor.
• Parpadeo ante la iluminación intensa o brillante.
• Fijación de la mirada a partir del mes de vida.
• Seguimiento visual a los 2-3 meses de vida.
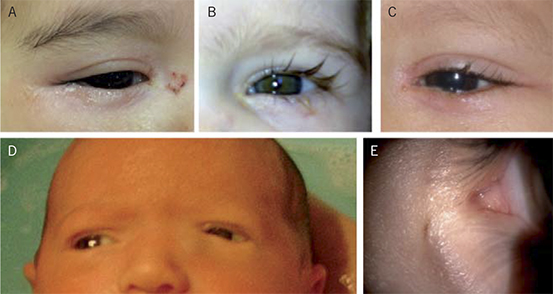
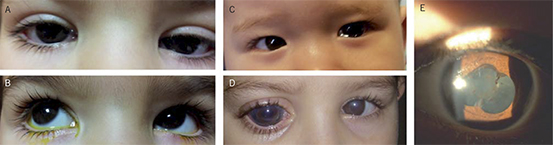
• Reflejo rojo del área pupilar al visualizar las pupilas con un oftalmoscopio a 1 metro de distancia (test de Brükner). Además de permitir detectar opacidades del cristalino (cataratas) o alteraciones de la retina (retinoblastoma), la detección de un reflejo rojo de brillo asimétrico entre ambos ojos sugiere una anisometropía. Debe realizarse en una habitación con poca luz.
• Motilidad ocular adecuada.
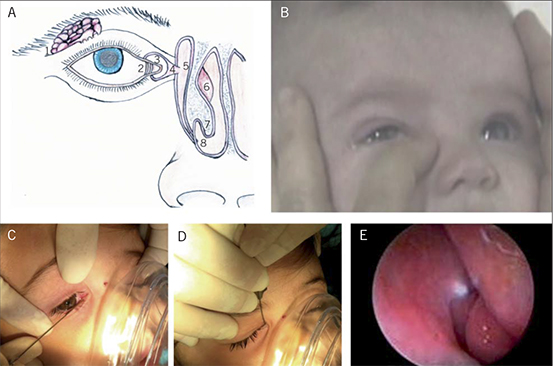
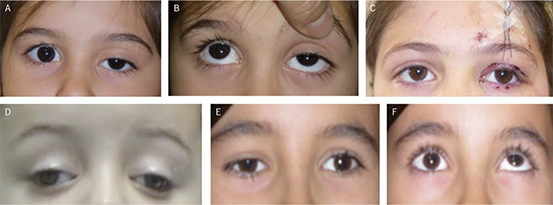
• Alineación ocular correcta. Es de utilidad explorar con una fuente de luz para visualizar el reflejo luminoso corneal centrado en las pupilas (test de Hirschberg) y, a continuación, es útil ocluir intermitentemente y alternativamente los ojos (maniobra de cover – uncover) que permite detectar forias (estrabismo latente). Un estrabismo intermitente en los 6 primeros meses de vida se puede considerar normal, pero no si es constante. A partir de esta edad cualquier pérdida de alineación es patológica.
Cualquier alteración en la evaluación de estos parámetros, puede ser debida a un defecto de refracción u otra anomalía visual, y requerirá derivación al oftalmólogo para evaluación.
Evaluación entre 1 a 6 años de edad
Las técnicas utilizadas, en nuestros programas de actividades preventivas, para la detección de los defectos de refracción en la etapa preescolar son, en la mayoría de los centros, los optotipos clásicos que miden la agudeza visual: E de Snellen, optotipos de Pigassou otros optotipos equivalentes y, se aplican de forma sistemática a los 3-4 años de edad. No obstante, en muchos casos no es posible obtener un resultado fiable a los 3 años, situación que aboca a la recitación del paciente, con el riesgo de pérdida de seguimiento o de diagnóstico tardío. Incluso cuando se realiza el cribado a los 4 años, en ocasiones, el resultado es poco fiable por falta de colaboración del paciente. Esperar a que el paciente sea mayor y colabore más implica siempre, en caso de que exista una anisometropía y riesgo de ambliopía, un diagnóstico y tratamiento tardío. El screening mediante optotipos es una técnica subjetiva, requiere colaboración del examinado, destreza del examinador y un tiempo de ejecución que, especialmente en las edades más críticas (3-4 años), no es desdeñable. Con excesiva frecuencia se difiere la exploración porque “el niño no colabora”(2). Una dificultad añadida la presentan los niños con retraso global de desarrollo cognitivo o con problemas de comunicación (hasta un 2-5 % de los niños), en los que pocas veces se consigue realizar una evaluación fiable con optotipos a esta edad.
La detección antes de los 3-4 años de los defectos visuales preexistentes, que generalmente cursan sin síntomas ni signos que permitan sospecharlos, es clave para minimizar los casos de ambliopía. Precisamente, es entre 1 a 3 años la “edad crítica” en la que se desarrollan la mayoría de las ambliopías si existe una anisometropía o un estrabismo no corregidos.
Con la finalidad de realizar una detección más precoz se han desarrollado nuevas herramientas, como los test de visión estereoscópica (poco utilizados en nuestro medio y que además también son subjetivos) y, más recientemente, los denominados autorefractómetros binoculares, que son dispositivos automáticos que permiten una valoración objetiva de la refracción visual a partir de los 6 meses de edad(2,4).
La razón por la que se ha establecido la edad de los 3-4 años para valorar la agudeza visual ha estado siempre condicionada por las técnicas disponibles (optotipos) para el cribado de toda la población pediátrica. Actualmente, la existencia de dispositivos automáticos que permiten valorar a estos pacientes desde los 6 meses permite cubrir una edad en la que los defectos potencialmente ambliogénicos ya están presentes. Estos instrumentos permiten, por lo tanto, explorar con garantías a todos los niños a edades mucho más precoces que los 3-4 años y evaluar también a los no colaboradores de 3-4 años o mayores, muy especialmente a la gran mayoría de niños con retrasos de desarrollo o problemas de comunicación.
Evaluación de la agudeza visual con optotipos
La evaluación subjetiva de la agudeza visual (AV) permite comprobar la presencia de una función visual adecuada o inadecuada, y es una prueba esencial para la detección de defectos visuales en la infancia. Precisa de la colaboración del niño y es posible realizarla en algunos niños muy colaboradores a partir de los 3 años y, en la mayoría de los casos, a partir de los 4 años. Para ello se utilizan distintos optotipos, como el de dibujos de Pigassou (Fig. 1) a partir de los 3 años, la E de Snellen (Fig. 2) a partir de los 4 años y optotipos de letras a partir de los 5-6 años de edad(1,2,4).
Figura 1. Optotipo de Pigassou. Dibujos fácilmente reconocibles para niños a partir de los 3 años de edad. Pueden nombrarlos o señalarlos en una lámina de plástico que contiene los mismos dibujos.
Figura 2. Optotipo con la E de Snellen. El niño debe indicar hacia donde van las puntas de la E verbalmente, indicándolo con el dedo o con la ayuda de una E de plástico o cartón rígido que coloca como la que se le muestra.
La evaluación con optotipos no detecta defectos de refracción, sino déficits de agudeza visual que, si está por debajo de la considerada como normal para la edad del niño o se detecta una diferencia de agudeza visual en más de 0,2 entre ambos ojos, obligará a remitir al paciente para evaluación por el oftalmólogo.
• Procedimiento: la exploración correcta requiere una iluminación adecuada, colocar la paciente a la distancia correcta (3-5 metros), según el optotipo utilizado, y realizar primero la evaluación binocular y, posteriormente, de cada ojo por separado, ocluyendo adecuadamente el ojo contrario; ya que los niños con hipermetropía tendrán generalmente una AV normal gracias a su capacidad de acomodación, es recomendable realizar en los niños con prueba de AV normal, una nueva medición con una lente de +2,0 dioptrías (D). En caso de tratarse de una paciente hipermétrope, seguirá mostrando una AV normal, mientras que el emétrope presentará una AV menor cuando se explora con dicha lente. En este caso el niño con AV normal con y sin lentes de +2,0 deberá remitirse al oftalmólogo para valorar la presencia de una hipermetropía(1,2).
• Limitaciones: el principal problema del screening de la AV con optotipos es que no es realizable en la mayoría de los casos de forma fiable antes de los 4 años de edad, requiere colaboración del paciente y pericia por parte del examinador. No permite explorar a la gran mayoría de niñas y niños con dificultades de comunicación y desarrollo. Permite detectar pacientes que presentan ametropías y anisometropías, pero a una edad relativamente tardía, especialmente en los niños afectos de ambliopía en los que sería deseable un diagnóstico más precoz(2).
Test de visión estereoscópica
Los test de visión estereoscópica son pruebas que exploran la estereopsis o visión en 3D que está ausente en caso de defectos de refracción con anisometropía y en los defectos de alineación visual, motivo por el cual se ha postulado como herramienta de screening para la ambliopía y el estrabismo(4).
Para que la visión estereoscópica tenga lugar el cerebro, debe poder fusionar dos imágenes similares pero diferentes que le llegan de cada ojo, lo que permite elaborar una imagen tridimensional. Si una de las imágenes es anulada por el cerebro, no habrá visión estereoscópica. Los defectos visuales que con mayor frecuencia producen pérdida de la visión estereoscópica son los estrabismos y las anisometropías, y su consecuencia es la ambliopía(5).
Test de Lang (Fig. 3)
Figura 3. Lang-stereotest. Test sencillo para evaluar la visión estereoscópica (tridemensional) sin necesidad de usar gafas polarizadas. La estrella se visualiza en visión bidimensional (monocular o sin visión estereoscópica). La luna, el elefante y el camión solo si el niño tiene una estereopsis adecuada.
El test de Lang es muy sencillo y rápido de realizar si el paciente colabora. No requiere el uso de gafas con lentes polarizadas. Consiste en una placa del tamaño de una postal en la que hay unas imágenes en 3D que el niño tiene que señalar cuando se realiza el test. Puede utilizarse de forma rutinaria a los 3 años de edad (o, en ocasiones, incluso a partir de los 2 años), adelantando por lo menos en 1-2 años la derivación al oftalmólogo en caso de sospecha de alteración de la visión binocular, tomando como referencia la aplicación del test de la E de Snellen a los 4 años.
El Lang-Stereotest II tiene 3 imágenes tridimensionales: luna, camión y elefante, y una imagen bidimensional: estrella, que se ve sin visión estereoscópica (visibles con un solo ojo), que sirve para captar la atención del paciente. La gran disparidad entre las 3 figuras y la fácil visualización de la estrella lo hace un test muy práctico en la consulta pediátrica.
• Procedimiento: para practicar el test se coloca la placa, con el observador delante del niño para poder observar sus movimientos oculares. Se le solicita que mire la lámina situada perpendicularmente a unos 40 cm de la cara del niño y se le pregunta si ve algo, observando sus movimientos oculares. Una vez identificado un objeto tridimensional se le indica que identifique otros adicionales. La respuesta puede ser verbal o señalando con el dedo. Si la visión estereoscópica es normal, identifica las 3 figuras tridimensionales correctamente. En el caso de defecto de la visión estereoscópica se identifica únicamente la estrella. Un test se considera positivo cuando se identifican correctamente las 3 figuras tridimensionales y es indicativo de una estereopsis correcta. Un test negativo o dudoso (identificación de una sola figura) requiere derivación al oftalmólogo. El Lang-Stereotest no mide la agudeza visual ni la refracción. Un resultado negativo solo indica una falta de visión estereoscópica(5,6).
Test de Titmus o test “de la mosca” (Fig. 4)
Figura 4. Fly Stereo Acuity Test o test de la “mosca”. Test de estereopsis que requiere el uso de gafas polarizadas y que permite que el paciente con visión estereoscópica adecuada visualice la mosca por delante de la lámina con imagen tridimensional.
Es el test de estereopsis más utilizado en la práctica clínica, ya que es de muy fácil comprensión y aplicación, tanto para niños como para adultos. Requiere que el paciente utilice unas gafas con filtros polarizados que al observar unas imágenes llamadas anáglifos (imágenes bidimensionales capaces de producir un efecto tridimensional) las percibe con un efecto de profundidad.
• Procedimiento: se le enseña la lámina con la mosca y se le colocan a continuación las gafas polarizadas y se le pregunta que cambios observa. Se le indica que toque las alas de la mosca y el observador comprueba que con los dedos no toca la lámina, indicativo que está observando la imagen en 3D. La mosca explora la estereopsis más gruesa. Adicionalmente, se puede explorar la estereopsis de forma más fina preguntando en relación a los círculos (puntos de Wyrth), cuál de ellos sobresale a los demás. Si el niño realiza bien la prueba, podemos asegurar que su visión estereoscópica es normal y, por tanto, presenta una adecuada visión binocular(8,9).
Requiere respuestas verbales y buena comprensión; por lo tanto, puede realizarse a partir de los 4-5 años de edad, por lo que no representa un avance en relación con el cribado mediante optotipos clásicos para la detección de ambliopías.
• Limitaciones: los test de estereopsis son pruebas subjetivas, que requieren de la colaboración del paciente con resultados falsos positivos y negativos con relativa frecuencia. La única función de estos test es detectar la falta de visión estereoscópica que presentan los niños con ambliopía o estrabismo, no permiten detectar defectos de refracción no ambliogénicos, ya que no evalúan la refracción visual ni la agudeza visual(2).
Pruebas instrumentales de diagnóstico visual: autorefractómetros
Los autorefractómetros binoculares automáticos son actualmente el método de elección para la detección precoz de las ametropías entre 1 año y los 4 años de edad.
La dificultad para la detección precoz de los déficits visuales con repercusión clínica significativa, especialmente la ambliopía, antes de los 4 años de edad, en la que el niño generalmente ya colabora para determinar su AV, limita la posibilidad de recuperación completa en muchos niños afectos. Por esta razón, se han desarrollado pruebas instrumentales actualmente disponibles y fácilmente aplicables en las consultas de Atención Primaria: los autorefractómetros binoculares.
Los autorefractómetros (Fig. 5 y 6), también denominados photoscreeners, son instrumentos que permiten medir de forma automática y objetiva la refracción visual de ambos ojos simultáneamente a partir de los 6 meses de edad. Generalmente, no será necesario utilizarlos en edades tan tempranas, salvo sospecha clínica, pero su utilización sistemática a partir de los 11-12 meses puede aportar grandes ventajas frente a las técnicas tradicionales previamente comentadas (2,4).
Figura 5. Autorefractómetro binocular PlusoptiX ® S12C. Muestra la imagen del niño en pantalla durante la prueba, y el resultado de la misma una vez realizada, con la indicación de “pasar” o “remitir” en función de la necesidad de derivación al oftalmólogo.
Figura 6. Autorefractómetro binocular Spot Vison Screener®. Muestra una representación de la alineación ocular en pantalla durante la prueba, y el resultado de la refracción una vez realizada, con la indicación de la necesidad o no de derivación al oftalmólogo.
Estos instrumentos utilizan infrarrojos y realizan automáticamente una fotoretinoscopia binocular por infrarrojos, por lo que se denominan autorefractómetros. Exploran, en pocos segundos, ambos ojos simultáneamente y requieren muy poca colaboración del paciente. Es suficiente que durante unos instantes el niño fije la mirada para que el aparato pueda obtener una medición válida.
El screening instrumental mediante autorefractómetro tiene, en Atención Primaria, varias ventajas respecto a los test tradicionales(2,7):
• Permite realizarlo en lactantes(>6 meses) y niños pequeños, cubriendo el rango de edad de 1-3 años inabordable con optotipos.
• Requiere únicamente una mínima colaboración del paciente.
• Útil en pacientes incapaces de comprender las indicaciones necesarias de los test de agudeza visual (retraso del desarrollo).
• Detección simultánea de los defectos de refracción y alineación.
• Rapidez y eficiencia.
A finales de 2012, la American Academy of Pediatrics (AAP) junto con a la American Academy of Ophtalmology (AAO), la American Association for Pediatric Ophtalmology and Strabismus (AAPOS) y la American Association of Certified Orthoptists elaboraron unas recomendaciones que avalaban el uso de aparatos de screening instrumental visual en la población pediátrica(7). En 2013, el comité de screening visual de la AAPOS revisó sus criterios para el screening visual basado en instrumentos, con la finalidad de conseguir una elevada especificidad en la detección de los factores de riesgo de ambliopía en los lactantes y niños pequeños (minimizar los falsos positivos en la derivación) y una elevada sensibilidad en niños mayores (minimizar los falsos negativos a una edad en la que disminuyen las posibilidades de tratamiento en caso de no detección del problema), y elaboraron unos criterios de derivación para astigmatismo, hipermetropía, anisometropía y miopía en función de la edad de screening: 12-30 meses, 31-48 meses y >48 meses(8).
Procedimiento para la realización de la prueba
La medición con un autorefractómetro requiere una habitación en la que no haya excesiva luz. Debe evitarse la luz natural intensa o muy directa y, si se utiliza luz artificial, deben evitarse bombillas incandescentes o halógenas, siendo adecuada la luz de fluorescentes y leds. El paciente debe mirar al frente hacia la cámara del dispositivo. Las pupilas deben estar alineadas con el dispositivo, que suele tener una imagen que llama la atención del niño para que este mire hacia el aparato. La mayoría de los autorefractómetros emiten además un sonido o luces que atraen la atención, una característica especialmente útil en lactantes. Desde una distancia de 1 m se realiza la medición de forma automática, que requiere solo 1 segundo aproximadamente, a partir del momento en que el aparato detecta correctamente ambas pupilas, ya que la medición es siempre binocular y simultánea. El tamaño de las pupilas debe ser de, al menos, 4 mm para poder hacer una medición correcta. El dispositivo detecta si el observador se encuentra demasiado cerca o alejado y realiza la medición cuando se encuentra a la distancia adecuada y ha podido detectar ambas pupilas correctamente. En caso de pupilas demasiado pequeñas o demasiado grandes, no se puede realizar la lectura, y es necesario adecuar la intensidad de la luz de la sala para conseguir modificar el tamaño pupilar en el rango adecuado(2).
El nombre, los datos de identificación y la fecha de nacimiento del paciente se introducen en el dispositivo mediante un teclado a través de una pantalla táctil. El software del aparato utiliza estos datos para calcular la edad y establecer los puntos de corte para decidir la derivación al oftalmólogo según el resultado de la refracción observada. Es posible almacenar los resultados e imprimir el informe con el resultado de la prueba. Las características de impresión, velocidad de captación de la imagen, determinación de los valores de corte para decidir la necesidad de derivación al oftalmólogo, varían en función de los distintos aparatos disponibles en el mercado(2).
Sensibilidad y especificidad de los instrumentos actualmente disponibles
La sensibilidad media para detectar factores de riesgo asociados a ambliopía, utilizando láminas u optotipos a los 4 años de edad que determinan agudeza visual, es del 77 %, mientras que con los autorefractómetros el rango oscila entre 81-92 %, con la ventaja de que puede realizarse la detección desde los 6 meses de vida, y con una fracción mínima de tiempo en comparación con el necesario para practicar la agudeza visual mediante láminas (optotipos)(2).
PlusoptiX ® S12C (Fig. 5) es un modelo de autorefractómetro para screening que tiene una sensibilidad y especificidad medias del 92 % y 88 % respectivamente, según el fabricante. El dispositivo permite escoger, antes de la medición, entre 5 tablas de referencia, que van desde la 1 (mayor sensibilidad y menor especificidad) hasta la 5 (mayor especificidad y menor sensibilidad). Los resultados de la medición se visualizan en una pantalla y el dispositivo indica “pasar” o “remitir” (Fig. 7), indicando la necesidad de derivación al oftalmólogo, en función de los resultados de la determinación, la edad del paciente y la tabla de referencia seleccionada.
Figura 7. Resultado de la refracción visual con la indicación de derivar al oftalmólogo, tal como se muestra en la pantalla del dispositivo cuando el explorador realiza la prueba con PlusoptiX ® S12C.
La información se almacena en formato PDF (en una tarjeta de memoria) y es imprimible a partir de dicho PDF vía ordenador o bien directamente a impresoras WiFi compatible (Fig. 8)(2).
Figura 8. Resultado en PDF imprimible de un test de refracción con el autorefractómetro PlusoptiX® S12C. Indica la refracción visual y el criterio de remisión al oftalmólogo en relación a los puntos de corte para cada parámetro, en función de la edad y la sensibilidad/especificidad de la tabla seleccionada. En este caso se muestra una anisometropía por hipermetropía del ojo izquierdo en un paciente de 16 meses de edad que debe remitirse al oftalmólogo para valoración.
Los datos de medición se visualizan en la pantalla y permiten al observador realizar su propia interpretación más allá de las indicaciones de “pasar” o “remitir” que definen los programas incorporados. En un reciente estudio el PlusoptiX ® A12 en 201 niños (402 ojos) de 7,63±3,41 años, presentó una sensibilidad, especificidad, valor predictivo positivo (VPP) y valor predictivo negativo (VPN): para miopía, de 86 %, 93 %, 82 % y 94 %, respectivamente; para astigmatismo, 85 %, 98 %, 88 % y 98 %, respectivamente; y para hipermetropía, de 40 %, 100 %, 100 % y 98 %, respectivamente(9).
Vila de Muga y cols.(10) realizaron un estudio prospectivo multicéntrico en 4 centros de Atención Primaria de Barcelona a pacientes entre 18 meses y 30 meses de edad, utilizando el Spot Vision Screener® (Fig. 6). En este estudio, el screening estuvo a cargo de las enfermeras y pediatras en las visitas del programa de actividades preventivas y todos ellos fueron posteriormente valorados por el equipo de oftalmología de referencia. El objetivo del estudio fue valorar si, en este grupo de edad (18-30 meses), Spot®Vision Screener era útil y preciso para detectar los factores de riesgo para desarrollar una ambliopía. Se incluyeron 435 pacientes, detectándose alteraciones en 42 (9,3 %). En este estudio la sensibilidad para detectar pacientes con factores de riesgo para ambliopía fue del 89 % y la especificidad del 91 %, con un VPP del 76 % y un VPP del 96 %. Cerca del 50 % de los pacientes derivados de 18-30 meses precisaron corrección óptica desde la primera valoración por el equipo de oftalmología, y a un 40 % con defecto de refracción confirmado sin indicación de corrección inicialmente, se les citó para seguimiento oftalmológico. La conclusión principal del estudio fue que el uso del autorefractómetro es útil y preciso en menores de 3 años(10).
Los autorefractómetros (photoscreeners) más utilizados en nuestro país son:
• PlusoptiX® S12 (Fig. 5).
• Spot Vision Screener® (Fig. 6).
Además de la evaluación de la refracción visual y detectar las ametropías, los autorefractómetros permiten medir el tamaño pupilar, la alineación visual, así como detectar opacidades en el eje visual (cataratas, glaucoma infantil, vítreo primario, retinoblastoma), que al impedir realizar la fotoretinoscopia darán como resultado la imposibilidad de realizar la medición, alertando al pediatra sobre la necesidad de derivar al paciente al oftalmólogo.
La mayor dificultad que presentan estos dispositivos (y también los optotipos en la medición de la agudeza visual) es la detección de algunas hipermetropías binoculares que no generan anisometropía, ya que los niños pueden tener una gran capacidad de acomodación que las compensa. Por ello, es recomendable que a partir de los 3-4 años se realice, además de la medición directa, otra medición de la refracción colocándole unas lentes de + 3 D. En el caso de una niña o niño sin hipermetropía, el autorefractómetro detectaría una miopía de aproximadamente el mismo valor que la lente. Si, por el contrario, la lectura del autorefractómetro indica “pasar” (no defecto), sugiere que el niño presenta una hipermetropía elevada (>3 D) que se compensa con las lentes y, por tanto, debería remitirse al oftalmólogo para valoración(2,8).
Limitaciones de los autorefractómetros
Según las tablas empleadas (puntos de corte de derivación), el número de falsos positivos puede ser elevado, especialmente en el caso hipermetropías sin anisometropía que, aunque existentes, pueden no requerir ninguna corrección en niños pequeños. La principal finalidad de estos instrumentos es la detección de la anisometropía como factor de riesgo para ambliopía. En caso de detección de hipermetropía bilateral aislada, astigmatismo o miopía en niños mayores de 4 años, es prudente determinar a continuación la agudeza visual con la E de Snellen u otro optotipo equivalente, con el fin de mejorar la especificidad de la detección y decidir la derivación al oftalmólogo. De hecho, es muy recomendable que a todos los niños y niñas se les siga realizando la medición de agudeza visual entre los 4 y 6 años, independientemente del resultado obtenido por el autorefractómetro. Es, por lo tanto, importante saber que la derivación puede ser inadecuada si no se interpretan correctamente todos los datos o los umbrales de derivación programados no son los correctos(2,8,10).
Ambos instrumentos comentados (PlusoptiX® y Spot Vision Screener®) permiten, mediante procedimientos diferentes, establecer los límites a partir de los cuales se considera conveniente una derivación oftalmológica.
Evaluación a partir de los 6 años
A partir de los 6 años de edad, el objetivo del screening visual ya no es detectar las ambliopías, que deberían haber sido diagnosticadas con anterioridad, sino aquellos defectos de refracción que puedan disminuir la capacidad visual del escolar e interferir en su aprendizaje, conducta o habilidades. A estas edades, muchos de estos defectos producirán síntomas o el paciente manifestará una dificultad visual, aunque algunos pueden seguir pasando desapercibidos. Por ello es relevante comprobar la capacidad visual, al menos, cada 2 años(1,2,4).
La técnica de elección para la evaluación de la capacidad visual en niños en la etapa escolar es la evaluación de la AV con optotipos, aunque si se dispone de un autorefractómetro binocular, la realización de ambas pruebas permite una evaluación de los posibles defectos visuales con máxima precisión para decidir, con alta sensibilidad y especificidad, la necesidad o no de derivación al oftalmólogo(2).
Conclusiones
La detección precoz de los defectos de refracción, habitualmente asintomáticos, es esencial para el pronóstico visual del paciente, para el desarrollo de sus habilidades o capacidades, y para una óptima calidad de vida.
La ambliopía es el defecto prevenible de pérdida permanente de la visión más importante en la edad pediátrica, y la causa más frecuente de la misma son los defectos de refracción asimétricos (anisometropías).
Entre los 1 y 3 años es la “edad crítica”, en la que se generan la mayoría de las ambliopías anisometrópicas y en las que su detección precoz e instauración de tratamiento adecuado, permite alcanzar los mejores resultados visuales para el paciente.
Los autorefractómetros son instrumentos portátiles que permiten a los profesionales de Atención Primaria explorar la visión a unas edades (menores de 4 años) en las que sin ellos resulta muy difícil, sino imposible en la consulta no especializada, detectar defectos de refracción y alineación visual, y muy especialmente anisometropías con alto riesgo de generar ambliopía y, por tanto, convierten a esta técnica instrumental como la de elección para el cribado de los defectos de refracción en niñas y niños de 1 a 4 años de edad en Atención Primaria. Además, permiten cribar a todos los niños con defectos del desarrollo y la comunicación, que actualmente no reciben, en ocasiones, una correcta atención al ser incluidos en el grupo de pacientes que “no colaboran”.
Conflicto de intereses
No hay conflicto de interés en la elaboración del manuscrito. Declaración de intereses: ninguno.
Bibliografía
1. American Academy of Pediatrics Committee on Practice and Ambulatory Medicine and Section of Ophthalmology; American Association of Certified Orthoptists; American Association for Pediatric Ophthalmology and Strabismus; American Academy of Ophthalmology. Eye examination in infants, children and young adults by pediatricians. Pediatrics. 2003; 111: 902-7.
2. Marès J, van Esso D. Detección precoz de los trastornos de refracción. Pediatr Integral. 2018; XXII: 24-31.
3. Holmes JM, Lazar EL, Melia BM, Astle WF, DagiL R, Donahue SP, et al. Effect of age on response to amblyopia treatment in children. Arch Ophthalmol. 2011; 129: 1451-7.
4. US Preventive Services Task Force. Vision screening for children 1 to 5 years of age: US Preventive Services Task Force recommendation statement. Pediatrics. 2011; 127: 340-6.
5. Manny RE, Martínez AT, Fern KD. Testing stereopsis in the pre-school child: is it clinically useful?J Ped Ophthalmol Strab. 1991; 28: 223-31.
6. Fricke TR, Siderov J. Stereopsis, stereotests, and their relation to vision screening and clinical practice. Clin Exp Optom. 1997; 80: 165-72.
7. Miller JM, Lessin HR, American Academy of Pediatrics Section on Ophthalmology Committee on Practice and Ambulatory Medicine, American Academy of Ophthalmology, American Association for Pediatric Ophthalmology and Strabismus, American Association of Certified Orthoptists. Instrument-based pediatric vision screening policy statement. Pediatrics. 2012; 130: 983-6.
8. Donahue SP, Arthur B, Neely DE, Arnold RW, Sibert D, Ruben JB. POS Vision Screening Committee. Guidelines for automated preschool vision screening: a 10 year, evidence-based update. Journal of AAPOS. 2013: 17: 4-8.
9. Fogel-Levin M, Doron R, Wygnanski-Jaffe T, Ancri O, Zion IB. A comparison of plusoptiX A12 measurements with cycloplegic refraction. Journal of AAPOS. 2016; 20: 310-4. Disponible en: https:doi.org/10.1016/j.jaapos.2016.04.006.
10. Vila-de Muga M, Van Esso D, Alarcon S, Wolley Dod C, Llop D, Callés A, et al. Instrument-based screening for amblyopia risk factors in a primary care setting in children aged 18 to 30 months. Eur J Pediatr. 2021; 189: 1521-7. Disponible en: https://doi.org/10.1007/s00431-020-03904-0.












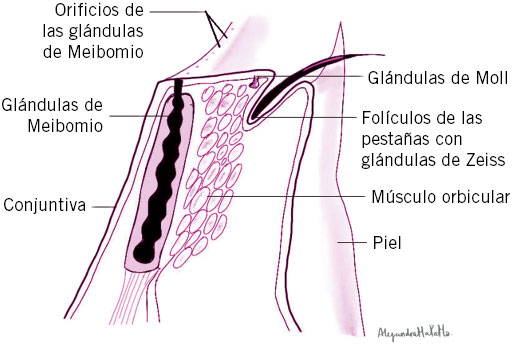










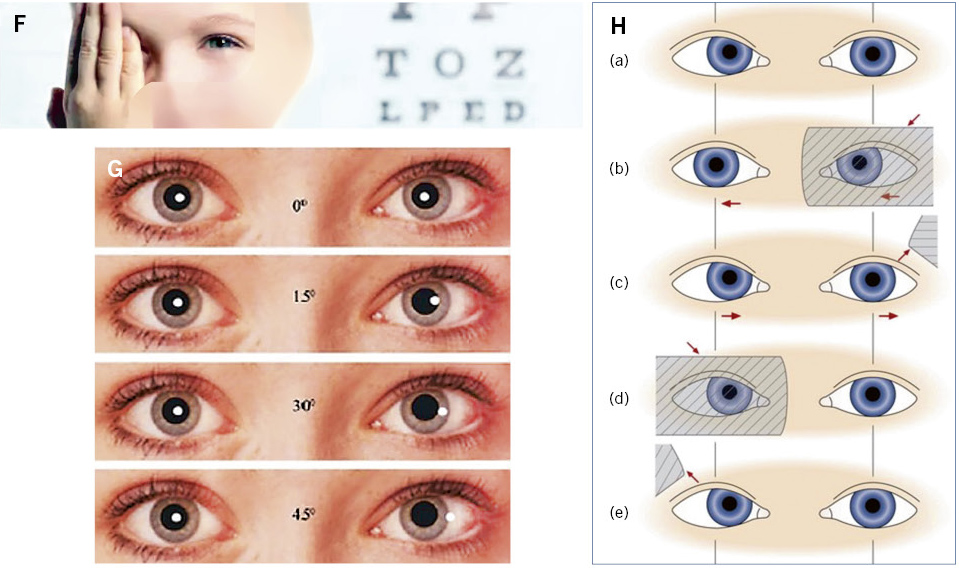
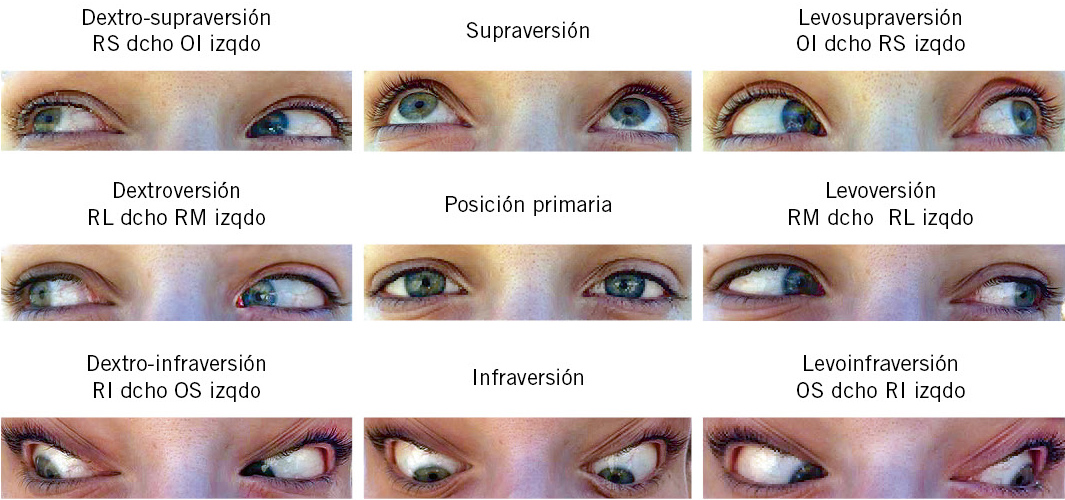
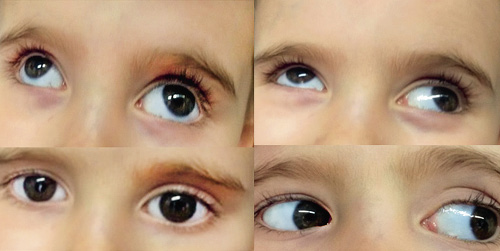
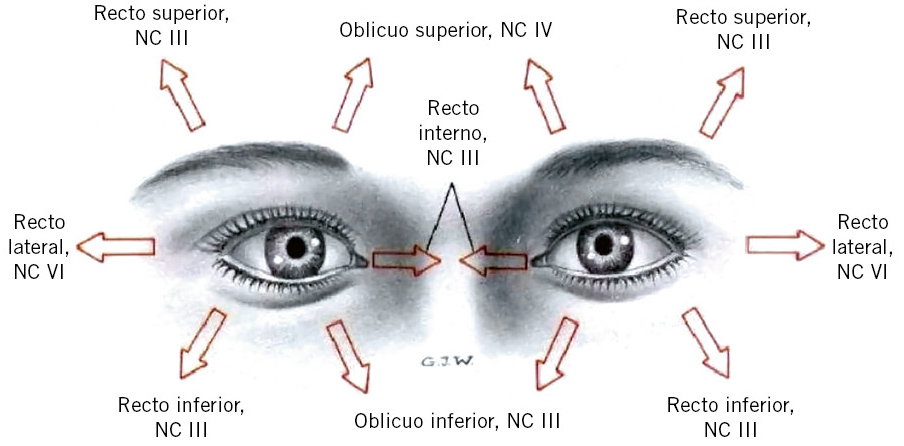

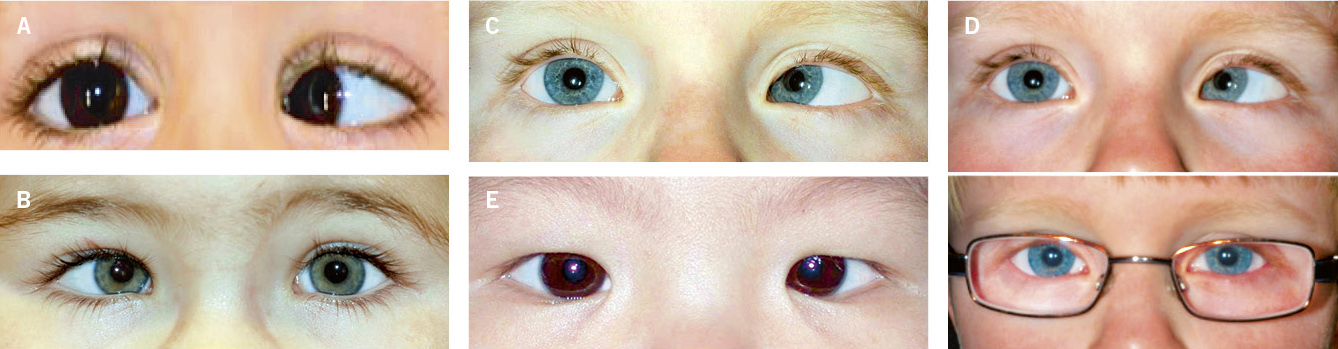
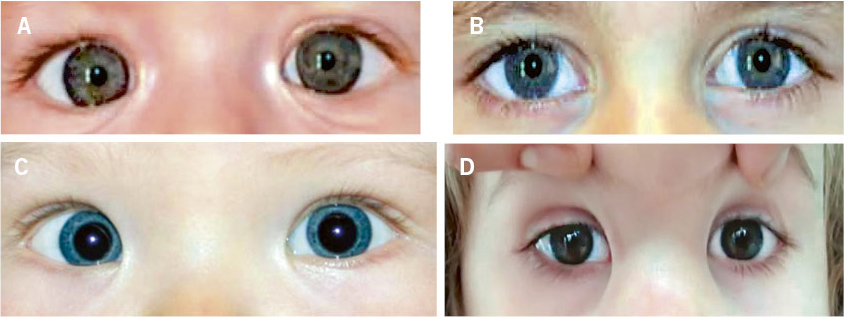
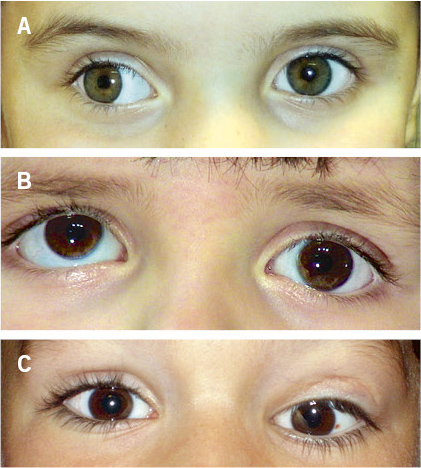
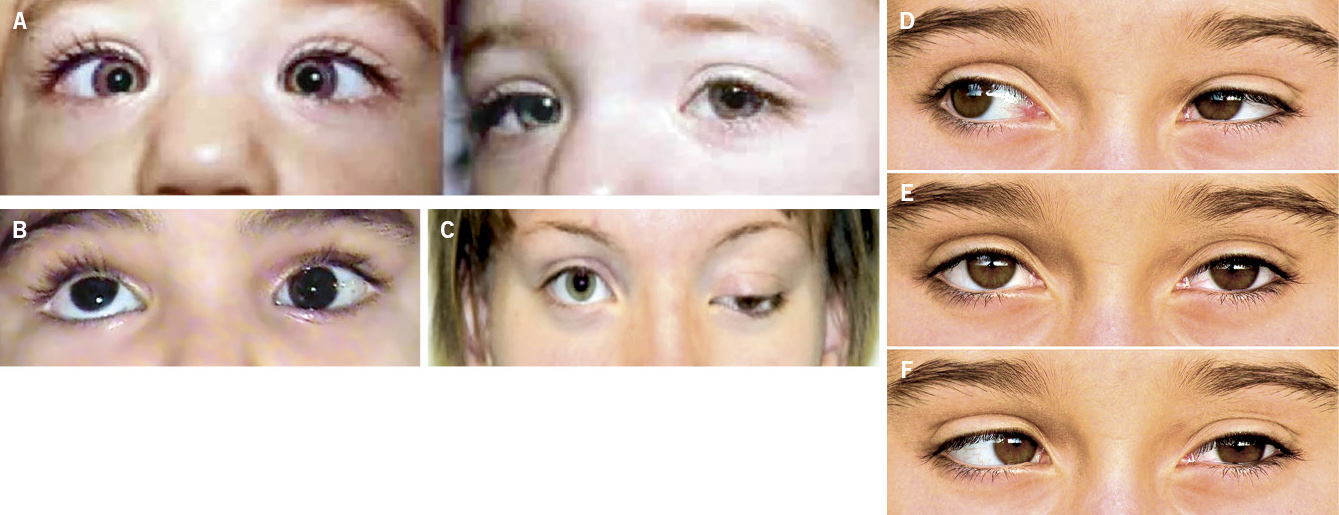
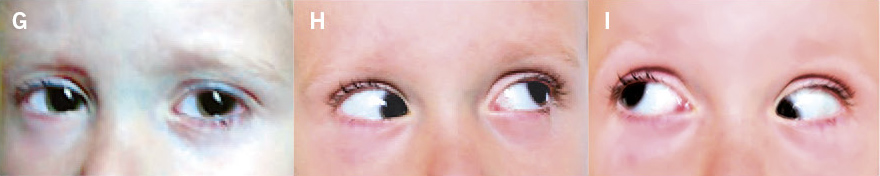
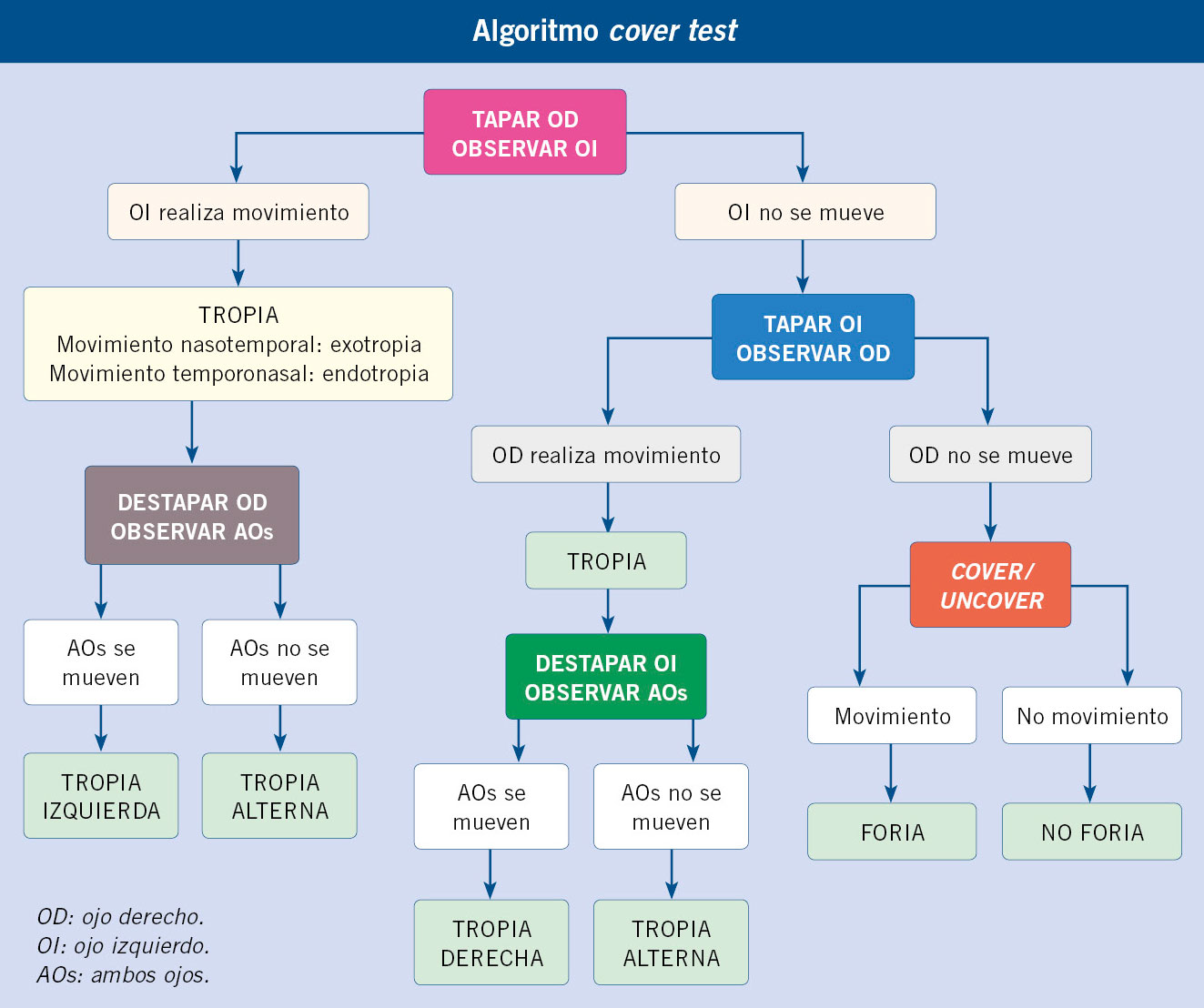



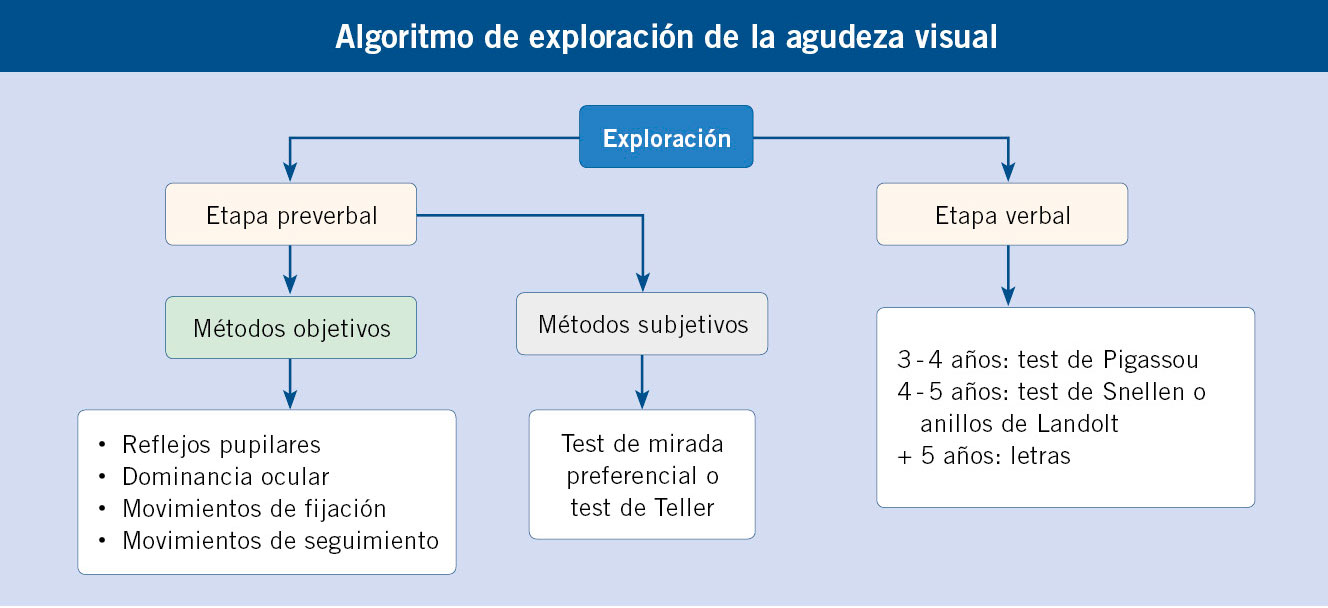

























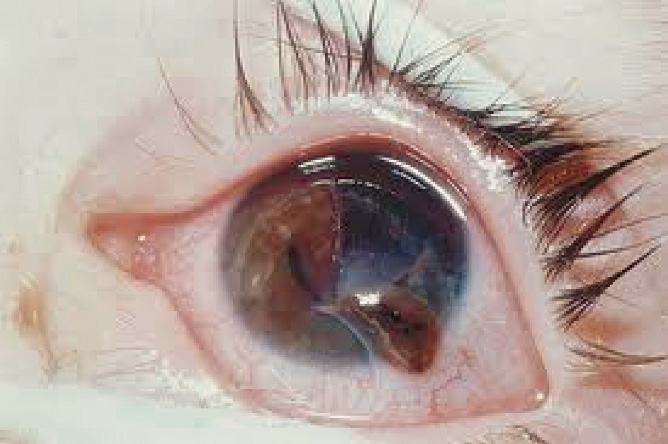
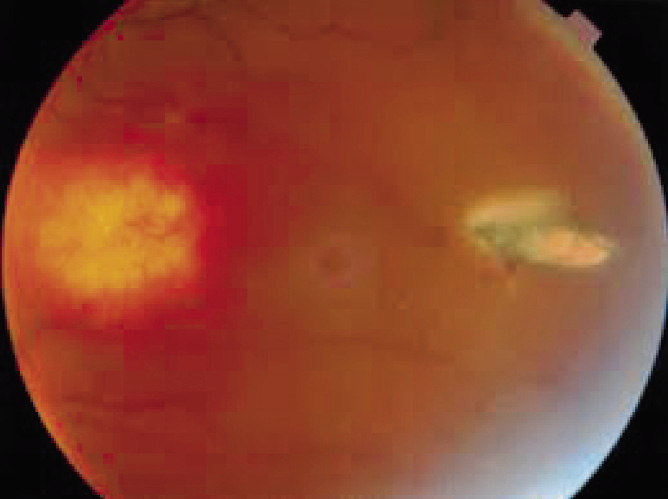



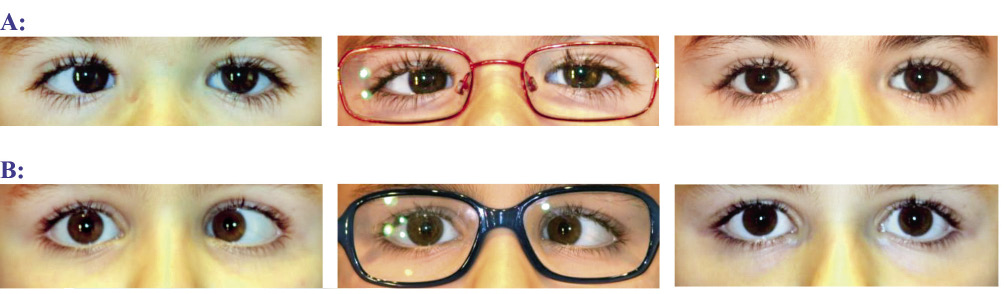
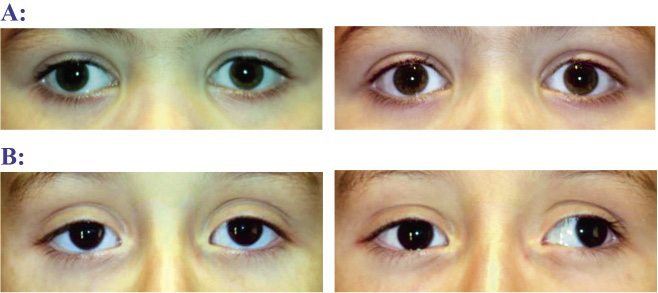
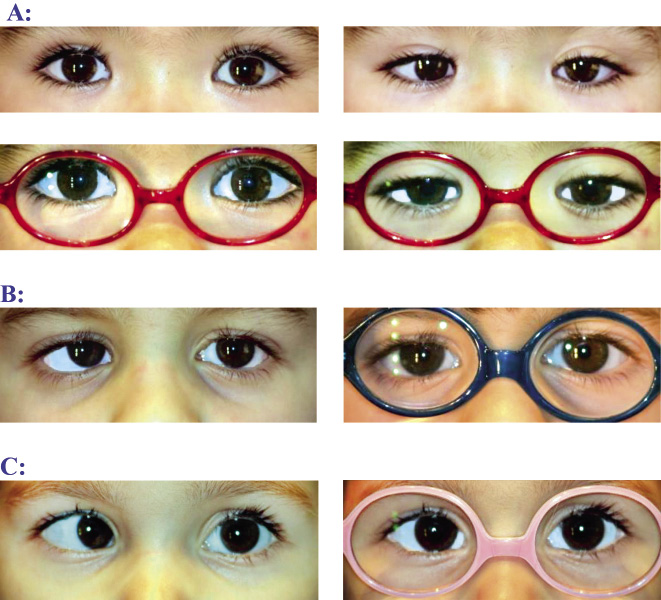

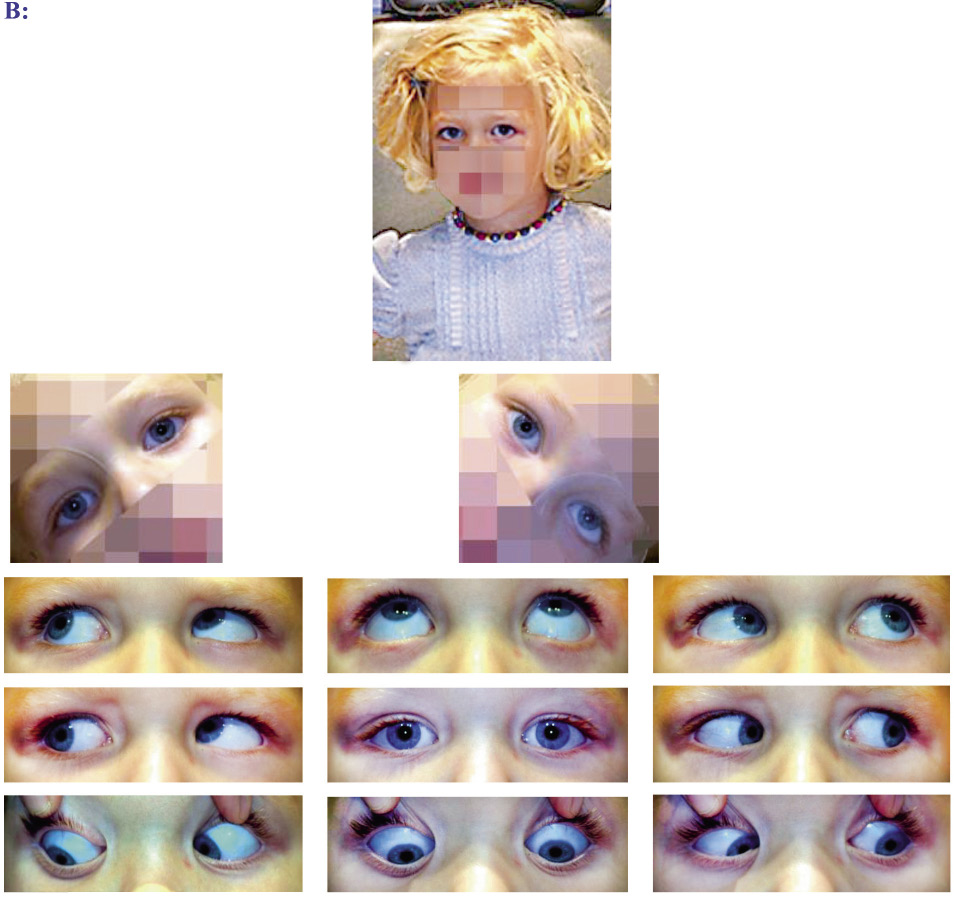
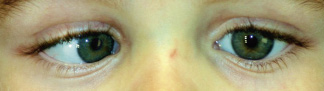






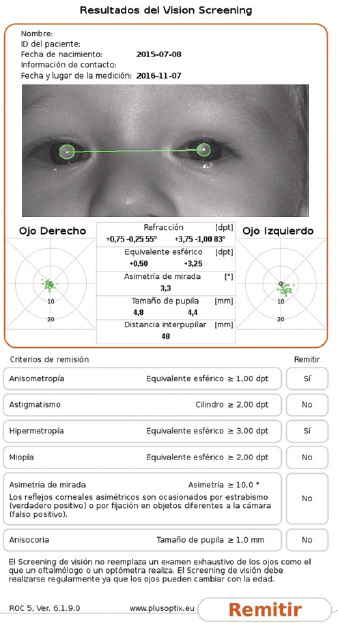







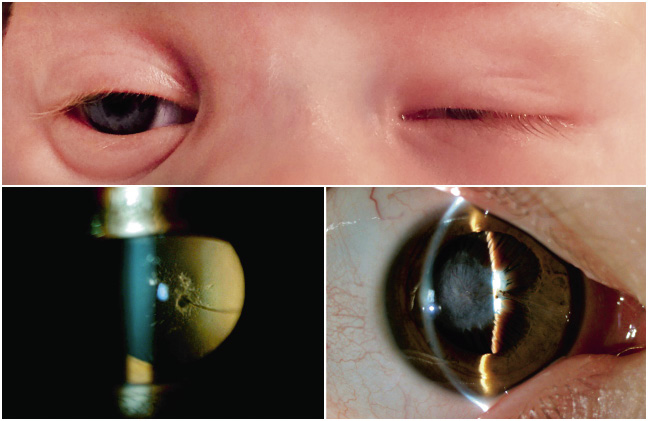

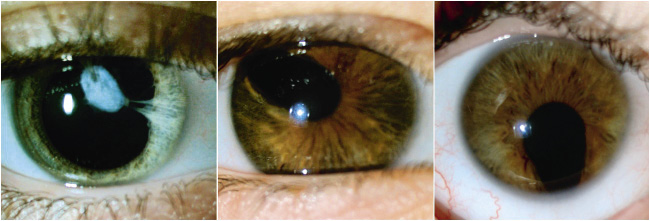






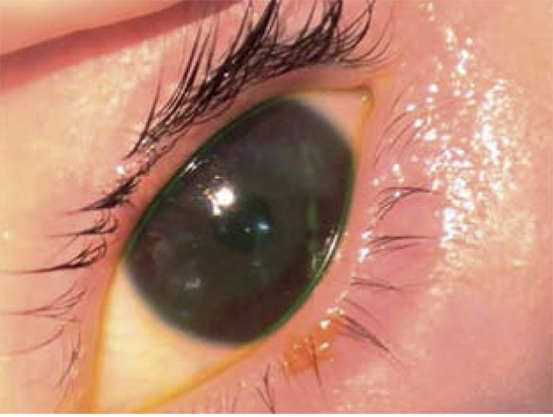
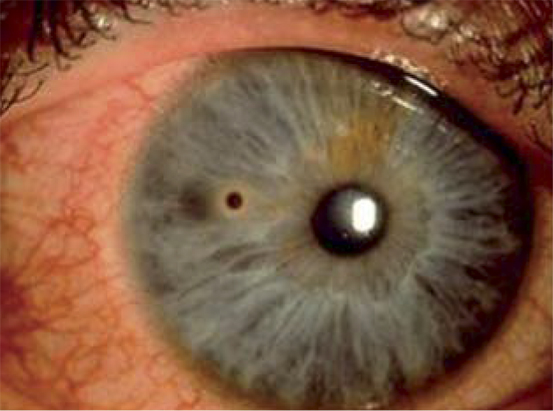

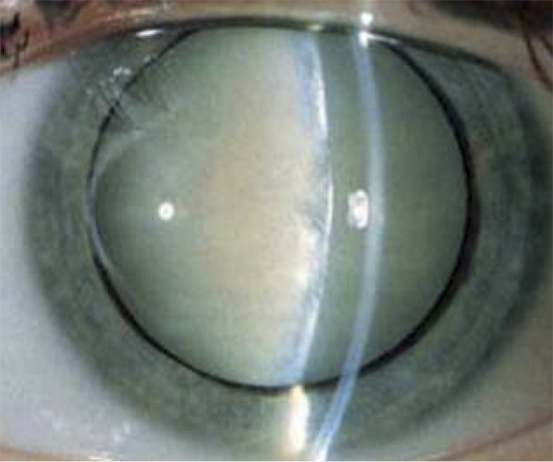
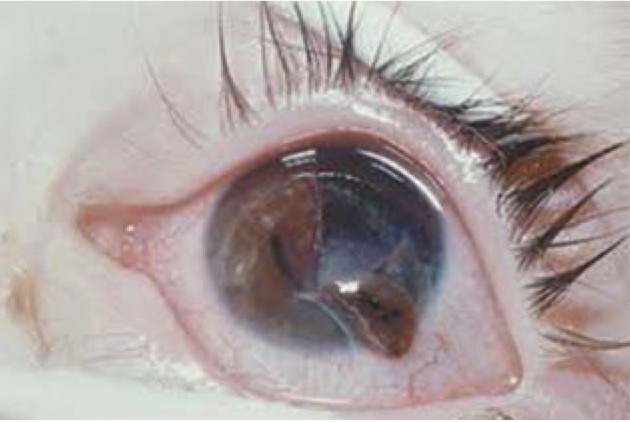

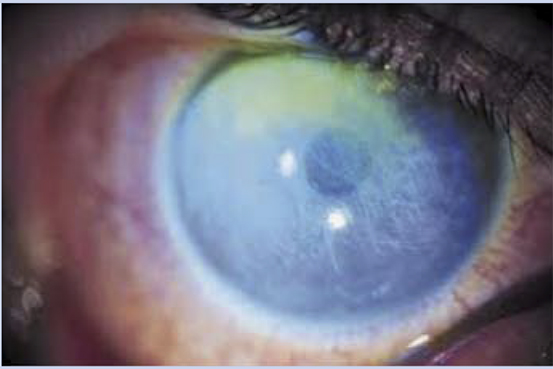



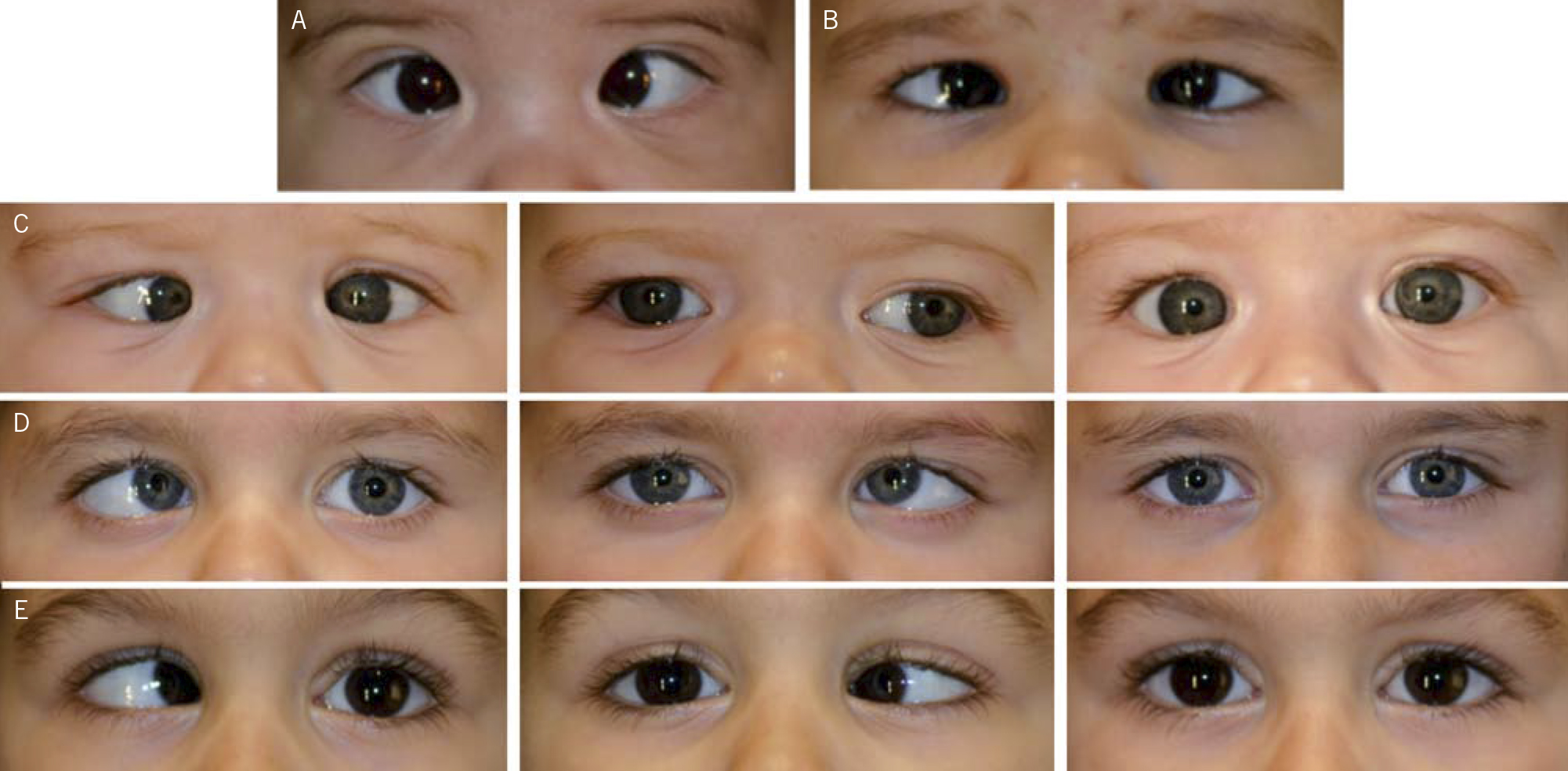 Figura 2.
Figura 2.  Figura 3.
Figura 3. 
 Figura 4.
Figura 4. 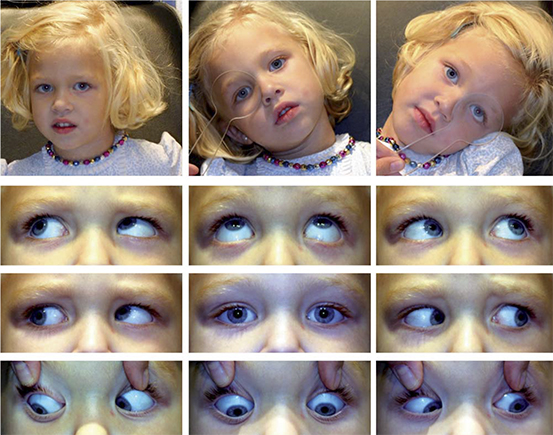 Figura 5.
Figura 5. 
 Figura 6.
Figura 6.  Figura 7. Arriba: primera visita. Abajo: a los 3 meses y con su corrección. En las imágenes de la izquierda la niña está fijando de lejos y en las de la derecha, de cerca.
Figura 7. Arriba: primera visita. Abajo: a los 3 meses y con su corrección. En las imágenes de la izquierda la niña está fijando de lejos y en las de la derecha, de cerca.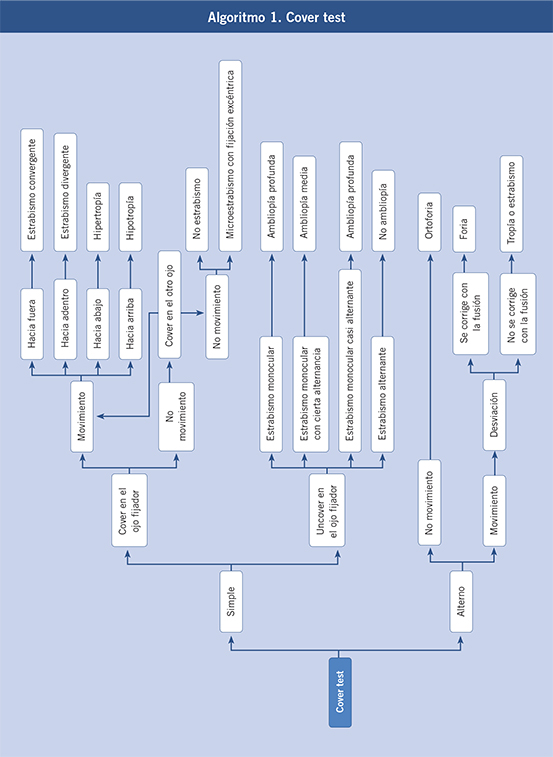



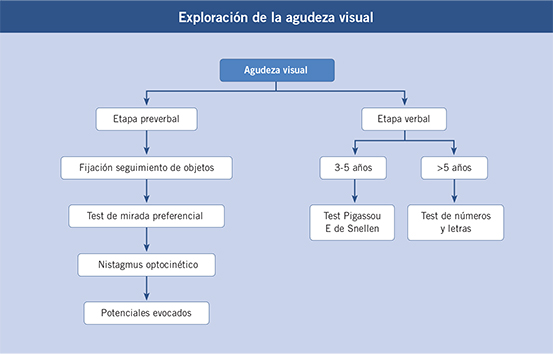

 Figura 1.
Figura 1. 
 Figura 2.
Figura 2.  Figura 3.
Figura 3.  Figura 4.
Figura 4.  Figura 5.
Figura 5.