Dolor abdominal crónico y recurrente. Infección por Helicobacter pylori
Conceptualización
DAR: más de 3 episodios de dolor suficientemente grave durante al menos 3 meses en el año previo al estudio; DAC: si dura al menos 2 meses.
En 1958, J. Apley y N. Naish, en un estudio de 1.000 escolares, denominan como DAR el que presentan niños con, al menos, 3 episodios de dolor suficientemente grave, que interfiera su actividad habitual, en un periodo no menor de 3 meses, con crisis continuas en el año precedente al estudio(1).En al año 2005, la Academia Americana de Pediatría (AAP) define DAC como aquel que supere los 2 meses de duración y recomiendan poner en marcha estudios para descartar organicidad o trastorno somatomorfo(2).
Epidemiología
Afecta al 10-19% de los niños que consultan.
El dolor abdominal de larga duración afecta al 10-19% de los niños que consultan en Pediatría. La prevalencia es del 11,8% y 17% en niños entre 4-6 años y adolescentes, respectivamente. En un 21%, el dolor es suficientemente intenso como para interferir su actividad habitual(3).
Clasificación
Se basa en la posible etiología orgánica, somática o funcional, según la edad y los criterios de Roma III (Tabla I).

En la práctica clínica, los niños con DAC pueden agruparse en mayores o menores de 4 años. Esta edad puede extenderse hasta los 7 años debido a la variabilidad en el desarrollo individual para expresar o no los síntomas. Sin embargo, los nuevos criterios de Roma III los separa definitivamente en menores y mayores de 4 años(4).
En los menores de 4 años, el DAC se establece como un “diagnóstico” y siempre se debe descartar organicidad o somatización; no puede establecerse el diagnóstico de “dolor abdominal funcional” al basarse este en un conjunto de síntomas que a esta edad no puede ser expresado por el niño.
En los mayores de 4 años, el DAC no es un diagnóstico sino un “síntoma” referible por el niño y el diagnóstico de funcional se acepta siguiendo los criterios de Roma III, que hacen referencia a un conjunto de síntomas que a esta edad sí pueden ser referidos por el niño. Debe descartarse organicidad y somatización. El dolor abdominal funcional es la causa más frecuente del DAC, es un diagnóstico específico, y aunque se ha usado de forma intercambiable como: “dolor no orgánico”, “dolor psicógeno” y “dolor abdominal recurrente”, la AAP y la NASPGHAN (North American Society Pediatric Gastroenterology, Hepatology and Nutrition) proponen en 2005 abandonar el DAR como sinónimo de dolor abdominal funcional y dolor abdominal psicógeno(2).
El DAC funcional, a su vez, lo podemos clasificar en una serie de subcategorías según criterios de Roma III para niños entre 4 y 18 años de edad que se recogen en la tabla II.

Fisiología
Se puede explicar por una hiperreactividad, hiperalgesia intestinal y convergencia víscero-somática a nivel cerebral del dolor intestinal.
En la generación y perpetuación del DAC, van a influir diversos factores etiopatogénicos:
• Existencia de una reactividad intestinal anormal frente a diferentes estímulos fisiológicos (alimentos, cambios hormonales, distensión intestinal), nociceptivos (procesos inflamatorios) o psicológicos estresantes (separación de los padres, ansiedad, etc.).
• Una disminución del umbral álgico en respuesta a cambios de presión abdominal.
• Hiperalgesia visceral relacionada con la intensidad de los síntomas. Se reconocen dos tipos.
- La hiperalgesia visceral primaria, ocasionada por los estímulos dolorosos precoces y múltiples que origina una sensibilización de las neuronas de los ganglios de la cadena dorsal, produciendo dolor ante estímulos habitualmente por debajo del umbral de dolor, hiperalgesia propiamente dicha o incluso por estímulos que normalmente no producen dolor, alodinia.
- La hiperalgesia secundaria, producida por incremento de la percepción consciente de dolor, que estaría ocasionada por cambios bioquímicos en la vía sensitiva aferente, que envía los estímulos dolorosos de la médula espinal a la corteza cerebral.
Los procesos inflamatorios de la mucosa causados por infecciones, alergias o enfermedades inflamatorias primarias pueden provocar una sensibilización de los nervios aferentes, iniciándose la hiperalgesia visceral. De hecho, algunos pacientes inician el cuadro de dolor a partir de una gastroenteritis aguda, frecuentemente producida por campylobacter o salmonella(2).
• La convergencia víscero-somática explica cómo las vías sensitivas de la piel, músculos abdominales y nervios aferentes viscerales, cuyos receptores se encuentran en la superficie serosa, en el mesenterio y dentro de la pared de las vísceras huecas, establecen sinapsis en las mismas inter-neuronas, produciendo dispersión del dolor visceral y dificultando la diferenciación entre dolor visceral y musculoesquelético que explica, además, el dolor referido o irradiado que se percibe en los dermatomas cutáneos que comparten el mismo nivel de la médula espinal que las entradas viscerales. Por ejemplo, los estímulos nociceptivos de la vesícula biliar entran en la médula espinal por las metámeras entre T5 a T10; por lo tanto, el dolor de una vesícula biliar inflamada puede ser percibido en la escápula. La localización del dolor en el cuadrante superior derecho en los pacientes con colecistitis aguda, generalmente, ocurre una vez que el peritoneo parietal que la recubre se inflama.
La expresión del dolor a nivel central está a su vez modulada por la interacción de una serie de factores: biológicos, medioambientales y psicológicos, que interactúan entre sí para modificar la respuesta al dolor. Todo ello se visualiza mediante un modelo biopsicosocial del padecimiento del DAC, desarrollado por J. S. Hyams y P. E. Hyman(6), cuando es aceptado por los padres y el paciente facilita su control y extinción (Fig. 1).

Figura 1. Modelo biopsicosocial del dolor abdominal(6,11).
Sistemática diagnóstica
Se establece básicamente con una historia clínica y exploración física exhaustivas, buscando los factores desencadenantes y los signos de alarma, relegando los exámenes complementarios a un segundo plano y solo si se sospecha organicidad.
Una historia clínica exhaustiva y una exploración física completa son las mejores herramientas para valorar a cualquier paciente con DAC. Algún examen complementario puede ser necesario, pero queda relegado a un segundo plano.
Conviene establecer la mejor relación de confianza posible con el niño y sus padres, compartiendo su preocupación y entendiendo el dolor como real, no imaginario. El objetivo ha de ser el de discernir si el origen del DAC es de causa orgánica, psicológica (somatización) o funcional, teniendo en cuenta que estas tres causas no son excluyentes entre sí y pueden coexistir e interactuar entre ellas. Es muy importante que, tanto el paciente como su familia, estén seguros de que el pediatra buscará cualquier causa identificable del DAC, permitiendo así establecer una alianza diagnóstico-terapéutica temprana.
La historia clínica ha de ser completa, considerando en primer lugar, posibles causas orgánicas del DAC, más relevantes en los niños menores de 7 años y, principalmente, en los de menos de 3-4 años. Pueden variar entre el 5-40%, dependiendo de: población estudiada, edad de inicio, definición de organicidad, exámenes complementarios realizados e interpretación de los mismos (Tabla III).

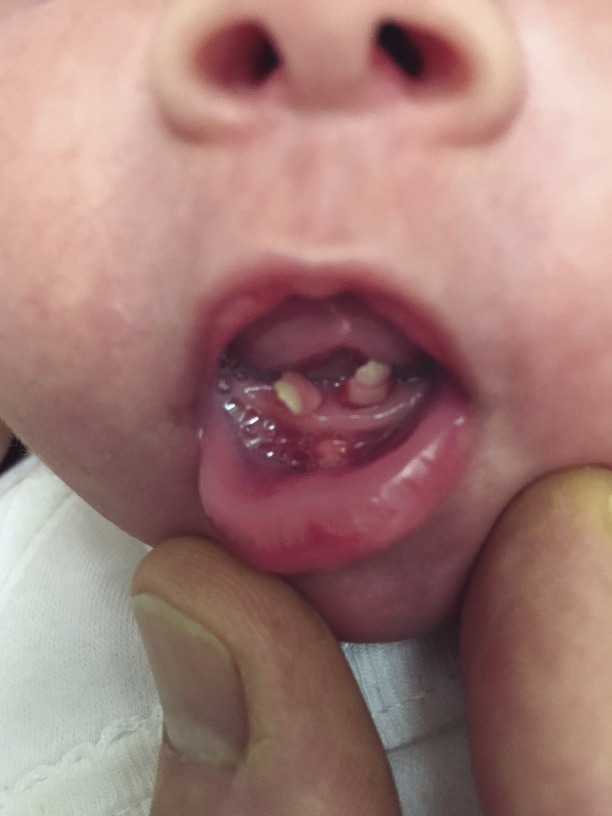
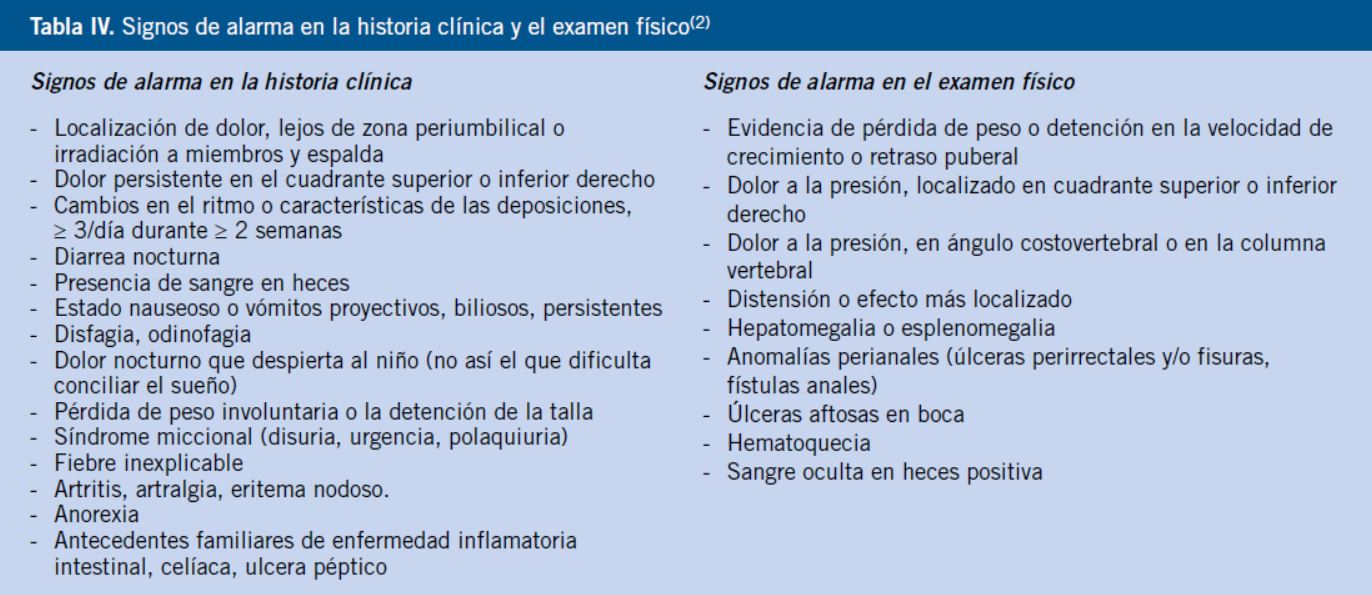
Se debe indagar sobre los signos de alarma, tanto al hacer la historia clínica como al realizar la exploración física (Tabla IV). Son la base para la indicación de los exámenes complementarios diagnósticos más o menos específicos, dirigidos y escalonados (Tabla V).

Varios estudios han demostrado que en ausencia de signos de alarma, hay poca evidencia de que las pruebas de laboratorio o imagen sean útiles para identificar una enfermedad orgánica(2) y tampoco el resultado de dichas pruebas parece influir en el pronóstico del DAC(8).
En la historia clínica, hay que preguntar sobre:
• Antecedentes familiares: dispepsia, úlceras duodenales, enfermedades digestivas (enfermedad inflamatoria intestinal, enfermedad celíaca), alergias o intolerancias alimentarias, cólicos nefríticos, litiasis en vesícula, malformaciones.
• Características del dolor: quemante, tipo cólico, como calambres, etc.
• Localización: peri-umbilical: propio del dolor funcional en niños mayores de 8 años, no así en menores de esta edad; epigástrico: dispepsia funcional, origen esófago, estómago, duodeno, páncreas; cuadrante superior derecho: vesícula biliar, hígado, cabeza de páncreas; cuadrante inferior derecho: apéndice, íleon terminal y ciego; cuadrante inferior izquierdo: recto-sigma, divertículo de Meckel, proctitis ulcerativa, síndrome intestino irritable funcional.
• Si es fijo o se irradia hacia la espalda, pensar en pancreatitis, hacia la ingle, descartar cólico renal.
• Severidad del mismo: se puede objetivar mediante una escala facial del dolor de Wong-Baker, útil para niños mayores de 3-5 años y hasta 13 años, siendo 0 no dolor, entre 1-3 dolor leve, 4-6 dolor moderado, 7-9 dolor intenso y 10 dolor insoportable (Fig. 2). Comprobar si altera la actividad familiar y del paciente, y cuál es la respuesta familiar para identificar actitudes que refuerzan dicho dolor.

Figura 2. Escala de Wong-Baker para niños de 3 hasta 13 años.
• Momento del día en que se inicia: nocturno y/o en la mañana temprano: migraña abdominal; de predominio nocturno: reflujo GE; su coincidencia o no con las comidas, en la enfermedad péptica sucede después de estas.
• Duración y frecuencia.
• Sintomatología asociada: rash, síntomas vagales, distención abdominal, afonía, tos crónica, diarrea, cefaleas, etc.
• Factores desencadenantes. Triggers: alimentos como: lácteos, intolerancia a lactosa o alergia PLV, cítricos, grasas, bebidas con cafeína, gaseosas, sorbitol que se encuentra en dulces, goma de mascar sin azúcar y otros. FODMAPs (oligosacáridos fermentables, disacáridos, monosacáridos y polioles), que son hidratos de carbono de cadena corta pobremente absorbidos que pueden conducir a la producción de gas y distensión del intestino grueso y dolor abdominal; otros alimentos que producen gases, como: frijoles, cebolla, apio, pera, plátano, albaricoque, ciruela, coles de Bruselas, germen de trigo, etc. Otros desencadenantes frecuentes son determinadas actividades que pueden estresar al paciente: escolares, extraescolares o familiares.
• Medidas adoptadas para alivio del dolor: medicación, evitar determinados alimentos, etc.
Cuando todo lo anterior es difícil de especificar, es conveniente realizar un calendario, de al menos una semana de duración, donde se registre todo lo mencionado.
Además, se ha de indagar sobre hábitos dietéticos del niño, ingesta de fibra (estreñimiento funcional), dietas de exclusión o caprichosas. Hábito intestinal: cantidad, frecuencia y consistencia de las heces, para lo cual puede servir la escala de Bristol (a los familiares se les suele pasar desapercibido el estreñimiento funcional). Si es una mujer, características de la menarquia y de la menstruación. Historia personal de cirugías previas (adherencias, malformaciones intestinales) y familiar de antecedentes de enfermedad gastrointestinal (síndrome de intestino irritable, migraña, enfermedad celíaca, péptica o inflamatoria).
Se debe confeccionar una historia psicosocial amplia, valorando la actitud del niño, de sus padres y la relación entre ambos, los antecedentes de trastornos psiquiátricos familiares, la presencia de eventos estresantes o disruptivos en la vida familiar, social o escolar, síntomas emocionales y conductuales, y funcionamiento familiar. En el caso de adolescentes, para realizar una evaluación psicosocial sistemática se le entrevistará directamente, sin presencia de sus padres, siendo de utilidad el acrónimo HEADSS: Home (hogar y familia), Education and employment (aspectos escolares, rendimiento escolar, notas, etc.); Activities (ejercicio, deportes y otras actividades extraescolares); Drugs (uso y relación con las drogas, alcohol, tabaco y otros); Sexuality (orientación sexual, experiencias, relaciones consentidas vs obligadas); y Suicide/depression (detección de síntomas depresivos, ideas suicidas)(9). Por otra parte, hay que identificar una serie de factores psicosociales predisponentes, tanto individuales como familiares, precipitantes y mantenedores del DAC por somatización, que se resumen en la tabla VI.

En la exploración física, ha de valorarse el aspecto general, peso, talla, estado de nutrición, velocidad de crecimiento, TA. Ha de incluirse una detallada exploración abdominal, palpación buscando masas, visceromegalias, puntos dolorosos, en particular, el signo de Carnett, que sirve para diferenciar el dolor parietal, (hasta el 20% de los DAC), del visceral. Se realiza con el paciente en decúbito supino, ejerciendo presión con el dedo sobre el punto doloroso y haciendo que el paciente contraiga la musculatura abdominal, realizando una flexión de la cabeza y el tronco. Dicho signo es positivo, dolor parietal, si el dolor aumenta o persiste con dicha maniobra, y negativo, dolor visceral, si se alivia o atenúa (sensibilidad del 78-85%, especificidad del 88-97%). Valoración, en su caso, del signo del psoas mediante maniobra de hiperextensión de la cadera (absceso del psoas). Evaluación de la madurez sexual, inmadurez concomitante con organicidad; exploración de la zona perianal (fístulas, fisuras, ano anterior); tacto rectal ineludible en todo niño con DAC y estreñimiento; y presencia de hoyuelo sacro-coccígeo con vellos. En las niñas, descartar hematocolpos, masas ováricas, etc.
La historia clínica extensa y una adecuada exploración física sirven para hacer una primera evaluación del cuadro clínico y orientan sobre la necesidad de qué exámenes complementarios iniciales solicitar. En ocasiones, puede estar indicada la colaboración del paido-psiquiatra, o incluso iniciar tratamiento de forma empírica. Ha de explicarse a los padres, de forma sencilla, la impresión diagnóstica, tanto si se sospecha un problema orgánico, psicosomático o funcional, así como lo que se espera de los exámenes complementarios y el posible pronóstico del DAC funcional, recordando que el 29% de los niños con DAC mantiene el dolor tras varios años de seguimiento(8). Es aquí donde la confianza en el pediatra ha de preservarse para un adecuado seguimiento y tratamiento de dicha patología.
Los exámenes complementarios, como se ha comentado, han de realizarse en función de la presencia de signos de alarma, solicitándose de forma escalonada y dirigidos según el diagnóstico de sospecha dado(10) (Tabla V).
En un primer nivel asistencial, se han de solicitar pruebas de laboratorio básicas, descartando la presencia de sangre oculta en heces, su positividad es un dato siempre a tener en cuenta, aunque es muy inespecífica, al igual que la PCR. En este nivel asistencial, la mayoría de los autores consideran que no parece estar justificado la realización de exploraciones para despistaje de enfermedad celíaca (EC) o helicobacter pylori, dado que se ha comprobado que solo 1/227 niños con DAC mayor de 5 años tiene EC(11); por otra parte, se ha encontrado igual prevalencia (30-40%) de helicobacter en pacientes con o sin DAC, además de lo inespecífico del dolor abdominal asociado a helicobacter. Por ello, no es recomendable este tipo de estudios en Atención Primaria(2,12).
Teniendo en cuenta que la prevalencia de hipercalciuria idiopática en España es del 6,5 y 7,8%, y en zonas con gran tasa de endogamia como La Gomera, entre 10,6 y 28,4%, creemos que está justificado determinar calcio, creatinina y citrato en primera orina de la mañana, ya que es una prueba no invasiva y barata, y en algunas series hasta el 14% de los niños con hipercalciuria presentan dolores abdominales (M. Luis Yanes et. al, Canarias Pediátrica, 2005, 29: 47-56).
Los estudios basales de imagen que pueden solicitarse, la ecografía pélvica y abdominal, no parecen tener rendimiento óptimo sin la presencia de alguno de los signos de alarma(2). En manos expertas y con los nuevos aparatos de ecografía, puede detectarse patología muy variada, del tracto urogenital, genitales femeninos, hepato-bilio-esplénica, malrotación intestinal, enfermedad inflamatoria intestinal, alteraciones vasculares mesentéricas (síndrome compresivo de arteria mesentérica superior), etc. No está justificado el uso de radiografía simple de abdomen de forma rutinaria, salvo para comprobación de fecaloma en la retención fecal funcional, o la detección de heces abundantes tras deposición en niños con estreñimiento oculto(10).
Ninguno de los exámenes complementarios es necesario para hacer el diagnóstico de DAC funcional en ausencia de signos de alarma, aunque se acepta que estas pueden ayudar a tranquilizar al paciente, familia y al propio médico sobre la ausencia de enfermedad orgánica, sobre todo, si el dolor empeora significativamente la calidad de vida del paciente(2,10). La realización de dichas pruebas, con el fin de tranquilizar o facilitar la aceptación de un diagnóstico de DAC funcional, debe ser equilibrada y proporcional, ya que la solicitud de excesivos exámenes complementarios adicionales podrían tener el efecto opuesto, reforzando los temores de los padres y del niño de padecer una enfermedad orgánica grave, afectando negativamente la confianza en el pediatra(13).
En un segundo nivel asistencial o incluso en AP según las posibilidades disponibles del petitorio, la pericia del pediatra y la sospecha clínica, puede solicitarse:
• Serología de enfermedad celíaca (IgA antitransglutaminasa tisular, IgG antigliadina) y remisión para endoscopia confirmativa en su caso.
• Detección de Ag en heces de helicobacter pylori y test C13 urea en aliento, remitiendo para confirmación de enfermedad péptica mediante endoscopia y tratamiento erradicador oportuno.
• Rast (determina IgE específica) o prick test a proteína de leche de vaca y a otros alimentos, en su caso, dejando los test de provocación y estudios más extensos de IgE específica para los servicios de alergología.
• Test de hidrógeno espirado con leche o solución de lactosa, para detección de intolerancia o malabsorción de lactosa, o con lactulosa, para diagnóstico de sobrecrecimiento bacteriano o intestino contaminado, y remisión para confirmación y tratamiento oportuno en su caso(14).
• Determinación de electrólitos en sudor y hormonas tiroideas en caso de DAC acompañado de estreñimiento.
• Test de embarazo en adolescentes con DAC y amenorrea secundaria.
• Determinación de calprotectina en heces, que ha mostrado ser un test de utilidad diagnóstico sensible, aunque no específico, para diferenciar aquellos niños que presentan patología orgánica y, por lo tanto, precisan de estudio colonoscópico, de los que muestran patología funcional y no necesitan esta técnica invasiva(15).
Hay que ser cautos en la interpretación de los resultados de estos estudios y la positividad de los test no siempre va indicar que sea la causa del DAC.
En un segundo o tercer nivel asistencial, una vez que el niño es remitido al especialista correspondiente (gastroenterólogo, cirujano pediátrico, ginecólogo, nutricionista, etc.), según la sospecha clínica específica, pueden ser necesarios otros exámenes: Phmetría, tránsito intestinal superior, enema opaco, endoscopia de tracto digestivo superior, colonoscopia, biopsia intestinal, manometría ano-rectal, TAC, RMN, cápsula endoscópica, laparoscopia… El pediatra de AP ha de conocer las indicaciones de dichas pruebas, aunque no se aborden en este tema.
Tratamiento del DAC
Se basa en medidas de apoyo biopsicosocial, siendo de escaso valor las medidas dietéticas o farmacológicas.
El tratamiento ha de tener en cuenta que, como se ha mencionado, las etiologías orgánicas, psicosomáticas o funcionales no son excluyentes y pueden interactuar en un número no despreciable de pacientes y, por lo tanto, a considerar desde un punto de vista terapéutico.
El tratamiento del DAC orgánico ha de ser etiológico, de la enfermedad orgánica diagnosticada, que puede ser anatómica, inflamatoria, metabólica o neoplásica.
El tratamiento del DAC por somatización corresponde al paido-psiquiatra, que debe establecer el tratamiento en colaboración con el pediatra de AP u hospitalario, identificando los factores predisponentes y precipitantes que pueden desencadenar dicha patología en una persona vulnerable, así como los factores de riesgo que pueden cronificar el proceso (Tabla VI).

El tratamiento del DAC funcional se basa en lo recogido en el consenso de la AAP y NASPGHAN en 2005(2), que consideran que la mayoría de los niños con DAC funcional pueden recibir tratamiento en el ámbito de AP, con una explicación de un modelo biopsicosocial de la enfermedad funcional, enmarcando esta en términos de un diagnóstico positivo en lugar de un diagnóstico de exclusión, ganándose la confianza familiar y asegurando un seguimiento periódico de apoyo clínico-terapéutico a la familia y al niño. Ello implica:
• Resumir los síntomas del paciente y explicar con términos sencillos que, siendo el dolor real y frecuente, es poco probable que sufra enfermedad orgánica. No obstante, como profesional, se estará atento por si apareciese algún signo de alarma. Puede compararse con la cefalea, un trastorno funcional frecuente, que experimentan la mayoría de los adultos y que muy raras veces se asocia con enfermedad grave.
• Aportar ejemplos claros y apropiados para la edad de los procesos que se asocian con hiperalgesia, como cicatrices en fase de curación, y las interacciones del cerebro y el intestino, como las diarreas y vómitos que pueden experimentar los niños en situaciones estresantes (p. ej., antes de un examen o de una competición deportiva importante).
• Establecer una relación de confianza con el niño y sus padres es importante, dado que un 29% de estos pacientes van a tener dolor abdominal persistente en el tiempo y es aquí donde la confianza en el pediatra se pone en juego. Se ha comprobado que la cronicidad del dolor abdominal funcional depende más de las característica de los padres que del niño y de que estos hayan o no aceptado el modelo biopsicosocial de la enfermedad antes mencionado(8,13).
• Establecer unos objetivos de tratamiento razonables, dirigidos, sobre todo, a la recuperación de la función normal, procurando mejorar la tolerancia al dolor, haciendo que el niño siga una vida familiar y escolar menos condicionada y mejorando la ansiedad y la depresión que todo dolor crónico puede causar, independientemente de la etiología.
La mayoría de los niños mejoran con métodos sencillos de apoyo psicológico y de modificación de su conducta para el mejor manejo del dolor abdominal.
Las medidas psicosociales que pueden estar al alcance del pediatra de AP, básicamente son:
• Las técnicas de relajación muscular, con ejercicios de respiración profunda o relajación muscular progresiva de diferentes grupos musculares, actuando como “coach” un miembro de la familia suficientemente adiestrado por el pediatra, si es necesario.
• La distracción, para desviar la atención del dolor mediante conversación, juegos o la imaginación guiada, también llamada hipnoterapia o autohipnosis, que es una técnica de distracción a través de la cual el niño entra en un estado de imaginación de sonidos y sensaciones que lo desconecta de los estímulos dolorosos.
Otras medidas psicosociales que precisan de un profesional psicoterapeuta más experto son:
• La terapia cognitivo-conductual, que incluye un programa individual de reeducación, relajación, manejo del estrés y técnicas de modificación de la conducta.
• Biofeedback (biorretroalimentación), técnica que proporciona una representación visual o auditiva de las respuestas fisiológicas al dolor y a la ansiedad (frecuencia cardiaca, temperatura de la piel, etc.).
Estas técnicas han demostrado igual o superior eficacia que la terapia médica estándar, en reducir la frecuencia e intensidad de los episodios de dolor(16).
En algunos casos, pueden ser útiles otras medidas dietéticas, manejo de los triggers o factores desencadenantes (ciertas restricciones dietéticas) y farmacológicas, para el tratamiento de síntomas predominantes, según el tipo de DAC.
Modificaciones dietéticas: en una revisión sistemática de 2009, se llegó a la conclusión de que no existe evidencia de alta calidad que indique que las intervenciones dietéticas son eficaces en el tratamiento del dolor abdominal funcional en niños(17). Por otra parte, las restricciones dietéticas pueden dar lugar a deficiencias nutricionales (Ca, Vit. D); por lo tanto, no parece justificado indicarlas en niños con DAC funcional. Sin embargo, en un tratamiento individualizado puede ensayarse una exclusión limitada a 2-4 semanas para determinados alimentos identificados como triggers o desencadenantes que ya se han comentado. Así, la limitación de FODMAPs parece útil en pacientes adultos con colon irritable, pero no se ha demostrado en niños. Puede restringirse los alimentos ricos en fructosa, en aquellos niños en los que se sospeche una intolerancia a la misma, siempre que se obtengan resultados positivos.
La exclusión de la lactosa por corto periodo de prueba puede ser útil, si la clínica hace sospechar intolerancia a la misma (dolor de tipo cólico, gases, borborigmo y diarrea líquida tras ingesta de alimentos ricos en lactosa) y, en los casos dudosos, podría indicarse un test de hidrógeno espirado para lactosa, complementando la dieta con aportes adecuados de Ca y vitamina D, incluso con sustitutos de la enzima lactasa. Sin embargo, en un estudio en niños con DAC funcional, no se encontró diferencia en la respuesta entre el grupo con déficit de lactasa y los que no la tenían al dar una dieta exenta de leche, ni tampoco con respecto al grupo control que siguió una dieta normal(17).
En cuanto al gluten, se han popularizado las dietas sin gluten para el tratamiento del DAC, bajo la hipótesis de una sensibilización a este o al trigo, sin evidencia de EC en la biopsia intestinal. No parece estar justificada dicha restricción, pues se ha evidenciado que menos del 4,4º/oo de niños con DAC tienen EC(11).
Los probióticos pueden ser útiles en el tratamiento del DAC funcional y, concretamente, se han utilizado en el síndrome de intestino irritable. Los mecanismos de acción no están claros, podrían mejorar los síntomas gastrointestinales restaurando el equilibrio microbiano en el intestino, mediante la competencia metabólica con los patógenos, restableciendo la barrera de la mucosa intestinal o alterando la respuesta inflamatoria intestinal. Los más usados han sido preparados comerciales que contienen: L. rhamnosus, L. reuteriy Saccharomyces boulardii. Los resultados no han sido concluyentes: en unos estudios, han demostrado disminuir la intensidad y frecuencia del dolor y, en otros, solo la intensidad, pero no la frecuencia.
Los aportes de fibra suplementaria soluble en agua, tipo psyllium hidrófilo mucoide (cáscara de ispaghula) o goma guar, en dosis tales que la ingesta total de fibra en gramos sea de no más de 5-10 + la edad del niño en años, se han utilizado para el DAC asociado con síndrome de intestino irritable en niños y estreñimiento funcional crónico, no así la fibra insoluble tipo salvado de trigo o maíz.
Las medidas farmacológicas: no hay evidencia suficiente en cuanto a sus beneficios, pero pueden prescribirse fármacos en niños con sintomatología grave que no han respondido a los tratamientos más simples y con la intención de mitigar alguno de los síntomas más molestos durante periodos de tiempo cortos, no más de 2 semanas. Se han utilizado diferentes fármacos(13):
• Medicamentos antiespasmódicos, tales como aceite de menta e hiosciamina. Se cree que son útiles para el dolor abdominal funcional y el síndrome de intestino irritable, a través de sus efectos en la disminución de los espasmos del músculo liso en el tracto gastrointestinal, que pueden ser responsables de síntomas tales, como dolor.
• El mentol, que es el ingrediente activo en el aceite de menta, es un monoterpeno cíclico con propiedades de bloqueo de los canales del calcio, que se supone que se activa en el músculo liso íleal y en el colon. Los efectos secundarios informados incluyen: ardor rectal, dolor esofágico o acidez estomacal y reacciones alérgicas. En los niños que recibieron aceite de menta, se evidenció una mejoría en la escala de gravedad de los síntomas del síndrome de colon irritable en comparación con el grupo placebo (p<0,001). Sin embargo, no hubo diferencia entre los grupos en cuanto a la acidez, eructos, patrón de heces y su consistencia.
• El aceite de menta (peppermint), aunque no disponible en España, en EE.UU. se presenta en dos formas comerciales: cápsulas con recubrimiento entérico de 187 mg/8 h para niños entre 30-45 kg y las de 374 mg/8 h para los mayores de 45 kg.
• La hiosciamina y diciclomina se consideran antiespasmódicos, debido a sus efectos anticolinérgicos en el músculo liso. La hiosciamina se ha utilizado en los niños durante un corto plazo para tratamiento de los síntomas del dolor gastro-intestinal, pero su uso a largo plazo se ha asociado con efectos secundarios anticolinérgicos, como: sequedad de boca, retención urinaria, visión borrosa, taquicardia, somnolencia y estreñimiento.
• Los antidepresivos pueden estar justificados dado la frecuente asociación de depresión al DAC. Estos pueden indicarse por el pediatra o paidopsiquiatra si la ansiedad y la depresión actúan como factores desencadenantes o perpetuantes del DAC.
Los mecanismos de acción incluyen la reducción de la percepción del dolor, la mejora del estado de ánimo y de los patrones de sueño, así como la modulación del tracto gastrointestinal, a menudo a través de efectos anticolinérgicos. Los antidepresivos, como los tricíclicos y los inhibidores selectivos de la recaptación de serotonina (ISRS), se han mostrado beneficiosos para el tratamiento del dolor abdominal funcional en adultos. Sin embargo, el uso de medicamentos antidepresivos en niños y adolescentes, se ha cuestionado recientemente por el aumento de pensamientos suicidas y/o alteración del comportamiento, aunque no se ha evidenciado que estos conduzcan a un mayor riesgo de suicidio.
• Los antidepresivos tricíclicos actúan no solo a través de vías noradrenérgicas y serotoninérgicas, sino que también tienen propiedades antihistamínicas y antimuscarínicas. Los agentes anticolinérgicos reducen la velocidad de tránsito en el tracto gastrointestinal, beneficiando a los pacientes con síndrome de intestino irritable en los que predomine la diarrea, pero a su vez pueden empeorar el estreñimiento. Es necesario realizar un ECG basal para la evaluación del síndrome de QT prolongado antes de iniciar el tratamiento, es lo que recomienda la American Heart Association, debido a la posibilidad de inducir arritmias cardíacas. En varios estudios, se ha comparado la amitriptilina con el placebo para el tratamiento de síndrome de intestino irritable, dolor funcional o dispepsia funcional en niños. La respuesta global al tratamiento fue de alivio del dolor abdominal, sin diferencia significativa entre los dos grupos (63 y 57,5%, respectivamente), aunque sí se redujeron las puntuaciones de ansiedad (p<0,0001) en el grupo de la amitriptilina, no evidenciándose tampoco diferencia en la discapacidad, depresión o puntuaciones de somatización durante el ensayo de 4 semanas.
• Los inhibidores selectivos de la recaptación de serotonina (ISRS) actúan mediante el bloqueo de la captación de la 5-hidroxitriptamina (5-HT) y el aumento de su concentración en las terminaciones nerviosas presinápticas. Además de sus efectos sobre el SNC en el estado de ánimo y la ansiedad, los ISRS también puede ser beneficiosos para el tratamiento del DAC. La serotonina es un neurotransmisor importante en el tracto gastrointestinal, ya que se encuentra en mayor concentración en las células enterocromafines del intestino. El papel exacto de la serotonina en el tracto GI no ha sido totalmente dilucidado, pero se ha implicado en la modulación de la motilidad del colon y el dolor visceral en el intestino. Son escasos los ensayos pediátricos aleatorizados y bien controlados sobre el uso de los ISRS en niños. El citalopram se ha ensayado en pacientes con edades entre 7-18 años, con dolor abdominal funcional durante 12 semanas, resultando que el 84% fueron respondedores mejorando la enfermedad. También, se informó de beneficios sobre el dolor abdominal, ansiedad, depresión y otros síntomas somáticos. Aunque estos resultados son prometedores, necesitan confirmarse con ensayos clínicos adicionales.
• Los inhibidores de la recaptación de monoaminas, como la duloxetina y la venlafaxina, representan un grupo reciente de medicamentos antidepresivos con efectos sobre los sistemas serotoninérgicos y adrenérgicos de inhibición del dolor. Estos medicamentos han mejorado el dolor en los pacientes con fibromialgia y neuropatía diabética, pero no se han realizado estudios sobre el tratamiento del dolor abdominal funcional pediátrico.
• La ciprohetadina es un medicamento con efectos antihistamínicos, anticolinérgicos, antiserotonérgicos y, posiblemente, bloqueante de los receptores del calcio usado para la estimulación del apetito y como preventivo de migraña. Puede utilizarse durante 2 semanas para prevenir el dolor y los vómitos en la migraña abdominal y en el síndrome de vómitos cíclicos.
• Los agentes procinéticos que estimulan la motilidad gastrointestinal, se han empleado para los pacientes con DAC, especialmente en condiciones que implican estreñimiento o retraso del vaciado gástrico, tales como el síndrome de intestino irritable y la dispepsia funcional. Los antagonistas de los receptores D2 de la dopamina, tales como la metoclopramida y la domperidona, mejoran la motilidad gástrica, pero su uso en dolor abdominal pediátrico y síndrome de intestino irritable está limitado por sus posibles efectos secundarios, incluyendo: reacciones extrapiramidales, somnolencia, agitación, irritabilidad y fatiga. La eritromicina, un antibiótico con propiedades agonistas del receptor de motilina en el estómago, a dosis de 1-2 mg/kg/dosis, también puede ser útil para los síntomas de dolor o dispepsia, pero no hay datos pediátricos que apoyen su uso rutinario en el DAC funcional.
• La loperamida es un agonista de los receptores opiáceos que ralentiza el tránsito colónico, actuando sobre los receptores del plexo mientérico del intestino grueso. Aunque la loperamida se usa comúnmente en el tratamiento de la diarrea y la urgencia en pacientes con síndrome de intestino irritable con predominio de diarrea, los estudios en adultos han demostrado eficacia solo contra los síntomas de la diarrea, pero no en el dolor abdominal.
• Por último, el sobrecrecimiento bacteriano en el intestino delgado se ha sugerido como una posible causa de los síntomas del síndrome de intestino irritable, tales como la producción de gas y la hinchazón anormal. El tratamiento de la proliferación bacteriana con antibióticos, como neomicina y rifaxamin, es beneficioso en adultos con síndrome de intestino irritable, pero se carece de estudios similares en niños y adolescentes(13).
• Los antisecretagogos o antiácidos se han utilizado en la dispepsia funcional con tratamientos de 4-6 semanas y resultados variables. Se distinguen:
- Bloqueantes de H2: cimetidina, famotidine, ranitidina o nizatidina.
- Inhibidores de la bomba de protones: omeprazol, lanzoprazol o esomeprazol.
Recomendaciones terapéuticas según cada subtipo de DAC
Tratamiento de la dispepsia funcional
Se recomiendan comidas poco voluminosas pero frecuentes, evitando los AINEs y alimentos que agravan la dispepsia (cafeína, picantes, comidas grasas). La dispepsia funcional tiene una alta tasa de respuesta al placebo. En casos tórpidos, puede ensayarse un tratamiento empírico con antagonistas de los receptores de H2, con inhibidores de la bomba de protones o con sucralfato durante 4-6 semanas, y si no hay respuesta retirarlo. En ocasiones, pueden ser útiles bajas dosis de procinéticos, antieméticos o antidepresivos tricíclicos.
Tratamiento del síndrome de intestino irritable
Se suele iniciar con cambios dietéticos, eliminando por un corto periodo de tiempo, 2-4 semanas de prueba, aquellos alimentos identificados como desencadenantes. No debe restringirse la lactosa, salvo prueba documentada de intolerancia o malabsorción de la misma, pues no hay evidencia de que su supresión disminuya los síntomas del DAC(17).
Una dieta rica en fibra soluble puede mejorar la sintomatología de los niños con síndrome de intestino irritable con predominio de estreñimiento, aunque con escasa efectividad.
Cuando la sintomatología persiste a pesar de los cambios dietéticos, la respuesta al placebo también es alta o pueden utilizarse diversos fármacos según la sintomatología predominante: espasmolíticos, menos recomendables los anticolinérgicos, cuando predomine los cólicos. Si la diarrea es el síntoma invalidante, aparte de una nota para el colegio para que se le permita ir al baño cuando lo solicite, no están justificadas las restricciones dietéticas, salvo si se identifica a la lactosa, sorbitol o fructosa como desencadenante de la misma. Tampoco está justificado el uso de antidiarreicos, dado que estas suelen ser de corta duración. Si son diarreas muy frecuentes, más de 3 deposiciones sueltas o acuosas/día, con duración de más de 2 semanas, hay que descartar causa orgánica. Puede estar justificado el tratamiento de la ansiedad, depresión y estrés, que suele asociarse al síndrome de intestino irritable, para el que son útiles los ISRS tipo fluoxetina.
Tratamiento de la migraña abdominal
Lo primordial es evitar desencadenantes alimentarios, farmacológicos o emocionales cuando estos se han identificado. Se han utilizado diversos fármacos como preventivos: propanolol, ciproheptadina, pizotifeno, algunos inhibidores del calcio (flunarizina) o el sumatriptan en los ataques agudos y en adolescentes.
Tratamiento del dolor abdominal funcional
Es importante establecer una alianza terapéutica con los padres y el niño. Las restricciones dietéticas solo están justificadas para aquellos alimentos desencadenantes de la sintomatología. Es imprescindible actuar sobre los factores psicosociales asociados con antidepresivos o no. El citalopran ha mostrado resultados favorables.
Seguimiento
Es fundamental para asegurar el control de la enfermedad y la confianza en el médico.
Los niños con DAC funcional requieren seguimiento regular para mantener la relación terapéutica, proporcionar una educación continua, tranquilizar al niño y a su familia, supervisar la respuesta a las diferentes pautas terapéuticas y controlar el desarrollo de signos de alarma a los que el pediatra de AP ha de estar siempre atento, para derivación al gastroenterólogo, psicólogo o paido-psiquiatra, según el caso; reconociendo el pediatra de AP sus limitaciones y la conveniencia de que el paciente acuda a un segundo escalón, en el caso de mala evolución o pérdida de la confianza.
Pronóstico
Depende más de la actitud de los padres ante el cuadro clínico, que del resto de medidas terapéuticas.
El DAC se resuelve en la mayoría de los niños, pero persiste hasta en un 29,1% a los 5 años de seguimiento, como se ha comentado. Los factores que favorecen la mejoría del DAC funcional son:
• La aceptación de un modelo biopsicosocial de la enfermedad.
• Sintomatología poco invalidante en el momento de la presentación, con poco tiempo de evolución.
• Obtención de una respuesta favorable al principio.
Las circunstancias que se han visto involucradas en la persistencia del DAC funcional son:
• No aceptación del modelo biopsicosocial por parte de los padres.
• Familias que refuerzan el papel de enfermo del paciente, no enviándolos al colegio o sacándolos del mismo por el dolor, magnificando las actuaciones terapéuticas y diagnósticas.
• Familias dolorosas, afectas de otros trastornos que producen dolor crónico: fibromialgias, colon irritable, enfermedades reumáticas.
• Presencia de acontecimientos vitales negativos: separación parental, muerte familiar, cambio de colegio.
• Larga duración del dolor, mayor de 6 meses antes de consultar.
• Edad menor de 6 años.
• Presencia de ansiedad y síntomas depresivos concomitantes.
Se ha comprobado que algunos de los niños con DAC funcional acaban desarrollando un síndrome de intestino irritable del adulto y presentan mayor riesgo de desarrollar ansiedad y depresión.
Infección por Helicobacter pylori y DAC
Introducción
La detección de una infección por helicobacter pylori no siempre indica un tratamiento del mismo.
En AP es muy frecuente el DAC; por otra parte, se conoce la alta incidencia de infección por helicobacter pylori (HP) en la población general y la posibilidad que esto se traduzca en enfermedad péptica en el adulto, que puede iniciarse desde la infancia tardía y adolescencia, con una sintomatología inespecífica similar al DAC. Además, existe la posibilidad de un diagnóstico relativamente sencillo y asequible de la infección por helicobacter, para ofrecer un tratamiento correctamente indicado. Esto ha generado una serie de controversias que se intentan aclarar.
¿Cuándo realizar estudio de infección por HP en AP?
Solo se ha de buscar HP, en pacientes con signos de alarma y que sean subsidiarios de tratamiento para erradicar al HP.
Para dar respuesta a la pregunta que se ha de plantear el pediatra de AP, de si debe o no iniciar el estudio de infección por HP en un niño con DAC con alta sospecha de ser causado por enfermedad péptica, relacionada con HP, ha de tener en cuenta que:
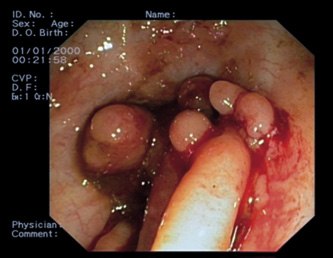
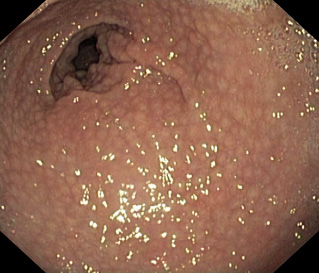
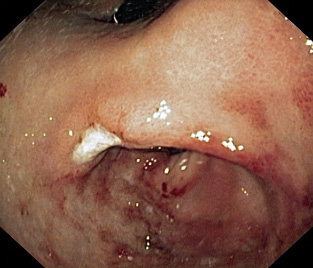
• El HP convive con el hombre desde hace más de 60.000 años. Es en el año 1982 cuando Barry J. Marshall y J. Robin Warren lo aíslan de la mucosa gástrica y, posteriormente, se considera factor de riesgo de primer orden para el desarrollo de: ulcus duodenal o gástrico, gastritis crónica activa, atrofia metaplásica, así como de adenocarcinoma gástrico y linfoma MALT (del inglés: tejido linfoide asociado a mucosa), sobre todo, en adultos. En los niños, las lesiones observadas más frecuentemente son: la gastritis antral superficial, que puede variar de leve eritema a intensa nodularidad, y en la biopsia observarse menor actividad neutrofílica y mayor linfocítica, a diferencia de los adultos; y, con muy poca frecuencia, el ulcusduodenal o gástrico e inexistente adenocarcinoma gástrico. Por otra parte, no parece tampoco estar clara la evolución de una situación a otra.
• La falta de relación de la presencia del germen con los síntomas de DAC, dado que la infección de HP se detecta con igual prevalencia entre pacientes con o sin DAC. Tampoco se encuentra evidencia concluyente entre dolor epigástrico e infección con HP en niños, mientras que sí parece relacionarse esta más con dolor abdominal inespecífico (aquel que no cumple completamente los criterios de dolor funcional) a nivel hospitalario, o sea en pacientes que previamente han sido remitidos por sospecha de organicidad, y no en pacientes de AP(2,12).
En vista de estos resultados, no parece justificado el estudio de HP en pacientes con DAC funcional típico, sino en niños con dolor epigástrico de corto tiempo de evolución y con signos de alarma (sangrado, dolor epigástrico superior, dolor abdominal inespecífico con anemia ferropénica refractaria, saciedad precoz, pérdida de peso inexplicable, disfagia progresiva, odinofagia, vómitos recurrentes, antecedentes familiares de cáncer gastrointestinal, cáncer esofágico-gástrico).
¿Cuál ha de ser la actitud diagnóstica-terapéutica?
Los exámenes no invasivos proporcionan un diagnóstico rápido y asequible en pacientes de AP con síntomas de alarma, pero su utilidad para indicar un tratamiento está en entredicho.
En los adultos con síntomas gastrointestinales altos, se acepta el diagnóstico no invasor de infección como causante de probable enfermedad péptica y tratamiento correspondiente según consenso de Maastricht III(18). En la edad pediátrica, la mayoría de protocolos propone el test de urea C13 en el aliento, con o sin la detección de Ag monoclonal en heces por ELISA (enzime linked immunosorbent assay), como diagnóstico de colonización con sensibilidad y especificidad próximas al 100%, que son las que indicarán la endoscopia confirmadora o no de presencia de enfermedad péptica susceptible de tratamiento para erradicar al HP y la confirmación, por estas pruebas no invasoras, de la efectividad de dicho tratamiento; evidentemente, todo ello en el ámbito hospitalario. Otros aceptan, de forma similar a los adultos, el uso de estos exámenes no invasores como abordaje inicial diagnóstico-terapéutico de los pacientes pediátricos, una vez descartadas otras causas de dolor abdominal, obviando la endoscopia en el diagnóstico inicial, pues si bien la especificidad es del 100%, no así la sensibilidad, y por lo tanto, no exenta del peligro de dejar sin tratar a los falsos negativos, a expensas de sobre-tratar falsos positivos de enfermedad péptica. Por último, hay autores que proponen el tratamiento de prueba con antisecretores, para indicar endoscopia en los casos de persistencia de los síntomas(19).
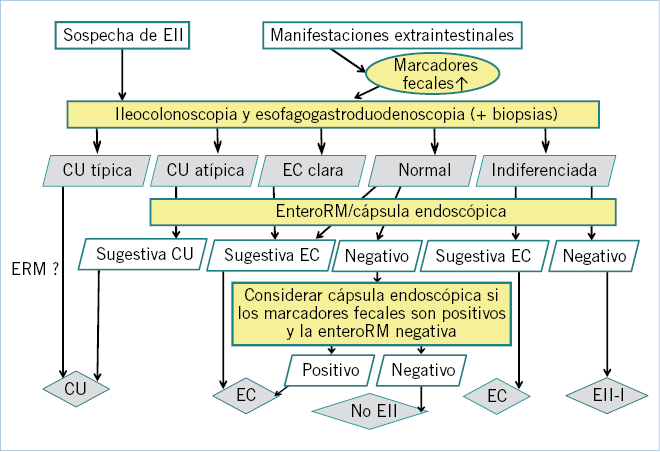
De lo anterior se deduce que, no hay recomendaciones claras sobre el abordaje inicial del diagnóstico en estos pacientes y que no parece indicada la búsqueda de HP en DAC funcional en niños en AP. Sin embargo, no es improcedente solicitar exámenes no invasivos si existe una fuerte sospecha de organicidad, de cara a efectuar un diagnóstico más rápido y preciso(12,19). Tampoco parece descabellado realizar tratamiento para erradicar HP en pacientes con síntomas dispépticos, pero no de alarma para desarrollar cáncer gástrico, con diagnóstico positivo de infección por HP mediante test de urea C13 en aliento y/o test Ag heces monoclonales, dejando la endoscopia para cuando existan signos de alarma o fracaso por posibles resistencias, según las recientes recomendaciones de Maastricht IV(21) (ver algoritmo diagnóstico terapéutico).
Pruebas diagnósticas para HP
El test de urea marcada con C13 es la prueba no invasiva prínceps de infección por HP y la endoscopia con test de ureasa rápido de confirmación de enfermedad péptica; la PCR, aunque no se usa de forma rutinaria, resulta prometedora para la detección del HP en cualquier muestra biológica.
Los exámenes complementarios pueden ser de dos tipos: no invasivos (de diagnóstico de infección) e invasivos (de diagnóstico de enfermedad péptica).
Los exámenes no invasivos son:
• El test del aliento con urea marcada con C13. Se basa en la capacidad que tiene el HP de producir ureasa, que hidroliza la urea administrada liberando en la respiración CO2 marcado que se determina por espectrometría de masas o espectrocolorimetría, siendo el test positivo si se detecta = de 4 ppm o 2,5 ppm, respectivamente, después de administrar 50 o 100 mg de urea marcada con C13, según que el peso sea menor o mayor de 35 kg, y con ayuno previo de al menos 6 horas. Esta prueba tiene una sensibilidad y especificidad cercana al 100% para el diagnóstico de infección por HP. Es el método más factible de seguimiento y control de la infección, es muy sencillo y puede realizarse a todas las edades, incluso en lactantes, aunque los resultados son menos fiables en niños menores de 6 años.
• Detección de antígenos monoclonales en heces mediante ELISA en niños infectados por HP. Presenta una sensibilidad y especificidad del 97%, no así con el uso de antígenos policlonales u otros métodos de laboratorio como inmunocromatografía, con resultados más heterogéneos(20). Este examen complementario es útil, tanto para el diagnóstico de infección como para el control del tratamiento de erradicación del HP junto con el test urea C13 en el aliento. Por otra parte, se cuenta con un test rápido de detección de Ag en heces cuyo resultado se puede conocer en la misma consulta. Hay que considerar que dicho test, al igual que el del aliento, pueden ver atenuada su sensibilidad y especificidad por toma previa de inhibidores de la bomba de protones (IBP), antibióticos o sangrado gástrico.
• Detección de Ac IgG anti HP en sangre periférica mediante ELISA o EIA (enzime immunoassay). Presenta una sensibilidad del 90% en adultos y especificidad entre el 50-90%, y menor del 60% en niños. Ha dejado de utilizarse como prueba diagnóstica o de control de la erradicación, ya que dicha serología puede persistir positiva hasta más de 18 meses post-erradicación, aunque conserva su validez para estudios epidemiológicos, al igual que la detección de Ac en orina o saliva, y en el caso de que no podamos suprimir el tratamiento anti-secretor. Por otra parte, se ha de tener en cuenta que, en las zonas geográficas donde haya una baja prevalencia (<20%) de infectados por HP, disminuye sensiblemente el valor predictivo positivo de dicha prueba, por lo tanto ante una serología positiva habría que pensar que se trate de un falso positivo que precise confirmación con otros test, como el del aliento con urea marcada o el de la determinación del Ag monoclonal en heces. En este escenario, una serología negativa tiene mayor valor predictivo negativo, o sea, podría ser útil para descartar la infección.
La detección por inmunoblot de Ac IgG circulantes frente a proteínas cag A y vac A (citotóxica y vacuolizante, respectivamente), que son factores implicados en la patogenicidad del HP y en su capacidad para generar úlcera péptica y cáncer gástrico, es un marcador de riesgo del HP.
• La determinación de DNA del HP por PCR (Polymerase Chain Reaction) en muestras de heces, tiene utilidad en el diagnóstico de infección activa de HP con especificidad del 98% (94,3-98,6%) y sensibilidad del 80,8% (75,3-85,6%). De momento, no sustituye a la determinación de Ag de HP en heces como medio diagnóstico de infección, aunque sí que es útil para determinar la presencia de HP en muestras de biopsias gástricas cuando el cultivo es difícil.
La endoscopia es un método invasivo, sensible y específico, para la confirmación de enfermedad péptica, el grado de afectación, la presencia de agente etiológico y, sobre todo, para la obtención de muestras para cultivo y valoración de resistencias microbianas o detección de factores de patogenicidad, como la proteína cag A y vac A. En las muestras de biopsia gástrica o duodenal en su caso, obtenidas de los diversos puntos de lesión, se pueden realizar los siguientes estudios:
• Test de ureasa rápida, en el mismo quirófano, que detecta la presencia de HP en pocos minutos sobre las muestras obtenidas. Tiene una sensibilidad del 90% y especificidad del 95%. Dicha sensibilidad puede verse disminuida por el tratamiento previo o la presencia de sangrado.
• Examen histológico, permite observar predominio de actividad inflamatoria linfocítica mayor que neutrofílica e identificar al HP por tinción de Giemsa o Gram. Tiene una especificidad del 100%, pero sensibilidad variable dado el riesgo de biopsias de zonas no afectas.
• Cultivo microbiológico tiene como hándicap, el lento crecimiento del HP, que puede precisar hasta de 8-10 días. Pero es útil para identificar diferentes cepas, resistencia microbiana y detección de factores de patogenicidad. Presenta una especificidad de 100%, pero sensibilidad variable, entre 60-98%; además, disminuye significativamente por tratamientos previos. Es muy influenciable por la técnica de recogida, conservación y procesamiento de la misma, para el adecuado cultivo. Se indica ante la presencia de sospecha de resistencia antibiótica, estudio de sensibilidad para el tratamiento de las reinfecciones.
• PCR (Polymerase Chain Reaction), su utilidad es la detección del ADN del HP en muestra de biopsia, por lo tanto diagnóstico de infección activa, identificación de mutaciones asociadas a resistencia antimicrobianas (p. ej. la mutación A2/93G se ha asociado a resistencia a claritromicina) y factores de virulencia de HP.
Tratamiento
La triple terapia sigue siendo válida, preferiblemente durante 14 días. Cuando esta fracasa, ha de comprobarse por medios invasivos y cultivo, el tratamiento más idóneo y la erradicación postratamiento, a la que puede contribuir el uso de algún probiótico.
El diagnóstico de infección por HP conlleva tratamiento en pacientes con sintomatología gastrointestinal y confirmación de enfermedad péptica mediante endoscopia gástrica. También, puede realizarse tratamiento en pacientes muy sintomáticos sin demostración de enfermedad péptica, con endoscopia negativa, pero con pruebas no invasivas positivas, test del aliento con urea marcada y Ag monoclonales en heces, sobre todo, cuando hay antecedentes familiares de enfermedad péptica o cáncer gástrico con HP positivo(21).
La realización previa de cultivo microbiológico y estudio de resistencias antibióticas en las muestras de biopsias no se recomienda de forma rutinaria, sino que se reserva para los pacientes con enfermedad refractaria, principalmente en los países donde hay una alta incidencia de resistencia a claritromicina y metronidazol (mayor del 15%).
La comprobación de erradicación mediante test de urea marcada en aliento o Ag en heces y, en su caso, endoscopia superior con cultivo en las muestras de biopsias, a las 4-6 semanas después de tratamiento, está indicada en pacientes que tienen síntomas persistentes después de tratamiento correcto de clínica dispéptica, los que presentan úlcera péptica asociada a HP y en los que se observa tejido linfoide asociado a mucosa gástrica o linfoma (MALT) en presencia de HP. No se usa de rutina en pacientes respondedores(21).
El tratamiento de primera línea, tanto en niños como en adultos, sigue siendo la triple terapia, que combina dos antibióticos con un antisecretor, inhibidor de la bomba de protones (IBP) o sales de bismuto (B). Los fármacos de uso más frecuente y las distintas pautas de tratamiento se encuentran en la tabla VII.
En los alérgicos a amoxicilina, puede sustituirse esta por metronidazol, tinidazol o levofloxacino.
Como antisecretores, pueden utilizarse tanto los IBP como las sales de bismuto, este último parece más eficaz que el primero, mostrando mayores tasas de erradicación, aunque es peor tolerado por los niños. La ranitidina puede ser una alternativa válida para los que no toleran el omeprazol.
La clásica triple terapia OCA (Tabla VII) sigue siendo el tratamiento válido en zonas de baja incidencia (<15%) de resistencia a macrólidos. En presencia de tasas elevadas de resistencia a claritromicina o metronidazol o bien porque el paciente los usa frecuentemente por otros motivos, se pueden utilizar otras alternativas de triple terapia, sustituyendo la claritromicina por metronidazol o levofloxacino y los IBP por las sales de B; esto es, usar el BAM/OAM. Se puede acudir a la terapia cuádruple, que combina dos antisecretores (IBP y B) con dos antibióticos (M, Tc o Dx), por ejemplo, BOMTc (Dx) para niños de más de 8 años. Hay que tener en cuenta que las tetraciclinas están contraindicadas en niños menores de 8 años, dados sus efectos deletéreos sobre el esmalte. También, se puede usar una terapia secuencial: OA durante 5 días, seguida de OCM/Tn por 5 días más u otras que las amplían hasta los 14 días: LzA durante 7 días, seguida de Lz C M por otros 7 días más. Este tipo de tratamiento secuencial no parece añadir beneficios significativos a la triple terapia en los niños y sí que puede incrementar los efectos secundarios.
En los casos de HP persistente en pacientes con enfermedad péptica previa, se ha usado terapia de rescate, en la que entra en juego el levofloxacino o el rifabutin (derivado semisintético de la rifampicina) en diferentes combinaciones: OALv o OAR. En estos casos, siempre está indicado el estudio previo de sensibilidad antimicrobiana que asegure un tratamiento específico.
En cuanto a la duración del tratamiento, existen discrepancias. Por lo general, son más eficaces los de 14 días; sin embargo, hay estudios que no encuentran diferencias significativas con los de 7 o 10 días, mejor tolerados.
Los IBP han de tomarse antes del desayuno, en medio ácido (yogur o zumo). Las sales de bismuto pueden darse media hora antes o después de las comidas y los antibióticos después de las comidas, para facilitar el contacto con la pared gástrica.
El tratamiento coadyuvante consiste en el uso de probióticos, concretamente, el lactobacilus reuteri o el sacharomyces boulardi mejoran la tolerancia a los antibióticos y disminuyen las diarreas, las náuseas y la dispepsia, e incluso pueden inhibir el crecimiento del HP mejorando las tasas de erradicación(22).
Bibliografía
Los asteriscos reflejan el interés del artículo a juicio del autor.
1. Apley J, Naish N. Recurrent abdominal pains: a field survey of 1,000 school children. Arch. Dis. Child. 1958; 33(168): 165–170.
2.*** American Academy of Pediatrics Subcommittee on Chronic Abdominal Pain, North American Society for Pediatric Gastroenterology Hepatology and Nutrition. Chronic abdominal pain in children. Pediatrics 2005; 115: 812-5.
3.* Saps M, Seshadri R, Sztainberg M, et al. A prospective school-based study of abdominal pain and other common somatic complaints in children. J Pediatr. 2009; 154(3): 322-6.
4.*** Appendix A. Rome III diagnostic criteria for functional gastrointestinal disorders. http://www.romecriteria.org/assets/pdf/19_RomeIII_apA_885-898.pdf (Accessed on July 18, 2013).
5. Cervero F. Neurophysiology of gastrointestinal pain. Baillieres Clin Gastroenterol. 1988; 2: 183.
6. Hyams JS, Hyman PE. Recurrent abdominal pain and the biopsychosocial model of medical practice. J Pediatr. 1998(4); 133: 473-78.
7. Boyle JT. Abdominal pain. In: Pediatric Gastrointestinal Disease: Pathophysioly, Diagnosis, Management, 4th, Walker WA; Goulet O, Kleinman RE, et al. (Eds); BC Decker Inc, Hamilton, On 2004. P. 232.
8.** Gieteling MJ, Bierma-Zeinstra SM, Passchier J, Berger MY. Prognosis of chronic or recurrent abdominal pain in children. J Pediatr Gastroenterol Nutr. 2008; 47: 316-26.
9.* John M. Goldenring, MD, MPH, & Eric Cohen, MD in: Contemporary Pediatrics, Getting into Adolescent Heads.1988.
10.** Wright NJ, Hammond PJ, Curry JI. Chronic abdominal pain in children: help in spotting the organic diagnosis.Arch Dis Child Educ Pract. Ed 2013; 98: 32-39.
11.** Hyams JS, Treem WR, Justinich CJ, et al. Characterization of symptoms in children with recurrent abdominal pain: resemblance to irritable bowel syndrome. J Pediatr Gastroenterol Nutr. 1995; 20(2): 209-14.
12.** Spee LA, Madderom MB, Pijpers M, et al. Association between helicobacter pylori and gastrointestinal symptoms in children. Pediatrics. 2010; 125(3): e651-69.
13.** Chiou E, Nurko S. Functional abdominal pain and irritable bowel syndrome in children and adolescents.Therapy. 2011; 8(3): 315-31.
14.* Hernández Hernández A. Estudio del perfil de hidrógeno espirado y permeabilidad intestinal en recién nacidos sometidos a fototerapia. Tesis doctoral. Universidad de La Laguna, Tenerife 1996: 40-63.
15.*** Bonnin Tomás A, Vila Vidal M, Rosell Camps A. Calprotectina fecal como marcador diferencial entre patología gastrointestinal orgánica y funcional. Rev Esp Enferm Dig. 2007; 99: 689-93.
16.** Levy RL, Langer SL, Walker LS, et al. Twelve-month follow-up of cognitive behavioral therapy for children with functional abdominal pain. JAMA Pediatr. 2013; 167(2): 178-84.
17.*** Huertas-Ceballos AA, Logan S, Bennett C, Macarthur C. Dietary interventions for recurrent abdominal pain (RAP) and irritable bowel syndrome (IBS) in childhood.Cochrane Database Syst Rev. 2009; CD003019.
18.*** Malfertheiner P, Megraud F, O’Morain C, Bazzoli F, El –Omar E, Graham D, et al. Current concepts in the management of Helicobacter pylori infection: the Maastricht III Consensus Report. Gut. 2007; 56: 772-81.
19.** Molina Arias M, Martínez-Ojinaga Nodal E. Helicobacter pylori. Tras la tempestad, ¿vendrá la calma? Evid Pediatr. 2010; 6: 26.
20.** Ochoa Sangrador C, Andrés de Llano JM: Algunas pruebas de detección de antígeno de Helicobacter pylori en heces son suficientemente válidas en la infancia. Evid Pediatr. 2011; 7: 65.
21.*** Malfertheiner P, Megraud F, O’Morain CA, et al. Management of Helicobacter pylori infection –the Maastricht IV/ Florence Consensus Report.Gut 2012; 61: 646-64.
22.* Szajewska H, Horvath A, Piwowarczyk A. Meta-analysis: the effects of Saccharomyces boulardii supplementation on Helicobacter pylori eradication rates and side effects during treatment. Aliment Pharmacol Ther. 2010; 32: 1069-79.
Bibliografía recomendada
- American Academy of Pediatrics Subcommittee on Chronic Abdominal Pain, North American Society for Pediatric Gastroenterology Hepatology and Nutrition. Chronic abdominal pain in children. Pediatrics 2005; 115: 812-5.
Este artículo constituye una verdadera guía, para la conceptualización, diagnóstico y tratamiento del dolor abdominal crónico de los niños. Este informe se ha preparado sobre la base de una revisión sistemática e integral y la clasificación de literatura médica. El subcomité examinó el valor diagnóstico y terapéutico de la historia médica y psicológica, pruebas de diagnóstico y terapia farmacológica y conductual. La presencia de síntomas o signos de alarma se asocia con una mayor prevalencia de enfermedad orgánica y, en ausencia de ellos, es poco probable encontrar enfermedad orgánica. La mayoría de los niños que acuden a la consulta del pediatra de Atención Primaria con dolor abdominal crónico es poco probable que requieran pruebas de diagnóstico. Los estudios pediátricos sobre intervenciones terapéuticas se mostraron limitados y no concluyentes en cuanto a su eficacia.
- Saps M, Seshadri R, Sztainberg M, et al. A prospective school-based study of abdominal pain and other common somatic complaints in children. J Pediatr. 2009; 154(3): 322-6.
El objetivo de este trabajo fue determinar la prevalencia y el impacto del dolor abdominal pediátrico. Para ello, se evaluaron 237 estudiantes de tercero a octavo grado de 2 escuelas públicas, semanalmente, durante 6 meses. Las conclusiones a las que llegan fueron que, el dolor abdominal es común en los niños en edad escolar y se asocia con una peor calidad de vida, comorbilidades psicológicas, absentismo escolar y ausencias al trabajo de los padres.
- Appendix A. Rome III diagnostic criteria for functional gastrointestinal disorders. http://www.romecriteria.org/assets/pdf/19_RomeIII_apA_885-898.pdf (Accessed on July 18, 2013).
Los criterios pediátricos de Roma II para los trastornos gastrointestinales funcionales (FGID) se definieron en 1999 para ser utilizados como herramientas de diagnóstico y avanzar en la investigación empírica. En este documento, el Comité de Roma III actualiza y revisa los criterios pediátricos. El proceso de toma de decisiones para definir los criterios de Roma III, para niños de 4 a 18 años, consistió en llegar a un consenso basado en la experiencia clínica y revisión de la literatura. En los nuevos criterios, desaparecen el síndrome de vómitos cíclicos, la rumia y la aerofagia, así como el estreñimiento funcional y la incontinencia fecal no retentiva. Otros cambios notables de Roma II que incluye Roma III son la disminución de 3 a 2 meses de duración de los síntomas necesarios para los trastornos crónicos y la modificación de los criterios de dolor abdominal funcional en niños y adolescentes. Roma III representa una evolución de Roma II y puede ser muy útil para los clínicos y los investigadores que se ocupan de los FGID en la infancia. La disponibilidad futura de los datos basados en la evidencia adicional es probable que conlleve una modificación de los criterios pediátricos para el “dolor abdominal crónico”, nuevo término acuñado por dicho consenso para describir el dolor abdominal intermitente o constante (de etiología funcional u orgánica) de, al menos, dos meses de evolución. El término “dolor abdominal crónico” abarca “el dolor abdominal recurrente”, por lo que este último concepto se desecha como diagnóstico.
- Gieteling MJ, Bierma-Zeinstra SM, Passchier J, Berger MY. Prognosis of chronic or recurrent abdominal pain in children. J Pediatr Gastroenterol Nutr. 2008; 47: 316-26.
La conclusión a la que se llega en este artículo, es el escaso valor diagnóstico y pronóstico de los exámenes complementarios en el DAC sin signos de alarma.
- John M. Goldenring, MD, MPH, & Eric Cohen, MD in: Contemporary Pediatrics, Getting into Adolescent Heads.1988.
En este capítulo, se explica ampliamente el uso de la herramienta HEADSS en la entrevista sistemática del Adolescente con DAC.
- Wright NJ, Hammond PJ, Curry JI. Chronic abdominal pain in children: help in spotting the organic diagnosis. Arch Dis Child Educ Pract. Ed 2013; 98: 32-39.
En este artículo, mediante la exposición de casos clínicos típicos, se repasa ampliamente la sistemática de estudio del dolor abdominal crónico y concluye:
• El DAC en los niños es común, afecta al 10-14% de los niños en el Reino Unido.
• Solo el 5-10% de los niños con DAC tiene una causa orgánica subyacente.
• Los exámenes complementarios no ayudan a distinguir entre el dolor abdominal orgánico y el funcional, en ausencia de síntomas y signos de alarma, y se deben evitar.
• El dolor abdominal funcional se maneja de manera óptima al hacer un diagnóstico positivo, brindando tranquilidad y educación, evitando extensas investigaciones y se centra en un retorno a la función normal en lugar de a la resolución del dolor.
• Los síntomas y signos de alarma deben impulsar una mayor investigación y derivación adecuada a un gastroenterólogo pediátrico o cirujano, como se indica en la guía basada en la evidencia proporcionada.
- Hyams JS, Treem WR, Justinich CJ, et al. Characterization of symptoms in children with recurrent abdominal pain: resemblance to irritable bowel syndrome. J Pediatr Gastroenterol Nutr. 1995; 20(2): 209-14.
En este estudio, se ha pretendido relacionar los síntomas en niños con dolor abdominal recurrente con el síndrome del intestino irritable (SII) del adulto, con el objetivo de encontrar un subgrupo que se asemeje a dicho síndrome. El estudio no solo confirma la heterogeneidad clínica de los niños con dolor abdominal recurrente, sino que también demuestra simultáneamente que la mayoría de los niños con este trastorno tienen síntomas que cumplen los criterios estandarizados para el SII en los adultos. La identificación de subgrupos de niños con dolor abdominal recurrente puede proporcionar un marco para el diagnóstico de la enfermedad funcional del intestino, así como establecer la necesidad de pruebas invasivas y costosas.
- Spee LA, Madderom MB, Pijpers M, et al. Association between helicobacter pylori and gastrointestinal symptoms in children. Pediatrics. 2010; 125(3): e651-69.
En esta revisión, no se encontró asociación entre dolor abdominal recurrente e infección por helicobacter pylori en los niños, ni evidencia concluyente para asociar dolor epigástrico con infección por H. pylori. Se halló evidencia de una asociación entre esta infección y dolor abdominal inespecífico, pero no se pudo confirmar este hallazgo en población atendida de forma ambulatoria. De acuerdo a esta revisión, parece que no estaría indicado la realización inicial, en Atención Primaria, de pruebas diagnósticas buscando H. pylori, dentro del algoritmo diagnóstico del dolor abdominal recurrente en niños. No obstante, sería de interés establecer una regla clínica sobre en qué situaciones se debería sospechar la existencia de la infección por H. pylori.
- Chiou E, Nurko S. Functional abdominal pain and irritable bowel syndrome in children and adolescents.Therapy. 2011; 8(3): 315-31.
Este artículo aborda la epidemiología, mecanismos propuestos, enfoque clínico y opciones terapéuticas para el manejo del dolor abdominal funcional y el síndrome de intestino irritable en niños y adolescentes, evidenciando la necesidad de establecer el dolor abdominal funcional como diagnóstico positivo, no de exclusión y su enfoque multidisciplinar e integrado.
- Hernández Hernández A. Estudio del perfil de hidrógeno espirado y permeabilidad intestinal en recién nacidos sometidos a fototerapia. Tesis doctoral. Universidad de La Laguna, Tenerife 1996: 40-63.
En esta tesis se hace un amplio y profundo estudio del test de hidrógeno espirado, su utilidad, indicaciones, interpretación y modo de realización a cualquier edad, incluida la neonatal.
- Bonnin Tomás A, Vila Vidal M, Rosell Camps A. Calprotectina fecal como marcador diferencial entre patología gastrointestinal orgánica y funcional. Rev Esp Enferm Dig. 2007; 99: 689-93.
En este artículo, los autores determinan el valor de la calprotectina fecal en una serie de 42 niños, comparando su utilidad en el diagnóstico y seguimiento de los mismos para la distinción entre patología orgánica y funcional, y llegan a la conclusión de que se trata de un marcador sensible, pero no específico, que permite seleccionar pacientes con enfermedad inflamatoria intestinal que requieren colonoscopia para su diagnóstico definitivo, disminuyendo o evitando su realización en pacientes con patología gastrointestinal funcional, por las incomodidades y dificultades que conlleva su realización en pacientes pediátricos.
- Levy RL, Langer SL, Walker LS, et al. Twelve-month follow-up of cognitive behavioral therapy for children with functional abdominal pain.JAMA Pediatr. 2013; 167(2): 178-84.
En este estudio, se ha reclutado a unos 200 niños con dolor abdominal funcional y se ha entrenado a los padres en tres estrategias: de aprendizaje social, de terapia cognitivo-conductual y una basada en la educación y apoyo. Los resultados sugieren la eficacia a largo plazo de una intervención breve para reducir las demandas de los padres y aumentar las habilidades de afrontamiento. Esta estrategia puede ser una alternativa viable para niños con dolor abdominal funcional.
- Huertas-Ceballos AA, Logan S, Bennett C, Macarthur C. Dietary interventions for recurrent abdominal pain (RAP) and irritable bowel syndrome (IBS) in childhood.Cochrane Database Syst Rev. 2009; CD003019.
Revisión amplia de Cochrane DS, que pone en evidencia la inutilidad de las diversas estrategias de modificaciones dietéticas en niños con dolor abdominal recurrente (DAR), porque en la mayoría es posible tratarles estimulando su confianza y con otras medidas sencillas. La conclusión es que hay una falta de pruebas de alta calidad sobre la efectividad de las intervenciones dietéticas. Esta revisión no aporta pruebas de que los suplementos de fibra, las dietas libres de lactosa o de suplementos de lactobacillus sean eficaces en el tratamiento de los niños con DAR.
- Malfertheiner P, Megraud F, O’Morain C, Bazzoli F, El –Omar E, Graham D, et al. Current concepts in the management of Helicobacter pylori infection: the Maastricht III Consensus Report. Gut. 2007; 56: 772-81.
En la tercera conferencia de consenso de Maastricht participaron expertos de 26 países, incluidos médicos de Atención Primaria, ampliando y renovando algunas de las directrices de Maastricht II. En la misma, los grupos de trabajo se ocuparon de tres temas relacionados con la infección por H. pylori: indicaciones/contraindicaciones para la erradicación, exámenes de diagnóstico y tratamiento de la infección, y prevención del cáncer gástrico y otras complicaciones. Se hacen una serie de recomendaciones amplísimas, tanto en aspectos diagnósticos como de tratamiento, algunas llamativas, como las siguientes: en el caso de la dispepsia, en países de baja incidencia de infección por HP, una alternativa es tratarla con la supresión ácida de prueba, dejando para el fracaso de esta la investigación de HP; la opción de iniciar tratamiento de erradicación en niños con síntomas abdominales superiores o anemia ferropénica refractaria a tratamiento con hierro basadas en diagnóstico de test urea C13 en aliento o antígeno monoclonal en heces; y distintas pautas de tratamientos antibióticos y estrategias ante la presencia de resistencia a los mismos.
- Molina Arias M, Martínez-Ojinaga Nodal E. Helicobacter pylori. Tras la tempestad, ¿vendrá la calma? Evid Pediatr. 2010; 6: 26.
Es un interesante artículo de revisión, muy crítico y como su título indica, el tiempo pone a cada cual en su sitio. Se discute la indicación de investigar la infección por HP, porque contamina a un alto porcentaje de la población mundial, así como las indicaciones para realizar la endoscopia y el tratamiento erradicador.
- Ochoa Sangrador C, Andrés de Llano JM: Algunas pruebas de detección de antígeno de Helicobacter pylori en heces son suficientemente válidas en la infancia. Evid Pediatr. 2011; 7: 65.
En este artículo, se confirma la validez de la determinación de Ag HP por ELISA monoclonales como prueba válida (sensibilidad y especificidad del 97% equivalente al test urea C13 en aliento) para el diagnóstico de infección por HP y su uso como comprobación de la erradicación postratamiento.
- Malfertheiner P, Megraud F, O’Morain CA, et al. Management of Helicobacter pylori infection –the Maastricht IV/ Florence Consensus Report.Gut. 2012; 61: 646-64.
En la cuarta Conferencia de Maastricht/Consenso de Florencia, 44 expertos de 24 países tomaron parte activa y examinaron los aspectos relacionados con el papel clínico de H. pylori. La reunión se centró en las indicaciones, el diagnóstico y los tratamientos de la infección por H. pylori, con énfasis adicional en la prevención, en particular, en la del cáncer gástrico. Se proporcionaron recomendaciones sobre la base de la mejor evidencia actual y plausibilidad para guiar a los médicos que participan en el manejo de esta infección, asociada con diversas condiciones clínicas, entre ellas: la estrategia de pruebas no invasivas, el test urea C13 en aliento y determinación de Ag monoclonal en heces, y qué tratamiento es apropiado en situaciones en las que el riesgo de que el paciente tenga cáncer gástrico es bajo. Dicho riesgo es para diferente punto de corte de edad, en pacientes dispépticos según los países. En los grupos de pacientes con un mayor riesgo de cáncer gástrico (más de un punto de la edad de corte local o con síntomas o signos de alarma), no se recomienda la estrategia anterior, sino la de tratamiento tras verificación endoscópica.
- Szajewska H, Horvath A, Piwowarczyk A. Meta-analysis: the effects of Saccharomyces boulardii supplementation on Helicobacter pylori eradication rates and side effects during treatment. Aliment Pharmacol Ther. 2010; 32: 1069-79.
El objetivo del estudio fue investigar los efectos del saccharomyces boulardii, administrado suplementando a la triple terapia de erradicación del helicobacter pylori en un total de 1.307 participantes, 90 de ellos niños, concluyendo que hay evidencias para recomendar el uso de S. boulardii junto con la triple terapia estándar como opción para aumentar las tasas de erradicación y reducción de los efectos secundarios generales relacionadas con el tratamiento, sobre todo, diarrea.
| Caso clínico |
|
Historia actual
Niña de 7 años y 9 meses edad, que acude a consulta por historia de, al menos, un año de evolución, consistente en dolor abdominal de tipo cólico, localización periumbilical, de 1-2 horas de duración, de predominio nocturno, antes de acostarse y después de cenar, pero que nunca ha llegado a despertarla, acompañado en ocasiones de sensación nauseosa y palidez facial, pero sin llegar a vomitar. Achacan el inicio de dichas crisis de dolor, a raíz de que un compañero de su edad, le dio un golpe en el estómago hace más de un año, sigue en el mismo cole, pero no en la misma aula. Dichos dolores se presentaban primero de forma esporádica, tanto en época escolar como en vacaciones, y se fueron haciendo más frecuentes, primero mensuales o cada 15-20 días, pero últimamente parecen ser más frecuentes y se suceden semanalmente, cediendo espontáneamente. Presenta un hábito intestinal con heces cada 1-2 días, la consistencia de las heces es variable, algo más duras (Bristol 2-3) en ocasiones y en otras normales (Bristol 4-5), no diarrea ni fiebre en ningún momento y curva de peso y talla normales, percentiles 50-75 y 90-97, respectivamente.
Antecedentes personales
Recién nacido a término (40 semanas) de peso adecuado a su edad gestacional (PRN: 3.480 g), test de APGAR 9/9, producto de parto eutócico. Desde el periodo neonatal tardío, se detecta escafocefalia y craneosinostosis de sutura sagital que se corrige mediante craniectomía laparoscópica a la edad de 13 meses, sin incidencias. A los 6 años, tuvo infección por giardia lamblia que se resolvió sin problemas.
Antecedentes familiares
Madre en la adolescencia fue intervenida de “apendicitis crónica”. Actualmente, afecta de “síndrome de colon irritable”. Comenta que no pudo estudiar por las molestias digestivas que le producían los exámenes.
Padre padece migraña.
Analítica: Hemograma, perfil bioquímico y enzimático, PCR normales, estudio del hierro, inmuno-globulinas normales, TSH, IgE específica a ácaros, proteínas de la leche y huevo negativas, orina A/S, estudio de Ca/Cr, oxalatos, citratos en orina normales, parásitos en heces, Ag anti HP en heces y sangre oculta en heces negativas.
Ecografía: abdominal, hígado, vesícula biliar, páncreas, riñones y vías urinarias normales, asas intestinales peristálticas, sin engrosamientos murales y sin líquido libre en cavidad abdominal.
|
|
|