 |
| Regreso a las bases |
G. Albi Rodríguez
Profesor asociado del Departamento de Anatomía, Histología y Neurociencia de la Facultad de Medicina de la Universidad Autónoma de Madrid. Facultativo especialista en Radiodiagnóstico del Hospital Infantil Universitario Niño Jesús. Madrid
Pediatr Integral 2012; XVI(7): 565-573
Valoración radiológica de imágenes líticas óseas
Introducción
Existe una gran variedad de patología ósea que puede afectar al niño. Puede ser tumoral, infecciosa, inflamatoria o malformativa. A su vez, clínicamente, se pueden manifestar como dolor óseo, aparecer de forma incidental en estudios de imagen realizados por otro motivo, presentarse como una fractura patológica, encuadrarse en procesos sistémicos, etc.
Las alteraciones óseas en los estudios radiológicos se pueden identificar de múltiples formas. En el presente artículo, nos vamos a centrar en aquellas lesiones que aparecen como imágenes líticas, en la mayoría de los casos por patología tumoral o infecciosa. Vamos a estudiar cómo se debe interpretar la radiografía simple en la que aparecen, qué hallazgos radiológicos nos van a obligar a hacer un estudio más exhaustivo, o qué lesiones no será necesario que investiguemos. También, describiremos las lesiones óseas malignas más frecuentes en la infancia, sobre todo tumores primarios, sus formas de presentación y sus características radiológicas; así como otras lesiones óseas de interés.
La técnica de imagen inicial de elección para la valoración de la patología ósea es la radiografía simple, que nos va a permitir detectar la mayoría de lesiones y establecer un diagnóstico diferencial bastante preciso. En muchas ocasiones, va a ser el único procedimiento que realicemos. La resonancia magnética (RM) se emplea para caracterizar la lesión detectada mediante la radiología, determinar su extensión y la afectación de partes blandas, y dar información útil al traumatólogo de cara a la cirugía. La tomografía computarizada (TC) se reserva para los casos en los que se quiere estudiar la existencia de afectación cortical, reacción perióstica o guiar una biopsia percutánea.
Interpretación
Cuando se explora radiológicamente una estructura ósea es obligatorio obtener dos proyecciones ortogonales, esto es, perpendiculares entre sí, para no pasar por alto patología que puede quedar oculta con un solo plano. Debe estar centrada y bien colimada en la zona de interés, por lo que es fundamental aportar en los datos clínicos la mayor cantidad de información posible.
La radiografía debe estar correctamente realizada desde un punto de vista técnico, de calidad de imagen suficiente para hacer un diagnóstico con la menor dosis de radiación posible y seguir el principio ALARA(1).
Datos clínicos
Para la interpretación de una lesión ósea identificada en una radiografía es imprescindible tener en cuenta: la edad del paciente, la localización y características de la lesión en la imagen(2,3).
Otros datos que pueden orientar en el diagnóstico son la existencia de dolor, fiebre, antecedente neoplásico, analítica compatible con un proceso infeccioso, etc.
Edad (Fig. 1)
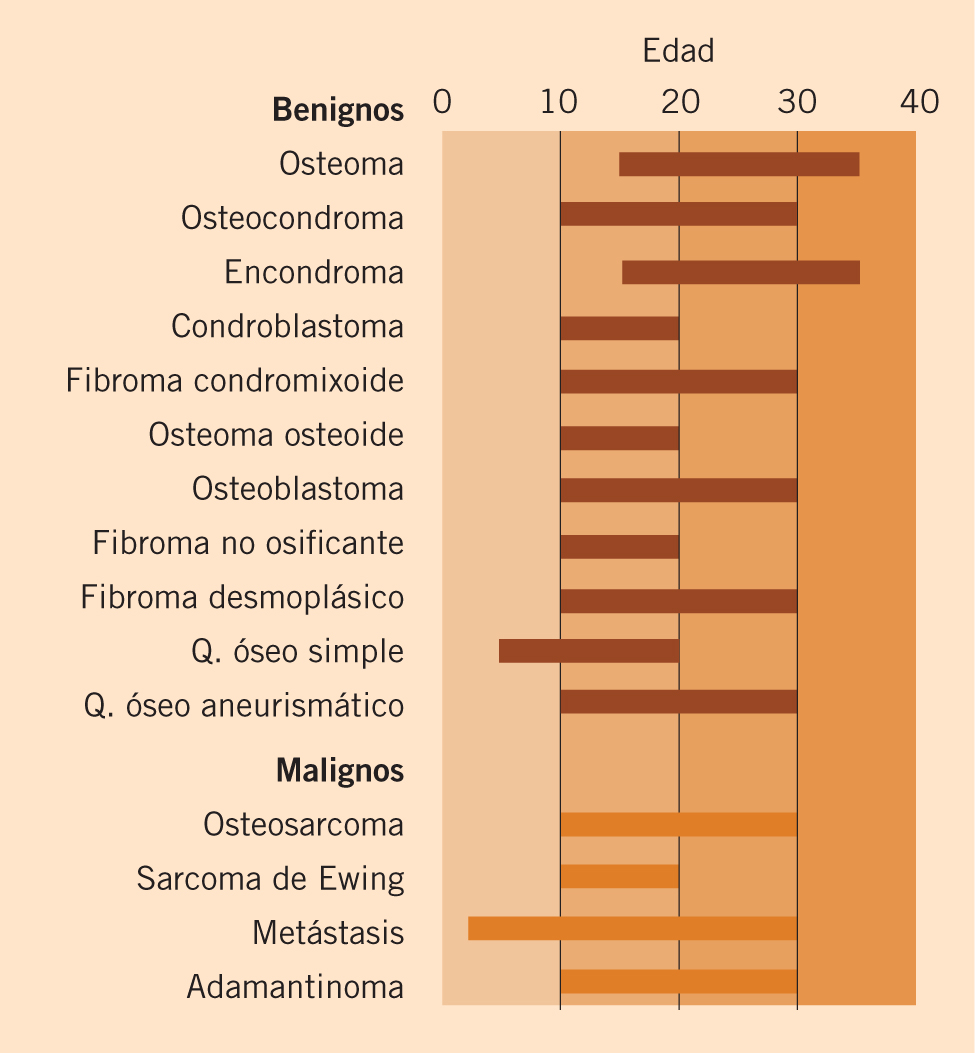
Figura 1. Esquema de la distribución por edades de las lesiones óseas benignas y malignas más frecuentes en menores de 40 años.
Es un dato fundamental para establecer un diagnóstico diferencial, la incidencia de muchas lesiones óseas varían con la edad. Existen lesiones exclusivas de la edad pediátrica, mientras que otras pueden aparecer tanto en niños como en adultos. Por ejemplo, el neuroblastoma metastásico es más frecuente en menores de 2 años; el osteosarcoma y el sarcoma de Ewing en menores de 30 años. El tumor de células gigantes no aparece en menores de 25 años, ya que ocurre cuando la fisis está cerrada. Entre la patología benigna que podemos ver en la edad pediátrica están: el granuloma eosinófilo, el quiste óseo aneurismático, el quiste óseo simple, el fibroma no osificante y el condroblastoma. Aunque también existe patología que puede presentarse a cualquier edad, como la displasia fibrosa o la osteomielitis(2-4).
El osteosarcoma y el sarcoma de Ewing son los tumores primarios malignos más frecuentes en la infancia, con un pico de incidencia entre los 10 y 25 años. Las metástasis óseas son infrecuentes en la edad pediátrica, a excepción, como se ha comentado anteriormente, del neuroblastoma metastásico(5).
Dolor
El dolor óseo en el niño es muy común y la causa suele ser obvia. Es necesario realizar una historia clínica y exploración física completa, no solo centrada en la zona del dolor, sino también se deben buscar síntomas y signos sistémicos. En determinadas ocasiones, se deberán hacer estudios de laboratorio y de imagen(6).
Cuando la causa del dolor no puede ser establecida por la historia clínica, la exploración física y la analítica, es preciso hacer un estudio de imagen de la zona afectada, inicialmente una radiografía simple. Tanto la patología maligna (osteosarcoma y sarcoma de Ewing) como benigna (osteomielitis, histiocitosis de células de Langerhans) pueden debutar como dolor óseo(7).
En algunos casos, como en el osteoma osteoide, el dolor presenta unas características especiales, ya que se produce, generalmente, por la noche y suele ceder con la ingesta de antiinflamatorios no esteroideos(3).
Otras lesiones son asintomáticas, como la displasia fibrosa, el encondroma, el fibroma no osificante y el quiste óseo solitario(3).
Valoración de la radiografía simple(3,4,8)
Lodwick, en la década de 1960, sistematizó la valoración de los tumores óseos, clasificó su morfología en función de la destrucción ósea, la reacción perióstica, la mineralización de la matriz tumoral y el tamaño y forma de la lesión(8).
Cuando se evalúa una patología ósea en la radiografía hay que estudiar:
• La cortical ósea, el periostio y las partes blandas.
• La densidad de la lesión: líticas, esclerosantes o mixtas; y la matriz tumoral.
• La localización y multiplicidad.
Cortical ósea
• Adelgazamiento cortical: festoneado endostal (como en el encondroma), agujeros intracorticales o reabsorción subperióstica.
• Engrosamiento cortical: en algunos casos, como en el osteoma osteoide o en la fractura de estrés, se produce una esclerosis reactiva perilesional.
• Fractura: se identifica una línea radiolucente sin esclerosis de sus márgenes.
• Expansión cortical: en las lesiones de crecimiento lento y continuo se produce una erosión endóstica progresiva con formación de hueso perióstico, lo que simula un “abombamiento” cortical. En las lesiones de crecimiento más rápido no da tiempo a la formación del neocórtex, por lo que su margen periférico es tan fino que no se identifica en la radiografía.
• Destrucción cortical: este signo se identifica en tumores malignos y en la osteomielitis, y se presenta de dos formas: agujero cortical, agujero de tamaño significativo con bordes irregulares; permeación cortical, la lesión atraviesa la cortical por múltiples perforaciones.
Periostio
Es una fina membrana que recubre la cortical del hueso que, cuando se ve agredida, reacciona formando hueso de distintas morfologías (Fig. 2):
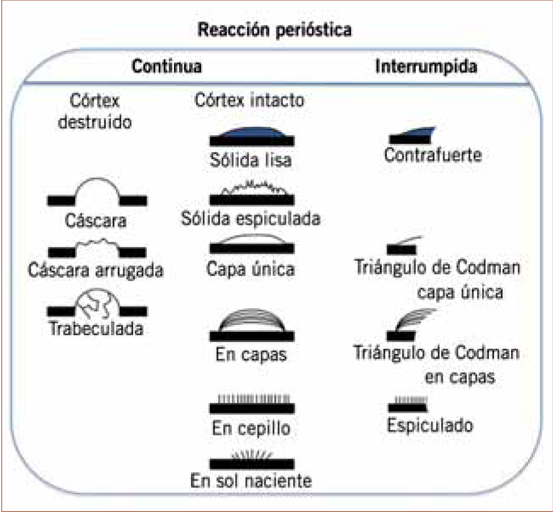
Figura 2. Esquema de los diferentes tipos de reacciones periósticas.
• Reacción perióstica sólida continua. Se aprecia una capa continua de hueso nuevo. Puede ser delgada (1-2 mm), gruesa (ondulante o elíptica densa) o en contrafuerte. Suele ser en procesos de evolución lenta, generalmente benignos, como el osteoma osteoide (reacción perióstica elíptica densa).
• Reacción perióstica discontinua. Se da en lesiones agresivas, tanto benignas (osteomielitis, granuloma eosinófilo, fracturas) como malignas (sarcoma de Ewing, osteosarcoma). Pueden ser “en capas de cebollas”, varias capas alternativas concéntricas radiotransparentes y radiopacas, en lesiones de crecimiento cíclico, como el sarcoma de Ewing. Espiculada, son espículas perpendiculares a la cortical como resultado de un crecimiento tumoral progresivo, en “patrón en sol naciente” (osteosarcoma) o “patrón en cepillo” (sarcoma de Ewing). Triángulo de Codman, el tumor destruye la cortical mediante un agujero y en su crecimiento los restos periósticos forman una estructura triangular en los bordes, aparece en lesiones de crecimiento rápido, como el osteosarcoma.
Partes blandas
La radiografía no permite valorar correctamente los tejidos blandos, ya que las estructuras musculares, tendinosas, vasculonerviosas o masas tumorales no calcificadas se identifican como densidad agua, indistinguibles entre sí. El desplazamiento u obliteración de las líneas grasas nos pueden poner sobre la pista de la existencia de una masa de partes blandas asociada a la lesión ósea.
Cuando nos encontramos una masa de partes blandas con afectación ósea, puede ser difícil determinar su origen, una ayuda es el epicentro de la lesión (fuera o dentro del hueso), la angulación de los bordes del agujero cortical (hacia fuera o hacia dentro del hueso) y la presencia de reacción perióstica en las lesiones óseas. Esta disyuntiva puede darse en lesiones agresivas, como en varios tipos de tumores malignos o en la osteomielitis.
Densidad de la lesión(3,8)
Pueden ser osteolíticas o esclerosas.
Cuando estudiamos una lesión lítica tenemos que introducir un concepto nuevo, el de zona de transición, la interfase entre el hueso sano y la lesión. En aquellas de crecimiento lento, el hueso es capaz de reaccionar rodeándolas, por lo que tienen bordes bien definidos (zona de transición estrecha entre la lesión y el hueso). En las de crecimiento rápido, al hueso sano no le da tiempo a formar una reacción frente a la lesión, presentan bordes mal definidos (zona de transición amplia). Según este concepto, Lodwick describió tres patrones básicos:
• Tipo I o patrón geográfico, área de destrucción completa del hueso con pérdida focal de la estructura y densidad óseas. Pueden ser con zona de transición estrecha (Tabla I) o amplia, y dependiendo de sus bordes se subdivide en:
– Tipo IA, bordes bien definidos escleróticos (zona de transición estrecha), generalmente benigna y de crecimiento lento.
– Tipo IB, bordes bien definidos no escleróticos (zona de transición estrecha).
– Tipo IC, bordes mal definidos (zona de transición amplia), orienta a lesiones agresivas, como el osteosarcoma o el sarcoma de Ewing.
• Tipo II o patrón apolillado, aparecen múltiples aéreas de destrucción ósea, de tamaño variable (2-5 mm), en lesiones de rápido crecimiento con una zona de transición amplia. Sugestivo de tumores malignos, aunque la osteomielitis o el granuloma eosinófilo pueden presentarse con este patrón.
• Tipo III o patrón permeativo, con múltiples áreas líticas de pequeño tamaño (menores de 2 mm), redondeadas, con una gran zona de transición, mal delimitada y con un margen casi imperceptible con el hueso sano. Un ejemplo de este patrón es el sarcoma de Ewing.
Las lesiones escleróticas siempre tienen una zona de transición estrecha independientemente de su agresividad, ejemplo de este tipo son el osteoma osteoide y el osteocondroma (exóstosis), o el osteosarcoma de tipo escleroso.
El patrón mixto, lítico-esclerótico, puede verse en la evolución de lesiones líticas benignas, como el fibroma no osificante, que llega a regresar espontáneamente. Durante la reparación de una fractura aparece un área de densidad mixta que evoluciona a un callo radiodenso, generalmente existe un antecedente traumático.
Matriz tumoral(3,8)
Ciertos tumores producen una sustancia extracelular mineralizada que se conoce como matriz, y que en algunos casos tiene una apariencia característica en la radiografía, de mucha utilidad para orientar el tipo histológico del tumor primario.
• Matriz osteoide: formación densa y amorfa de osteoide, con forma de calcificaciones algodonosas o de nubes, como en el osteosarcoma.
• Matriz cartilaginosa: son calcificaciones puntiformes, irregulares (en racimos o en palomitas de maíz) o curvilíneas (forma de comas, arcos o anillos). Patrón visualizado en tumores cartilaginosos como el encondroma o el osteocondroma.
• Matriz fibrosa: se identifica en la radiografía simple como un aumento uniforme de densidad, con un aspecto en vidrio deslustrado, y aparece en lesiones como la displasia fibrosa.
• Matriz grasa: es muy difícil de detectar mediante la radiología simple, para ello se requiere una TC. Se visualiza en el lipoma intraóseo.
Trabeculación(3)
En algunas lesiones se pueden identificar imágenes lineales densas en su interior, como en el quiste óseo aneurismático (trabéculas finas horizontales) o en el osteosarcoma telangiectásico.
Localización y multiplicidad(3,5,8)
Hay que valorar la distribución en el esqueleto, la localización en el hueso y si existe la posibilidad de encontrarnos varias lesiones en diferentes huesos.
En cuanto a la distribución de la patología ósea en la infancia, los tumores y las infecciones predominan en los huesos largos, alrededor de las rodillas y en el húmero proximal. Los tumores cartilaginosos en las manos y en los pies suelen ser benignos. El cordoma aparece en el clivus o el sacro. En la columna vertebral, los tumores malignos suelen presentarse en los cuerpos vertebrales; mientras que, los benignos lo hacen en los elementos posteriores, como el quiste óseo aneurismático o el osteoblastoma.
Un dato importante en el diagnóstico diferencial es la localización dentro del hueso (Tabla II), ya que refleja el sitio de mayor actividad celular. En la adolescencia, las zonas de mayor actividad son las metáfisis alrededor de la rodilla y en el húmero proximal; el osteosarcoma suele ser metafisario o metafisodiafisario, mientras que el sarcoma de Ewing es típicamente diafisario, aunque también puede originarse en la metáfisis. Otros tumores diafisarios son los originados en la médula ósea, como la leucemia, los linfomas, los neuroblastomas y los granulomas eosinófilos. Aunque hay que recordar que la patología tumoral que se desarrolla a partir de células de la médula ósea puede ocurrir a lo largo de todo el hueso. Las lesiones epifisarias en el niño son limitadas, podemos encontrarnos condroblastomas, abscesos (piógenos o tuberculosos) y, menos frecuentemente, osteomas osteoides, encondromas y granulomas eosinófilos.
La localización en el plano transversal también es de gran utilidad, pueden ser medular central, medular excéntrico, cortical o paraostal/yuxtacortical. Para determinar este hallazgo es fundamental, como se ha comentado anteriormente, realizar las exploraciones radiológicas en dos proyecciones ortogonales. También son de gran importancia la RM y la TC. Como ejemplos:
• Medular central: quiste óseo simple, displasia fibrosa, sarcoma de Ewing.
• Medular excéntrico: quiste óseo aneurismático.
• Cortical: osteoma osteoide, fibroma no osificante.
• Paraostal/yuxtacortical: osteocondroma, osteosarcoma paraostal.
Hay que tener en cuenta que lesiones que típicamente son excéntricas pueden aparecer centralmente cuando alcanzan un gran tamaño o el hueso afectado es de pequeño calibre.
Algunas lesiones tumorales, como los osteocondromas o la histiocitosis de células de Langerhans, pueden desarrollarse en varios huesos simultáneamente. También ocurre en la leucemia, el neuroblastoma metastásico o en la osteomielitis crónica recurrente multifocal.
Datos radiológicos de benignidad vs. malignidad(2,3)
La radiología simple en muchas ocasiones nos va a permitir determinar qué lesiones hay que ignorar o cuáles deben ser biopsiadas o tratadas, ya sea por sospecha de malignidad o por riesgo de producirse una fractura patológica.
En el estudio de las lesiones óseas no debemos emplear, en general, los términos de benignidad o malignidad, sino que debemos determinar la agresividad de la lesión. Como hemos comentado anteriormente, existen lesiones benignas, como la osteomielitis, que comparten características radiológicas de agresividad con la patología tumoral maligna.
A modo de resumen, las características radiológicas de baja agresividad son:
• Bordes bien definidos o esclerosos.
• Zona de transición estrecha.
• Ausencia de reacción perióstica o reacción perióstica sólida continua.
En contra, datos de agresividad son:
• Los bordes mal definidos de la lesión (tipo IC).
• Los patrones apolillado o permeativo.
• La destrucción cortical.
• La reacción perióstica discontinua (en capas de cebolla, espiculada o el triángulo de Codman).
• La presencia de masa de partes blandas.
Patología específica
Osteosarcoma(9,10)
Es el tumor óseo primario más frecuente en la infancia, sobre todo durante la pubertad, cuando ocurre un rápido crecimiento.
Histológicamente se trata de una neoplasia compuesta por células madre mesenquimales productoras de osteoide o hueso inmaduro. Se pueden clasificar de varias maneras, por la existencia de una enfermedad ósea previa, por el tipo histológico, o por la localización en el hueso. Así, el osteosarcoma clásico o convencional se origina del centro medular del hueso, mientras que los periostal y paraostal o yuxtacortical se producen en la superficie ósea. En este artículo nos vamos a referir, sobre todo, al osteosarcoma convencional, clásico o central.
• Osteosarcoma convencional, clásico o central (Figs. 3-5):

Figura 3. Radiografía de la rodilla derecha en la que se aprecia un osteosarcoma clásico situado en la metáfisis proximal de la tibia. Se observa una lesión lítica con formación de matriz tumoral en su interior (calcificaciones mal definidas), con destrucción cortical y con un pequeño componente de partes blandas (flecha).

Figura 4. Osteosarcoma en la metáfisis proximal del fémur, con una masa de partes blandas (flecha gruesa) y matriz tumoral (flecha fina).
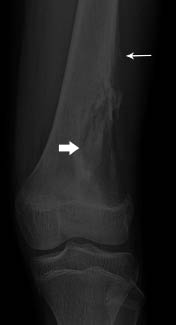
Figura 5. Osteosarcoma en la metáfisis proximal del fémur (flecha gruesa); lesión con signos de agresividad, destrucción cortical y reacción perióstica laminada discontinua tipo “triángulo de Codman” (flecha fina).
Edad: ocurre, fundamentalmente, en la 2ª-3ª década de la vida.
Género: más frecuentemente, en varones.
Clínica: dolor, tumefacción, limitación a la movilidad, calor y fiebre.
Localización: en metáfisis de los huesos largos (80%), fémur, tibia y húmero. El 50-75% de los casos en huesos de la rodilla. Menos frecuente en la diáfisis y excepcionales en la epífisis. La afectación rara de la columna suele ser en los cuerpos vertebrales.
Hallazgos radiológicos: lo habitual es un patrón mixto de osteólisis y osteoesclerosis. Aparece una lesión lítica agresiva metafisaria intramedular, mal definida, con rotura cortical y una gran masa de partes blandas. Formación de matriz ósea en forma de focos de esclerosis. Con reacciones periósticas agresivas, como el triángulo de Codman o el espiculado en “sol naciente”. Pueden extenderse a epífisis y a diáfisis.
• Osteosarcoma telangiectásico. Se trata de un tipo histológico especial, con unas peculiaridades en la imagen, ya que presentan unas cavidades quísticas llenas de sangre.
Como en el osteosarcoma convencional, asienta en las metáfisis de los huesos tubulares, más frecuentemente en el fémur.
Se visualiza como una lesión lítica, expansiva, grande, sin formación de hueso perióstico, con masa de partes blandas. En la RM se pueden identificar unas cavidades quísticas con niveles líquido-líquido, parecidas a las que se aprecian en el quiste óseo aneurismático.
El osteosarcoma plantea el diagnóstico diferencial con el sarcoma de Ewing, lo fundamental es detectar los datos de agresividad de ambas entidades para no pasarlas por alto; y la osteomielitis.
Otras técnicas de imagen, como la TC y la RM, se utilizan para estudiar la extensión, la relación con estructuras neurovasculares vecinas y la respuesta al tratamiento, o realizar una biopsia guiada con TC.
Sarcoma de Ewing(7,9,10) (Figs. 6 y 7)

Figura 6. Lesión lítica permeativa en el radio, con destrucción cortical en forma de pequeños agujeros (punta de flecha), metafisodiafisaria distal, con una fractura asociada (flecha). Sarcoma de Ewing de localización poco habitual.
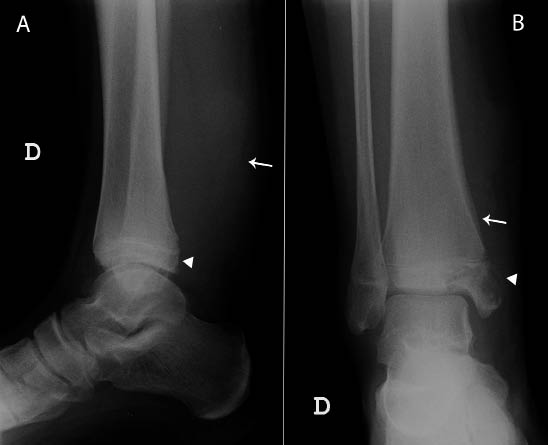
Figura 7. Radiografía lateral (A) y anteroposterior (B) del extremo distal de la pierna derecha, se aprecia una lesión ósea metafisoepifisaria tibial distal, con destrucción cortical (punta de flecha en A y B), reacción perióstica sólida lisa (flecha en B) pero con un gran componente de partes blandas (flecha en A), que se corresponde con un sarcoma de Ewing.
Es el segundo tumor óseo primario de la infancia. Es una neoplasia formada por células redondas, pequeñas y azules, originadas de células de la cresta neural.
Edad: el 95% de los casos ocurren entre los 5 y los 30 años.
Clínica: similar al osteosarcoma, con dolor, tumefacción, fiebre, pérdida de peso, anemia y leucocitosis.
Localización: característicamente, en huesos de la mitad inferior del cuerpo, en huesos largos de las extremidades inferiores, seguidos de la pelvis y columna. En orden de frecuencia: fémur, ilion, tibia, húmero, peroné y costillas. En los huesos tubulares es metafisodiafisario o diafisario. En la columna predomina la afectación sacra y de los cuerpos vertebrales. En el tórax asienta, fundamentalmente, en las costillas.
Hallazgos radiológicos: reflejan la agresividad de este tipo de neoplasia. Puede presentarse como una lesión lítica intramedular mal definida, con un patrón permeativo o apolillado, y con destrucción cortical; también como una lesión mixta lítica-esclerótica o predominantemente esclerótica. A menudo con reacción perióstica agresiva discontinua laminada en capas o espiculada en cepillo. Asocia gran masa de partes blandas. Al contrario que en el osteosarcoma, no es frecuente la formación de matriz tumoral.
La RM se emplea para determinar su extensión, tamaño y relaciones con las estructuras vecinas.
El diagnóstico diferencial se debe hacer con el osteosarcoma, el linfoma y con la osteomielitis.
Osteomielitis(7) (Figs. 8 y 9)
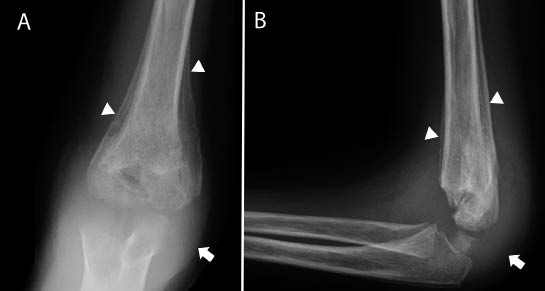
Figura 8. Radiografía anteroposterior (A) y lateral (B) del codo derecho, con una lesión lítica en el extremo distal del húmero, que presenta una importante reacción perióstica en capas (puntas de flechas), en relación con una osteomielitis que asocia una artritis de la articulación del codo (flechas).
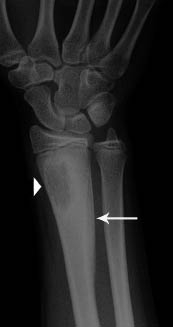
Figura 9. Lesión lítica en la metáfisis distal del radio derecho (punta de flecha) con reacción perióstica en capas (flecha), que se corresponde con una osteomielitis.
En los niños suele ser de origen hematógeno. Clínicamente, puede ser difícil de diagnosticar, en los niños pequeños se puede manifestar como cojera o dolor al movimiento pasivo, con fiebre, leucocitosis y proteína C reactiva (PCR) elevada, aunque en algunos casos puede ser normal. El hemocultivo es positivo solo en un 32-60% de los casos. El cultivo del aspirado del hueso afectado puede ser negativo en un 40-60%. El microorganismo más frecuente es el Staphylococcus aureus, seguido por el estreptococo beta hemolítico, el Streptococcus pneumoniae, la E. coli y la Pseudomona aeruginosa.
Puede ser aguda, subaguda o crónica. En un solo hueso o multifocal.
Suele afectar a las metáfisis de los huesos largos, sobre todo al fémur distal y a la tibia proximal, como el osteosarcoma.
En las primeras fases, la radiografía puede ser normal o sólo apreciarse edema en las partes blandas adyacentes a la metáfisis afectada. Se evidencia destrucción ósea y reacción perióstica a las 2-3 semanas. La destrucción suele ser de aspecto moteado, mal definida, con diferentes grados de pérdida cortical y, generalmente, en las metáfisis. Las reacciones periósticas pueden ser laminadas, en “capas de cebollas”, espiculadas o como un “triángulo de Codman”.
En la osteomielitis subaguda o crónica se puede formar un absceso de Brodie en la metáfisis, con un tamaño entre 1 y 4 cm. Radiológicamente, se visualiza como una lesión lítica redondeada u ovalada con esclerosis periférica, con una zona de transición estrecha y bien definida, al contrario de lo que ocurre en la osteomielitis aguda.
Histiocitosis de células de Langerhans(7,11,12)
Esta entidad se considera que puede manifestarse de tres formas distintas: el granuloma eosinófilo, la más leve, como lesiones óseas líticas únicas o múltiples, de curso benigno con un 100% de supervivencia con mínimo o ningún tratamiento; la enfermedad de Hand-Schüller-Christian, la más variada, crónica; y la enfermedad de Letterer-Siwe, aguda, que puede afectar a cualquier órgano y tiene peor pronóstico.
Las tres entidades tienen en común que, histológicamente, se encuentran células histiocíticas específicas (células de Langerhans) que contienen cuerpos citoplásmicos de inclusión.
El pico de incidencia es entre uno y cuatro años, aunque su presentación puede ser a cualquier edad.
El hueso es el órgano que más frecuentemente se afecta, y la mayoría de los casos se manifiestan como una lesión ósea solitaria, con predilección por los huesos planos, siendo la localización más frecuente el cráneo, seguida por la pelvis, la columna vertebral, la mandíbula y las costillas. Es la causa más frecuente de vértebra plana en la infancia. En un tercio de los casos se pueden afectar los huesos largos, sobre todo el fémur, el húmero y la tibia. En estos la localización más habitual es la diáfisis (58%) seguida por la metáfisis.
Los pacientes se presentan con edema y/o dolor que, inicialmente, solo es por la noche. La afectación vertebral puede tener un componente de partes blandas que, en ocasiones, puede dar síntomas neurológicos.
En cuanto a los estudios de imagen, la mejor técnica es la radiología simple; de hecho, cuando se sospecha o confirma esta entidad, es imprescindible realizar una serie ósea para descartar una afectación múltiple. La TC es muy útil para valorar las lesiones que afectan a los huesos planos, sobre todo la base del cráneo que, por su complejidad anatómica, es muy difícil de evaluar con radiología simple. La RM se utiliza para la evaluación de los huesos largos, el cráneo y el sistema nervioso central.
Los hallazgos radiológicos pueden variar dependiendo de la fase de la enfermedad. En la fase aguda, en el cráneo y en la pelvis aparecen como áreas líticas bien definidas sin esclerosis marginal. En los huesos largos se pueden presentar con rasgos de agresividad, como lesiones líticas con un patrón permeativo de márgenes mal definidos, similar al sarcoma de Ewing o a la osteomielitis. En ocasiones, el interior de la lesión puede tener un fragmento de hueso intacto conocido como secuestro, que lo diferencia de procesos malignos. Pueden evolucionar hacia la curación con bordes esclerosos bien definidos o progresar con un festoneado endostal, erosión cortical, reacción perióstica y masa de partes blandas. En la fase crónica, las lesiones son más definidas, con esclerosis reactiva alrededor, que puede ser un signo de curación y de buen pronóstico.
En el cráneo, las lesiones se suelen localizar en el díploe, son redondeadas u ovaladas con márgenes bien definidos, denominadas lesiones en sacabocados (Fig. 10). Cuando se afecta de forma desigual las tablas interna y externa dan un aspecto biselado. Cuando el secuestro aparece en el interior de una lesión craneal se le ha llamado “secuestro en botón”, que en niños también se puede dar en procesos infecciosos, quistes dermoides y epidermoides, necrosis por radiación y curación de un defecto quirúrgico. La reacción perióstica está ausente en lesiones que afectan a la bóveda craneal.
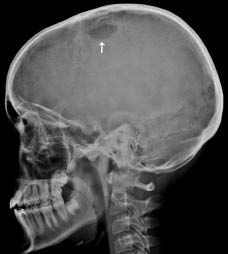
Figura 10. Lesión lítica en el díploe craneal (flecha), bien definida, de bordes no esclerosos, en relación con histiocitosis de células de Langerhans.
Cuando asienta en la mandíbula o en el hueso maxilar, se produce una destrucción del hueso alveolar, y da una apariencia de “diente flotante”.
En la columna espinal existe una predilección por los cuerpos vertebrales torácicos, seguidos por los lumbares y cervicales. La afectación de los elementos posteriores es menos frecuente. Generalmente se manifiesta como una vértebra plana (Fig. 11) y, en ocasiones, como un acuñamiento anterior del cuerpo vertebral. En la TC y la RM se puede identificar el componente de partes blandas epidural que puede asociarse a estas lesiones. La recuperación total o parcial de la altura del cuerpo vertebral suele ser la tónica habitual en la curación de una vértebra plana, de modo que los déficit neurológicos generalmente se resuelven según se produce la curación ósea.
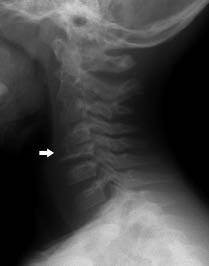
Figura 11. “Vértebra plana” (flecha), como manifestación de una histiocitosis de células de Langerhans (granuloma eosinófilo).
Osteoma osteoide(10)
Es un tumor osteoblástico benigno, que aparece frecuentemente entre los 7 y los 25 años, generalmente en varones. Se manifiesta característicamente como dolor óseo nocturno que mejora con los salicilatos. Puede acompañarse de edema e inflamación de partes blandas.
El hueso que más se afecta es el fémur, seguido de la tibia, entre ambos suman el 50% del total de casos. Habitualmente, asienta en la diáfisis de los huesos largos, aunque puede extenderse a la metáfisis. Cuando aparece en las vértebras, suele ser en los elementos posteriores, sobre todo, en las lumbares.
Radiológicamente, se visualiza como una lesión lítica ovalada o redondeada rodeada por una zona de esclerosis. En los huesos largos aparece típicamente en la cortical ósea como un área radiolúcida de pequeño tamaño, habitualmente menor de un centímetro, con esclerosis y engrosamiento de la cortical que lo rodea. El “nidus” o lesión lítica puede ser uniformemente radiolucente o presentar calcificaciones en su interior, y suele localizarse en el centro de la zona esclerótica (Fig. 12). Se diferencia de las fracturas de estrés en que estas suelen ser lineales, y del osteoblastoma en que este generalmente es de mayor tamaño.
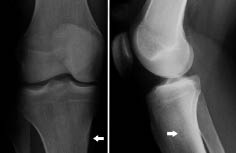
Figura 12. Radiografía anteroposterior (A) y lateral (B) de la rodilla derecha, en la que se aprecia un osteoma osteoide en la metáfisis proximal de la tibia (flecha), como una lesión lítica cortical, menor de 1 cm, y con una pequeña calcificación en su interior (en B).
En los huesos del carpo, tarso o epífisis de los huesos largos, se localiza en el hueso esponjoso como una lesión bien delimitada, parcial o totalmente calcificada. Si aparece cuando un núcleo de osificación no está del todo desarrollado, puede producir una alteración en el crecimiento normal de la fisis.
En la columna vertebral suelen producir dolor intenso, por la noche y con los movimientos, a menudo acompañado de escoliosis. La lesión se localiza en el lado cóncavo de la curva. Se puede apreciar esclerosis de los pedículos, las láminas, los procesos articulares y, menos frecuentemente, de los procesos transversos o espinosos.
Como mejor se identifica el nidus es con la TC o la RM.
Fibroma no osificante y defecto fibroso cortical(10,13)
Son lesiones óseas frecuentes, histológicamente similares. Ambos términos se usan indistintamente, aunque el primero se aplica más correctamente a las lesiones mayores sintomáticas y, el segundo, a alteraciones más pequeñas y asintomáticas.
Pueden manifestarse como una fractura patológica o ser un hallazgo incidental en una radiografía simple.
Suelen aparecer como lesiones líticas en la cortical de la metáfisis de los huesos largos, fémur y tibia, fundamentalmente, a poca distancia de la fisis. Tienen una morfología ovalada o esférica, son bien definidas, sin reacción perióstica (Fig. 13). Las lesiones de mayor tamaño son más alargadas y de aspecto lobulado, pueden tener adelgazamiento o expansión cortical.

Figura 13. Lesión lítica cortical de borde escleroso y festoneado, en la metáfisis proximal del fémur izquierdo (flecha), compatible con un defecto fibroso cortical.
Por los hallazgos radiológicos específicos no es necesario hacer otros métodos de imagen. Y por su historia natural no se realiza ninguna medida terapéutica, ya que suele seguir una secuencia: inicialmente puede aumentar, luego migrar en dirección a la diáfisis, disminuir, desarrollar un borde esclerótico y, finalmente, desaparecer.
Bibliografía
1. Frush DP, Frush KS. The ALARA concept in pediatric imaging: building bridges between radiology and emergency medicine: consensus conference on imaging safety and quality for children in the emergency setting, Feb. 23-24, 2008, Orlando, FL – Executive Summary. Pediatr Radiol. 2008; 38(Suppl 4): S629-32.
2. Wyers MR. Evaluation of pediatric bone lesions. Pediatr Radiol. 2010; 40: 468-73.
3. Berná Mestre JD, Puerta Sales A, Berná Serna JD. Principios de interpretación radiológica en el aparato locomotor. En: Cura JL del, Pedraza S, Gayete A, eds. Radiología Esencial. Madrid: Ed. Médica Panamericana; 2009. p. 721-7.
4. Balach T, Stacy GS, Peabody TD. The clinical evaluation of bone tumors. Radiol Clin North Am. 2011; 49: 1079-93.
5. Davies AM. Imaging in skeletal paediatric oncology. Eur J Radiol. 2001; 37: 79-94.
6. Junnila JL, Cartwright VW. Chronic musculoskeletal pain in children: part I. Initial evaluation. Am Fam Physician. 2006; 74: 115-22.
7. McCarville MB. The child with bone pain: malignancies and mimickers. Cancer Imaging. 2009; 9: S115-21.
8. Hwang S, Panicek DM. The evolution of musculoskeletal tumor imaging. Radiol Clin North Am. 2009; 47: 435-53.
9. Kaste SC. Imaging pediatric bone sarcomas. Radiol Clin North Am. 2011; 49: 749-65.
10. Resnick D, Greenway GD. Tumores y lesiones seudotumorales de los huesos: imágenes y anatomopatología de las lesiones específicas. En: Resnick D, ed. Huesos y articulaciones en imagen. Madrid: Marbán; 2001. p. 991-1063.
11. Resnick D. Lipidosis, histiocitosis e hiperlipoproteinemias. En: Resnick D, ed. Huesos y articulaciones en imagen. Madrid: Marbán; 2001. p. 615-20.
12. Azouz EM, Saigal G, Rodríguez MM, Podda A. Langerhans´ cell histiocytosis: pathology, imaging and treatment of skeletal involvement. Pediatr Radiol. 2005; 35: 103-15.
13. Vanel D. The incidental skeletal lesion: ignore or explore? Cancer Imaging. 2009; 9: S38-43.



