 |
| Temas de FC |
B. Rosich del Cacho*, Y. Mozo del Castillo**
*Médico adjunto, Servicio de Pediatría, Hospital Universitario Joan XXIII, Tarragona. **Médico adjunto, Servicio de Hemato-Oncología Pediátrica y Trasplante de Progenitores Hematopoyéticos, Hospital Universitario La Paz, Madrid
| Resumen
La anemia se define como una reducción de la concentración de la hemoglobina por debajo de los niveles considerados normales para la edad, sexo y raza. Es el resultado de un desequilibrio entre la producción y la destrucción de hematíes, que caracteriza o acompaña a diferentes patologías. Se trata del problema hematológico más frecuente en la infancia, cuya causa principal es la ferropenia. Con frecuencia, las manifestaciones clínicas son inespecíficas. El diagnóstico comienza con: un hemograma, el frotis de sangre periférica y los parámetros bioquímicos de hemólisis y del metabolismo del hierro. Se revisa la aproximación diagnóstica general del niño con anemia, proponiendo un enfoque basado en un algoritmo a partir de los datos hematológicos básicos. Finalmente, se aporta un breve listado de referencias bibliográficas básicas. |
| Abstract
Anemia is defined as a reduction in hemoglobin concentration below normal levels for age, gender and ethnicity. It is the result of an imbalance between the production and destruction of red blood cells, which characterizes or accompanies various conditions. It is the most common hematological abnormality in childhood, the main cause of which is iron deficiency. Clinical manifestations are often nonspecific. Diagnosis begins with a full blood count, peripheral blood smear and biochemical parameters of hemolysis and iron metabolism. The overall diagnostic approach of the child with anemia is here reviewed, and an algorithm is proposed based on basic hematological data. Finally, a brief list of references is provided. |
Palabras clave: Anemia; Niño; Lactante; Clasificación; Diagnóstico.
Key words: Anemia; Child; Infant; Classification; Diagnosis.
Pediatr Integral 2021; XXV (5): 214 – 221
Anemias. Clasificación y diagnóstico
Introducción
La anemia se define como la reducción de la concentración de hemoglobina o de hematocrito, cuyas cifras normales dependen de la edad, sexo y raza. La anemia ferropénica es el trastorno hematológico más prevalente de la infancia.
En este capítulo, se revisan los conceptos generales de la anemia en la infancia y su abordaje diagnóstico. La anemia ferropénica (causa más frecuente de anemia en Pediatría) y las anemias hemolíticas se tratan de forma específica en otros capítulos.
Definición(1,2)
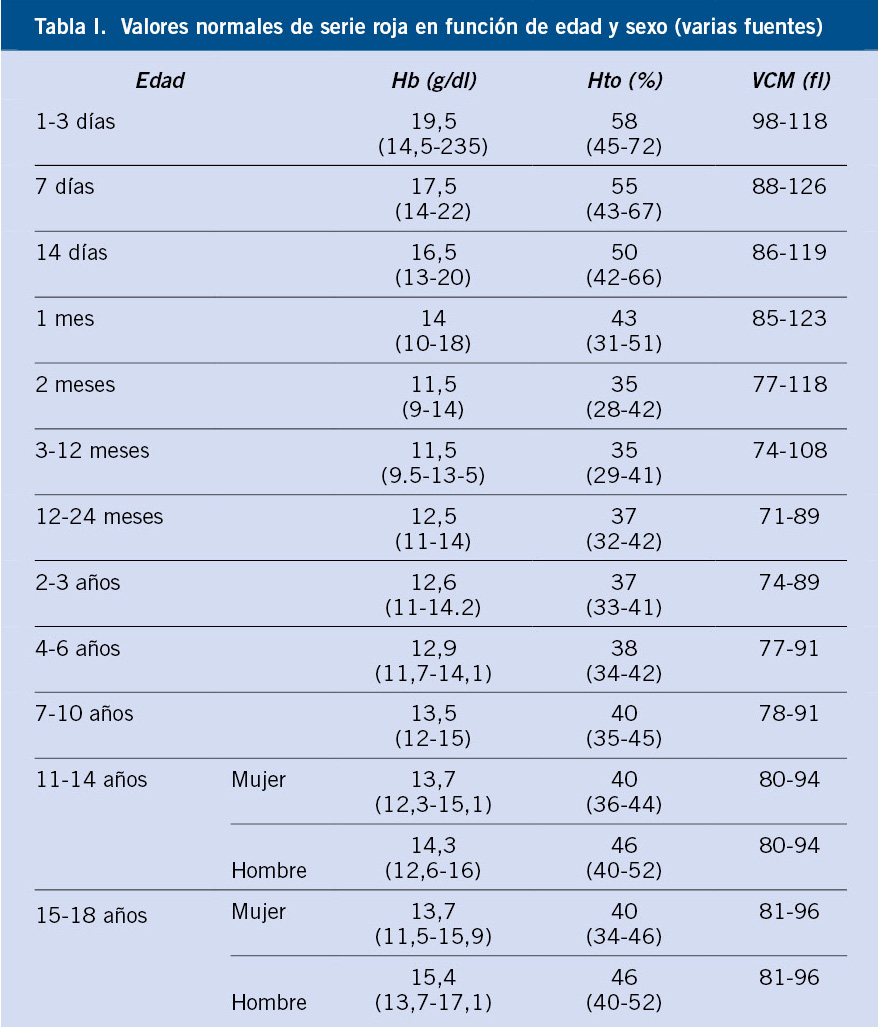
De origen griego, la palabra anemia significa “sin sangre”. Se define como la reducción de la concentración de hemoglobina (Hb), masa eritrocitaria o hematocrito en sangre periférica por debajo de 2 desviaciones estándar (-2DE) para la edad, sexo y raza del paciente (Tabla I).
• Hemoglobina (Hb): proteína compleja constituida por grupos hemo que contienen hierro y una porción proteica, la globina. La concentración de este pigmento eritrocitario se presenta en gramos (g) por 100 ml (dl) de sangre completa.
• Hematocrito (Hto): fracción del volumen de la masa eritrocitaria respecto del volumen total sanguíneo. Se expresa como porcentaje (%).
Epidemiología(2-4,7)
La anemia constituye el trastorno hematológico más frecuente en la edad pediátrica. En 2008, la Organización Mundial de la Salud (OMS) publicó los resultados de una encuesta de 192 estados miembros, estableciendo los siguientes umbrales de Hb por grupos de edad:
• 11 g/dl en niños de 0,5-4,99 años (edad preescolar).
• 11,5 g/dl entre los 5-11,99 años.
• 12 g/dl a los 12-14,99 años.
La prevalencia mundial de anemia fue del 47,4% ([IC95] 45,7-49,1) en niños de edad preescolar y 25,4% ([IC95] 19,9-30,9) en niños en edad escolar. La prevalencia en preescolares varió ampliamente según el país, encabezada por los países de América del Sur y África. Esto se debe a que la ferropenia supone el 50% de esa prevalencia y está íntimamente ligada a las carencias nutricionales, por tanto, a las condiciones sociales y de desarrollo en esos países.
Además de tener claro que el déficit de hierro es la causa más frecuente de anemia en la edad pediátrica a nivel mundial, debemos tener en cuenta los factores y las causas de este trastorno que influyen en su prevalencia:
• Edad: la cifra de Hb y Hto varía a lo largo de la infancia (Tabla I), así como las causas de anemia difieren según la edad de los pacientes:
- Nacimiento-3 meses: la Hb es máxima (16,5-18,5 g/dl) en el recién nacido y desciende hasta 9-10 g/dl entre las 6-9 semanas de vida, como consecuencia del incremento de la oxigenación de los tejidos y un descenso drástico de la eritropoyesis; es lo que se denomina “anemia fisiológica del lactante”. Toda anemia en este grupo de edad que difiera de las características de la anemia fisiológica (Hb < 9 g/dl, anemia antes del mes de vida o signos de hemólisis) requerirá un estudio más exhaustivo.
- 3-6 meses: durante este periodo es poco frecuente la ferropenia, siendo preciso descartar hemoglobinopatías.
- 6 meses-adolescencia: existen diferencias en las cifras de Hb según edad y sexo (Tabla I). Durante toda esta etapa, la principal causa de anemia es la ferropenia.
• Sexo: a partir de la pubertad, la secreción de testosterona induce un incremento de la masa eritrocitaria, por lo que la cifra normal de Hb es mayor en el varón que en la mujer. Por otra parte, algunas anemias hereditarias son ligadas al cromosoma X, siendo más frecuentes en varones (p. ej.: deficiencia de glucosa-6-fosfato deshidrogenasa (G6PDH) y anemia sideroblástica).
• Raza y etnia: se observan cifras normales de Hb con alrededor de 0,5 g/dl menos en niños negros respecto a las observadas en caucásicos o asiáticos. Las HbS y HbC son más frecuentes en población negra e hispana. Además, dentro de un mismo país existen áreas de mayor prevalencia de hemoglobinopatías, parásitos endocelulares, como la malaria e infestación con parásitos intestinales que impactan sobre la prevalencia de anemia. Así, los síndromes talasémicos tienen mayor prevalencia en el litoral mediterráneo, gran parte de África, Oriente Medio, subcontinente indio y sureste asiático; en cambio, el déficit de G6PDH se objetiva, sobre todo, en áreas endémicas de paludismo, ya que parece suponer un factor protector frente a esta infección (mayor prevalencia entre: judíos kurdos, sardos, nigerianos, afroamericanos, filipinos y griegos).
• Altura sobre el nivel del mar: a mayor altura sobre el nivel del mar, mayor cifra de Hb, ya que el menor contenido de oxígeno en el aire resulta en un estímulo para la hematopoyesis.
Fisiopatología(2,5)
La anemia es el resultado del desequilibrio entre producción y pérdida de hematíes. La redistribución de la sangre, el estímulo de la eritropoyesis y la disminución de la afinidad de la Hb por el O2, son mecanismos compensatorios.
La eritropoyesis se desarrolla fundamentalmente en la médula ósea durante la vida post-natal y adulta (en el periodo fetal y hasta los 6 meses de vida extrauterina participan también el seno endodérmico, donde se inicia a las 3-4 semanas de gestación, y el hígado, posteriormente). Son diversos factores reguladores (el principal, la saturación de oxígeno en sangre) los que actúan sobre las células peritubulares de los riñones dedicadas a la síntesis de eritropoyetina (EPO), hormona que actúa sobre los precursores hematopoyéticos de la médula ósea, que finalmente dan lugar a los hematíes maduros. Durante este proceso complejo de diferenciación y maduración hasta la producción del eritrocito maduro, se requiere también la participación de diferentes moléculas, factores de crecimiento (G y GM-CSF), oligoelementos (como el hierro, fundamental para la elaboración del grupo hemo de la Hb, el cobre y el zinc) y citoquinas (IL 1, 3, 4, 6, 9 y 11).
Los eritrocitos maduros tienen forma de disco bicóncavo, en su interior están llenos de Hb y están desprovistos de mitocondrias u otros orgánulos. La Hb, compuesta de 4 subunidades de globina y grupos hemo, está implicada en el intercambio de oxígeno y dióxido de carbono en todo el cuerpo.
Después de que los eritrocitos han estado en circulación durante un periodo prolongado (vida media 120 días), son captados y destruidos por el sistema retículo-endotelial del bazo. Para mantener unos niveles de Hb normales, debe existir un equilibrio entre la pérdida continua de los eritrocitos senescentes y la eritropoyesis en la médula ósea. Por tanto, la anemia es el resultado del desequilibrio entre producción (disminuida) y destrucción o pérdida de hematíes (aumentada).
Existen distintos mecanismos de compensación como respuesta adaptativa a la situación de anemia:
• Redistribución del flujo sanguíneo: garantiza la oxigenación de los órganos vitales (cerebro y miocardio), con la consiguiente vasoconstricción en zonas menos necesitadas, como piel y riñón.
• Estímulo de la eritropoyesis: mediado por un aumento de la síntesis de EPO, cuyo principal desencadenante es la hipoxia tisular. Este mecanismo solo es efectivo si la médula ósea es capaz de responder con el aumento de la producción de hematíes y el consiguiente aumento de reticulocitos en sangre periférica.
• Aumento de la capacidad de la Hb para ceder oxígeno a los tejidos: a través de un aumento de la concentración de 2,3-difosfoglicerato, que disminuye la afinidad de la Hb por el O2 y favorece la oxigenación de los tejidos.
Entender todo ello, ayudará a comprender las manifestaciones clínicas y la clasificación fisiopatológica de las anemias, que se explican en los siguientes apartados.
Manifestaciones clínicas(4,6)
La anemia puede tener tanto manifestaciones clínicas inespecíficas como síntomas y signos guía para el diagnóstico etiológico.
El cuadro clínico del síndrome anémico tiene unas manifestaciones comunes determinadas por: los mecanismos de adaptación, la edad de aparición, la enfermedad subyacente y la forma de instauración (aguda o crónica):
• Palidez de piel y mucosas: consecuencia directa del descenso de Hb y la vasoconstricción periférica que acompaña. En ocasiones, la palidez no se hace evidente hasta que la cifra de Hb desciende por debajo de 8 g/dl y puede ser difícil de apreciar según sea la pigmentación de la piel.
• Síntomas y signos cardiocirculatorios (palpitaciones, taquicardia, soplo sistólico, disnea de esfuerzo y taquipnea): en general, obedecen a la puesta en marcha de los mecanismos compensatorios por el descenso de volemia, y son más evidentes cuanto mayor sea el grado de anemia y la rapidez de su instauración.
• Síntomas generales (cefalea, irritabilidad, cambios de humor, astenia, anorexia): debidos a la hipoxia tisular. En las anemias crónicas, además puede haber repercusión en otros órganos, dando lugar a: disfunción neurológica (alteración del desarrollo psicomotor, dificultad de aprendizaje), retraso puberal, osteopenia, alteraciones cardiológicas (hipertrofia ventricular izquierda que puede llegar a insuficiencia cardiaca), etc.
• Síntomas acompañantes: derivados de las causas y mecanismos patogénicos implicados, como por ejemplo:
- Anemias hemolíticas: ictericia, coluria, dolor abdominal, esplenomegalia (por el papel del bazo en la destrucción de eritrocitos) o hepatoesplenomegalia (por eritropoyesis extramedular), litiasis biliar y alteraciones óseas (por eritropoyesis extramedular).
- Anemias carenciales: trastornos tróficos de piel y mucosas.
- Anemias de origen central (medular): sangrados e infecciones si asocian trombopenia y leucopenia.
Diagnóstico(2,7-9)
Una adecuada anamnesis y exploración física, el hemograma con índices eritrocitarios, reticulocitos, frotis de sangre periférica y bioquímica, son herramientas rentables para el enfoque diagnóstico de la anemia.
Anamnesis
Una adecuada historia clínica es el punto de partida para el diagnóstico etiológico de la anemia. Además de prestar atención a la edad, género, raza y procedencia geográfica del paciente, se debe interrogar sobre los siguientes:
• Síntomas (v. apartado anterior): inicio y velocidad de instauración, tolerancia, historia de sangrados (digestivos, menstruales, etc.), síntomas sugestivos de hemólisis, etc.
• Antecedentes neonatales: edad gestacional, grupo sanguíneo, historia de hospitalización por ictericia/anemia, resultados de cribado neonatal de enfermedades endocrino-metabólicas (en España, incluye la anemia de células falciformes).
• Antecedentes patológicos: episodios previos de anemia y su tratamiento, presencia de coagulopatía, enfermedades concomitantes (infecciosas y/o inflamatorias), problemas malabsortivos (p. ej., enfermedad celiaca).
• Antecedentes familiares: la existencia de historia de: anemia, ictericia, litiasis biliar, esplenomegalia o necesidad de colecistectomía en familiares, puede orientar hacia el diagnóstico de anemias hemolíticas hereditarias.
• Dieta: orientada a considerar posibles déficits nutricionales (hierro, vitamina B12 y ácido fólico). Es importante documentar el tipo de lactancia, la cantidad y la posibilidad de suplementos/fortificación. La presencia de pica puede orientar a déficit de nutrientes. A tener en cuenta que la ingesta de determinados alimentos (p. ej.: habas) puede desencadenar crisis hemolíticas en el déficit de G6PDH.
• Exposición a fármacos/tóxicos: medicaciones (antibióticos, antiinflamatorios, anticomiciales), hierbas, productos homeopáticos, agua potable con nitratos, oxidantes o productos con plomo.
Exploración física
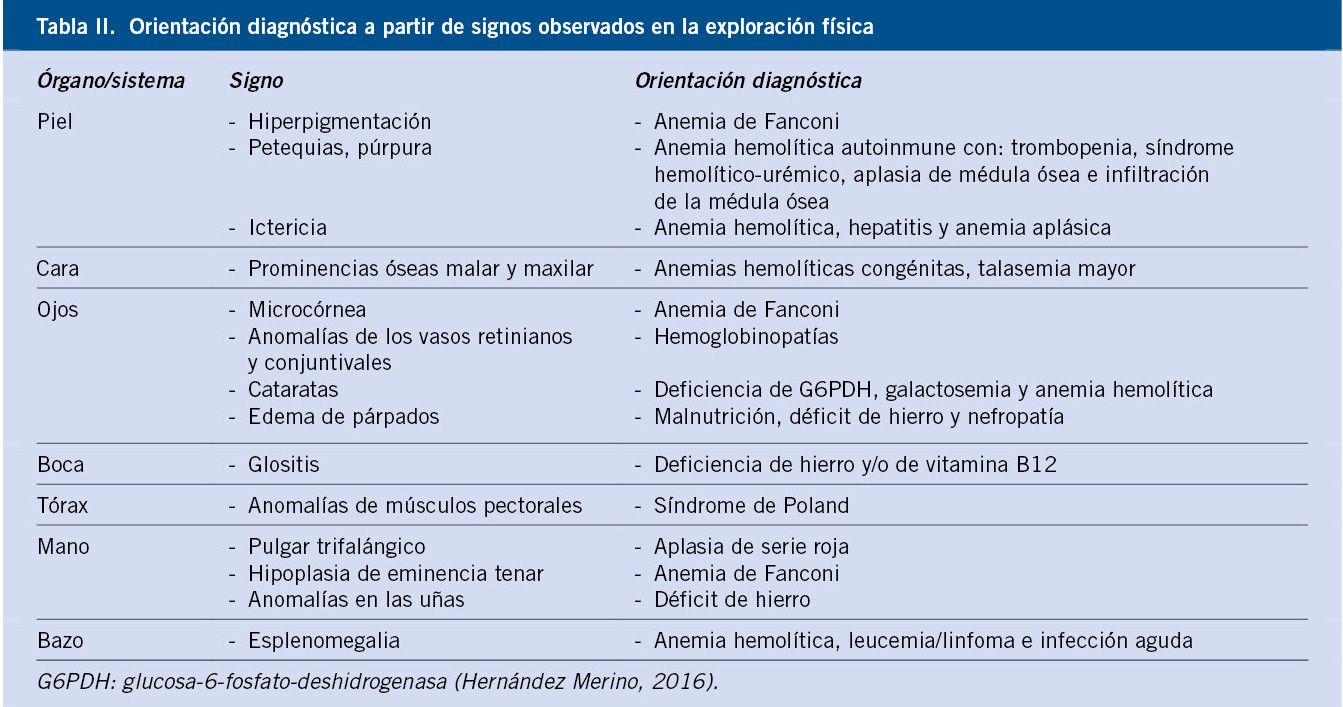
Debe prestarse especial atención a: piel, ojos, boca, facies, tórax, manos y abdomen. La palidez cutánea es un dato específico, pero poco sensible; también lo es la taquicardia, como manifestación de gravedad. La ictericia y la hepatoesplenomegalia, características de la hemólisis, son igualmente datos específicos, pero con relativa escasa sensibilidad.
En la tabla II, se exponen algunos signos físicos con capacidad para orientar hacia una causa determinada de anemia.
Pruebas complementarias
Las pruebas complementarias deben comenzar por un hemograma con índices eritrocitarios y un exhaustivo examen del frotis de sangre periférica. Además, los estudios de primer nivel precisan de: recuento reticulocitario, bioquímica básica y estudio de metabolismo del hierro.
En cualquier estudio de anemia, deberemos tener en cuenta los siguientes parámetros del hemograma, que ayudarán en la clasificación de la anemia y por consiguiente en su diagnóstico etiológico:
• Volumen corpuscular medio (VCM): es la media del tamaño (fl) de los hematíes. Según este valor, se realizará la clasificación morfológica de las anemias (v. siguiente apartado).
• Amplitud de distribución de los eritrocitos (ADE/RDW): informa de la coexistencia de poblaciones de hematíes de diferentes tamaños. Este parámetro ayuda a diferenciar entre ferropenia y talasemia, ya que en la primera suele ser elevado, debido a la distinta distribución de la Hb según el hierro disponible en cada momento; mientras que en las talasemias, suele ser normal (aunque puede estar elevado), porque la distribución de Hb es uniforme.
• Índice de producción reticulocitaria (IPR): los reticulocitos informan sobre la capacidad regenerativa de la médula ósea, por lo que este parámetro permitirá hacer una clasificación fisiopatológica de la anemia (v. siguiente apartado). Los valores normales del IPR se sitúan entre 2 y 3. La interpretación correcta de la cifra de reticulocitos necesita el ajuste de la cifra bruta (%) según la cifra real de hematíes de cada paciente, mediante la fórmula reflejada en la figura 1.
Figura 1. Fórmula para el ajuste de la cifra de reticulocitos.
• Revisión del frotis de sangre periférica: debe ser realizado por un hematólogo experto. El tamaño y la morfología de los hematíes pueden ser primordiales para identificar trastornos como: drepanocitosis (células falciformes), esferocitosis (esferocitos), hemoglobinopatías (células en diana), hemólisis (cuerpos de Heinz), etc. Además, la presencia de otras citopenias o leucocitosis con formas inmaduras puede orientarnos a ciertas etiologías (infecciones, aplasia/hipoplasia medular, infiltración de la médula ósea por leucemia/linfoma, etc.).
• Metabolismo del hierro: la ferritina es el parámetro más útil para medir los depósitos de hierro; valores por debajo de 15 µg/l son indicativos de ferropenia. Sin embargo, su utilidad se ve limitada por comportarse como un reactante de fase aguda, incrementándose con la inflamación/infección y la destrucción tisular.
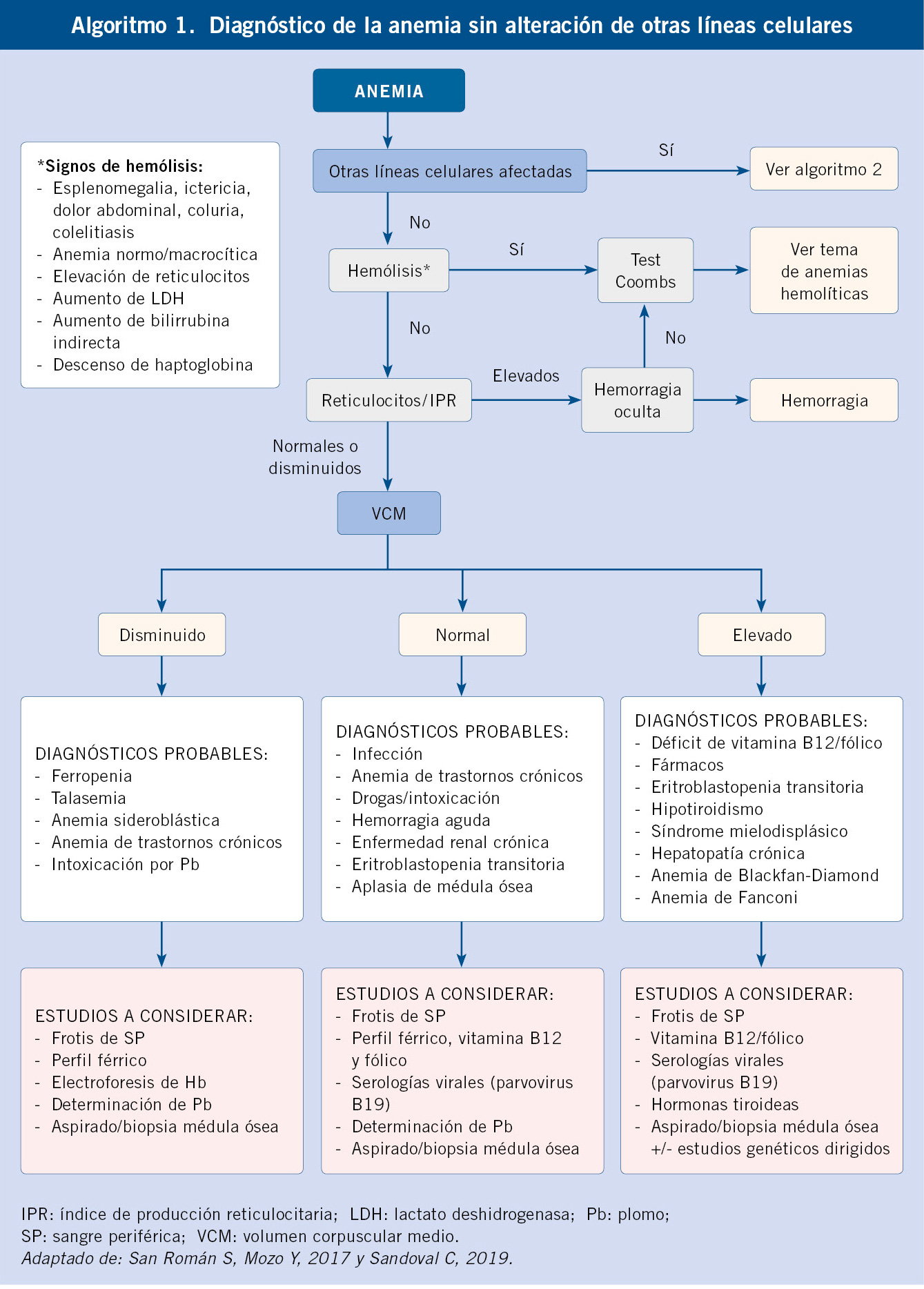
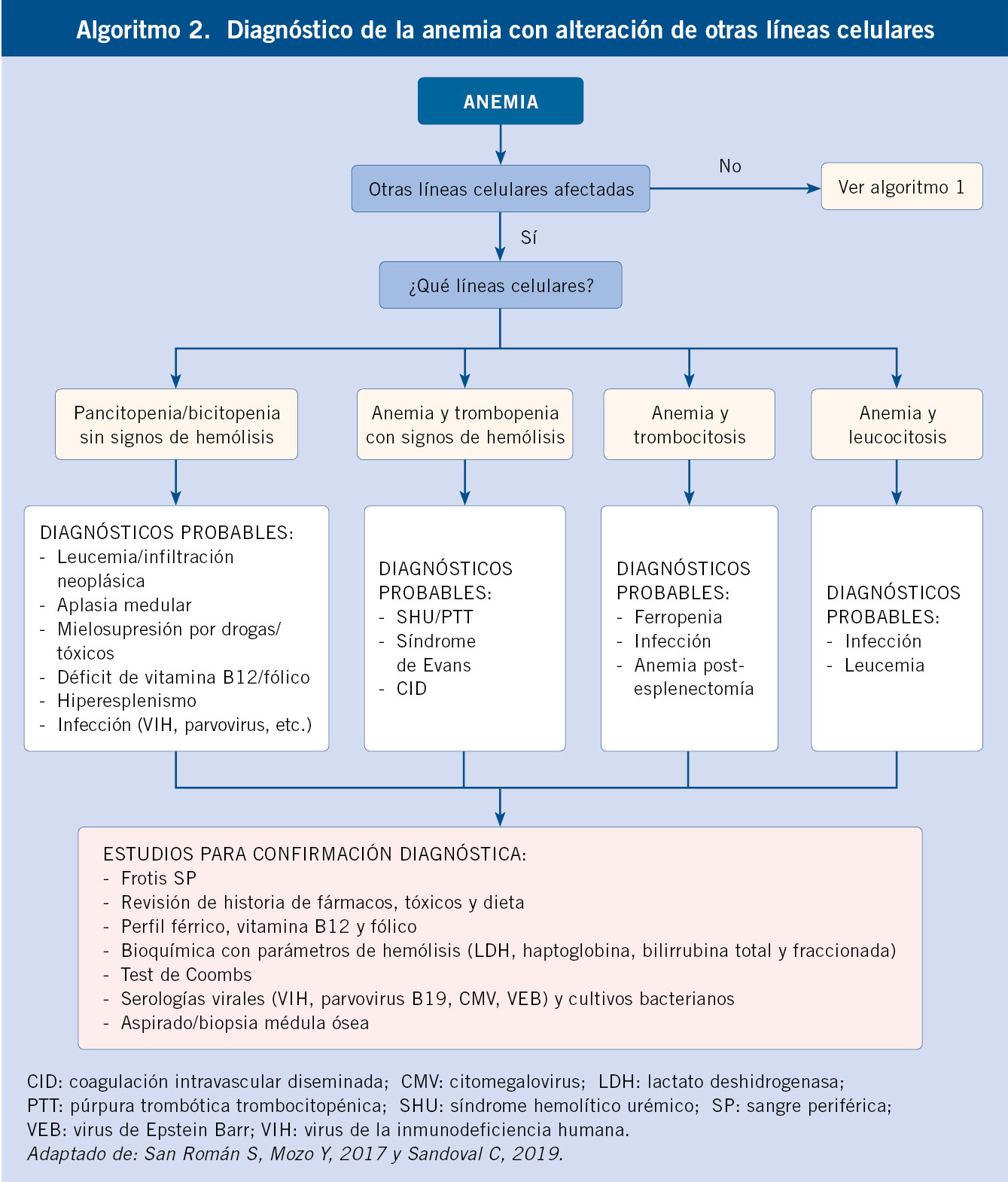
Según los resultados previos, deberemos ampliar el examen con estudios de segundo nivel (Algoritmos diagnósticos, algoritmos 1 y 2):
- Si reticulocitosis y datos sugestivos de hemólisis, se debe descartar la existencia de anemia hemolítica y solicitar: haptoglobina, test de Coombs para determinar autoinmunidad, y si resulta negativo, electroforesis de hemoglobinas para descartar hemoglobinopatía (teniendo en cuenta que la HbF es predominante en los primeros meses de vida, y su disminución es más lenta en la enfermedad de células falciformes, persistiendo en cantidad variable) y/o cuantificación de enzimas (G6PDH, piruvato-kinasa) para estudiar las enzimopatías, y/o estudios de membrana (fragilidad osmótica, citometría) para las membranopatías.
- Si macrocitosis (VCM elevado): puede haber una causa carencial (vitamina B12, ácido fólico) o hipotiroidismo (solicitar TSH y T4L), pero siempre hay que tener presente que se puede tratar de un trastorno madurativo central (realizar aspirado/biopsia médula ósea).
- Si reticulocitopenia y descartada la infección por parvovirus B19, realizar aspirado/biopsia de médula ósea para valorar origen central de la anemia.
Clasificación de las anemias(2,7-9)
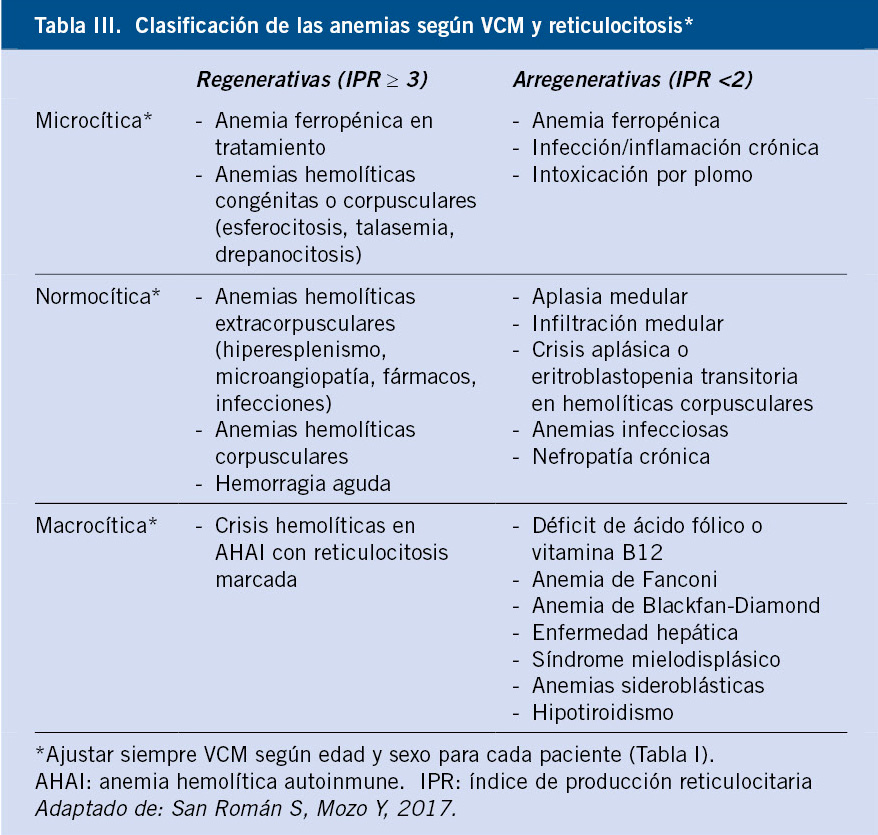
Las clasificaciones morfológica y fisiopatológica de las anemias son complementarias y se requieren para el enfoque del diagnóstico etiológico.
Con ayuda de los parámetros obtenidos en las exploraciones complementarias de primer nivel, se realizan las clasificaciones morfológica y fisiopatológica de la anemia, que conducirán a determinar su etiología tras la realización de las pruebas complementarias pertinentes (Tabla III y Algoritmos 1 y 2).
• Clasificación morfológica: basada en el VCM (Tabla I).
- Microcítica: VCM ≤ percentil 2,5 para la edad, sexo y raza. En la infancia, son por excelencia la anemia por déficit de hierro y las talasemias.
- Normocítica: VCM normal (percentil entre 2,5 y 97,5) para edad sexo y raza. Puede deberse a: pérdidas de sangre, trastornos crónicos, infecciones o ser el estado inicial de anemias micro o macrocíticas.
- Macrocítica: VCM ≥ percentil 97,5 para edad, sexo y raza. Las más frecuentes en la infancia son por déficit de vitamina B12 y/o fólico o por exposición a ciertos fármacos (p. ej.: anticonvulsivantes e inmunosupresores). También puede encontrarse macrocitosis en anemias agudas regenerativas, por la presencia de reticulocitosis, y en trastornos madurativos de la médula ósea (mielodisplasia y aplasia).
• Clasificación fisiopatológica: basada en la capacidad regenerativa medular, determinada a través del IPR.
- Regenerativas: presentan una respuesta reticulocitaria elevada (reticulocitos > 3% o IPR ≥ 3). Son ejemplos: anemias hemolíticas y secundarias a hemorragia.
- A/hiporregenerativas: respuesta reticulocitaria normal o baja para el grado de anemia (reticulocitos < 1-1,5% o IPR < 2). Traduce la existencia de una médula hipo/inactiva por diferentes motivos: déficit de sustratos (hierro, fólico, vitamina B12), infiltración medular tumoral, infecciones, enfermedades de depósito (Nieman-Pick, Gaucher…) o aplasia congénita o adquirida.
Función del pediatra de Atención Primaria
• Desde Atención Primaria, se pueden solicitar: hemograma con índices eritrocitarios, reticulocitos, bioquímica con parámetros de hemólisis y perfil férrico, con los que se puede hacer el enfoque diagnóstico de la mayoría de las anemias en la edad pediátrica.
• En nuestro medio, las anemias que con más frecuencia puede ver el pediatra de Atención Primaria son: la anemia ferropénica, la anemia fisiológica del lactante, la β-talasemia heterocigota o rasgo talasémico, la anemia de trastornos crónicos, la anemia por hemorragia y, actualmente también, la anemia de células falciformes.
• En general, es susceptible de derivación a atención especializada cualquier anemia que curse con: otra citopenia, las hemoglobinopatías, las anemias hemolíticas, las arregenerativas, las que no responden a tratamiento, y siempre que exista cualquier otro signo de alarma.
Bibliografía
Los asteriscos muestran el interés del artículo a juicio de las autoras.
1. Glader B. Las anemias. En: Kliegman RM, Behrman RE, Jenson HB, Stanton BF, ed. Nelson. Tratado de Pediatría. 18ª edición, Barcelona. Elsevier España; 2009. p. 2003-6.
2. Hernández Merino A. Anemias en la infancia y adolescencia; clasificación y diagnóstico. Pediatr Integral. 2016; XX(5): 287-96.
3. Word Health Organization. Worldwide prevalence of anemia 1993-2005: WHO global database on anemia. Geneva: World Health Organization; 2008.
4.** Allali S, Brousse V, Sacri AS, Chalumeau M, de Montalembert M. Anemia in children: prevalence, causes, diagnostic work-up, and long-term consequences. Expert Rev Hematol. 2017; 10: 1023-8.
5.** Arrizabalaga B, González FA, Remacha. Eritropatología. Edición Ambos Marketing Services. Barcelona. 2017.
6.** Prudencio García-Paje M. Aproximación diagnóstica al paciente con anemia. En: Madero L, Lassaletta A, Sevilla J, ed. Hematología y Oncología Pediátricas. 3ª edición, Madrid. Ergon; 2015. p. 81-6.
7.*** Sandoval C. Approach to the child with anemia (Revisión de literatura vigente hasta: septiembre de 2020. Última actualización: 20 de junio de 2019). Disponible en: www.uptodate.com.
8.** San Román Pacheco S, Mozo del Castillo Y. Síndrome anémico. En: Guerrero-Fdez. J, Cartón Sánchez A, Barreda Bonis A, Menéndez Suso J, Ruiz Domínguez J, ed. Manual de Diagnóstico y Terapéutica en Pediatría. 6ª edición, Madrid. Editorial Panamericana; 2017. p. 1117-30.
9. Buttarello M. Laboratory diagnosis of anemia: are the old and new red cell parameters useful in classification and treatment, how? Int J Lab Hematol. 2016; 38: 123-32.
10. Sevilla Navarro J. Abordaje de la anemia microcítica; nuevas herramientas diagnósticas. En: AEPap, ed. 7º Curso de Actualización en Pediatría 2010. Madrid: Exlibris Ediciones; 2010. p. 239-9.
Bibliografía recomendada
- Allali S, Brousse V, Sacri AS, Chalumeau M, de Montalembert M. Anemia in children: prevalence, causes, diagnostic work-up, and long-term consequences. Expert Rev Hematol. 2017; 10: 1023-8.
Artículo que resume de forma práctica, las causas de anemia en Pediatría y las pruebas complementarias necesarias para su diagnóstico, dando especial importancia a la comorbilidad que esta patología implica a largo plazo.
- Arrizabalaga B, González FA, Remacha. Eritropatología. Edición Ambos Marketing Services. Barcelona. 2017.
Texto de hematología general, adecuado para el estudio de la hematopoyesis y de la fisiopatología de las anemias.
- Prudencio García-Paje M. Aproximación diagnóstica al paciente con anemia. En: Madero L, Lassaletta A, Sevilla J, ed. Hematología y Oncología Pediátricas. 3ª edición, Madrid. Ergon; 2015. p. 81-6.
Capítulo donde se realiza una exposición general sobre las anemias en Pediatría, de utilidad para hacer un acercamiento global al tema. En el mismo libro, existen otros capítulos dedicados a la descripción de los distintos tipos de anemia en mayor profundidad.
- Sandoval C. Approach to the child with anemia (Revisión de literatura vigente hasta: septiembre de 2020. Última actualización: 20 de junio de 2019). Disponible en: www.uptodate.com.
Esta fuente de medicina basada en la evidencia, que se mantiene actualizada con frecuencia, ofrece una completa revisión de las anemias infantiles con una exposición muy didáctica.
- San Román Pacheco S, Mozo del Castillo Y. Síndrome anémico. En: Guerrero-Fdez. J, Cartón Sánchez A, Barreda Bonis A, Menéndez Suso J, Ruiz Domínguez J, ed. Manual de Diagnóstico y Terapéutica en Pediatría. 6ª edición, Madrid. Editorial Panamericana; 2017. p. 1117-30.
Exposición del tema de las anemias en la infancia, con prácticas tablas y algoritmos.
| Caso clínico |
|
Anamnesis Niña de 7 años que consulta por palidez progresiva y cuadro clínico de un mes de evolución de astenia, inicialmente atribuida por la familia a diversos procesos infecciosos de probable etiología viral (gastroenteritis, catarro de vías altas y otitis), sin precisar, ninguno de ellos, ingreso o antibioterapia. Actividad física conservada. No ha presentado: fiebre, sudoración, anorexia, pérdida de peso ni dolores osteomusculares. Recibió mebendazol en el mes previo a la consulta como tratamiento de oxiuriasis, e ibuprofeno de forma ocasional. Su pediatra solicita una analítica en la que destaca Hb de 8 g/dl. Se sospecha origen carencial y/o parainfeccioso, y se prescribe ferroterapia. Acude hoy a consulta pasadas dos semanas del inicio del tratamiento para control clínico y analítico. Antecedentes personales • Vacunación al día, según el calendario de su comunidad autónoma. • Sin alergias conocidas. • No antecedentes médico-quirúrgicos de interés. • Animales domésticos: perro, desde hace 10 años, correctamente vacunado. • Reside en zona urbana. No viajes recientes. • Ejercicio: natación. Antecedentes familiares • Padres y hermano de 10 años sanos. • Abuela materna: anemia carencial. • No otros antecedentes de interés. Exploración física Peso: 20 kg. Tª: 36,5ºC. Frecuencia respiratoria: 22 rpm. Frecuencia cardiaca: 105 lpm. Tensión arterial sistólica/diastólica: 115/65 mmHg. Buen estado general. Palidez cutáneo-mucosa marcada. No exantemas ni petequias. Eupneica. Buena perfusión periférica, llenado capilar < 2 segundos, pulsos periféricos presentes y simétricos. Auscultación cardiaca: ruidos rítmicos, soplo sistólico II/VI. Auscultación pulmonar: normal. Orofaringe normal. Otoscopia bilateral normal. No adenopatías. Abdomen blando, indoloro, sin masas ni megalias. Peristaltismo conservado. No signos de irritación peritoneal. Glasgow 15/15, colaboradora, signos meníngeos negativos, sin focalidad neurológica. Pruebas complementarias • Hemograma: Hb: 6,5 g/dl; VCM: 89 fl; leucocitos: 4,76×109/l; neutrófilos: 0,98×109/l; linfocitos: 3,61×109/l; monocitos: 0,16×109/l; plaquetas: 120×109/l; VPM: 10 fl. Reticulocitos: 21 x109/l (0,7%). • Bioquímica: glucosa: 80 mg/dl; urea: 25 mg/dl; creatinina: 0,4 mg/dl; sodio: 140 mEq/l; potasio: 4,1 mEq/l; cloruro: 105 mEq/l; GOT: 29 UI/l; GPT: 21 UI/l; bilirrubina total: 0,4 mg/dl; LDH: 206 UI/l; fósforo: 5,5 mg/dl; calcio total: 10 mg/dl.
|





 Anemia. Classification and diagnosis
Anemia. Classification and diagnosis 