 |
| Temas de FC |
J. Pellegrini Belinchón, S. de Arriba Méndez*
Pediatra de Atención Primaria. Centro Salud Pizarrales. Salamanca. Coordinador del Grupo de Trabajo de Asma de la SEPEAP.
*Médico adjunto de Pediatría. Hospital Nuestra Señora de Sonsoles. Ávila
| Resumen
El asma es la enfermedad crónica más frecuente en Pediatría. El tratamiento del asma infantil se basa en tres pilares fundamentales: educación del paciente asmático y de su familia, medidas de control de los factores que empeoran la enfermedad y el tratamiento farmacológico. En este capítulo, se revisa el tratamiento farmacológico actual de la crisis de asma y el tratamiento de mantenimiento de la enfermedad. |
| Abstract
Asthma is the most common chronic disease among children. Treatment of childhood asthma is based on three pillars: education of the patient and his/her family; control measures of the factors that worsen the disease; and drug therapy. This chapter reviews the current pharmacological treatment of the crisis and maintenance treatment of the disease. The national and international consensus, the clinical practice guidelines and manuals agree that the ultimate goal of treatment is to achieve and maintain total control of asthma. This means no limitations on the child’s normal activity, absence of symptoms, exacerbations and normal lung function. It is not always possible to fully achieve it but all efforts must be aimed at this purpose. |
Palabras clave: Asma infantil; Tratamiento; Crisis; Fármacos antiasmáticos.
Key words: Childhood asthma; Treatment; Crisis; Anti-asthma drugs.
Pediatría Integral 2012; XVI(2): 131-140
Tratamiento del asma. Crisis aguda. Tratamiento de fondo
Introducción
Todavía hay muchos aspectos de la historia natural del asma que se desconocen, el conocimiento etiopatogénico de la enfermedad va mejorando y, en el momento actual, en lactantes, se reconoce la existencia de fenotipos distintos de asma(1), y en niños a partir de 3 años se ha podido constatar en muchos casos inflamación eosinofílica y remodelado de vías aéreas comparable a la de los niños mayores y adultos(2) lo que ha condicionado cambios en el tratamiento del asma.
Tratamiento farmacológico. Fármacos utilizados
Antes de hablar de los distintos fármacos a utilizar en el tratamiento del asma, hay que hacer una serie de consideraciones con respecto al tratamiento farmacológico.
Previamente a iniciar cualquier tratamiento, es preciso haber realizado un diagnóstico correcto y precoz, necesariamente clínico en el caso del lactante y niño pequeño y, con pruebas funcionales respiratorias cuando la edad lo permita. Se debe hacer la clasificación de la gravedad antes de iniciar una pauta concreta y enseñar, explicar, ensayar, demostrar y comprobar la técnica inhalatoria, teniendo en cuenta la habilidad y preferencias del paciente y/o cuidadores.
En el tratamiento del asma, se considera de elección la vía inhalada para los ß2 agonistas de corta o larga acción y para los corticoides. En el tratamiento de una crisis de asma, se considera de elección la vía oral antes que la parenteral para la administración de los corticoides.
Se debe utilizar la pauta más simple posible en cuanto al número de fármacos, número de dosis y dispositivos de inhalación, facilitándolo siempre por escrito y se debe realizar un seguimiento programado para ajustar el plan de tratamiento, evaluar su efectividad, monitorizar su adherencia y educar en los aspectos deficitarios. Los dispositivos MDI (inhaladores presurizados) se administrarán siempre con una cámara espaciadora adaptada a la edad del niño hasta que se compruebe fehacientemente su capacidad para utilizarlos sin cámara.
La idoneidad del tratamiento de mantenimiento se debe evaluar dependiendo de: días y noches libres de síntomas, hoja de síntomas en lactantes o niños pequeños o incapaces de utilizar medidas objetivas, pruebas funcionales respiratorias (espirometría y/o FEM), empleo de medicación de alivio y de corticoides orales, ingresos hospitalarios y valoración por parte del paciente de su calidad de vida o con la utilización de test.
Antes de aumentar la dosis o número de fármacos en el tratamiento de mantenimiento, comprobaremos que la adherencia, la técnica inhalatoria y las medidas de evitación de desencadenantes sean correctas.
En el asma estacional, el tratamiento se instaurará varias semanas antes del inicio de la estación.
En todos los centros de Atención Primaria, deben existir los recursos terapéuticos necesarios para atender a un paciente con asma (3,4).
Los fármacos utilizados se exponen en la tabla I(4-9).

Broncodilatadores ß2 adrenérgicos de acción corta
Son los fármacos más eficaces para controlar la crisis asmática. Aunque se pueden administrar por vía inhalada, oral, subcutánea o intravenosa, se debe utilizar la vía inhalada; ya que, el fármaco se libera en su lugar de acción y se obtiene una máxima eficacia con mínimos efectos sistémicos. El efecto broncodilatador comienza casi de inmediato, el 75% del efecto máximo se alcanza a los 5 minutos y dura entre 2 y 6 horas(3). El salbutamol y la terbutalina son los más empleados, actualmente, por su acción ß2 agonista más selectiva, eficacia y seguridad. Se aconseja su uso exclusivamente “a demanda”, cuando el paciente tenga síntomas. La necesidad de un uso frecuente de estos medicamentos indica un tratamiento de base insuficiente.
En el tratamiento de la crisis, las dosis recomendadas dependen de la gravedad de la crisis y de la respuesta a las dosis iniciales. El fármaco más utilizado es el salbutamol, disponible en solución para nebulizar, inhalador presurizado y en polvo seco. La terbutalina en polvo seco se puede utilizar para el tratamiento de la crisis en niños mayores que utilicen correctamente el sistema Turbuhaler®. El broncodilatador debe administrarse en tandas de 2-10 pulsaciones de 100 µg de salbutamol hasta conseguir la respuesta. En crisis leves, una tanda de 2-4 pulsaciones puede ser suficiente y en las crisis graves puede ser necesario administrar hasta diez pulsaciones. Los agonistas ß2 adrenérgicos en nebulización deben restringirse sólo para los casos en los que el paciente requiera un aporte de oxígeno para normalizar su SaO2. La nebulización continua no ofrece grandes ventajas respecto a la nebulización intermitente, en iguales dosis totales administradas(5).
Los efectos secundarios más frecuentes son la taquicardia y el temblor que, aunque pueden ser molestos para el niño, no se ha descrito que supongan riesgos importantes(6).
Anticolinérgicos
Los anticolinérgicos son antagonistas competitivos de la acetilcolina. El más utilizado es el bromuro de ipratropio. En este momento, su utilización solo está indicada asociada a los ß2 agonistas de rescate durante las primeras 48 horas de una crisis asmática grave. Fuera de esta indicación, no está demostrada su eficacia. Su inicio de acción es más lento, entre 30 y 60 minutos.
La dosis nebulizada es de 250 µg/4-6 horas en pacientes de menos de 30 kg y 500 µg/4-6 horas en pacientes de más de 30 kg. La dosis con cámara de inhalación es de 40-80 µg (2-4 pulsaciones). Se administran dosis frecuentes cada 20 ó 30 minutos. En los lactantes, su uso en combinación con los agonistas b2 adrenérgicos inhalados se ha mostrado efectiva en el tratamiento de las crisis más graves.
Corticoides sistémicos (GC)
Se deben utilizar siempre corticoides de vida media corta (prednisona, metilprednisolona, hidrortisona), que tienen una vida media de 8-12 horas, nunca corticoides depot. Son antiinflamatorios y bloquean la mayor parte de los escalones de la cascada inflamatoria; aunque, debido a su farmacocinética, tienen un comienzo de acción lento (requieren al menos 4 horas para hacer su efecto), además, son capaces de reducir la hiperreactividad bronquial y mejorar la función pulmonar. Han demostrado mayor beneficio cuando se utilizan precozmente.
Las indicaciones de los corticoides sistémicos en el asma en el niño y adolescente son:
• En pautas cortas (5-7 días) para el tratamiento de crisis moderadas o graves y en las leves que no responden de forma mantenida a los broncodilatadores de acción rápida. Se utilizan en este caso a dosis de 1-2 mg/kg/día de prednisona o equivalente, con un máximo de 60 mg/día repartido en 1-3 dosis diarias. Es de elección la vía oral frente a la parenteral. Las pautas cortas se pueden retirar de forma brusca, ya que no parecen afectar al eje hipotálamo-hipófiso-suprarrenal.
• Como tratamiento continuado del asma persistente grave, cuando no hay otra posibilidad de controlar el asma. Se debe utilizar siempre la dosis mínima posible capaz de mantener al paciente bajo control. La retirada debe ser siempre paulatina. Aunque la necesidad de corticoide oral a largo plazo en el niño es excepcional, su manejo exige siempre la utilización concomitante de otros antiasmáticos que permitan utilizar la menor dosis posible por vía sistémica y habrá que hacer reiterados intentos para abandonar esta terapia por sus importantes efectos secundarios.
Corticoides inhalados (GCI)
Dada su alta afinidad y selectividad por el receptor, permiten un potente efecto antiinflamatorio local, acciones terapéuticas mantenidas, prolongada permanencia en el pulmón y una baja biodisponibilidad oral. Reducen los síntomas de asma y el número de exacerbaciones. Los CI disponibles en España son: dipropionato de beclometasona (DBP), budesonida (BD), propionato de fluticasona (PF) y ciclesonida (autorizada en mayores de 12 años), pero sólo BD y PF son los recomendados por los consensos actuales. Se debe utilizar siempre la mínima dosis eficaz de CI (Tabla II).

Los lactantes y menores de 3 años con factores de riesgo para desarrollar un asma persistente (Índice Predictivo de Asma, IPA)(4) muestran una buena respuesta al tratamiento con GCI(5). Los preescolares con episodios intermitentes de sibilancias relacionados con infecciones virales presentan una respuesta escasa al tratamiento con GCI. En niños mayores de tres años, la eficacia de los glucocorticoides inhalados está suficientemente demostrada, con una mejoría de los parámetros clínicos, funcionales y de inflamación bronquial, y constituyen la primera línea de tratamiento.
Habitualmente, se utilizan en dos dosis diarias. Los GCI, en el momento actual, no deben utilizarse como tratamiento sintomático en las crisis agudas de asma. Los efectos secundarios locales, como: disfonía o muguet son, generalmente, de fácil control y no suelen precisar la suspensión del tratamiento. Los efectos sistémicos son dosis dependientes y a dosis bajas y medias son prácticamente inexistentes.
Broncodilatadores b2 adrenérgicos de acción prolongada
Nunca se deben utilizar como medicación aislada, debiéndose asociar siempre a un corticoide inhalado. La dosis recomendada en niños es de 6 µg dos veces al día, para el formoterol y de 50 µg, dos veces al día, para el salmeterol. Los ß2 adrenérgicos de acción prolongada son fármacos seguros si se utilizan adecuadamente. En el momento actual, no se recomiendan como medicación de rescate y, en los tratamientos combinados utilizados de forma ajustable según sintomatología, se debería establecer una dosis máxima (100 µg/día de salmeterol y 36 µg/día de formoterol) para que el paciente no inhale cantidades excesivas de este tipo de broncodilatador.
En España hay preparados para administrar por vía inhalada en el mismo dispositivo salmeterol/fluticasona y formoterol/budesonida. Estas combinaciones se utilizan en el caso del asma persistente que no esté controlada con el uso de corticoides inhalados a dosis bajas o medias. No están autorizados para el uso en menores de cuatro años, en el caso del salmeterol, y de 6 años el formoterol; por lo que, debe esperarse a tener más datos sobre su seguridad para recomendarlos por debajo de esta edad.
Antileucotrienos (ARLT)
Los leucotrienos cisteinílicos, a través de su receptor de tipo 1, producen broncoconstricción, hiperreactividad bronquial, aumento de la secreción mucosa y de la permeabilidad vascular, aumento del tono muscular y proliferación del músculo liso bronquial, teniendo por ello un papel importante en la fisiopatología del asma.
El único fármaco de este grupo autorizado en España que se utiliza en niños (a partir de los seis meses de edad) es el montelukast. Se utiliza por vía oral y en dosis única nocturna. Su metabolismo no parece influirse por las comidas copiosas o grasas.
Parecen mejorar el asma inducida por ejercicio físico o por alérgenos y, en niños pequeños, podrían mejorar las exacerbaciones inducidas por virus. Añadido a corticoides inhalados, parece mejorar la función pulmonar y disminuir el número de crisis.
Cuando se ha evaluado la utilidad de los antileucotrienos asociados a los corticoides inhalados, se ha observado un efecto antiinflamatorio complementario, lo cual permite la reducción de la dosis de corticoide. Este efecto parece menor que con la asociación de un broncodilatador ß2 adrenérgico de acción prolongada al corticoide. En monoterapia, también parece tener efecto beneficioso, pero menor que los corticoides inhalados(4-7).
Cromonas
Aunque tradicionalmente se consideraron como parte del tratamiento del asma, las revisiones actuales no las consideran mejores que el placebo, por lo que, los consensos actuales ya no las incluyen.
Metilxantinas
Su única indicación actual es como tratamiento agregado en caso de asma grave no controlada con GCI. Se precisan más estudios para definir la relación riego-beneficio.
Anticuerpos monoclonales anti-IgE
Se basan en el hecho de que la IgE, unida a sus receptores de alta afinidad de mastocitos y células dendríticas, tendría un papel fundamental en el asma y en la rinitis alérgica.
Estos anticuerpos (omalizumab) son de uso hospitalario y solo se utilizan en casos muy puntuales de asma alérgica grave con mala respuesta a corticoides inhalados. Algunos estudios han demostrado que el omalizumab reduce el número de agudizaciones y las visitas a urgencias de estos pacientes, así como permite rebajar la dosis de corticoide utilizada.
Tratamiento de la crisis de asma
Los objetivos al tratar una crisis de asma son: tratar la hipoxemia, revertir la obstrucción y evitar las recaídas.
Ante un niño con síntomas de presentar una crisis asmática, en primer lugar, hay que realizar una valoración rápida de la gravedad de la crisis para determinar si es necesaria una actuación inmediata y aplicar el tratamiento. En el Centro de Salud, o en el primer escalón de urgencias, la valoración inicial de la crisis asmática se basa, fundamentalmente, en patrones clínicos y necesariamente ha de hacerse de la forma más sencilla y rápida posible. En la tabla III, se recoge el Pulmonary Score, aplicable a todas las edades. En esta tabla, se puntúa de 0 a 3 puntos cada uno de los tres apartados, a más puntuación, mayor gravedad. Para medir el trabajo respiratorio, se valora exclusivamente el uso de los esternocleidomastoideos, músculos que se han relacionado bien con el grado de obstrucción (Tabla III).

En todos los Centros de Salud debe existir un pulsioxímetro para medir la saturación de oxígeno (SaO2); ya que, contribuye de forma fundamental a valorar la gravedad de la crisis. En la tabla IV, se recoge de forma combinada el cálculo de la gravedad de la crisis asmática combinando el Pulmonary Score y la SaO2.

En la figura 1, se detalla el tratamiento propuesto para tratar la crisis asmática según la gravedad(4,5,9).

Figura 1. Tratamiento de la crisis asmática en niños.
Es preciso hacer alguna consideración:
• Una vez iniciado el tratamiento, es necesario realizar una historia clínica rápida y dirigida, encaminada a obtener datos de la enfermedad: clasificación y terapia de mantenimiento, tiempo de evolución de la crisis y terapia empleada, posibles precipitantes y condicionantes, existencia de enfermedades asociadas e historia de crisis graves anteriores.
• Como exploración complementaria, de forma habitual, se realizará la pulsioximetría; la valoración de pico de flujo se puede hacer en pacientes entrenados que se controlen de forma habitual con este sistema. Radiografía de tórax en caso de que sea la primera crisis, se sospechen complicaciones o existan dudas diagnósticas.
• Se aconseja individualizar la dosis de los fármacos de acuerdo con la gravedad de la crisis y con su respuesta al tratamiento.
• En general, para crisis leves y moderadas, se prefiere utilizar MDI con cámara de inhalación antes que la nebulización por lo que, para evitar problemas de logística, en centros de salud y hospitales, se debe recomendar a los niños y a sus familias que, cuando acudan a urgencias, lo hagan con su cámara y su inhalador.
• En crisis graves, si se dispone de sistema de nebulización tipo Jet con oxígeno, utilizarlo asociando a los ß2 adrenérgicos de acción corta el bromuro de ipratropio.
• Se debe instaurar oxígeno, en caso preciso, para mantener la saturación por encima del 94%.
• Se debe plantear el traslado al hospital siempre que se trate de una crisis grave, aunque en principio responda al tratamiento, y se debe realizar en una ambulancia medicalizada. También, en caso de sospecha de complicaciones o cuando haya antecedentes de crisis de alto riesgo.
• Una pauta corta de corticoides orales se debe utilizar en las crisis moderadas (aunque esto está en revisión actualmente, que sea en todas las moderadas) o graves, incluso en aquellas leves que no hayan respondido satisfactoriamente a la terapia con ß2 adrenérgicos de acción corta. Dosis de prednisona de 1-2 mg/kg/día durante 3-5-7 días. Si no se mantiene más de 10 días, se puede retirar sin hacer pauta descendente.
Tratamiento farmacológico de mantenimiento
Antes de comenzar a hablar del tratamiento farmacológico, hay que hacer algunas consideraciones para lactantes con sibilancias recurrentes/asma y fenotipos.
Varios grupos de investigadores han iniciado cohortes de seguimiento para determinar la historia natural de los niños con sibilancias a través de los años y, desde el ya estudio clásico de Martínez con la cohorte de Tucson, se han aceptado como válidos varios fenotipos fundamentales de sibilancias durante la infancia(10,11).
Los tres fenotipos manejados en el momento actual se describen en la tabla V. Cuando un niño comienza en los primeros años de vida con episodios recurrentes de sibilancias es importante, desde un punto de vista práctico, intentar clasificarlo en alguno de estos tres fenotipos para valorar el pronóstico y enfocar el tratamiento según las evidencias disponibles en el momento actual.

Para ello, se han desarrollado unos Índices Predictivos de Asma (IPA)(12) que indican que los niños menores de 3 años que cumplen al menos un criterio mayor o dos menores de los citados a continuación, tendrán una mayor probabilidad de padecer asma persistente atópica:
Criterios mayores:
• Diagnóstico médico de asma en alguno de los padres.
• Diagnóstico médico de dermatitis atópica en el niño.
Criterios menores:
• Diagnóstico médico de rinitis alérgica a los 2-3 años.
• Sibilancias en ausencia de catarros.
• Eosinofilia en sangre periférica igual o superior al 4%.
Los niños con IPA+ tienen un riesgo superior de padecer asma activa a los 6-13 años que los que presentan IPA–.
Posteriormente, Guilbert, en 2004, introdujo un nuevo criterio mayor: sensibilización alérgica al menos a un aeroalérgeno(13).
También, se ha demostrado que los niños menores de un año con dermatitis atópica y una IgE específica a proteínas de huevo elevada presentan un 80% de probabilidad de desarrollar patología alérgica respiratoria (rinitis y/o asma) a los 4 años(14).
Clasificación de la gravedad del asma
Esta clasificación se utiliza para orientar el tratamiento en un primer momento; posteriormente, los cambios de medicación dependerán de la evolución clínica y del control de la enfermedad. La clasificación se describe en la tabla VI.

El recientemente publicado “Consenso sobre el tratamiento de asma en Pediatría” en España y la GEMA(4,5) orientan el inicio del tratamiento de base en los fenotipos antes descritos y hace una clasificación entre mayores y menores de 3 años.
Una vez iniciado el tratamiento según la clasificación de gravedad del asma, la GINA(7) pone de relieve que el objetivo del tratamiento es conseguir un adecuado control de la enfermedad y se considera que el niño está controlado cuando:
• Puede hacer actividad física sin limitaciones.
• Presenta sintomatología nula o mínima.
• No presenta reagudizaciones.
• No precisa medicación de rescate.
• Función pulmonar normal.
• Variabilidad del FEM <20%.
• Se han evitado los efectos adversos de la medicación.
Niños menores de 3 años
El tratamiento inicial de mantenimiento en el niño menor de 3 años se describe en la tabla VII.
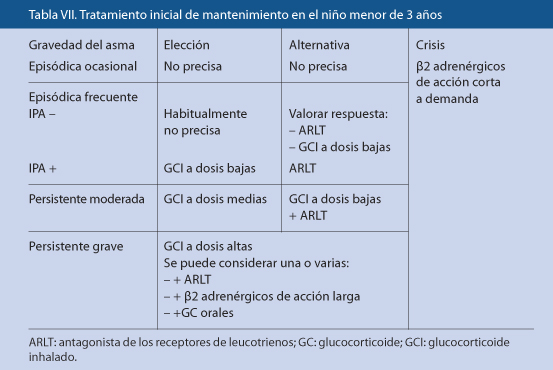
El consenso español propone que una vez iniciado el tratamiento, se cite al niño y a su familia y se le pase un cuestionario para intentar objetivar la respuesta a este tratamiento inicial. Propone el Cuestionario Control del Asma en Niños (CAN) (puede verse en la Tabla XII del capítulo anterior), que consta de 9 preguntas, con 5 posibles respuestas, que se puntúan cada una de 0 a 4 puntos. La puntuación máxima es de 36 puntos y la mínima de 0 puntos. A más puntuación peor control. Se considera deficientemente controlado un niño a partir de 8 puntos, aunque en este momento se está considerando elevar esta puntuación.
En la figura 2, se expone el tratamiento escalonado según el grado de control.

Figura 2. Tratamiento de mantenimiento escalonado del asma en menores de 3 años.
Es preciso hacer algunas puntualizaciones para esta edad(4-7,9):
• Existen pocos trabajos que apoyen con seguridad los tratamientos propuestos, por lo que se debe iniciar un tratamiento y modificarlo o interrumpirlo si no es efectivo. De todas formas, las recomendaciones propuestas se basan en que los menores de 3 años tienen receptores ß2 que funcionan, los fármacos antinflamatorios tienen las mismas propiedades que en otras edades y los efectos secundarios de los ß2 de acción corta y antinflamatorios son similares; si bien, en el momento actual, no hay evidencia de que estos fármacos funcionen en los niños diagnosticados de bronquiolitis y/o con sibilancias producidas por virus.
• La mayoría de los episodios de sibilancias en estas edades son secundarios a infecciones virales, relacionados en muchos casos con la asistencia a guardería, y dejarán de tener síntomas con la edad, a pesar del tratamiento empleado. Se debe valorar suspender el tratamiento en primavera-verano y, antes de iniciarlo en otoño, valorar la necesidad, según la clínica. Valorar de forma individual la posibilidad del “rinovirus de septiembre”.
• Hay evidencia de que los niños con sibilancias recurrentes e IPA+ pueden responder adecuadamente a los GCI. Con IPA– su utilidad es dudosa a estas edades.
• Los ARLT podrían ser útiles para reducir el número de exacerbaciones inducidas por virus y para disminuir la inflamación bronquial en niños atópicos.
• En el momento actual, no se deben utilizar en estas edades los ß2 de acción prolongada, salvo en casos de asma grave y decisión y control hospitalarios.
Niños mayores de 3 años
El tratamiento inicial de mantenimiento en el niño mayor de 3 años se describe en la tabla VIII.

Tras iniciar el tratamiento según la gravedad del asma, se realiza control con el CAN y se va controlando de forma escalonada.
En la figura 3, se expone el tratamiento escalonado según el grado de control.

Figura 3. Tratamiento de mantenimiento escalonado del asma en mayores de 3 años.
Es preciso hacer alguna puntualización sobre el tratamiento de mantenimiento en esta edad:
• Los ß2 adrenérgicos de acción larga no deben utilizarse nunca en monoterapia, siempre asociados a GCI. Cuando ambos fármacos se asocian, mejoran el control y permiten reducir las dosis de GCI.
• La efectividad de los GCI está bien contrastada a esta edad.
• Aunque los ARLT son eficaces a estas edades, tienen menor capacidad antinflamatoria que los GCI. Cuando ambos fármacos se asocian, mejoran el control.
• A cualquier edad, el control del niño con asma moderada o grave debe hacerse siempre coordinado con otros especialistas, alergólogos infantiles o neumólogos pediátricos del hospital de referencia.
• El descenso de medicación se realizará de forma progresiva, pasando de un nivel al inmediatamente inferior.
Inmunoterapia
La administración se realiza habitualmente de forma subcutánea; aunque últimamente se está utilizando inmunoterapia sublingual, parece que se precisan más estudios para valorar su efectividad.
La inmunoterapia por vía subcutánea con vacunas de alérgenos es un tratamiento eficaz para el asma alérgica bien controlada con niveles bajos o medios de tratamiento (escalones terapéuticos 2-4), siempre que se haya demostrado una sensibilización mediada por IgE frente a aeroalérgenos comunes que sea clínicamente relevante, se utilicen extractos bien caracterizados y estandarizados biológicamente(15,16) y se evite el uso de mezclas complejas(5,17).
Está indicada cuando no es posible evitar la exposición al alérgeno, cuando no se consigue un adecuado control de los síntomas de asma con la medicación adecuada o cuando éste provoca efectos adversos o es rechazado por el paciente o su familia. Se utiliza en asma episódica frecuente o moderada cuando existe sensibilización a un único alérgeno o a un alérgeno predominante del que se disponga de extractos de alta calidad estandarizados biológicamente. Se utiliza también en asma leve con rinitis importante que afecta especialmente a la calidad de vida del paciente. La inmunoterapia no debe prescribirse a pacientes con asma grave o no controlada, por el elevado riesgo de reacciones adversas graves, incluso mortales(4,5).
La inmunoterapia está contraindicada en los niños con inmunodeficiencia o con enfermedades hepáticas o renales graves, en enfermedades no mediadas por IgE o en situaciones sociales que no permitan un seguimiento correcto.
La inmunoterapia subcutánea sólo debe administrarse por personal entrenado y en centros donde se disponga de los medios necesarios para tratar una posible reacción general grave. El paciente debe permanecer 30 minutos en observación después de la inyección subcutánea; es, en ese tiempo, cuando se han descrito las raras, aunque posibles, reacciones graves.
La inmunoterapia aporta, como ventajas adicionales, el mantenimiento de los beneficios clínicos obtenidos hasta varios años después de la retirada del tratamiento, el freno de la progresión de la rinoconjuntivitis alérgica por pólenes al desarrollo de asma o la aparición de nuevas sensibilizaciones en pacientes monosensibles(5).
Bibliografía
Los asteriscos reflejan el interés del artículo a juicio del autor.
1. Martínez F. Epidemiology of wheezing in infants and preschoold children. En: Martínez FD, Godfrey S (eds.). Wheezing disorders in the preschoold child. New York: Martin Dunitz; 2003. p. 1-19.
2. Saglani S, Malmstrom K, Peikonen AS, Malmberg LP, Lindahl H, Kajosaari M, et al. Airway remodelling and inflammation in symptomatic infants with reversible airflow obstruction. Am j Respir Crit Care Med. 2005; 171: 722-7.
3.** Rodríguez Fernández Oliva CR, Pardos Martínez C, García Merino A, Úbeda Sansano MI, Callén Blecua MT, Praena Crespo M. Recursos para la puesta en marcha de un programa de Atención al niño con asma. Documentos del GVR (DT-GVR-5) [consultado 16/10/2011]. Disponible en: www.aepap.org/gvr/protocolos.htm
4.*** Castillo Laita JA, De Benito Fernández J, Escribano Montaner A, Fernández Benítez M, García de la Rubia S, Garde Garde J, et al. Consenso sobre el tratamiento del asma en pediatría. An Pediatr (Barc). 2007; 67(3): 253-73.
5.*** Grupo Español para el manejo del asma (GEMA). Guía Española para el Manejo del Asma. 2009. Disponible en: www.gemasma.com (accedido el 16/10/2011).
6. Villa Asensi JR, Pérez Frías J. Tratamiento farmacológico. En: García-Marcos Álvarez L, Garde Garde J, Escribano Montaner A, Malmierca Sánchez F (eds.). Asma en Pediatría. Barcelona: Edipharma; 2002. p. 153-83.
7.*** Global Initiative for Asthma (GINA). Global Strategy for Asthma Management and Prevention. Disponible en: http:// www.ginasthma.org/ (accedido el 16/10/2011).
8. Badorrey I, Morera-Prat J. Diccionario del asma. Barcelona: Temis Medical; 2009.
9. Pellegrini Belinchón J, De Arriba Méndez S, Malmierca Sánchez F. Educación y tratamiento del asma. Pediatr Integral. 2008; XII(2): 137-50.
10. Martínez FDWA, Taussig LM, Holberg CJ, Halonen M, Morgan WJ. Asthma and wheezing in the first six years of life. The Group Health Medical Associates. N Engl J Med. 1995; 332(3): 133-8.
11. Taussig LM, Wrigt AL, Holberg CJ, Halonen M, Morgan WJ, Martínez FD. Tucson Children’s Respiratory Study: 1980 to present. J Allergy Clin Immunol. 2003; 111(4): 661-75.
12.** Castro-Rodríguez JA, Holberg CJ, Wright AL, Martínez FD. A clinical index to define risk of asthma in young children with recurrent wheezing. Am J Respir Crit Care Med. 2000; 162: 1403-6.
13. Guilbert TW, Morgan, W, Krawiec M, Lemanske RF Jr, Sorkness C, Szefler SJ, et al. The Prevention of Early Asthma in Kids study: design, rationale and methods for the Childhood Asthma Research and Education network. Control Clin Trials. 2004; 25(3): 286-310.
14. Tariq SM, Matthews SM, Hakim EA, Arshad SH. Egg allergy in infancy predicts respiratory allergic disease by 4 years of age. Pediatr Allergy Immunol. 2000; 11(3): 162-7.
15. Abramson MJ, Puy RM, Weiner JM. Is allergen immunotherapy effective inasthma? A meta-analysis of randomized controlled trials. Am J Respir Crit Care Med. 1995; 151: 969-74.
16.** Abramson MJ, Puy RM, Weiner JM. Allergen immunotherapy for asthma. Cochrane Database Syst Rev. 2003; (4): CD001186.
17. Adkinson NF Jr, Eggleston PA, Eney D, Goldstein EO, Schuberth KC, Bacon JR, et al. A controlled trial ofimmunotherapy for asthma in allergicchildren. N Engl J Med. 1997; 336(5): 324-31.
Bibliografía comentada
– Rodríguez Fernández Oliva CR, Pardos Martínez C, García Merino A, Úbeda Sansano MI, Callén Blecua MT, Praena Crespo M. Recursos para la puesta en marcha de un programa de Atención al niño con asma. Documentos del GVR (DT-GVR-5) [consultado 16/10/2011]. Disponible en: www.aepap.org/gvr/protocolos.htm
Un buen protocolo, totalmente actualizado (20 de junio 2011) que contempla todas las necesidades para la implantación de un programa de atención al niño con asma, con numerosos enlaces de interés y datos concretos sobre tratamiento de la crisis y de mantenimiento.
– Castillo Laita JA, De Benito Fernández J, Escribano Montaner A, Fernández Benítez M, García de la Rubia S, Garde Garde J, et al. Consenso sobre el tratamiento del asma en pediatría. An Pediatr (Barc). 2007; 67(3): 253-73.
Consenso sobre el asma en Pediatría donde por primera vez se han puesto de acuerdo todas las Sociedades que en España tienen relación con esta patología. El primer autor del presente artículo es coautor de consenso en representación de la SEPEAP, por lo que, necesariamente, gran parte de éste se basa en el recientemente publicado consenso.
– Grupo Español para el manejo del asma (GEMA). Guía Española para el Manejo del Asma. 2009. Disponible en: www.gemasma.com (accedido el 16/10/2011).
Imprescindible para el manejo de esta patología, tanto en adultos como en niños. La última versión es de 2009 y aporta las últimas evidencias disponibles y consensos de expertos.
– Global Initiative for Asthma (GINA). Global Strategy for Asthma Management and Prevention. Disponible en: http:// www.ginasthma.org/ (accedido el 16/10/2011).
Consenso internacional sobre el diagnóstico y tratamiento del asma, elaborado por el National Heart, Lung and Blood Institute de los EE.UU., con la colaboración de especialistas representantes de la mayor parte del mundo. Se encuentran las últimas actualizaciones del GINA 2010. Entre otros objetivos, pretende mejorar el manejo del asma y la disponibilidad y accesibilidad a tratamientos efectivos.
– Castro-Rodríguez JA, Holberg CJ, Wright AL, Martínez FD. A clinical index to define risk of asthma in young children with recurrent wheezing. Am J Respir Crit Care Med. 2000; 162: 1403-6.
Se definen los conceptos de sibilancias recurrentes, asma y fenotipos, descritos y desarrollados en el artículo con los criterios de Índices Predictivos de Asma (IPA).
| Caso clínico |
|
Niña de 13 años que vive en una provincia castellana. Hace 4 años fue diagnosticada de asma por clínica y pruebas funcionales. Estudiada en el Servicio de Alergia, es alérgica a pólenes de gramíneas, hongos, ácaros y epitelio de gato. Antecedentes familiares Padre: rinitis primaveral, alérgico a gramíneas. Madre: dermatitis atópica. En casa no hay gatos ni otras mascotas. Tiene un hermano de 5 años que vive sano. Antecedentes personales Adenoidectomía a los 4 años por hipertrofia adenoidea e hipoacusia. Drenajes transtimpánicos. Varicela a los 8 años. No consta en la historia clínica bronquiolitis ni haber presentado procesos de broncoespasmo en los primeros años de vida. No asistencia a guardería, se escolarizó a los 3 años. A los 5 años comenzó con rinitis durante el mes de mayo y al año siguiente, en el mes de junio y parte de julio, presentó por primera vez 2 procesos de broncoespasmo, acompañados de rinitis y prurito ocular. A partir de de los 8 años, presenta sintomatología perenne que se agudiza cuando va a casa de los abuelos en un pueblo. Es una planta baja, de adobe y antigua, con algo de humedad. En los últimos años, episodios de sibilancias (número de 6-8/año). En el último año, acudió al Servicio de Urgencias en 2 ocasiones (no precisó ingreso). Posteriormente, diagnosticada de sinusitis maxilar. Curó con tratamiento antibiótico, mejorando la sintomatología asmática. Asintomática en las intercrisis, se despierta por la noche 1-2 veces al mes y tiene pitos con esfuerzos intensos cuando hace deporte. |

